金枪鱼因具良好的营养和感官品质在全球范围内被誉为优质食品,是最受欢迎的海鲜产品之一[1]。该物种绝大部分是以保持其最新鲜状态的方式在全球范围内进行采购和分销,通常被称为“生鱼片级”[2]。然而,它是一种季节性的鱼,在冷藏贮存条件下的保质期有限[3],由于其脆弱的肌肉组织中水和不饱和脂肪酸含量高,以及内源性蛋白酶活性高,易变质和腐烂,对产品的经济价值产生不利影响[4]。为满足市场对金枪鱼的消费需求,保持金枪鱼捕后新鲜度和延长其货架期对金枪鱼产业增值至关重要。
目前,食品安全问题加速了天然多糖和可生物降解的复合薄膜包装材料领域的发展[5]。多糖基可食性涂膜作为一种新型的保鲜技术,绿色环保,可通过形成保护膜减少食品与外界环境的接触达到保鲜效果[6]。多糖基可食性涂膜一般以喷雾、浸泡涂膜或薄膜包裹方式作用于食品表面,其中浸泡涂膜操作较简单、适用范围广泛[7]。薄膜/涂层由天然存在的可再生资源(多糖、蛋白质、脂质和复合材料)制备,可以食用且无需处理[8]。壳聚糖(chitosan,CS)和羧甲基纤维素钠(sodium carboxymethyl cellulose,CMC)是较常用的多糖基可食用涂膜剂[9-11]。CS是甲壳素脱除部分乙酰基后的产物,具有相对较高的抗氧化和抗菌活性,也常用于生产可生物降解或可食用的薄膜[12]。CMC是一种通过羧甲基化得到的改性纤维素[13],也是一种具有水溶性特征的高分子化合物,有良好的成膜性能和透气性[14]。CMC同时具有稳定的内部网络结构,可用于提高复合膜的性能[15]。LAN等[13]研究发现海藻酸钠/CS/CMC对复合膜具有积极作用,显示出优异的机械性能,并用作膜复合物中的主要结构。JANNATYHA等[11]将纳米纤维素/CMC和纳米CS/CMC复合薄膜的机械、阻隔和抗菌性能作比较,发现将不同含量的纳米CS加入到CMC膜中,能够降低其物理性质(水溶性、水分含量、吸湿性),纳米CS/CMC复合材料更能改善物理性能,同时具有较好的抗菌活性。综上所述,单一涂膜剂由于其自身组成和结构,成膜性、机械性、阻隔性、稳定性等可能存在不足,复配后效果更好。
基于此,为明确黄绿卷毛菇多糖(Floccularia luteovirens polysaccharides,FLPs)与CS、CMC基质混合制备的复合保鲜涂膜对金枪鱼贮藏期间的保鲜效果,本研究以鲜切金枪鱼鱼片作为材料,研究FLPs与CS、CMC基质复合保鲜涂膜对贮藏期间鲜切金枪鱼鱼片的汁液流失率、菌落总数、挥发性盐基氮(total volatile basic nitrogen,TVB-N)、硫代巴比妥酸(thiobarbituric acid reactive substances,TBARS)、脂肪氧化和感官品质劣变的影响,为可食性涂膜在金枪鱼鱼片贮藏保鲜中的应用提供参考。
1 材料与方法
1.1 材料与试剂
FLPs,实验室制备;金枪鱼(鲜切鱼片)背部肌肉,舟山平太荣远洋渔业集团有限公司;平板计数琼脂(分析纯),上海博微生物科技有限公司;氧化镁、硼酸、TBARS(均为分析纯),国药集团化学试剂有限公司;CS(食品级),上海阿拉丁生化科技有限公司;CMC(食品级),济南允诚生物科技有限公司。
1.2 仪器与设备
Biomate 3S紫外可见分光光度计,上海超体生物科技有限公司;DHR-1流变仪,美国沃特斯有限公司;Zetasizer Nano ZS纳米粒度、Zeta电位分析仪,英国马尔文仪器有限公司;S-25 pH计,梅特勒-托利多仪器(上海)有限公司;C-MAG-HS-4磁力搅拌器,德国IKA公司;HH-S4恒温数显水浴锅,江苏盛蓝仪器制造有限公司;KDN-102凯氏定氮仪,上海纤检仪器有限公司;LS-BSOL压力蒸汽灭菌器,上海申安医疗器械厂。
1.3 实验方法
1.3.1 FLPs复合保鲜涂膜的制备
将1.5 g CS溶于50 mL 2%(体积分数)乙酸溶液中,60 ℃下磁力搅拌至完全溶解,得到0.03 g/mL的CS溶液,再分别配置4 mg/L、8 mg/L的FLPs溶液,按照1∶1体积比复配,加入0.6 g甘油后充分混合,制备出CS复合涂膜液。将2 g CMC充分溶解在100 mL去离子水中配制成0.02 g/mL的CMC溶液,分别与4 mg/L、8 mg/L的FLPs溶液1∶1体积比复配后充分混匀制备出CMC复合涂膜液。
1.3.2 金枪鱼肉前处理
将10 g左右新鲜的金枪鱼背部肌肉在无菌条件下进行切片(4 cm×4 cm×1 cm)。将样品随机分为7组用于涂膜处理,包括3个CS处理组(CS、CS-4 mg/L FLPs、CS-8 mg/L FLPs)和3个CMC处理组(CMC、CMC-4 mg/L FLPs和CMC-8 mg/L FLPs)以及空白对照组。各组样品在相应溶液中浸泡10 min[鱼片与溶液料液比约1∶3(g∶mL)]后沥干,密封在聚乙烯袋后平放在托盘里置于4 ℃的冰箱中贮藏,分别在第0、2、4、6、8和10天取样测定。
1.3.3 复合涂膜液性能表征的测定
1.3.3.1 抗氧化活性的测定
参照DAI等[16]文献中的方法测定FLPs复合保鲜涂膜的DPPH自由基清除率并稍作修改,具体操作如下:将样品组、对照组及空白组充分混匀后避光孵育30 min,随后通过离心分离获得上清液,利用紫外分光光度计于517 nm波长下测定各组吸光值,根据公式(1)计算DPPH自由基清除率:
DPPH自由基清除率![]()
(1)
式中:a,2 mL乙醇+2 mL的DPPH-乙醇溶液(0.2 mmol/L)在517 nm处的吸光度值;b,2 mL样品+乙醇(体积分数为75%)在517 nm处的吸光值;c,2 mL样品+DPPH-乙醇溶液(0.2 mmol/L)在517 nm处的吸光值。
1.3.3.2 Zeta电位的测定
参照LIANG等[17]的方法,使用纳米粒度电位仪测定涂膜液的Zeta电位。
1.3.3.3 流变特性的测定
参照LIANG等[17]的方法略作修改,通过食品流变仪测定涂膜液流变特性,温度设定为25 ℃,剪切速率范围设定为0.1~200 s-1,记录FLPs复合保鲜涂膜动态黏度随剪切速率变化曲线。
1.3.4 复合保鲜涂膜对金枪鱼片保鲜效果
1.3.4.1 pH测定
按照GB/T 5009.237—2016《食品安全国家标准 食品pH值的测定》中方法测定,使用校正后的pH计测量各组金枪鱼鱼片样品的pH值。
1.3.4.2 汁液流失率测定
参照李凯龙等[18]文献中的方法测定金枪鱼鱼片的汁液流失率,即分别称量金枪鱼鱼片在贮藏前的质量(m0)和贮藏一段时间后的质量(mt),根据公式(2)计算其汁液流失率:
汁液流失率![]()
(2)
1.3.4.3 TVB-N值测定
按照GB 5009.228—2016《食品安全国家标准 食品中挥发性盐基氮的测定》中方法测定,对各组金枪鱼鱼片样品的总TVB-N值进行测定。
1.3.4.4 TBARS值测定
参考ZOU等[19]方法测定TBARS值的方法并稍作修改。称取7.5 g三氯乙酸和0.1 g EDTA,加入100 mL去离子水充分溶解。称取5 g金枪鱼肉加入配置溶液,8 000 r/min均质1 min,静置30 min后离心过滤。将5 mL滤液与等体积的0.02 mol/L TBARS溶液混匀沸水浴30 min。冷却至室温,532 nm处测定吸光度,结果以mg丙二醛(malondialdehyde, MDA)/kg金枪鱼鱼片样品表示。
1.3.4.5 菌落总数的测定
按照GB 4789.2—2022《食品安全国家标准 食品微生物学检验 菌落总数测定》中方法测定,用平板计数法对各组金枪鱼鱼片样品的菌落总数进行测定,结果以lg CFU/g表示。
1.3.4.6 金枪鱼鱼片感官品质测定
参照KAEWPRACHU等[20]方法对金枪鱼鱼片进行感官分析并略作修改。将由8名受过训练的专家小组成员采用9分制对不同感官属性的金枪鱼鱼片进行评估,主要包括鱼片总体品质、气味、颜色和质地4项指标,其中9.0~7.0分表示鱼片具有非常好或高的可接受性,6.9~4.0表示鱼片具有良好或中等的可接受性,3.9~1.0则代表鱼片不可被接受。
1.4 数据统计与分析
使用Excel 2021对数据进行整理,实验结果使用SPSS 23.0统计软件进行单因素方差分析(ANOVA),并用Duncan法进行多重比较,差异显著的标准为P<0.05。各组实验重复3次,数据表示为“平均值±标准差”。
2 结果与分析
2.1 FLPs复合保鲜涂膜的DPPH自由基清除率
DPPH自由基清除率是评价材料抗氧化能力的关键指标,清除率越高,表明活性成分对自由基的中和能力越强。如图1所示,CS涂膜和CMC涂膜的自由基清除率为17.79%和10.36%,而添加4 mg/L、8 mg/L FLPs的复合涂膜清除率分别提升至47.21%、64.71%、34.79%、49.81%,较CS组和CMC组分别增加29.42%、46.92%、24.43%、39.45%。这与KUMAR等[15]和ERANDA等[21]研究结论相印证,其研究表明CS及其衍生物通过自由基清除和金属离子螯合作用展现出显著的抗氧化活性,而添加来自植物多酚的天然抗氧化剂可进一步提高CS的抗氧化值。本实验结果进一步显示,DPPH自由基清除率随FLPs添加量的增加呈显著上升趋势。特别值得注意的是,本实验制备的FLPs复合保鲜涂膜表现出良好的DPPH自由基清除率(最高达64.71%),表明FLPs不仅可以作为独立抗氧化成分,还可通过与CS的协同作用进一步增强复合保鲜涂膜的抗氧化能力。
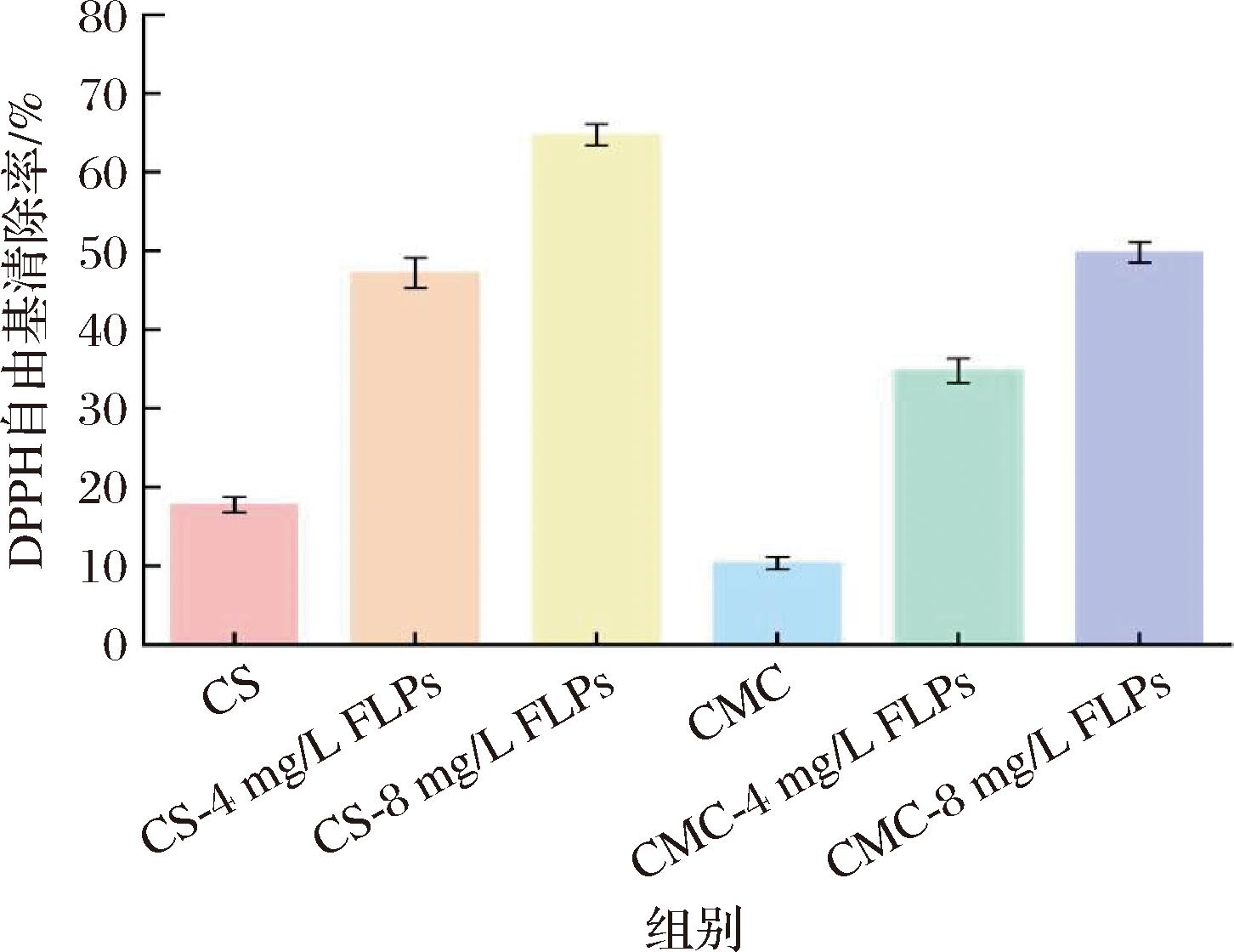
图1 FLPs复合保鲜涂膜的DPPH自由基清除率
Fig.1 The DPPH free radical scavenging rate of FLPs composite preservation coating
2.2 FLPs复合保鲜涂膜的Zeta电位
Zeta电位是表征乳液体系稳定性的关键参数之一。基于HUANG等[22]提出的胶体稳定性理论,当分散相颗粒的Zeta电位绝对值大于30 mV时,静电排斥作用可有效克服范德华引力,从而使体系处于高度稳定状态。如图2所示,本研究中所制备的FLPs复合保鲜涂膜的Zeta电位绝对值均大于30 mV,表明该保鲜涂膜的体系较稳定,这一特性有助于涂膜液在鱼肉表面形成致密、连续的阻隔层,进而延缓水分流失与微生物侵染,提升保鲜效能。上述胶体稳定性理论在CS基复合膜的实际应用中得到了广泛验证。例如,WANG等[23]在酸浆花萼总黄酮-CS复合膜的制备中发现,当复合膜体系的Zeta电位绝对值达到稳定阈值时(>30 mV),其形成的致密阻隔层可显著抑制冰鲜牛肉的水分迁移与脂质氧化,这一机制与本研究中CS-FLPs复合涂膜通过高Zeta电位(正值大于30 mV)维持金枪鱼保鲜效能的路径高度吻合。
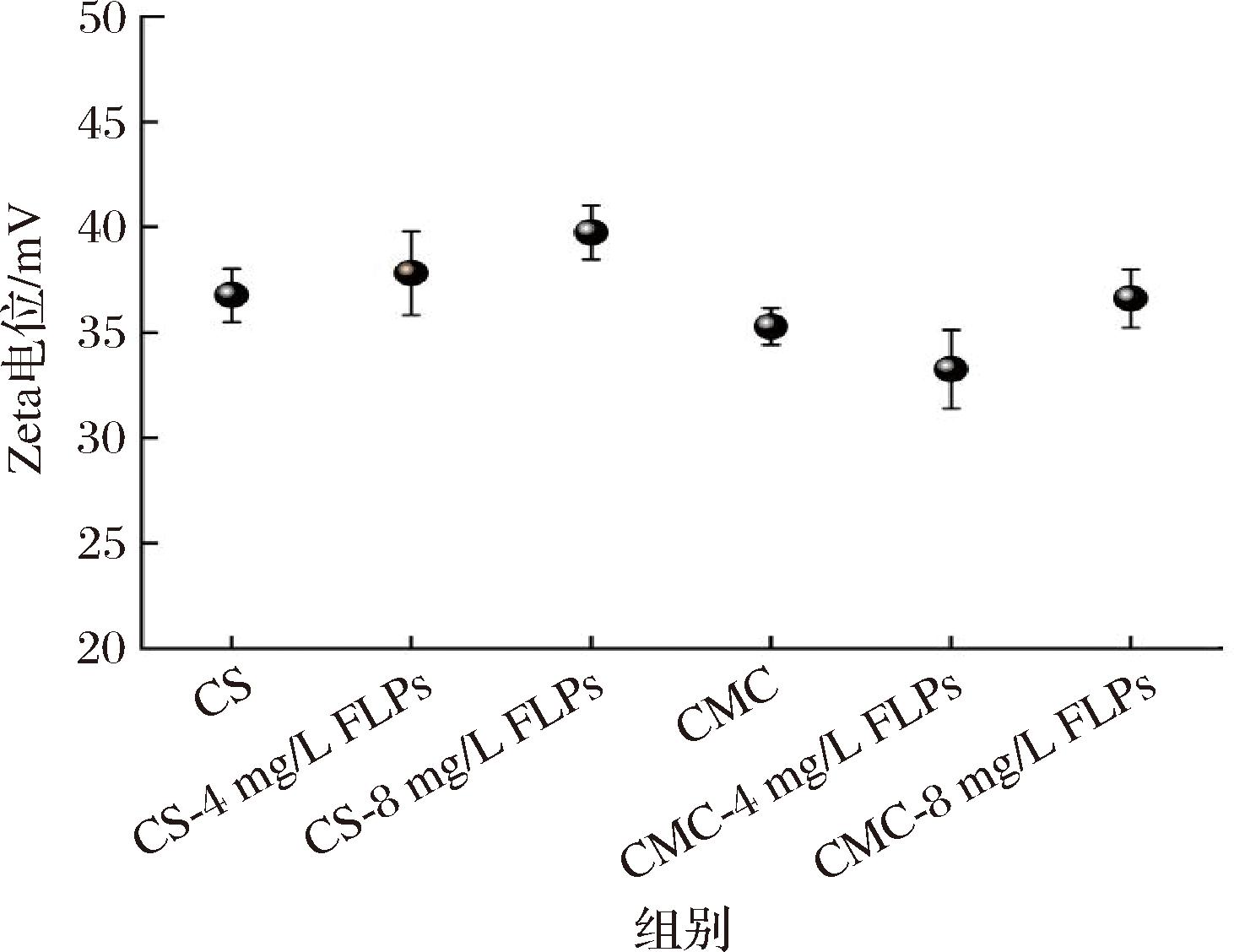
图2 FLPs复合保鲜涂膜的Zeta电位
Fig.2 Zeta potential of FLPs composite preservation coating
2.3 FLPs复合保鲜涂膜流变特性分析
流变学特性分析结果表明,CS与CMC基涂膜体系均呈现典型的假塑性流体特征。如图3所示,在剪切速率递增过程中,各实验组溶液黏度呈现规律性衰减,这种剪切稀化现象与高分子溶液的流变学特性相吻合。值得注意的是,当FLPs添加比例提升时,溶液内大分子链缠结程度加剧,导致体系黏弹性显著增强。但流变测定数据显示所有样品在测试范围内的动态黏度始终维持在7 Pa·s阈值之下,这与DU等[24]提出的涂膜液稳定性判定标准(η<0.7 Pa·s)高度吻合。该现象证实了各梯度涂膜体系具有理想的均质分散特性,其三维网络结构能有效维持系统稳定性,避免因局部黏度过载导致的成膜不均问题。
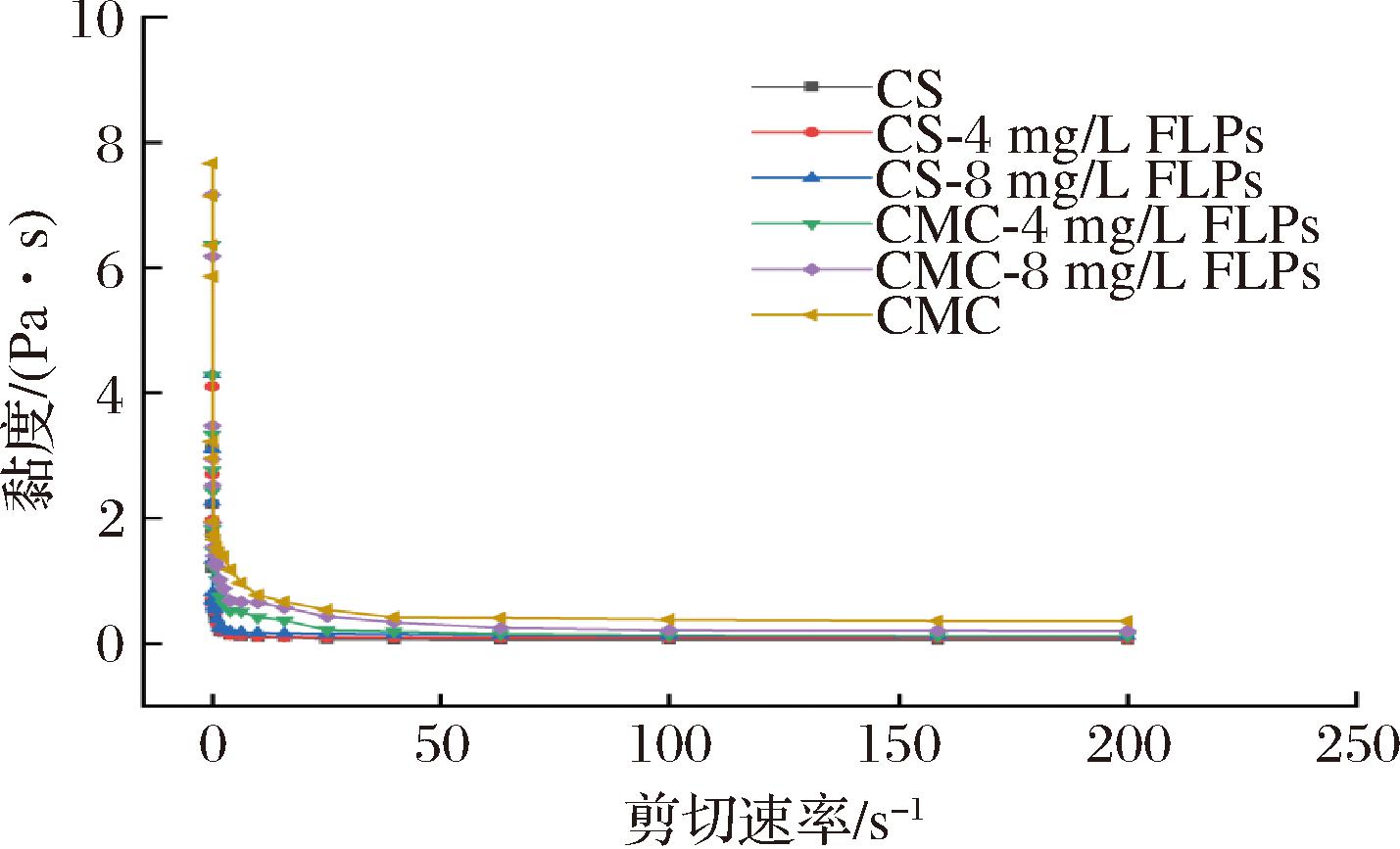
图3 FLPs复合保鲜涂膜的流变特性
Fig.3 Rheological properties of FLPs composite preservation coating
2.4 FLPs复合保鲜涂膜对金枪鱼鱼片pH的影响
图4为不同FLPs复合涂膜对金枪鱼鱼片涂膜后贮藏期间pH值的变化。7组样品pH值随贮藏时间的延长呈现先下降后上升的趋势,这与XIAO等[25]的研究中pH值的变化趋势一致。在鱼死亡初期,鱼肌肉中ATP会分解产生有机酸以及糖原降解后产生乳酸,导致样品组pH值下降[26]。而在贮藏第4天,pH值出现上升是因为鱼肉被蛋白酶和微生物分解产生碱性化合物,如氨、三甲胺和组胺[27]。贮藏期间,与空白对照组相比,经过CS涂膜和CMC涂膜的样品的pH值变化始终较缓慢。在第8天时空白组、CS和CMC对照组的pH值分别达到6.69、6.27、6.40,而添加FLPs的涂膜样品组pH值为5.74~6.20。其中,CS-8 mg/L FLPs处理组pH值的变化速率最缓慢,说明其效果最好。这说明FLPs复合涂膜可抑制鱼片贮藏过程中酶和微生物的作用,减缓pH值的变化,进而延长金枪鱼的货架期。
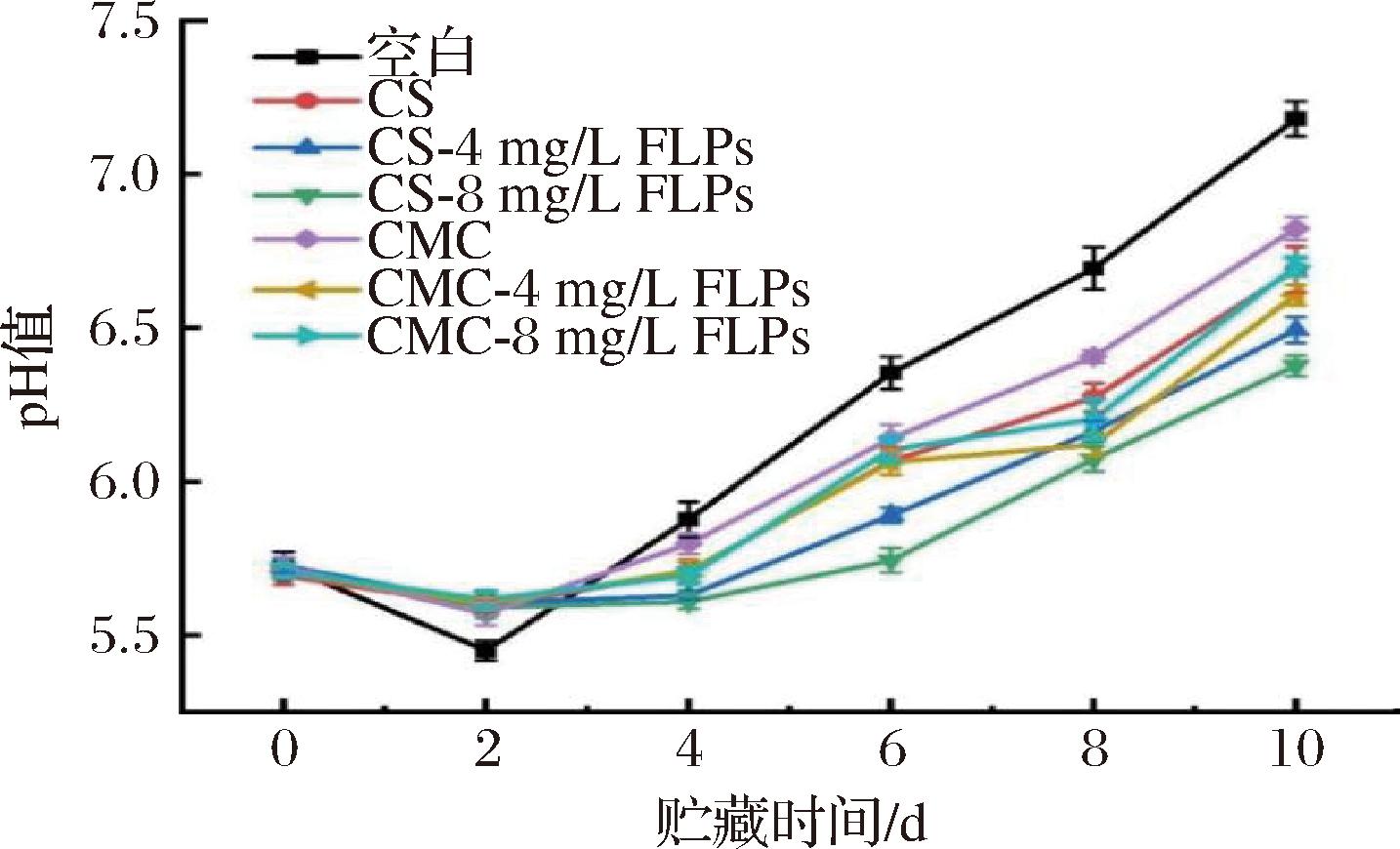
图4 FLPs复合保鲜涂膜对金枪鱼鱼片pH的影响
Fig.4 The effect of FLPs composite freshness coating on the pH of tuna fillets
2.5 FLPs复合保鲜涂膜对金枪鱼鱼片汁液流失率的影响
图5为不同FLPs复合液对金枪鱼鱼片涂膜后贮藏期间汁液流失率的变化。在贮藏过程中,各样品处理组的汁液流失率呈现不断增长的趋势,从第2天的0.32%~1.82%增加到第10天的2.66%~7.05%,且空白组显著高于涂膜组(P<0.05)。这说明涂膜处理的金枪鱼表面能够形成保护膜,延缓了营养成分和水分的流失[28]。其中CMC对照组的汁液流失率基本高于CS对照组和复合涂膜组,CS-8 mg/L FLPs组汁液流失率整体最低,其余样品组差异不显著(P>0.05)。这说明了CMC膜液对鱼肉的保护效果有限,CS-8 mg/L FLPs复合膜液能更好地保证鱼肉的新鲜度和营养价值。这一发现与CS基复合膜在水产品保鲜中的应用研究趋势相吻合。例如,WANG等[23]在酸浆花萼总黄酮-CS复合膜对冰鲜牛肉的保鲜研究中发现,添加0.15%总黄酮的CS基组(质量分数,总黄酮与CS的质量比)可将汁液流失率控制在5%以下(11 d)。YU等[29]采用CS/玉米淀粉-蔓越橘花青素纳米复合膜处理南美白对虾,前8 d汁液流失率也稳定低于5%。上述研究与本文中CS-8 mg/L FLPs组(10 d)汁液流失率为2.66%的实验结果均表明,CS基质中引入特定功能成分(如多糖、黄酮类或花青素)可增强涂膜阻隔性和持水性,显著抑制贮藏过程中水产品的水分迁移与营养流失。值得注意的是,尽管目标物种(金枪鱼/牛肉/对虾)和功能添加剂类型不同,但CS基复合膜对汁液流失率的抑制作用具有普适性,进一步验证了该技术路径在食品保鲜领域的应用潜力。
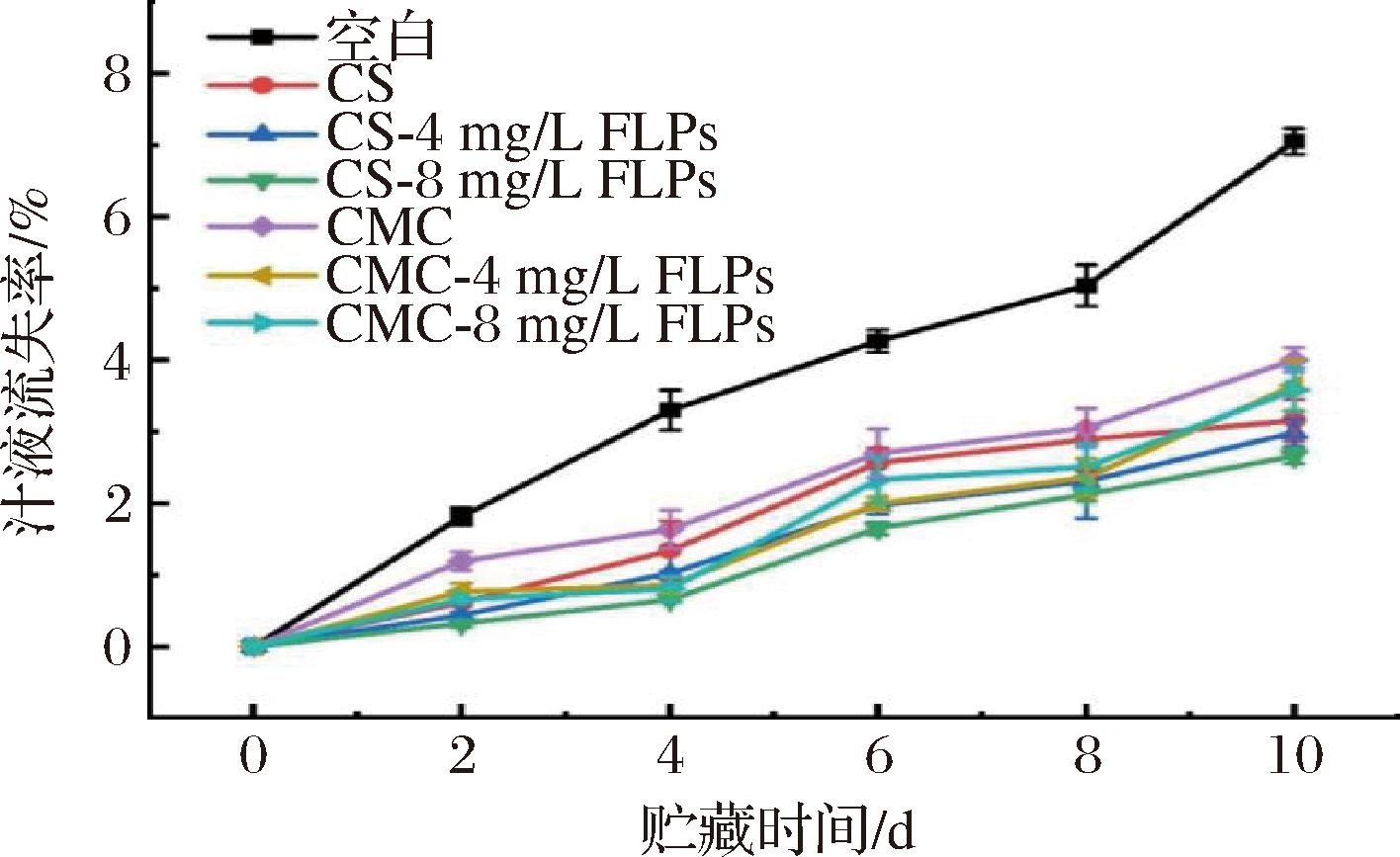
图5 FLPs复合保鲜涂膜对金枪鱼鱼片汁液流失率的影响
Fig.5 The effect of FLPs composite freshness coating on the drip loss of tuna fillets
2.6 FLPs复合保鲜涂膜对金枪鱼鱼片TVB-N的影响
TVB-N常被用于评估鱼类初期腐败,当TVB-N值低于15 mg/100 g时,可判定为优级品,当该值高于30 mg/100 g时,则可视为已完全腐败,消费者不能接受[30]。图6为不同的FLPs复合液对金枪鱼鱼片涂膜后贮藏期间TVB-N的变化。未涂膜处理和涂膜处理的金枪鱼鱼肉TVB-N含量在贮藏期间均显著增加(P<0.05),这是由内源酶和/或腐败微生物降解蛋白质产生的氨类物质引起的。第6天时,空白组和CMC组样品的TVB-N值高于可接受限值(30 mg/100 g)[31]。除CS-8 mg/L FLPs外,其他涂膜样品组在贮藏第10天均不符合食用标准,且在抑制TVB-N的生成顺序依次为:CS-4 mg/L FLPs、CMC-4 mg/L FLPs、CS、CMC-8 mg/L FLPs(P<0.05)。实验结果与JIANG等[32]使用明胶水溶性CS结合美拉德肽薄膜保鲜蓝鳍金枪鱼切片的研究结果相似,所有实验组样品贮藏至第4天时鱼片TVB-N值均未超过可接受限值(30 mg/100 g),且CS-8 mg/L FLPs组样品品质接近于优级品。实验表明FLPs的加入使CS和CMC膜液对酶和微生物抑制作用增强,CS-FLPs复合涂膜对延缓鱼片蛋白氧化的作用效果要优于CMC-FLPs复合涂膜,CS-8 mg/L FLPs可延长货架期4 d。
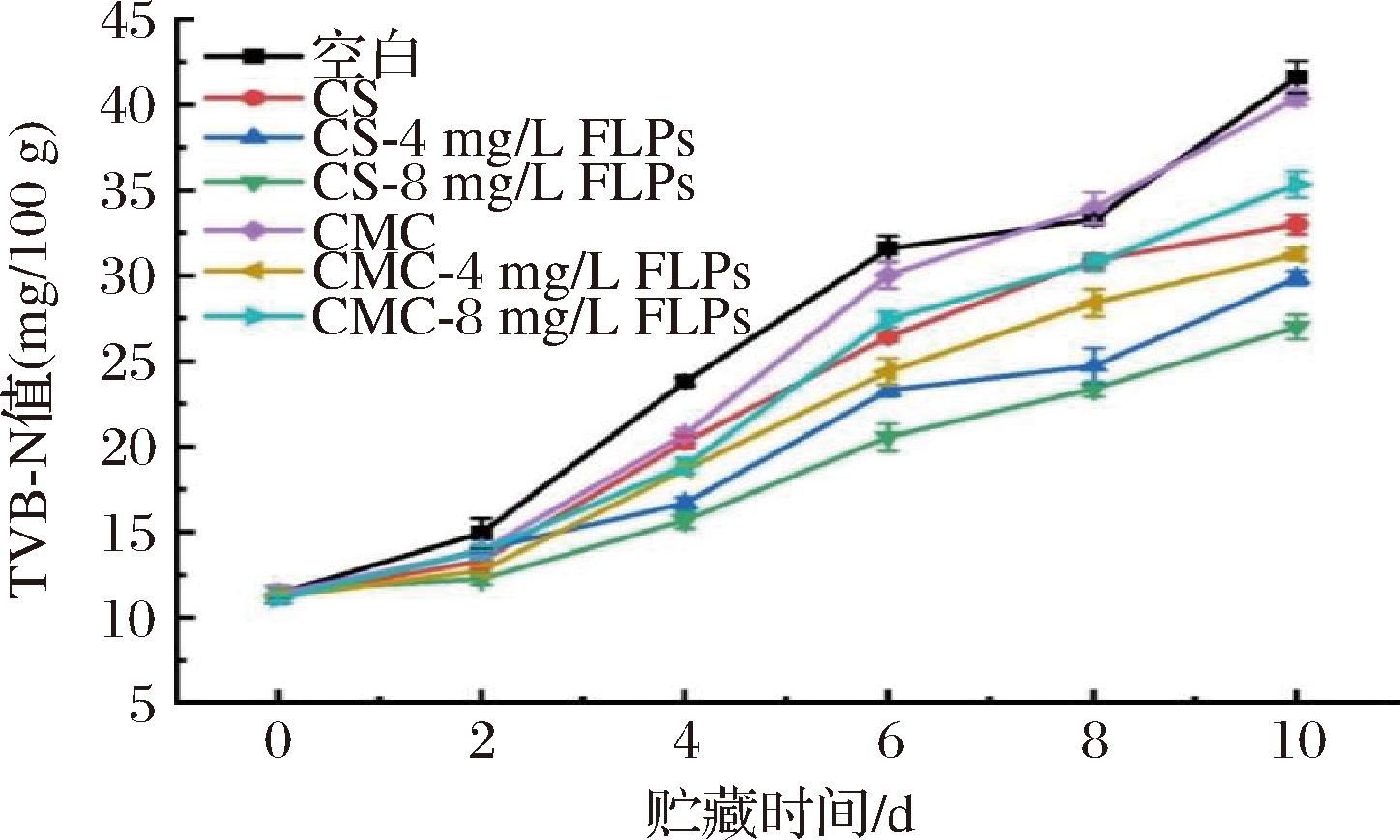
图6 FLPs复合保鲜涂膜对金枪鱼鱼片TVB-N的影响
Fig.6 The effect of FLPs composite freshness coating on the TVB-N of tuna fillets
2.7 FLPs复合保鲜涂膜对金枪鱼鱼片TBARS的影响
TBARS值可衡量水产品中脂肪氧化程度[33]。不同的FLPs复合液对金枪鱼鱼片涂膜后贮藏期间TBARS值的变化如图7所示。随着贮藏时间的延长,7组样品的TBARS水平在不断上升,其中空白组和CMC对照组的上升速率最快。这是由于脂质氢过氧化物和过氧化物降解产物的积累引起的,这些氢过氧化物和过氧化物是在不饱和脂肪酸的氧化过程中产生的[34]。在贮存过程中,脂质氧化会导致鱼品质变差。随着贮存时间的延长,鱼脂肪被氧化分解成游离脂肪酸和过氧化物等简单化合物,进而导致肌肉损伤、鱼肉质量差和TBARS值升高[34]。这一结果与SUN等[35]和ZHANG等[36]的研究中TBARS值变化趋势一致。在贮藏前6 d,其他涂膜的TBARS值差异不显著(P>0.05)。在第10天,CS-8 mg/L FLPs组鱼肉的TBARS值为0.87 mg MDA/kg,比空白组和CS组分别下降了34.59%和28.69%,说明其能够显著地减缓鱼片中TBARS水平的上升速率,这与FLPs良好的抗氧化活性和CS-8 mg/L FLPs形成的涂膜有更好的氧气阻隔性能有关[22]。
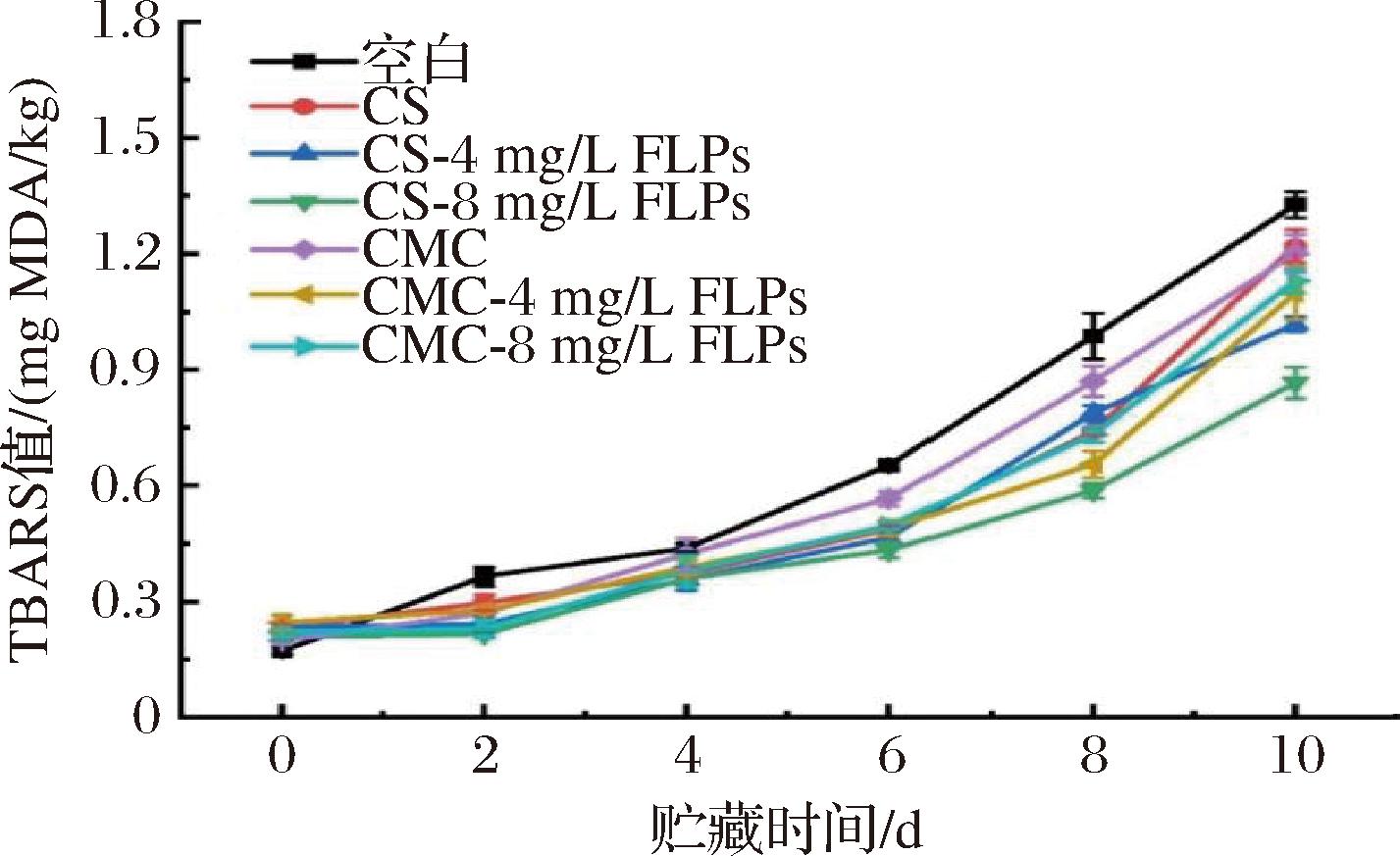
图7 FLPs复合保鲜涂膜对金枪鱼鱼片TBARS的影响
Fig.7 The effect of FLPs composite freshness coating on the TBARS of tuna fillets
2.8 FLPs复合保鲜涂膜对金枪鱼鱼片菌落总数的影响
如图8所示为不同FLPs复合保鲜涂膜对金枪鱼鱼片涂膜后贮藏期间菌落总数的变化。GB 10136—2015《食品安全国家标准 动物性水产制品》中规定即食生制动物性水产品菌落总数的可接受范围为5 lg CFU/g以下,图8中金枪鱼鱼片的初始菌落总数为2.62 lg CFU/g。所有处理组的菌落总数都随着贮藏时间延长不断增加,从初始的2.62 lg CFU/g至第10天时,CS组、CS-4 mg/L FLPs组、CS-8 mg/L FLPs组、CMC组、CMC-4 mg/L FLPs、CMC-8 mg/L FLPs分别上升至7.48、7.03、6.34、7.38、6.67、6.91 lg CFU/g。其中,CS-8 mg/L FLPs和CMC-4 mg/L FLPs菌落总数分别比空白组降低了22.49%和18.46%,显著低于鱼类的最大食用限量(7 lg CFU/g),0~6 d时菌落总数显著低于即食生制动物性水产品最大限值(5 lg CFU/g)[37]。实验结果与SABU等[2]使用CS和柠檬皮提取物复合涂膜来延长冷藏黄鳍金枪鱼肉的货架期以及BALTI等[38]使用红藻胞外多糖涂膜抑制虾贮藏过程中细菌生长的结果一致,实验组菌落总数含量均显著低于鱼类的最大食用限量(7 lg CFU/g)。这说明CS-8 mg/L FLPs和CMC-4 mg/L FLPs复合涂膜液明显降低了菌落总数水平,通过抑制微生物生长可延长金枪鱼的货架期。
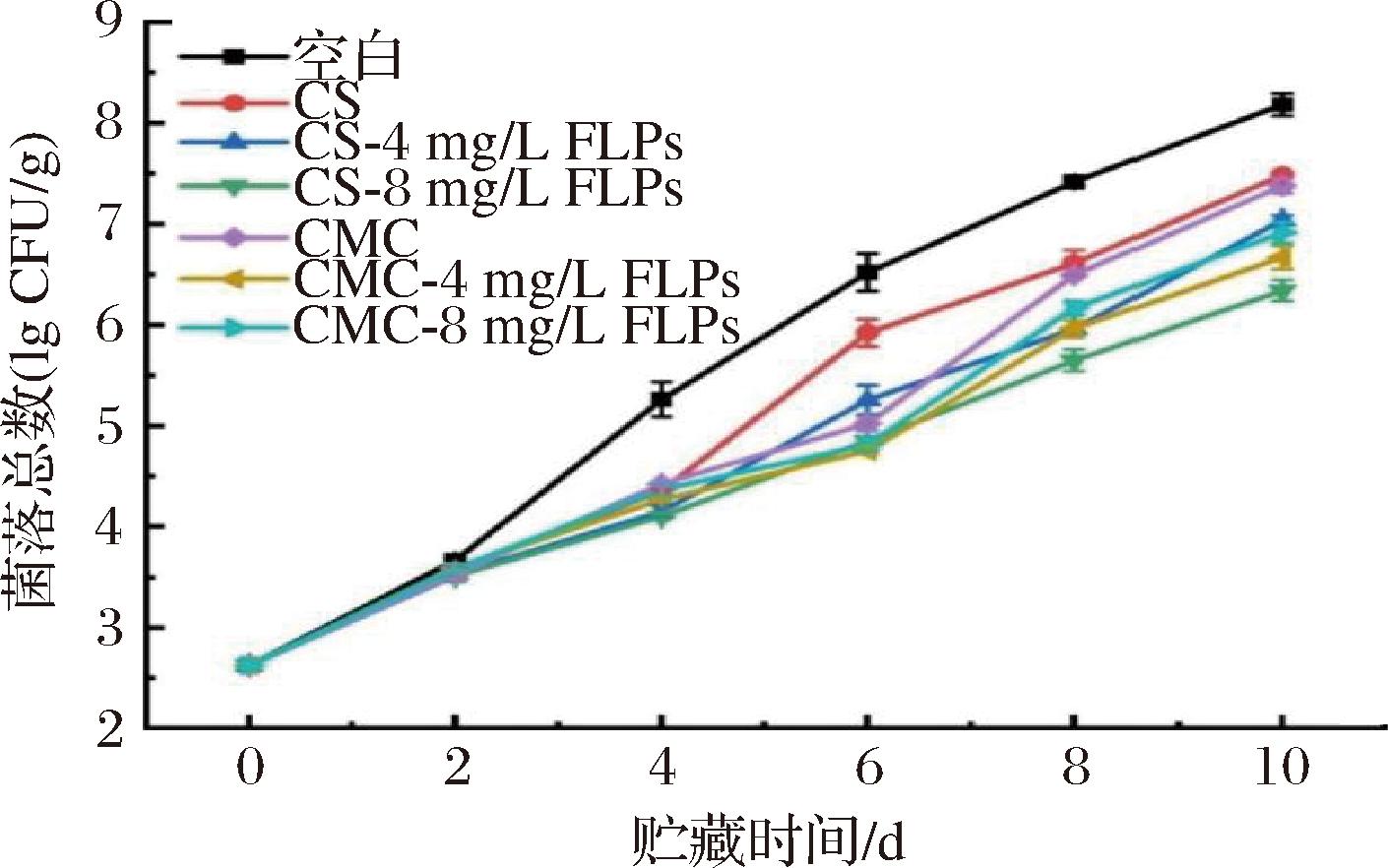
图8 FLPs复合保鲜涂膜对金枪鱼鱼片菌落总数的影响
Fig.8 The effect of FLPs composite freshness coating on the total plate count of tuna fillets
2.9 FLPs复合保鲜涂膜对金枪鱼鱼片感官的影响
图9为不同FLPs复合液对金枪鱼涂膜后贮藏期间感官整体可接受度的变化。在贮藏期间,各处理组中鱼片的质地、气味和色泽都发生了不同程度的劣变,同时其整体品质的可接受度也在不断下降。这一现象可能是与鱼片的营养流失、脂肪蛋白氧化和微生物繁殖等相关。从第4天开始,空白组样品开始出现轻微酸败、变色、质地变软等,而涂膜样品组的各感官上仍有良好的可接受度(P<0.05),说明了鱼片经涂膜后感官品质下降较缓慢。在贮藏中后期(6~10 d),CS-8 mg/L FLPs样品组的整体可接受度评分显著高于其他涂膜组,在贮藏长达10 d后仍具有中等的可接受度(大于3.9分),这表明CS-8 mg/L FLPs处理的金枪鱼仍在可接受度范围内。结果表明,向CS中加入抗氧化物质8 mg/L FLPs能够有效抑制蛋白氧化和脂肪氧化,保证金枪鱼鱼片的新鲜度,延长其货架期。这一实验结果符合CS基涂膜保鲜领域的研究趋势,与JIANG等[32]通过美拉德肽结合CS基对金枪鱼的保鲜实验中观察到金枪鱼片货架期显著延长(空白组2~4 d,美拉德肽组8 d)的结果具有一致性。2项研究共同表明,向CS基质中加入功能性成分(如FLPs或美拉德肽)可协同抑制氧化反应与微生物增殖,有效延缓鱼片感官品质劣变。值得注意的是,本研究中8 mg/L FLPs处理组在贮藏末期(10 d)仍维持中等感官接受度的特性,可能与其多糖分子特有的抗氧化活性(如自由基清除率)及涂膜机械稳定性密切相关,这为拓展天然抗氧化剂在水产品保鲜中的应用提供了新的实验依据。
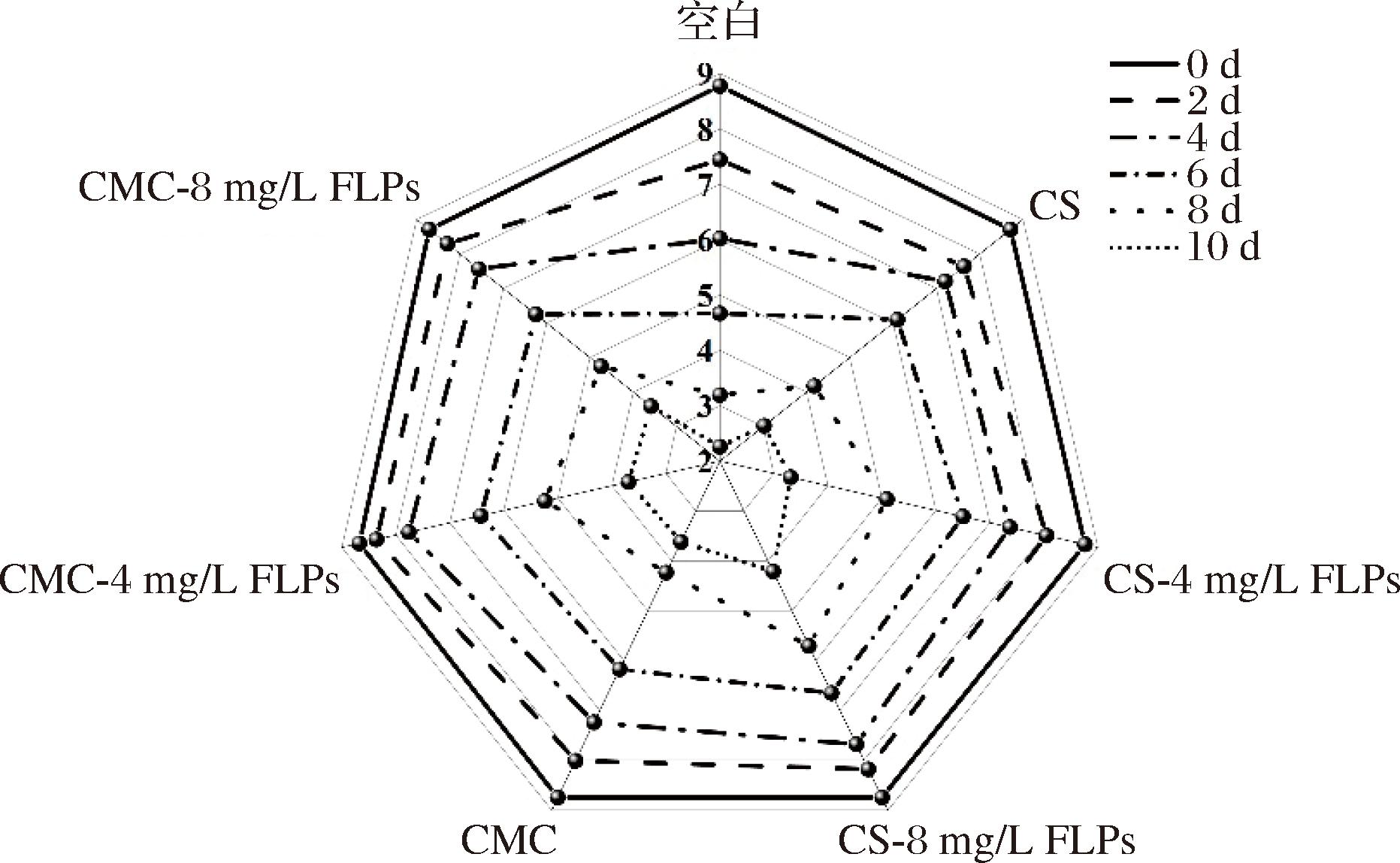
图9 FLPs复合保鲜涂膜对金枪鱼鱼片整体接受度的影响
Fig.9 The effect of FLPs composite freshness coating on the overall acceptability of tuna fillets
3 结论
本文以金枪鱼为研究对象,通过对比CS、CMC、CS-FLPs和CMC-FLPs复合保鲜涂膜对金枪鱼鱼片涂膜保鲜处理后贮藏期间品质的影响,对比pH、汁液流失率、TBARS、TVB-N、菌落总数和感官等指标,评估不同保鲜涂膜组对金枪鱼鱼片的保鲜效果。
结果表明,通过综合对比不同实验组pH的变化速率、汁液流失、脂肪氧化、蛋白分解、微生物生长和感官等重要指标,经涂膜处理的金枪鱼鱼片保鲜效果要显著优于空白对照组(P<0.05)。CS-8 mg/L FLPs涂膜组在贮藏10 d后具有较好的感官接受度,菌落总数、汁液流失率、TVB-N和TBARS值较空白组分别下降了22.49%、4.39%、14.62 mg/100 g、0.46 mg MDA/kg,能够显著减缓金枪鱼鱼片的pH、汁液流失率、TVB-N、TBARS和菌落总数含量的增加,并能较好地维持金枪鱼鱼片的感官,可延长贮藏金枪鱼鱼片的货架期4 d。
[1] CHAMORRO F, CASSANI L, GARCIA-OLIVEIRA P, et al.Health benefits of bluefin tuna consumption:(Thunnus thynnus) as a case study[J].Frontiers in Nutrition, 2024, 11:1340121.
[2] SABU S, ASHITA T, STEPHY S.Chitosan and lemon peel extract coating on quality and shelf life of yellowfin tuna (Thunnus albacares) meat stored under refrigerated condition[J].Indian Journal of Fisheries, 2020, 67(1):114-122.
[3] RAMIREZ-SUAREZ J C, MORRISSEY M T.Effect of high pressure processing (HPP) on shelf life of albacore tuna (Thunnus alalunga) minced muscle[J].Innovative Food Science &Emerging Technologies, 2006, 7(1-2):19-27.
[4] WANG X Y, XIE J, CHEN X J.Differences in lipid composition of Bigeye tuna (Thunnus obesus) during storage at 0 ℃and 4 ℃[J].Food Research International, 2021, 143:110233.
[5] LIU T, TANG Q L, LEI H Y, et al.Preparation, physicochemical and biological evaluation of chitosan Pleurotus ostreatus polysaccharides active films for food packaging[J].International Journal of Biological Macromolecules, 2024, 254:127470.
[6] 丁捷, 刘春燕, 黄彭, 等.果蔬可食性保鲜涂膜技术应用及机理最新研究进展[J].食品与发酵工业, 2023, 49(4):318-327.DING J, LIU C Y, HUANG P, et al.Latest research progress on edible coating applications and their mechanisms in fruits and vegetables[J].Food and Fermentation Industries, 2023, 49(4):318-327.
[7] 李慧, 包海蓉 天然多糖保鲜剂在水产品冷藏中的保鲜机理及应用形式[J].食品与发酵工业, 2021, 47(10):271-277.LI H, BAO H R.Mechanism and application of natural polysaccharide preservatives inaquatic products refrigeration[J].Food and Fermentation Industries, 2021, 47(10):271-277.
[8] HASSAN B, ALI SHAHID CHATHA, HUSSAIN A I, et al.Recent advances on polysaccharides, lipids and protein based edible films and coatings:A review[J].International Journal of Biological Macromolecules, 2018, 109:1095-1107.
[9] ZHANG K, CHEN Q, XIAO J, et al.Physicochemical and functional properties of chitosan-based edible film incorporated with Sargassum pallidum polysaccharide nanoparticles[J].Food Hydrocolloids, 2023, 138:108476.
[10] ZHAO Y L, ZHOU S Y, XIA X D, et al.High-performance carboxymethyl cellulose-based hydrogel film for food packaging and preservation system[J].International Journal of Biological Macromolecules, 2022, 223:1126-1137.
[11] JANNATYHA N, SHOJAEE-ALIABADI S, MOSLEHISHAD M, et al.Comparing mechanical, barrier and antimicrobial properties of nanocellulose/CMC and nanochitosan/CMC composite films[J].International Journal of Biological Macromolecules, 2020, 164:2323-2328.
[12] DEVLIEGHERE F, VERMEULEN A, DEBEVERE J.Chitosan:Antimicrobial activity, interactions with food components and applicability as a coating on fruit and vegetables[J].Food Microbiology, 2004, 21(6):703-714.
[13] LAN W T, HE L, LIU Y W.Preparation and properties of sodium carboxymethyl cellulose/sodium alginate/chitosan composite film[J].Coatings, 2018, 8(8):291.
[14] NASIBI S, NARGESI KHORAMABADI H, AREFIAN M, et al.A review of Polyvinyl alcohol/Carboxiy methyl cellulose (PVA/CMC) composites for various applications[J].Journal of Composites and Compounds, 2020, 2(3):68-75.
[15] KUMAR S, MUKHERJEE A, DUTTA J.Chitosan based nanocomposite films and coatings:Emerging antimicrobial food packaging alternatives[J].Trends in Food Science &Technology, 2020, 97:196-209.
[16] DAI Q Y, HUANG X, JIA R J, et al.Development of antibacterial film based on alginate fiber, and peanut red skin extract for food packaging[J].Journal of Food Engineering, 2022, 330:111106.
[17] LIANG D Y, WANG C J, LUO X M, et al.Preparation, characterization and properties of cinnamon essential oil nano-emulsion formed by different emulsifiers[J].Journal of Drug Delivery Science and Technology, 2023, 86:104638.
[18] 李凯龙, 徐文泱, 向俊, 等.含肉桂精油的壳聚糖涂层对冷藏草鱼片的保鲜作用[J].食品与发酵工业, 2022, 48(3):226-232.LI K L, XU W Y, XIANG J, et al.The preservative effect of chitosan coatings enriched with cinnamon oil on refrigerated grass carp flakes[J].Food and Fermentation Industries, 2022, 48(3):226-232.
[19] ZOU J H, LIU X M, WANG X P, et al.Influence of gelatin-chitosan-glycerol edible coating incorporated with chlorogenic acid, gallic acid, and resveratrol on the preservation of fresh beef[J].Foods, 2022, 11(23):3813.
[20] KAEWPRACHU P, OSAKO K, BENJAKUL S, et al.Shelf life extension for Bluefin tuna slices (Thunnus thynnus) wrapped with myofibrillar protein film incorporated with catechin-Kradon extract[J].Food Control, 2017, 79:333-343.
[21] ERANDA D H U, CHAIJAN M, PANPIPAT W, et al.Gelatin-chitosan interactions in edible films and coatings doped with plant extracts for biopreservation of fresh tuna fish products:A review[J].International Journal of Biological Macromolecules, 2024, 280:135661.
[22] HUANG M Y, WANG H H, XU X L, et al.Effects of nanoemulsion-based edible coatings with composite mixture of rosemary extract and ε-poly-l-lysine on the shelf life of ready-to-eat carbonado chicken[J].Food Hydrocolloids, 2020, 102:105576.
[23] WANG J M, LI Z T, WU X R, et al.Preparation of Physalis alkekengi L.Calyx total flavonoids-chitosan composite film and its effect on preservation of chilled beef[J].International Journal of Biological Macromolecules, 2024, 283(Pt 2):137768.
[24] DU H J, HU Q H, YANG W J, et al.Development, physiochemical characterization and forming mechanism of Flammulina velutipes polysaccharide-based edible films[J].Carbohydrate Polymers, 2016, 152:214-221.
[25] XIAO Z K, LIU C Y, RONG X Y, et al.Development of curcumin-containing polyvinyl alcohol/chitosan active/intelligent films for preservation and monitoring of Schizothorax prenanti fillets freshness[J].International Journal of Biological Macromolecules, 2023, 253:127343.
[26] FU L L, RU Y, HONG Q L, et al.Active packaging coatings based on agarose caffeate:Preparation, characterisation, and application in grass carp (Ctenopharyngodon idellus) preservation[J].Food Packaging and Shelf Life, 2023, 37:101089.
[27] CAI M H, ZHONG H, LI C Z, et al.Application of composite coating of Nostoc commune Vauch polysaccharides and sodium carboxymethyl cellulose for preservation of salmon fillets[J].International Journal of Biological Macromolecules, 2022, 210:394-402.
[28] LIU J L, LAN W Q, SUN X H, et al.Effects of chitosan grafted phenolic acid coating on microbiological, physicochemical and protein changes of sea bass (Lateolabrax japonicus) during refrigerated storage[J].Journal of Food Science, 2020, 85(8):2506-2515.
[29] YU Y H, XU J L, XU J, et al.Preparation and characterization of chitosan/corn starch based films loaded with Vaccinium vitis-idaea anthocyanin nano complexes and the application in shrimp preservation[J].International Journal of Biological Macromolecules, 2025, 303:140734.
[30] PRABHAKAR P K, VATSA S, SRIVASTAV P P, et al.A comprehensive review on freshness of fish and assessment:Analytical methods and recent innovations[J].Food Research International, 2020, 133:109157.
[31] TAPILATU Y, NUGRAHENI P S, GINZEL T, et al.Nano-chitosan utilization for fresh yellowfin tuna preservation[J].Aquatic Procedia, 2016, 7:285-295.
[32] JIANG W, HU S W, LI S J, et al.Evaluation of the preservation effect of gelatin-water soluble chitosan film incorporated with Maillard peptides on bluefin tuna (Thunnus thynnus) slices packaging[J].LWT, 2019, 113:108294.
[33] 陈露珠, 李念, 裴诺, 等.普鲁兰多糖/羧甲基壳聚糖复合膜的制备及其对罗氏沼虾的保鲜效果[J].食品与发酵工业, 2021, 47(24):137-143.CHEN L Z, LI N, PEI N, et al.Preparation of pullulan/carboxymethyl chitosan composite membrane and its fresh-keeping effect on Macrobrachium rosenbergii[J].Food and Fermentation Industries, 2021, 47(24):137-143.
[34] SUN L J, SUN J J, THAVARAJ P, et al.Effects of thinned young apple polyphenols on the quality of grass carp (Ctenopharyngodon idellus) surimi during cold storage[J].Food Chemistry, 2017, 224:372-381.
[35] SUN X Y, GUO X B, JI M Y, et al.Preservative effects of fish gelatin coating enriched with CUR/βCD emulsion on grass carp (Ctenopharyngodon idellus) fillets during storage at 4 ℃[J].Food Chemistry, 2019, 272:643-652.
[36] ZHANG M M, TAO N P, LI L, et al.Non-migrating active antibacterial packaging and its application in grass carp fillets[J].Food Packaging and Shelf Life, 2022, 31:100786.
[37] ZHAO X, CHEN L, WONGMANEEPRATIP W, et al.Effect of vacuum impregnated fish gelatin and grape seed extract on moisture state, microbiota composition, and quality of chilled seabass fillets[J].Food Chemistry, 2021, 354:129581.
[38] BALTI R, BEN MANSOUR M, ZAYOUD N, et al.Active exopolysaccharides based edible coatings enriched with red seaweed (Gracilaria gracilis) extract to improve shrimp preservation during refrigerated storage[J].Food Bioscience, 2020, 34:100522.