蛋白质是人体发育和维持人体健康的重要营养物质。目前,动物蛋白仍然是人类膳食蛋白的重要来源。预计到2050年,全球对动物蛋白的需求将翻一番[1]。然而,由于人们对环境、动物福利和健康的日益关注,素食主义在近些年越来越受欢迎。因此,使用植物蛋白源如油籽、谷物和豆类等作为动物蛋白的替代品是满足食物蛋白质需求的好方法。其中,南瓜籽蛋白作为一种新兴的植物蛋白备受关注。南瓜籽粕中蛋白质的比例可达60%~65%[2]。南瓜籽蛋白能满足人体所需的必需氨基酸,尤其是儿童所必需的组氨酸[3]。此外,南瓜籽蛋白还具有降血压、抗氧化、抗衰老等生物活性功能[4]。
在加工过程中,植物蛋白的溶解性、乳化性、起泡性等功能特性对食品的感官品质有重要作用。一般可以通过化学、物理或酶修饰的方法来提高蛋白质的功能特性,以满足其在食品生产中的需要[5]。例如SUN等[6]通过热处理辅助pH偏移的方法制备南瓜籽分离蛋白(pumpkin seed protein isolate,PSPI)纳米颗粒,结果表明,改性后的PSPI乳化性能显著提高,内部油相体积分数可达80%,且乳液的稳定性显著提高。ZHANG等[7]通过碱溶酸沉结合蛋白谷氨酰胺酶对南瓜籽蛋白进行处理,利用酶法脱酰胺显著提高了南瓜籽蛋白的溶解性和乳化性。此外,通过pH偏移结合高强度超声波处理南瓜籽蛋白或表没食子儿茶素没食子酸酯(epigallocatechin gallate,EGCG)共价修饰南瓜籽蛋白,也可以显著提高南瓜籽蛋白的功能特性[8]。但是,针对PSPI的改性研究中,采用热处理这一单一手段的研究相对较少。热处理作为最常见的物理改性方法,与化学修饰相比,不会产生安全问题,并且可以显著降低生产成本[9]。也可以避免酶修饰方法中生物酶反应条件严格、易失活、回收困难、成本高等缺点[9]。已有研究表明,加热或高温处理过的牛奶具有比新鲜牛奶更破碎,更脆的结构,因此更容易被人类消化和吸收[10]。根据YANG等[11]对漆树种子蛋白的研究发现,当加热温度升高时,蛋白质的三级结构解聚,提高了表面疏水性和乳化性能。
本课题组前期研究表明,PSPI的变性温度为87 ℃ 和104 ℃[12]。基于此,本实验设计了在不同热处理温度(80、90、100、120 ℃)分别处理20 min和40 min 后,PSPI结构特性(表面疏水性、内源荧光、二级结构、Zeta电位、粒径、微观结构)和功能特性(溶解性、乳化性、起泡性)的变化,以期为提高PSPI的利用价值提供理论和方法依据。
1 材料与方法
1.1 实验材料
南瓜籽,枣庄华都电子商务有限公司;总蛋白测试盒(考马斯亮蓝法),南京建成生物工程研究所;1-苯胺基萘-8-磺酸(1-anilinonaphthalene-8-sulfonic acid, ANS),阿拉丁化学试剂公司。
1.2 仪器与设备
722可见分光光度计,中国优科仪器有限公司;IKA高速剪切仪,德国IKA集团;Chirascan V100型号仪器,英国应用光物理公司;F-7000荧光分光光度计,日本日立公司;JSM-7610 F,日本东京JEOL公司;Nano ZS 90粒度分析仪,英国马尔文仪器有限公司。
1.3 实验方法
1.3.1 脱脂南瓜籽粉的制备
将南瓜籽粉与正己烷以1∶5(质量比)混合,在40 ℃ 下搅拌1 h进一步除去南瓜籽粉中的脂质,重复3次。最后将混合物在通风橱中干燥(20 ℃)。
1.3.2 不同加热条件下PSPI的制备
以脱脂南瓜籽粉为原料,采用碱溶酸沉法制备PSPI。将南瓜籽粉与去离子水以1∶30(质量比)混合。用1 mol/L NaOH溶液将混合液的pH值调节至10.5,并在室温下搅拌60 min,然后离心(4 000×g)20 min获得上清液。接着,用1 mol/L HCl溶液将上清液的pH值调至4.5。离心(4 000×g)20 min后得到PSPI沉淀,用1 mol/L NaOH溶液中和,透析除盐后进行冷冻干燥。将一定量的PSPI在烘箱中进行热处理(温度为80、90、100、120 ℃,时间为20 min和40 min),对照组(Control)不加热。
1.3.3 溶解性
配制1%(质量分数)的蛋白质溶液,常温搅拌60 min,然后离心(1 800×g)20 min,取上清液。用总蛋白测试盒测定上清液中的蛋白质含量,计算如公式(1)所示:
可溶性蛋白质含量![]()
(1)
1.3.4 乳化特性
参考HUANG等[13]方法测定PSPI的乳化性质,并进行微小修改。将2 mL大豆油和6 mL 0.1%(质量分数)PSPI溶液混合(0.02 mol/L磷酸盐缓冲液,pH 7.0),均质1 min(14 000×g)。分别在均质后的0 min和10 min,从容器底部吸取50 μL乳液,分别用5 mL 0.1%(质量分数)SDS溶液稀释。使用722可见分光光度计在500 nm波长下分析稀释的乳液,分别得到吸光度值A0和吸光度值A10。乳化活性(emulsifying activity indexes, EAI)和乳化稳定性(emulsion stability indexes, ESI)的计算如公式(2)和公式(3)所示:
(2)
(3)
式中:T为常数2.303;A0表示均质后第0 min时吸光值;A10表示均质后第10 min时吸光值;c表示蛋白质的浓度,mg/mL;φ表示油相所占比。
1.3.5 起泡性和起泡稳定性
参考ZHANG等[14]的方法,将0.5 g PSPI溶于10 mL 0.02 mol/L的磷酸盐缓冲溶液(pH 7.0),搅拌1 h。取5 mL PSPI溶液于50 mL离心管中,用IKA高速剪切仪以14 000 r/min的速度对其进行剪切。计算连同空气的连续相的体积(起泡能力),计算如公式(4)所示:
起泡能力![]()
(4)
通过测定在室温条件下静置30 min后泡沫体积相对于原始泡沫体积的百分比,泡沫稳定性的计算如公式(5)所示:
泡沫稳定性![]()
(5)
1.3.6 表面疏水性
利用ANS的荧光探针测定PSPI的表面疏水性(H0)[15]。首先,配制PSPI(2 mg/mL)溶液,涡旋2 min。以4 000×g的转速离心15 min获得的上清液为PSPI储备液,通过总蛋白测试盒测定其浓度。然后用磷酸盐缓冲液将样品稀释到一系列质量浓度(0.02~0.50 mg/mL)。通过磷酸盐溶液(0.01 mol/L,pH7)配制8 mmol/L ANS贮备液。添加20 μL ANS溶液到4 mL样品溶液中,在激发波长为390 nm,发射波长为470 nm,狭缝为5 nm条件下测定混合液的荧光强度。H0指数为荧光强度和蛋白质浓度回归曲线的斜率。
1.3.7 二级结构
参考王晓辉等[16]的方法,将PSPI样品放置于1 mm 的比色皿中,采用Chirascan V100型号仪器测试。测试波长为190~240 nm;扫描速度为100 nm/min;带宽为1 nm;步长1 nm;反应时间为0.5 s;利用CD pro软件分析α-螺旋、β-折叠、β-转角、无规则卷曲相对含量。
1.3.8 粒径及Zeta电位
离心后的蛋白上清液用磷酸盐缓冲液(0.01 mol/L,pH 7.0)稀释至1.0 mg/mL,温度为25 ℃下测量电位与粒径。
1.3.9 内源荧光光谱
参考JIANG等[17]的方法,通过F-7000荧光分光光度计测定PSPI的内源荧光光谱。首先将PSPI(1 mg/mL)分散在磷酸盐缓冲液(0.01 mmol/L,pH 7.0)中。然后在280 nm激发波长和300~400 nm发射波长下测定PSPI溶液的内源荧光。扫描速度为2 400 nm/min。激发和发射狭缝宽度分别设定为5 nm和2.5 nm。
1.3.10 扫描电子显微镜(scanning electron microscope, SEM)
参考KIM等[18]的方法,通过SEM测定PSPI的表面形貌。将干燥样品均匀地放置在双面导胶上,洗耳球吹扫至无蛋白粉末落下,然后在10 kV加速电压下进行喷金,置于扫描电子显微镜下,放大1 000和10 000倍数下观察PSPI样品的形态特征。
1.4 数据分析
所有数据平行测定3次,结果取平均值,采用SPSS 26.0、Nicolet Omnic和Peak Fit 4.12软件对数据进行统计分析,Origin 2018c作图。
2 结果与分析
2.1 不同加热条件对PSPI溶解性的影响
溶解性是蛋白质的一项重要功能特性,对蛋白质的凝胶能力和乳化能力有很大影响。不同加热条件下PSPI样品的溶解性如图1所示。未加热PSPI的溶解性为16.72%。当热处理条件为80 ℃(20 min)、80 ℃(40 min)和90 ℃(20 min),PSPI的溶解性没有发生显著变化(P>0.05)。而当加热条件为90 ℃(40 min)、100 ℃(20 min)、100 ℃(40 min)、120 ℃(20 min)和120 ℃(40 min)时,PSPI的溶解性显著升高(P<0.05),分别提高了39.00%、8.67%、17.94%、32.89%和32.48%。可能是因为这些条件下蛋白分子间的交联和折叠占主导作用,疏水性基团包埋于结构内部,形成一些可溶性聚集体,从而提高了样品的溶解度[19]。
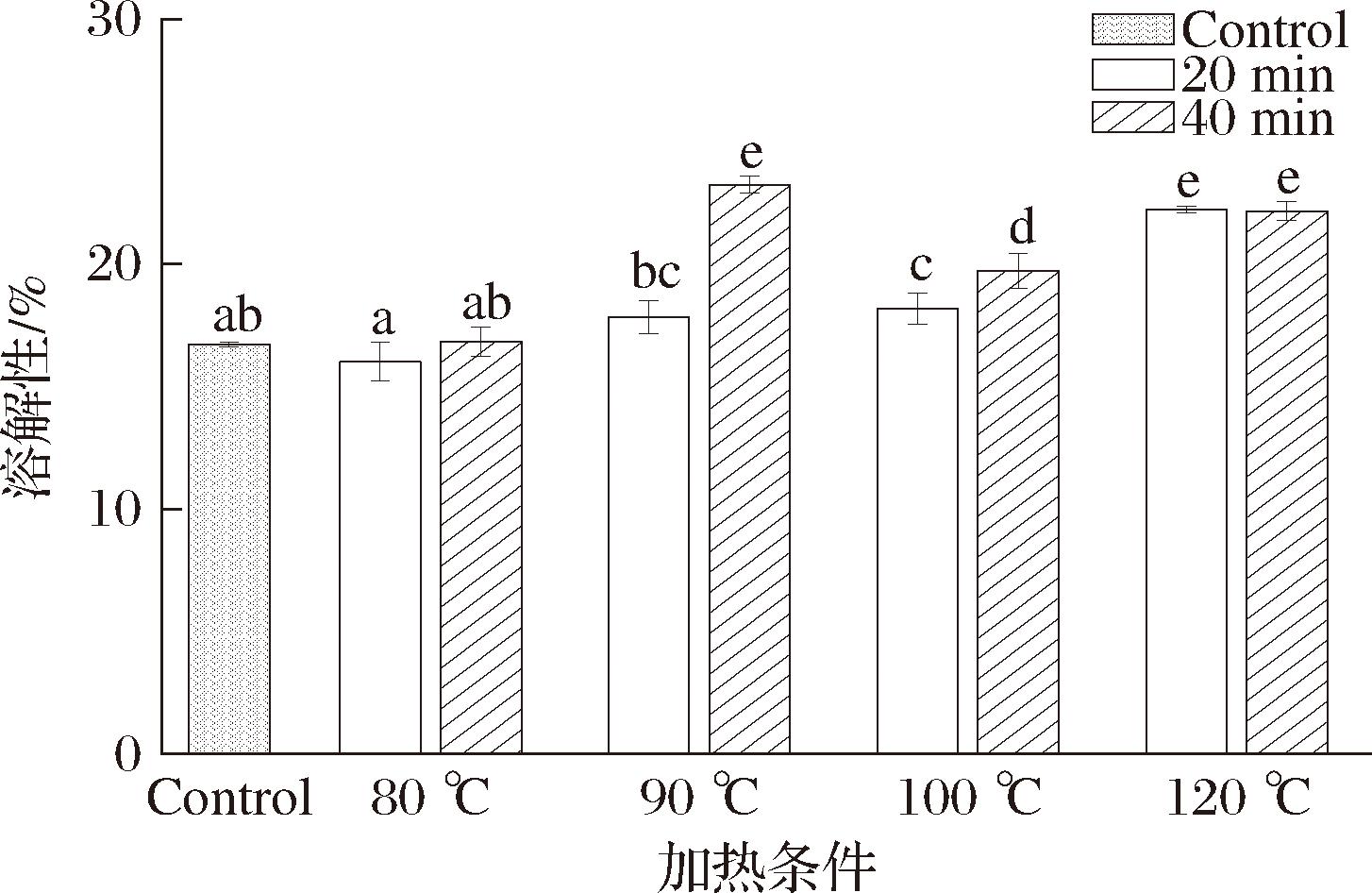
图1 不同加热条件对PSPI蛋白溶解性的影响
Fig.1 Solubility of PSPI under different heat treatments
注:不同小写字母表示差异显著(P<0.05)(下同)。
2.2 不同加热条件对PSPI乳化活性和乳化稳定性的影响
在食品工业中,乳化剂是使用量最大的添加剂之一。蛋白质由于同时具备疏水性和亲水性基团,因此成为乳化剂的重要来源。蛋白质的乳化性受到多种因素的影响,包括其自身的结构因素(如分子大小、表面疏水性、溶解性、分子柔韧性)以及外部环境因素(如pH值和离子强度)。此外,不同的分离方法也会对蛋白质的乳化性产生影响[20]。蛋白质的乳化性主要体现在其在油水界面快速吸附的能力,而乳化稳定性则反映了乳液形成小液滴并保持稳定的应变能力[21]。由图2和图3可知,当加热条件为80 ℃(40 min)、90 ℃(40 min)、100 ℃(40 min)和120 ℃(40 min)时,PSPI样品的乳化活性显著提高(P<0.05),分别提高了118.75%、110.77%、53.59%和72.47 %。当加热条件为90 ℃(20 min)、90 ℃(40 min)、100 ℃(20 min)、100 ℃(40 min)、120 ℃(20 min)和120 ℃(40 min)时,PSPI的乳化稳定性显著升高(P<0.05),分别提高了22.53%、30.39%、88.29%、23.12%、52.20%和29.33%,可能是由于热处理导致了可溶性蛋白聚集体的形成,这些聚集体降低了界面张力,增加了吸附蛋白的数量,进而提高了乳化性能[22]。
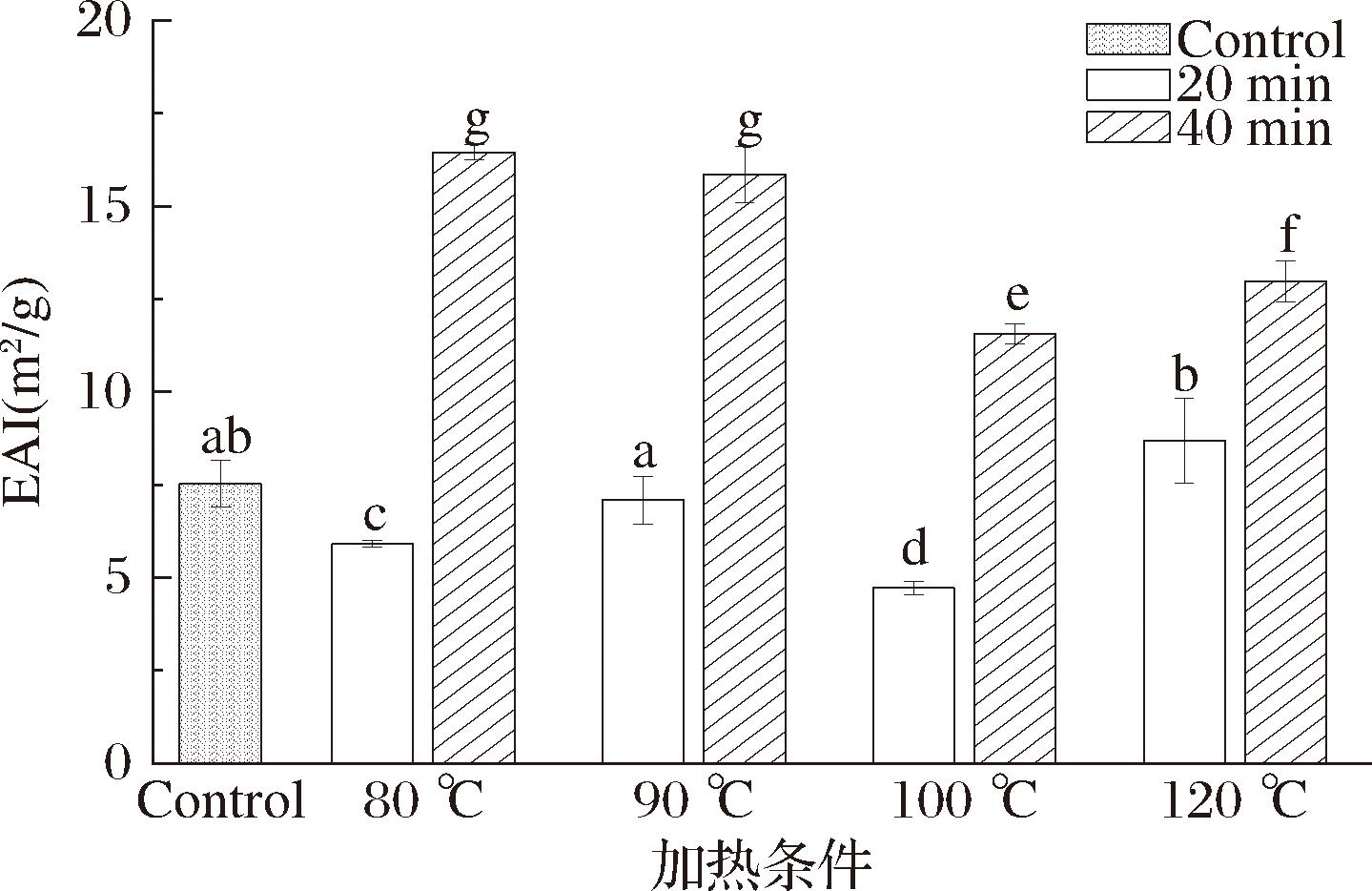
图2 不同加热条件对PSPI乳化活性的影响
Fig.2 Emulsifying activity of PSPI under different heat treatments
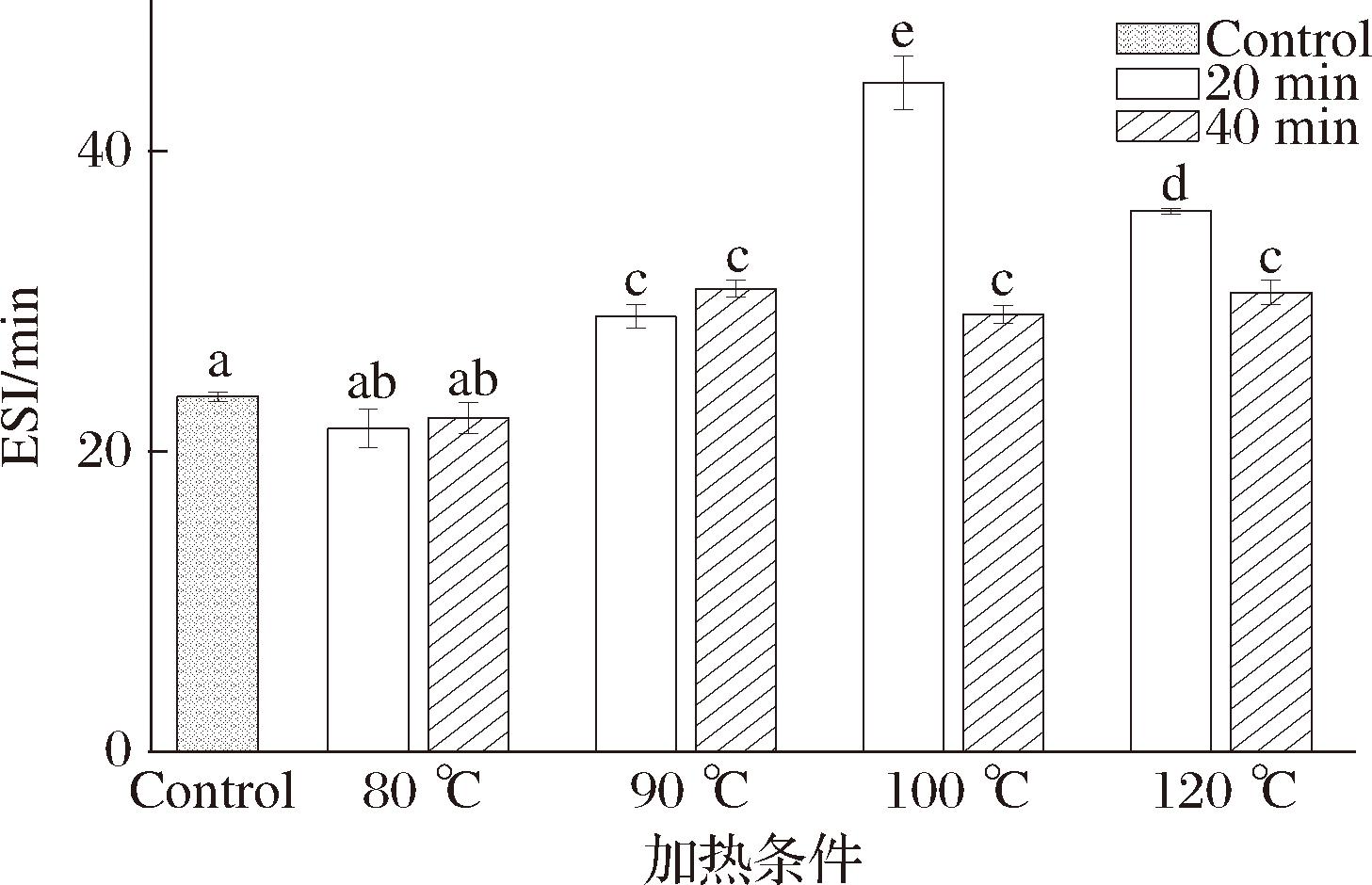
图3 不同加热条件对PSPI乳化稳定性的影响
Fig.3 Emulsifying stability of PSPI under different heat treatments
2.3 不同加热条件对PSPI起泡能力和起泡稳定性的影响
起泡能力指的是蛋白质在气体/空气液滴周围形成一层泡沫的能力。蛋白质的起泡能力不仅取决于其自身的界面性质,如降低表面张力的能力、分子结构的柔韧性、两亲性、电荷分布等物理化学性能,还取决于离子强度、pH、体系、温度、对其他蛋白质的竞争吸附等[23]。起泡稳定性是蛋糕和冰激凌的重要性能。不同加热条件下PSPI的起泡能力和起泡稳定性如图4和图5所示。当加热条件为90 ℃(40 min)、100 ℃(20 min)、100 ℃(40 min)时,PSPI的起泡能力显著提高(P<0.05),分别提高了27.67%、16.67%和24.11%,可能是由于溶解度的提高有助于蛋白质快速到达气-液界面形成泡沫[24]。当加热温度继续升高到120 ℃时,蛋白的起泡能力发生下降,可能是由于加热导致巯基氧化,形成二硫键,同时蛋白质发生过度变性,最终形成更大聚集体,而过多的二硫键阻碍了蛋白质的灵活性,影响了油滴在表面的吸附[25]。但是,热处理不能提高PSPI的起泡稳定性,尤其当加热条件为80 ℃(20 min)和80 ℃(40 min)时,PSPI样品的起泡稳定性降低(P<0.05),分别降低了17.24%和13.74%,可能是蛋白聚集体在气泡表面的吸附不均匀,形成了局部薄弱区域,影响了气泡的稳定性。ZHAO等[26]研究表明热处理结合碱诱导(pH 12)能够提高大米谷蛋白的起泡能力,但不能提高其起泡稳定性。
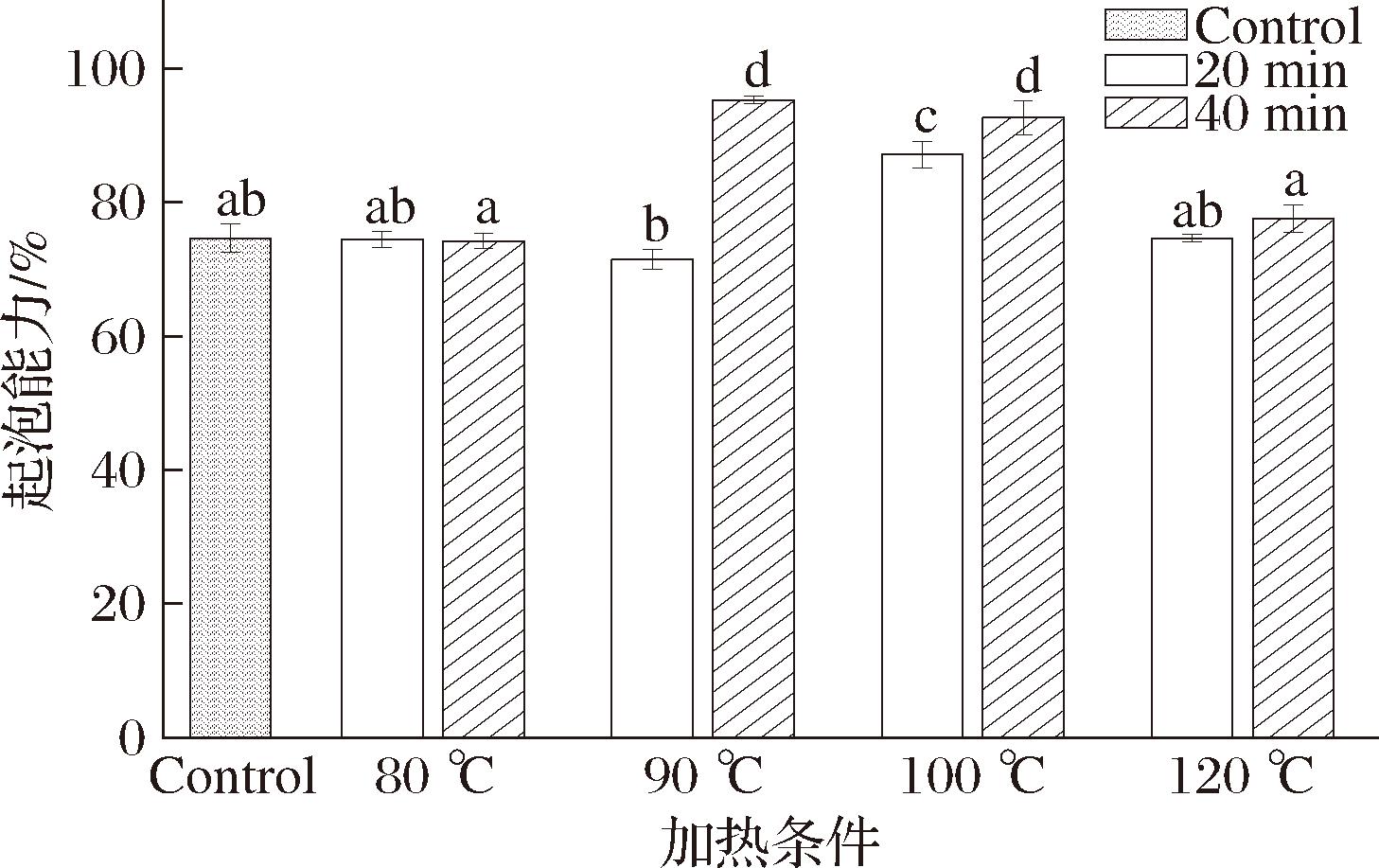
图4 不同加热条件对PSPI起泡能力的影响
Fig.4 Foam ability of PSPI under different heat treatments
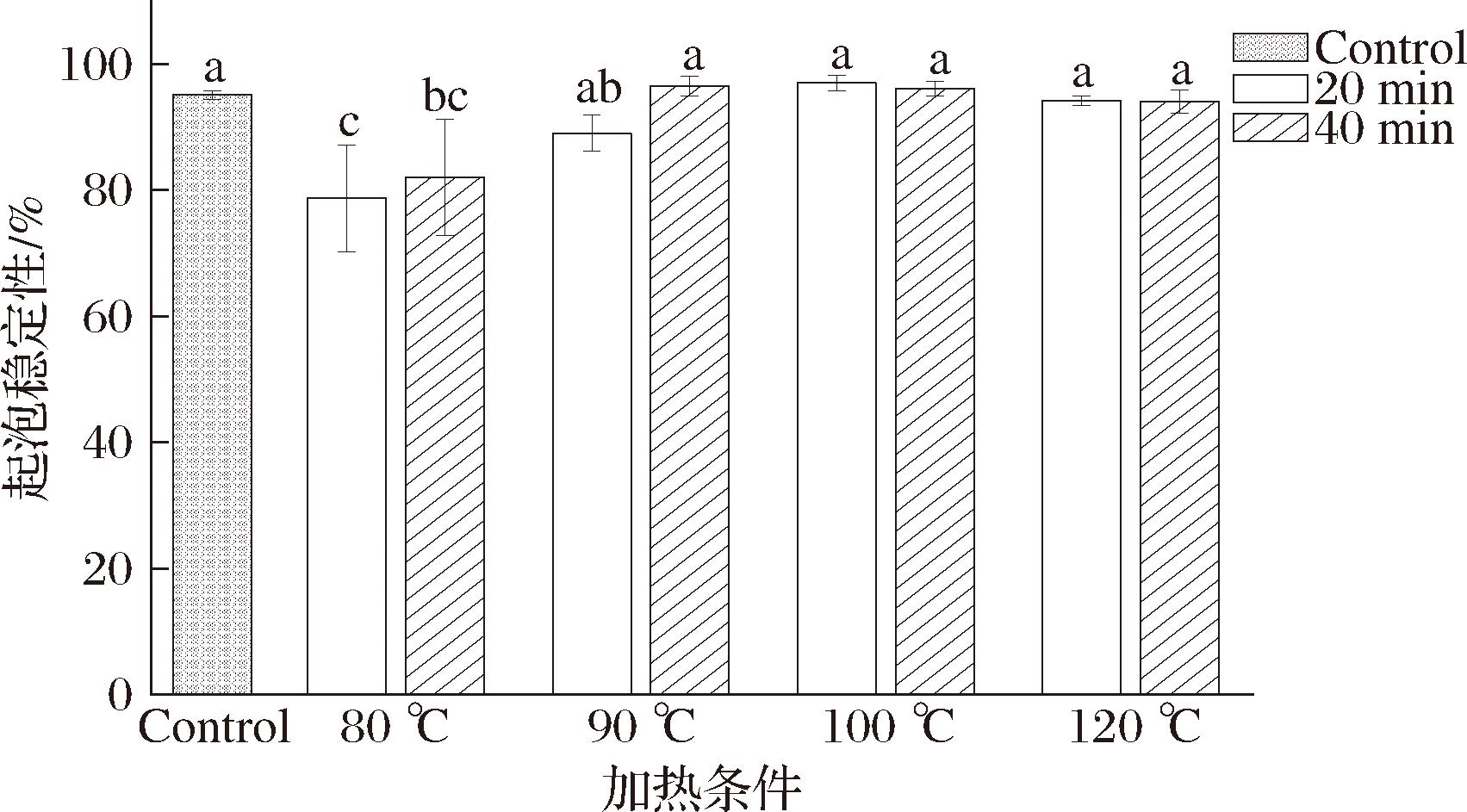
图5 不同加热条件对PSPI起泡稳定性的影响
Fig.5 Foam stability of PSPI under different heat treatments
2.4 不同加热条件对PSPI表面疏水性的影响
表面疏水性与蛋白质的乳化性和起泡性等功能特性密切相关,是一种常见的评估蛋白质结构变化的手段。如图6所示,与未处理的PSPI样品相比,热处理后的PSPI的表面疏水性发生显著下降(P<0.05)。加热条件为80 ℃(20 min)、80 ℃(40 min)、90 ℃(20 min)、90 ℃(40 min)、100 ℃(20 min)、100 ℃(40 min)、120 ℃(20 min)和120 ℃(40 min)的样品,其表面疏水性分别下降了35.72%、30.95%、41.91%、43.42%、41.45%、44.17%、26.22%和41.70%。可能是当加热强度超过一定阈值时,蛋白结构先伸展至最大程度,随后因额外热能输入,多肽链剧烈运动并碰撞,重新聚集成团,疏水基团再次被包埋于分子内部,致使表面疏水性降低[19]。
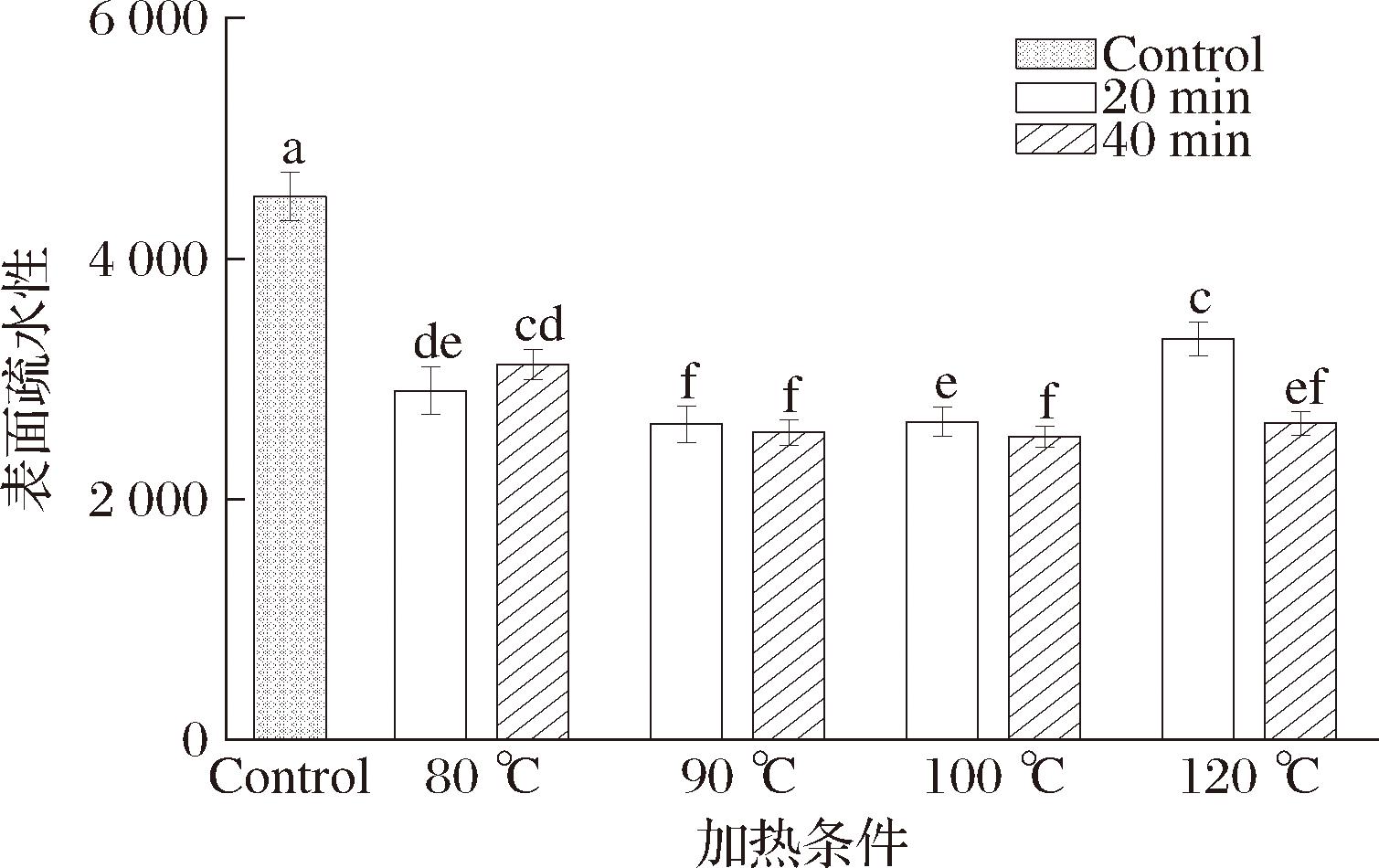
图6 不同加热条件对PSPI表面疏水性的影响
Fig.6 Surface hydrophobicity of PSPI under different heat treatments
2.5 不同加热条件对PSPI二级结构的影响
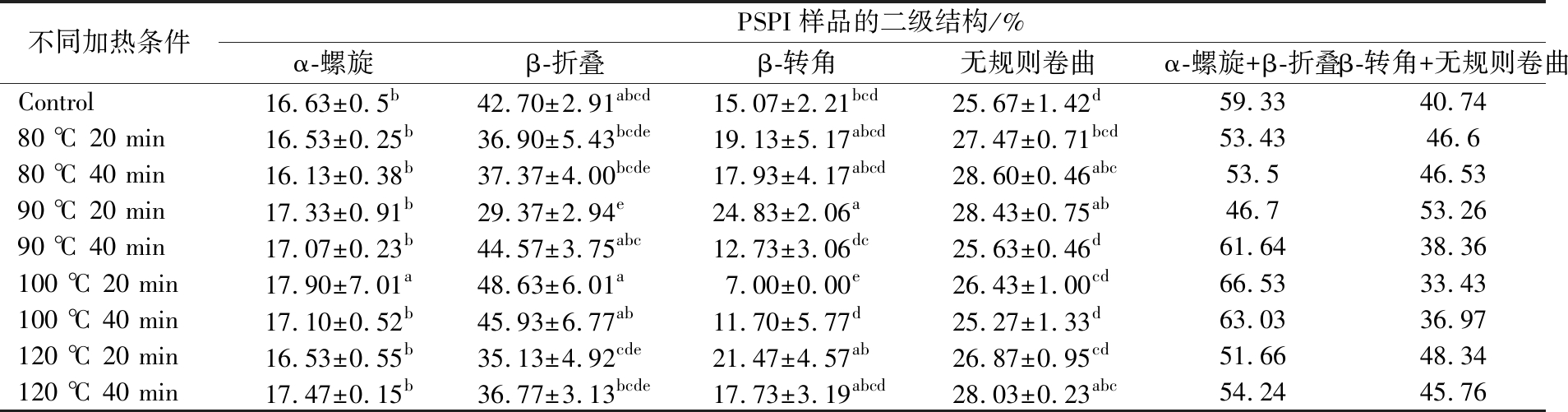
不同加热条件下PSPI蛋白二级结构的相对含量如表1所示。未加热PSPI样品的主要结构是β-折叠(42.70%)、其次是无规则卷曲(25.67%)、α-螺旋(16.63%)和β-转角(15.07%)。通常,α-螺旋和β-折叠埋在多肽链内,并利用C![]() O和C
O和C![]() N之间的分子间作用力来稳定二级结构,相比于无规则卷曲具有更强的稳定性和紧密程度[27]。与空白对照相比,当加热条件为80 ℃(20 min)、80 ℃(40 min)、90 ℃(20 min)时,PSPI样品α-螺旋和β-折叠的总含量较低,而β-转角和无规则卷曲的总含量较高,表明此时PSPI的结构变得松散和无序,可能是在加热过程中,稳定二级结构的氢键被破坏,导致蛋白质分子部分变性并展开,从而破坏了折叠的蛋白质结构,这种变化通常是由于氢键、盐键和疏水键等维持二级结构的作用力被破坏所导致[28]。当加热温度为90 ℃(40 min)、100 ℃(20 min)、100 ℃(40 min)时,PSPI样品中α-螺旋和β-折叠的含量升高,而β-转角和无规则卷曲降低,表明此加热条件可以使PSPI样品具有更稳定的二级结构[29]。而当温度升高至120 ℃(20 min和40 min)时,PSPI样品α-螺旋和β-折叠的含量发生下降,而β-转角和无规则卷曲的含量升高,蛋白的稳定性发生下降。
N之间的分子间作用力来稳定二级结构,相比于无规则卷曲具有更强的稳定性和紧密程度[27]。与空白对照相比,当加热条件为80 ℃(20 min)、80 ℃(40 min)、90 ℃(20 min)时,PSPI样品α-螺旋和β-折叠的总含量较低,而β-转角和无规则卷曲的总含量较高,表明此时PSPI的结构变得松散和无序,可能是在加热过程中,稳定二级结构的氢键被破坏,导致蛋白质分子部分变性并展开,从而破坏了折叠的蛋白质结构,这种变化通常是由于氢键、盐键和疏水键等维持二级结构的作用力被破坏所导致[28]。当加热温度为90 ℃(40 min)、100 ℃(20 min)、100 ℃(40 min)时,PSPI样品中α-螺旋和β-折叠的含量升高,而β-转角和无规则卷曲降低,表明此加热条件可以使PSPI样品具有更稳定的二级结构[29]。而当温度升高至120 ℃(20 min和40 min)时,PSPI样品α-螺旋和β-折叠的含量发生下降,而β-转角和无规则卷曲的含量升高,蛋白的稳定性发生下降。
表1 不同加热条件对PSPI二级结构的影响
Table 1 Secondary structure contents of PSPI under different heat treatments
注:不同小写字母表示差异显著(P<0.05)(下同)。
不同加热条件PSPI样品的二级结构/%α-螺旋β-折叠β-转角无规则卷曲α-螺旋+β-折叠β-转角+无规则卷曲Control16.63±0.5b42.70±2.91abcd15.07±2.21bcd25.67±1.42d59.3340.7480 ℃ 20 min16.53±0.25b36.90±5.43bcde19.13±5.17abcd27.47±0.71bcd53.4346.680 ℃ 40 min16.13±0.38b37.37±4.00bcde17.93±4.17abcd28.60±0.46abc53.546.5390 ℃ 20 min17.33±0.91b29.37±2.94e24.83±2.06a28.43±0.75ab46.753.2690 ℃ 40 min17.07±0.23b44.57±3.75abc12.73±3.06dc25.63±0.46d61.6438.36100 ℃ 20 min17.90±7.01a48.63±6.01a7.00±0.00e26.43±1.00cd66.5333.43100 ℃ 40 min17.10±0.52b45.93±6.77ab11.70±5.77d25.27±1.33d63.0336.97120 ℃ 20 min16.53±0.55b35.13±4.92cde21.47±4.57ab26.87±0.95cd51.6648.34120 ℃ 40 min17.47±0.15b36.77±3.13bcde17.73±3.19abcd28.03±0.23abc54.2445.76
2.6 不同加热条件对PSIP可溶性蛋白粒径的影响
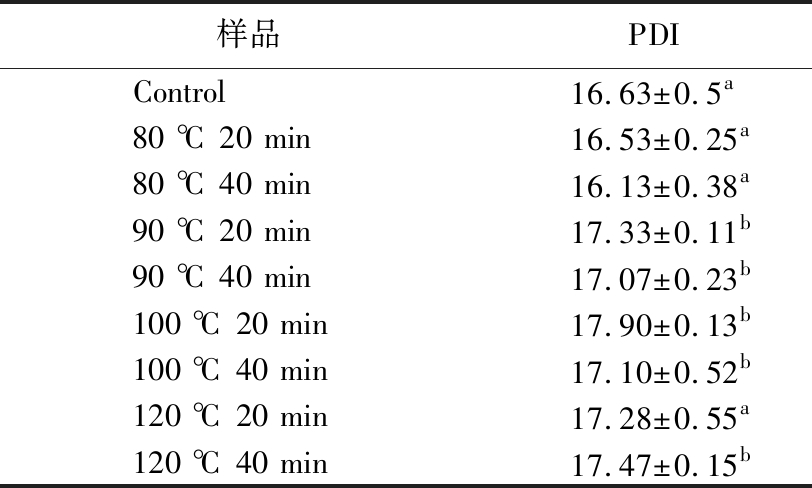
PSPI可溶性蛋白的主峰粒径分布范围为100~1 000 nm。PDI反映了粒径分布范围。PDI值越高表示颗粒大小的范围越宽,增加了潜在的非均质性[30]。不同加热条件下PSPI可溶性蛋白的PDI如表2所示。与未处理的蛋白相比,热处理(>80 ℃)提高了PSPI可溶性蛋白的PDI值,表明可溶性蛋白的粒径范围变宽。此外,热处理后PSPI可溶性蛋白粒径范围整体右移(图7),表明PSPI可溶性蛋白的粒径增大,尤其是120 ℃(40 min)处理的样品,在大于1 000 nm处出现一个小峰,可能是由于热处理后的PSPI形成了可溶性蛋白聚集体,进而提高了可溶性蛋白的粒径。
表2 不同加热条件对PSPI可溶性蛋白PDI的影响
Table 2 PDI of PSPI under different heat treatments
样品PDIControl16.63±0.5a80 ℃ 20 min16.53±0.25a80 ℃ 40 min16.13±0.38a90 ℃ 20 min17.33±0.11b90 ℃ 40 min17.07±0.23b100 ℃ 20 min17.90±0.13b100 ℃ 40 min17.10±0.52b120 ℃ 20 min17.28±0.55a120 ℃ 40 min17.47±0.15b
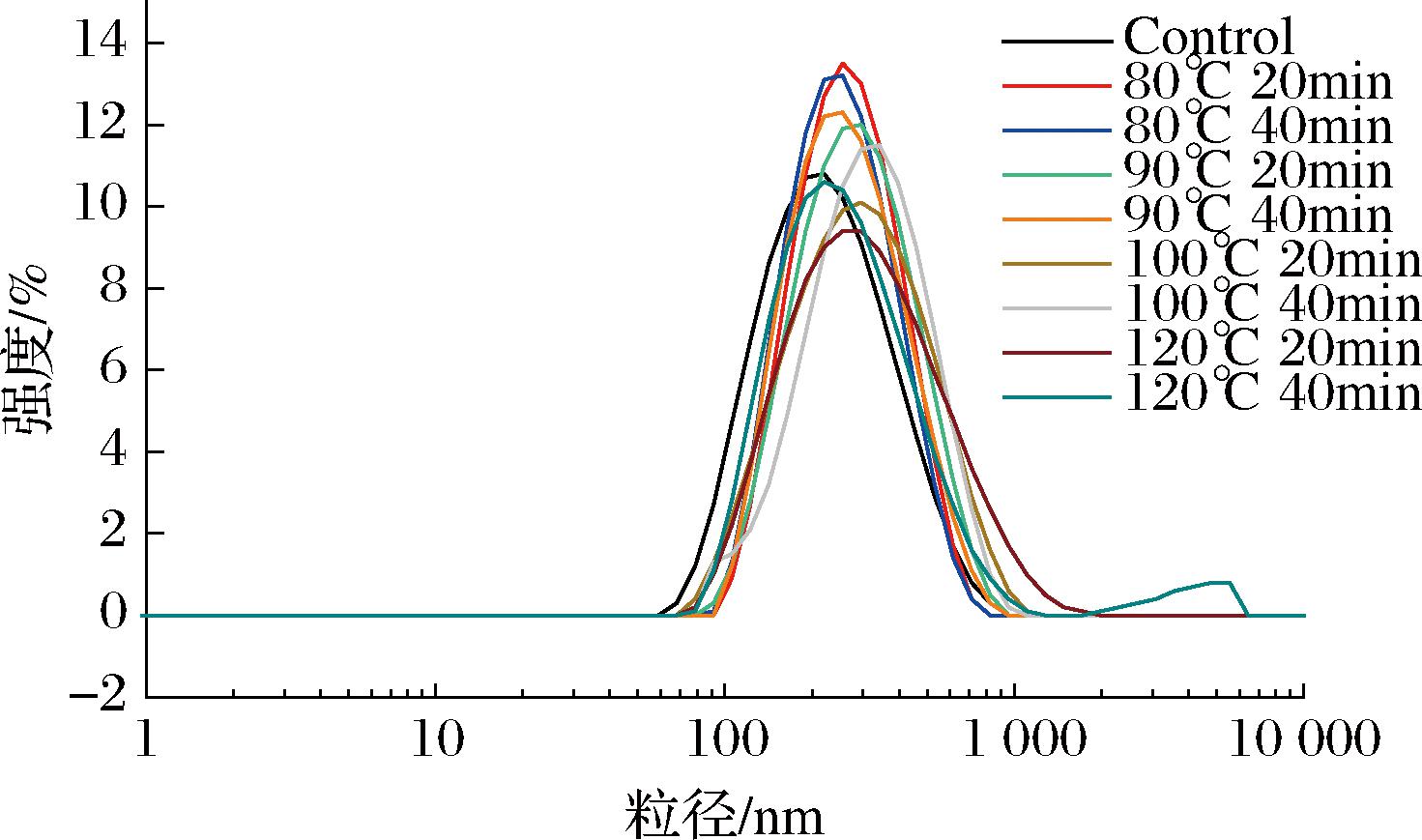
图7 不同加热条件对PSPI可溶性蛋白粒径的影响
Fig.7 Particle size of PSPI soluble protein under different heat treatments
2.7 不同加热条件对PSPI电位的影响
ζ电位反映了颗粒表面的电荷状态,确定悬浮颗粒的分散和聚集。由表3可知,不同热处理条件下,PSPI的电位在-18.83~-20.43。与对照样品相比,热处理条件为80 ℃(20 min)、90 ℃(20 min)和120 ℃(20 min)的样品,其电位的绝对值发生下降,表明分子表面电荷量减少,静电斥力减弱,静电吸引使蛋白质聚集,稳定性变差[31]。热处理条件为80 ℃(40 min)、90 ℃(40 min)、100 ℃(20 min)和100 ℃(40 min)的样品,其电位的绝对值增大,表明PSPI表面之间存在较强的静电斥力,增加了其稳定性[26]。
表3 不同加热条件对PSPI可溶性蛋白Zeta电位的影响
Table 3 Zeta potential of PSPI soluble protein under different heat treatments

Control80 ℃90 ℃100 ℃120 ℃20 min40 min20 min40 min20 min40 min20 min40 min-19.73±0.70abc-19.43±0.42cd-20.27±0.32ab-18.83±0.40d-19.5±0.44cd-20.43±0.25a-20.27±0.32ab-19.6±0.36bc-19.77±0.31abc
2.8 不同加热条件对PSPI内源荧光的影响
蛋白质的内源荧光主要来源于分子中带有芳香基团的氨基酸残基,如色氨酸、酪氨酸等。通过表征这些残基中发色团的相互作用(特别是色氨酸的环境极性),可以用来分析蛋白质的三级结构[32]。蛋白质内源性色氨酸荧光对于其周边微环境的极性非常敏感,当蛋白质处于折叠状态时,色氨酸残基主要位于蛋白质内核这样的疏水环境中,此时被激发的色氨酸具有相对较高的荧光强度;而当蛋白质部分或完全展开时,有更多的色氨酸残基暴露于蛋白质分子表面,此时被激发的色氨酸荧光强度降低[33]。不同加热条件对PSPI内源荧光的影响如图8所示。与未热处理的PSPI蛋白相比,热处理后的PSPI蛋白的内源荧光强度增强,表明热处理后PSPI蛋白可能发生了重折叠,色氨酸残基被包裹在蛋白质内部的疏水环境中,此时被激发的色氨酸具有相对较高的荧光强度。
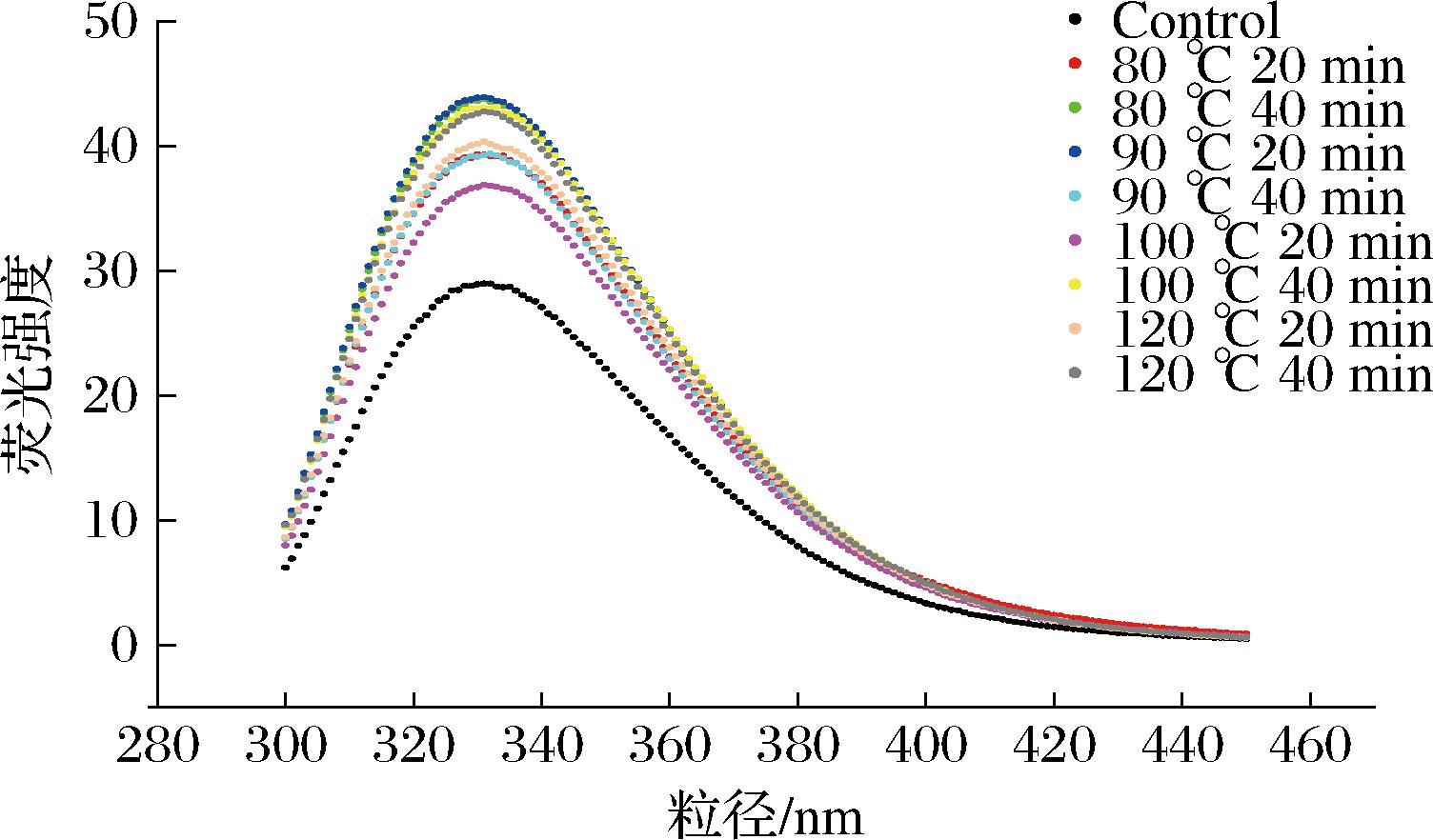
图8 不同加热条件对PSPI 内源荧光的影响
Fig.8 Intrinsic fluorescence of PSPI under different heat treatments
2.9 不同加热条件对PSPI微观结构的影响
热处理对PSPI颗粒大小、形状及聚集情况的影响如图9(放大1 000倍)和图10(放大10 000倍)所示。未进行热处理的PSPI蛋白结构较为完整,热处理后的PSPI蛋白结构变得松散、破碎颗粒较多,破碎程度较为明显,尤其是加热条件为100 ℃和120 ℃的PSPI样品(图9)。未热处理的PSPI蛋白表面比较光滑。热处理后的PSPI表面形貌粗糙,质地变得疏松(图10),表明热处理可以破坏PSPI的块状致密结构。这与MIR等[34]的研究结果一致,即超过80 ℃的热处理会导致藜麦蛋白形成多孔结构。

图9 不同加热条件下PSPI的扫描电镜图(放大1 000倍)
Fig.9 SEM photographs of PSPI under different heat treatments at 1 000-fold magnification

图10 不同加热条件下PSPI的扫描电镜图(放大10 000倍)
Fig.10 SEM photographs of PSPI under different heat treatments at 10 000-fold magnification
3 结论与讨论
本研究探讨了不同热处理温度(80、90、100和120 ℃)分别处理20 min和40 min,对PSPI功能特性及结构特性的影响。结果表明,热处理对PSPI的功能特性有显著的积极影响。经过热处理,PSPI能够形成可溶性蛋白聚集体,这一变化有效提升了蛋白的溶解性、乳化性以及起泡性。微观结构表明,热处理后的PSPI结构变得更加疏松。此外,热处理后PSPI表面疏水性降低和内源荧光强度增强,表明热处理后PSPI蛋白分子可能发生重新折叠和聚集。
综上所述,热处理是一种有效改善南瓜籽蛋白功能特性的物理方法,同时对PSPI的结构特性产生影响。这些发现为南瓜籽蛋白在食品加工中的应用提供了理论支持,也为开发新型植物蛋白产品提供了科学依据。
[1] ![]() M, MI
M, MI AN A, TIWARI B.Eco-innovative technologies for extraction of proteins for human consumption from renewable protein sources of plant origin[J].Trends in Food Science &Technology, 2018, 75:93-104.
AN A, TIWARI B.Eco-innovative technologies for extraction of proteins for human consumption from renewable protein sources of plant origin[J].Trends in Food Science &Technology, 2018, 75:93-104.
[2] ![]() L,
L, ![]() S, et al.Production of enzymatic hydrolysates with antioxidant and angiotensin-I converting enzyme inhibitory activity from pumpkin oil cake protein isolate[J].Food Chemistry, 2011, 124(4):1316-1321.
S, et al.Production of enzymatic hydrolysates with antioxidant and angiotensin-I converting enzyme inhibitory activity from pumpkin oil cake protein isolate[J].Food Chemistry, 2011, 124(4):1316-1321.
[3] VINAYASHREE S, VASU P.Biochemical, nutritional and functional properties of protein isolate and fractions from pumpkin (Cucurbita moschata var.Kashi Harit) seeds[J].Food Chemistry, 2021, 340:128177.
[4] 刘艳荣. 南瓜籽蛋白制备及其活性多肽的研究[D].太原:山西大学, 2011.LIU Y R.Study on preparation isolated proteins and active peptides from pumpkin seeds[D].Taiyuan:Shanxi University, 2011.
[5] AKHARUME F U, ALUKO R E, ADEDEJI A A.Modification of plant proteins for improved functionality:A review[J].Comprehensive Reviews in Food Science and Food Safety, 2021, 20(1):198-224.
[6] SUN Y J, WANG Q B, LI C, et al.Preparation of pumpkin seed protein isolate nanoparticles by heat-assisted pH-shifting:Enhanced emulsification performance and dispersibility[J].Journal of Food Engineering, 2024, 377:112087.
[7] ZHANG Q, OUYANG K F, HUANG F, et al.Evaluating the effects of protein-glutaminase treatment on the structural and functional properties of pumpkin (Cucurbita moschata) seed protein[J].International Journal of Biological Macromolecules, 2025, 309:142989.
[8] YILDIZ G.From seed to solution:Enhancing techno-functionality and digestibility of pumpkin seed protein isolate through high-intensity ultrasound, high-pressure processing, and pH-shifting[J].Food Chemistry, 2025, 474:143222.
[9] NIKBAKHT NASRABADI M, SEDAGHAT DOOST A, MEZZENGA R, et al.Modification approaches of plant-based proteins to improve their techno-functionality and use in food products[J].Food Hydrocolloids, 2021, 118:106789.
[10] YE A Q, CUI J, DALGLEISH D, et al.Effect of homogenization and heat treatment on the behavior of protein and fat globules during gastric digestion of milk[J].Journal of Dairy Science, 2017, 100(1):36-47.
[11] YANG X Y, SHI L S, GONG T, et al.Structural modification induced by heat treatments improves the emulsifying attributes of lacquer seed protein isolate[J].International Journal of Biological Macromolecules, 2022, 222:1700-1708.
[12] GAO D, HELIKH A, DUAN Z H, et al.Thermal, structural, and emulsifying properties of pumpkin seed protein isolate subjected to pH-shifting treatment[J].Journal of Food Measurement and Characterization, 2023, 17(3):2301-2312.
[13] HUANG X, TU R, SONG H B, et al.Fabrication and characterization of gelatin-EGCG-pectin ternary complex:Formation, mechanism, emulsion stability, and structure[J].Journal of the Science of Food and Agriculture, 2023, 103(3):1442-1453.
[14] ZHANG D H, CAI Y P, LAO F, et al.Steam cooking drives alterations of proteomics, protein structural and functional properties in rice (Oryza sativa L.)[J].Food Bioscience, 2024, 59:103899.
[15] HUANG Z R, SUN J, ZHAO L Z, et al.Analysis of the gel properties, microstructural characteristics, and intermolecular forces of soybean protein isolate gel induced by transglutaminase[J].Food Science &Nutrition, 2022, 10(3):772-783.
[16] 王晓辉, 朱婷伟, 孟凡聪, 等.大豆蛋白对面团中醇溶蛋白组成和结构的影响研究[J].食品与发酵工业, 2025, 51(1):223-230. WANG X H, ZHU T W, MENG F C, et al. Study on influence of soybean protein on composition and structure of gliadin in dough[J]. Food and Fermentation Industries, 2025, 51(1):223-230.
[17] JIANG S S, DING J Z, ANDRADE J, et al.Modifying the physicochemical properties of pea protein by pH-shifting and ultrasound combined treatments[J].Ultrasonics Sonochemistry, 2017, 38:835-842.
[18] KIM M J, CHOI S J, SHIN S I, et al.Resistant glutarate starch from adlay:Preparation and properties[J].Carbohydrate Polymers, 2008, 74(4):787-796.
[19] 李春强, 刘俊, 赵虹霏, 等.加热-超声-pH偏移联合改性大豆球蛋白纳米颗粒的制备及稳定性研究[J].中国食品学报,2023, 23(10):178-194.LI C Q, LIU J, ZHAO H F, et al.Studies on preparation and stability of SG nanoparticles modified by heating-ultrasound-pH shifting[J].Journal of Chinese Institute of Food Science and Technology, 2023, 23(10):178-194.
[20] KAN X H, CHEN G J, ZHOU W T, et al.Application of protein-polysaccharide Maillard conjugates as emulsifiers:Source, preparation and functional properties[J].Food Research International, 2021, 150:110740.
[21] BOYE J I, AKSAY S, ROUFIK S, et al.Comparison of the functional properties of pea, chickpea and lentil protein concentrates processed using ultrafiltration and isoelectric precipitation techniques[J].Food Research International, 2010, 43(2):537-546.
[22] HU X, ZHAO M M, SUN W Z, et al.Effects of microfluidization treatment and transglutaminase cross-linking on physicochemical, functional, and conformational properties of peanut protein isolate[J].Journal of Agricultural and Food Chemistry, 2011, 59(16), 8886-8894.
[23] ESMAEILI M, RAFE A, SHAHIDI S A, et al.Functional properties of rice bran protein isolate at different pH levels[J].Cereal Chemistry, 2016, 93(1):58-63.
[24] 张婷, 陈美如, 于一丁, 等.生物酶解影响蛋白起泡特性的因素及机理研究进展[J].食品科学, 2022, 43(7):298-304.ZHANG T, CHEN M R, YU Y D, et al.Progress in understanding the factors influencing the effect of enzymatic hydrolysis on protein foaming characteristics and the underlying mechanisms[J].Food Science, 2022, 43(7):298-304.
[25] HU J Y, YU B, YUAN C, et al.Influence of heat treatment before and/or after high-pressure homogenization on the structure and emulsification properties of soybean protein isolate[J].International Journal of Biological Macromolecules, 2023, 253:127411.
[26] ZHAO M, XIONG W F, CHEN B X, et al.Enhancing the solubility and foam ability of rice glutelin by heat treatment at pH12:Insight into protein structure[J].Food Hydrocolloids, 2020, 103:105626.
[27] RESENDIZ-VAZQUEZ J A, UR AS-SILVAS J E, ARM J P, et al.Effect of ultrasound-assisted enzymolysis on jackfruit (Artocarpus heterophyllus) seed proteins:Structural characteristics, technofunctional properties and the correlation to enzymolysis[J].Journal of Food Processing &Technology, 2019, 10:1-11.
AS-SILVAS J E, ARM J P, et al.Effect of ultrasound-assisted enzymolysis on jackfruit (Artocarpus heterophyllus) seed proteins:Structural characteristics, technofunctional properties and the correlation to enzymolysis[J].Journal of Food Processing &Technology, 2019, 10:1-11.
[28] AHMED J, AL-RUWAIH N, MULLA M, et al.Effect of high pressure treatment on functional, rheological and structural properties of kidney bean protein isolate[J].LWT-Food Science and Technology, 2018, 91:191-197.
[29] 王进英, 冶梓芩, 马金鸽, 等. 超声改性对菜籽分离蛋白和亚麻分离蛋白品质特性的影响[J]. 食品与发酵工业, 2025, 51(19):199-206.WANG J Y, YE Z Q, MA J G, et al. Effects of ultrasound modification on quality properties of canola protein isolate and flaxseed protein isolate[J]. Food and Fermentation Industries, 2025, 51(19):199-206.
[30] LI C Y, TIAN Y C, LIU C H, et al.Effects of heat treatment on the structural and functional properties of Phaseolus vulgaris L.protein[J].Foods, 2023, 12(15):2869.
[31] ZHAO Y Y, YUAN Y B, YUAN X R, et al.Physicochemical, conformational and functional changes of quinoa protein affected by high-pressure homogenization[J].LWT-Food Science and Technology, 2023, 173:114343.
[32] CHEN W J, WANG W J, MA X B, et al.Effect of pH-shifting treatment on structural and functional properties of whey protein isolate and its interaction with (-)-epigallocatechin-3-gallate[J].Food Chemistry, 2019, 274:234-241.
[33] 韩馨蕊, 李朝蕊, 范鑫, 等.赖氨酸对冷冻损伤肌原纤维蛋白凝胶性能的影响[J].食品科学, 2022, 43(2):1-7.HAN X R, LI C R, FAN X, et al.Effect of L-lysine on gelling properties of myofibrillar protein damaged by freezing[J].Food Science, 2022, 43(2):1-7.
[34] MIR N A, RIAR C S, SINGH S.Improvement in the functional properties of quinoa (Chenopodium quinoa) protein isolates after the application of controlled heat-treatment:Effect on structural properties[J].Food Structure, 2021, 28:100189.