冠突散囊菌(Eurotium cristatum),别名“金花菌”,该菌隶属于散囊菌目(Eurotiales)发菌科(Emericiaceae)散囊菌属(Eurotium),其菌落结构主要由子囊果与菌丝构成[1]。冠突散囊菌对营养物质需求低,环境适应能力强,能高效利用多种氮源与碳源,使其在茶叶发酵中影响茶叶品质和风味的形成[2]。在发酵过程中可合成并分泌多种酶类,酶通过催化茶叶中的化学成分,使茶叶在发酵过程中发生一系列生化反应,让茶叶呈现独特的色泽、香气和风味特征[3]。近年来,众多研究表明经冠突散囊菌发酵的茶叶,如秋季绿茶在丰富茶汤滋味的同时,还降低了茶的涩味[4]。邹金美等[5]的研究进一步表明,冠突散囊菌固体发酵铁观音茶显著增加茶红素和茶褐素的含量,改善茶汤风味和品质。此外,冠突散囊菌对挥发性有机化合物(volatile organic compounds,VOCs)的调控作用亦是研究热点,可优化茶叶的挥发性风味成分谱系,有效抑制陈味相关化合物的生成,同时促进花香类挥发性物质的合成与积累[6]。
苦水玫瑰(Rosa sertata×Rosa rugosa)作为一种具有显著生态特性和较高经济价值的植物资源,属于蔷薇科(Rosaceae)蔷薇属(Rosa),是传统红玫瑰(Rosa rugosa)和钝齿蔷薇(Rosa sertata)的自然杂交种[7]。苦水玫瑰因产于甘肃省永登县苦水镇而得名,是黄河流域的一种特殊食用花卉[8]。此外,苦水玫瑰还具备极强的水土保持能力,是一种高效的生态修复植物。与此同时,苦水玫瑰在化妆品、食品加工以及保健品开发等多个领域亦展现出巨大的应用潜力[9]。然而,截至目前,针对苦水玫瑰在花叶茶领域相关应用的研究仍相对有限[10]。
鉴于冠突散囊菌在发酵茶叶过程中能有效改善茶叶中的营养成分,提升茶叶品质,本研究以苦水玫瑰花叶茶为样品,对其进行3种处理:一是未经发酵处理的苦水玫瑰花叶茶原样;二是经自然发酵的苦水玫瑰花叶茶;三是经冠突散囊菌发酵处理的苦水玫瑰花叶茶,研究3种不同处理方式对苦水玫瑰花叶茶营养品质及抗氧化活性的影响,开发苦水玫瑰花叶茶相关产品,为提高苦水玫瑰的食用价值和副产物的利用率提供科学依据和理论参考。
1 材料与方法
1.1 材料与试剂
原料:苦水玫瑰,于2024年6月11日在海东市互助县采摘;
菌株:冠突散囊菌GICC 2099,由青海省风险评估实验室保存;
试剂:葡萄糖、谷氨酸、无水乙醇(均为分析纯),国药集团化学试剂有限公司;甲醇、醋酸乙酯、95%(体积分数)乙醇、正丁醇、茚三酮、氯化亚锡、谷氨酸、蒽酮,天津市福晨化学试剂有限公司;福林酚、没食子酸,北京索莱宝科技有限公司;芦丁标准品(纯度≥98.0%),上海麦克林生化科技股份有限公司。
1.2 仪器与设备
SW-CJ-2FD净化工作台,上海沪净医疗器械有限公司;LDZM-80L灭菌锅,上海申安医疗器械厂;Bluepard电热恒温培养箱,上海一恒科学仪器有限公司;ZG-TP203千分之一分析天平,武义珠恒电子有限公司;TU-1810紫外可见分光光度计,北京普析通用仪器有限责任公司;安捷伦1260高效液相色谱仪,安捷伦科技公司。
1.3 实验方法
1.3.1 冠突散囊菌菌种活化
在超净工作台内,用接种针从培养平板上挑取冠突散囊菌菌落,将其接种于马铃薯琼脂培养基上。培养基在28 ℃下恒温培养,培养周期约为1周,以供后续实验使用[11]。
1.3.2 冠突散囊菌固体菌种制备
准确称取30.00 g麦麸于150 mL锥形瓶中,加入适量蒸馏水拌匀,置于高压灭菌锅中,于128 ℃下灭菌2 h。灭菌完成后,立即将锥形瓶放置在超净工作台内冷却至室温,用灭菌药匙取1.3.1节中活化的冠突散囊菌接种在麦麸培养基上,于28 ℃下恒温培养7 d左右,在此期间需不时抖动,使菌体均匀生长。当冠突散囊菌布满整个麦麸培养基时,即表明固体菌种制备完成[5]。
1.3.3 冠突散囊菌固体发酵茶叶
精确称取30.00 g苦水玫瑰花叶茶于17 cm×36 cm的聚丙烯塑料袋,加入48 mL蒸馏水,使茶叶的水分含量保持在60%左右并封口,摇晃塑料袋使花茶叶与蒸馏水充分混合。混合后的花茶叶在121 ℃下灭菌2 h。灭菌后,将样品转移到超净台上冷却至室温。在超净工作台内将冠突散囊菌固体菌种接种于苦水玫瑰花叶茶上,于28 ℃培养12 d。将发酵完的样品真空冷冻干燥后,粉碎,置阴凉处保存备用。
1.3.4 可溶性总糖、单糖和二糖含量的测定
采用苯酚-硫酸法测定[12-13]。葡萄糖为标准品,建立标准曲线,绘制得到的线性方程为y=5.882 2x+0.031 7,R2=0.999 4,其中x表示茶多糖质量浓度,单位为g/L。
糖组分含量的计算如公式(1)所示:
(1)
式中:X,糖组分含量,mg/mL;C,供试液中肉碱的质量浓度,mg/mL;V,样品提取液体积,mL;D,稀释倍数;m,样品的质量或体积,g或mL。
1.3.5 游离氨基酸含量的测定
参照黄德娜等[14]的方法。谷氨酸为标准品,标准线性方程y=1.341 3x-0.146,R2=0.999,x单位为g/L。
1.3.6 总黄酮含量的测定
准确称取1.00 g苦水玫瑰样品粉末,采用超声辅助乙醇提取法[70%(体积分数)乙醇,料液比1∶25(g∶mL),300 W,50 ℃,20 min,4 000 r/min],离心10 min,取上清液,定容并稀释,制备苦水玫瑰总黄酮待测液[15]。芦丁为标准品,建立标准曲线绘制得到线性回归方程y=0.229x+0.045 1,R2=0.999 9,x的单位为g/L。
1.3.7 茶多酚含量的测定
用福林酚法测定茶多酚含量[16],没食子酸为标准品,建立标准曲线,绘制得到线性回归方程y=0.011 5x+0.066 5,相关系数R2=0.999 2,其中x的单位为g/L。首先将0.200 g样品加入到70 ℃的70%(体积分数)甲醇溶液中,然后在70 ℃的水浴中浸提10 min(隔5 min摇1次),浸提后的溶液冷却至室温,3 500 r/min离心10 min。最后用预热过的70%甲醇溶液洗涤剩余的残渣1~2次。
1.3.8 咖啡因含量的测定
参照吴以龙等[17]的方法,按照公式(2)计算咖啡因含量:
(2)
式中:X,咖啡因含量,μg/g;C,供试液中咖啡因的质量浓度,μg/mL;V,样品提取液体积,mL;M,样品的质量,g。
1.3.9 儿茶素含量的测定
依据GB/T 8313—2018《茶叶中茶多酚和儿茶素类含量的检测方法》,具体提取方法参照1.3.7节。按照公式(3)计算儿茶素含量:
(3)
式中:X,儿茶素含量,μg/g;C,供试液中各儿茶素组分的质量浓度,μg/mL;V,样品提取液体积,mL;M,样品的质量,g。
1.3.10 茶黄素、茶红素、茶褐素测定
茶色素的定量分析采用比色系统分析法进行测定。茶色素提取过程通过热水浸提法实现[18]。准确称量2.00 g茶叶样品,加100 mL沸水,在恒温下浸提30 min。浸提完成后,将样品进行离心分离,收集上清液,制得待测茶汤样品。
1.3.11 抗氧化能力的测定
参照张桂芳等[19]的方法,测定DPPH自由基清除能力;参照张靖鹏等[20]的方法,测定ABTS阳离子自由基清除能力;参考傅志丰等[21]的方法,测定羟自由基清除能力。
1.4 数据处理
对冠突散囊菌发酵茶、苦水玫瑰花叶发酵茶和苦水玫瑰花叶茶分别进行3次重复实验,SPSS 26软件进行数据分析及显著性分析,Origin 2021软件绘图。测定结果以“平均值±标准差”表示。
2 结果与分析
2.1 糖类和游离氨基酸含量测定结果
如图1所示,果糖、葡萄糖、蔗糖和麦芽糖的保留时间分别为4.070、4.423、5.273、5.890 min。通过标准曲线法对各糖类物质进行了定量分析,所得到的标准回归方程分别为:果糖的回归方程y=53 492.72x-1 566.048,R2=0.999 8;葡萄糖的回归方程为y=51 021.08x-849.155,R2=0.999 7;蔗糖的回归方程为y=60 540.12x-1 452.118,R2=0.999 9;麦芽糖的回归方程为y=49 977.38x-1 397.325,R2=0.999 8。
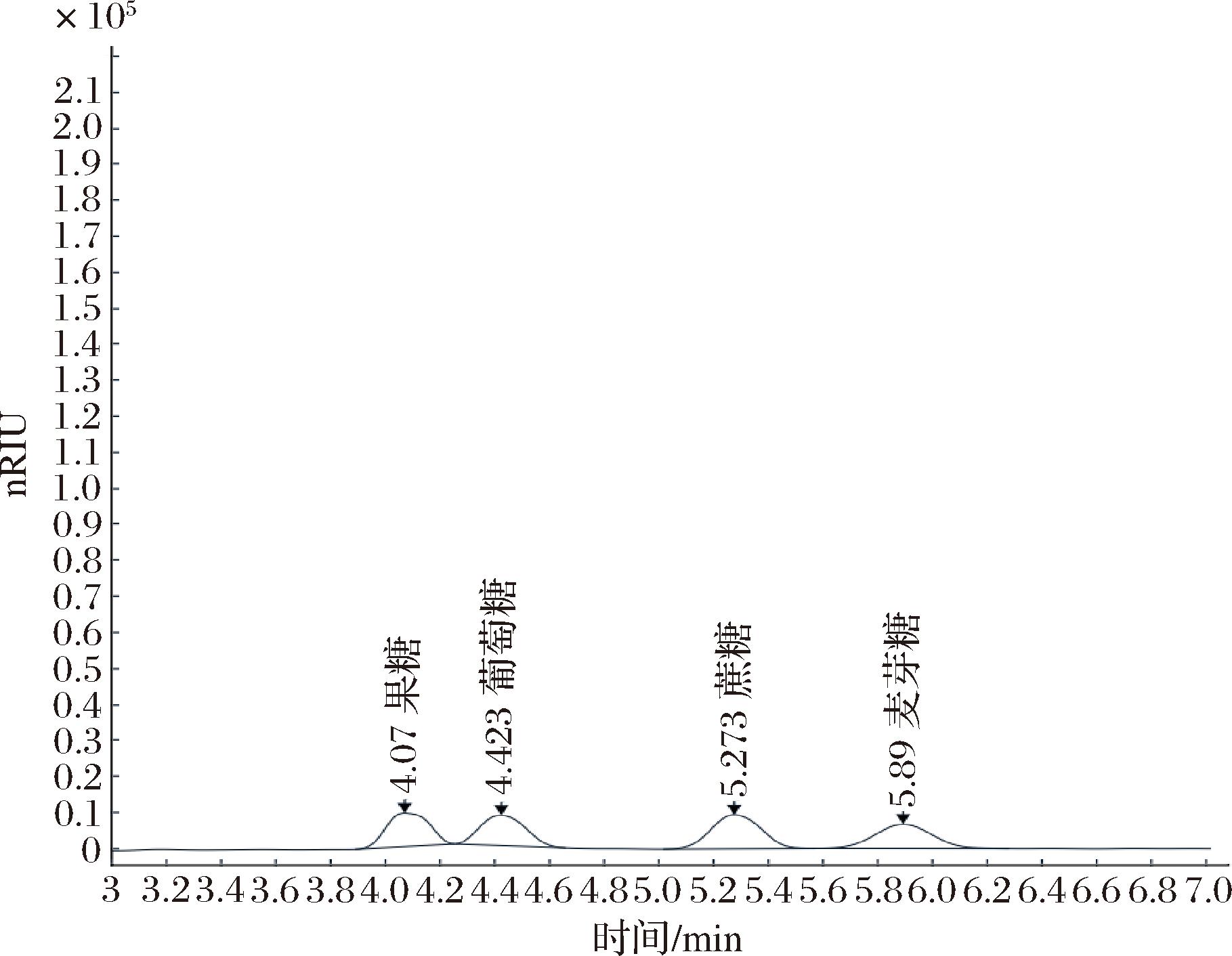
图1 可溶性单糖和二糖标准液相色谱图
Fig.1 Liquid chromatograms of soluble monosaccharides and disaccharide standards
由表1可知,与不同发酵处理的2组相比,未经发酵处理的苦水玫瑰花叶茶可溶性总糖含量最高,达到9.145 mg/g,说明未发酵苦水玫瑰花叶茶中多糖、单糖等未被微生物分解利用,其中的糖含量保存完整。相比不同发酵的处理组,经冠突散囊菌发酵的苦水玫瑰花叶茶总糖含量(5.200 mg/g)显著低于自然发酵的苦水玫瑰花叶茶中总糖含量(7.189 mg/g),降低了38.25%。这可能是由于冠突散囊菌在发酵过程中消耗了大量的可溶性糖,并通过分泌胞外酶,如淀粉酶、纤维素酶等有效分解了多糖异转化为小分子物质(如有机酸等)。陈琳琳等[22]使用冠突散囊菌发酵夏秋茶,发酵后可溶性糖含量显著降低。与自然发酵的苦水玫瑰花叶茶相比,冠突散囊菌发酵茶中果糖含量(0.660 mg/g)、葡萄糖含量(1.791 mg/g)和蔗糖含量(0.292 mg/g)分别降低了87.55%、56.04%和78.65%。这可能是由于在发酵过程中冠突散囊菌等微生物利用茶叶中的糖类物质(如葡萄糖、果糖、蔗糖等)进行生长和繁殖,通过代谢途径将这些糖转化为能量、细胞物质或其他代谢产物(如有机酸、醇类、酯类等),从而导致糖含量降低;同时,还可通过一系列的生化反应转化为其他物质,也会使糖含量降低。而麦芽糖在3种不同茶叶中均未检出。与未发酵组相比,在冠突散囊菌发酵茶的水溶液中,冠突散囊菌发酵茶游离氨基酸含量显著降低(P<0.05),降低了51.99%。这可能与冠突散囊菌菌丝在生长过程中利用茶叶中的氨基酸合成自身菌体蛋白有关,即在冠突散囊菌发酵绿茶中观察到发酵后游离氨基酸含量的显著下降,进一步支持了这一推测[23]。
表1 三种茶中的营养物质测定结果
Table 1 Determination results of nutrients in three types of tea

注:“—”表示没有检出;同列不同小写字母表示差异显著(P<0.05)(下同)。
样品总糖/(mg/g)果糖/(mg/g)葡萄糖/(mg/g)蔗糖/(mg/g)麦芽糖/(mg/g)游离氨基酸/%冠突散囊菌发酵茶5.200±0.059c0.660±0.148c1.791±0.074c0.292±0.006c—3.135±0.014c苦水玫瑰花叶发酵茶7.189±0.281b5.303±0.005b4.074±0.013b1.368±0.005b—3.637±0.400b苦水玫瑰花叶茶9.145±0.051a15.911±0.004a12.452±0.004a7.711±0.006a—4.765±0.028a
2.2 三种活性物质的测定
咖啡因标准液相色谱图如图2所示,咖啡因保留时间为6.070 min,咖啡因标准线性方程为y=27.142x-18.009,R2=0.999 9。
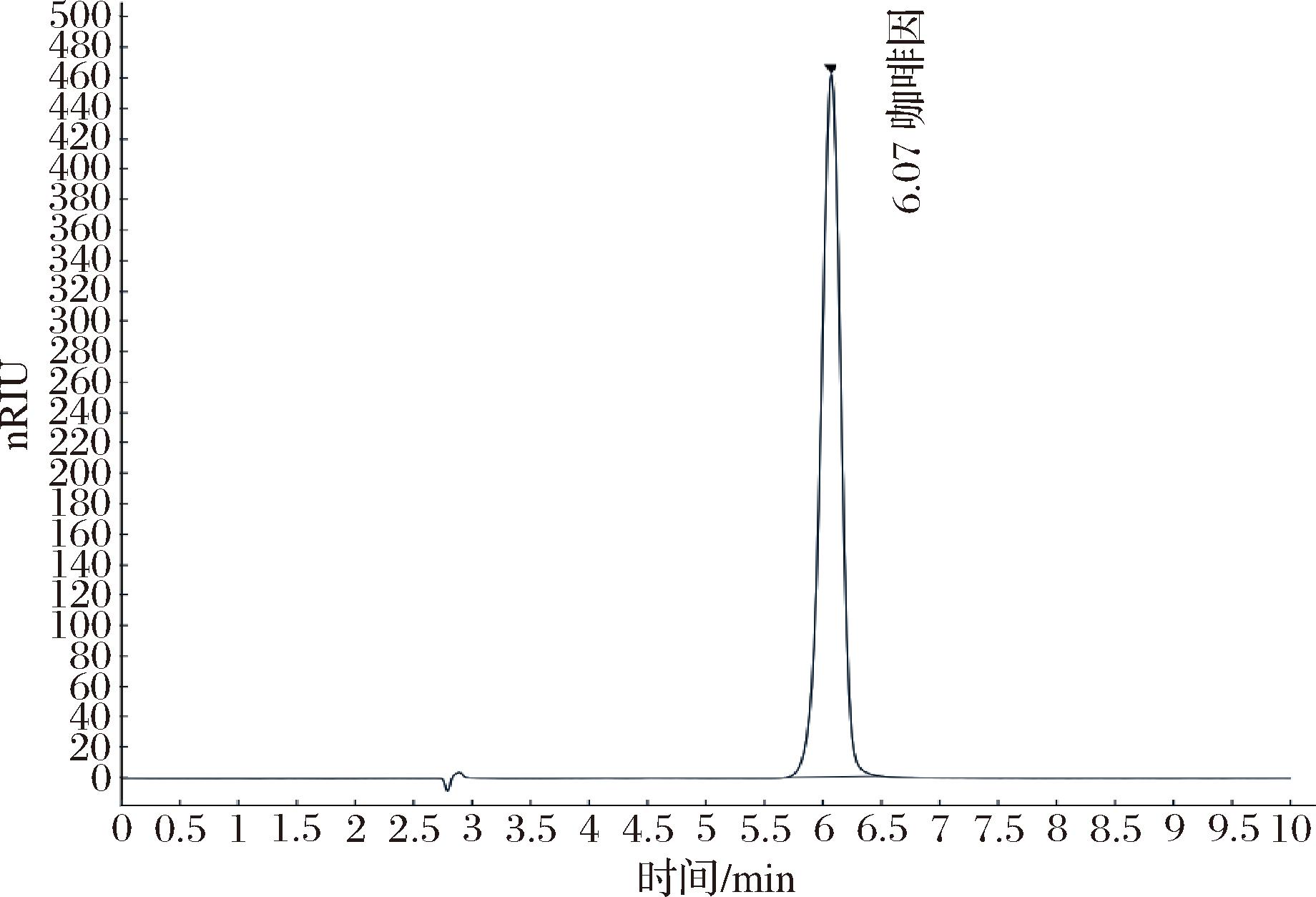
图2 咖啡因STD 200标准液相色谱图
Fig.2 Caffeine STD 200 standard liquid chromatogram
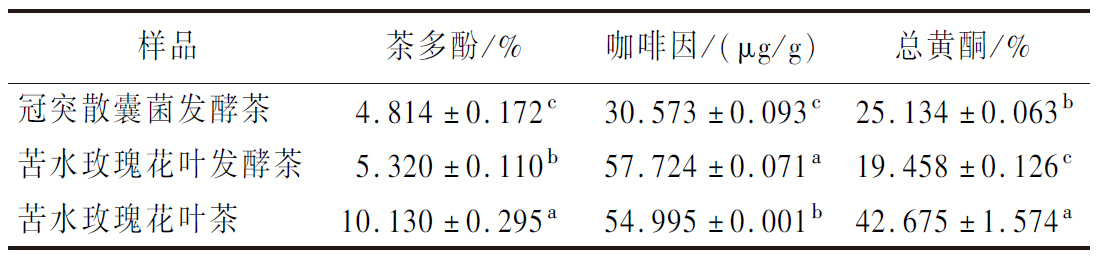
如表2所示,未经发酵的苦水玫瑰花叶茶总黄酮含量最高,其次是冠突散囊菌发酵茶,最后是苦水玫瑰花叶发酵茶,分别为42.675%、25.134%和19.458%。这可能是由于不经过发酵处理的苦水玫瑰花叶茶黄酮类化合物处于原始形态,化学结构相对稳定,没有微生物的参与和酶促反应,因此能更好地保持其生物活性和含量。与自然发酵的苦水玫瑰相比,经冠突散囊菌发酵的苦水玫瑰花叶茶的总黄酮含量显著提高(P<0.05),提高了29.17%。这一结果表明,冠突散囊菌菌丝体在发酵过程中能有效降解苦水玫瑰花叶茶中的成分,并将其转化为黄酮类化合物,从而使发酵过程中黄酮类化合物的含量增加。马艳蕊等[24]用冠突散囊菌发酵桑叶红茶中发现发酵组总黄酮含量显著升高。与自然发酵的苦水玫瑰花叶茶相比,冠突散囊菌发酵的茶叶中茶多酚含量和咖啡因含量显著降低(P<0.05),分别降低了10.51%和88.81%。这可能是由于冠突散囊菌在发酵过程中降解和利用了茶多酚。茶多酚是茶叶苦涩味的主要成分,其含量的降低表明发酵过程在一定程度上缓解了茶叶的涩味。近年来,利用冠突散囊菌发酵茶叶的例子越来越多,相关研究表明,经冠突散囊菌发酵的茶叶其茶多酚含量显著性下降[23,25-28],这与本研究结果相一致。而咖啡因是茯砖茶中主要的苦味成分,其含量降低可减轻苦涩味并改善口感,但同时可能削弱其健胃提神等保健功效。因此,茯砖茶加工需在降低苦涩味与保留保健功能间寻求平衡,以优化品质和功能[29]。王亚丽等[30]研究结果表明经冠突散囊菌发酵会使茶叶中咖啡因含量明显降低。其可能原因在于在湿热作用下,咖啡因与蛋白质等物质发生缔合致使其下降,减轻了苦水玫瑰花叶茶的苦涩味;同时黄酮类物质与咖啡因形成络合物,降低咖啡因含量,形成苦水玫瑰花叶茶醇和滋味[31],同时在此阶段可能由于冠突散囊菌生长旺盛,也会消耗大量的咖啡因。而未经发酵处理的苦水玫瑰花叶茶茶多酚含量和咖啡因含量显著高于另外2个处理组,可能是因为茶多酚在没有外力作用下,化学结构相对稳定,不易发生氧化、聚合或分解等反应,还可能是因为未经发酵的苦水玫瑰花叶茶通常采用低温干燥的方式进行加工,这种加工方式能够避免高温对茶多酚的降解作用,从而更好地保留其含量。而且未经发酵的加工过程中,通常不会引入酸性或碱性物质,因此茶多酚的化学稳定性更高,咖啡因亦是如此。
表2 三种茶中的活性物质测定结果
Table 2 Results of the determination of active substances in three types of tea
2.3 儿茶素类物质含量测定结果
儿茶素作为茶叶中多酚类物质的关键组成部分,在标准液相色谱分析中具有特征性表现。如图3所示,表没食子儿茶素(epigallocatechin, EGC)、表儿茶素没食子酸酯(epigallocatechin gallate acid, ECG)、儿茶素(catechin, +C)、表儿茶素(epicatechin, EC)和表没食子儿茶素没食子酸酯(epigallocatechin gallate, EGCG)的保留时间分别为5.744、19.461、6.371、11.124、8.825 min。
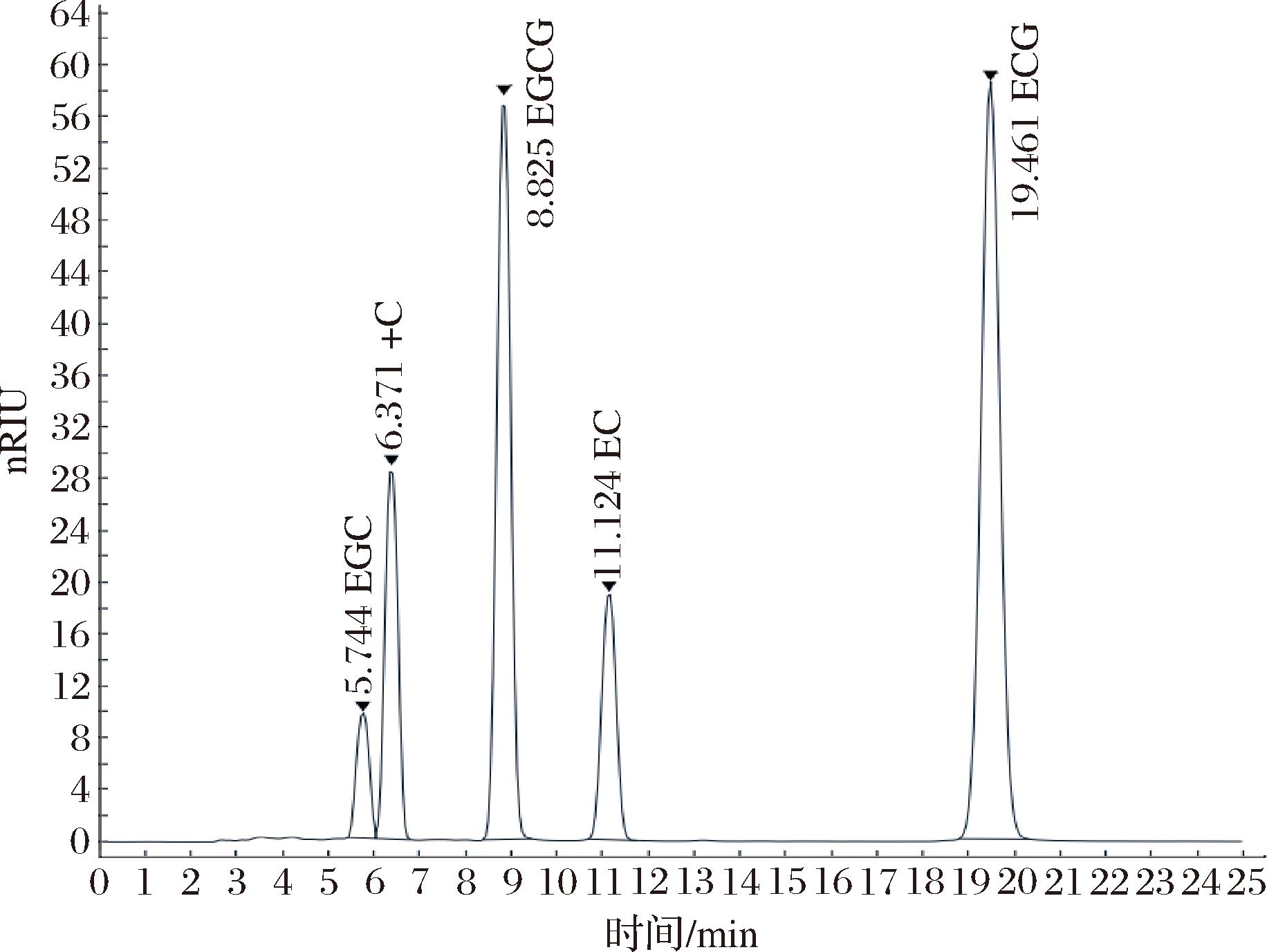
图3 儿茶素标准液相色谱图
Fig.3 Catechin standard liquid chromatogram
由表3可知,与自然发酵的苦水玫瑰花叶茶相比,冠突散囊菌发酵茶总儿茶素含量(2.672 mg/g)、表没食子儿茶素含量(0.816 mg/g)和表没食子儿茶素没食子酸酯含量(0.404 mg/g)显著降低(P<0.05),分别降低了70.69%、89.29%和61.85%,而儿茶素含量(1.212 mg/g)则显著增加(P<0.05),增加了79.04%。此外,在3种不同处理下的茶叶中酯型表儿茶素没食子酸酯均未检出,这可能是由于发酵过程中酯型表儿茶素没食子酸酯发生了酶促水解或转化,而未经发酵的苦水玫瑰花叶茶在前处理或加工过程中,导致少量酯型表儿茶素没食子酸酯发生水解或氧化,因此3种处理的茶叶中酯型表儿茶素没食子酸酯被消耗,所以均未检出。简单型儿茶素,如表没食子儿茶素和表儿茶素可能通过酶促氧化生成其他中间产物,从而导致其在发酵茶中的含量减少。酯型儿茶素如表没食子儿茶素没食子酸酯的酯键也可能被微生物分泌的酶水解,进而使其含量降低。本研究中,冠突散囊菌发酵茶儿茶素含量显著(P<0.05)高于另外2个处理下茶叶中的儿茶素含量,可能是由于冠突散囊菌在发酵过程中使儿茶素衍生物或中间代谢产物进一步转化生成了儿茶素,或者微生物的代谢活动增强了儿茶素的稳定性,使其在发酵过程中相对含量上升。
表3 三种茶中的儿茶素测定结果 单位:mg/g
Table 3 Determination results of catechins in three types of tea

样品总儿茶素表没食子儿茶素表儿茶素没食子酸酯儿茶素表儿茶素表没食子儿茶素没食子酸酯冠突散囊菌发酵茶2.672±0.072c0.816±0.011c—1.212±0.059a0.240±0.019b0.404±0.005c苦水玫瑰花叶发酵茶9.116±0.019b7.622±0.006a—0.254±0.008c0.181±0.009c1.059±0.001b苦水玫瑰花叶茶26.244±0.016a7.513±0.006b—0.783±0.005b16.885±0.013a1.063±0.003a
2.4 茶色素测定结果
如表4所示,与自然发酵的苦水玫瑰花叶茶相比,冠突散囊菌发酵茶中茶黄素和茶红素含量分别降低了52.58%和61.62%,其中茶褐素含量显著升高(P<0.05),提高了83.48%。说明茶色素的形成可能是因为儿茶素的氧化聚合反应,提高了茶色素的生物活性。在冠突散囊菌发酵过程中,儿茶素含量降低的原因可能是儿茶素经酶的催化发生聚合反应,转化为茶褐素和茶红素。冠突散囊菌在茶叶发酵过程中,儿茶素经酶促氧化作用,生成茶黄素,茶黄素进一步氧化为茶褐素与茶红素。
表4 三种茶中的茶色素测定结果
Table 4 Determination results of tea pigment in three types of tea

样品茶黄素/%茶红素/%茶褐素/%(茶褐素+茶红素)/茶黄素冠突散囊菌发酵茶0.194±0.004c5.386±0.182c8.930±0.049a73.684±7.762a苦水玫瑰花叶发酵茶0.409±0.003a8.705±0.038a4.867±0.026c33.197±0.181c苦水玫瑰花叶茶0.255±0.004b8.340±0.040b5.258±0.032b53.329±0.785b
2.5 DPPH自由基清除能力比较
DPPH自由基清除率测定结果如图4所示。冠突散囊菌发酵茶和苦水玫瑰花叶发酵茶相比,DPPH自由基清除能力略有增强,冠突散囊菌发酵茶清除率为90.7%,苦水玫瑰花叶发酵茶清除率为89.7%。但与苦水玫瑰花叶茶相比,苦水玫瑰花叶发酵茶清除率略低,苦水玫瑰花叶茶清除率接近于冠突散囊菌发酵茶清除率,苦水玫瑰花叶茶清除率为90.0%,原因可能是未经发酵的苦水玫瑰花叶茶中,保留了茶叶本身高含量的天然抗氧化成分(如总黄酮、儿茶素等),这些物质具有较强的DPPH自由基清除能力。欧阳梅等[32]研究者观察到,经冠突散囊菌发酵的绿茶表现出较强的DPPH自由基清除能力。这一现象可能由于发酵过程中,微生物分泌的酶将部分糖苷型抗氧化物质(如黄酮苷)转化为高活性游离型衍生物(如黄酮苷元),同时产生茶褐素等新抗氧化成分,最终清除率略高于未发酵茶。因此其含量的增加可能是导致清除能力增强的关键因素。
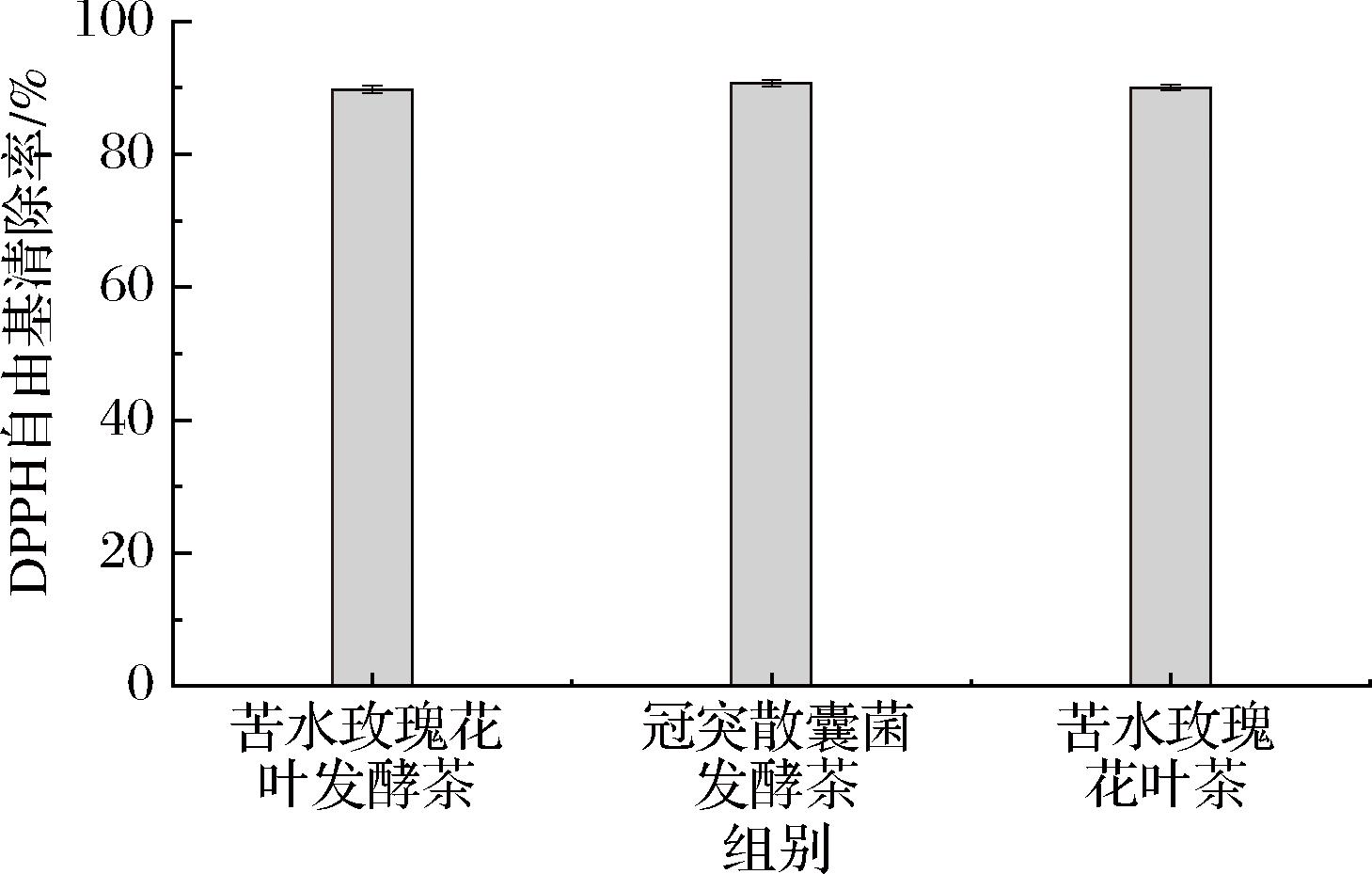
图4 三种处理下DPPH自由基清除能力结果
Fig.4 Results of DPPH radical scavenging activity with three treatment conditions
2.6 ABTS阳离子自由基清除能力测定
ABTS阳离子自由基清除率如图5所示。经冠突散囊菌发酵的茶叶ABTS阳离子自由基清除能力最强,其次是苦水玫瑰花叶发酵茶,最后是苦水玫瑰花叶茶。它们的清除率分别为96.3%、93.7%和89.7%。ABTS阳离子自由基清除率的改变可能与发酵后茶叶中黄酮的活性形式、结构及成分间的协同作用相关。文治瑞等[33]的研究发现,金花茶中的黄酮类化合物对ABTS阳离子自由基具有显著的清除效果。
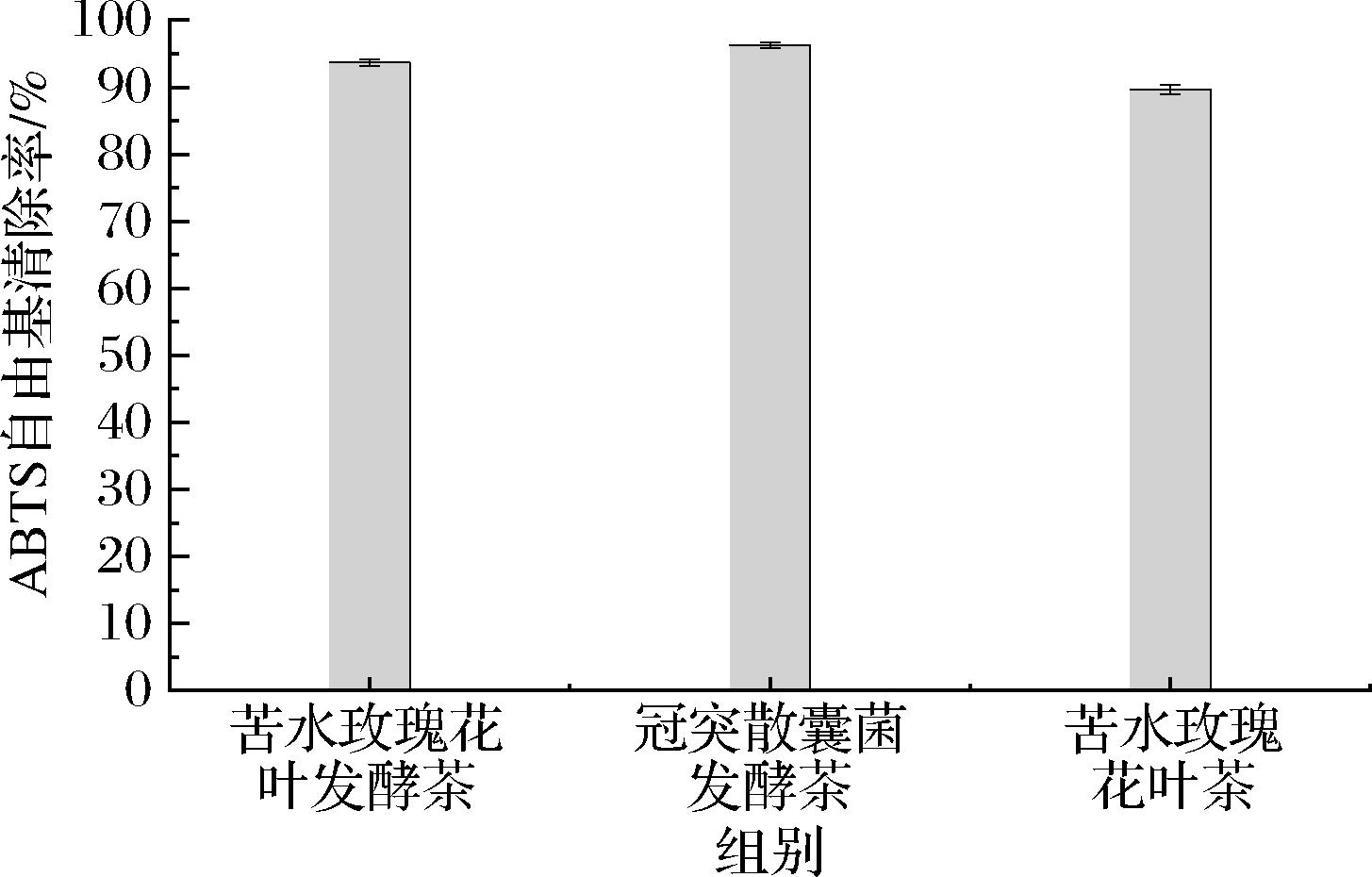
图5 三种处理下ABTS阳离子自由基清除能力结果
Fig.5 Results of ABTS cation radical scavenging capacity with three treatment conditions
2.7 清除羟自由基能力比较
清除羟自由基的能力如图6所示。经冠突散囊菌发酵的苦水玫瑰花叶茶具有较高的清除羟自由基的能力,清除能力达到43.05%,而经自然发酵的苦水玫瑰花叶茶和未经发酵处理的苦水玫瑰花叶茶清除羟自由基的能力差异不显著,分别为35.80%和34.39%,这可能是由于发酵后茶叶中茶黄酮和茶色素含量的增加。吕娜等[34]的研究指出,茶黄酮具有高效的羟自由基清除能力。
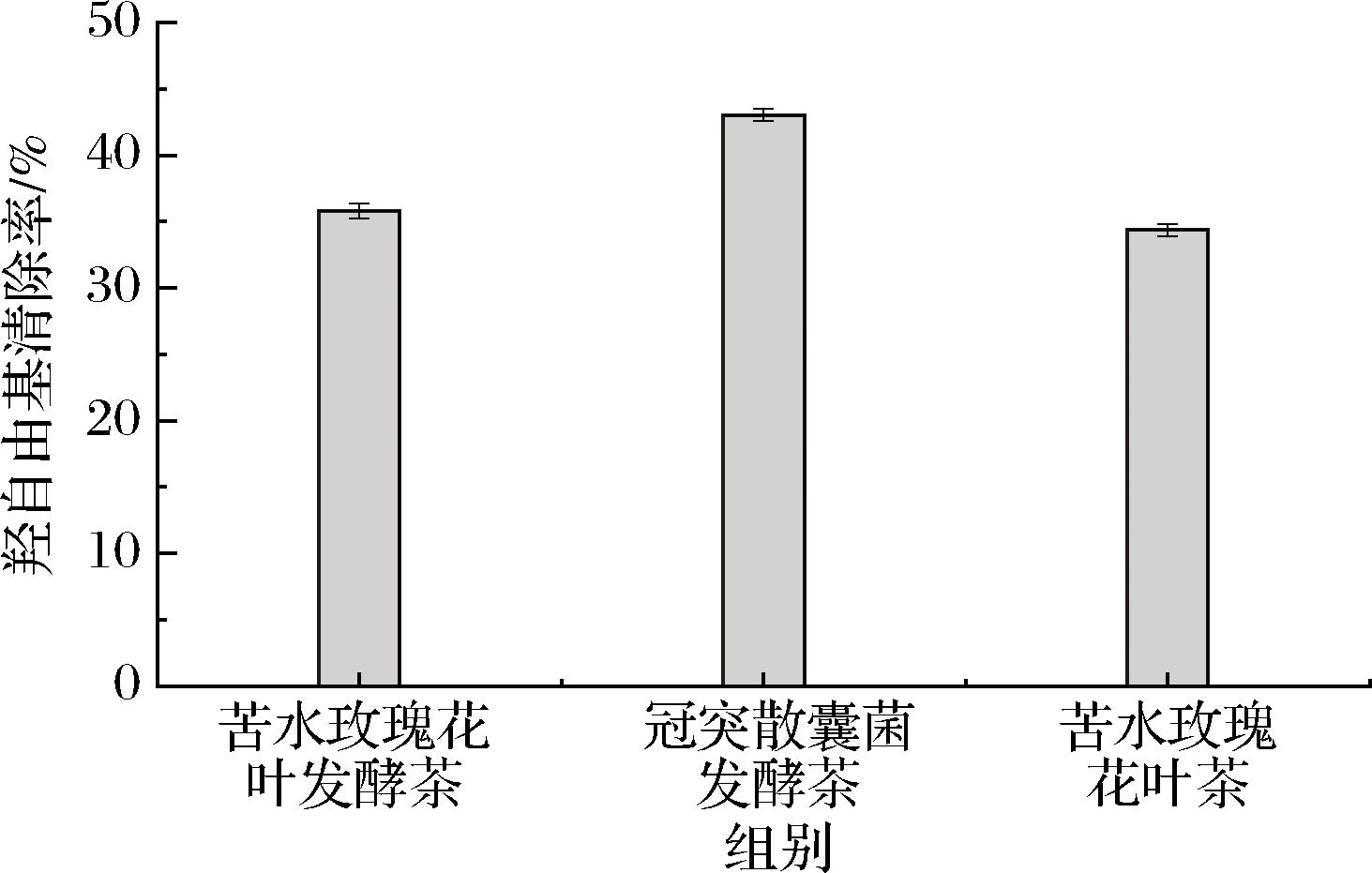
图6 三种处理下羟基自由基清除能力结果
Fig.6 Results of hydroxyl radical scavenging capacity with three treatment conditions
3 结论与讨论
冠突散囊菌在发酵茶叶时分泌的淀粉酶和氧化酶等酶类,将茶叶中的蛋白质和淀粉分解为单糖,利用多酚类物质,转化成对人体有益的物质,使茶叶品质和口感得到提升[23,35-36]。本研究发现冠突散囊菌发酵茶总儿茶素含量(2.672 mg/g)下降了70.69%,儿茶素含量(1.212 mg/g)增加了79.04%,这可能是由于儿茶素的衍生物或中间代谢产物转化生成了儿茶素,使其在发酵过程中相对含量上升。而自然发酵的苦水玫瑰花叶茶和未经发酵的苦水玫瑰花叶茶表没食子儿茶素和表没食子儿茶素没食子酸酯有略微显著变化,可能是由于自然发酵下参与的微生物发酵与冠突散囊菌发酵存在显著差异,自然发酵过程中的优势微生物主要为酵母菌、乳酸菌等,这类微生物的代谢活动多集中于糖类与有机酸的代谢,对咖啡因的代谢转化能力相对较弱。因此,在缺乏冠突散囊菌的特定酶的作用下,咖啡因含量在自然发酵过程中保持相对稳定。同时,发酵后的茶褐素含量显著增加(P<0.05),增加了83.48%,这可能是由于冠突散囊菌分泌的酶类催化酚类物质或茶黄素的氧化反应,促进了茶褐素的生成[32,35]。而未经发酵的苦水玫瑰花叶茶中可溶性总糖、葡萄糖、果糖、蔗糖含量高于经冠突散囊菌发酵和自然发酵的苦水玫瑰花叶茶,可能是没有微生物的代谢活动导致糖类的分解和转化,使糖类含量保持相对稳定。
抗氧化实验结果显示,冠突散囊菌发酵茶表现出显著的抗氧化能力。通常认为,茶多酚、黄酮类化合物以及茶色素等成分是茶叶中发挥抗氧化作用的关键活性物质[33-34,37-38]。冠突散囊菌发酵茶茶多酚含量显著(P<0.05)下降,下降了10.51%。但经冠突散囊菌发酵处理的茶叶表现出较好的抗氧化活性,因为发酵过程中黄酮结构转化、生成新抗氧化物质,且各类成分产生协同效应,多种因素影响了总黄酮的含量。茶汤风味的形成机制是多种呈味物质相互作用的结果,主要包括苦味、涩味、鲜味、酸味和咸味等。其中,苦涩味的形成与茶多酚及儿茶素类化合物相关,而氨基酸和茶色素在赋予茶汤鲜味以及刺激性口感方面发挥着重要作用[39]。利用冠突散囊菌发酵恰好降低了茶叶茶汤的苦涩味,一定程度上改善了冠突散囊菌发酵茶的营养和风味。
[1] CHEN Y L, WANG Y L, CHEN J X, et al.Bioprocessing of soybeans (Glycine max L.) by solid-state fermentation with Eurotium cristatum YL-1 improves total phenolic content, isoflavone aglycones, and antioxidant activity[J].RSC Advances, 2020,10(29):16928-16941.
[2] 蔡正安, 刘素纯, 刘仲华, 等.茯砖茶中冠突散囊菌纤维素酶的酶学性质研究[J].茶叶科学, 2010,30(1):57-62.CAI Z A, LIU S C, LIU Z H, et al.Cellulase enzymatic property of Eurotium cristatum from brick tea[J].Journal of Tea Science, 2010, 30(1):57-62.
[3] 胡治远, 刘素纯, 徐正刚.黑茶中“金花菌”线粒体基因组序列测定及系统发育分析[J].菌物学报, 2021,40(1):135-151.HU Z Y, LIU S C, XU Z G.Sequencing and phylogenetic analysis of the mitochondrial genome of the “Jinhua-Jun” isolated from fermented dark tea[J].Mycosystema, 2021, 40(1):135-151.
[4] XIAO Y, LI M Y, LIU Y, et al.The effect of Eurotium cristatum (MF800948) fermentation on the quality of autumn green tea[J].Food Chemistry, 2021, 358:129848.
[5] 邹金美, 宋宗仁, 蔡咚玲, 等.冠突散囊菌固体发酵铁观音茶的主要活性成分及其抗氧化性分析[J].食品工业科技, 2021,42(22):369-375.ZOU J M, SONG Z R, CAI D L, et al.Analysis on the main active components and antioxidant activity of tieguanyin tea fermentation by Eurotium cristatum[J].Science and Technology of Food Industry, 2021, 42(22):369-375.
[6] 林俊涵, 林红梅, 潘志斌, 等.基于非靶向代谢组学的冠突散囊菌发酵代谢产物分析[J].福建农业科技, 2023,54(6):1-10.LIN J H, LIN H M, PAN Z B, et al.Analysis of the fermentation metabolites from Eurotium cristatum based on the non-targeted metabolomics[J].Fujian Agricultural Science and Technology, 2023, 54(6):1-10.
[7] 郭鹏辉,王瑾书,韦体,等.苦水玫瑰的开发利用现状与发展对策[J].安徽农学通报,2017,23(13):31-33;38.GUO P H, WANG J S, WEI T, et al.The present situation of exploitation and utilization and development countermeasures of rose sertata × R.Rugosa Yu.et.ku[J].Anhui Agricultural Science Bulletin, 2017, 23(13):31-33;38.
[8] 肖明, 邓艳芳, 刘文卓, 等.黄河上游丘陵地引种苦水玫瑰适应性评价[J].中国水土保持, 2022, (12):57-60;7.XIAO M, DENG Y F, LIU W Z, et al.Adaptability evaluation of Rosa sertata×Rosa rugosa introduced into hilly land of the upper Yellow River[J].Soil and Water Conservation in China, 2022, (12):57-60;7.
[9] 颜子曦, 李永慧, 孟德豪, 等.苦水玫瑰中49项营养及活性成分指标分析与评价[J].北京林业大学学报, 2023,45(2):120-128.YAN Z X, LI Y H, MENG D H, et al.Analysis and evaluation of 49 nutritional and active component indexes of Kushui rose(Rosa setate×R.Rugosa)[J].Journal of Beijing Forestry University, 2023, 45(2):120-128.
[10] 陈兴都, 蒋玉梅, 李霁昕, 等.苦水玫瑰叶芽饮料加工工艺的优化[J].食品工业科技, 2013,34(6):320-324;333.CHEN X D, JIANG Y M, LI J X, et al.Optimization of processing of Kushui rose leafgems beverage[J].Science and Technology of Food Industry, 2013, 34(6):320-324;333.
[11] 罗冰. 茯砖茶发酵菌生物学特性及其发酵剂制备研究[D].西安:陕西科技大学, 2014.LUO B.Study on biological characteristics of fermentation fungus from Fuzhuan brick tea and preparation of starter[D].Xi’an:Shaanxi University of Science and Technology, 2014.
[12] 张国广, 沈琳, 黄冰晴, 等.灵芝固体发酵龙眼核提取物的主要活性成分及其抗氧化性[J].食品工业科技, 2019,40(2):53-57.ZHANG G G, SHEN L, HUANG B Q, et al.Main active components and antioxidant activity of extracts from Ganoderma lucidum solid fermentation Longan seed[J].Science and Technology of Food Industry, 2019, 40(2):53-57.
[13] 丁笑莉, 高建, 高源, 等.用高效液相色谱法测定食品中总糖含量方法探讨[J].中国公共卫生管理, 2012,28(6):814-815.DING X L, GAO J, GAO Y, et al.Discussion on determination of total sugar content in food by high performance liquid chromatography[J].Chinese Journal of Public Health Management, 2012, 28(6):814-815.
[14] 黄德娜, 李锋, 曾承露.都匀毛尖绿茶与红茶中氨基酸含量的测定[J].云南化工, 2020, 47(11):75-77.HUANG D N, LI F, ZENG C L.Determination of amino acids content in Duyun Maojian green tea and black tea[J].Yunnan Chemical Technology, 2020, 47(11):75-77.
[15] 赵保堂, 杨富民, 朱秀萍, 等.藜麦多酚的超声辅助提取工艺优化及体外抗氧化活性研究[J].食品与发酵科技, 2018,54(4):8-15.ZHAO B T, YANG F M, ZHU X P, et al.Optimization of ultrasonic assisted extraction of Chenopodium quinoa polyphenol and antioxidant activity[J].Food and Fermentation Sciences &Technology, 2018, 54(4):8-15.
[16] 林军. 遮阴影响铁观音暑茶品质的机理研究[D].福州:福建农林大学, 2015.LIN J.Study on the mechanism of summer Tieguanyin tea’S (Camellia sinensis (L.) O.Kuntze) quality under different shading conditions[D].Fuzhou:Fujian Agriculture and Forestry University, 2015.
[17] 吴以龙, 王康, 武增才, 等.高效液相色谱法测定与比较5种不同提取方法提取的茶叶咖啡因[J].食品研究与开发, 2023,44(3):195-200.WU Y L, WANG K, WU Z C, et al.Determination and comparison of tea caffeine extracted by five different extraction methods by high performance liquid chromatography[J].Food Research and Development, 2023, 44(3):195-200.
[18] 米水杉, 韩宝瑜.黄化茶树叶色、干茶、汤色色度季节变化及其与茶汤色素的关联性[J].茶叶通讯, 2023,50(4):468-478.MI S S, HAN B Y.Seasonal changes in leaf color, dry tea and tea soup color chromaticity of etiolated tea trees and their correlation with tea soup pigments[J].Journal of Tea Communication, 2023, 50(4):468-478.
[19] 张桂芳, 张东杰, 鹿保鑫, 等.不同萌发时间黑豆芽总黄酮含量及DPPH自由基清除能力的测定[J].食品科技, 2020,45(12):39-45.ZHANG G F, ZHANG D J, LU B X, et al.Determination of total flavonoid content and DPPH free radical scavenging ability of black bean sprouts at different germination times[J].Food Science and Technology, 2020, 45(12):39-45.
[20] 张靖鹏, 彭岩枫, 张得钧.枸杞清汁酶解澄清工艺优化及体外抗氧化作用[J].食品研究与开发, 2024,45(1):83-91.ZHANG J P, PENG Y F, ZHANG D J.Optimization of enzymatic hydrolysis for clarification and antioxidant activity in vitro of Lycium barbarum clear juice[J].Food Research and Development, 2024, 45(1):83-91.
[21] 傅志丰, 王慧宾, 邓朝阳, 等.响应面法优化超声波辅助提取虎奶菇多酚工艺及其抗氧化活性分析[J].粮食与油脂, 2025,38(4):120-125.FU Z F, WANG H B, DENG C Y, et al.Optimization of ultrasoud-assisted extraction of polyphenols from Pleurotus tuber-regium (Fr.) Sing by response surface methodology and analysis of its antioxidant activity[J].Cereals &Oils, 2025, 38(4):120-125.
[22] 陈琳琳, 邱树毅, 罗小叶, 等.夏秋茶发花工艺及发花过程中主要物质成分变化[J].食品工业, 2017,38(9):71-75.CHEN L L, QIU S Y, LUO X Y, et al.The fungus grow processing of summer-autumn tea and the changes of main components during the fungus growing[J].The Food Industry, 2017, 38(9):71-75.
[23] XIAO Y, ZHONG K, BAI J R, et al.The biochemical characteristics of a novel fermented loose tea by Eurotium cristatum (MF800948) and its hypolipidemic activity in a zebrafish model[J].LWT, 2020, 117:108629.
[24] 马艳蕊, 王顺明, 李学震, 等.桑黄与冠突散囊菌发酵桑叶红茶功能性对比[J].中国食用菌, 2022,41(3):55-58;64.MA Y R, WANG S M, LI X Z, et al.Comparative on the functional properties of mulberry black tea fermented by Phellinus igniarius and Eurotium cristatum[J].Edible Fungi of China, 2022, 41(3):55-58;64.
[25] 刘菲, 薛志慧, 叶倩林, 等.“发花”对白茶风味品质的影响研究[J].茶叶科学, 2016,36(3):301-311.LIU F, XUE Z H, YE Q L, et al.Study on effect of fungal-fermentation process on flavor quality in white tea[J].Journal of Tea Science, 2016, 36(3):301-311.
[26] 黄婧. “金花”菌的分离鉴定及其对茶叶成分的生物转化[D].福州:福建师范大学, 2013.HUANG J.Isolation and identification of “Jinhua” fungi and its biotransformation of tea constituents[D].Fuzhou:Fujian Normal University, 2013.
[27] 龚受基, 滕翠琴, 曹惠怡, 等.冠突散囊菌对夏秋绿茶发酵的影响[J].食品科技, 2020,45(1):134-140.GONG S J, TENG C Q, CAO H Y, et al.Influences on summer-autumn tea fermented with Eurotium cristatum[J].Food Science and Technology, 2020, 45(1):134-140.
[28] 黄浩. “散茶发花”的微生物与化学机制研究[D].长沙:湖南农业大学, 2014.HUANG H.Study the microorganisms and chemical mechanism in the “fungal fementation with loose tea”[D].Changsha:Hunan Agricultural University, 2014.
[29] 刘武嫦, 仇云龙, 黄建安, 等.冠突散囊菌对发花黑毛茶品质呈味成分的影响[J].食品安全质量检测学报, 2015,6(5):1554-1560.LIU W C, QOU Y L, HUANG J A, et al.Studies on Eurotium cristatum fungus growing affects quality tasting ingredients of primary dark tea[J].Journal of Food Safety and Quality Testing, 2015, 6(5):1554-1560.
[30] 王亚丽, 秦俊哲, 黄亚亚, 等.冠突散囊菌对茯砖茶品质形成的影响[J].食品与发酵工业, 2018,44(4):194-197.WANG Y L, QIN J Z, HUANG Y Y, et al.Effect of the quality of Fuzhuan brick tea fermented in Eurotium cristatum[J].Food and Fermentation Industries, 2018, 44(4):194-197.
[31] 谭超, 郭刚军, 李宝才, 等.普洱茶茶褐素理化性质与光谱学性质研究[J].林产化学与工业, 2010,30(4):53-58.TAN C, GUO G J, LI B C, et al.Physico-chemical and spectral properties of theabrownin from Pu-erh tea[J].Chemistry and Industry of Forest Products, 2010, 30(4):53-58.
[32] 欧阳梅, 熊昌云, 屠幼英, 等.冠突散囊菌对茶叶品质成分及其抗氧化活性影响[J].菌物学报, 2011,30(2):343-348.OUYANG M, XIONG C Y, TU Y Y, et al.Effects of Eurotium cristatum on tea quality and antioxidant activity[J].Mycosystema, 2011, 30(2):343-348.
[33] 文治瑞, 王佳菜, 刘丽明, 等.超声波辅助提取金花茶中黄酮类物质工艺及体外抗氧化研究[J].食品安全质量检测学报, 2020,11(13):4364-4370.WEN Z R, WANG J C, LIU L M, et al.Study on the ultrasonic assisted extraction of flavonoids from Camellia chrysantha and the antioxidant in vitro[J].Journal of Food Safety and Quality, 2020, 11(13):4364-4370.
[34] 吕娜, 张伟臻, 陈林龙, 等.安吉白茶黄酮抗氧化活性的体外实验研究[J].毒理学杂志, 2014,28(5):389-392.LYU N, ZHANG W Z, CHEN L L, et al.Experimental study on antioxidant activity of flavonoids from Anji white tea in vitro[J].Journal of Toxicology, 2014, 28(5):389-392.
[35] XIAO Y, LI M Y, WU Y P, et al.Structural characteristics and hypolipidemic activity of theabrownins from dark tea fermented by single species Eurotium cristatum PW-1[J].Biomolecules, 2020, 10(2):204.
[36] 邹敏敏, 董其惠, 黄彦, 等.冠突散囊菌发酵黑毛茶提取液的研究[J].生物加工过程, 2019,17(4):409-417.ZOU M M, DONG Q H, HUANG Y, et al.Submerged liquid fermentation of raw dark tea by Eurotium cristatum[J].Chinese Journal of Bioprocess Engineering, 2019, 17(4):409-417.
[37] PIETTA P G.Flavonoids as antioxidants[J].Journal of Natural Products, 2000, 63(7):1035-1042.
[38] ZHANG J J, MENG G Y, ZHAI G Y, et al.Extraction, characterization and antioxidant activity of polysaccharides of spent mushroom compost of Ganoderma lucidum[J].International Journal of Biological Macromolecules, 2016, 82:432-439.
[39] 杜继煜, 白岚, 白宝璋.茶叶的主要化学成分[J].农业与技术, 2003(1):53-55.DU J Y, BAI L, BAI B Z.Main chemical constituents of tea[J].Agriculture and Technology, 2003,23(1):53-55.