陈皮(Chenpi)为芸香科植物橘Citrus reticulata Blanco及其栽培变种的干燥成熟果皮[1],主要分布于我国南方地区,主产地为广东、四川、浙江、湖北等省[2],是一味常用的药食同源中药,性温,味苦辛[1],具有化痰,止咳平喘、调节肠胃、改善心血管功能等作用[1,3],且因陈皮具有独特的芳香气味,通常被用于制作药膳,如陈皮酒、陈皮普洱茶、陈皮粥等[4],也可作为调味品为其他食物增加风味。蒸陈皮是岭南地区的特色炮制品,由陈皮通过清蒸法制得而成[5],蒸制后的陈皮,辛燥之性缓和[6],尤其适用于岭南人中焦脾胃虚弱的体质[3,7],在岭南地区得到广泛的临床应用。另外,陈皮蒸制后,辛香燥烈的气味减小,香气变得柔和,更令人舒适,可提高消费者的接受度。因此其在功能食品开发与应用上具有良好前景。目前,关于蒸陈皮的研究多集中在蒸制工艺优化、蒸制前后化学成分变化和药效学研究等方面[3,7-10],其风味研究较少。
陈皮的香气是其主要的风味来源,因此气味特征分析是陈皮风味评价的关键指标之一。传统气味评判依赖人工经验,通过鼻嗅的方式完成,但难以保证其客观性与准确性。电子鼻是一种拟人嗅觉系统的气味检测技术,其传感器可客观、快速准确地区分各种气味特征,实现品种分类[11-12]。挥发性成分也是陈皮风味评价的重要指标[13]。但目前关于蒸陈皮的香气特征变化的相关研究较少,多围绕陈皮蒸制前后挥发性成分的变化展开,且研究中多采用水蒸气蒸馏法提取挥发油后,通过GC-MS技术进行定性定量分析,制备过程较复杂,研究耗时[6,12],且挥发性成分在长时间加热中可能发生变化[14]。而顶空固相微萃取-气相-质谱联用技术(headspace solid-phase microextraction-gas chromatography-mass spectrometry,HS-SPME-GC-MS)可在样品无损的条件下,采用顶空进样的方式对其挥发性成分进行定性定量分析,具有灵敏度高、检测速度快、不需要溶剂的优越性[15-16],目前已逐渐广泛应用于食药领域。
挥发性成分的研究种类繁多,难以确定各类成分对食品整体风味的影响程度,整体气味与挥发性成分的感觉阈值和相对含量密切相关。相对气味活度值(relative odor activity value,ROAV)可根据化合物的感觉阈值和香气丰度来分析化合物对食品整体风味的贡献度,将主观的气味特征量化[17],广泛应用于食品风味研究。陈皮蒸制后香气特征发生明显变化,与陈皮相比,蒸陈皮风味与功效独特,可作为功能食品与化妆品、香料等行业开发的新原料,因此有必要对其香气进行研究,探究陈皮蒸制前后的挥发性成分与香气特征的变化。
本研究通过利用电子鼻与HS-SPME-GC-MS技术对陈皮及蒸陈皮的整体气味与具体成分进行客观性评价,结合ROAV对陈皮与蒸陈皮的差异性香气成分进行解析,并对气味与其所含挥发性成分进行相关性研究,可为进一步阐释陈皮蒸制前后的风味特征变化提供参考,为蒸陈皮的质量控制与制备工艺研究提供新的评价途径,并为其在食品、化妆品、香料等行业的应用提供依据。
1 材料与方法
1.1 实验材料
4批陈皮药材(编号1~4)均由广州采芝林药业有限公司提供,样品及产地信息见表1。
表1 陈皮样品信息
Table 1 Information of Chenpi samples
编号产地批号陈皮蒸陈皮1广东220409C1Z12四川CP-230725-01C2Z23浙江CP2023071902C3Z34湖北CP-230731-01C4Z4
1.2 仪器与设备
CNose-18电子鼻(包含18个MOS传感器,其主要响应物质见表2),上海保圣实业发展有限公司;Agilent 7890B/5977A气相色谱质谱联用仪、Agilent HP-5MS气相色谱柱(30 m×250 μm,25 μm),美国安捷伦公司;65 μm固相微萃取仪-纤维头(PDMS/DVB,蓝色),美国SUPELCO公司;京制00000246号电子天平,赛多利斯科学仪器有限公司;BL-100电子天平,厦门佰伦斯电子科技有限公司;DGX-g243B-2鼓风干燥箱,上海福玛实验设备有限公司;600Y高速多功能粉碎机,永康市铂欧五金制品有限公司。
表2 电子鼻传感器主要响应物质
Table 2 The main substances that the electronic nose sensors respond to
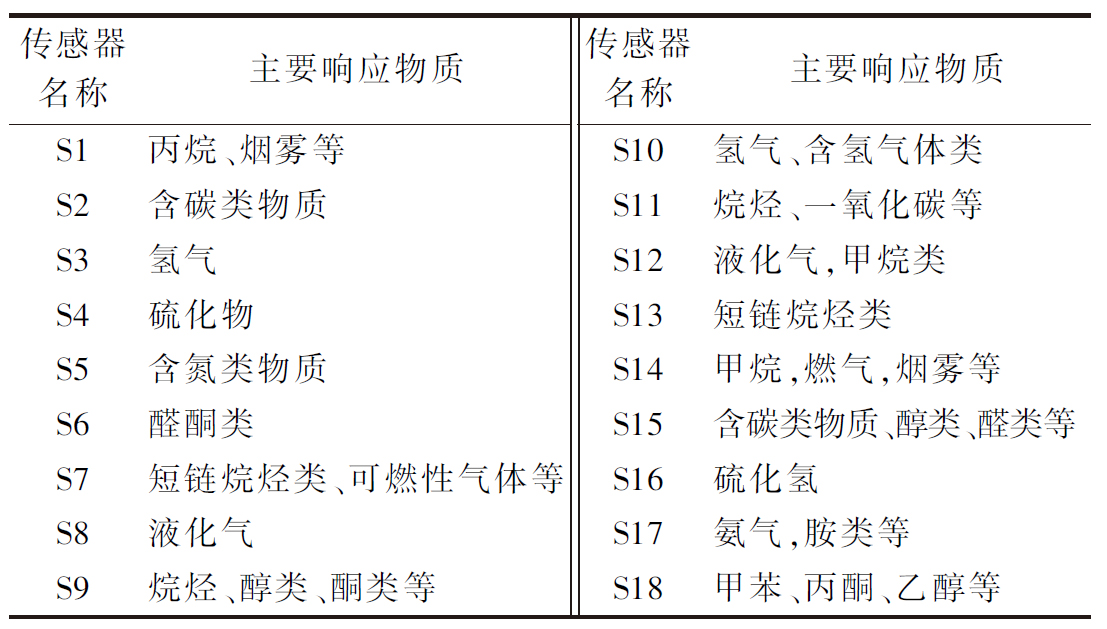
1.3 实验方法
1.3.1 样品的制备
1.3.1.1 陈皮
取各批次陈皮药材,除去杂质,喷淋清水,润透,切丝,干燥,制得陈皮饮片[1],编号C1~C4,备用。
1.3.1.2 蒸陈皮
取各批次陈皮饮片,按1984年版《广东省中药炮制规范》[5],喷淋清水闷润2 h,蒸制4 h,闷18 h,取出,50 ℃干燥6 h,制得蒸陈皮饮片,编号Z1~Z4,备用。
1.3.2 电子鼻检测
1.3.2.1 供试品的制备
分别称取陈皮样品C1~C4、蒸陈皮样品Z1~Z4约3.0 g(体积约为进样瓶1/3)置于40 mL电子鼻样品瓶中,加盖密封,封口膜封口,静置18 h,使顶空瓶中充盈样品气体。每份样品平行制备3份测定,取平均值进行数据分析。
1.3.2.2 测定方法
采用直接顶空进样法。预热仪器20 min,直接将进样针头插入含样品的密封样品瓶中,进行电子鼻检测。以电子鼻响应值的主成分分析相近度为指标,考察样品静置时间和信号采集时间,确定静置时间为18 h,信号采集时间60 s,传感器自清洗时间120 s,检测样品流速为60 mL/min,进行测定。
1.3.3 HS-SPME-GC-MS检测
1.3.3.1 供试品的制备
将电子鼻检测所用样品粉碎(过3号筛),取约1.0 g,精密称定,置于10 mL顶空进样瓶中,密封后放置在样品盘,待检。每份样品平行制备3份测定,取平均值进行数据分析。
1.3.3.2 顶空条件
样品瓶加热温度120 ℃,平衡时间15 min;定量环温度130 ℃,进样时间1 min;传输线温度140 ℃;压力平衡时间0.5 min。
1.3.3.3 气相色谱条件
色谱柱为HP-5 MS弹性石英毛细管柱(30 m×0.25 mm×0.25 μm);程序升温:初始温度50 ℃,以10 ℃/min升至100 ℃,保持1 min;以20 ℃/min升至140 ℃,保持1 min;以5 ℃/min升至165 ℃,保持1 min;以20 ℃/min升至250 ℃,保持1 min;进样口温度为220 ℃;载气为高纯度氦气(纯度>99.999%);柱前压为9.8 psi;柱流量为1.0 mL/min;分流进样,分流比为10∶1;溶剂延迟时间3.6 min。
1.3.3.4 质谱条件
离子源EI源;离子源温度230 ℃;四级杆温度150 ℃;电子能量70 eV;倍增管电压1.2 kV;接口温度230 ℃;质荷比范围40~450 m/z。
1.3.3.5 定性分析
参考相关文献[16],利用NIST14标准谱库检索化合物,选取匹配度(positive match,P.Match)>85%的化合物,结合CAS号及参考相关文献对化合物定性分析,鉴别成分。采用面积归一化法,根据不同化合物峰面积计算其相对质量分数(%),结果用“平均值±标准差”来表示。
1.3.4 ROAV分析
香气活度值(odor activity values,OAV)是挥发性成分的含量与感觉阈值的比值,表示挥发性成分对样品风味的贡献度,参考刘登勇等[18]的方法,计算如公式(1)所示:
(1)
ROAV通常用于确定每种挥发性成分对主要气味的贡献,ROAV越大,对气味的贡献越大。将对样品气味贡献最大的组分的ROAVmax赋值为100,其他挥发性组分计算如公式(2)所示,参考ZHANG等[19]的方法:
(2)
式中:Ci和Ti分别为相对含量(每种化合物的峰强度占待测定化合物总峰强度的百分比)和每种挥发性成分的感觉阈值(空气中的阈值:mg/m3)。Cmax和Tmax是样品中OAV最大的化合物的相对含量和感觉阈值[19]。
1.4 数据分析
每组数据均重复测定3次。利用迈维云平台(https://cloud.metware.cn)进行主成分分析(principal component analysis, PCA),正交偏最小二乘判别分析(orthogonal partial least squares-discriminant analysis,OPLS-DA),筛选出变量投影重要性(variable importance in projection,VIP)≥1的差异成分,绘制相关性热图。雷达图、总离子流图、柱形图通过使用Origin Pro 2021软件绘制。
2 结果与分析
2.1 电子鼻结果分析
2.1.1 电子鼻分析陈皮与蒸陈皮的整体气味特征
取数据采集60 s内传感器最大响应值,绘制陈皮与蒸陈皮的电子鼻气味特征图(图1),结果显示陈皮蒸制前后的气味差异主要体现在S1、S2、S5、S6、S8、S9、S12、S14、S15、S18传感器,且S6、S9、S12、S14、S15、S18传感器差异最大,说明陈皮蒸制前后的气味变化主要体现在含氢气体、含碳物质、醇类、醛类、酮类等挥发性物质上。
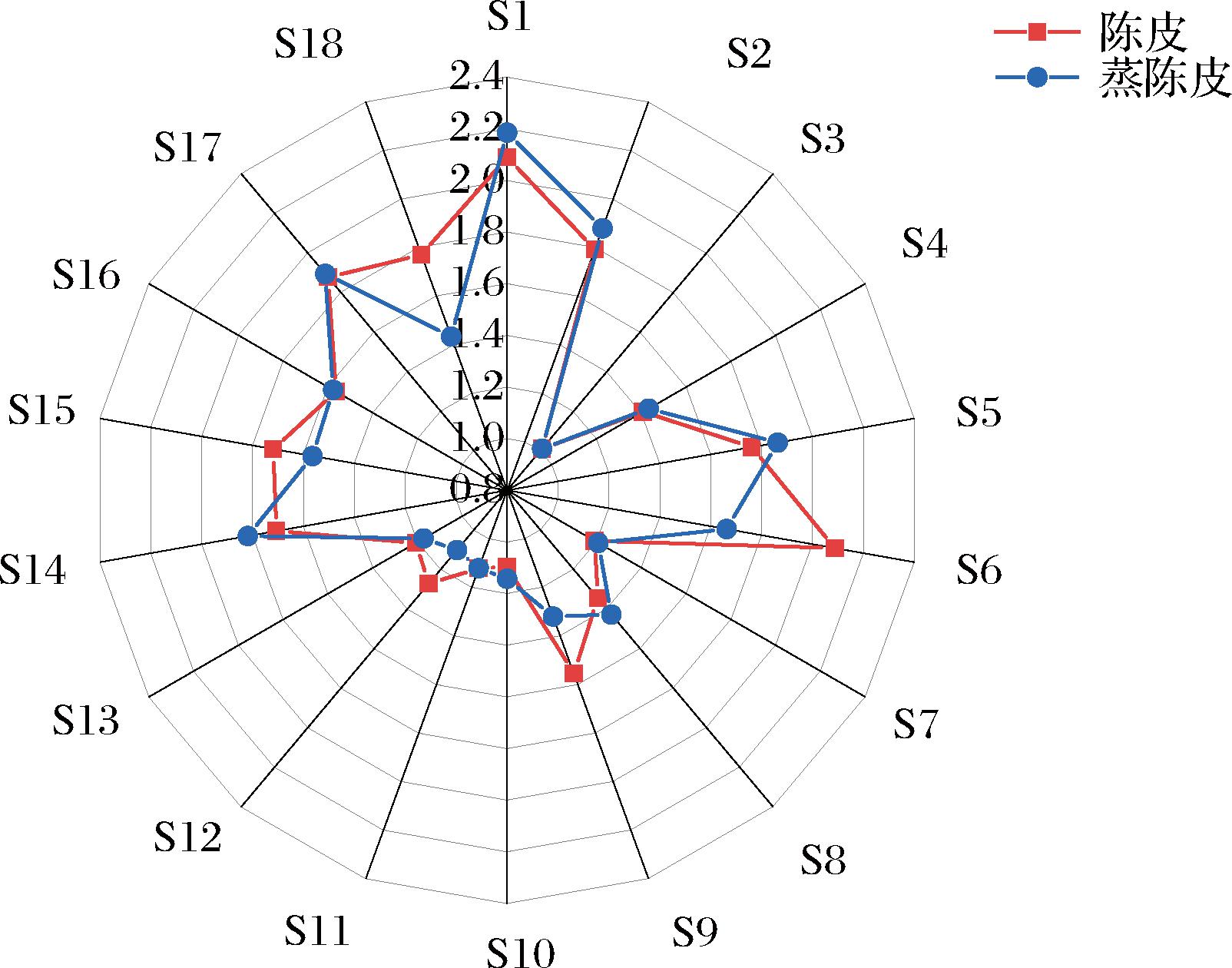
图1 陈皮与蒸陈皮的气味特征雷达图
Fig.1 Radar map response value of electronic nose sensor of Chenpi and steamed Chenpi
2.1.2 电子鼻检测数据的多元统计分析
如图2所示,对电子鼻分析所得陈皮、蒸陈皮的气味数据建立OPLS-DA模型,如图2-a所示,样品的气味特征基本可以被区分为两类,一类为陈皮,另一类为蒸陈皮,提示陈皮蒸制前后气味发生了较为明显的变化。模型拟合指数R2X=0.859、R2Y=0.887,模型预测指数Q2=0.815,拟合指数和模型预测指数>0.5表示该模型稳定性越好,且具备较好的预测能力[15]。VIP可反映OPLS-DA模型中因子对整体特征的贡献程度,VIP≥1的传感器,即为陈皮与蒸陈皮气味差异的特征传感器,按VIP≥1筛选出传感器S9、S18、S15、S6、S12、S10,与陈皮与蒸陈皮的气味特征雷达图结果大致相符,说明结果可靠,该模型可通过分析样品的电子鼻传感器特征,对陈皮蒸制前后的气味特征进行区分。
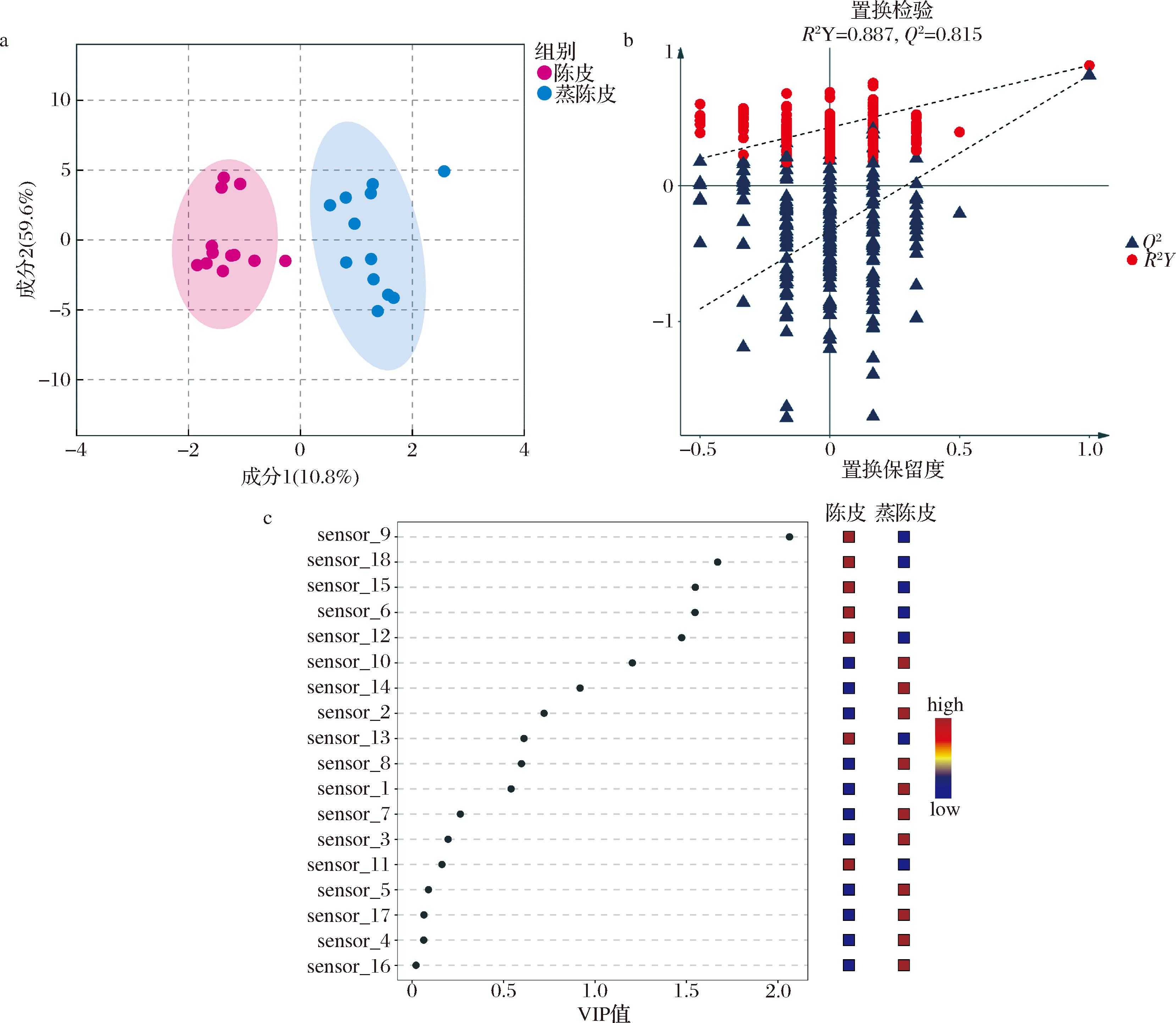
a-OPLS-DA模型得分图;b-模型交叉验证结果;c-VIP值
图2 陈皮与蒸陈皮的电子鼻分析
Fig.2 Electronic nose analysis of Chenpi and steamed Chenpi
2.2 陈皮与蒸陈皮的挥发性成分分析
2.2.1 陈皮与蒸陈皮的HS-SPME-GC-MS测定结果分析
为探究陈皮与蒸陈皮的特征挥发性化合物,按上述顶空进样及GC-MS条件对4个主产地的陈皮及其蒸制品中的挥发性成分进行分析,并采用面积归一化法,根据化合物峰面积计算其相对质量分数(%),见电子版增强出版附表1[15,20-26](https://doi.org/10.13995/j.cnki.11-1802/ts.043310)。根据挥发性成分的峰面积及保留时间参数,绘制陈皮与蒸陈皮的总离子流图如图3所示,与陈皮相比,蒸陈皮在保留时间为12~16 min有明显的特征峰,据表3可知其为倍半萜烯类。结果共鉴别出31种化合物,陈皮与蒸陈皮的共有成分为13种。陈皮鉴别出23种化合物,包括醛类4种、醇类4种、酚类2种、单萜烯类4种、倍半萜烯类6种、酮类1种、酯类1种、芳香烃类1种;蒸陈皮21种,鉴定出醛类3种、醇类0种、酚类1种、单萜烯类4种、倍半萜烯类11种、酮类1种、酯类1种。HS-SPME-GC-MS技术具有样品处理简便、灵敏度高,并可避免大量有机溶剂使用,减少环境污染等优点,但也存在检测范围有限等不足。因此与以往的研究相比,本研究中鉴定出的醇、醛类数量较少[27],可能与本研究使用的顶空固相微萃取技术有关。蒸制后化合物种类减少,不同类别的化合物含量有所增减。蒸制是一个加热过程,加热会使挥发性成分挥发减少[6];萜烯类、醇类和酚类等物质的相对总量变化程度较大,说明化合物之间可能发生了相互转化[28]。
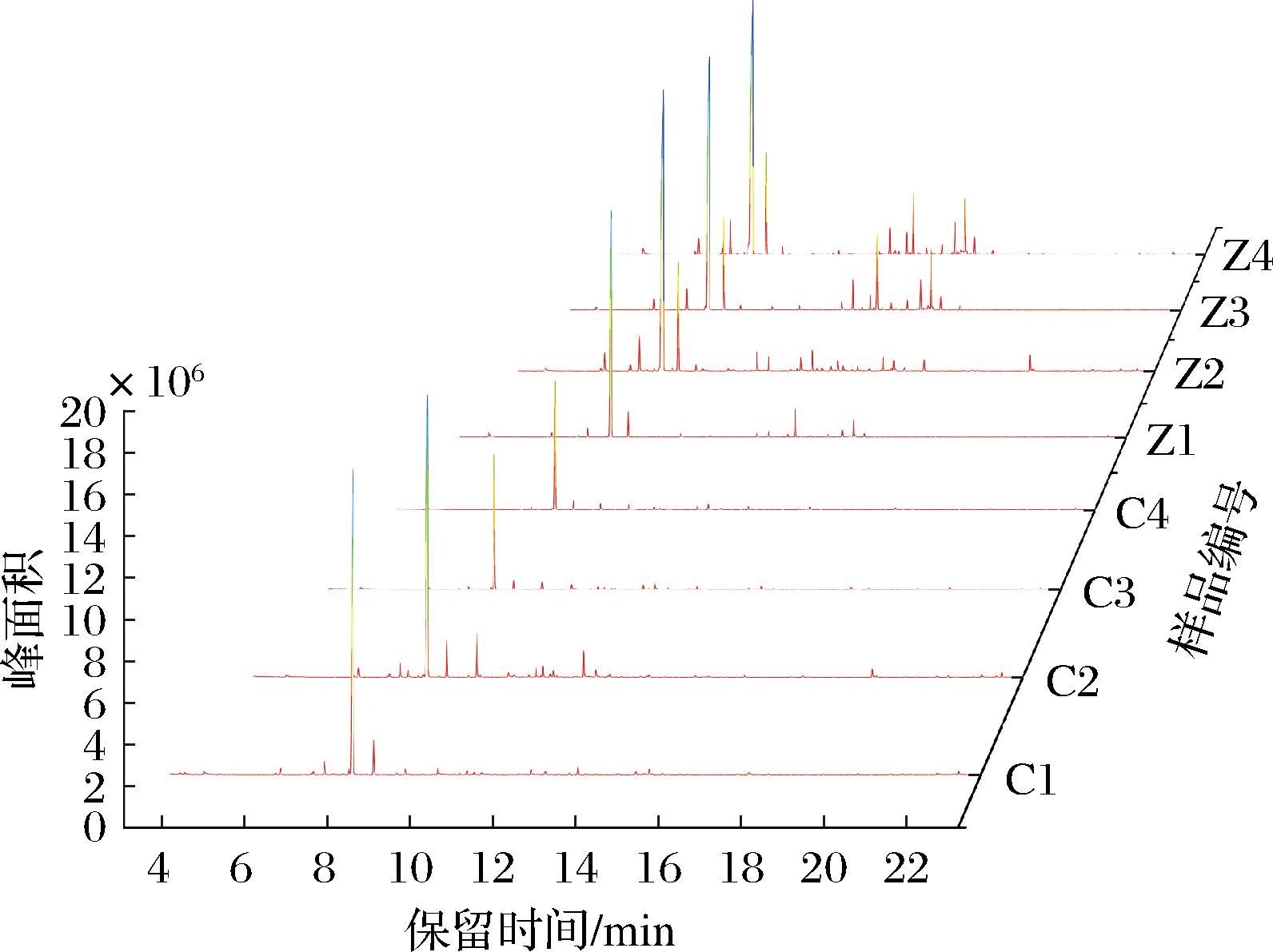
图3 样品气相色谱总离子流图
Fig.3 Total ion chromatography of the samples
表3 不同产地陈皮与蒸陈皮挥发性成分的ROAV
Table 3 ROAV of volatile components of Chenpi and steamed Chenpi from different origins
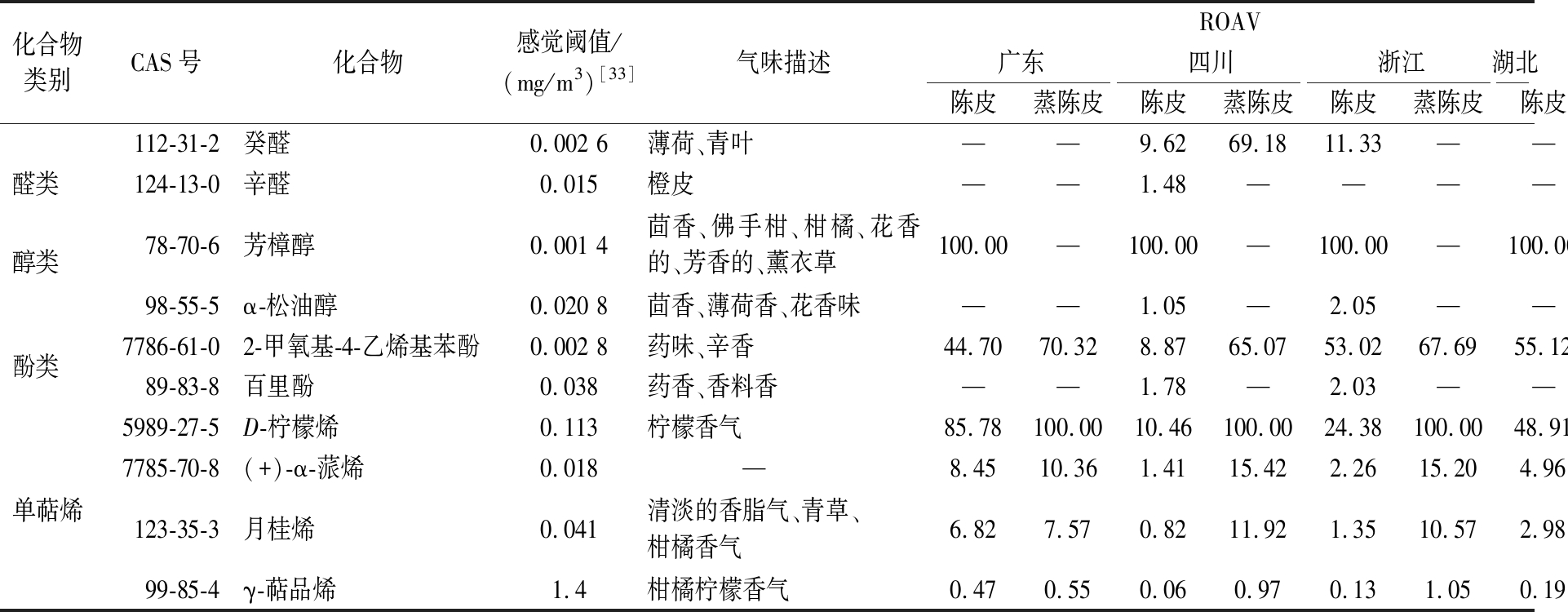
注:表中阈值均为化合物在空气中的感觉阈值;“—”表示样品中未检出,也表示未在相关文献查阅到相关信息。
化合物类别CAS号化合物感觉阈值/(mg/m3)[33]气味描述ROAV广东四川浙江湖北陈皮蒸陈皮陈皮蒸陈皮陈皮蒸陈皮陈皮蒸陈皮112-31-2癸醛0.002 6薄荷、青叶——9.62 69.18 11.33 ———醛类 124-13-0辛醛0.015橙皮——1.48 —————醇类 78-70-6芳樟醇0.001 4茴香、佛手柑、柑橘、花香的、芳香的、薰衣草100.00—100.00 —100.00 —100.00 —98-55-5α-松油醇0.020 8茴香、薄荷香、花香味——1.05 —2.05 ———酚类 7786-61-02-甲氧基-4-乙烯基苯酚0.002 8药味、辛香44.7070.32 8.87 65.07 53.02 67.69 55.12—89-83-8百里酚0.038药香、香料香——1.78 —2.03 ———5989-27-5D-柠檬烯0.113柠檬香气85.78 100.00 10.46 100.00 24.38 100.00 48.91 100.00 7785-70-8(+)-α-蒎烯0.018 —8.45 10.36 1.41 15.42 2.26 15.20 4.96 15.14 单萜烯123-35-3月桂烯0.041清淡的香脂气、青草、柑橘香气6.82 7.57 0.82 11.92 1.35 10.57 2.98 12.99 99-85-4γ-萜品烯1.4柑橘柠檬香气0.47 0.55 0.06 0.97 0.13 1.05 0.19 0.90
不同产地的陈皮蒸制前后的变化存在一定差异(图4-a),因此通过堆积百分比柱状图(图4-b)来展示产地之间的差异及共同之处:所有产地的陈皮蒸制后醇类含量均为0;除广东以外的其他产地陈皮蒸制后醛类、酚类均下降;所有产地的倍半萜类含量在蒸制后显著上升且种类增加,但各产地的单萜类增减趋势有所不同。4个产地的陈皮蒸制前后均以D-柠檬烯这一单萜烯为相对含量最高的挥发性成分,除四川外的其他产地陈皮蒸制后D-柠檬烯均有所下降,广东的下降幅度最大。广东产区的陈皮醛类、酚类含量明显低于其他地区,而蒸制后不降反升,猜测可能是单萜烯转化为醛类、酚类等。各产地的蒸陈皮倍半萜化合物种类及数量不同,据文献报道,陈皮鉴定出的烯烃类成分多含手性中心,存在多种异构体[29],不同产地独有的部分倍半萜化合物实际为同分异构体,如δ-杜松烯和β-杜松烯,β-毕澄茄烯和顺式-β-古巴烯。综上,各产地的陈皮与蒸陈皮的挥发性成分有所差异,共同之处是陈皮蒸制前后的风味特征差异可能主要在于醇类、酚类、倍半萜烯类的含量不同。
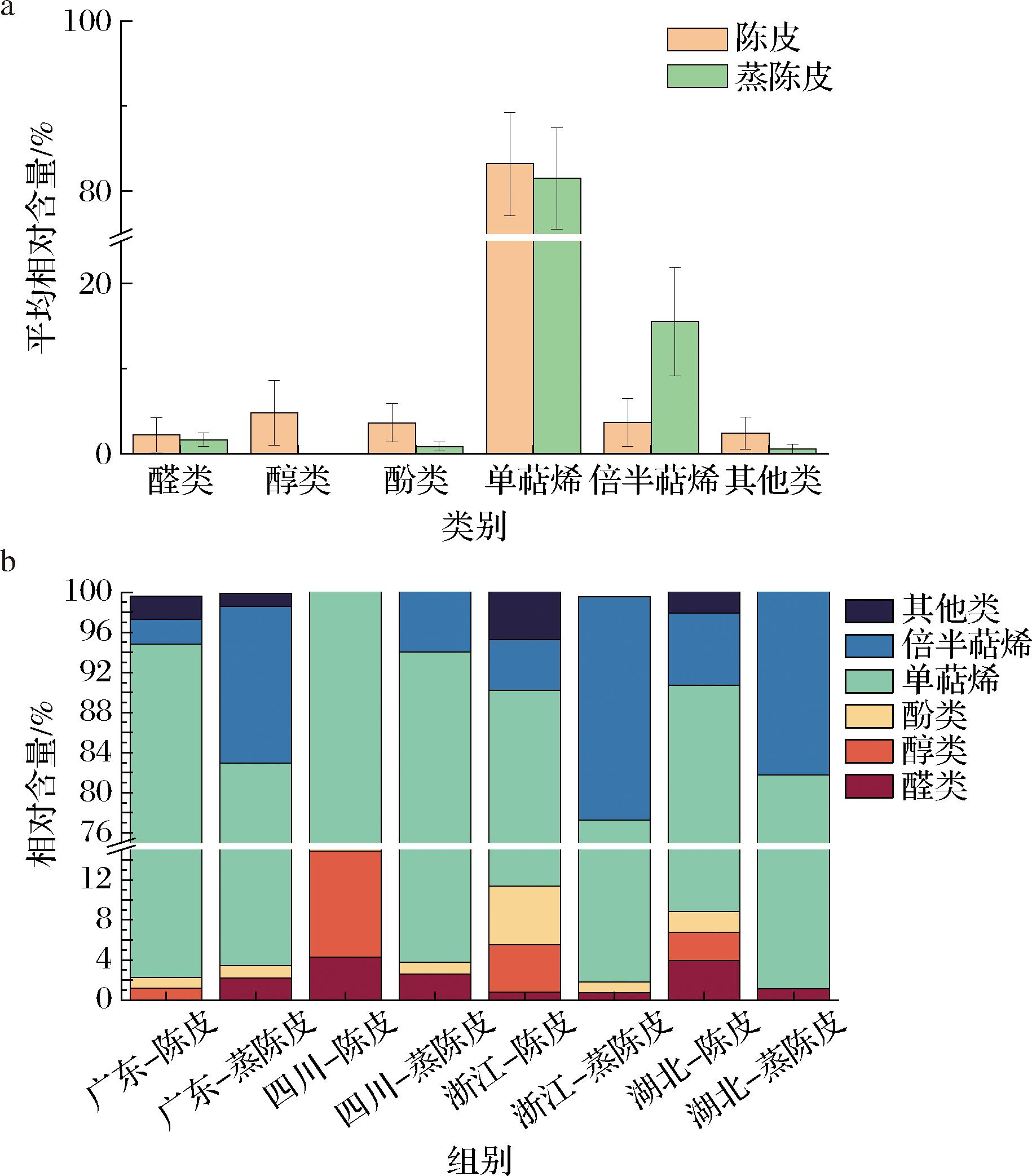
a-陈皮与蒸陈皮的挥发性成分类别含量图; b-不同产地的陈皮与蒸陈皮挥发性成分类别含量百分比图
图4 陈皮蒸制前后挥发性成分含量类别分析
Fig.4 Analysis of the content and types of volatile components in Chenpi before and after steaming
本研究所选的广东、四川、浙江、湖北4个省份是陈皮的主产区,较具代表性,但由于陈皮来自橘(Citrus reticulata Blanco)及其栽培变种。中药材饮片厂采购不限制品种基原,不同产地和不同品种的陈皮虽然在药理作用上的差异较小,但其所含的成分存在较大差异[30]。产地与品种的多样性导致陈皮质量参差不齐[14],影响了陈皮成分研究的一致性。在后续的研究中应注重研究蒸陈皮的品种或产地,以减少影响因素。
2.2.2 陈皮与蒸陈皮挥发性成分的多元统计分析
为进一步探究陈皮与蒸陈皮的主要差异挥发性物质,对不同产地的陈皮与蒸陈皮31种成分进行OPLS-DA,如图5所示,筛选出VIP≥1的14个具有显著差异的成分,包括倍半萜烯6种、单萜烯2种、芳香烃1种、醇类2种、酚类2种、酯类1种。蒸制后芳樟醇、α-松油醇、百里酚含量均下降,古巴烯为新增化合物,结果与高明等[6]的研究结果一致。14个差异性化合物中,各产地陈皮蒸制后倍半萜烯类含量均呈上升趋势,醇类、芳香烃、酯类均呈下降趋势;除广东产区外,其余3个主产地的陈皮蒸制后γ-萜品烯和月桂烯、2-甲氧基-4-乙烯基苯酚均呈下降趋势,趋势基本一致,较有参考价值,可作为区分陈皮蒸制前后挥发性物质差异的依据。本次分析模型的自变量拟合指数R2X=0.615,因变量拟合指数R2Y=0.994,模型预测指数Q2=0.998,经过200次置换检验,Q2回归线与纵轴的相交点<0,且R2Y左侧的所有点均比右侧的最高点低,说明不存在过拟合,该模型验证具有良好效果,可以用于陈皮与蒸陈皮成分差异的鉴别分析[31]。
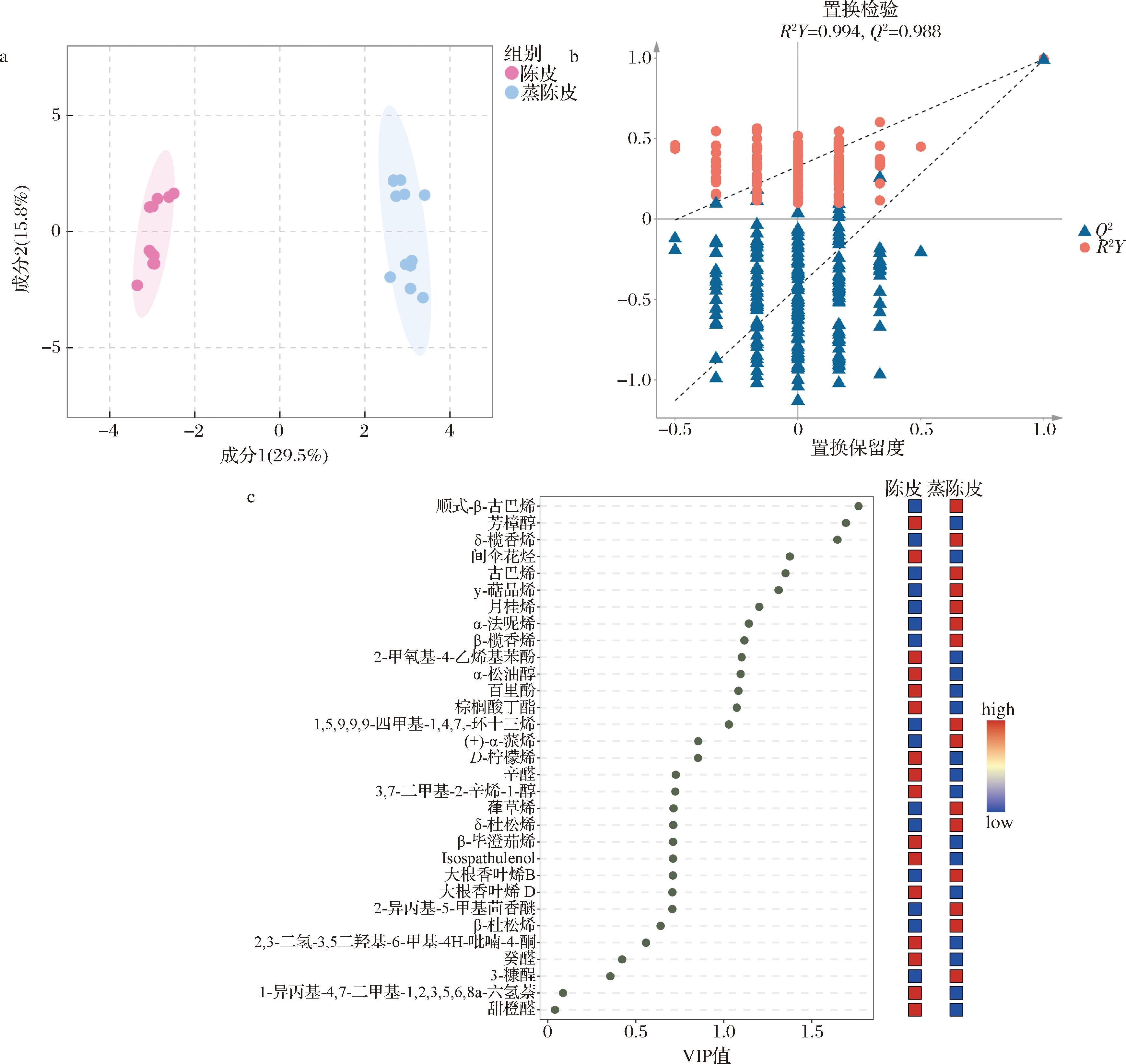
a-OPLS-DA模型得分图;b-模型交叉验证结果;c-VIP值
图5 陈皮与蒸陈皮差异化合物分析
Fig.5 Analysis of differential compounds between Chenpi and steamed Chenpi
2.3 陈皮与蒸陈皮气味与化学成分的相关性分析
为进一步分析陈皮蒸制前后气味和挥发性成分变化的关系,将陈皮与蒸陈皮的电子鼻传感器数据与VIP≥1的14个挥发性成分相对含量进行Pearson相关分析并绘制可视化热图(图6),分析可得,传感器S6、S9、S12、S18与芳樟醇、α-松油醇、百里酚、2-甲氧基-4-乙烯基苯酚呈正相关,与α-法呢烯、β-榄香烯、古巴烯、顺式-β-古巴烯等萜烯类呈负相关;传感器S8、S14与δ-榄香烯、γ-萜品烯、顺式-β-古巴烯等萜烯类呈正相关,与间伞花烃呈负相关。相关性结果表明传感器S6、S9、S12、S18对醇类、酚类、萜烯类都较敏感。表明传感器S8、S14对萜烯类、芳香烃类较敏感,对醇类、酚类不敏感,与其响应物质描述基本一致。结合电子鼻检测结果,陈皮与蒸陈皮的气味差异主要体现在传感器S6、S9、S12、S14、S18,这5个传感器较为稳定且与关键挥发性成分的相关性较强。结合陈皮蒸制前后的挥发性成分组成变化,推测芳樟醇、α-松油醇、百里酚、2-甲氧基-4-乙烯基苯酚等醇类、酚类,α-法呢烯、β-榄香烯、δ-榄香烯、顺式-β-古巴烯等倍半萜烯以及γ-萜品烯是区分陈皮与蒸陈皮气味差异的主要物质基础,电子鼻技术可用于快速判断蒸陈皮生产过程中的气味及质量变化。
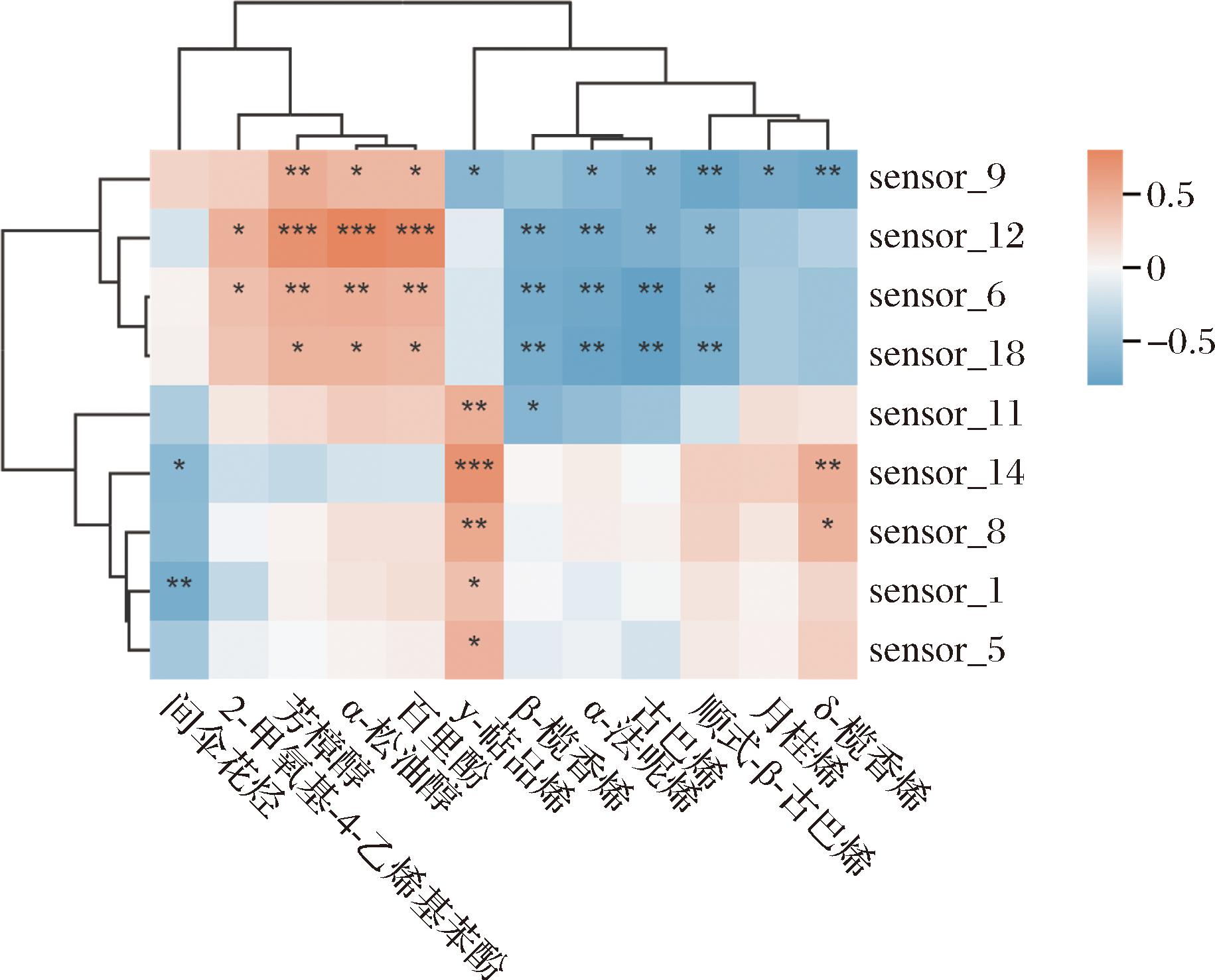
图6 电子鼻传感器与陈皮、蒸陈皮挥发性成分的 Person相关性热图
Fig.6 Person correlation heat map of electronic nose sensor and volatile components of CRP and steamed CRP
注:颜色代表Pearson相关系数的正负,*代表显著性: *P<0.05,**P<0.01,***P<0.005。
2.4 陈皮与蒸陈皮的ROAV分析
ROAV法在评估香气物质对整体香气的贡献方面起着关键作用,可用于确定不同样品气味差异的关键香气成分。分别对4个产地的陈皮与蒸陈皮的挥发性成分计算其ROAV,见表3。先按公式(1)对所有能查找到感觉阈值的化合物的OAV进行计算,将其中OAV最大的化合物的ROAV赋值100,以此按公式(2)计算其他化合物的ROAV,ROAV≥1的化合物被认为是关键香气化合物,而0.1≤ROAV<1的化合物则修饰了整体风味[27]。
ROAV的大小与其感觉阈值及样品中的相对含量密切相关。感觉阈值是相对气味活度值分析中的关键因素。同一个化合物的感觉阈值因其测定介质的不同而不同,笔者在查阅文献中发现,部分研究在空气中测定,却误用水中的感觉阈值,可能产生一定的误差。因此,本研究使用样品粉末直接顶空进样测定,不添加溶剂,因此以空气为介质,查找化合物在空气中的感觉阈值,以确保结果准确。在已获取阈值的10种化合物中,醛类、醇类、酚类及单萜烯类(γ-萜品烯除外)均为关键香气组分。其中,芳樟醇因阈值最低,其茴香、柑橘香与花香特征在陈皮中占据主导地位,成为各产地陈皮的核心香气成分[32]。而蒸制后陈皮中D-柠檬烯的相对含量占比最高,其柠檬香成为主导,同时月桂烯与γ-萜品烯含量的增加进一步强化了柑橘香调[31],赋予蒸陈皮更突出的青草香与淡雅脂香。
对比蒸制前后香气特征发现,陈皮以芳樟醇的复合花香和α-松油醇的薄荷香为主,兼具百里酚的药香、辛香[31];蒸制后则转向D-柠檬烯和月桂烯等单萜烯赋予的令人舒适的柑橘、柠檬果香。而癸醛、辛醛等醛类的青叶香、橙皮香与2-甲氧基-4-乙烯基苯酚的药香、辛香,其贡献度则与各产地样品中相应化合物的含量呈正相关。此外,倍半萜烯类虽具有木香、青香等柔和香气,但因缺乏公开的阈值数据,未能计算其ROAV,需进一步研究以明确其作用。该结果揭示了陈皮蒸制后香气变化的化学基础,为品质调控与蒸陈皮的应用提供了理论依据。
3 结论
本研究采用电子鼻与HS-SPME-GC-MS技术以及ROAV法分析了陈皮蒸制前后的香气特征变化。研究发现,陈皮与蒸陈皮的总体香气存在明显差异,顺式-β-古巴烯、芳樟醇等14种挥发性成分与蒸制所致的香气变化密切相关。陈皮中芳樟醇、α-松油醇、百里酚等醇、酚类含量较高,可呈现出花香、薄荷香和药香等较浓烈的香气;蒸制后,萜烯类成分含量升高,可赋予蒸陈皮令人舒适的柑橘香基调与较柔和的木质香。
蒸陈皮在岭南地区的疾病治疗、食疗保健等方面应用非常广泛,但深入研究较少。本研究借助快速、无损的电子鼻及HS-SPME-GC-MS等检测技术,对其香气特征进行分析阐释,可为蒸陈皮的快速质量评价方法的建立奠定基础,并可为其在功能食品、化妆品、香精香料等领域的应用开发提供参考依据。
[1] 国家药典委员会. 中华人民共和国药典:一部[M].2020年版.北京:中国医药科技出版社,2020:199-200.Chinese Pharmacopoeia Commission.Pharmacopoeia of the People's Republic of China:Part I[M].2020 edition.Beijing:China Medical Science Press;2020:199-200.
[2] ZHANG X W, JIANG Y N, ZENG J S, et al.Phytochemistry, pharmacological properties and pharmacokinetics of Citri Reticulatae Pericarpium:A systematic review[J].Journal of Ethnopharmacology, 2024, 333:118503.
[3] 陈晓旭,刘聪,王丽霞,等.基于电子眼技术和化学指纹图谱的陈皮与蒸陈皮质量差异分析[J].中国实验方剂学杂志,2023,29(10):202-208.CHEN X X, LIU C, WANG L X, et al.Quality difference analysis of raw and steamed products of Citri Reticulatae Pericarpium based on electronic eye technique and chemical fingerprint[J].Chinese Journal of Experimental Traditional Medical Formulae, 2023, 29(10):202-208.
[4] YU X, SUN S, GUO Y Y, et al.Citri Reticulatae Pericarpium (Chenpi):Botany, ethnopharmacology, phytochemistry, and pharmacology of a frequently used traditional Chinese medicine[J]. Journal of Ethnopharmacology, 2018, 220:265-282.
[5] 广东省卫生厅. 广东省中药炮制规范[M].广州:广东省卫生厅,1984:127-128.Guangdong Provincial Department of Health.Processing Specifications for Chinese Medicinal Materials in Guangdong Province[M].Guangzhou:Guangdong Provincial Department of Health;1984:127-128.
[6] 高明,徐小飞,陈康,等.陈皮炮制前后挥发性成分的比较研究[J].中药材,2012,35(7):1046-1048.GAO M, XU X F, CHEN K, et al.Study on the difference between components in volatile oil of Citrus reticulata before and after being processed[J].Journal of Chinese Medicinal Materials, 2012, 35(7):1046-1048.
[7] 熊海均.蒸陈皮的炮制工艺、质量标准及药效学研究[D].成都:成都中医药大学,2021.XIONG H J.Processing technology, quality standards, and pharmacological studies of steamed Citri Reticulatae Pericarpium[D].Chengdu:Chengdu University of Traditional Chinese Medicine, 2021.
[8] 刘聪.四制香附和蒸陈皮的质量评价研究[D].太原:山西医科大学,2021.LIU C.Quality evaluation studies on cyperi rhizoma praeparata and steamed Citri Reticulatae Pericarpium[D].Taiyuan:Shanxi Medical University, 2021.
[9] 方嘉雯,麦淑仪,孟江,等.基于近红外光谱的陈皮炮制品快速质量评价研究[J].广东药科大学学报,2023,39(1):79-87.FANG J W, MAI S Y, MENG J, et al.Study on the rapid quality evaluation of processed Citri Reticulatae Pericarpium based on near-infrared spectroscopy[J].Journal of Guangdong Pharmaceutical University, 2023, 39(1):79-87.
[10] CHEN S H, CHEN Z Y, O’NEILL ROTHENBERG D O, et al.Short-term steaming during processing impacts the quality of Citri Reticulatae ‘Chachi’ peel[J].Food Chemistry, 2024, 447:138964.
[11] XU Q J, LI Q R, YANG T, et al.Comprehensive quality evaluation of fermented‐steaming Fructus Aurantii based on chemical composition, flavor characteristics, and intestinal microbial community[J].Journal of Food Science, 2024, 89(5):2611-2628.
[12] 谢带琴,林羡,余元善,等.柑橘属水果加工制品中挥发性风味物质的无损检测技术研究进展[J].农产品加工,2025(5):99-108;114.XIE D Q, LIN X, YU Y S, et al.Research progress of non-destructive detection technology of volatile flavor substances in citrus fruits and their dried products[J].Agricultural Product Processing, 2025(5):99-108;114.
[13] 杜玲玲,孟晓伟,胡伊涵,等.不同陈化年份陈皮(樟头红)挥发成分差异的电子鼻与HS-GC-MS对比分析[J].食品科学, 2025, 46(11):253-262.DU L L, MENG X W, HU Y H, et al.Integration of electronic nose and headspace gas chromatography-mass spectrometry for differentiating the volatile compositions of citri reticulatae pericarpium made from Citrus reticulata Blanco var.zhany shuensis f.aged for different years[J].Food Science, 2025, 46(11):253-262.
[14] 刘主洁,林彤,侯惠婵,等.气相离子迁移谱与气相色谱区分广陈皮和陈皮的比较研究[J].药物分析杂志,2022,42(9):1554-1560.LIU Z J, LIN T, HOU H C, et al.Comparative investigation of citrus reticulate ‘Chachi’ and other Citrus reticulata Blanco varieties by HS-GC-IMS and HS-GC[J].Chinese Journal of Pharmaceutical Analysis, 2022, 42(9):1554-1560.
[15] 王金源,张佳慧,庄莉萍,等.HS-SPME-GC-TOF-MS结合ROAV分析花果香型红茶特征香气成分[J].天然产物研究与开发,2023,35(12):2015-2026.WANG J Y, ZHANG J H, ZHUANG L P, et al.Analysis of characteristic aroma compounds of black tea with flowery-fruity flavour by HS-SPME-GC-TOF-MS combined with ROAV[J].Natural Product Research and Development, 2023, 35(12):2015-2026.
[16] 商杰,彭嘉玉,郑郁清,等.基于电子鼻和HS-GC-MS技术结合相对气味活度值分析甘草不同炮制品气味差异及其物质基础[J].中国中药杂志,2024,49(19):5218-5228.SHANG J, PENG J Y, ZHENG Y Q, et al.Electronic nose, HS-GC-MS, and relative odor activity value reveal odor differences and material basis of Glycyrrhizae radix et Rhizoma products processed with different methods[J].China Journal of Chinese Materia Medica, 2024, 49(19):5218-5228.
[17] 郑郁清,彭嘉玉,郭静英,等.顶空气相色谱-质谱法结合相对气味活度值法分析谷糠、麦麸、蜜糠、蜜麸4种辅料的风味成分[J].中草药,2024,55(13):4361-4372.ZHENG Y Q, PENG J Y, GUO J Y, et al.HS-GC-MS combined with relative odor activity value method to analyze flavor components of four excipients:Chaff, bran, honey chaff and honey bran[J].Chinese Traditional and Herbal Drugs, 2024, 55(13):4361-4372.
[18] 刘登勇,周光宏,徐幸莲.确定食品关键风味化合物的一种新方法:“ROAV”法[J].食品科学,2008,29(7):370-374.LIU D Y, ZHOU G H, XU X L.“ROAV” method:A new method for determining key odor compounds of Rugao ham[J].Food Science, 2008, 29(7):370-374.
[19] ZHANG K Y, GAO L L, ZHANG C, et al.Analysis of volatile flavor compounds of corn under different treatments by GC-MS and GC-IMS[J].Frontiers in Chemistry, 2022, 10:725208.
[20] 田竹希,龙明秀,李咏富,等.玛瑙红樱桃果实不同发育阶段香气成分分析[J].食品工业科技,2022,43(7):333-342.TIAN Z X, LONG M X, LI Y F, et al.Study on aroma constituents of Manaohong cherry cultivar at different development stages[J].Science and Technology of Food Industry, 2022, 43(7):333-342.
[21] 杨洁慧,杜佳林,李静文,等.HS-GC-MS结合ROAV分析不同品种橘红花挥发性成分[J].中国现代中药,2024,26(4):616-624. YANG J H, DU J L, LI J W, et al.Detection of volatile components in Flos citri grandis from different plant varieties by HS-GC-MS combined with ROAV[J].Modern Chinese Medicine, 2024, 26(4):616-624.
[22] 于海燕,敖婷,廖晗雪,等.不同乳酸菌对发酵芸豆乳风味特征的影响[J].食品科学,2024,45(22):180-188.YU H Y, AO T, LIAO H X, et al.Effects of different lactic acid bacteria on flavor characteristics of fermented kidney bean milk[J].Food Science, 2024, 45(22):180-188.
[23] 潘奕丞,钱敏,赵培静,等.顶空固相微萃取-气相色谱-质谱法分析脐橙中挥发性成分[J].食品安全质量检测学报,2023,14(17):231-240.PAN Y C, QIAN M, ZHAO P J, et al.Analysis of volatile components in Citrus sinensis Osbeck by headspace solid phase microextraction coupled with gas chromatography-mass spectrometry[J].Journal of Food Safety &Quality, 2023, 14(17):231-240.
[24] 李丽,蒋景龙,胡佳乐,等.HS-SPME-GC-MS与ROAV相结合的4种柑橘果皮精油关键香气物质分析[J].现代食品科技,2024,40(5):221-230.LI L, JIANG J L, HU J L, et al.Analysis of key aroma compounds in essential oils from the fruit peels of four citrus varieties by HS-SPME-GC-MS combined with relative odor activity value[J].Modern Food Science and Technology, 2024, 40(5):221-230.
[25] 赵志强,陈罗君,饶雨,等.基于HS-SPME-GC-MS对不同等级双井绿茶香气物质的研究[J].食品工业科技,2024,45(10):273-281.ZHAO Z Q, CHEN L J, RAO Y, et al.Aroma compounds of different grades shuangjing green tea based on HS-SPME-GC-MS[J].Science and Technology of Food Industry, 2024, 45(10):273-281.
[26] 黄晨,曹慧颖,郭德军,等.基于气相色谱-质谱法和电子鼻技术分析不同烘烤度荔枝木对荔枝白兰地陈酿风味的影响[J].食品科学,2024,45(22):173-179.HUANG C, CAO H Y, GUO D J, et al.Effects of different toasting degrees of lychee wood on the flavor of lychee brandy analyzed by electronic nose and gas chromatography-mass spectrometry[J].Food Science, 2024, 45(22):173-179.
[27] 刘格格,毕金峰,苟敏,等.基于GC-MS及电子鼻技术结合化学计量法表征8种白桃关键香气的差异[J].食品科学,2023,44(18):277-285.LIU G G, BI J F, GOU M, et al.Gas chromatography and electronic nose combined with chemometrics to investigate differences in key aroma components in eight white-fleshed peach cultivars[J].Food Science, 2023, 44(18):277-285.
[28] 丘芷柔,陈彤,贺丽苹,等.固相微萃取优化/GC-MS法分析不同年份陈皮的挥发性成分[J].现代食品科技,2017,33(7):238-244.QIU Z R, CHEN T, HE L P, et al.Analysis of the volatile compounds in dried tangerine peel of different years by optimized solid phase micro-extraction/gas chromatography-mass spectrometry[J].Modern Food Science and Technology, 2017, 33(7):238-244.
[29] 高婷婷,杨绍祥,刘玉平,等.陈皮挥发性成分的提取与分析[J].食品科学,2014,35(16):114-119.GAO T T, YANG S X, LIU Y P, et al.Extraction and analysis of volatile components of tangerine peel[J].Food Science, 2014, 35(16):114-119.
[30] 李俊健,林锦铭,高杰贤,等.陈皮挥发油提取、成分分析及应用的研究进展[J].中国调味品,2021,46(8):169-173.LI J J, LIN J M, GAO J X, et al.Research progress on extraction, composition analysis and application of essential oils from Citrus reticulata Blanco[J].China Condiment, 2021, 46(8):169-173.
[31] 陈霖虹,肖更生,徐玉娟,等.不同贮藏方式陈皮精油成分及其抗氧化活性分析[J].食品与发酵工业,2025,51(3):215-224. CHEN L H, XIAO G S, XU Y J, et al.Analysis of essential oil composition and antioxidant activity of Pericarpium Citri Reticulatae in different storage methods[J].Food and Fermentation Industries, 2025, 51(3):215-224.
[32] 王雪,潘兆平,陈嘉序,等.湖南省16种柑橘陈皮加工适宜性分析[J].中国食品学报,2024,24(10):355-370.WANG X, PAN Z P, CHEN J X, et al.Suitability analysis of 16 citrus varieties for processing Pericarpium Citri Reticulatae in Hunan Province[J].Journal of Chinese Institute of Food Science and Technology, 2024, 24(10):355-370.
[33] 里奥·范海默特.化合物香味阈值汇编[M].北京:科学出版社, 2015.LIAO FHMT.Compilations of Flavour Threshold Values in Water and Other Media [M].Beijing:Science Press, 2015.