L-丝氨酸是一种重要的非必需氨基酸,具有重要的生理功能,参与体内蛋白质、脂肪和磷脂的合成与代谢过程,在食品、化妆品和医药领域具有广泛的应用[1]。L-丝氨酸是构成蛋白质的基本氨基酸之一,是甘氨酸和半胱氨酸等氨基酸合成的关键前体物质,为蛋白质的形成提供必要的成分[2]。L-丝氨酸在脂肪和脂肪酸的新陈代谢中扮演着关键角色,影响脂肪的分解和利用,维持体内脂肪代谢的平衡[3]。L-丝氨酸还参与体内细胞膜磷脂、鞘磷脂、糖脂等生物分子的合成,调控细胞膜的制造与加工,以及肌肉组织和神经细胞鞘的合成,在细胞增殖和分化过程中发挥重要作用[3]。此外,作为细胞内重要的C1单位供体,L-丝氨酸在多种生化反应中发挥重要作用,参与了嘌呤、嘧啶等多种腺苷类、核苷酸类化合物的生物合成[4-5]。研究表明,L-丝氨酸还参与体内多种生理活动,包括调节中枢神经系统发育,控制细胞增殖,促进免疫细胞的生长和功能等,在生物体内发挥重要的生理功能,是维持生物体正常生理活动不可或缺的重要氨基酸之一[3,5-6]。鉴于L-丝氨酸重要的生理作用,L-丝氨酸及其衍生物在医药领域应用广泛。L-丝氨酸是第三代氨基酸输液剂的成分之一,可以缓解大脑损伤,提高大脑机能,其衍生物磷脂酰丝氨酸可延长神经递质活力,治疗老年痴呆和记忆受损等症状[7]。此外,L-丝氨酸被开发作为营养补充剂和食品添加剂,增加食品风味和提高营养水平。L-丝氨酸具有较高的保湿性,还被应用于多种高级化妆品中,维持皮肤角质层的水分[8]。近年来,随着对L-丝氨酸生理功能研究的不断深入,多种下游应用产品持续开发,L-丝氨酸需求量不断增大,市场规模持续提升。
目前,L-丝氨酸主要通过蛋白水解法、化学合成法以及酶催化法进行生产[1,8-9]。然而上述方法存在生产成本高、产物转化率低以及环境污染等问题,严重限制了L-丝氨酸的生产规模和市场应用。相比之下,微生物发酵法具有环境友好,底物可再生,生产周期短以及过程条件温和等优势,是生产L-丝氨酸的理想方法[10-11]。近年来,研究人员在改造微生物发酵生产L-丝氨酸方面开展了大量的研究工作,随着合成生物学的发展,多种微生物代谢工程技术被应用于L-丝氨酸工程菌种的选育和改造过程中,以获得最优的生产菌种[1-2]。在此过程中需要对大量的菌种进行评估,存在大量的L-丝氨酸分析和检测工作。目前常用的L-丝氨酸检测方法主要有化学检测法(包括变色酸-分光光度法、纸层析-分光光度法、茚三酮显色法等)和高效液相色谱法[12]。然而化学检测法通常存在灵敏度差、准确度低、步骤繁琐等问题,尤其是在发酵液中组分复杂的情况下高效检测L-丝氨酸较为困难,而高效液相色谱法(HPLC)存在检测时间长、效率低等问题,对于样品多、工作量大的L-丝氨酸生产菌的高通量筛选并不适用。基于上述问题,本研究建立了一种基于酶催化的L-丝氨酸快速检测方法,通过酶特异性催化将L-丝氨酸浓度与NADPH生产速率关联,实现L-丝氨酸的高效快速检测。该方法具有检测速度快、特异性强、检测通量高等优点,为L-丝氨酸工程菌种的高通量筛选和评估提供了重要的工具方法。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株和质粒
大肠杆菌(Escherichia coli)DH5α由本实验室保藏,用于本实验中质粒构建。E.coli BL21(DE3)用于蛋白表达。大肠杆菌表达质粒pET21b由本实验室保藏,主要用于目的蛋白的表达与纯化。
1.1.2 试剂
L-丝氨酸(L-ser)、甘氨酸、苏氨酸、半胱氨酸、丙氨酸、缬氨酸、天冬氨酸、谷氨酸、赖氨酸、精氨酸、组氨酸、苯丙氨酸、亮氨酸、异亮氨酸、蛋氨酸、酪氨酸、色氨酸、脯氨酸等氨基酸,北京索莱宝生物科技有限公司。烟酰胺腺嘌呤二核苷酸(NAD+)、烟酰胺腺嘌呤二核苷酸磷酸(NADP+),上海源叶生物试剂有限公司。
1.1.3 培养基和溶液
LB培养基(g/L):酵母粉5.0,胰蛋白胨10.0,NaCl 10.0;细胞裂解缓冲液:20 mmol/L Na2HPO4,200 mmol/L NaCl,pH 7.5;洗杂缓冲液:20 mmol/L Na2HPO4,200 mmol/L NaCl,20 mmol/L咪唑,pH 7.5;洗脱缓冲液:20 mmol/L Na2HPO4,200 mmol/L NaCl,500 mmol/L咪唑,pH 7.5;蛋白保存缓冲液:20 mmol/L Na2HPO4溶液,50 g/L甘油,pH 7.5。
1.2 仪器与设备
SX-700 高压灭菌锅,天美(中国)科学仪器有限公司;TC-XP-D 基因扩增仪,赛默飞世尔科技公司;HPX-9082MBE 恒温培养箱,上海一恒科学仪器有限公司;H2O3-100C 加热制冷型金属浴,卡尤迪生物科技有限公司;JY-SCZ2+ 蛋白电泳仪,北京君意东方电泳设备;5810R 台式冷冻离心机,德国Eppendorf公司;DK-8D 水浴锅,上海一恒仪器;Scientz-IID 超声破碎仪,宁波新芝公司;Synergy neo2 SMHTS 多功能酶标仪,美国伯腾仪器有限公司;Agilent 1260 高效液相色谱仪,美国Agilent公司;ME204 天平,Mettler Toledo;Mettler Toledo 高速振荡培养摇床,江苏新春兰科学仪器有限公司。
1.3 实验方法
1.3.1 质粒构建
来源于铜绿假单胞菌(Pseudomonas aeruginosa)和蚕豆农杆菌(Agrobacterium fabrum)的丝氨酸脱氢酶(L-serine dehydrogenase,SerDH)编码基因(UniProt:Q9I5I6和Q8U8I2)由金斯瑞生物科技公司合成。使用Thermo Scientific® Phusion超保真DNA聚合酶,以合成基因为模板,分别使用引物对Afsdh-F:TATACATATGAGCGGCACCATTCTGATTAC/Afsdh-R:GTGC-TCGAGGCTTTCGCGATACACTTGAAAGC,和Pasdh-F:CATATGAAACAGATTGCGTTTATTG/Pasdh-R:CTCGAG-CTGACCTTGGGTCGGATCAAAC,通过PCR获得AFSerDH和PASerDH的基因片段。然后利用限制性内切酶Nde Ⅰ和Xho Ⅰ将目的基因片段连接至pET21b上,转化至E.coli DH5α感受态细胞中,在含有100 μg/mL氨苄青霉素的LB平板上培养。通过菌落PCR方法验证,将构建正确的质粒转化至E.coli BL21感受态细胞中,分别获得重组菌E.coli BL21-AFSerDH和E.coli BL21-PASerDH。
1.3.2 蛋白表达和纯化
从-80 ℃冰箱冻存甘油管中取菌液,接种于含有100 μg/mL氨苄青霉素的LB液体培养基中,37 ℃过夜培养。将过夜培养的重组菌按照1%(体积分数)的接种量转接至LB液体培养基中,在37 ℃、200 r/min条件下培养,当菌液OD600值达到0.6~0.8后,加入终浓度0.4 mmol/L IPTG,16 ℃、200 r/min条件下继续培养20 h。随后在4 ℃、6 000 r/min条件下离心收集菌体,使用裂解缓冲液重悬菌体后,超声处理20 min,离心收集上清液为粗酶液。
本研究采用镍柱亲和层析法对目标蛋白进行纯化。将收集的上清液上样到Ni-NTA亲和层析柱中,使用洗杂缓冲液洗出杂蛋白后,使用洗脱缓冲液洗脱含有HIS标签的目标蛋白,使用Milipore Amicon Ultra 15超滤管对目标蛋白浓缩后,贮存在保存缓冲液中,分装后存于-80 ℃冰箱中。对获得的粗蛋白和纯化蛋白使用SDS-PAGE进行检测分析。
1.3.3 L-丝氨酸-3-脱氢酶活性测定
L-丝氨酸在L-丝氨酸-3-脱氢酶的作用下偶联NAD(P)+氧化生成NAD(P)H。因此本研究以反应过程中NADPH的生成速率来检测L-丝氨酸-3-脱氢酶的活性。酶催化反应体系为50 mmol/L Tris-HCl(pH=8.0),10 mmol/L L-丝氨酸,1 mmol/L NAD(P)+,0.5 μg酶,反应体系为200 μL,37 ℃下孵育20 min,在酶标仪下测定340 nm处的吸光度变化值。酶活性单位定义:每分钟催化生成1 μmol/L NADPH所需的酶量为1个酶活性单位(1 U)。在此条件下,分别对AFSerDH的最适温度、最适pH和动力学常数进行了测定。
1.3.4 AFSerDH催化底物特异性测定
将丝氨酸、甘氨酸、苏氨酸、半胱氨酸、丙氨酸、缬氨酸、亮氨酸、异亮氨酸、天冬氨酸、天冬酰胺、谷氨酰胺、谷氨酸、赖氨酸、精氨酸、组氨酸、蛋氨酸、酪氨酸、色氨酸、苯丙氨酸、脯氨酸等20种氨基酸配制成浓度为10 mmol/L的溶液。利用AFSerDH分别对上述20种氨基酸进行酶催化测试分析,反应体系为:50 mmol/L碳酸钠-碳酸氢钠(pH=9.5),2 mmol/L NADP+,10 mmol/L L-丝氨酸,AFSerDH纯化酶。在40 ℃条件下反应20 min,利用酶标仪测定340 nm处吸光度的变化。为验证AFSerDH对L-丝氨酸催化的特异性,本研究将上述20种氨基酸进行等量混合,比较分析AFSerDH对混合溶液和L-丝氨酸标准液的酶活性。
1.3.5 标准曲线制定和加标回收实验
配制终浓度为2、4、6、8、10 mmol/L的L-丝氨酸标准液,按照优化的L-丝氨酸反应条件,测定不同浓度L-丝氨酸标准液在340 nm处吸光度的变化值,以不加L-丝氨酸的反应体系为对照组。随后以L-丝氨酸浓度为横坐标,以340 nm处吸光度的变化值为纵坐标,绘制回归曲线。
取L-丝氨酸发酵液,利用HPLC法和酶法分别测定其中L-丝氨酸的含量。向发酵液中加入不同浓度的L-丝氨酸,随后利用酶法测定混合液中L-丝氨酸的含量,比较分析对照样本和回归样本中L-丝氨酸的含量。
1.3.6 HPLC测定L-丝氨酸含量
本研究采用通用氨基酸检测方法分析L-丝氨酸的含量[13]。HPLC检测系统为Agilent 1260,色谱柱为Agilent ZORBAX Eclipse AAA色谱柱(4.6 mm×150 mm,5 μm)。流动相为A相:40 mmol/L磷酸二氢钠溶液(pH=7.8),B相:V(乙腈)∶V(甲醇)∶V(水)=45∶45∶10。流速:2.0 mL/min;检测波长:338 nm;柱温:40 ℃。
2 结果与分析
2.1 基于酶催化的L-丝氨酸检测方法的设计
L-丝氨酸脱氢酶催化L-丝氨酸脱氢反应,过程中涉及辅因子NAD(P)+的氧化生成NAD(P)H。因此,L-丝氨酸脱氢酶催化反应能够将L-丝氨酸浓度与NAD(P)H的生成偶联起来,NAD(P)H的生成速率与L-丝氨酸浓度呈正比[13-14]。基于上述原理,通过在340 nm吸光度条件下测定NAD(P)H的生成速率,能够直接测定L-丝氨酸的浓度。目前,存在2种类型的L-丝氨酸脱氢酶,包括L-丝氨酸-2-脱氢酶(EC 1.4.1.7)和L-丝氨酸-3-脱氢酶(EC 1.1.1.276)。其中L-丝氨酸-2-脱氢酶催化L-丝氨酸C2位氨基氧化生成羟基丙酮酸,而L-丝氨酸-3-脱氢酶催化C3位置羟基的脱氢反应生产2-氨基丙二酸半醛,随后自发分解成2-氨基乙醛和CO2[15]。需要注意的是,L-丝氨酸-2-脱氢酶催化C2位氧化脱氨反应的吉布斯自由能为ΔG=(20.6±1.7) kJ/mol,L-丝氨酸-3-脱氢酶催化C3位脱氢反应的吉布斯自由能ΔG=(-19.2±6.9) kJ/mol。相比之下,L-丝氨酸-3-脱氢酶反应具有热力学优势,对L-丝氨酸检测过程十分有利。因此,本研究选择L-丝氨酸-3-脱氢酶作为催化酶设计开发L-丝氨酸高效检测方法。L-丝氨酸-3-脱氢酶反应方程如公式(1)所示:
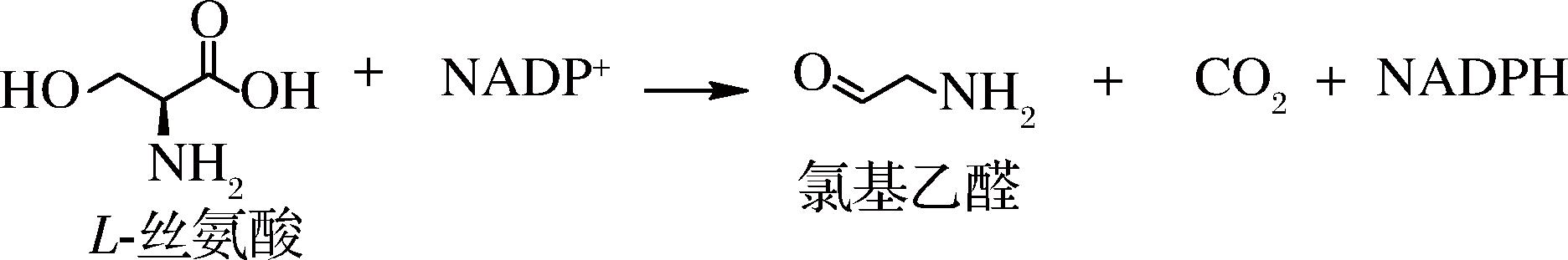
(1)
2.2 L-丝氨酸-3-脱氢酶的筛选与表征
基于对L-丝氨酸-3-脱氢酶催化反应分析,本研究从BRENDA数据库中选择了2个具有较高活性的L-丝氨酸-3-脱氢酶,分别为来源于P.aeruginosa的L-丝氨酸-3-脱氢酶基因Pasdh(UniProt:Q9I5I6,编码基因为:PA0743,annotated as sdh)和来源于A. fabrum的L-丝氨酸-3-脱氢酶Afsdh(UniProt:Q8U8I2,编码基因为:sdh)[14-15]。为鉴定和筛选最优的L-丝氨酸-3-脱氢酶候选蛋白,本研究对2个酶分别进行蛋白表达纯化和酶活测定。
将上述基因按照大肠杆菌密码子偏好性进行密码子优化。将目的基因Pasdh和Afsdh分别连接至pET21b表达载体上,并且在C端添加His标签用于后期纯化,构建表达载体pET21b-Pasdh和pET21b-Afsdh。将构建的质粒分别转入E.coli BL21(DE3)中,构建重组菌株BL21-AFSerDH和BL21-PASerDH,为鉴定和筛选最优的L-丝氨酸-3-脱氢酶候选蛋白,本研究对2个酶分别进行蛋白表达纯化和酶活测定。分别对AFSerDH和PASerDH进行表达纯化。SDS-PAGE分析(图1)显示,PASerDH的蛋白分子质量约为31 kDa,AFSerDH的蛋白分子质量为27 kDa,与预期结果基本一致。而且SDS-PAGE表明,PASerDH和AFSerDH均具有良好的蛋白表达水平,其中AFSerDH比PASerDH具有更多的蛋白表达量,更适用于大规模蛋白表达和生产。
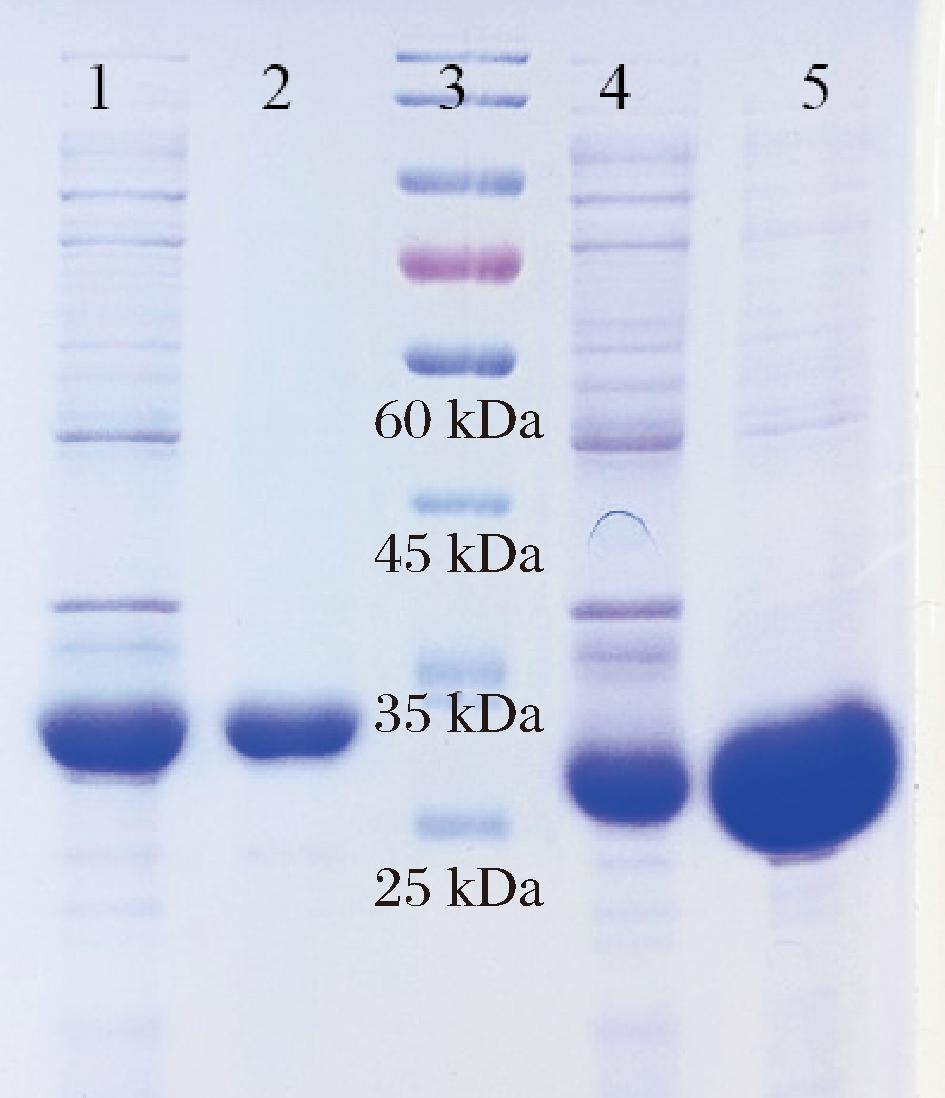
泳道1-PASerDH破碎上清液;泳道2-PASerDH纯化酶; 泳道3- Protein ladder marker;泳道4-AFSerDH破碎上清液; 泳道5-AFSerDH纯化酶。
图1 SDS-PAGE检测分析
Fig.1 SDS-PAGE analysis
随后本研究对PASerDH和AFSerDH的酶催化特性进行了研究,比较分析了2个酶分别以NAD+和NADP+为辅因子条件下的催化活性。酶催化体系为:
50 mmol/L Tris-HCl(pH=8.5),2 mmol/L NAD(P)+,0.5 μg纯化酶,10 mmol/L L-丝氨酸,37 ℃条件下孵育20 min后,在340 nm波长下检测吸光度的变化。结果如图2所示,PASerDH对辅因子NAD+比NADP+具有更高偏好性,在2 mmol/L NAD+条件下其活性达到1.49 U/mg,而在NADP+条件下其活性仅为0.21 U/mg。有趣的是,AFSerDH呈现出与PASerDH完全相反的辅因子偏好性,AFSerDH在2 mmol/L NADP+条件下其活性达到6.93 U/mg,而在NAD+条件下则无活性,说明AFSerDH对辅因子NADP+的偏好性较为严谨。随后本研究通过序列比对分析发现,PASerDH和AFSerDH具有较低的序列相似性,而且PASerDH表现出NAD(P)+辅因子保守性结合位点(GXGXXG)(图3),而AFSerDH则未找出相应的结合位点,其催化机制需进一步探究。需要注意的是,AFSerDH的酶活性是PASerDH酶活性的4.65倍,表现出更高L-丝氨酸的催化效率,是开发L-丝氨酸检测方法的理想候选酶。因此,本研究选择AFSerDH进行下一步研究。
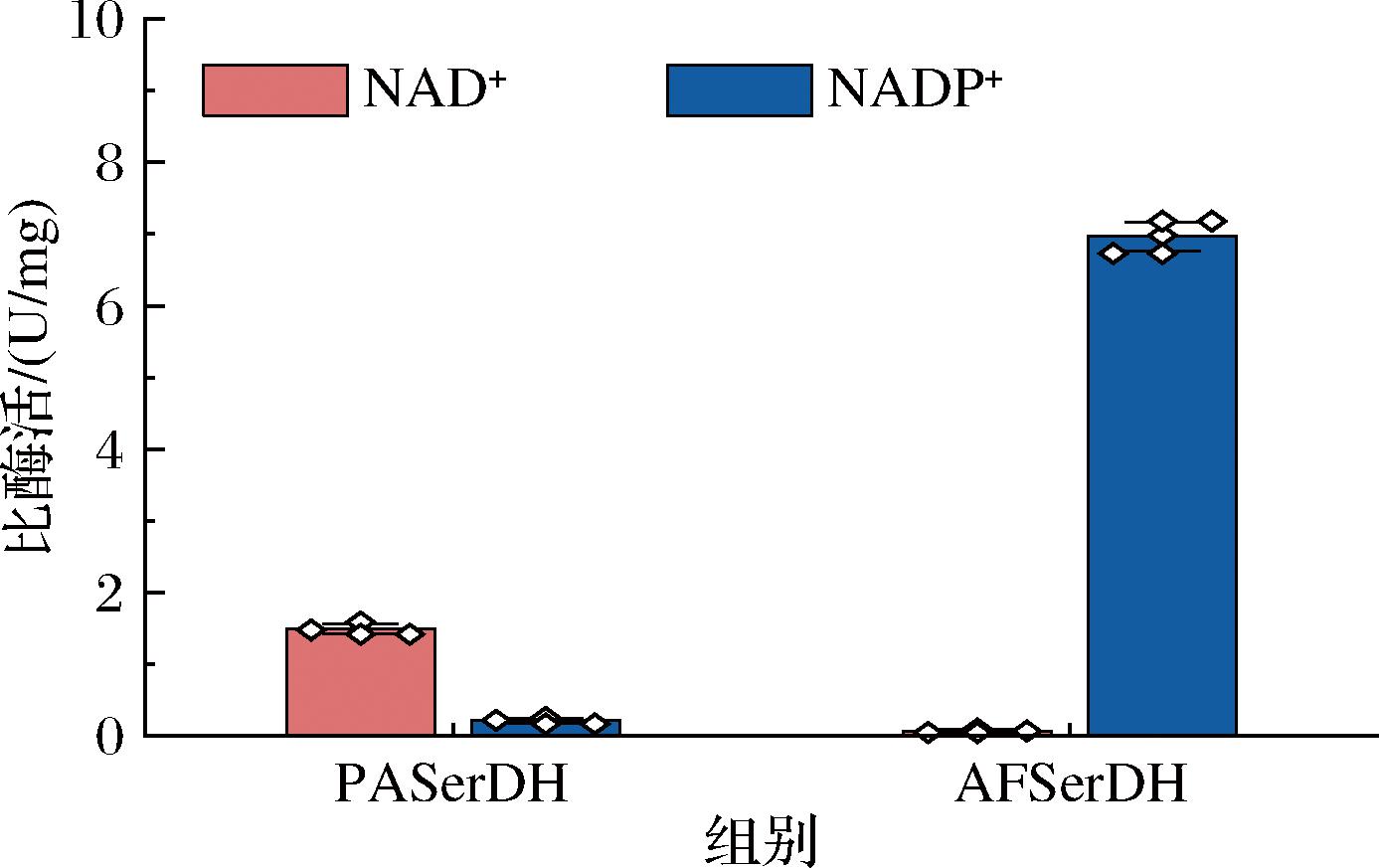
图2 不同L-丝氨酸-3-脱氢酶催化特性的比较分析
Fig.2 Comparative analysis of catalytic properties of different L-serine-3-dehydrogenases
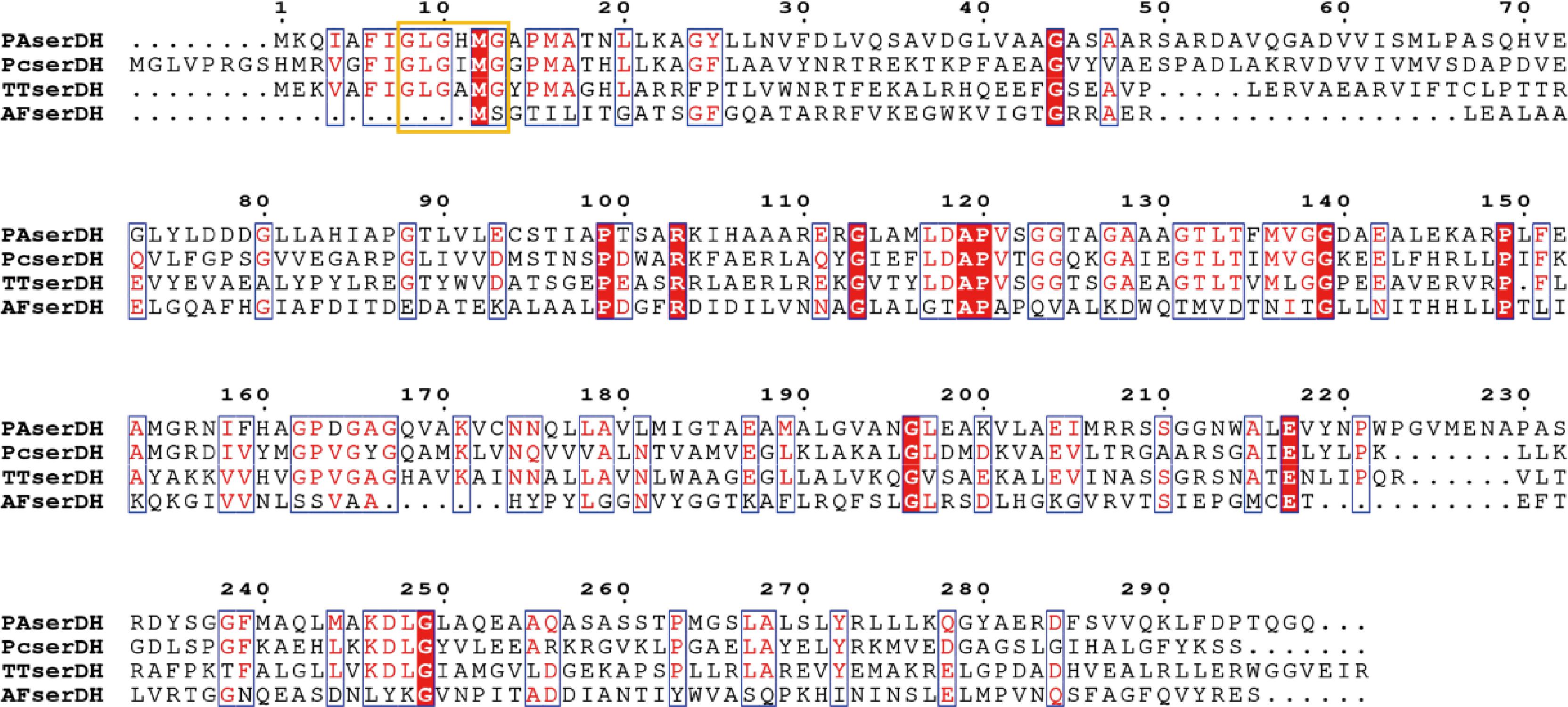
图3 L-丝氨酸-3-脱氢酶序列比对分析
Fig.3 Sequence alignment of L-serine-3-dehydrogenase
注:PcserDH来源于Pyrobaculum calidifontis;TTSerDH来源于Thermus thermophilus。黄色框线代表辅因子结合位点。
2.3 AFSerDH酶学性质测定
2.3.1 AFSerDH最适pH研究
为进一步探究AFSerDH的催化特性,本研究研究了pH、温度和金属离子对AFSerDH催化活性的影响。在2 mmol/L NADP+,10 mmol/L L-丝氨酸条件下,分别测定AFSerDH在不同pH(6.5、7、7.5、8、8.5、9、9.5、10、10.5、11)条件下的酶活性。选择不同pH缓冲体系的缓冲液,在pH=6.5~8时,使用50 mmol/L的3-吗啉丙磺酸(3-morpholine propanesulfonic acid,3-MOPS)进行测定;在pH=8~9.5时,使用50 mmol/L的三羟甲基氨基甲烷盐酸盐(Tris-HCl);在pH=9.5~10.5时,使用50 mmol/L的碳酸钠-碳酸氢钠溶液进行测定。结果如图4-A所示,AFSerDH在酸性和中性pH条件下具有较低的催化活性,随着pH的升高,其催化活性逐渐升高,在pH=9.5条件下,其酶活性达到最高9.8 U/mg。但是随后pH继续升高,其酶活性急剧下降。结果表明,AFSerDH在pH值为9.5条件下表现出最适的催化活性。
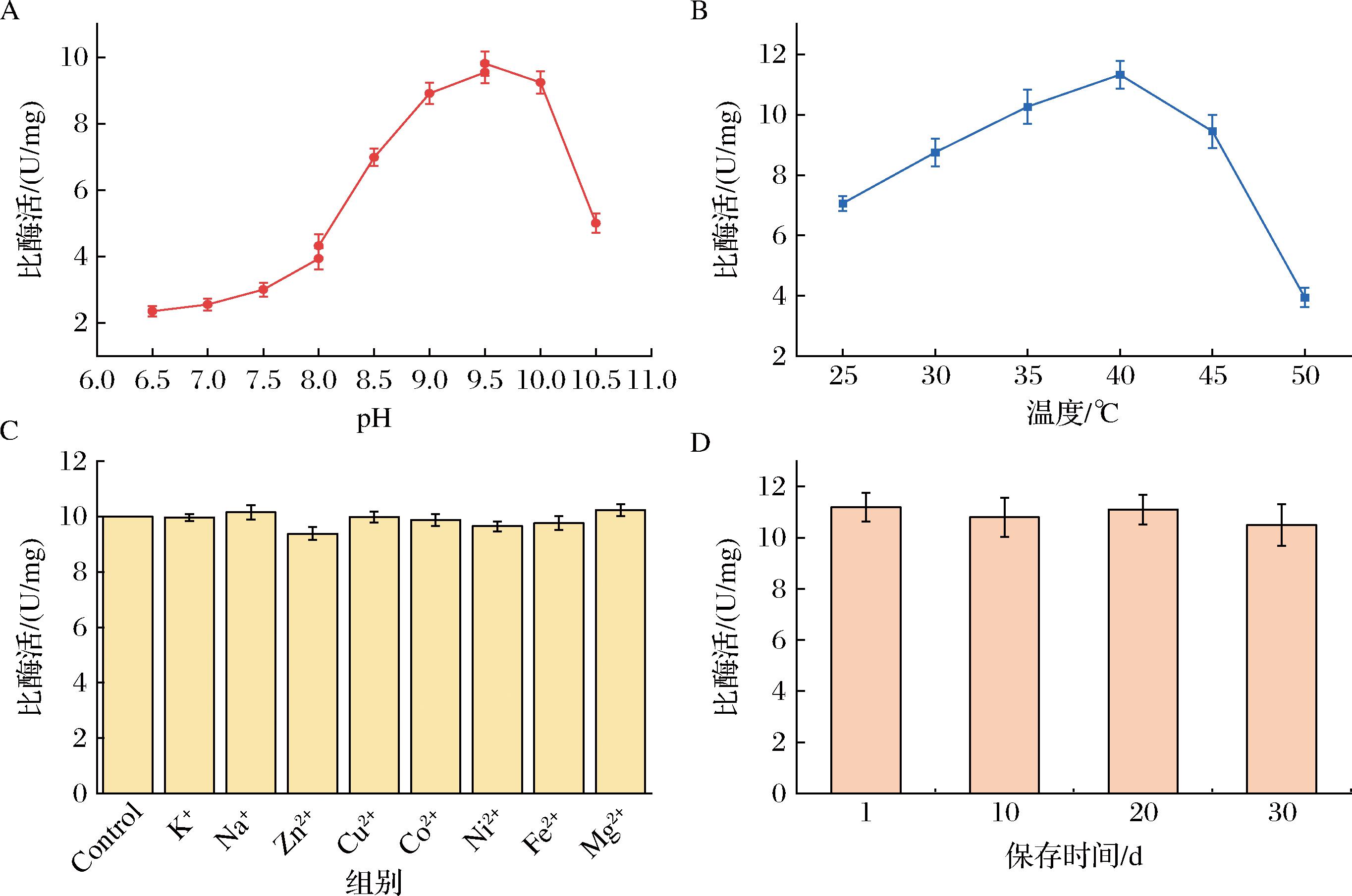
A-pH对AFSerDH酶活性的影响;B-温度对AFSerDH酶活性的影响;C-金属离子对AFSerDH酶活性的影响;D-保存时间对AFSerDH酶活性的影响
图4 AFSerDH酶学性质测定
Fig.4 Enzymatic characterization of AFSerDH
2.3.2 AFSerDH最适温度研究
随后本研究进一步探究了温度对AFSerDH催化活性的影响。在pH 9.5最适条件下,分别测定了AFSerDH在不同温度25、30、35、37、40、45 ℃条件下酶活性。结果如图4-B所示,重组酶AFSerDH在25~40 ℃条件下,酶活性随着温度的升高逐渐提高,在40 ℃条件下酶活性达到最高为11.3 U/mg,随后随着温度的进一步提高,其活性急剧下降。由于L-丝氨酸检测体系需要较高的酶催化活性,因此确定催化体系的最适条件参数为pH 9.5和40 ℃。
2.3.3 金属离子对AFSerDH酶活性的影响
在发酵液中通常存在大量的微量金属离子,因此本研究探究了不同金属离子对AFSerDH催化活性的影响。结果表明,在存在1 mmol/L常见金属离子K+、Na+、Zn2+、Cu2+、Co2+、Ni2+、Fe2+、Mg2+条件下,AFSerDH的酶活性几乎不受影响,仍能保持较高的催化活性(图4-C)。结果说明AFSerDH能够有效拮抗金属离子的影响,适用于分析复杂发酵液环境中L-丝氨酸的含量。
2.3.4 保存时间对AFSerDH酶活性的影响
除了酶活性外,酶的稳定性也是影响检测体系的重要因素。因此本研究探究了保存时间对AFSerDH酶活性的影响。将纯化后的AFSerDH保存于-80 ℃ 冰箱中,分别将保存时间为1、10、20、30 d的酶进行活性测定。结果表明保存1、10、20、30 d的比酶活为11.2、10.8、11.1、10.5 U/mg(图4-D)。结果表明AFSerDH具有良好的稳定性,在-80 ℃条件下保存30 d后仍能保持较高的催化活性,能够实现L-丝氨酸样品的长时间连续检测。
2.3.5 AFSerDH酶动力学常数测定
本研究对AFSerDH的动力学常数进行了分析测试。在最适pH和最适催化温度条件下(pH 9.5,40 ℃),分别测定了AFSerDH在不同底物L-丝氨酸浓度(0~400 mmol/L)和不同辅因子NADP+浓度条件的酶活性,计算AFSerDH对底物L-丝氨酸和NADP+的Km和Vmax。结果如图5所示,在过量辅因子NADP+浓度条件下,AFSerDH对底物L-丝氨酸的Km为11.57 mmol,Vmax为14.99 U/mg,kcat为565.6 min-1,而在过量底物L-丝氨酸条件下,AFSerDH对NADP+的Km为0.99 mmol,Vmax为15.91 U/mg,kcat为558.7 min-1。
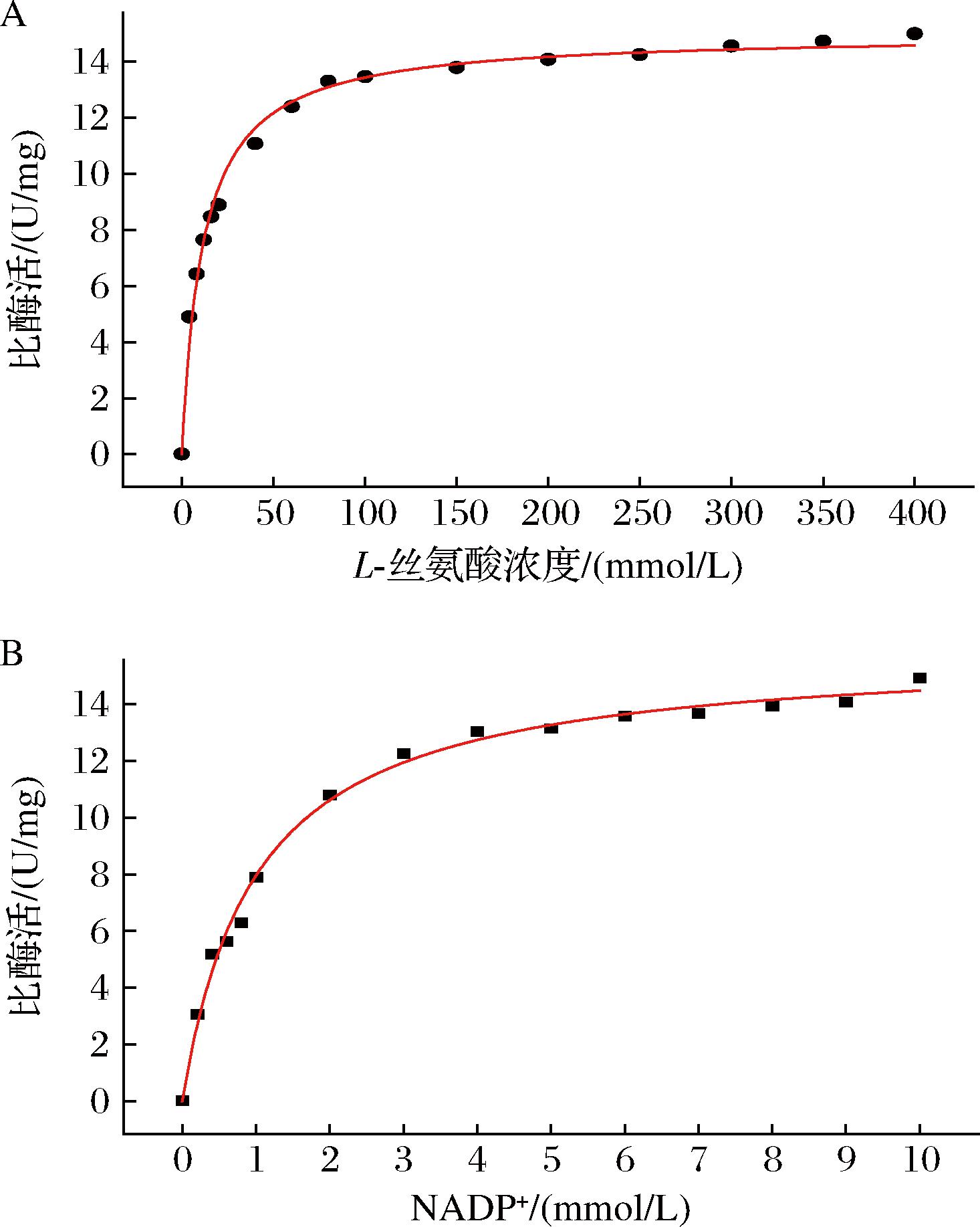
A-AFSerDH对L-丝氨酸的催化动力学常数测定; B-AFSerDH对NADP+的催化动力学常数测定
图5 AFSerDH对不同底物的酶动力学常数测定
Fig.5 Determination of kinetic constants of AFSerDH toward different substrates
2.3.6 AFSerDH催化底物特异性分析
底物特异性是影响检测方法开发与应用的关键指标。因此,本研究对AFSerDH催化底物特异性进行了分析,检测AFSerDH对20种氨基酸底物的催化活性。结果如图6-A所示,AFSerDH在20种氨基酸底物测试中,仅对L-丝氨酸表现出较高的酶活性,而对其他氨基酸均未表现出活性。结果表明AFSerDH对底物L-丝氨酸具有十分严谨的选择性。为进一步探究L-丝氨酸的催化反应是否受到其他氨基酸的影响,本研究在10 mmol/L的L-丝氨酸溶液中加入等量的20种氨基酸,检测AFSerDH对混合氨基酸的催化活性,以等浓度的L-丝氨酸标准液为对照,检测10 min内340 nm处吸光度的变化情况。结果如图6-B所示,混合氨基酸溶液底物在340 nm处的吸光度升高值与对照组基本一致,说明AFSerDH催化反应具有良好的特异性和稳定性,不受到其他氨基酸的干扰,能够满足复杂环境中L-丝氨酸的高效检测。
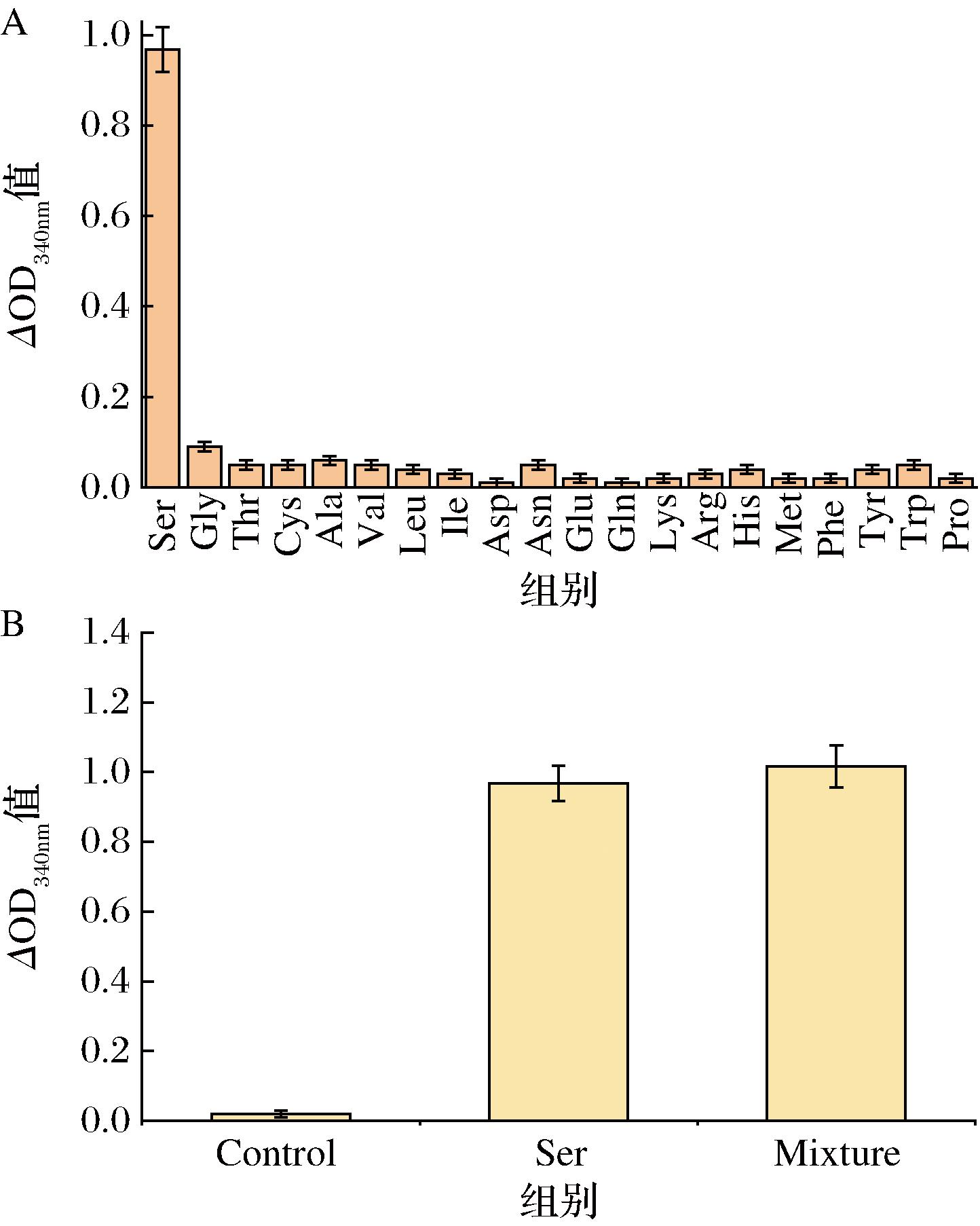
A-AFSerDH对不同氨基酸的催化活性;B-AFSerDH对 氨基酸混合液的催化活性
图6 AFSerDH催化底物特异性分析
Fig.6 Substrate specificity analysis of AFSerDH
2.4 基于酶催化的L-丝氨酸检测方法的建立和优化
2.4.1 AFSerDH酶浓度优化
AFSerDH酶量是影响反应速率的关键因素。在L-丝氨酸检测体系中,AFSerDH需要保持过量水平,以保证L-丝氨酸浓度与酶活性的相关性。因此本研究对L-丝氨酸反应体系中AFSerDH的酶浓度进行了测试优化。酶催化体系为:50 mmol/L碳酸钠-碳酸氢钠(pH值=9.5),1 mmol/L NADP+,10 mmol/L L-丝氨酸,AFSerDH纯化酶。在40 ℃条件下反应20 min,测定340 nm处吸光度的变化。结果如图7所示,在0.5~2 U/mL时,反应速率随着酶量的增加而增大,当酶量达到2 U/mL时,反应速率达到最大。同时再增加酶量,反应速率不再增加。因此确定在10 mmol/L L-丝氨酸条件下,AFSerDH的浓度为2 U/mL。
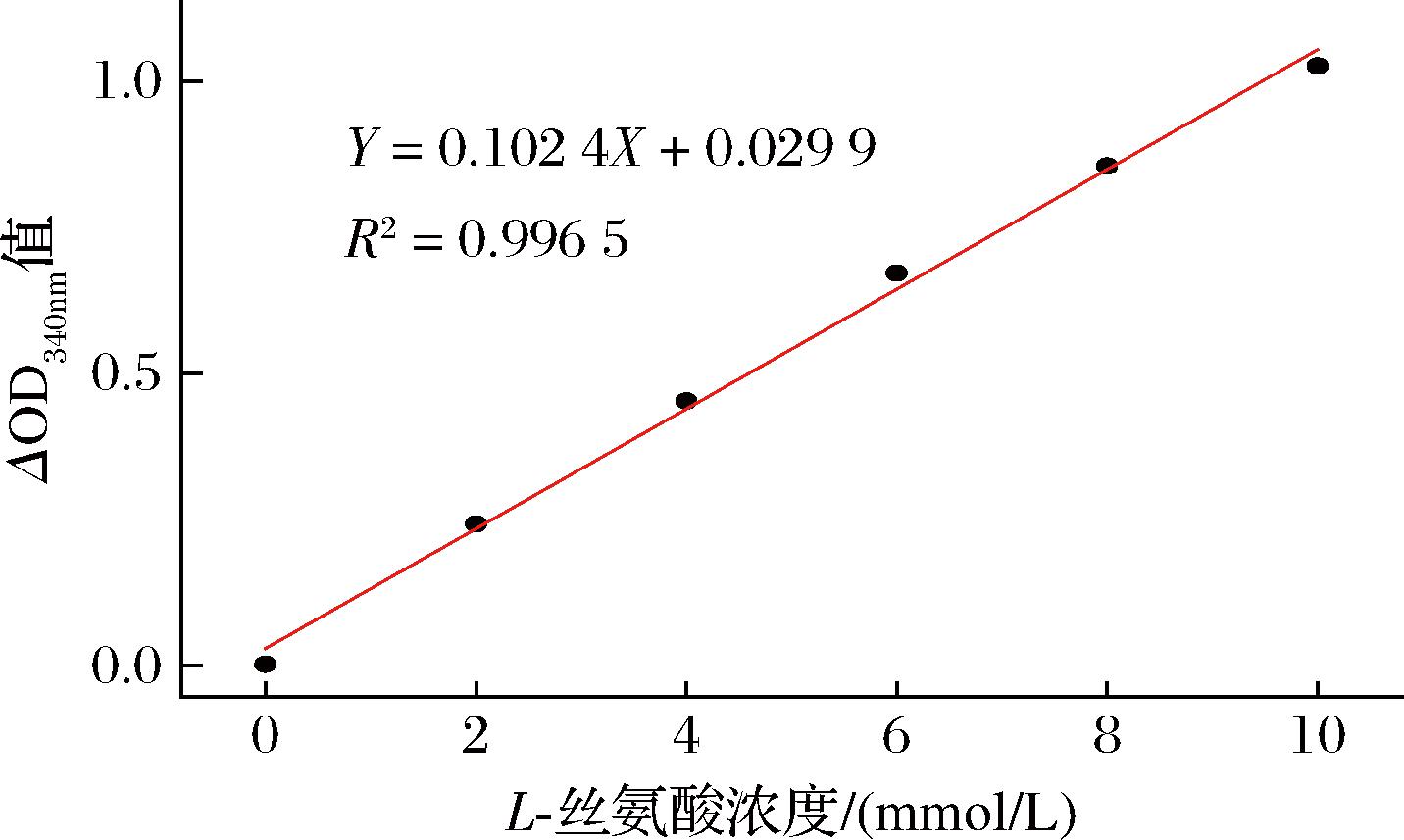
图7 L-丝氨酸检测标准曲线
Fig.7 L-serine detection standard curve
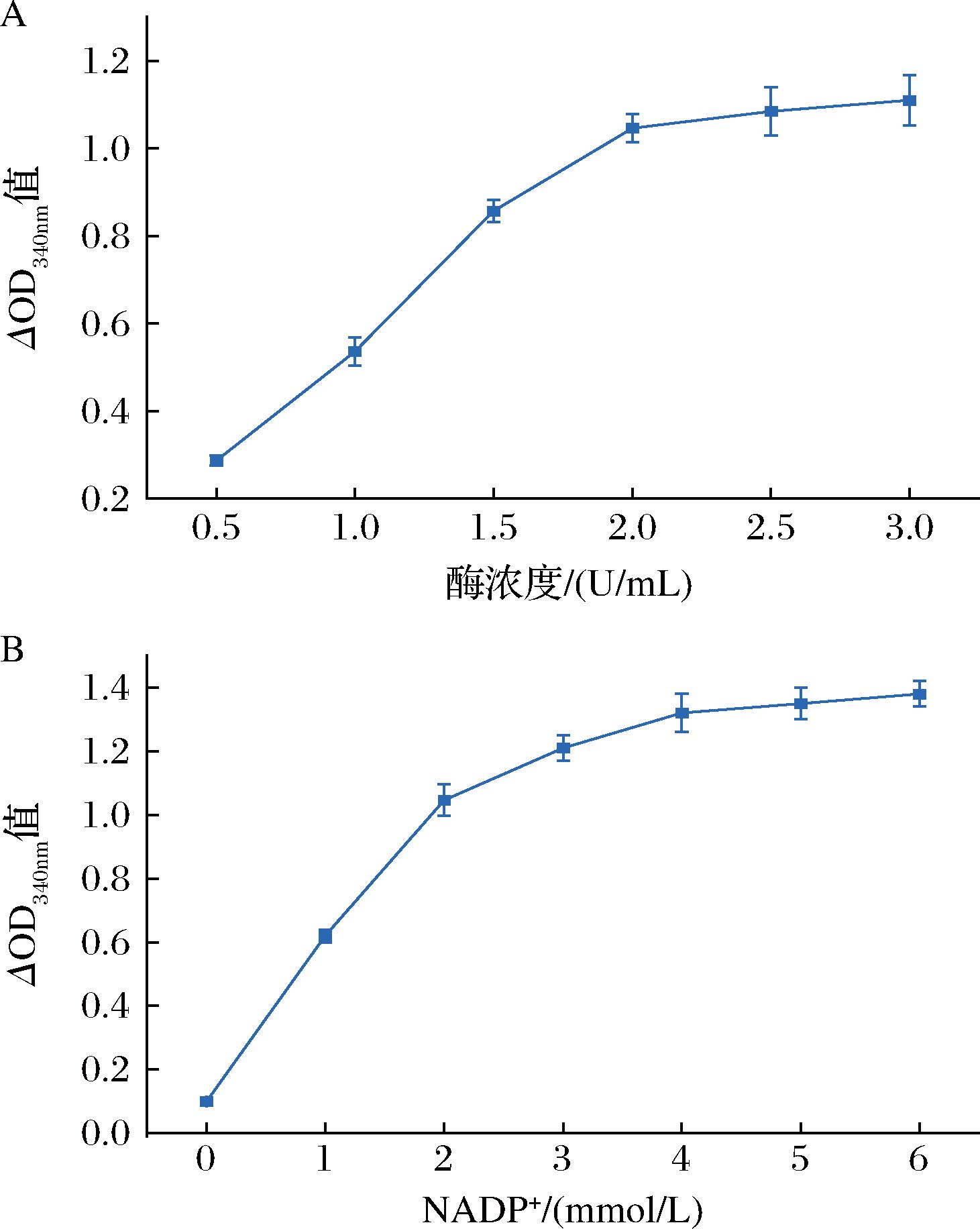
A-AFSerDH酶浓度优化;B-NADP+浓度优化
图7 基于酶催化的L-丝氨酸检测方法的建立和优化
Fig.7 Establishment and optimization of an enzyme-catalyzed detection method for L-serine
2.4.2 NADP+浓度优化
辅因子NADP+的浓度是影响L-丝氨酸反应速率的另一个关键因素。在L-丝氨酸检测体系中,NADP+的浓度也应保持过量水平,从而使AFSerDH的酶活性只与L-丝氨酸的浓度正相关。因此本研究对反应体系中NADP+的浓度进行了优化。在2.4.1节所述反应体积条件下,向L-丝氨酸反应体系中加入终浓度为1、2、3、4、5、6 mmol/L的NADP+,测定AFSerDH的酶活性。结果如图7所示,AFSerDH催化活性随着NADP+浓度的升高而升高,当NADP+浓度达到3 mmol/L,反应速率达到最大。因此选择L-丝氨酸反应体系中NADP+的最佳浓度为3 mmol/L。
2.4.3 基于酶催化的L-丝氨酸检测方法的建立和标准曲线绘制
基于对AFSerDH催化体系的优化,本研究建立了L-丝氨酸酶法检测方法。该方法使用的催化体系为:50 mmol/L碳酸钠-碳酸氢钠(pH=9.5),3 mmol/L NADP+,AFSerDH 2 U/mL,检测温度为40 ℃,反应时间为20 min,使用分光光度计或酶标仪测定340 nm 处吸光度的变化。随后利用L-丝氨酸标准液,配制浓度为0~10 mmol/L的L-丝氨酸,分别测定不同样品中的L-丝氨酸含量。结果表明,L-丝氨酸浓度为0~10 mmol/L时340 nm处吸光度的上升值(ΔOD340nm)与L-丝氨酸浓度呈良好的线性关系,标准曲线的回归方程为Y=0.102 4X+0.029 9,R2=0.996 5(图8)。结果说明,本研究建立的基于酶催化的L-丝氨酸检测方法在0~10 mmol/L检测阈值范围内,具有较高的检测灵敏度和准确性,适用于L-丝氨酸的高效快速检测。
2.5 L-丝氨酸检测方法的回收率测定
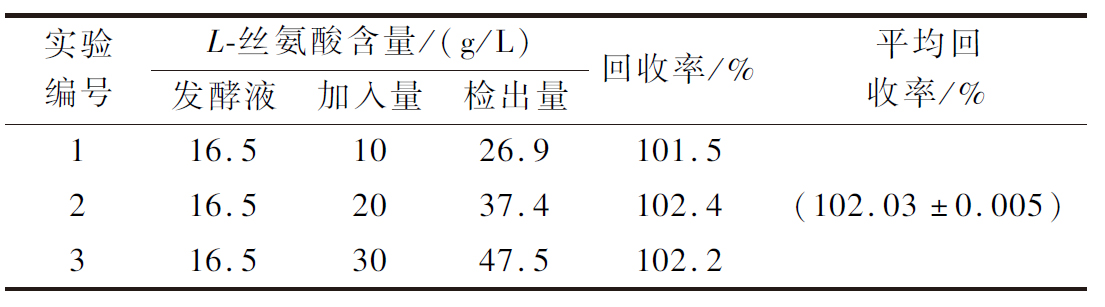
为了进一步验证基于酶催化的L-丝氨酸检测方法在实际生产过程的应用,本研究利用L-丝氨酸检测方法对L-丝氨酸发酵液中L-丝氨酸的含量和加标回收率进行了测定(表1)。在L-丝氨酸发酵液中加入终质量浓度为10、20、30 g/L的L-丝氨酸标准液,混匀后利用L-丝氨酸酶催化检测方法对混合液中的L-丝氨酸含量进行测定,以HPLC法为对照。结果表明,HPLC法和酶法检测的L-丝氨酸发酵液中的L-丝氨酸含量分别为16.5、16.9 g/L,结果基本一致。通过加标回收实验分析,L-丝氨酸酶法检测方法的平均回收率达到102.03%。综上所述,本研究建立的L-丝氨酸酶催化检测方法具有良好的准确性,能有效测定发酵液中L-丝氨酸的含量,能够满足实际生产过程中L-丝氨酸含量的快速检测分析。
表1 发酵液中L-丝氨酸回收率测定
Table 1 Determination of L-serine recovery in fermentation broth
3 结论
本研究针对目前L-丝氨酸检测方法灵敏性低、特异性差、操作复杂等问题,利用L-丝氨酸-3-脱氢酶的催化特性,将L-丝氨酸浓度和NADPH生成量偶联,建立了一种简单快速的L-丝氨酸酶法检测方法,实现了L-丝氨酸样品浓度的高效快速检测。本研究通过对AFSerDH酶学性质的分析和催化体系的优化,建立了L-丝氨酸酶法检测体系,该体系包括50 mmol/L碳酸钠-碳酸氢钠缓冲液(pH=9.5),3 mmol/L NADP+,AFSerDH 2 U/mL,检测温度为40 ℃,检测L-丝氨酸的浓度为1~10 mmol/L。本研究建立的L-丝氨酸酶法检测方法具有简单快速、专一性强、检测效率高等特点,能够在较短时间内完成大量L-丝氨酸浓度的检测工作,从而实现L-丝氨酸工程菌种的高通量检测和评估,为L-丝氨酸工业菌种的高通量选育提供了重要的技术支撑。
[1] ZHANG X M, XU G Q, SHI J S, et al.Microbial production of L-serine from renewable feedstocks[J].Trends in Biotechnology, 2018, 36(7):700-712.
[2] XU G Q, ZHANG X M, XIAO W H, et al.Production of L-serine and its derivative L-cysteine from renewable feedstocks using Corynebacterium glutamicum:Advances and perspectives[J].Critical Reviews in Biotechnology, 2024, 44(3):448-461.
[3] ![]() M.Serine metabolism in health and disease and as a conditionally essential amino acid[J].Nutrients, 2022, 14(9):1987.
M.Serine metabolism in health and disease and as a conditionally essential amino acid[J].Nutrients, 2022, 14(9):1987.
[4] ROSA-TÉLLEZ S, ALC NTARA-ENGU
NTARA-ENGU DANOS A, MART
DANOS A, MART NEZ-SEIDEL F, et al.The serine-glycine-one-carbon metabolic network orchestrates changes in nitrogen and sulfur metabolism and shapes plant development[J].The Plant Cell, 2024, 36(2):404-426.
NEZ-SEIDEL F, et al.The serine-glycine-one-carbon metabolic network orchestrates changes in nitrogen and sulfur metabolism and shapes plant development[J].The Plant Cell, 2024, 36(2):404-426.
[5] DANG S, JAIN A, DHANDA G, et al.One carbon metabolism and its implication in health and immune functions[J].Cell Biochemistry and Function, 2024, 42(1):e3926.
[6] YE L S, SUN Y C, JIANG Z L, et al.L-serine, an endogenous amino acid, is a potential neuroprotective agent for neurological disease and injury[J].Frontiers in Molecular Neuroscience, 2021, 14:726665.
[7] BRASSIER A, VALAYANNOPOULOS V, BAHI-BUISSON N, et al.Two new cases of serine deficiency disorders treated with L-serine[J].European Journal of Paediatric Neurology, 2016, 20(1):53-60.
[8] 克丽凤, 张伟国, 钱和.L-丝氨酸的生产及其应用[J].江苏食品与发酵, 2001(2):19-22.KE L F, ZHANG, W G, QIAN H.Production and application of L-serine [J].Jiangsu Food and Fermentation, 2001(2):19-22.
[9] 刘岩, 王慧, 史吉平, 等.微生物法生产L-丝氨酸代谢工程研究进展[J].生物技术通报, 2015,31(8):44-49.LIU Y, WANG H, SHI J P, et al.Research progress on metabolic engineering for microbial production of L-serine[J].Biotechnology Bulletin, 2015,31(8):44-49.
[10] MUNDHADA H, SEOANE J M, SCHNEIDER K, et al.Increased production of L-serine in Escherichia coli through adaptive laboratory evolution[J].Metabolic Engineering, 2017, 39:141-150.
[11] ZHANG X M, GAO Y J, CHEN Z W, et al.High-yield production of L-serine through a novel identified exporter combined with synthetic pathway in Corynebacterium glutamicum[J].Microbial Cell Factories, 2020, 19(1):115.
[12] 李忠财, 董会娜, 张大伟, 等.L-丝氨酸检测技术的研究进展[J].工业微生物, 2016, 46(5):61-65.LI Z C, DONG H N, ZHANG D W, et al.Development of analytical methods for L-serine[J].Industrial Microbiology, 2016, 46(5):61-65.
[13] WEI L, ZHAO J H, WANG Y R, et al.Engineering of Corynebacterium glutamicum for high-level γ-aminobutyric acid production from glycerol by dynamic metabolic control[J].Metabolic Engineering, 2022, 69:134-146.
[14] TCHIGVINTSEV A, SINGER A, BROWN G, et al.Biochemical and structural studies of uncharacterized protein PA0743 from Pseudomonas aeruginosa revealed NAD+-dependent L-serine dehydrogenase[J].Journal of Biological Chemistry, 2012, 287(3):1874-1883.
[15] CHOWDHURY E K, HIGUCHI K, NAGATA S, et al.A novel NADP+-dependent serine dehydrogenase from Agrobacterium tumefaciens[J].Bioscience, Biotechnology, and Biochemistry, 1997, 61(1):152-157.