2021年5月,国际益生菌和益生元科学协会发布后生元共识声明,将后生元定义为:对宿主健康有益的无生命微生物和/或其成分的制剂[1]。研究表明后生元具有调节免疫[2-4]、抗氧化[3-4]、抗炎抑菌[4]、修饰肠道微生物群[3]等多方面健康作用。由于后生元良好的益生特性,产业界已将后生元视为继益生菌、益生元和合生制剂之后的第四代微生态产品。
我国针对可食用菌种质量检测方法的主要依据是GB 4789.34—2016《食品安全国家标准 食品微生物学检验 双歧杆菌检验》和GB 4789.35—2023《食品安全国家标准 食品微生物学检验 乳酸菌检验》等,均是采用稀释涂布平板法利用最适培养基对活性微生物总数进行测定,但是该方法不适用于后生元中灭活菌体的检测[5]。实验研究中常采用的灭活菌体总数的检验方法多是细菌计数板法[6]、荧光染色法[7]、荧光定量PCR法[8]、数字PCR法[9-10]等,上述方法大多具有结果不稳定、费时费力、样品匀液易出现凝聚、无法区分死/活细胞、仅适用于单一菌种的检验、操作复杂的缺点[11-13]。
流式细胞术(flow cytometry-based method,FCM)利用特异性荧光染料染色,能够对细胞进行计数统计,具有速度快、灵敏度高的优点[14-15]。国内外许多学者将其用于乳酸菌、食源性致病菌和酵母的活菌计数[15-17],并在乳制品、饮料中实际应用。国际标准化组织发布的ISO 19344:2015《牛奶和乳制品.发酵剂、益生菌和发酵产品.用流式细胞术对乳酸菌的定量》,以及我国海关总署发布的SN/T 5436—2022《乳及乳制品发酵剂、发酵产品中乳酸菌计数 流式细胞仪法》,其适用范围均是针对食品中活性食品用菌剂的活菌总数检测。我国目前缺少适用于各类食品中灭活微生物细胞总数检验的相关标准[18],无法保证后生元产品及添加灭活食品用菌剂产品的质量,不利于保障消费者的合法权益。本研究通过优化实验方法,采用SYTO 9和碘化丙啶(propidium iodide,PI)染料对活性/灭活菌体进行染色,再利用流式细胞仪检测其荧光信号,从而实现对产品中的灭活菌体总数的准确测定。
本研究以益生菌菌株和后生元产品为研究对象,结合流式细胞术和平板计数法(plate counting method,PCM),建立了一种后生元样品中具有完整菌体形态的灭活菌体的快速定量检测方法,旨在进一步缩短检测周期、提高定量检测的准确性,以期实现后生元样品中具有完整菌体形态的灭活菌体总数的快速、高效、精确定量检测,为后生元产品的市场化和商业化提供重要的技术保障。
1 材料与方法
1.1 材料与试剂
MRS肉汤培养基、MRS琼脂培养基,青岛海博生物技术有限公司;L-半胱氨酸盐酸盐一水物,上海源叶生物科技有限公司;刃天青,上海麦克林生化科技有限公司;PBS,北京索莱宝科技有限公司;荧光PI染料(货号556463),美国BD Biosciences公司;荧光染料SYTOTM Green Fluorescent Nucleic Acid Stains(货号S34854),美国Thermo Fisher Scientific公司。0.22 μm过滤器(Millipore,SLW033LS),Merck公司;螺口厌氧试管,北京紫烟科技有限公司。本实验所用益生菌菌株信息如表1所示,本实验所用后生元样品信息如表2所示。
表1 实验所用益生菌菌株
Table 1 List of all probiotics used in this study

表2 实验用后生元样品
Table 2 List of all postbiotics used in this study

编号样品名称生产菌种说明书标识总菌数/(CFU/mL)1HSY01唾液联合乳杆菌CECT5713≥1.00E+112HSY02植物乳植杆菌2.00E+123HSY03GBW-LP001(CGMCC No.22078)2.00E+114HSY04唾液联合乳杆菌LS97、嗜酸乳杆菌LA85、副干酪乳酪杆菌LC861.20E+115HSY05嗜酸乳杆菌DDS-1、鼠李糖乳酪杆菌UALr-06、动物双歧杆菌乳亚种UABla-124.00E+106HSY06动物双歧杆菌乳亚种CECT81451.50E+107HSY07动物双歧杆菌乳亚种B420、动物双歧杆菌乳亚种HN019、嗜酸乳杆菌NCFM、副干酪乳酪杆菌Lpc-37、动物双歧杆菌乳亚种BI-04、植物乳植杆菌Lp-1152.50E+098HSY08植物乳植杆菌6595、鼠李糖乳酪杆菌HN001、短双歧杆菌M-16V、动物双歧杆菌乳亚种HN019、动物双歧杆菌乳亚种Bi-07、动物双歧杆菌乳亚种BL-041.50E+10
1.2 仪器与设备
Accuri C6 PLUS流式细胞仪,美国BD Biosciences公司;恒温培养箱,上海精宏实验设备有限公司;HZQ-X100恒温振荡培养箱,江苏太仓市实验设备厂;CAW400SG厌氧工作站,上海磐麦科技有限公司;DLQ120-B智能厌氧制备系统,北京艾思普科技有限公司;BSC-1600ⅡB2生物安全柜,苏州安泰空气技术有限公司;JBCJT-880A超净工作台,北京九彬医疗科技有限公司;Microfuge 16台式离心机,贝克曼库尔特(美国)股份有限公司;QIQIAN-08无菌均质器,上海启前电子科技有限公司;MX-S涡旋混匀仪,大龙兴创实验仪器(北京)股份公司;CKX53倒置显微镜,北京捷盈科技有限公司。
1.3 实验方法
1.3.1 样品液的制备
活菌菌悬液制备:表1中的1~8号菌株接种到5 mL的MRS液体培养基37 ℃好氧振荡培养,9~14号菌株接种于同样体积的厌氧MRS液体培养基中,37 ℃厌氧静置培养12 h。涡旋振荡后吸取1 mL菌悬液,5 000 r/min离心10 min后弃上清液,收集菌体,用1 mL无菌PBS重悬,得到活菌菌悬液,备用。
灭活菌悬液制备:在1 mL活菌发酵液中加入4 mg/mL的热灭活保护剂(海藻酸钠和甘油的混合物),将混合液加热升温至80 ℃,维持60 min进行热灭活[19];热灭活后将混合液5 000 r/min离心10 min,去上清液,收集菌体,用1 mL无菌PBS重悬,得到灭活菌悬液,备用。
后生元样品液制备:以无菌操作称取2 g后生元样品于198 mL无菌PBS中,装入无菌均质袋中,在均质器中以10 次/s的速度均质5~10 min,直至样品分散均匀,在显微镜下(物镜100倍放大倍率)确认无细胞凝聚团,得到后生元样品悬液,备用。
1.3.2 流式细胞术计数
采用流式细胞术分别统计样品中活菌数、具有完整菌体形态的灭活菌体数和细菌总数。用无菌PBS以无菌操作将1.3.1节中的样品液采用10倍梯度稀释制成适宜稀释度的菌悬液(浓度107~108 CFU/mL[20])。吸取880 μL无菌PBS和100 μL稀释后的样品溶液于1.5 mL离心管中,避光加入10 μL的0.15 mmol/L PI工作液和10 μL的0.001 mmol/L SYTO 9工作液,涡旋混匀后37 ℃避光孵育15 min。
采用Accuri C6 PLUS流式细胞仪,设置上样体积50 μL,上样速度35 μL/min,阈值3 000(FSC-H通道),以FITC荧光通道检测SYTO 9标记的总菌数,以PerCP荧光通道检测PI标记的灭活菌体数。按照流式细胞仪操作指南,进行上机检测,每个样品进行5次平行测定,检测需在染色后45 min内完成。检测结束后圈定合适的门进行计数。
1.3.3 平板计数法活菌计数
采用平板计数法统计样品中的活菌数。用无菌PBS以无菌操作对1.3.1节中的样品液进行10倍梯度稀释,直至稀释到合适的梯度(浓度102~103 CFU/mL)。吸取1 mL稀释液和50 ℃计数琼脂混匀铺平皿,每个梯度重复3次。同时在另一个平皿直接注入培养基做空白对照。将平板放置37 ℃培养箱中培养48 h后计数。菌落个数取3个平板计数结果的平均值。
1.3.4 流式细胞术区分死活菌的验证
参照1.3.1节的方法获得益生菌活菌和灭活菌悬液。PI染料具有膜选择性通透性,不能穿过活菌的细胞膜,只能穿过破损的细胞膜而对细胞核染色[21]。将不同体积比(0∶100、25∶75、50∶50、75∶25、100∶0)的益生菌活菌和灭活菌悬液混匀,与SYTO 9和PI进行染色孵育后采用流式细胞术检测。
1.3.5 流式分析定量检测后生元样品中灭活菌体的验证
参照第1.3.1节的方法获得益生菌灭活菌悬液和后生元样品悬液。将不同体积比(0∶100、10∶90、20∶80、50∶50、80∶20、90∶10、100∶0)的益生菌灭活菌悬液和后生元样品悬液混匀,与SYTO 9和PI进行染色孵育后采用流式细胞术检测。
1.4 数据分析
利用Excel软件和Origin软件对数据进行分析和处理,统计学描述采用“平均值±标准差”,并比较和评价流式细胞术计数结果与平板计数结果的相关性。
2 结果与分析
2.1 流式细胞术可信度检测
将制备的益生菌活菌和灭活菌悬液分别按照不同体积比例混合均匀,再采用流式细胞术进行检测。结果显示如表3所示。流式细胞术测得的灭活菌和活菌的数量比例与添加比例接近(图1),说明流式细胞术在区分活菌和灭活菌体方面具有较高的灵敏度和特异性,可以定量测量益生菌活菌数和灭活菌体数。将益生菌的灭活/活菌计数结果比值与其添加比例进行最佳拟合线性回归分析(图2),结果活菌和灭活菌体的R2分别为0.997 9和0.996 3,均高于LIVE/DEAD Baclight试剂盒说明书Demo实验的R2值,说明本实验中所用染料浓度、染色时间以及活/灭活菌体的圈定门均在合适范围内,适合进行计数实验。
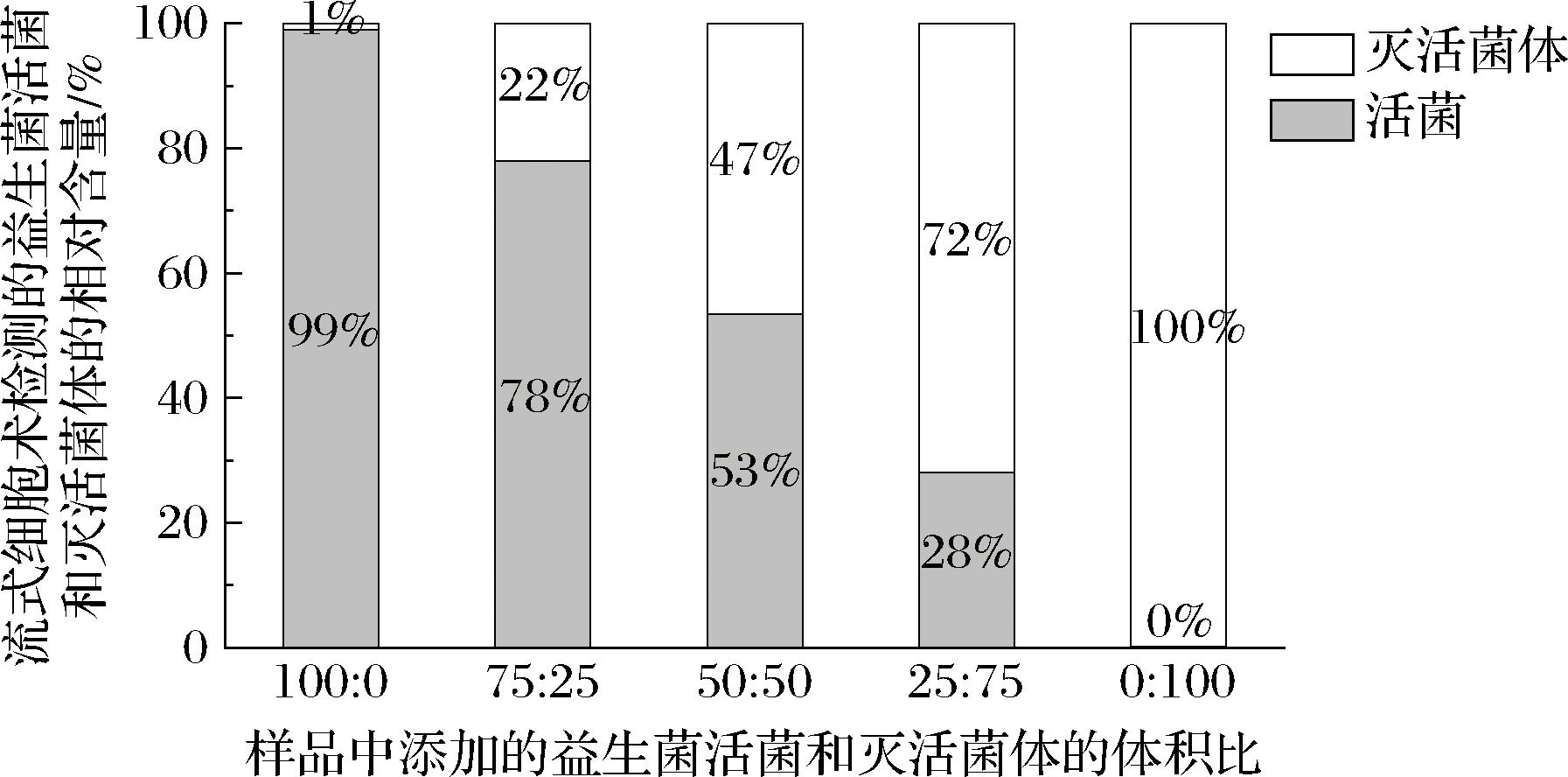
图1 流式细胞术检测的益生菌活菌和灭活菌体的百分比
Fig.1 Percentage of live and inactivated probiotics detected by FCM
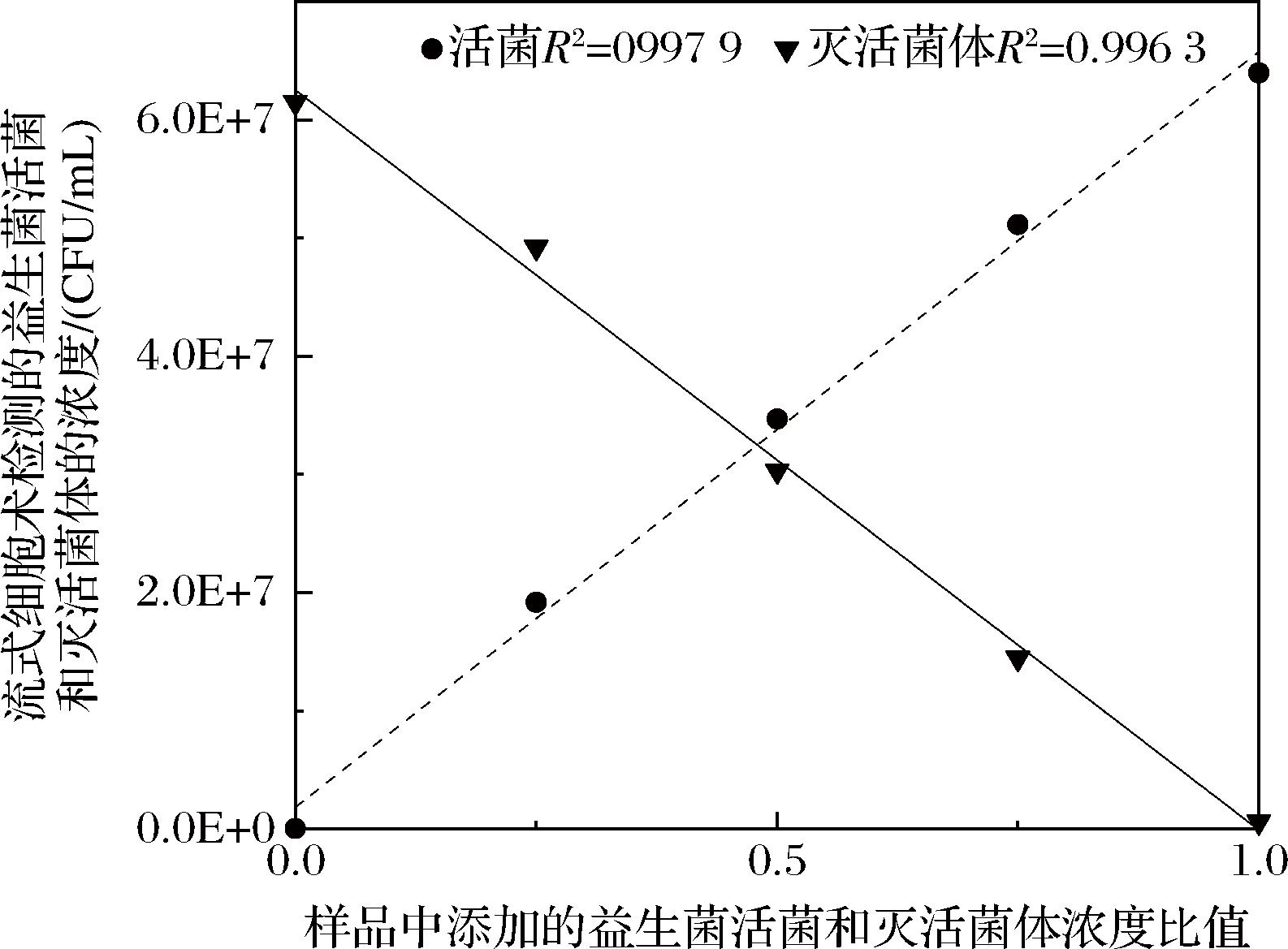
图2 流式细胞术对益生菌活菌和灭活菌体定量检测值的线性回归分析
Fig.2 The linear regression analysis of quantitative detection values for live and inactivated probiotics by FCM
表3 流式细胞术检测的益生菌活菌和灭活菌体浓度
Table 3 Live bacterial counts and inactivated bacterial counts of the probiotics by FCM
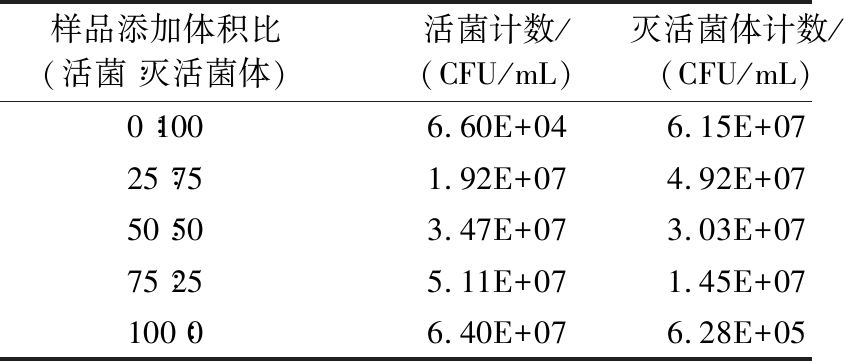
样品添加体积比(活菌∶灭活菌体)活菌计数/(CFU/mL)灭活菌体计数/(CFU/mL)0∶1006.60E+046.15E+0725∶751.92E+074.92E+0750∶503.47E+073.03E+0775∶255.11E+071.45E+07100∶06.40E+076.28E+05
2.2 流式细胞术定量检测益生菌灭活菌体
14株活化后接种培养的益生菌的发酵液经无菌PBS稀释10倍梯度后,分别采用流式细胞术与平板计数法进行活菌数检测;剩余的菌液进行热灭活,用无菌PBS稀释并制备3个不同浓度的灭活菌体试样,采用流式细胞术进行灭活菌体计数,定量结果如表4所示。如图3和图4所示,当待检试样稀释到合适的梯度(菌悬液浓度106~107 CFU/mL)进行流式分析检测时,流式细胞术检测出的活菌数与平板计数法检测的活菌数结果基本一致且线性良好(R2=0.995 5),验证了流式细胞术可精准定量活菌,其结果能与经典的平板计数法相互印证;流式细胞术检测出的活菌数与流式细胞术检测出的灭活菌体数结果基本一致且线性良好(R2=0.994 3),表明流式细胞术能够准确定量灭活菌体数,且本研究所选的热灭活处理方式不改变菌体的总数;流式细胞术检测出的灭活菌体数与平板计数法检测的活菌数结果基本一致且线性良好(R2=0.990 2),证明了灭活后流式细胞术检测的灭活菌体数量准确反映了原始的活菌数。因此,使用流式细胞术定量检测具有完整菌体形态的灭活菌体数量具有可行性。
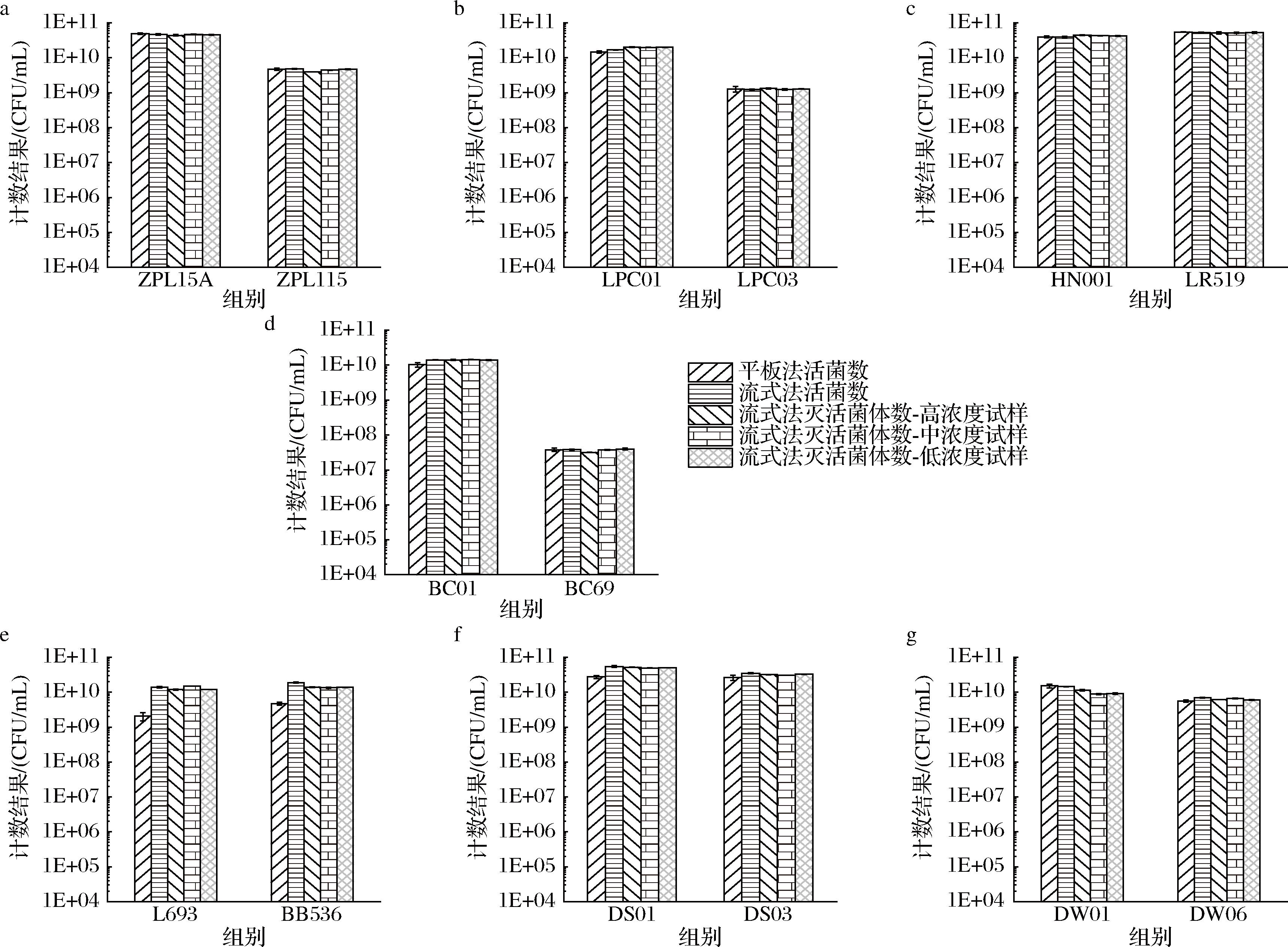
a-植物乳植杆菌;b-副干酪乳酪杆菌;c-鼠李糖乳酪杆菌;d-凝结魏茨曼氏菌;e-长双歧杆菌长亚种;f-短双歧杆菌;g-动物双歧杆菌动物亚种
图3 流式细胞术与平板计数法检测益生菌活菌和灭活菌体的结果
Fig.3 The results of quantitative detection for live probiotics by FCM/PCM and inactivated probiotics by FCM
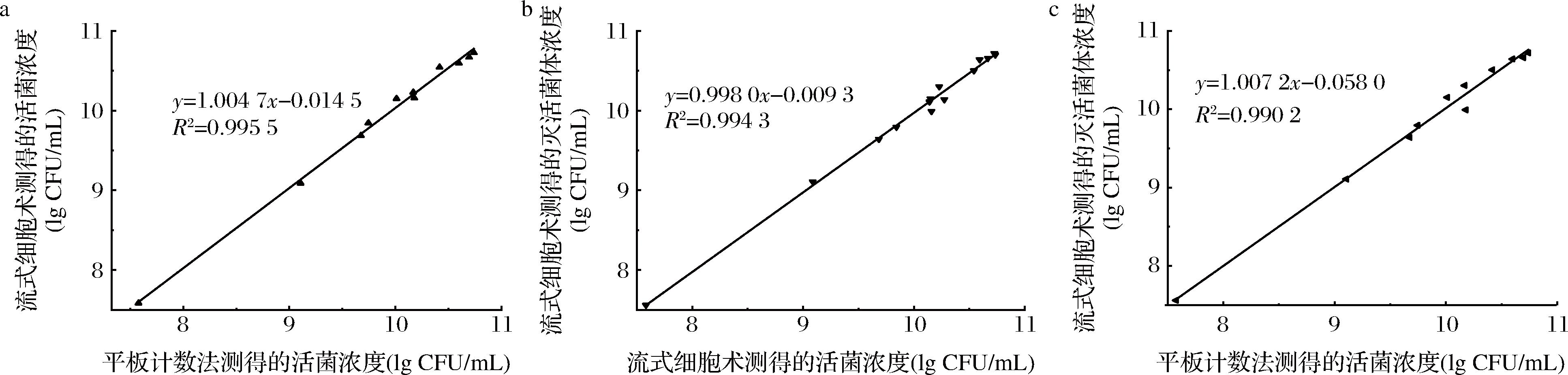
a-平板法活菌计数与流式法活菌计数的线性关系;b-流式法活菌计数与流式法灭活菌体计数的线性关系;c-平板法活菌计数与流式法灭活菌体计数的线性关系
图4 流式细胞术与平板计数法定量检测益生菌活菌和灭活菌体的线性关系
Fig.4 The linear relationship between the results of quantitative detection for live probiotics by FCM/PCM and inactivated probiotics by FCM
表4 14株益生菌的定量结果 单位:CFU/mL
Table 4 Quantitative bacterial counts of 14 probiotics
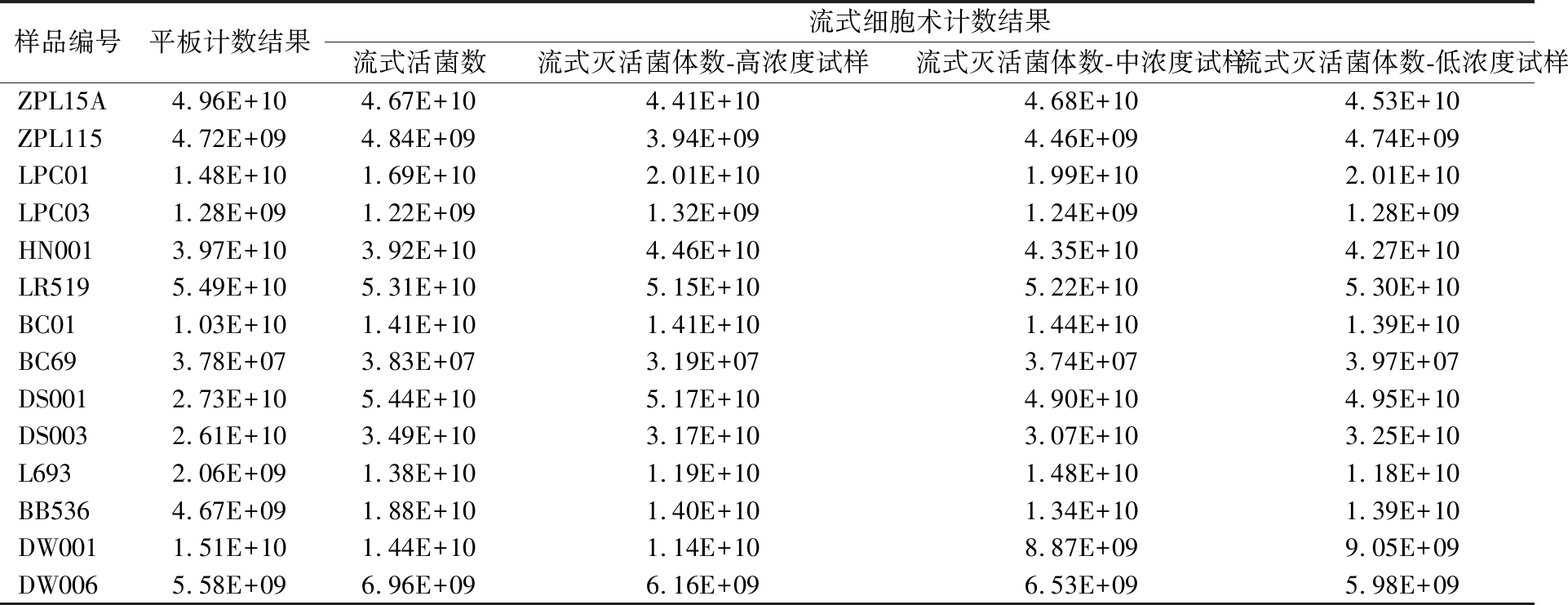
样品编号平板计数结果流式细胞术计数结果流式活菌数流式灭活菌体数-高浓度试样流式灭活菌体数-中浓度试样流式灭活菌体数-低浓度试样ZPL15A4.96E+104.67E+104.41E+104.68E+104.53E+10ZPL1154.72E+094.84E+093.94E+094.46E+094.74E+09LPC011.48E+101.69E+102.01E+101.99E+102.01E+10LPC031.28E+091.22E+091.32E+091.24E+091.28E+09HN0013.97E+103.92E+104.46E+104.35E+104.27E+10LR5195.49E+105.31E+105.15E+105.22E+105.30E+10BC011.03E+101.41E+101.41E+101.44E+101.39E+10BC693.78E+073.83E+073.19E+073.74E+073.97E+07DS0012.73E+105.44E+105.17E+104.90E+104.95E+10DS0032.61E+103.49E+103.17E+103.07E+103.25E+10L6932.06E+091.38E+101.19E+101.48E+101.18E+10BB5364.67E+091.88E+101.40E+101.34E+101.39E+10DW0011.51E+101.44E+101.14E+108.87E+099.05E+09DW0065.58E+096.96E+096.16E+096.53E+095.98E+09
2.3 流式细胞术定量检测后生元样品中灭活菌体的可行性
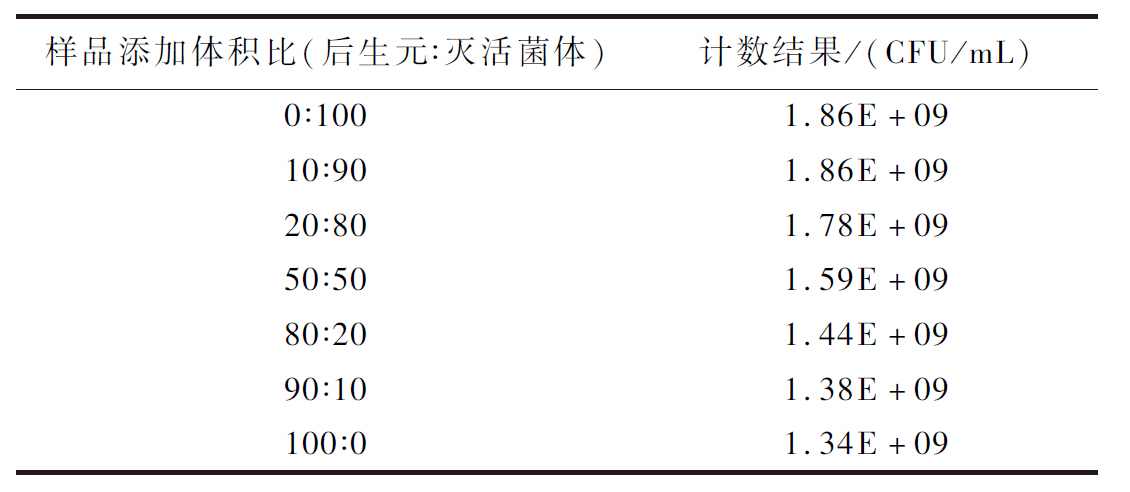
将制备的益生菌灭活菌悬液与后生元样品液分别按照不同体积比混合均匀以制备混合样品,再采用流式细胞术进行检测,结果显示如表5所示。将混合样品的计数结果与益生菌灭活菌体和后生元样品的添加比例进行最佳拟合线性回归分析(图5),结果得到相关系数R2为0.995 1,显示两者之间具有良好的线性相关性,这表明流式细胞术能够实现对后生元样品中灭活菌体数的准确定量,且具有抗复杂基质干扰能力。
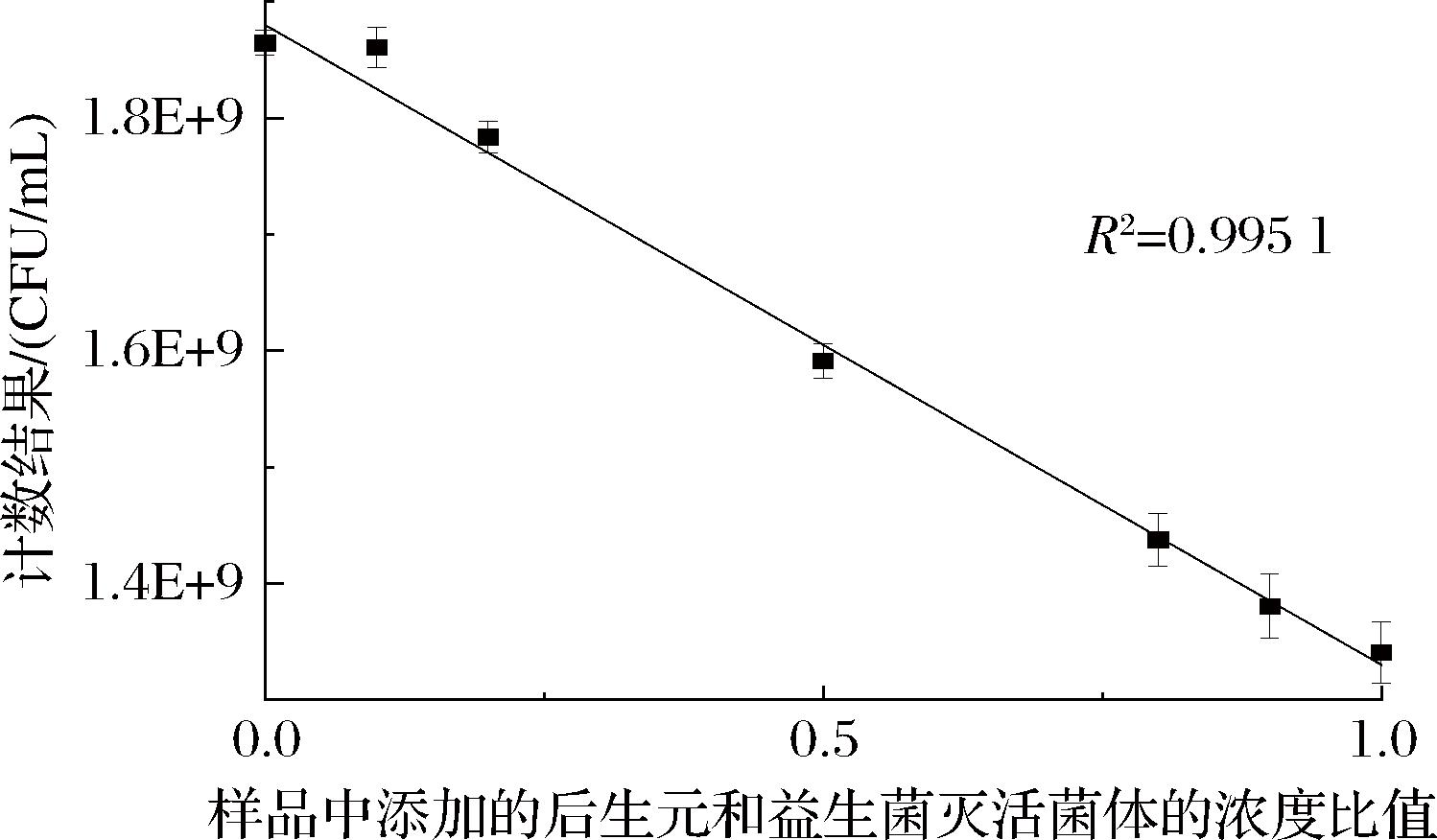
图5 流式细胞术检测益生菌灭活菌体与后生元混合样品的线性回归分析
Fig.5 Linear regression analysis of mixed samples of inactivated probiotic bacteria and postbiotics detected by FCM
表5 流式细胞术检测益生菌灭活菌体与后生元混合样品的结果
Table 5 The bacterial count of mixed samples of inactivated probiotics and postbiotics detected by FCM
2.4 流式细胞术定量检测后生元样品中灭活菌体
后生元样品液经无菌PBS稀释10倍梯度后,采用流式细胞术对后生元样品中的灭活菌体数进行定量检测。如图6所示,当待检试样稀释到合适的梯度(菌悬液浓度106~107 CFU/mL)进行流式分析检测时,流式细胞术检测出的后生元样品灭活菌体数与其说明书上标识的灭活菌体数结果基本一致。基于灭活菌体定量结果的高度准确性(与标识值一致)及抗基质干扰能力(混合体系线性验证),流式细胞术通过定量具有完整形态的灭活菌体数,可推荐为后生元产品检测的可靠独立质控手段。
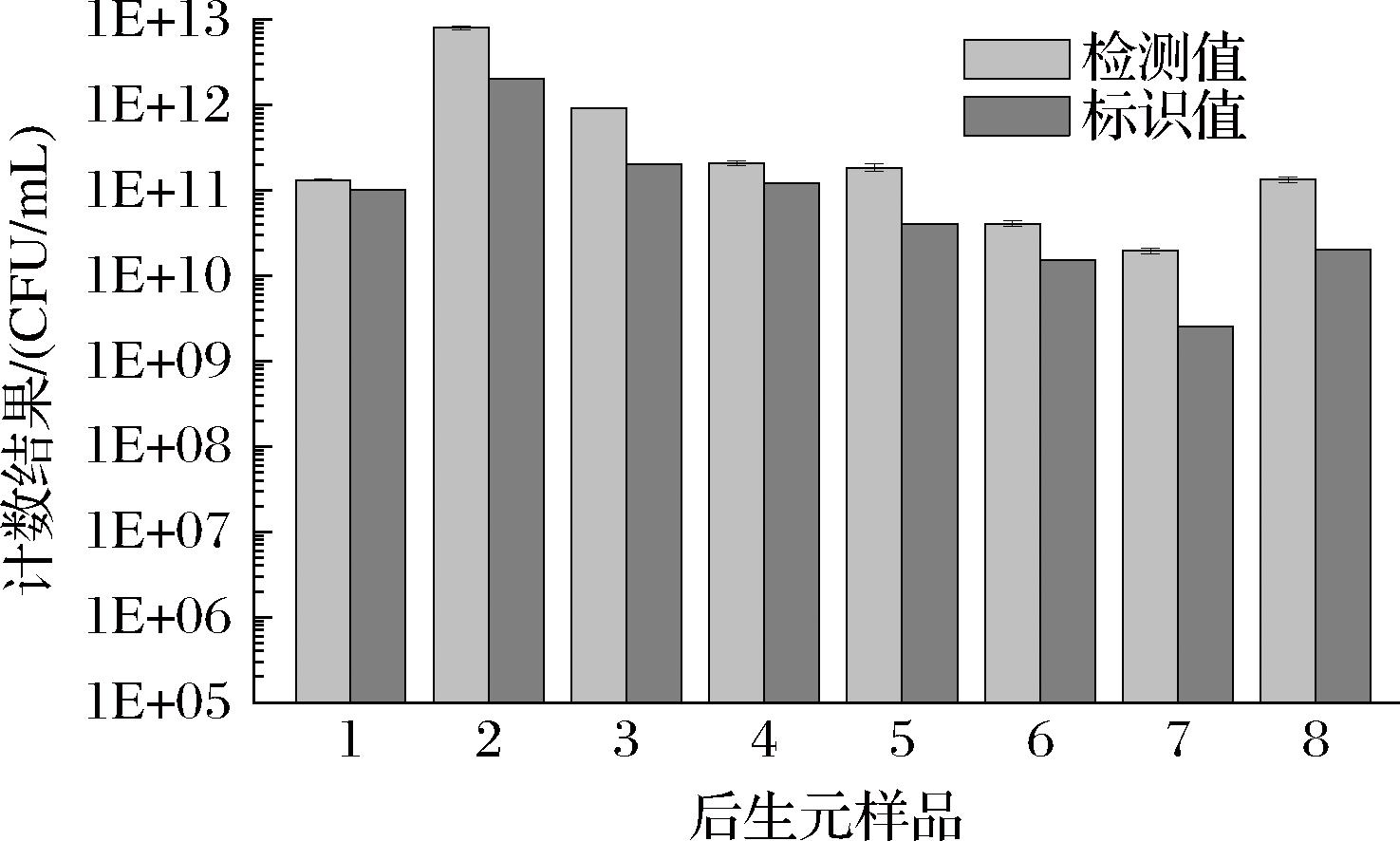
图6 后生元样品的流式细胞术检测值和说明书标识值
Fig.6 FCM-detection count and indicated count of postbiotic samples
3 结论与讨论
后生元制剂由于不需要考虑微生物活性,在食品领域具有更强的适用性,已被广泛应用于各类食品产品中。本研究建立了一种基于流式细胞术的后生元样品中具有完整菌体形态的灭活菌体的快速定量检测方法,为后生元产品的质量控制提供了一种新的技术手段,有利于促进后生元产业健康稳定发展。
流式细胞术作为一种先进的细胞分析技术,其在微生物检测领域的应用逐渐得到关注。本研究将流式细胞术应用于后生元样品中灭活菌体的定量检测,不仅扩展了流式细胞术的应用范围,也为后生元产品的质量控制提供了新的思路。对比实验表明流式细胞术的检测结果与平板计数法基本一致,但流式细胞术具有更高的检测效率和更简便的操作流程,能够实现对大量样品的快速分析。此外,流式细胞术还能够通过多参数分析,进一步了解细胞的状态和特性,为深入研究后生元产品提供更多的信息。
[1] HILL C, GUARNER F, REID G, et al. The International Scientific Association for Probiotics and Prebiotics consensus statement on the scope and appropriate use of the term probiotic[J]. Nature Reviews Gastroenterology &Hepatology, 2014, 11(8):506-514.
[2] MEHTA J P, AYAKAR S, SINGHAL R S.The potential of paraprobiotics and postbiotics to modulate the immune system:A Review[J].Microbiological Research, 2023, 275:127449.
[3] ZHAO X J, LIU S, LI S M, et al.Unlocking the power of postbiotics:A revolutionary approach to nutrition for humans and animals[J].Cell Metabolism, 2024, 36(4):725-744.
[4] 中华预防医学会微生态学分会, 北京伍连德公益基金会微生态健康管理专家委员会.后生元的研究及应用现状专家共识[J].中国微生态学杂志, 2023, 35(2):218-222.YUAN J L.Scientific consensus on research and application status of postbiotic[J].Chinese Journal of Microecology, 2023, 35(2):218-222.
[5] 皎丹. 食品微生物快速检测技术[J].现代食品, 2018(21):125-126;134.JIAO D.Rapid detection technology of food microorganisms[J].Modern Food, 2018(21):125-126;134.
[6] 张伟, 王巍杰, 张小乐.涂片显微计数法快速测定发酵饲料中细菌总数[J].华北理工大学学报(自然科学版), 2017, 39(1):114-120.ZHANG W, WANG W J, ZHANG X L.Smear microscopic counting method for rapid determination of total bacteria in fermented feed[J].Journal of North China University of Science and Technology(Natural Science Edition), 2017, 39(1):114-120.
[7] ROSS J, BOON P I, SHARMA R, et al.Variations in the fluorescence intensity of intact DAPI-stained bacteria and their implications for rapid bacterial quantification[J].Letters in Applied Microbiology, 1996, 22(4):283-287.
[8] 刘艳艳. 鲜乳细菌总数荧光定量PCR检测方法的建立[D].长春:吉林大学, 2014.LIU Y Y.Establishment of real-time PCR methods for detection of total bacteria in raw milk[D].Changchun:Jilin University, 2014.
[9] 张娜娜. 发酵乳及乳酸菌饮料中嗜酸乳杆菌检测方法比较研究[D].上海:上海师范大学, 2018.ZHANG N N.Comparative study on the detection methods of Lactobacillus acidophilus in fermented milk and lactic acid bacteria drinks[D].Shanghai:Shanghai Normal University, 2018.
[10] 赵丽青, 房保海, 殷培军, 等.沙门氏菌微滴式数字PCR定量检测方法的建立[J].中国口岸科学技术, 2024, 6(6):79-85.ZHAO L Q, FANG B H, YIN P J, et al.Establishment of droplet digital PCR assay for quantitative detection of Salmonella[J].China Port Science and Technology, 2024, 6(6):79-85.
[11] 王圣民, 王明月, 金光弼.流式细胞仪在细胞绝对计数方法中的应用及其进展[J].青岛医药卫生, 2023, 55(1):67-71.WANG S M, WANG M Y, JIN G B.Advance and application of flow cytometry in absolute cell counting[J].Qingdao Medical Journal, 2023, 55(1):67-71.
[12] BOYTE M E, BENKOWSKI A, PANE M, et al.Probiotic and postbiotic analytical methods:A perspective of available enumeration techniques[J].Frontiers in Microbiology, 2023, 14:1304621.
[13] 柏春玲, 董馨忆.应用流式细胞仪准确进行细胞计数的参数设定[J].昆明医科大学学报, 2014, 35(6):129-132.BAI C L, DONG X Y.Parameter settings for accurate cell counting by flow cytometer[J].Journal of Kunming Medical University, 2014, 35(6):129-132.
[14] DOHERTY S B, WANG L, ROSS R P, et al.Use of viability staining in combination with flow cytometry for rapid viability assessment of Lactobacillus rhamnosus GG in complex protein matrices[J].Journal of Microbiological Methods, 2010, 82(3):301-310.
[15] 姜凯. 基于流式细胞术的乳酸菌快速计数方法研究和活性判定[D].上海:上海师范大学, 2018.JIANG K.A rapid counting method and activity determination of lactic acid bacteria based on flow cytometry[D].Shanghai:Shanghai Normal University, 2018.
[16] 黄生权, 付萌, 唐青涛, 等.流式细胞术检测单增李斯特菌与酿酒酵母[J].现代食品科技, 2014, 30(3):195-200.HUANG S Q, FU M, TANG Q T, et al.Detection of Saccharomyces cerevisiae and Listeria monoeytogenes by flow cytometry[J].Modern Food Science and Technology, 2014, 30(3):195-200.
[17] BENSCH G, RÜGER M, WASSERMANN M, et al.Flow cytometric viability assessment of lactic acid bacteria starter cultures produced by fluidized bed drying[J].Applied Microbiology and Biotechnology, 2014, 98(11):4897-4909.
[18] 中国食品科学技术学会益生菌分会. 后生元的研究现状及产业应用[J].中国食品学报, 2022, 22(8):416-426.Probiotics Society of the Chinese Institute of Food Science and Technology.Research of postbiotics and industrial application[J].Journal of Chinese Institute of Food Science and Technology, 2022, 22(8):416-426.
[19] 姜庆梅. 一种微生态制剂及其制备方法:中国, CN108157595A[P].2018-06-15.JIANG Q M.A microecological preparation and its preparation method:China, CN108157595A[P].2018-06-15.
[20] 王斌, 隋志伟, 刘思渊, 等.基于流式分析技术的奶粉中金黄色葡萄球菌活菌快速定量检测方法研究[J].计量学报, 2021, 42(2):250-258.WANG B, SUI Z W, LIU S Y, et al.Rapid and quantitative detection of viable Staphylococcus aureus in milk powder based on flow cytometry technology[J].Acta Metrologica Sinica, 2021, 42(2):250-258.
[21] NETZEL T L, NAFISI K, ZHAO M, et al.Base-content dependence of emission enhancements, quantum yields, and lifetimes for cyanine dyes bound to double-strand DNA:Photophysical properties of monomeric and bichromomphoric DNA stains[J].The Journal of Physical Chemistry, 1995, 99(51):17936-17947.