全球范围内,食源性疾病作为一个主要的公共安全问题得到了广泛的关注。食源性疾病可导致严重的健康危害,在已知的250余种食源性致病菌中,2/3的食源性疾病是由细菌病原菌引发的[1]。大肠埃希氏菌(Escherichia coli)O157:H7是一种可以引起严重身体危害的食源性致病菌,感染此菌可引起出血性结肠炎、溶血性尿路综合症和血栓性血小板紫癜[2]。目前,微生物学的金标准包括培养和鉴别性诊断,4~7 d才能得到确切的实验结果,既繁琐又耗时。为了使因细菌病原菌导致的食源性疾病得到很好的预防和治疗,关键问题是快速准确地检测出细菌病原菌。因此,开发一种具有高敏感性和高特异性识别的细菌病原菌检测方法显得尤为重要[3]。
到目前为止,许多快速和高敏感的细菌病原体的检测方法得到了发展,其中,在快速、准确诊断细菌病原体方面,以分子生物学为基础的方法得到了长足的发展。核酸扩增技术在分子诊断和医疗实践中起到重要的作用,以PCR为基础的核酸扩增技术大量兴起,比说巢式PCR、实时定量PCR、基于核酸序列的扩增(nucleic acid sequence-based amplification,NASBA)[4]。然而,这些方法需要复杂的温度循环设备扩增核酸,同时也需要昂贵的仪器输出实验结果,更为重要的是这些方法的特异性能力有限,常会有假阳性结果出现。在近年,滚环扩增(rolling circle amplification,RCA)应用比较广泛,RCA的优点为在恒温的环境下完成扩增,可以识别单碱基错配,相对于PCR反应有较低的假阳性发生几率,产物为一条长的含有若干与环状探针互补的重复单链DNA序列便于信号的集中[5]。最近,RCA结合各种生物传感器运用于微生物检测得到了广泛的研究,比如超分支RCA为基础的电化学发光生物传感器[6]、RCA为基础的金纳米天线-电学DNA生物传感器[7]、RCA为基础的表面等离子体共振生物传感器[8]、RCA为基础的石英晶体微量天平生物传感器[9]。
本研究以大肠埃希氏菌O157:H7为检测对象,环状探针为目标物特异性识别原件,RCA放大目标物信号,SYBR Green Ⅱ结合单链DNA后荧光信号显著增强,荧光强度与单链DNA的数量相关,结合实时定量荧光输出可以实现实时定量的荧光信号监测,也可在紫外灯的照射下实现定性的信号可视化输出,从而建立一种简单、快速、特异性良好、灵敏度较高的基于滚环扩增的双模态信号输出生物传感器,既可用于实验室检测,也可用于现场可视化检测的食源性微生物的检测方法。
1 材料与方法
1.1 材料与试剂
1.1.1 试剂
T4 DNA连接酶、Taq DNA连接酶、E.coli DNA连接酶、外切酶Ⅰ、外切酶Ⅲ、Phi29 DNA聚合酶,新英格兰生物公司;限制性内切酶QuickCutTM EcoRⅠ、QuickCutTM HindⅢ、QuickCutTM BamHⅠ,大连宝生物工程公司;dNTP Mixture、TIANamp细菌基因组DNA提取试剂盒,天根生化科技有限公司;SYBR GreenⅡ(10 000×),北京索莱宝科技有限公司。
1.1.2 核酸序列
以E.coil O157:H7的rfbE基因为目标,设计一系列核酸序列,包括环状探针、捕获探针、目的序列、单碱基错配序列。委托苏州金唯智生物科技有限公司合成。具体序列见表1。
表1 核酸序列
Table 1 Nucleic acid sequences
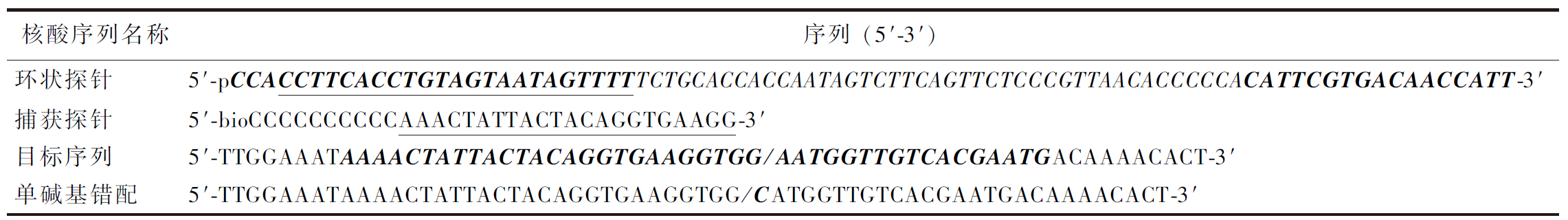
注:环状探针的5′磷酸化以便于连接,黑色加粗斜体完全与目的序列的黑色加粗斜体互补,下划线部分与捕获探针的下划线部分完全互补;目的序列的斜线部分的左右黑色加粗斜体表示分别与环状探针的5′和 3′末端黑色加粗斜体完全互补;单碱基错配的黑斜体序列与目标序列的相应位置单碱基错配。
1.2 仪器与设备
CFX-96荧光定量PCR仪、Gel Doc 2000凝胶成像分析系统,美国Bio-Rad公司;SQP分析电子天平,赛多利斯科学仪器(北京)公司;DYY-6C电泳仪,北京市六一仪器厂;SY-1-2电热恒温水浴锅,天津欧诺仪器仪表有限公司。
1.3 实验方法
1.3.1 实验原理
用于本实验的探针包括线形环状探针(图1-A)和捕获探针,选择E.coli O157:H7的rfbE基因作为目的序列,在线形环状探针的5′、3′末端有可和目标序列完全互补的碱基序列,在线形环状探针的中间部分C(图1-A)有可与捕获探针完全杂交的通用区域。
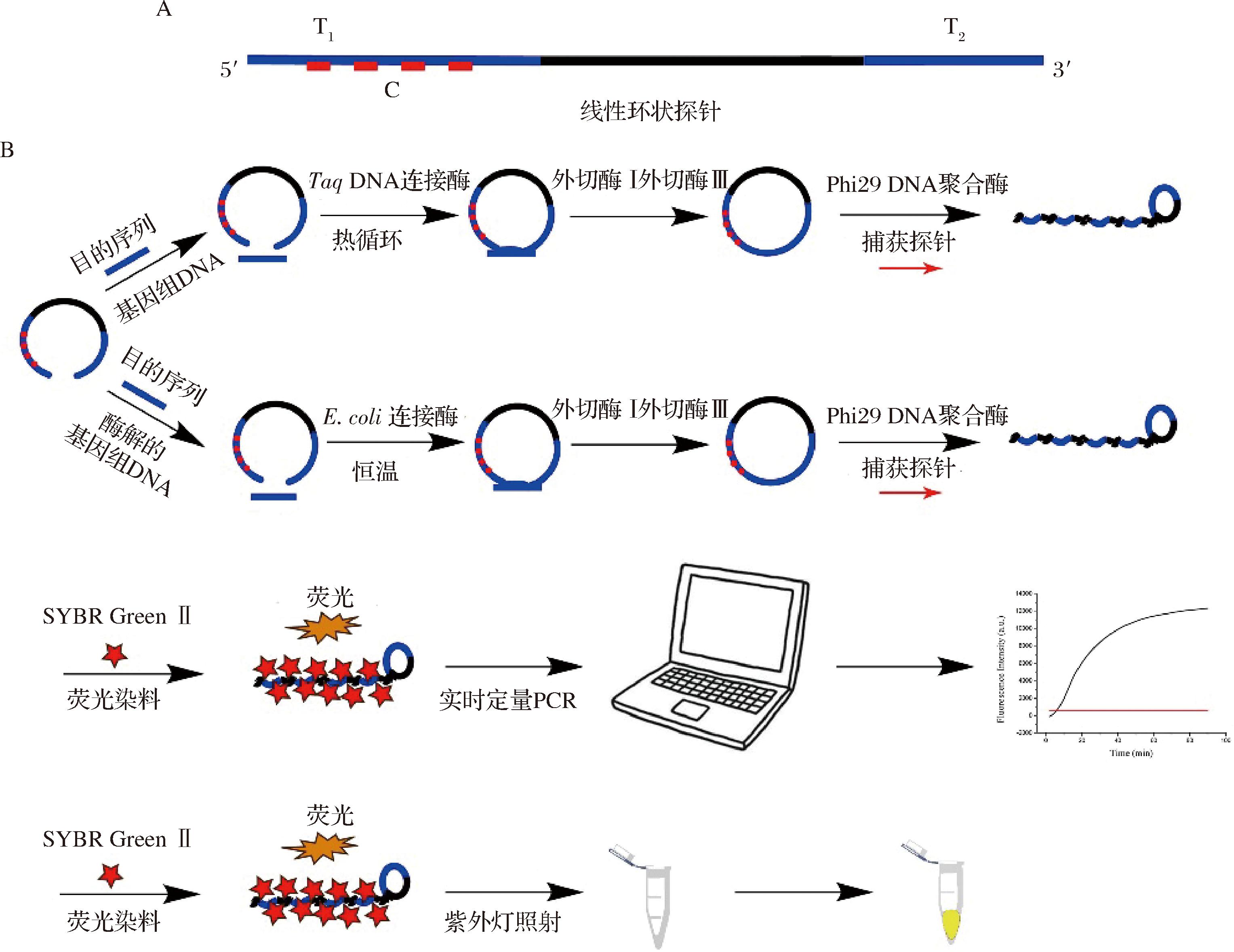
图1 基于RCA的双模态信号输出生物传感器的检测原理
Fig.1 Schematic diagram of the RCA-based bi-modality signal output biosensor
检测原理如图1所示,当目的序列可与线形环状探针的5′、3′末端完全杂交,5′、3′末端由E.coil DNA连接酶(Taq DNA连接酶)连接和环化,E.coil DNA连接酶(Taq DNA连接酶)不允许任何的错配,即使是单碱基的错配也会影响环化的形成。E.coil DNA连接酶耐高温能力不强,适用于恒温连接,为了保证所有的基因组DNA全部与线性环状探针连接,所以基因组DNA需要先用限制性内切酶进行片段化[10]以便于和线性环状探针的5′或3′末端进行杂交连接;Taq DNA连接酶耐高温能力较强,基因组DNA不需要片段化就可在温度循环的条件下将基因组DNA和线性环状探针的5′或3′末端进行杂交连接,所以适用于具有PCR仪器的条件下。连接后的体系在外切酶Ⅰ和外切酶Ⅲ的作用下将未反应的环状探针和目标物DNA分解,以免假阳性的出现。随后,捕获探针作为引物与环状探针的特定序列互补区域杂交进而在Phi29 DNA聚合酶和dNTPs存在的条件下引发RCA反应,RCA的产物是一条长的串联的与环状探针互补的重复的单链DNA序列[11]。RCA反应体系中存在SYBR GreenⅡ荧光染料,随着RCA反应的进行,单链DNA序列的数量增加,所产生的荧光信号被实时定量PCR监测,在不具备大型仪器实验条件的地方(如现场检验),也可以选择E.coil DNA连接酶在恒温条件下进行反应,在紫外灯的照射下观察荧光的变化从而实现结果的可视化。
1.3.2 实时定量荧光信号输出模式的检测方法
10 μL的反应体系中,Taq DNA连接酶buffer 1 μL,环状探针1 μmol/L,合成目标序列或单碱基错配序列10 nmol/L(提取的细菌基因组DNA 1 μL),10 U的Taq DNA连接酶,反应条件预变性94 ℃ 4 min;变性94 ℃ 30 s,连接60 ℃ 5 min,15个循环;95 ℃ 15 min,快速冰浴5 min。为了移除未反应的环状探针和线性的目的序列,上述混合反应物被加入到以下的反应体系中,1×buffer Ⅰ、外切酶Ⅰ和外切酶Ⅲ各10 U,37 ℃孵育60 min,95 ℃ 15 min失活。以上Taq DNA连接酶连接的产物加到25 μL的反应体系(包含1×Phi29 DNA 聚合酶buffer、1 μmol/L捕获探针)50 ℃孵育30 min后,加入5 U的Phi29 DNA聚合酶、1×SYBR GreenⅡ、1 mmol/L dNTPs、5 μg BSA,然后35 ℃孵育90 min,2 min收集1次荧光信号,65 ℃ 10 min酶失活。
1.3.3 借助紫外灯照射可视化信号输出模式的检测方法
在10 μL的反应体系中,E.coli DNA连接酶buffer 1 μL,环状探针1 μmol/L,合成目标序列10 nmol/L(提取的细菌基因组DNA预处理混合物1 μL),95 ℃孵育5 min,迅速冰浴静置10 min,该混合物在50 ℃连接60 min,加入10 U的T4 DNA连接酶或E.coli DNA连接酶,30 ℃孵育60 min。为了移除未反应的环状探针和线性的目的序列,上述混合反应物被加入到以下的反应体系中,1×bufferⅠ、外切酶Ⅰ和外切酶Ⅲ各10 U,37 ℃孵育60 min,95 ℃ 15 min失活。以上E.coli DNA 连接酶连接的产物加到25 μL的反应体系(包含1×Phi29 DNA聚合酶buffer、1 μmol/L捕获探针)50 ℃孵育30 min后,加入5 U的Phi29 DNA聚合酶、1×SYBR Green Ⅱ、1 mmol/L dNTPs、5 μg BSA, 然后35 ℃孵育90 min,65 ℃ 10 min酶失活,在紫外灯的照射下与阴性样品对照观察荧光强度变化,实现可视化信号的输出。
1.3.4 细菌基因组DNA的制备
实验所用7株菌为:大肠埃希氏菌O157:H7(ATCC 35150)、大肠埃希氏菌(CICC 10305)、金黄色葡萄球菌(ATCC 25923)、表皮葡萄球菌(ATCC14990)、腐生葡萄球菌(ATCC 49907)、铜绿假单胞菌(ATCC 27853)、单增李斯特菌(ATCC 7644),以上菌株贮存于本实验室。在37 ℃的LB培养基中培养过夜,按照TIANamp细菌DNA提取试剂盒的说明书提取基因组DNA。提取的基因组DNA用TE缓冲液洗脱后,在-20 ℃下保存。微生物基因组DNA的浓度根据试剂盒的说明书进行计算。在RCA反应之前,通过使用Quick CutTM EcoRⅠ、Quick CutTM HindⅢ和Quick CutTM BamHⅠ[10]将提取的基因组DNA进行片段化,用上述3种酶酶解消化30 min。
1.3.5 实际样品的制备
当地市场购得牛奶样品和鸡胸肉样品,以上样品均被证实不含大肠埃希氏菌O157:H7。
首先用8.5 g/L无菌氯化钠溶液清洗以上样品。随后,鸡胸肉样品通过匀浆器以8 000 r/min的速度匀浆2 min(样品与8.5 g/L无菌氯化钠的料液比为1∶10,g∶mL);牛奶样品直接用8.5 g/L无菌氯化钠溶液稀释10倍。将处于指数生长期的E.coli O157:H7加入到以上牛奶样品和鸡胸肉样品中,制得2组人工污染的阳性样品。
将上述2组人工污染的阳性样品放入质量分数为7.5%的氯化钠肉汤培养基中,在37 ℃下培养过夜。按照TIANamp细菌DNA试剂盒的说明提取细菌基因组DNA。用TE缓冲液洗涤提取的DNA并将其保存在-20 ℃备用[10]。
2 结果与分析
2.1 连接酶的选择
环状探针准确高效地识别目的序列是本研究关键,为了选取特异性良好、效率高的连接酶,本研究选择T4 DNA连接酶、E.coli DNA连接酶、Taq DNA连接酶分别用于目标DNA、单碱基错配DNA、阴性控制进行RCA反应,结果显示,对于阴性控制来说,3种连接酶均无荧光增加的现象发生,说明均无RCA产物的单链DNA产生;但是对于单碱基错配DNA来说,只有T4 DNA连接酶有荧光增加的现象,此现象说明:T4 DNA连接酶对单碱基识别能力欠别,而E.coli DNA 连接酶、Taq DNA 连接酶均对单碱基错配的连接有很好的识别能力,因此本研究选用E.coli DNA连接酶、Taq DNA连接酶作为连接线性环状探针和目标DNA的连接酶。
2.2 连接环化条件的优化
E.coli DNA连接酶和Taq DNA连接酶用于本研究,因此对以上2种酶的最佳条件进行优化。
2.2.1 E.coli DNA 连接酶连接环化条件的优化
2.2.1.1 杂交连接温度的优化
目标DNA与线性环状探针的有效的杂交结合是RCA扩增反应特异性识别目标物的关键,因此,对杂交连接温度进行考察。用1 nmol/L目标DNA和1 μmol/L的环状探针在45~65 ℃的梯度杂化连接温度下优化,在杂交连接温度为50 ℃时得到了最大的荧光增强值。因此选择50 ℃作为目标DNA与线性环状探针的杂交连接温度。将无该温度杂交连接的体系与有该杂交连接的体系作比较,其他条件均一样,结果显示无该杂化连接的荧光增加值明显低于有该杂化连接的体系,因此,该杂化连接温度对RCA扩增反应起重要作用。
2.2.1.2 E.coli DNA连接酶作用温度的优化
为了确保E.coli DNA连接酶在适宜的温度下进行连接反应,在50 ℃杂交连接完成的1 nmol/L目标DNA和1 μmol/L的环状探针的混合物,添加10 U的E.coli DNA连接酶,连接酶在15~50 ℃的梯度温度下进行环化连接,酶的作用温度为30 ℃时有最大的荧光增强值,故选择30 ℃作为E.coli DNA 连接酶的作用温度。
2.2.1.3 E.coli DNA 连接酶添加量的选择
E.coli DNA 连接酶添加量对目标DNA与线性环状探针的环化连接效果起重要作用,因此在50 ℃ 杂化连接完成的1 nmol/L目标DNA和1 μmol/L的环状探针的混合物中添加0、1、5、10、15 U的E.coli DNA连接酶,结果显示:添加量为0时无荧光增加,说明环化的环状探针的形成与否对RCA产物的形成具有至关重要的作用,随着添加量的增加荧光值增加,10 U 时达到最大值,故选择10 U为E.coli DNA连接酶添加量。
E.coil DNA 连接酶在30 ℃即可完成环状探针与目的基因的连接,适用于恒温连接,用于现场借助紫外灯输出可视化信号输出模式的检测方法。
2.2.2 Taq DNA 连接酶的连接环化条件的优化
2.2.2.1 Taq DNA 连接酶作用温度的优化
由于Taq DNA连接酶较E.coli DNA连接酶有较强的耐高温能力,对于Taq DNA连接酶作用的目标DNA与线性环状探针的杂交连接和环化连接同时进行。在1 nmol/L目标DNA和1 μmol/L的环状探针的混合物中添加15 U Taq DNA 连接酶,温度由45 ℃增加到65 ℃,每5 ℃递增进行该反应,结果显示在60 ℃时荧光增加值最大,故选择60 ℃为Taq DNA连接酶的作用温度。
2.2.2.2 Taq DNA 连接酶添加量的选择
由于Taq DNA连接酶添加量影响目标DNA与线性环状探针的环化连接效果以及RCA反应,在1 nmol/L目标DNA和1 μmol/L的环状探针的混合体系中添加0、5、10、15、20 U的Taq DNA连接酶,结果显示,添加量为0时无荧光增加,随着添加量的增加直到15 U时达到了荧光增加量的最大值,故选择15 U作为Taq DNA 连接酶添加量。
Taq DNA连接酶耐高温能力强,经过94 ℃预变性与变形后,在60 ℃仍具有高的连接活性,适用于实验室实时定量荧光信号输出模式的检测方法。
2.3 RCA条件的优化
2.3.1 捕获连接温度的优化
捕获探针作为引物连接到环化的环状探针上引发RCA扩增反应,捕获探针与环化环状探针的杂化连接对RCA扩增顺利进行起到重要作用。本研究对此杂化连接温度进行优化,1 nmol/L目标DNA和1 μmol/L的环状探针在以上优化的条件下连接,添加1 μmol/L的捕获探针,温度从45 ℃增加到70 ℃以5 ℃ 为梯度进行优化,结果如图2-A所示,在50 ℃时具有最大的荧光增强值,因此选择50 ℃作为捕获连接温度。
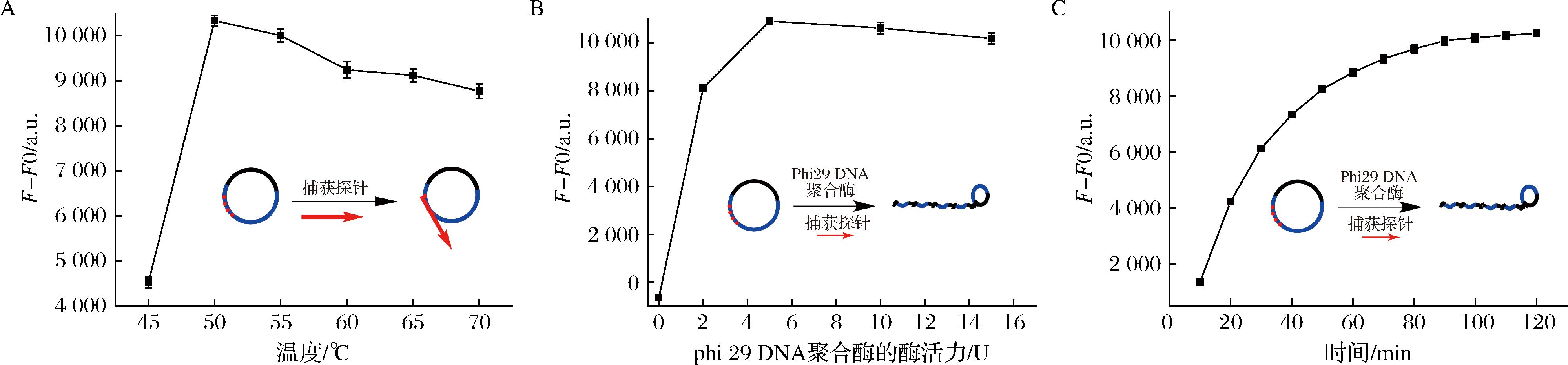
A-捕获连接的温度优化;B-Phi29 DNA聚合酶的最佳酶活优化;C-RCA扩增时间的优化
图2 RCA的条件优化
Fig.2 Optimization condition of RCA
2.3.2 Phi29 DNA聚合酶添加量的选择
Phi29 DNA聚合酶添加量对RCA扩增顺利进行起到重要作用,1 nmol/L目标DNA、1 μmol/L的环状探针和添加1 μmol/L的捕获探针在以上优化的条件下进行反应,在该体系中添加Phi29 DNA 聚合酶进行RCA反应,Phi29 DNA 聚合酶添加量分别为0、2、5、10、15 U,结果如图2-B所示,在添加量为5 U时的荧光增强值较其他添加量大,所以选择5 U的Phi29 DNA聚合酶添加量开展实验。
2.3.3 RCA扩增持续时间的研究
在以上优化的条件下,在1 nmol/L目标DNA、1 μmol/L的环状探针和添加1 μmol/L的捕获探针的体系中进行RCA反应,监测10~120 min的荧光值的变化,如图2-C所示,随着时间荧光值在急剧上升,90 min以后趋于平稳,分析原因可能是原料的耗尽、产物的大量产生阻止了反应平衡的进行。为了节约检测时间,所以选择RCA扩增时间为90 min。
2.4 基于滚环扩增的双模态信号输出生物传感器的灵敏性
为了考察该检测方法在实时定量荧光信号输出模式测定中的灵敏度,在优化的实验条件下,向检测体系中添加0 ~ 5×10-1 ng/μL微生物基因组 DNA对其进行考察,结果如图3-A所示,在微生物基因组DNA添加量为0 ng/μL的情况下,荧光发射光谱为最小值,随着微生物基因组DNA添加量的增加,荧光发射光谱逐渐增加。荧光发射光谱增加值(F-F0)浓度在5×10-3~5×10-1 ng/μL微生物基因组DNA浓度对数值之间呈良好的线性关系(R2=0.997 12,图3-B),根据20个空白样品平均值与3倍的标准偏差的和得出本方法的最低检测限(limit of detection,LOD)为5.048×10-3 ng/μL微生物基因组DNA。
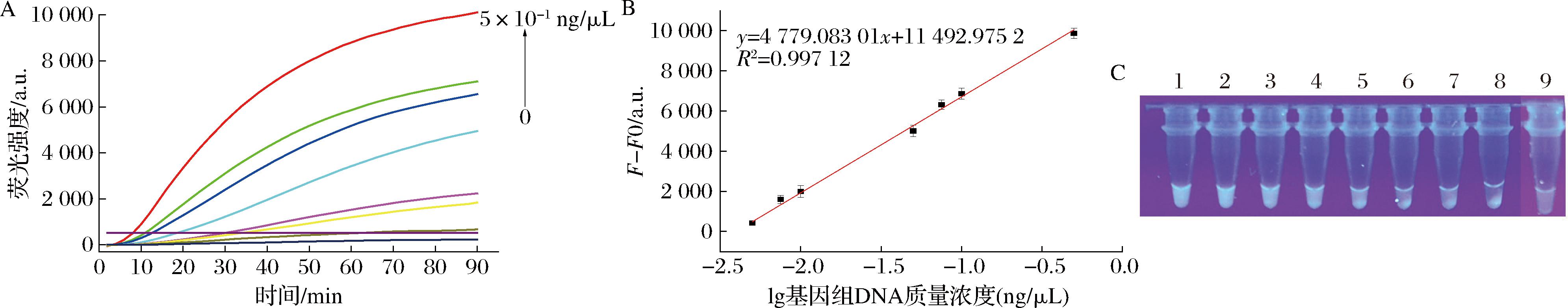
A-基于滚环扩增的双模态信号输出生物传感器在不同微生物基因组DNA浓度下的荧光发射光谱; B-基于滚环扩增的双模态信号输出生物传感器的标准曲线;C-紫外线灯照射下信号响应的可视化方式的灵敏度
图3 基于滚环扩增的双模态信号输出生物传感器的灵敏度
Fig.3 Sensitivity of the RCA-based bi-modality signal output biosensor
注:C图中1~9分别代表基因组DNA添加量为5×10-1、1×10-1、7.5×10-2、5×10-2、1×10-2、7.5×10-3、5×10-3、1×10-3、0 ng/μL。
为了评价该方法紫外灯照射可视化信号输出模式的敏感性,在优化的实验条件下对E.coli O157:H7基因组DNA的一系列浓度进行了分析。结果如图3-C显示,随着基因组DNA的质量浓度从7.5×10-1~5×10-3 ng/μL逐渐降低,样品的荧光强度也逐渐变弱。当基因组DNA浓度降低到7.5×10-3 ng/μL以下时,肉眼将无法分辨与阴性对照的颜色变化。因此,紫外灯照射可视化信号输出模式检测基因组DNA的定性检测限为7.5×10-3 ng/μL。
将本研究建立的检测方法灵敏度与其他相似的分析方法相比较,如表2所示,本研究的灵敏度与文献报道的其他相似的检测方法的LOD相媲美,本文建立的方法可通过紫外灯照射可视化信号输出模式的定性现场检测和通过实时定量荧光信号输出模式定量实验室检测,并且有较宽的线性检测范围(5×10-3~5×10-1 ng/μL微生物基因组DNA)。
表2 建立的方法与其他检测方法的比较
Table 2 Comparison of the established method with other detection methods
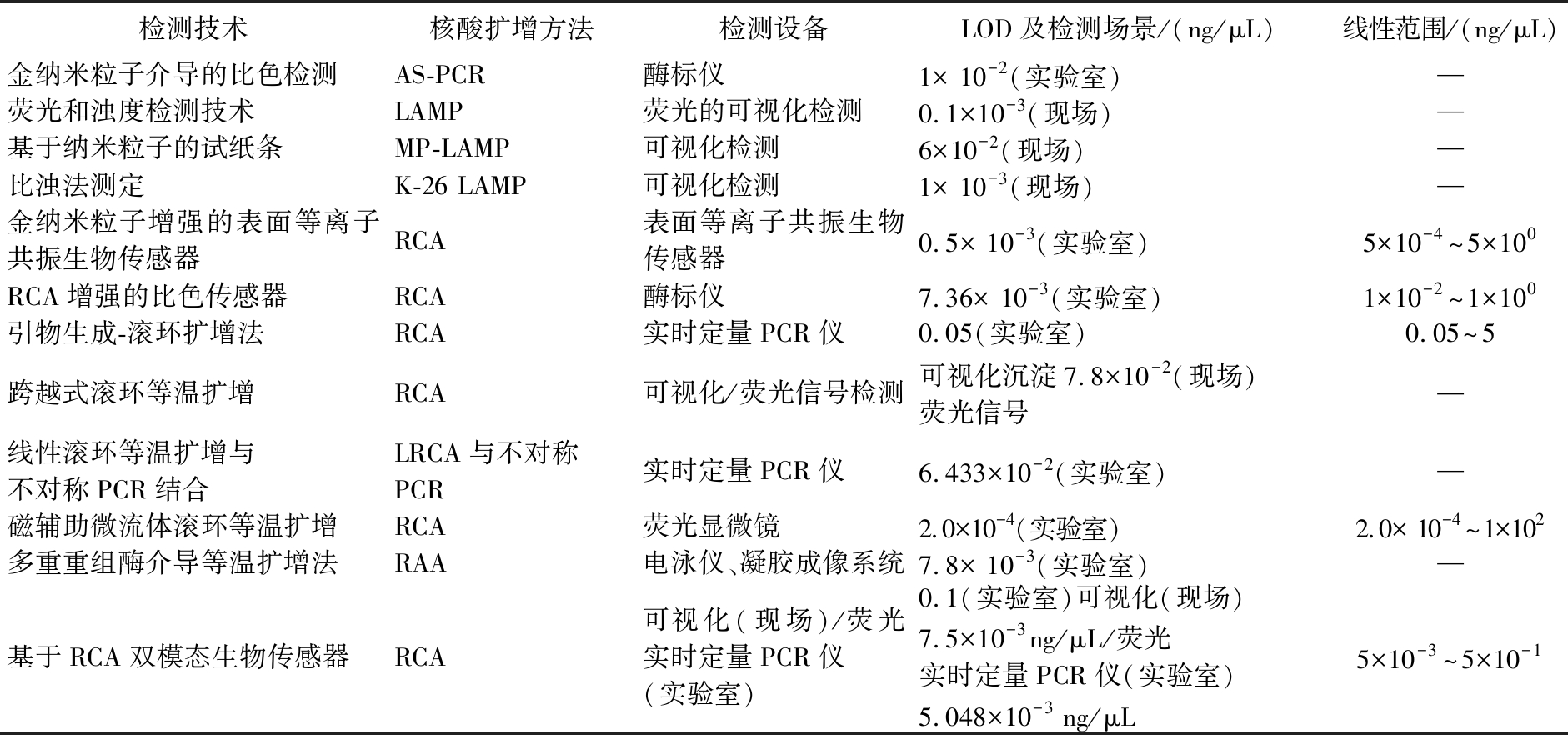
注:AS-PCR(不对称聚合酶链式反应asymmetric polymerase chain reaction);LAMP(loop-mediated amplification);MP-LAMP(肺炎支原体环介导等温扩增Mycoplasma pneumoniae-loop-mediated isothermal amplification);K-26 LAMP(杜氏利什曼原虫复合物K26抗原编码基因环介导等温扩增K26 antigen-coding gene of Leishmania donovani complex-loop-mediated isothermal amplification);RAA(重组酶辅助扩增recombinase-aid amplification)。
检测技术核酸扩增方法检测设备LOD及检测场景/(ng/μL)线性范围/(ng/μL)参考文献金纳米粒子介导的比色检测AS-PCR酶标仪1× 10-2(实验室)—[12]荧光和浊度检测技术LAMP荧光的可视化检测0.1×10-3(现场)—[13]基于纳米粒子的试纸条MP-LAMP可视化检测6×10-2(现场)—[14]比浊法测定K-26 LAMP可视化检测1× 10-3(现场)—[15]金纳米粒子增强的表面等离子共振生物传感器RCA表面等离子共振生物传感器0.5× 10-3(实验室)5×10-4^5×100[8]RCA增强的比色传感器RCA酶标仪7.36× 10-3(实验室)1×10-2^1×100[10]引物生成-滚环扩增法RCA实时定量PCR仪0.05(实验室)0.05^5[5]跨越式滚环等温扩增RCA可视化/荧光信号检测可视化沉淀7.8×10-2(现场)荧光信号—[16]线性滚环等温扩增与不对称PCR结合LRCA与不对称PCR实时定量PCR仪6.433×10-2(实验室)—[17]磁辅助微流体滚环等温扩增RCA荧光显微镜2.0×10-4(实验室)2.0× 10-4^1×102[18]多重重组酶介导等温扩增法RAA电泳仪、凝胶成像系统7.8× 10-3(实验室)—[19]基于RCA双模态生物传感器RCA可视化(现场)/荧光实时定量PCR仪(实验室)0.1(实验室)可视化(现场)7.5×10-3ng/μL/荧光实时定量PCR仪(实验室)5.048×10-3 ng/μL5×10-3^5×10-1本研究
2.5 基于滚环扩增的双模态信号输出生物传感器的特异性
为了考察该检测方法对于细菌基因组的特异性识别能力,本研究选择大肠埃希氏菌O157:H7(图4-A-A和图4-B-1)、大肠埃希氏菌(图4-B-2)、金黄色葡萄球菌(图4-B-3)、表皮葡萄球菌(图4-B-4)、腐生葡萄球菌(图4-B-5)、铜绿假单胞菌(图4-B-6)、单增李斯特菌(图4-B-7)和以上菌的混合菌(图4-A-B和图4-B-8)进行特异性检测,结果如图4所示,该方法可实现不与非O157:H7大肠埃希氏菌同属间和种属间的金黄色葡萄球菌、表皮葡萄球菌、腐生葡萄球菌、铜绿假单胞菌、单增李斯特菌发生交叉反应,该结果表明本文建立的方法具有良好的特异性。
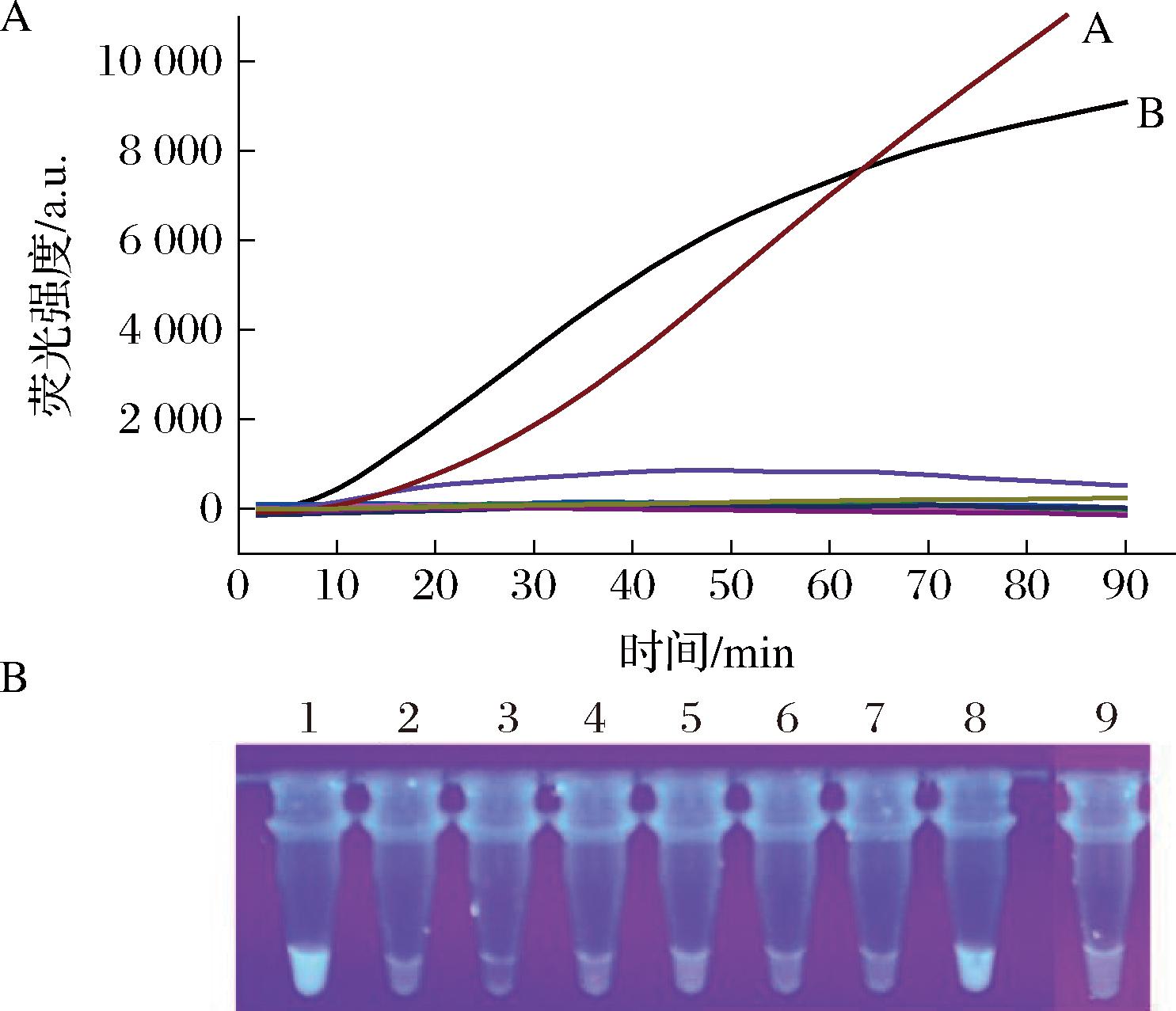
A-实时定量荧光输出模式的特异性;B-紫外线灯照射下信号响应输出模式的特异性
图4 基于滚环扩增的双模态信号输出生物传感器的特异性
Fig.4 Specificity of the RCA-based bi-modality signal output biosensor
注:B图中1~9分别代表大肠埃希氏菌O157:H7、大肠埃希氏菌、 金黄色葡萄球菌、表皮葡萄球菌、腐生葡萄球菌、铜绿假单胞菌、 单增李斯特菌、以上7种菌的混合液、阴性对照组。
2.6 食品样品的分析
为验证该分析方法在食品样品中检测细菌基因组DNA的实用性,利用所开发的方法和GB 4789.36—
2016《食品安全国家标准 食品微生物学检验 大肠埃希氏菌O157:H7/NM检验》第一法 常规培养法对人工污染大肠埃希氏菌O157:H7的牛奶样品和鸡肉样品进行分析,结果如表3所示,人工污染的牛奶和鸡肉样品的实时定量荧光信号为(6 246.33±288.41) a.u.和(9 313±332) a.u.,与阴性对照[(199±17.78) a.u.和(209±15.10) a.u.]有极显著性差异(P<0.01),新建立方法的实时定量荧光信号输出模式的检测结果和借助紫外灯输出可视化信号输出模式的检测结果均与GB 4789.36—2016《食品安全国家标准 食品微生物学检验 大肠埃希氏菌O157:H7/NM检验》第一法有良好的一致性。
表3 检测食品样品
Table 3 Analysis of food samples (n=3)

样品样品种类检测结果实时定量荧光信号(发射波长520 nm)/a.u.紫外可视化信号GB 4789.36—2016《食品安全国家标准 食品微生物学检验大肠埃希氏菌O157:H7/NM检验》牛奶样品 样品 199±17.78阴性阴性人工污染样品6 246.33±288.41阳性阳性鸡胸肉样品样品 209±15.10阴性阴性人工污染样品9 313±332阳性阳性
3 结论
本文针对大肠埃希氏菌O157:H7构建了一种基于滚环扩增的双模态信号输出生物传感器,既可在实验室通过实时定量荧光变化实现实时定量的信号监测,也可在现场利用紫外灯照射下实现定性的信号可视化输出。该方法具有实时定量输出模式下较宽的分析范围(5×10-3~5×10-1 ng/μL微生物基因组DNA)和高的灵敏度(现场可视化模式7.5×10-3ng/μL 和实验室荧光实时定量PCR输出模式5.048×10-3 ng/μL微生物基因组DNA)。该方法不与非O157:H7大肠埃希氏菌同属间和种属间的金黄色葡萄球菌、表皮葡萄球菌、腐生葡萄球菌、铜绿假单胞菌、单增李斯特菌发生交叉反应,特异性良好。该检测方法对人工污染食品样品进行检测,验证了其潜在应用价值。该双模态检测技术在食品中大肠埃希氏菌O157:H7的检测方面具有良好的实用性和明显的优势。
[1] KADARIYA J, SMITH T C, THAPALIYA D.Staphylococcus aureus and staphylococcal food-borne disease:An ongoing challenge in public health[J].BioMed Research International, 2014, 2014(1):827965.
[2] LI Y, LIU H M, HUANG H, et al.A sensitive electrochemical strategy via multiple amplification reactions for the detection of E.coli O157:H7[J].Biosensors &Bioelectronics,2020,147:111752.
[3] LIN M W, QUINTELA I A, WU V C H, et al.Review of recent advances in aptasensor for the detection of pathogenic Escherichia coli O157:H7[J].Journal of Food Safety, 2025, 45(3):e70017.
[4] MOHSEN M G, KOOL E T.The discovery of rolling circle amplification and rolling circle transcription[J].Accounts of Chemical Research, 2016, 49(11):2540-2550.
[5] JANG E J, KIM T Y, LIM J A, et al.Primer generation-rolling circle amplification method optimized for the detection of pathogenic bacteria[J].Biotechnology and Bioprocess Engineering, 2024, 29(5):890-901.
[6] LONG Y, ZHOU X M, XING D.Sensitive and isothermal electrochemiluminescence gene-sensing of Listeria monocytogenes with hyperbranching rolling circle amplification technology[J].Biosensors and Bioelectronics, 2011, 26(6):2897-2904.
[7] RUSSELL C, WELCH K, JARVIUS J, et al.Gold nanowire based electrical DNA detection using rolling circle amplification[J].ACS Nano, 2014, 8(2):1147-1153.
[8] SHI D C, HUANG J F, CHUAI Z R, et al.Isothermal and rapid detection of pathogenic microorganisms using a nano-rolling circle amplification-surface plasmon resonance biosensor[J].Biosensors &Bioelectronics, 2014, 62:280-287.
[9] YAO C Y, XIANG Y, DENG K, et al.Sensitive and specific HBV genomic DNA detection using RCA-based QCM biosensor[J].Sensors and Actuators B:Chemical, 2013, 181:382-387.
[10] LI Y N, WANG J Y, WANG S, et al.Rolling circle amplification based colorimetric determination of Staphylococcus aureus[J].Microchimica Acta, 2020, 187(2):119.
[11] KUMAR Y.Isothermal amplification-based methods for assessment of microbiological safety and authenticity of meat and meat products[J].Food Control,2021, 121:107679.
[12] DENG H, ZHANG X, KUMAR A, et al.Long genomic DNA amplicons adsorption onto unmodified gold nanoparticles for colorimetric detection of Bacillus anthracis[J].Chemical Communications, 2013,49(1):51-53.
[13] YAO X F, LI P F, XU J H, et al.Rapid and sensitive detection of Didymella bryoniae by visual loop-mediated isothermal amplification assay[J].Frontiers in Microbiology, 2016,7:1372.
[14] WANG Y C, WANG Y, JIAO W W, et al.Development of loop-mediated isothermal amplification coupled with nanoparticle-based lateral flow biosensor assay for Mycoplasma pneumoniae detection[J].AMB Express, 2019,9(1):196
[15] DE AVELAR D M, CARVALHO D M, RABELLO A.Development and clinical evaluation of loop-mediated isothermal amplification (LAMP) assay for the diagnosis of human visceral leishmaniasis in Brazil[J].BioMed Research International, 2019, 2019(1):8240784.
[16] YANG Q, ZHANG Y Z, LI S, et al.Saltatory rolling circle amplification for sensitive visual detection of Staphylococcus aureus in milk[J].Journal of Dairy Science, 2019, 102(11):9702-9710.
[17] 谭雅冰.滚环扩增技术对中华绒螯蟹“牛奶病”病原二尖梅奇酵母的检测研究[D].沈阳:沈阳农业大学,2024.TAN Y B.Detection of Mycelia bicuspidata, the pathogen of “milk disease” in Eriocheir sinensis by rolling circle amplification technique[D].Shenyang:Shenyang Agricultural University, 2024.
[18] KUMARI S, KUMAR M, RAMESH S, et al.A simple magnetic-aided microfluidic screening approach for rabies virus via rolling circle amplification[J].Microchemical Journal, 2025, 208:112345.
[19] 秦爱,李根容,邓方进,等.多重重组酶介导等温扩增技术检测食品中3种食源性致病菌[J].食品安全质量检测学报,2024,15(5):97-104.QIN A, LI G R, DENG F J, et al.Determination of 3 kinds of foodborne pathogens in food by multiplex recombinase aided amplification technology[J].Journal of Food Safety &Quality, 2024, 15(5):97-104.