食源性致病菌感染是全球公共卫生面临的重大挑战,会引发消费者多种疾病,严重威胁人类生命健康。食源性致病菌在食品加工等过程中面临亚致死应激时会进入活的不可培养(viable but nonculturable,VBNC)状态,这种休眠状态有助于细菌在复杂多变的环境中生存,从而避免在应激条件下完全死亡[1]。这可能是食源性致病菌的一种生存策略,使细菌在不利环境下能够保持一定的生存能力,等待适宜条件到来时再恢复生长并繁殖,完成复苏[2]。
细菌VBNC状态的复苏是指细菌从一种特殊的、难以检测和培养的生存状态,通过特定的机制和条件,转变为能够被常规培养方法检测到并正常生长繁殖的过程[3]。对该过程的深入了解有助于解释细菌在自然环境中的生存方式、其与人类健康和环境的关系。VBNC细菌是目前研究的热点领域之一,多数研究集中于诱导后表型及诱导机制,对VBNC细菌复苏的相关研究尚存在许多争议。有研究表明可以通过解除环境中的压力因素使VBNC细菌复苏[4],然而也有研究表明VBNC细菌复苏并不是一个简单的逆过程,往往在特殊的条件才能复苏[5]。触发VBNC细菌复苏的条件主要是环境因素的改变,也涉及细菌内部生理机制的调整,且VBNC细菌呈现周期性方式复苏,并非任意时刻都能实现复苏[6]。综上,VBNC复苏效果因细菌个体差异而异,不同个体生理状态、基因表达及所处微环境不同,都会影响复苏进程与结果。
1 VBNC细菌的危害
在传统的微生物学研究中,人们将细菌的可培养性判定为细菌存活的金标准。然而,近年研究发现,食源性致病菌在环境胁迫下,会进入一种特殊的生理状态,即VBNC状态[7]。该状态下细菌虽保有基础代谢活性,却无法在常规培养基上生长形成可见菌落,导致检测时出现假阴性结果。此类状态的细菌可长期存留于食品加工链及供水系统中,且对常规抗生素耐药,也可能导致慢性感染或复发。同时,由VBNC细菌引起的公共安全事件也层出不穷。据报道,日本发生了一系列由VBNC大肠杆菌污染的盐渍鲑鱼子引起的食物中毒事件[8];鱿鱼干燥时,肠道沙门氏菌受NaCl胁迫可能进入VBNC状态,进而引发了日本又一次食源性疾病爆发[9];阿根廷也曾在霍乱流行期间检出VBNC态霍乱弧菌,这些均构成重大公共卫生威胁[10]。
然而,由于不同细菌的生物学特性不同、环境诱导因素及其与宿主互作模式也存在显著差异,食源性致病菌VBNC状态的危害在相关领域引发了诸多讨论。一方面,部分研究为其潜在危害性提供了直接证据:实验显示处于VBNC状态的痢疾志贺氏菌仍具致病性[11];副溶血性弧菌、溶藻弧菌在VBNC状态下仍可复苏并保留毒力特征,传代后毒力可恢复[12];大肠杆菌在VBNC状态下保留毒力[13]。另一方面,多项研究对VBNC状态的致病力提出质疑:FORSMAN等[14]发现,VBNC土拉弗朗西斯菌无法引发小鼠免疫反应且无存活菌体;CAPPELIER等[15]和LINDB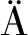 CK等[16]证实,VBNC单核细胞增生李斯特菌在动物模型和细胞实验中均无毒性;LOTHIGIUS等[17]发现水环境诱导的VBNC产肠毒素大肠杆菌丧失肠毒素合成能力。这些研究表明,VBNC细菌的危害具有不确定性与复杂性,诱导条件和细菌之间的差异决定了VBNC状态的病原体是致病力还是非致病力。
CK等[16]证实,VBNC单核细胞增生李斯特菌在动物模型和细胞实验中均无毒性;LOTHIGIUS等[17]发现水环境诱导的VBNC产肠毒素大肠杆菌丧失肠毒素合成能力。这些研究表明,VBNC细菌的危害具有不确定性与复杂性,诱导条件和细菌之间的差异决定了VBNC状态的病原体是致病力还是非致病力。
2 促使VBNC细菌复苏的因素
VBNC状态是细菌应对不利条件的一种生存策略,当环境变得适宜时,VBNC细菌可以复苏,重新恢复生长和繁殖能力。复苏是指细菌从VBNC状态转变为可培养状态的过程[18]。目前,VBNC细菌的复苏方法主要是去除初始诱导条件,如恢复温度、补充营养和调节pH。然而,VBNC细菌的复苏过程并非简单的逆反应,而是受到多种因素共同调控的复杂过程[19]。在实际的食品加工、贮存与运输的过程中,由于不同的环境因素诱导食源性致病菌进入VBNC状态的机制不同,从而导致VBNC细菌所需的复苏条件的差异。表1是对VBNC细菌诱导及复苏条件的总结。
表1 促进 VBNC 细菌复苏过程的条件
Table 1 Conditions that facilitate the resuscitation of VBNC bacteria
2.1 物理因素
近年研究揭示了多种物理因素对VBNC细菌复苏的调控作用。其中,温度在VBNC细菌复苏过程中起着重要调控作用。在复苏过程中,将温度恢复至生理适宜范围可有效诱导低温胁迫下进入VBNC状态的细菌复苏。例如,金黄色葡萄球菌(从4 ℃到37 ℃)、副溶血性弧菌(从4 ℃到25 ℃)、创伤弧菌(从4 ℃到23 ℃)在低温下进入VBNC,升高温度可使VBNC细菌复苏[20-22]。这些温度变化可能通过调节基因表达和促进蛋白质合成来恢复细菌活性。此外,其他物理因素如氧气浓度、渗透压、超声波和光照等,同样在细菌复苏过程中发挥着关键作用。这些复苏条件通常是根据初始诱导条件(如低温、饥饿、氧化应激等)来选择,从而实现VBNC细菌的高效复苏。
2.2 化学因素
仅通过消除初始胁迫条件的物理因素(如温度)往往难以实现理想的复苏效果,需加入化学物质协同作用完全恢复细菌的可培养性[35-36]。化学因素在调控VBNC状态细菌复苏中扮演关键角色。复苏过程中,常添加的化学物质包括营养物质(氨基酸、维生素、糖、脂肪酸等)、抗氧化剂(丙酮酸钠、KatG等)、复苏因子(Rpf、YeaZ、AI-2等)、表面活性剂(Tween 80)等。具体而言,营养物质与适宜温度(37 ℃)的协同作用为VBNC细菌提供了代谢重建的微环境[37]。在营养物质不足以打破休眠状态时,添加Rpf有利于实现VBNC细菌的复苏[38]。特别是在营养成分改变、生长速率降低的培养基中进入VBNC状态的细菌,此时Rpf在其复苏过程中发挥作用。类似地,YeaZ作为Rpf的类似蛋白,也能有效促进VBNC细菌复苏。另外,一些抗氧化剂也能有效复苏VBNC细菌。例如,在适宜温度(25~37 ℃)下添加丙酮酸钠、KatG等化学物质可以有效复苏VBNC细菌[27,39]。并且,一些蛋白酶可与KatG形成功能互补,提高复苏效率[4,40]。上述研究表明,化学复苏依赖于代谢底物供给、氧化应激缓解及信号通路激活的协同,但不同细菌对化学刺激的响应存在特异。
2.3 生物因素
除了向培养基中添加外源性化学复苏因子外,将VBNC细菌与可分泌化学复苏因子的细菌共培养也能达到复苏的效果[3,31,41]。这些细菌作为宿主与VBNC细菌共培养,宿主分泌的复苏信号分子可以促进细菌复苏。宿主环境是VBNC细菌复苏的天然庇护所[37]。此外,VBNC细菌还能与真核生物共培养实现复苏。研究发现,VBNC幽门螺杆菌与变形虫共培养48 h后形态恢复且可培养性显著提升[28];进一步通过小鼠感染实验证明,VBNC幽门螺杆菌在小鼠体内也能复苏[29]。这些研究主要强调生物因素通过调控微环境来驱动VBNC细菌复苏。
3 细菌复苏的机制
3.1 主动复苏
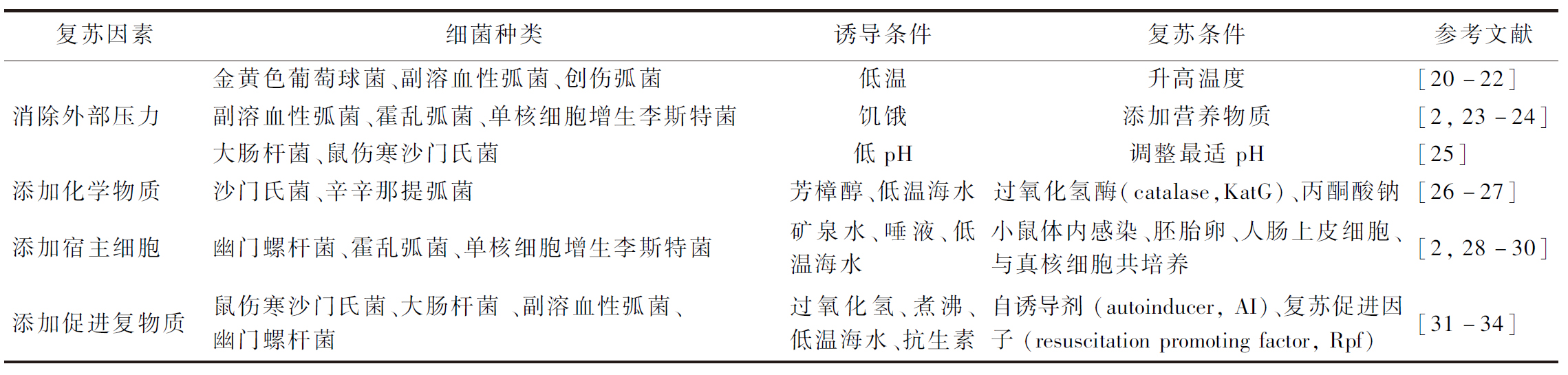
主动复苏机制里,细菌内部的信号调控与代谢恢复极为关键。图1揭示了细菌群体感应与复苏促进因子的复苏机制。
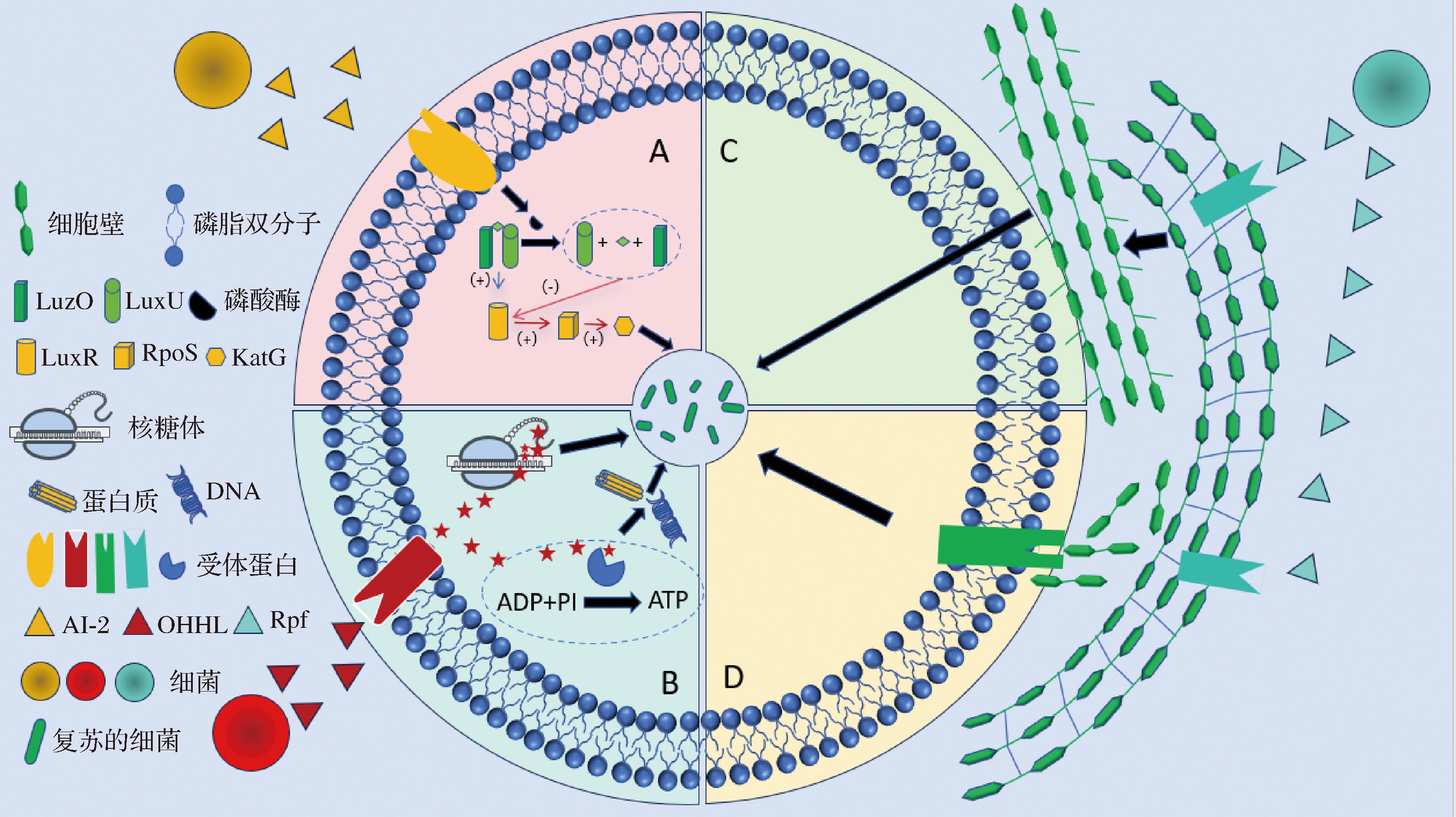
图1 由AI-2介导的复苏(A)、OHHL介导的复苏(B)和Rpf介导的复苏(C)、(D)[3,41]
Fig.1 AI-2-mediated resuscitation (A), OHHL-mediated resuscitation (B), and Rpf-mediated resuscitation (C) and (D)[3,41]
注:发光调节蛋白(luminescence regulatory protein,LuxO);磷酸转移酶(phosphotransferase,LuxU);自诱导物响应转录调节因子(autoinducer responsive transcriptional regulator,LuxR);RNA聚合酶因子(RNA polymerase sigma factor S,RpoS);N-3-氧代-己酰-L-高丝氨酸内酯[N-(3-oxohexanoyl)-L-homoserine lactone,OHHL]。
3.1.1 群体感应
细菌群体感应(quorum sensing,QS)作为种内与种间通讯的核心机制,通过动态调控信号分子的合成与感知,协调VBNC细菌的复苏进程[42]。QS产生的信号分子被称为AI,主要包括酰基-高丝氨酸内酯(N-acyl-homoserine lactones,AHLs)型信号、短寡肽(autoinducing peptides,AIPs)型信号和AI-2。通常,这些信号分子以低细菌浓度持续产生,在环境中的积累浓度达到阈值后,该信号将与其受体蛋白相互作用,导致细菌基因表达发生协调变化,重塑细胞生理状态[3]。有研究表明,QS系统可触发KatG的表达,以复苏VBNC细菌[31]。进一步研究发现,AI-2介导的复苏过程依赖于周质结合蛋白(periplasmic binding protein,LuxP)和双组分传感器激酶(two component sensor kinase,LuxQ)受体系统的精密调控[41-42]。当胞外AI-2浓度显著升高时,LuxP/Q蛋白二聚体通过特异性结合AI-2分子激活其磷酸酶活性。该酶通过去磷酸化作用阻断LuxO和LuxU的信号传导链,导致LuxR表达水平下调。值得注意的是,LuxR作为RpoS的反向调控元件,其表达抑制将引发RpoS蛋白的显著累积。RpoS的激活进一步驱动KatG等抗氧化蛋白的合成,有效清除胞内活性氧,修复氧化损伤的细胞结构(如DNA与膜系统),最终恢复细胞的代谢活性与可培养性。此通路揭示了VBNC细菌复苏过程中QS系统参与KatG的激活过程。另外,VBNC细菌代谢降低,通过重启能量代谢解除休眠状态是关键。OHHL属于AHLs的一种,是革兰氏阴性菌群体感应的核心信号分子,与AI-2等其他自诱导剂共同协调细菌的群体行为[43]。OHHL的复苏功能则通过蛋白调节因子(opacity regulator,OpaR)转录调控因子的构象重编程实现[44]。OHHL分子通过氢键网络与疏水作用力与OpaR蛋白形成稳定复合物,诱导其空间构象变化,进而激活两类关键生理程序。一方面,OHHL-OpaR复合物直接结合至ATP合酶基因启动子区,显著提升该酶的表达水平。ATP合酶的富集驱动氧化磷酸化过程,使胞内ATP库迅速恢复,为DNA复制、翻译等基础代谢活动提供能量保障。另一方面,OpaR可特异性抑制毒素-抗毒素系统中毒素蛋白的表达,解除其对核糖体功能与细胞分裂的抑制作用。这种双重调控策略不仅重启能量代谢,更通过解除生长抑制信号实现细胞周期再激活。
3.1.2 Rpf
Rpf是一类由特定细菌分泌的胞外溶菌酶样蛋白,其通过靶向调控细胞壁重塑与信号转导,可促进非生长或休眠细胞的复苏和生长[45]。Rpf在许多研究中都表现出了良好的复苏效果。类似的蛋白质广泛存在于许多革兰氏阳性细菌中。Rpf可与复苏促进因子相互作用蛋白(resuscitation promoting factor interacting protein,Rip A)的蛋白质形成复合物,VBNC细菌复苏依赖于复合物对肽聚糖(peptidoglycan,PG)的水解[46]。有研究表明,在该复合物中,Rpf裂解N-乙酰胞壁酸和N-乙酰基-D-葡糖胺之间的β-1,4-糖苷键,而Rip A是一种裂解多肽的内肽酶。2种蛋白质在分裂细胞的隔膜处共定位,并产生协同作用以水解分枝杆菌PG。这种类型的细胞壁水解会直接刺激VBNC细菌复苏,因为PG的肽部分在VBNC状态下被严重交联以抵抗外部压力[3]。除此之外,另外一些研究则聚焦于Rpf-Rip复合物介导的化学生物信号传递[47]。当Rpf-Rip复合物水解PG产生游离多肽片段时,这些片段可作为扩散性信号分子与VBNC细菌膜表面的丝氨酸/苏氨酸蛋白激酶(protein kinase B,PknB)特异性结合,促进细胞生长[3]。
3.2 被动复苏
低温、寡营养、紫外线照射等不利条件均可诱导细菌进入VBNC状态,相对应地,通过提高培养温度、添加某些营养物质、添加自由基清除剂、与宿主细胞共培养等方法去除环境诱导因子可以实现VBNC状态细菌的复苏,如图2所示。
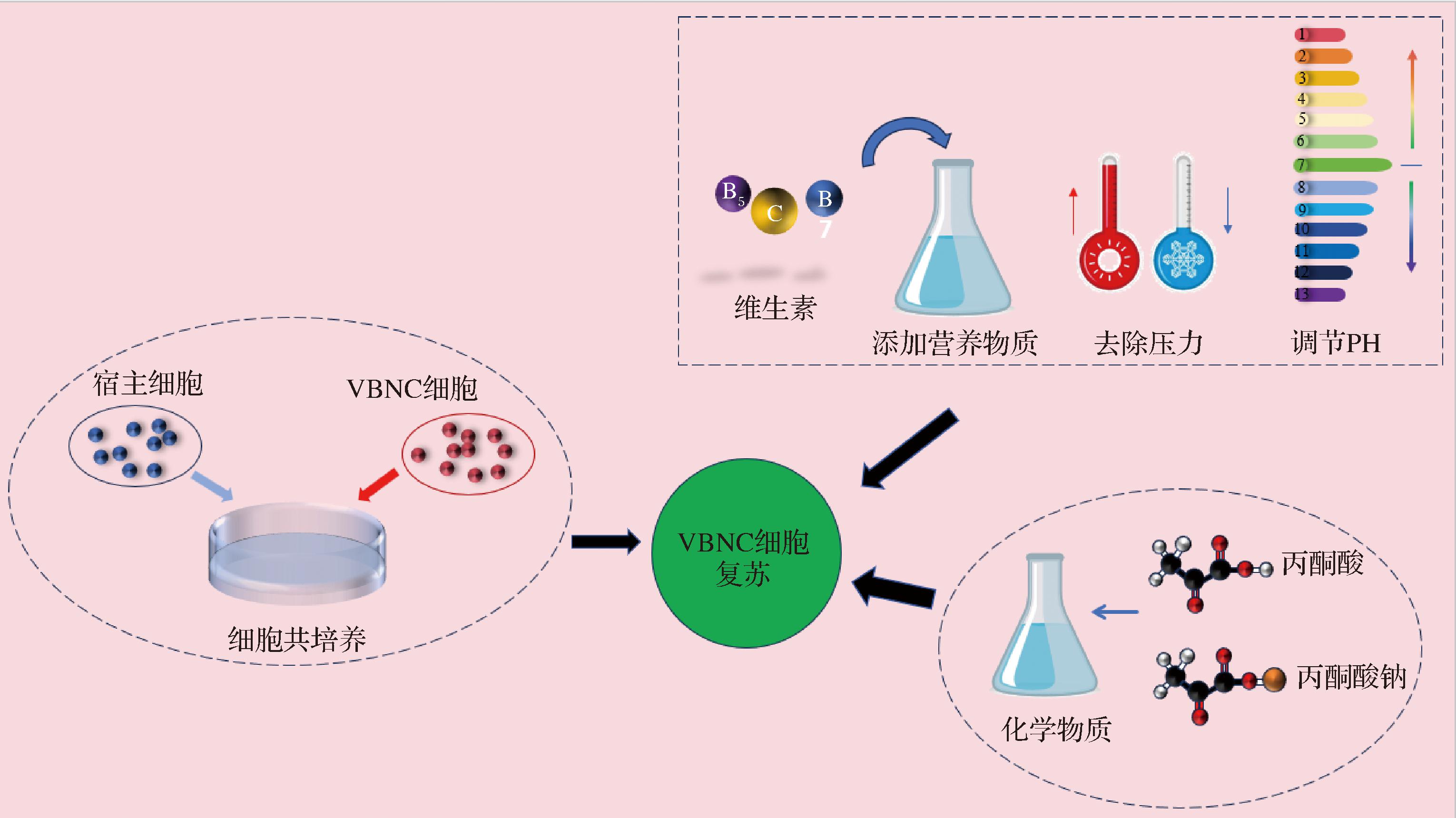
图2 改善培养环境、添加营养物质和化学物质促使VBNC细菌复苏
Fig.2 Improving the culture environment and adding nutrients and chemicals to promote the revival of VBNC bacteria
3.2.1 补充营养物质
营养物质为细胞的生命活动提供基础支持,通过分解代谢将碳水化合物、脂肪等有机物转化为ATP,驱动细胞分裂、物质运输等生理过程,如图3所示。有研究表明,VBNC细菌中的ATP是驱动复苏过程的主要能量来源[48]。通过去除诱导因素,补充营养物质,在适宜的条件下培养,VBNC细菌中残留的ATP可激活Preiss-Handler和挽救途径合成烟酰胺腺嘌呤二核苷酸(Nicotinamide adenine dinucleotide,NAD+),从而提高细胞代谢活性,促进复苏[49-50]。因此,补充营养物质是使VBNC细菌复苏的重要手段。
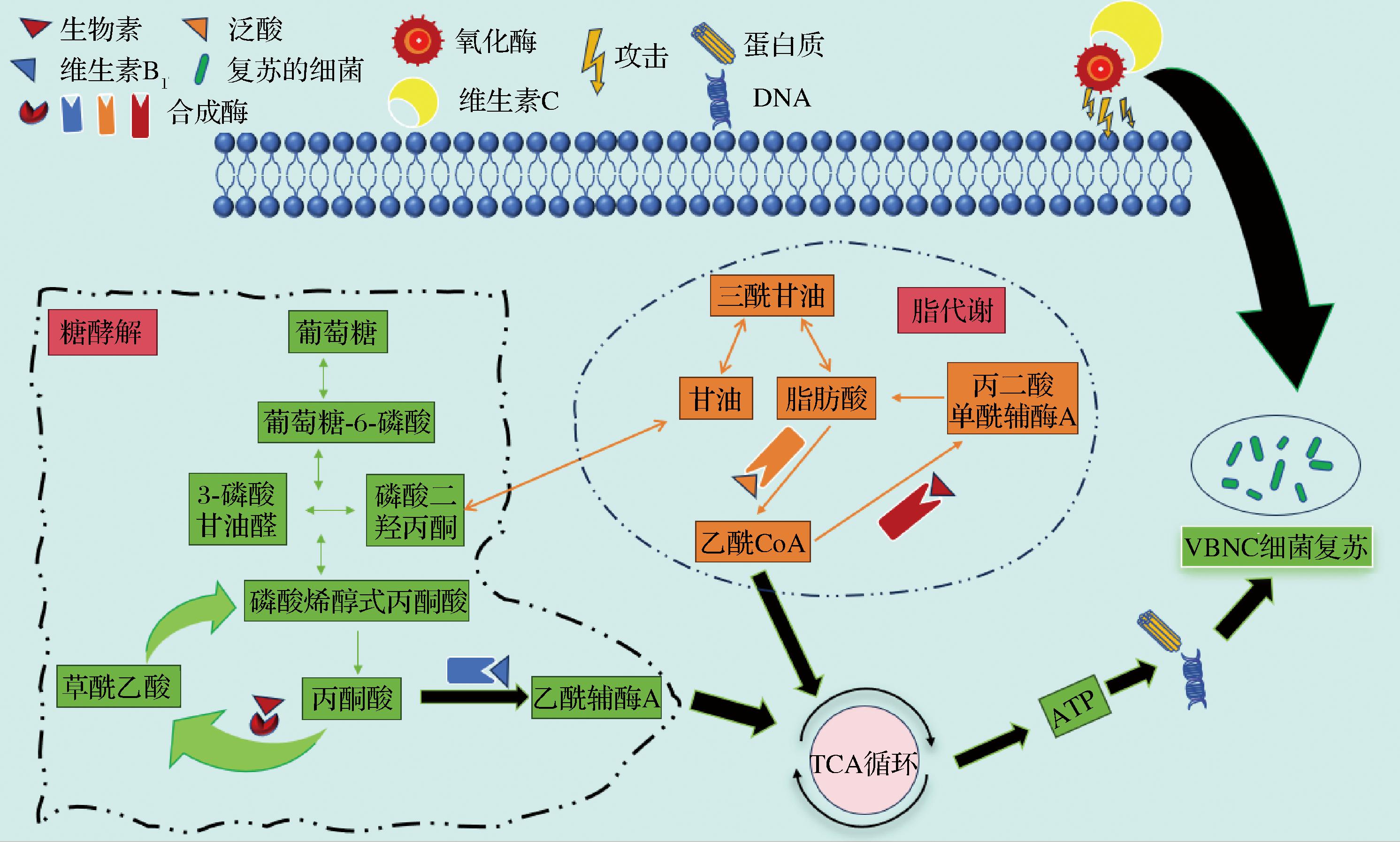
图3 营养物质通过TCA循环和修复细胞膜驱动VBNC细菌复苏
Fig.3 Nutrients drive the recovery of VBNC bacteria through TCA circulation and cell membrane repair
维生素等关键营养物质通过激活糖异生和三羧酸(tricarboxylic acid,TCA)循环中的核心酶或辅酶系统,协同恢复VBNC细菌的能量代谢稳态[51]。具体而言,维生素B1可转化为硫胺素焦磷酸,参与丙酮酸脱氢酶复合体形成,催化丙酮酸转化为乙酰辅酶A。泛酸是合成辅酶A的关键成分,而辅酶A是细菌代谢的核心辅因子,泛酸通过合成辅酶A促进脂肪酸分解和乙酰-辅酶A生成,重启TCA循环以产生ATP及中间代谢产物[52];同时,辅酶A还参与细胞内的脂质代谢平衡,补充泛酸可能促进肽聚糖层的修复,恢复细胞壁完整性[53]。生物素作为羧化酶辅酶,在VBNC细菌的复苏中主要起到2个关键作用。首先,生物素可通过激活丙酮酸羧化酶增强糖异生能力,为TCA循环补充碳骨架并联动提升ATP合成效率,其次,还可通过激活乙酰-辅酶A羧化酶催化乙酰-辅酶A生成丙二酸单酰-辅酶A,恢复细胞膜脂质合成能力,从而修复VBNC状态下受损的膜结构[54]。另外,VBNC状态的形成常与氧化应激有关。维生素C作为强还原剂,可能通过中和细菌周围的活性氧,减轻氧化损伤,恢复细菌的代谢活性[55]。
总体来说,补充营养物质主要是通过增强糖代谢、脂代谢和TCA循环通路为修复细胞提供能量物质,从而逆转和改善VBNC细菌的低代谢停滞状态和细胞功能,最终重建能量供应网络以满足复苏所需的生物合成与基础代谢需求。
3.2.2 添加抗氧化剂
自由基对细菌细胞具有很强的损伤作用,会破坏细胞膜、蛋白质和核酸等生物大分子,导致细胞生理功能受损,这是细菌进入VBNC状态的重要原因之一。丙酮酸是重要的化学复苏试剂,丙酮酸不仅是糖酵解途径中重要的产物,而且还是重要的自由基清除剂,既可以进入TCA循环,也可减少活性氧对细胞的损伤。一方面,丙酮酸转化为乙酰-辅酶A,进入TCA循环,加速ATP合成,为细胞提供能量,增强了细胞的能量代谢,使细菌能够获得足够的能量来启动复苏过程[56]。
另一方面,丙酮酸钠作为自由基清除剂,直接中和过氧化氢等活性氧,阻断氧化损伤链式反应。减少自由基损伤后,细胞膜的完整性得以恢复,膜上的离子通道、转运蛋白等功能恢复正常,保证细胞内外物质的正常交换[57]。
3.2.3 与宿主细胞共培养
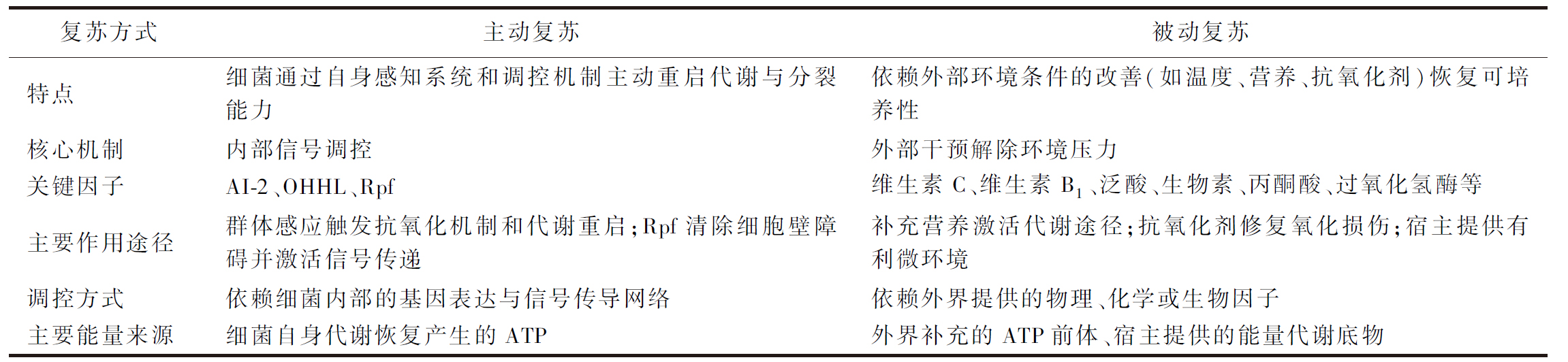
VBNC细菌复苏涉及多种因素和机制,根据复苏过程中驱动力的差异,复苏方式可分为主动复苏与被动复苏,具体比较见表2。其中,环境条件的改变是VBNC细菌复苏的关键因素[41]。宿主细胞可能通过自身代谢活动调节环境的酸碱度、渗透压等,使环境更适宜细菌生长,还为VBNC细菌提供能量和物质基础,促进细菌恢复生长和代谢活性[58]。并且,宿主细胞能分泌一些细胞因子和信号分子,这些信号分子与细菌表面受体结合,启动复苏相关基因的表达,激活细菌内部特定的信号通路,促使细菌从休眠状态苏醒,恢复可培养性[4]。
表2 主动复苏与被动复苏的比较
Table 2 Comparison of active and passive resuscitation
4 细菌复苏后的生理特性
4.1 复苏过程中细胞的形态变化
当细菌进入VBNC状态时,会通过显著缩小细胞表面积降低能量消耗[59]。复苏后的细胞与正常状态的细胞形态和大小相似,细胞结构完整,细胞长度增加,恢复至饱满杆状,细胞内容物致密均匀、充盈,整体形态圆润无皱缩[60-63]。这种形态改变具有可逆性特征,当移除环境胁迫并提供适宜复苏条件时,细菌能够恢复到正常的形态。这表明,应激因子的去除为细菌复苏创造了有利条件,使得细胞能够逐步恢复到较为正常的生理形态。这些研究揭示了VBNC细菌的形态调控策略,实现从生存模式向生长模式的转变。
4.2 复苏过程中细胞的代谢状态变化
在细菌的形态变化过程中,VBNC细菌的代谢功能也会发生变化。范佳慧[63]的研究显示,细菌在胁迫时呼吸活性显著降低,复苏时逐步恢复。此呼吸活性变化影响能量变化。胁迫初期细菌增加ATP,随胁迫持续ATP水平下降并进入VBNC状态,复苏后细菌可恢复能量平衡状态,使ATP浓度恢复至胁迫前。这种能量变化与糖原等储能物质的动态变化密切相关。作为重要的胞内储备聚合物,糖原在细菌进入VBNC状态过程中持续降解,而在复苏后又能迅速回升至对数期水平[64-65]。进一步从酶活性角度研究发现,VBNC细菌在复苏过程中,部分酶的活性会显著增强[5, 66]。这一现象暗示着细菌代谢活性的增强,从另一个层面证实了VBNC细菌复苏后代谢功能的改变。研究者从蛋白质组学层面进行深入研究,进一步证实了复苏细胞代谢活性显著提升,许多蛋白表达全面上调,涉及蛋白质合成、分泌系统、跨膜转运、黏附、运动和其他重要过程[67]。这些发现共同揭示了细菌在VBNC状态转换过程中,通过调控储能物质的分解与合成来维持代谢,为其在恶劣环境中的存活和复苏提供了关键的生物学基础。
4.3 复苏后细胞的生长和功能特性
在VBNC细菌复苏过程中,代谢状态的重启为细菌的生长和功能恢复提供能源物质。细菌代谢功能的变化也影响着VBNC细菌的生长和功能特性的变化。首先,从细菌生长的角度来看,VBNC细菌复苏后可培养性与正常细胞的可培养性差异逐渐缩小,且复苏后细胞可培养菌数接近接种浓度[61,63]。甚至一些研究还观察到复苏后的VBNC细菌展现出比正常细菌更高的最大培养浓度[68]。其次,VBNC细菌复苏后的功能特性呈现出显著提升的趋势,从整体表现来看,几乎能够恢复到正常细菌的功能水平。以嗜联苯红球菌为例,其对有机污染物具备很强的降解能力。相关研究深入对比了不同接种状态下该菌种的降解效率,结果表明,复苏后细菌的石油降解率显著高于VBNC细菌,与正常细菌的石油降解率相差不大,主要取决于复苏方法[63,68-69]。此外,复苏后细菌对外界不利条件的抵抗能力和致病能力也有一定的变化。有研究发现,对低温诱导的VBNC细菌进行高温复苏后,其对紫外辐射和热激的耐受性与正常细胞相似,但对冷激的抵抗能力弱于正常细胞,对高渗透的抵抗能力高于正常细胞[60]。VBNC细菌仍保持致病潜能,伴随着复苏的实现,细菌的致病能力也得以恢复,与正常细胞一致[60-62]。
5 总结与展望
VBNC状态作为微生物应对环境胁迫的重要生存策略,近年来受到广泛关注。本综述对食源性致病菌形成VBNC状态的危害、复苏因素、复苏机制和复苏后细菌的生理特性4个方面进行总结。食源性致病菌VBNC状态在全球各地都引发了疫情,并且在适宜条件下可复苏并致病。这引起了公众对VBNC状态下的食源性致病菌在公共卫生和食品安全方面的重视。目前研究对VBNC细菌的复苏方法有物理刺激、化学刺激、活性蛋白或宿主共培养等。主要复苏方法的选取通常以初始诱导条件作为参考依据,复苏效果也因菌株的特异性存在一些差异。根据文献调研分析,绝大部分研究是将VBNC细菌添加到营养条件充足、温度适宜的培养基中,对于复苏效果不佳时,添加复苏促进因子可以提高复苏VBNC细菌的效率。复苏后,关于细胞的生理特性和对宿主的毒力侵染研究较少,一些研究表明,VBNC细菌复苏后细胞的结构形态、代谢状态、生长和功能特性都恢复到正常细胞水平。因此,针对目前食源性致病菌VBNC状态的复苏研究方向展望如下:1)未来需要加强对水体和食品中致病菌的监测,应针对高风险菌株建立VBNC风险评估模型,以精准识别并阻断潜在传播链,保障食品安全与公共健康。2)未来可开展VBNC的诱导时间与复苏时间的关系研究。3)未来需探索化学与物理联合干预策略在细菌修复与食品安全中的应用潜力,并进一步分析化学因子促进VBNC细菌复苏的分子调控机制。4)未来需加强VBNC细菌复苏后的细胞生理特性和对宿主的毒力侵染研究。
[1] ARVANITI M, OROLOGAS-STAVROU N, TSITSILONIS O E, et al.Induction into viable but non culturable state and outgrowth heterogeneity of Listeria monocytogenes is affected by stress history and type of growth[J].International Journal of Food Microbiology, 2024, 421:110786.
[2] CARVALHO F, CARREAUX A, SARTORI-RUPP A, et al.Aquatic environment drives the emergence of cell wall-deficient dormant forms in Listeria[J].Nature Communications, 2024, 15:8499.
[3] PAN H X, REN Q.Wake up! resuscitation of viable but nonculturable bacteria:Mechanism and potential application[J].Foods, 2023, 12(1):82.
[4] PROSDOCIMI E M, ARIOLI S, MAPELLI F, et al.Cell phenotype changes and oxidative stress response in Vibrio spp. induced into viable but non-culturable (VBNC) state[J].Annals of Microbiology, 2023, 73(1):1.
[5] LI X X, REN Q, SUN Z B, et al.Resuscitation promotion factor:A pronounced bacterial cytokine in propelling bacterial resuscitation[J].Microorganisms, 2024, 12(8):1528.
[6] PROGULSKE-FOX A, CHUKKAPALLI S, GETACHEW H, et al.VBNC, previously unrecognized in the life cycle of Porphyromonas gingivalis?[J].Journal of Oral Microbiology, 2022, 14(1):1952838.
[7] ZHANG Z Q, SHI Y C, CUI T L, et al.The effects and cell phenotype changes in Escherichia coli O157:H7 induced into VBNC state by l-malic acid at low temperature[J].Food Bioscience, 2024, 60:104301.
[8] MAKINO S I, KII T, ASAKURA H, et al.Does Enterohemorrhagic Escherichia coli O157∶H7 enter the viable but nonculturable state in salted salmon roe?[J].Applied and Environmental Microbiology, 2000, 66(12):5536-5539.
[9] ASAKURA H, MAKINO S I, TAKAGI T, et al.Passage in mice causes a change in the ability of Salmonella enterica serovar Oranienburg to survive NaCl osmotic stress:Resuscitation from the viable but non-culturable state[J].FEMS Microbiology Letters, 2002, 212(1):87-93.
[10] AULET O, SILVA C, FRAGA S G, et al.Detection of viable and viable nonculturable Vibrio cholerae O1 through cultures and immunofluorescence in the Tucumán rivers, Argentina[J].Revista da Sociedade Brasileira de Medicina Tropical, 2007, 40(4):385-390.
[11] RAHMAN I, SHAHAMAT M, CHOWDHURY M A, et al.Potential virulence of viable but nonculturable Shigella dysenteriae type 1[J].Applied and Environmental Microbiology, 1996, 62(1):115-120.
[12] BAFFONE W, CITTERIO B, VITTORIA E, et al.Retention of virulence in viable but non-culturable halophilic Vibrio spp[J].International Journal of Food Microbiology, 2003, 89(1):31-39.
[13] LIU Y M, WANG C, TYRRELL G, et al.Production of Shiga-like toxins in viable but nonculturable Escherichia coli O157:H7[J].Water Research, 2010, 44(3):711-718.
[14] FORSMAN M, HENNINGSON E W, LARSSON E, et al.Francisella tularensis does not manifest virulence in viable but non-culturable state[J].FEMS Microbiology Ecology, 2000, 31(3):217-224.
[15] CAPPELIER J M, BESNARD V, ROCHE S, et al.Avirulence of viable but non-culturable Listeria monocytogenes cells demonstrated by in vitro and in vivo models[J].Veterinary Research, 2005, 36(4):589-599.
[16] LINDB CK T, ROTTENBERG M E, ROCHE S M, et al.The ability to enter into an avirulent viable but non-culturable (VBNC) form is widespread among Listeria monocytogenes isolates from salmon, patients and environment[J].Veterinary Research, 2010, 41(1):8.
CK T, ROTTENBERG M E, ROCHE S M, et al.The ability to enter into an avirulent viable but non-culturable (VBNC) form is widespread among Listeria monocytogenes isolates from salmon, patients and environment[J].Veterinary Research, 2010, 41(1):8.
[17] LOTHIGIUS Å, SJÖLING Å, SVENNERHOLM A M, et al.Survival and gene expression of enterotoxigenic Escherichia coli during long-term incubation in sea water and freshwater[J].Journal of Applied Microbiology, 2010, 108(4):1441-1449.
[18] XU H S, ROBERTS N, SINGLETON F L, et al.Survival and viability of nonculturable Escherichia coli and Vibrio cholerae in the estuarine and marine environment[J].Microbial Ecology, 1982, 8(4):313-323.
[19] ZHAO Q, XU Z W, LIU X, et al.Formation and recovery of Listeria monocytogenes in viable but nonculturable state under different temperatures combined with low nutrition and high NaCl concentration[J].Food Research International, 2024, 192:114774.
[20] 廖新浴. 低温等离子体诱导活的不可培养(VBNC)状态金黄色葡萄球菌的机制研究[D].杭州:浙江大学, 2021.LIAO X Y.The molecular mechanisms of viable but nonculturable Staphylococcus aureus by nonthermal plasma (NTP) [D].Hangzhou:Zhejiang University, 2021.
[21] RAO N V, SHASHIDHAR R, BANDEKAR J R.Induction, resuscitation and quantitative real-time polymerase chain reaction analyses of viable but nonculturable Vibrio vulnificus in artificial sea water[J].World Journal of Microbiology and Biotechnology, 2014, 30(8):2205-2212.
[22] WONG H C, WANG P, CHEN S Y, et al.Resuscitation of viable but non-culturable Vibrio parahaemolyticus in a minimum salt medium[J].FEMS Microbiology Letters, 2004, 233(2):269-275.
[23] YOON J H, LEE S Y.Characteristics of viable-but-nonculturable Vibrio parahaemolyticus induced by nutrient-deficiency at cold temperature[J].Critical Reviews in Food Science and Nutrition, 2020, 60(8):1302-1320.
[24] FERNáNDEZ-DELGADO M, GARCíA-AMADO M A, CONTRERAS M, et al.Survival, induction and resuscitation of Vibrio cholerae from the viable but non-culturable state in the Southern Caribbean Sea[J].Revista Do Instituto de Medicina Tropical de Sao Paulo, 2015, 57(1):21-26.
[25] NICOL M S, GIOFFR
M S, GIOFFR A, CARNAZZA S, et al.Viable but nonculturable state of foodborne pathogens in grapefruit juice:A study of laboratory[J].Foodborne Pathogens and Disease, 2011, 8(1):11-17.
A, CARNAZZA S, et al.Viable but nonculturable state of foodborne pathogens in grapefruit juice:A study of laboratory[J].Foodborne Pathogens and Disease, 2011, 8(1):11-17.
[26] 卢梓荧, 陈梓涵, 何欣忆, 等.芳樟醇诱导肠炎沙门氏菌进入活的不可培养状态的研究[J].中国食品学报, 2024, 24(7):79-87.LU Z Y, CHEN Z H, HE X Y, et al.Research on induction of Salmonella enteritidis into viable but nonculturable state by linalool[J].Journal of Chinese Institute of Food Science and Technology, 2024, 24(7):79-87.
[27] ZHONG L, CHEN J, ZHANG X H, et al.Entry of Vibrio cincinnatiensis into viable but nonculturable state and its resuscitation[J].Letters in Applied Microbiology, 2009, 48(2):247-252.
[28] DEY R, RIEGER A, BANTING G, et al.Role of amoebae for survival and recovery of ‘non-culturable’ Helicobacter pylori cells in aquatic environments[J].FEMS Microbiology Ecology, 2020, 96(10):fiaa182.
[29] 陈曦. 唾液诱导幽门螺杆菌VBNC状态的机制研究[D].成都:四川大学, 2021.CHEN X.The mechanism of saliva-induced Helicobacter pylori VBNC status[D].Chengdu:Sichuan University, 2021.
[30] SENOH M, GHOSH‐BANERJEE J, RAMAMURTHY T, et al.Conversion of viable but nonculturable Vibrio cholerae to the culturable state by co-culture with eukaryotic cells[J].Microbiology and Immunology, 2010, 54(9):502-507.
[31] LIAO H B, ZHONG X W, XU L, et al.Quorum-sensing systems trigger catalase expression to reverse the oxyR deletion-mediated VBNC state in Salmonella typhimurium[J].Research in Microbiology, 2019, 170(2):65-73.
[32] LIU Y M, KUMBLATHAN T, UPPAL G K, et al.A hidden risk:Survival and resuscitation of Escherichia coli O157:H7 in the viable but nonculturable state after boiling or microwaving[J].Water Research, 2020, 183:116102.
[33] YOON J H, BAE Y M, JO S, et al.Optimization of resuscitation-promoting broths for the revival of Vibrio parahaemolyticus from a viable but nonculturable state[J].Food Science and Biotechnology, 2021, 30(1):159-169.
[34] AKTAS D, BAGIROVA M, ALLAHVERDIYEV A M, et al.Resuscitation of the Helicobacter pylori coccoid forms by resuscitation promoter factor obtained from Micrococcus luteus[J].Current Microbiology, 2020, 77(9):2093-2103.
[35] PINTO D, ALMEIDA V, ALMEIDA SANTOS M, et al.Resuscitation of Escherichia coli VBNC cells depends on a variety of environmental or chemical stimuli[J].Journal of Applied Microbiology, 2011, 110(6):1601-1611.
[36] WEI C J, ZHAO X H.Induction of viable but nonculturable Escherichia coli O157:H7 by low temperature and its resuscitation[J].Frontiers in Microbiology, 2018, 9:2728.
[37] CHEN S, LI X, WANG Y H, et al.Induction of Escherichia coli into a VBNC state through chlorination/chloramination and differences in characteristics of the bacterium between states[J].Water Research, 2018, 142:279-288.
[38] YE Z, LI H X, JIA Y Y, et al.Supplementing resuscitation-promoting factor (Rpf) enhanced biodegradation of polychlorinated biphenyls (PCBs) by Rhodococcus biphenylivorans strain TG9T[J].Environmental Pollution, 2020, 263:114488.
[39] MORISHIGE Y, KOIKE A, TAMURA-UEYAMA A, et al.Induction of viable but nonculturable Salmonella in exponentially grown cells by exposure to a low-humidity environment and their resuscitation by catalase[J].Journal of Food Protection, 2017, 80(2):288-294.
[40] DEBNATH A, MIYOSHI S I.The impact of protease during recovery from viable but non-culturable (VBNC) state in Vibrio cholerae[J].Microorganisms, 2021, 9(12):2618.
[41] DONG K, PAN H X, YANG D, et al.Induction, detection, formation, and resuscitation of viable but non-culturable state microorganisms[J].Comprehensive Reviews in Food Science and Food Safety, 2020, 19(1):149-183.
[42] 李桂英, 刘建莹, 安太成.水体消毒过程中活的不可培养细菌的形成与复苏机制研究进展[J].生态环境学报, 2023, 32(7):1333-1343.LI G Y, LIU J Y, AN T C.The formation and resuscitation mechanisms of viable but nonculturable bacteria during water disinfection processes[J].Ecology and Environmental Sciences, 2023, 32(7):1333-1343.
[43] PARK S Y, HWANG B J, SHIN M H, et al.N-acylhomoserine lactonase producing Rhodococcus spp.with different AHL-degrading activities[J].FEMS Microbiology Letters, 2006, 261(1):102-108.
[44] 周奎, 王润东, 宫梦学, 等.基于4D非标记定量蛋白质组学技术解析OHHL调控OpaR蛋白驱动VBNC态副溶血弧菌复苏的机制[C].中国食品科学技术学会第二十一届年会论文摘要集.重庆, 2024:73-74.ZHOU K, WANG R D, GONG M X, et al.Based on 4D label-free quantitative proteomics technology, the mechanism of OHHL regulating OpaR protein-driven revival of Vibrio parahaemolyticus was analyzed[C].The 21st Annual Meeting of Cifst.Chongqing, 2024:73-74.
[45] MURUGAN K, VASUDEVAN N.Intracellular toxicity exerted by PCBs and role of VBNC bacterial strains in biodegradation[J].Ecotoxicology and Environmental Safety, 2018, 157:40-60.
[46] AYDIN I, SAIJO-HAMANO Y, NAMBA K, et al.Structural analysis of the essential resuscitation promoting factor YeaZ suggests a mechanism of nucleotide regulation through dimer reorganization[J].PLoS One, 2011, 6(8):e23245.
[47] MIR M, ASONG J, LI X R, et al.The extracytoplasmic domain of the Mycobacterium tuberculosis Ser/Thr kinase PknB binds specific muropeptides and is required for PknB localization[J].PLoS Pathogens, 2011, 7(7):e1002182.
[48] YANG D, WANG W X, ZHAO L, et al.Resuscitation of viable but nonculturable bacteria promoted by ATP-mediated NAD+ synthesis[J].Journal of Advanced Research, 2024, 60:27-39.
[49] PARDEE A B, BENZ E Jr, ST PETER D A, et al.Hyperproduction and purification of nicotinamide deamidase, a microconstitutive enzyme of Escherichia coli[J].The Journal of Biological Chemistry, 1971, 246(22):6792-6796.
[50] PETRACK B, GREENGARD P, CRASTON A, et al.Nicotinamide deamidase from mammalian liver[J].Journal of Biological Chemistry, 1965, 240(4):1725-1730.
[51] 刘玉杰, 邵文泰, 张浩, 等.活的非可培养状态细菌的培养和复苏条件的研究[J].食品安全质量检测学报, 2022, 13(24):8144-8151.LIU Y J, SHAO W T, ZHANG H, et al.Study on the culture and recovery conditions of viabile but nonculturable bacteria[J].Journal of Food Safety &Quality, 2022, 13(24):8144-8151.
[52] MILLER J W, RUCKER R B.Pantothenic Acid[M].Present Knowledge in Nutrition.Academic Press, 2020:273-287.
[53] DIBBLE C C, BARRITT S A, PERRY G E, et al.PI3K drives the de novo synthesis of coenzyme A from vitamin B5[J].Nature, 2022, 608(7921):192-198.
[54] YU W J, SUN F Q, SHEN C F, et al.Resuscitation of viable but nonculturable microorganisms:A highly promising strategy for enhanced bioremediation[J].Critical Reviews in Environmental Science and Technology, 2025, 55(12):904-927.
[55] KODICEK E, LAWSON D E M, WILSON P W.Biological activity of a polar metabolite of vitamin D3[J].Nature, 1970, 228(5273):763-764.
[56] DAWKINS M J R, JUDAH J D, REES K R.Mechanism of oxidative phosphorylation[J].Nature, 1958, 182(4639):875-876.
[57] NATH K A, ENRIGHT H, NUTTER L, et al.Effect of pyruvate on oxidant injury to isolated and cellular DNA[J].Kidney International, 1994, 45(1):166-176.
[58] WU J H, WANG Q Q, WANG D D, et al.Axenic and gnotobiotic insect technologies in research on host-microbiota interactions[J].Trends in Microbiology, 2023, 31(8):858-871.
[59] 邓晓凤. 紫外联合氯诱导抗性细菌进入VBNC状态及其复苏研究[D].福州:福建师范大学, 2022.DENG X F.VBNC state antibiotic resistant bacteriainduced by UV/chlorine disinfection and its resuscitation[D].Fuzhou:Fujian Normal University, 2022.
[60] 钟琳红. 辛辛那提弧菌、哈维氏弧菌和鳗弧菌活的非可培养状态的研究[D].青岛:中国海洋大学, 2009.ZHONG L H.Study of the viable but non-culturable state of Vibrio cincinnati, V.harveyi, and V.anguillarum[D].Qingdao:Ocean University of China, 2009.
[61] 孙丰蓉. 哈维氏弧菌活的非可培养状态的研究[D].青岛:中国海洋大学, 2008.SUN F R.The investigation of Vibrio harveyi in viable but nonculturable state[D].Qingdao:Ocean University of China, 2008.
[62] 杜萌. 几种常见致病菌的活的非可培养状态研究[D].青岛:中国海洋大学, 2007.DU M.The investigation of several normal pathogens in viable but nonculturable state[D].Qingdao:Ocean University of China, 2007.
[63] 范佳慧. 嗜联苯红球菌在典型逆境下的休眠与复苏机制及土壤修复应用[D].杭州:浙江大学, 2023.FAN J F.Mechanism study on dormancy and resuscitation of Rhodaccoccus biphenylivorans under typical stress and application in soil remediation[D].Hangzhou:Zhejiang University, 2023.
[64] CHEN L P, YU F, SHI H H, et al.Effect of salinity stress on respiratory metabolism, glycolysis, lipolysis, and apoptosis in Pacific oyster (Crassostrea gigas) during depuration stage[J].Journal of the Science of Food and Agriculture, 2022, 102(5):2003-2011.
[65] WILSON W A, ROACH P J, MONTERO M, et al.Regulation of glycogen metabolism in yeast and bacteria[J].FEMS Microbiology Reviews, 2010, 34(6):952-985.
[66] SU X M, ZHANG S, MEI R W, et al.Resuscitation of viable but non-culturable bacteria to enhance the cellulose-degrading capability of bacterial community in composting[J].Microbial Biotechnology, 2018, 11(3):527-536.
[67] ZHONG Q P, WANG B, WANG J, et al.Global proteomic analysis of the resuscitation state of Vibrio parahaemolyticus compared with the normal and viable but non-culturable state[J].Frontiers in Microbiology, 2019, 10:1045.
[68] 陈诗源, 陈吉祥, 王永刚, 等.苯诱导石油降解红平红球菌(Rhodococcus erythropolis)KB1形成VBNC状态及复苏特征研究[J].环境工程, 2024, 42(1):184-190.CHEN S Y, CHEN J X, WANG Y G, et al.Formation of viable but non-culturable state of Rhodococcus erythropolis kb1 induced by high concentration benzene and characteristics its resuscitated cells[J].Chinese Journal of Environmental Engineering, 2024, 42(1):184-190.
[69] 陈飞飞. 环境应激胁迫苍白杆菌FP1非可培养状态的形成、特征及转录组研究[D].兰州:兰州理工大学, 2022.CHEN F F.Studies on formation, characterization and transcriptome analysis of the viable but non-culturable state of Ochrobactrum sp.FP1 under environmental stress[D].Lanzhou:Lanzhou University of Technology, 2022.