葡萄酒非酿酒酵母(non-Saccharomyces)是指在葡萄酒生产中除酿酒酵母(Saccharomyces cerevisiae)之外的其他酵母菌种。截至2021年,非酿酒酵母共涉及子囊菌门(Ascomycota)和担子菌门(Basidiomycota)的葡萄汁有孢汉逊酵母(Hanseniaspora uvarum)、东方伊萨酵母(Iessatchenkia orientalis)、美极梅奇酵母(Metschnikowia pulcherrima)和戴尔有孢圆酵母(Torulaspora delbrueckii)等在内的293个酵母种[1]。非酿酒酵母主要来源于葡萄园环境、土壤及葡萄表面。过去,非酿酒酵母在葡萄酒发酵过程中被视为有害酵母或腐败酵母。然而,最新研究表明非酿酒酵母对葡萄酒品质具有积极贡献,包括通过酶促反应产生芳香化合物、增加甘油产量、降低乙醇含量以及稳定酒液色泽[2-8]。值得注意的是,这些酿酒学特性大多具有菌种和菌株特异性,因此准确的菌种鉴定与菌株区分尤为重要。
酵母菌的传统鉴别主要基于形态学和生理学特征,包括:培养特征观察(如MEDINA等[9]的研究发现,WL培养基上葡萄有孢汉逊酵母(Hanseniaspora vineae)呈亮绿色菌落而S.cerevisiae为哑光奶油色)、显微形态分析(细胞形态、胞内结构和繁殖方式,如M.pulcherrima有巨大脂质球)以及生理生化检测(碳源同化、β-葡萄糖苷酶活性和锂耐受性等)。这些传统方法虽系统全面,但存在操作繁琐、结果易受培养条件影响,且无法实现菌株水平区分等局限[10-11]。也有蛋白分析、同工酶谱和气相色谱等方法,但也因依赖生理特性而存在重现性争议[12]。
相较而言,分子生物学技术通过直接解析基因组信息,不受细胞生理状态影响,准确性高、重复性好[13]。该类技术基于rDNA序列的系统发育特征进行鉴定,关键靶标为种间变异率高的ITS-5.8S rDNA区域和测序分辨率高的26S rDNA D1/D2区。近年来,分子生物学技术在非酿酒酵母的鉴定与分型中取得了显著进展。在菌种鉴定方面,主要采用ESTEVE-ZARZOSO等[14]开发的基于ITS-5.8S rDNA的限制性片段长度多态性技术。另一种常用的酵母菌种鉴定方法是KURTZMAN等[15]所述的扩增26S rDNA的D1/D2结构域并进行测序。这些方法已被多项研究证实其对非酿酒酵母菌种鉴定有效性[16-17]。在菌株分型领域,目前已发展出多种有效的技术手段,能够实现对非酿酒酵母菌株水平的高效区分。其中,随机扩增多态性DNA(random amplified polymorphic DNA,RAPD)技术被广泛应用于菌株遗传多样性分析。MATEUS等[18]采用该技术对自然发酵葡萄酒体系中的酵母群落进行研究,发现H.uvarum、耐热克鲁维酵母(Lachancea thermotolerans)和M.pulcherrima等优势酵母物种在菌株水平上呈现显著的遗传多态性。此外,BARQUET等[19]开发了一种基于tRNA基因的新型分子分型方法—Tandem repeat-tRNA(TRtRNA)指纹图谱法,该方法通过优化引物序列组合,能够更精准地实现非酿酒酵母的菌株分型。利用该技术,成功区分了M.pulcherrima、H.vineae、H.uvarum、仙人掌有孢汉逊酵母(Hanseniaspora opuntiae)、泽普林假丝酵母(Candida zemplinina)等物种内的不同菌株。分子生物学技术的进步显著提升了非酿酒酵母的鉴定能力,但其分型标准化建设严重滞后于酿酒酵母成熟的Interdelta体系。目前该领域虽存在多种分型方法,却缺乏普遍认可的标准化方案,且面临系统性不足、和不同方法学的比较与整合缺失等问题。为此,本文系统梳理了当前非酿酒酵母菌种鉴定和菌株区分的主要分子技术并详细阐述了其核心原理、标准化操作程序、技术优势及应用限制,同时整合了该领域的前沿研究成果,旨在为科研工作者和产业技术员提供科学的方法选择指导,促进该领域检测规范的统一与完善。
1 菌种鉴定方法
1.1 核糖体基因测序
核糖体基因(5.8S、18S、26S)成簇排列形成转录单元,这些转录单元在基因组中串联重复100~200次。如图1所示,每个转录单元包含:编码区[18S(小亚基SSU)、5.8S、26S(大亚基LSU)基因];间隔区[内部转录间隔区(ITS):ITS1分隔18S与5.8S基因,ITS2分隔5.8S与26S基因;外部转录间隔区(ETS)];单元间分隔[非转录间隔区(NTS)]。另外图中还标明了常规测序所用的引物位置,即ITS区域所用引物(ITS1和ITS4)和26S rDNA D1/D2区域所用引物(NL1和NL4)。
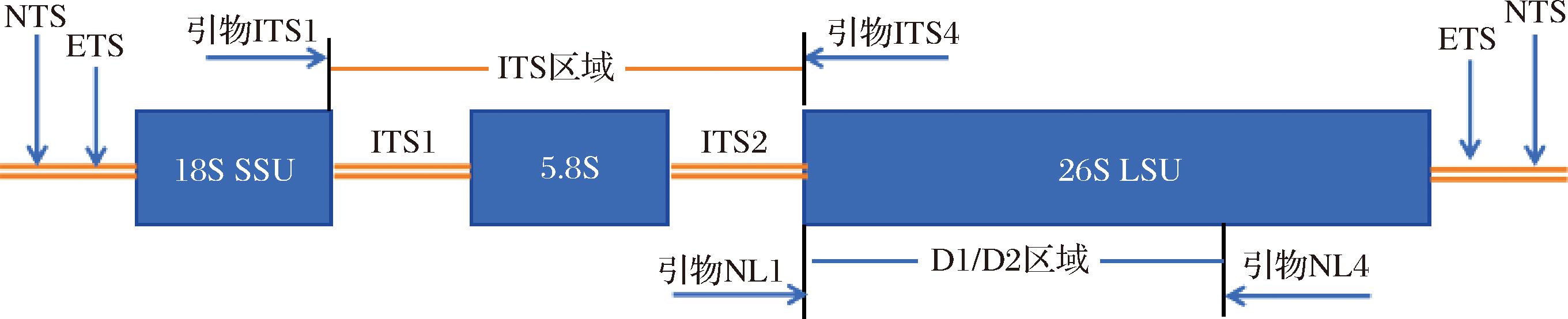
图1 核糖体DNA结构及不同区域相关引物[20]
Fig.1 Structure of nuclear ribosomal DNA and related primers
核糖体基因测序是目前非酿酒酵母分子鉴定中最常用的方法。该方法的核心原理是利用rDNA串联重复的结构特性(多拷贝易扩增)和保守/可变区域的进化梯度,通过靶向扩增高变区域,分析序列差异实现物种鉴定。该技术的标准操作流程如图2-a所示,主要包括以下步骤:a)基因组DNA提取:通常采用商业化的真菌DNA提取试剂盒或经典酚-氯仿法;b)PCR扩增:设计通用引物扩增靶标区域[ITS区域所用引物(ITS1和ITS4)或26S rDNA D1/D2区域所用引物(NL1和NL4)];c)扩增产物验证:通过琼脂糖凝胶电泳确认单一明亮条带,切胶纯化目标片段;d)测序反应:纯化后的PCR产物送测;e)数据分析:将测序结果与NCBI、UNITE等公共数据库进行比对,并利用MEGA等软件构建系统发育树进行分析。
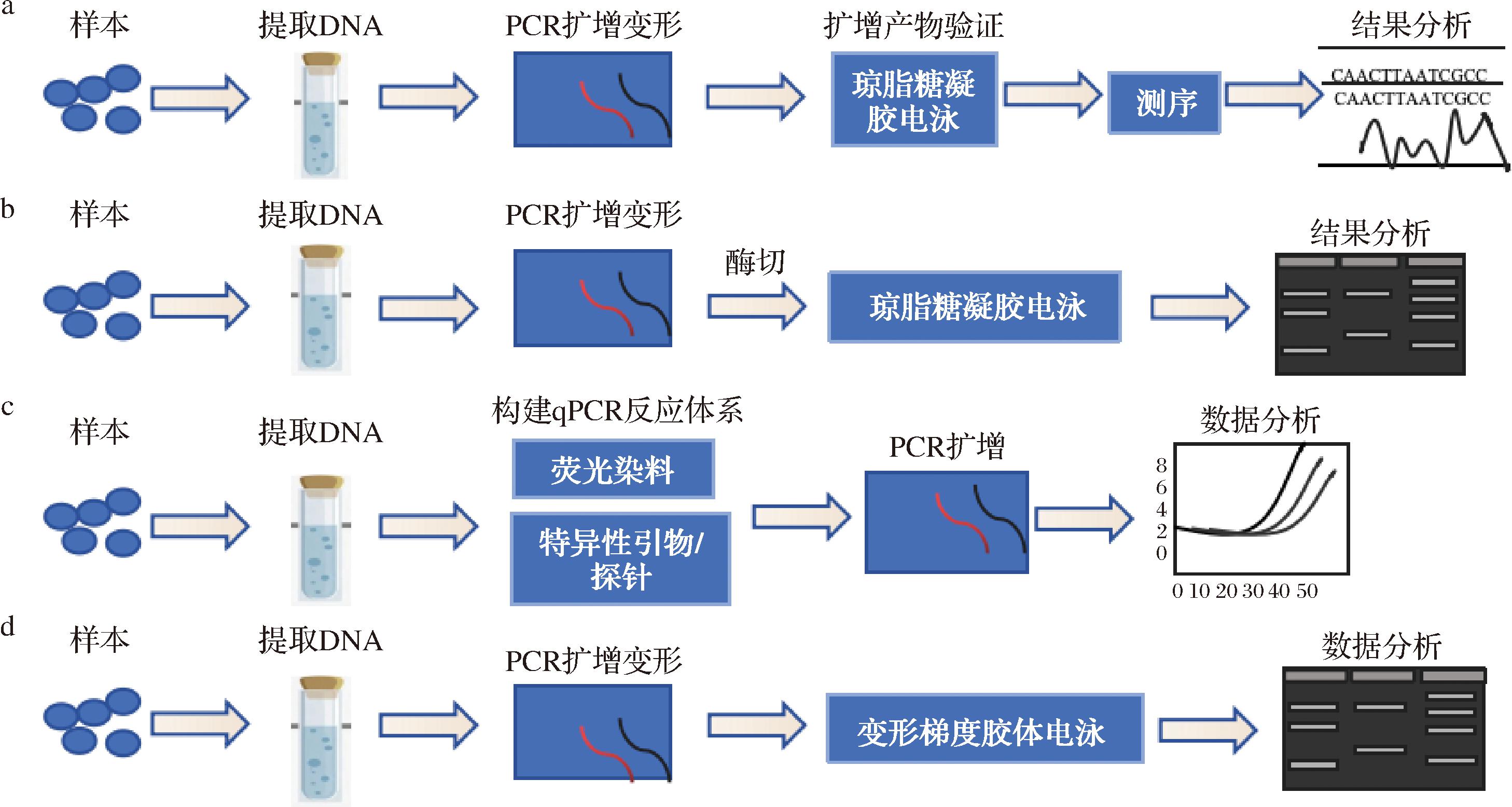
a-核糖体区域测序;b-核糖体区域的限制性分析;c-实时定量PCR;d-变性梯度凝胶电泳
图2 酵母菌种鉴定技术流程图
Fig.2 Technical flowchart of yeast species identification
ITS1-5.8S-ITS2区域和26S rDNA D1/D2区域的测序技术已广泛应用于非酿酒酵母的菌种鉴定。如FENG等[21]通过对ITS1-5.8S-ITS2区域测序,鉴定出包括H.uvarum、H.opuntiae、发酵毕赤酵母(Pichia fermentans)、克鲁维毕赤酵母(Pichia kluyveri)、库德里阿兹威毕赤酵母(Pichia kudriavzevii)等在内的29种非酿酒酵母。VOCE等[22]通过26S rDNA D1/D2区域测序对20株酵母进行鉴定,结果显示:非酿酒酵母为13株,分属5个不同种(H.uvarum、H.opuntiae、Monilinia fructicola、P.kluyveri、Starmerella bacillaris)。为了提高菌种鉴定的准确性,ZABUKOVEC等[23]同时结合了ITS1-5.8S-ITS2区域和26S rDNA D1/D2区域测序,共鉴定出18株非酿酒酵母,分属为4个不同种,包括:H.uvarum(5株)、P.kudriavzevii(3株)、Saturnispora diversa(2株)、S.bacillaris(8株)。研究表明,某些酵母菌种(如H.uvarum)的ITS区域存在种内多态性,可能会影响鉴定准确性[24]。同时需要注意的是,测序鉴定技术的可靠性在很大程度上依赖于参考数据库的完整性,对于尚未被收录的新菌种或稀有菌种,可能会出现鉴定失败的情况。测序技术虽然能够直接反映基因序列差异,具有较高的精确性,并且凭借高效、可靠的特点成为当前非酿酒酵母鉴定的主流方法,但在实际应用中仍建议结合其他分子生物学方法,以进一步提高鉴定结果的准确性。
1.2 核糖体基因限制性片段长度多态性分析
核糖体基因限制性片段长度多态性分析(ribosomal DNA restriction fragment length polymorphism,rDNA-RFLP),又称扩增核糖体DNA限制性分析(amplified ribosomal DNA restriction analysis,ARDRA),是一种基于rDNA多态性的分子鉴定技术。其核心原理是通过限制性内切酶特异性切割rDNA序列,利用电泳分离产生的片段长度多态性图谱实现菌种鉴定。该技术的标准操作流程如图2-b所示:a)DNA提取:获取样本基因组DNA作为模板;b)PCR扩增:使用rDNA通用引物(如ITS1/ITS4)扩增目标区域(酵母鉴定常用ITS区域);c)酶切消化:选择合适限制性内切酶处理PCR产物;d)电泳分析:琼脂糖凝胶分离酶切片段,染色观察条带分布;e)结果分析:与Yeast-ID数据库进行条带模式比对,完成物种鉴定。
核糖体基因限制性片段长度多态性分析在酵母鉴定中具有操作简便、成本低廉、结果重现性好等显著优势。如CORBU等[25]采用ITS1-5.8S-ITS2区域的PCR-RFLP技术,在自然发酵葡萄酒汁中鉴定出6株酵母,其中非酿酒酵母包括H.uvarum、M.pulcherrima、T.delbrueckii、P.kudriavzevii。然而,该方法存在近缘物种区分能力不足、依赖数据库对比、实验重复性波动等局限,难以满足现代酵母分类研究的全面需求。因此,目前普遍采用PCR-RFLP与测序技术联用的策略:MATEO等[26]通过该组合方法鉴定了M.pulcherrima、出芽短梗霉(Aureobasidium pullulans)等6种非酿酒酵母;L PEZ-ENR
PEZ-ENR QUEZ等[27]使用该方法从484株酵母中鉴定出55株非酿酒酵母(占11%),分属5个属、10个种,包括:Hanseniaspora meyeri(1株)、耐渗透压有孢汉逊酵母(Hanseniaspora osmophila)(1株)、季也蒙毕赤酵母(Pichia guilliermondii)(2株)、P.kudriavzevii(13株)、T.delbrueckii(3株)、Wickerhamomyces anomalus(16株)、Papiliotrema laurentii(1株)、Pichia terrestris(1株)、Rhodotorula mucilaginosa(4株)、Naganishia globosa(13株)。这种组合方法已广泛应用于酵母鉴定领域[28-29],其优势在于:既保留了RFLP技术的快速筛查特性,又通过测序技术保证了鉴定结果的精确性,从而实现了检测效率与结果可靠性的最优平衡。
QUEZ等[27]使用该方法从484株酵母中鉴定出55株非酿酒酵母(占11%),分属5个属、10个种,包括:Hanseniaspora meyeri(1株)、耐渗透压有孢汉逊酵母(Hanseniaspora osmophila)(1株)、季也蒙毕赤酵母(Pichia guilliermondii)(2株)、P.kudriavzevii(13株)、T.delbrueckii(3株)、Wickerhamomyces anomalus(16株)、Papiliotrema laurentii(1株)、Pichia terrestris(1株)、Rhodotorula mucilaginosa(4株)、Naganishia globosa(13株)。这种组合方法已广泛应用于酵母鉴定领域[28-29],其优势在于:既保留了RFLP技术的快速筛查特性,又通过测序技术保证了鉴定结果的精确性,从而实现了检测效率与结果可靠性的最优平衡。
1.3 实时PCR或定量PCR(quantitative real-time PCR,qPCR)
qPCR是一种在PCR扩增过程中实时监测荧光信号,从而对目标DNA进行定性和定量分析的技术。该方法实现菌种鉴定核心原理是利用ITS和LSU基因的序列保守性与特异性,通过特异性引物设计、荧光定量扩增及熔解曲线分析,将核酸序列信息转化为可量化的荧光信号,实现对目标菌种的快速鉴定。该技术的操作流程如图2-c所示:a)DNA提取:从样本中提取DNA并纯化;b)构建qPCR反应体系:配制含特异性引物和荧光标记的qPCR体系(包含模板DNA、特异性引物/探针、Taq酶、dNTPs及荧光标记物);c)PCR扩增:进行30~40个温度循环(95 ℃→55~65 ℃→72 ℃),实时监测荧光信号获取循环阈值(Ct值);d)数据分析:通过熔解曲线分析(熔解温度(Tm值)差异)结合Ct值及阳性对照,与已知菌种数据库比对来区分物种。
实时PCR凭借高灵敏度与特异性、快速高效、兼具菌种鉴定与定量分析等优势,在葡萄酒非酿酒酵母研究中得到广泛应用。ZOTT等[30]开发了特异性qPCR引物体系,用于检测葡萄汁、发酵过程及成品酒中的I.orientalis、M.pulcherrima、T.delbrueckii和C.zemplinina。WANG等[31]建立了可同时检测7种酵母的qPCR方法,包括出A.pullulan、Brettanomyces bruxellensis、Candida californica、Curvibasidium pallidicorallinum等。为提升对B.bruxellensis的检测效率,MITINA等[32]优化了qPCR检测方案。尽管该技术存在依赖已知菌种信息(无法鉴定未知物种)、存在非特异性扩增风险以及引物设计严格等局限性,但其为难以培养的酵母提供了高效检测方案。凭借快速高效的特点,qPCR技术已成为酿酒微生物检测领域不可或缺的重要分析工具。
1.4 变性梯度凝胶电泳
变性梯度凝胶电泳(denaturing gradient gel electrophoresis,DGGE)是一种基于DNA序列差异的微生物群落分析的技术。其原理是扩增目标基因(如26S rDNA或ITS区),利用不同DNA序列在变性剂梯度凝胶中解链行为的差异进行分离,通过DNA片段迁移速率的变化快速检测微生物多样性。该方法的具体操作步骤如图2-d所示,主要包括以下步骤:a)DNA提取:从葡萄酒发酵样品中提取微生物总DNA;b)PCR扩增:使用特异性引物扩增目标片段;c)DGGE电泳:制备含线性变性梯度的聚丙烯酰胺凝胶。将PCR产物加载到凝胶上,进行电泳分离;d)染色与成像:电泳后,用核酸染料染色,然后在紫外灯下观察并拍照;e)条带分析:通过条带图谱与标准菌株的DGGE图谱比对,确定菌种归属。
COCOLIN等[33]首次采用DGGE技术研究葡萄酒发酵过程中的酵母菌群动态,成功检测到传统培养法未能发现的H.osmophila菌种。该技术的优势在于无需预知物种DNA序列即可鉴定葡萄酒中的微生物组成。然而,不同物种可能因具有相同的电泳迁移率而导致结果误判。因此,实际应用中研究者常通过切胶回收条带并进行测序来验证鉴定结果。例如,URSO等[34]采用此方法研究了干燥葡萄酿制甜葡萄酒过程中酵母菌的生物多样性及动态变化,在甜酒发酵初期额外鉴定出了C.zemplinina和H.uvarum这2种酵母。研究表明,DGGE结合切胶测序是鉴定葡萄酒发酵过程中酵母群落的有效方法[35-36]。但该方法也存在局限:无法区分死菌与活菌,且鉴定结果依赖于测序比对。为提高准确性,有必要结合基于培养的方法进行分析。
温度梯度凝胶电泳(temperature gradient gel electrophoresis,TTGE)是一种基于线性温度梯度,用于分离DNA分子的技术。有研究展示了PCR-TTGE技术在葡萄酒发酵过程中酵母种群分析中的应用潜力[37]。与传统的平板培养方法相比,PCR-TTGE能更快速、全面地揭示发酵过程中酵母种群的动态变化,尤其在检测难以培养的酵母时优势显著。但由于PCR可能受葡萄酒中某些化合物抑制,样品处理时需特别注意。
基于上述菌种鉴定方法,本文对其在非酿酒酵母菌种鉴定中的应用情况进行总结比较,并呈现于表1中。
表1 葡萄酒非酿酒酵母菌种鉴定的分子技术及其应用
Table 1 Molecular techniques for identifying non-Saccharomyces yeast species in wine and their applications

技术所用引物鉴定物种参考文献ITS区域测序ITS1、ITS4H.uvarum、H.meyeri、H.opuntiae、P.fermentans、P.kluyveri、P.kudriavzevii、P.terricola、S.bacillaris、A.pullulans、Filobasidium floriforme、Sporidiobolus pararoseus、C.californica、Candida railenensis、Meyerozyma carpophila[21]26S rDNA D1/D2区域测序NL1、NL4H.uvarum、H.opuntiae、M.fructicola、P.kluyveri、S.bacillaris[22]26S rDNA D1/D2区域测序和ITS区域测序NL1、NL4、ITS1、ITS4H.uvarum、P.kudriavzevii、Saturnispora diversa、S.bacillaris[23]ITS1-5.8S-ITS2区域的PCR-RFLPITS1、ITS4H.uvarum、M.pulcherrima[25]ITS1、ITS4、NL1、NL4M.pulcherrima、A.pullulans、Cryptococcus uzbekistanensis、R.mucilaginosa、C.adeliensis、Quambalaria cyanescens[26]ITS1-5.8S-ITS2区域的PCR-RFLP与26S rDNAD1/D2区域测序ITS1、ITS4、NL1、NL4H.meyeri、H.osmophila,P.guilliermondii、P.kudriavzevii、T.delbrueckii、W.s anomalus[27]ITS1、ITS4、NL1、NL4H.uvarum、H.opuntiae、S.bacillaris、P.terricola、P.fermentans、P.kluyveri、T.delbrueckii、蜂假丝酵母(Candida apicola)、微小囊担菌(Cystobasidi-um minutum)[28]
续表1

技术所用引物鉴定物种参考文献ITS1-5.8S-ITS2区域的PCR-RFLP与ITS区域测序ITS1、ITS4W.anomalus、H.vineae、H.uvarum、M.pulcherrima、C.railenensis、T.del-brueckii、S.bacillaris[29]ISA 1、ISA 2、MPL3、MPR3、Tods L2、Tods R2、Hauf 2L、Hauf 2R、CZ-2、CASTI.orientalis、M.pulcherrima、T.delbrueckii、C.zemplinina、H.uvarum、H.guilliermondii[30]实时PCRApF3、ApR3、BbF1、BbR1、CpR1f、CpR3、Mt8F、Mt8R、ScF1、ScR1A.pullulans、B.bruxellensis、C.californica、C.pallidicorallinum、M.pulcher-rima、M.chrysoperlae、S.bayanus[31]p35、p36B.bruxellensis[32]PCR-DGGENL1-GC、LS2H.uvarum、S.bacillaris、拜耳接合酵母(Zygosaccharomyces bailii)、Cryp-tococcus victoriae、A.pullulans[36]
2 菌株区分方法
2.1 染色体脉冲场凝胶电泳
染色体脉冲场凝胶电泳(pulsed-field gel electrophoresis,PFGE)是一种分离大分子质量DNA(如染色体DNA)的电泳技术。在酵母的研究领域,染色体脉冲场凝胶电泳常被称为核型分析,该技术的核心原理是通过交替变换电场方向,实现大分子质量DNA的高效分离。如图3-a所示为具体操作流程。
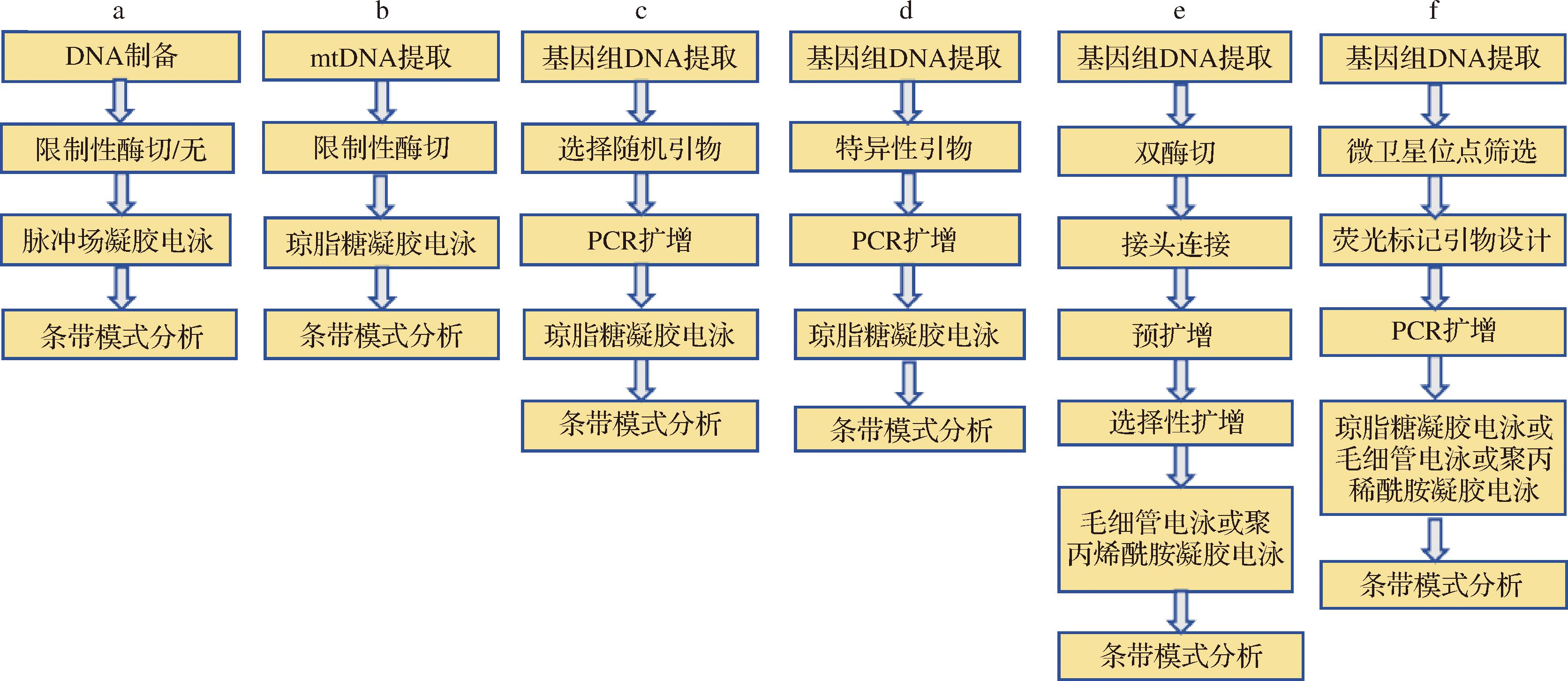
a-PFGE;b-mtDNA-RFLP;c-RAPD;d-TRtRNA;e-AFLP;f-SSR
图3 酵母菌株区分技术流程
Fig.3 Technical flowchart of yeast strain differentiation
有研究者将核型分析方法成功应用于非酿酒酵母的菌株区分[38-39]。然而,由于某些酵母菌株(如B. bruxellensis)的染色体数目通常较少,传统的PFGE分析可能无法有效区分这些菌株。为解决这一问题,MIOT-SERTIER等[40]首次将限制性内切酶分析脉冲场凝胶电泳(restriction enzyme analysis-pulsed field gel electrophoresis,REA-PFGE)技术系统应用于B.bruxellensis的菌株分型,对比验证多种PCR(5种RAPD引物、2种微卫星引物)技术,确立REA-PFGE其分型效果优于传统PCR方法。后续RENAULT等[41]的研究证实REA-PFGE对T.delbrueckii菌株的区分效率高于单一PCR方法。尽管REA-PFGE具有高分辨率,能够区分近缘菌株且无需预先了解基因组信息,也不依赖特定引物或探针,但其操作耗时费力、成本较高且技术门槛较高,限制了该技术的广泛应用。
2.2 线粒体DNA(mtDNA)的限制性分析
线粒体DNA的限制性分析(restriction analysis of mitochondrial DNA,mito-RFLP)是一种基于限制性内切酶对线粒体DNA进行特异性切割的分子分型技术。该技术的核心原理是基于不同菌株mtDNA序列的天然多态性,通过限制性内切酶对特异性识别位点的切割,产生具有菌株差异的片段长度多态性,从而揭示遗传变异。QUEROL等[42]提出了一种无需复杂设备的mtDNA提取方案,显著降低了操作难度和成本。图3-b展示了具体操作流程:mtDNA提取(从样本中分离纯化线粒体DNA);限制性酶切(使用特定限制性内切酶对mtDNA进行消化,切割特定序列位点);电泳分析(琼脂糖凝胶电泳、紫外下观察条带模式并记录);分型统计(根据条带模式差异进行比对和分型,统计群体遗传特征)。
线粒体DNA的限制性分析具有操作简便快速、成本低廉、特异性强且多态性分辨率高以及结果直观等显著优势。该方法已成功应用于多种非酿酒酵母菌株的区分中:如AGNOLUCCI等[43]在对5株B.bruxellensis参考菌株进行分型时发现,其中HinfⅠ酶切mtDNA可区分其中2株。MARTORELL等[44]用HinfⅠ内切酶对63株D.bruxellensis的mtDNA进行酶切,得到3种不同的分子模式;对32株P.guilliermondii分型,得到7种不同的限制性模式。CSOMA等[45]使用7种限制性内切酶对41株S.bacillaris进行分型,发现DraⅠ酶切区分出27种模式,HinfⅠ区分出19种模式。尽管mito-RFLP具有诸多优势,但其应用存在以下限制:其分型结果依赖于特定限制性内切酶的选择(不同酶可能产生不同分型结果);酶切反应条件(如温度、时间、酶量)的微小变化可能影响结果重现性;不同实验室间的结果比较可能存在困难。由于上述局限性,该技术在非酿酒酵母研究中的应用相对较少。然而,在特定场景下,它仍可作为快速、经济的初步分型工具。
2.3 基于PCR的分子技术
基于PCR技术的分子分型方法因其快速、高效的特点,已成为当前葡萄酒酵母菌株区分的重要技术手段。这些方法包括:无需限制性内切酶即可检测DNA多态性的RAPD和微卫星分析等常用技术。所有技术均采用寡核苷酸引物与酵母DNA目标序列特异性结合,通过耐热DNA聚合酶进行25~45个循环的扩增(每个循环包括变性、退火和延伸步骤),使目标DNA呈指数增长。扩增产物经1.4%琼脂糖凝胶电泳后,可观察到菌株特异的条带模式,从而实现菌株区分。扩增条件(特别是退火温度)因技术而异。接下来本文将详细介绍RAPD、TRtRNA、AFLP和SSR这4种分子分型方法。
2.3.1 RAPD
RAPD技术的核心原理是使用单一随机设计的短引物(通常为10个碱基对)对基因组DNA进行非特异性扩增,通过引物与模板DNA的随机匹配产生多态性扩增条带。由于不同物种或菌株的基因组序列存在差异,这些随机引物结合位点的分布和数量也会有所不同,从而产生具有多态性的DNA指纹图谱,该方法的具体操作流程如图3-c所示。
该技术主要优势体现在其操作简便、分析速度快、通量高,且不需要预先了解目标物种的基因组序列信息,这使得RAPD在对未知基因组生物的研究中具有独特的应用价值。如BINATI等[46]在筛选具有优良酿酒特性的本土非酿酒酵母研究中发现,该技术可将其中46株S.bacillaris分为8个基因聚类,12株L.thermotolerans分为2个基因聚类。CORBU等[47]则使用5种引物(OPA03、OPA11、OPA18、OPE18、M13)将4株P.kudriavzevii分为3个基因型。其他研究也证实了该技术在非酿酒酵母菌株水平上的区分效率可靠[48-50]。RAPD技术虽然是一种快速评估遗传多样性的有效工具,但也存在明显的局限性。由于单个随机引物提供的信息量有限,通常需要组合多个不同序列的随机引物的扩增结果才能获得足够的区分能力。这一技术缺陷导致RAPD的实验条件难以标准化,使得不同实验室之间的结果可比性较差,数据解读也较为复杂。然而,在资源有限的实验室或对研究对象的基因组信息知之甚少的情况下,RAPD仍不失为一种快速评估遗传多样性的有效工具。
2.3.2 TRtRNA
TRtRNA是一种创新性的分子指纹图谱技术。该技术巧妙结合了基因组中两类特征性序列:高度变异的串联重复序列(tandem repeats,TR)和相对保守的tRNA基因间隔区。这种双重靶向的设计理念使其在微生物分型领域展现出独特优势,特别适用于非酿酒酵母的菌株区分。该方法的具体操作流程如图3-d所示。
TRtRNA-PCR在非酿酒酵母菌株水平上的区分效率已得到验证。如SGOUROS等[51]通过TRtRNA-PCR和RAPD技术对3株T.delbrueckii进行种内分型,发现TRtRNA-PCR能有效区分2种亚型,而RAPD无法分辨。NISIOTOU等[52]评估了该方法与RAPD技术在多种重要非酿酒酵母(包括L.thermotolerans,M.pulcherrima,H.guilliermondii、H.uvarum、I.orientalis等)中的分型效率,发现TRtRNA-PCR(ISSR-MB)对L.thermotolerans和M.pulcherrima效果较好,但对T.delbrueckii和P.anomala完全无效。LI等[53]将该技术应用于中国宁夏地区非酿酒酵母多样性研究,发现386株H.uvarum被分为6个谱型,59株C.zemplinina分为7个谱型,而某些物种(如F.elegans和N.albida)无法通过此方法区分。
该技术具有分辨效能突出、操作便捷、经济、突破基因组信息限制和数据重现性优异等优势,特别适合资源有限的实验室开展大规模菌株筛查。然而,该方法依赖tRNA序列,导致一些tRNA基因簇保守性过高的菌株无法区分,且对部分物种的分辨率有限,需结合其他方法进行鉴定,以提高准确性。
2.3.3 扩增片段长度多态性(amplified fragment length polymorphism,AFLP)
AFLP是一种基于PCR的高效DNA指纹技术,通过结合限制性酶切和选择性扩增来检测基因组DNA的多态性。该技术具体操作流程如图3-e所示:首先利用限制性内切酶消化目标微生物的基因组DNA,产生具有黏性末端的DNA片段;随后将特定接头连接至这些酶切片段的末端;最后,针对接头和酶切位点序列设计特异性引物进行PCR扩增,扩增产物可通过琼脂糖凝胶或聚丙烯酰胺凝胶电泳分离并检测,从而获得DNA指纹图谱。
DE BARROS LOPES等[54]首次系统地将AFLP技术应用于酵母菌株基因分型,发现26株S.cerevisiae可区分为6种基因型,7株D.bruxellensis可分为2种基因型。后续研究者也将该技术用于不同非酿酒酵母菌株的区分[55-56]。然而该技术存在操作繁琐、依赖精密仪器、扩增竞争导致数据复杂化、非共显性标记无法评估杂合度,以及DNA质量要求高等局限性。为此,ESTEVE-ZARZOSO等[57]开发了简化AFLP方案,通过优化引物设计和电泳条件降低成本并提升实用性,更适合葡萄酒微生物生态学的常规分析,但分辨率有所降低。在实际应用中,高分辨率需求应优先选择传统AFLP,而工业常规检测则可权衡选择简化AFLP,这一技术体系为非酿酒酵母分型提供了灵活解决方案,但需根据具体研究目标和条件选择合适方法。
2.3.4 简单序列重复标记(simple sequence repeat,SSR)
SSR又称微卫星标记,是基于基因组短串联重复序列的分子标记技术。SSR由1~6个核苷酸为核心单元的短串联重复序列构成,在基因组中广泛分布且重复次数具高度多态性。该技术通过检测重复单元变异来区分不同菌株。该方法的具体操作流程如图3-f所示:设计引物,根据SSR两侧的保守单拷贝序列设计特异性引物,确保扩增包含重复区域;然后进行PCR扩增,利用设计的引物对目标SSR位点进行扩增,不同等位基因因重复次数不同产生不同长度的片段;最后进行电泳检测,通过凝胶电泳或毛细管电泳或丙烯酰胺凝胶电泳分离PCR产物,根据条带大小差异判断SSR多态性。
该技术在非酿酒酵母菌株区分中的有效性已得到验证。例如,BANILAS等[58]首次开发了L.thermotolerans的SSR分型方法,研究发现其区分能力指数为0.818,显著高于传统TRtRNA-PCR方法的能力指数(0.592)。随后,VICENTE等[59]开发了一种更简单、高效且低成本的方法,通过多重PCR和琼脂糖电泳简化了L.thermotolerans的SSR分型流程。相较于BANILAS等[58]依赖毛细管电泳的方法,该方法进一步降低了成本,同时保持了良好的可重复性。CSOMA等[60]用该方法对36株Z.lentus进行基因分型,共发现16种不同带型。PFLIEGLER等[61]对35株来自不同地理位置的C.zemplinina进行分型发现,该方法引物GTG5检测到的多样性最高(17种模式),而其他引物(如RF2)仅区分出少数模式。DIMOPOULOU等[62]对23株B.bruxellensis进行基因分型,分为4种基因型。尽管该技术相较于RAPD和AFLP需要设计物种特异性引物,且对数据库依赖性较强,但因其具有高多态性、成本可控和技术成熟等特点,在非酿酒酵母菌株的区分及群体遗传研究中仍具有不可替代的优势。
基于上述4种方法,本文总结比较了它们在葡萄酒非酿酒酵母研究中的应用(表2),可以看出RAPD技术对B.bruxellensis表现出最佳分型效果(15株对应15种基因型),TRtRNA在H.uvarum分型中效果突出(最高获得7种基因型)。不同酵母物种对分型方法的响应差异显著,如T.delbrueckii用RAPD可区分17种基因型,而TRtRNA则未能检测到差异。
表2 葡萄酒非酿酒酵母菌株区分的分子技术及其应用
Table 2 Molecular techniques for differentiating non-Saccharomyces yeast strains in wine and their applications
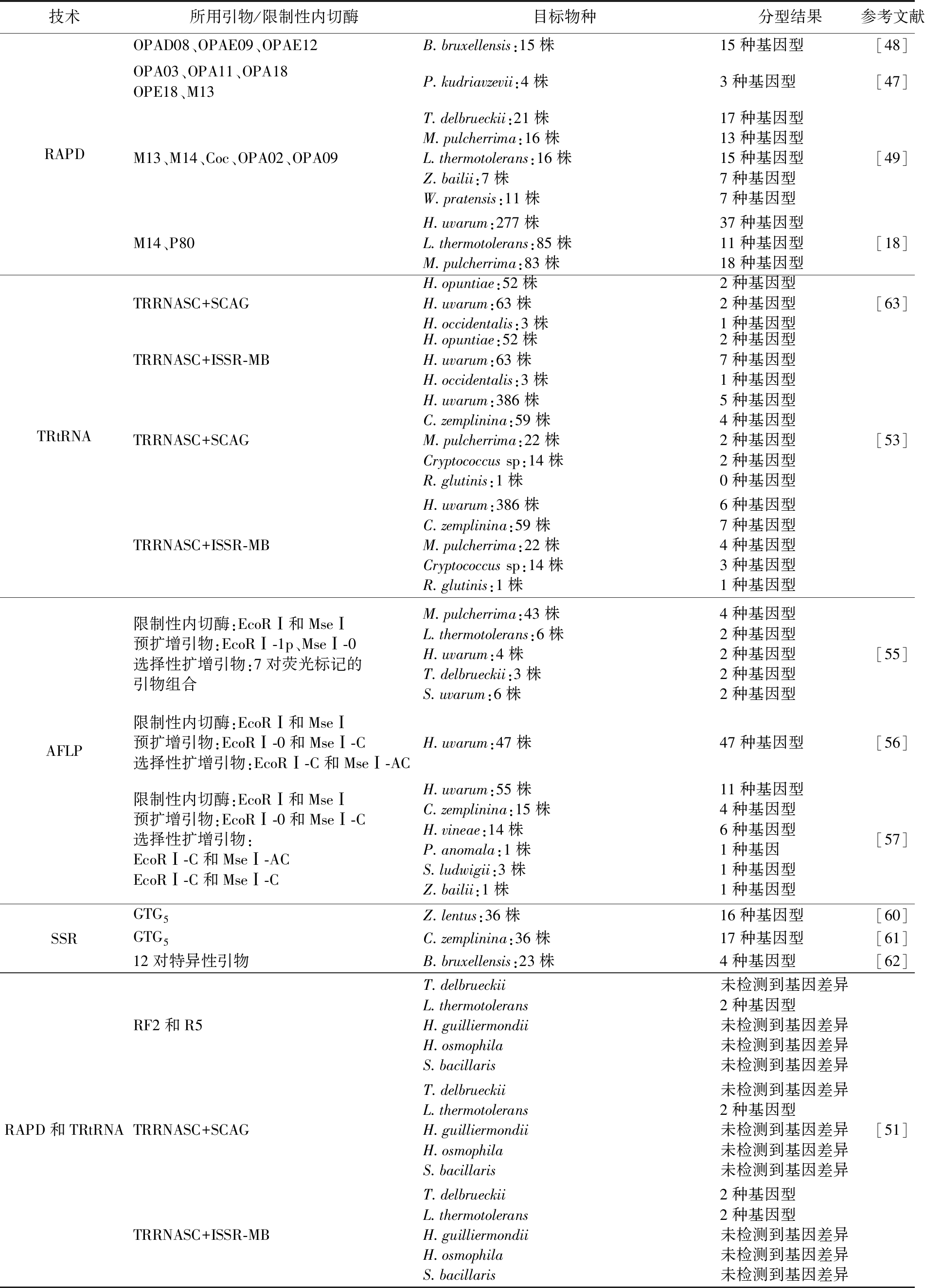
技术所用引物/限制性内切酶目标物种分型结果参考文献RAPDOPAD08、OPAE09、OPAE12B.bruxellensis:15株15种基因型[48]OPA03、OPA11、OPA18OPE18、M13P.kudriavzevii:4株3种基因型[47]M13、M14、Coc、OPA02、OPA09T.delbrueckii:21株M.pulcherrima:16株L.thermotolerans:16株Z.bailii:7株W.pratensis:11株17种基因型13种基因型15种基因型7种基因型7种基因型[49]M14、P80H.uvarum:277株L.thermotolerans:85株M.pulcherrima:83株37种基因型11种基因型18种基因型[18]TRtRNATRRNASC+SCAGH.opuntiae:52株H.uvarum:63株H.occidentalis:3株2种基因型2种基因型1种基因型[63]TRRNASC+ISSR-MBH.opuntiae:52株H.uvarum:63株H.occidentalis:3株2种基因型7种基因型1种基因型TRRNASC+SCAGH.uvarum:386株C.zemplinina:59株M.pulcherrima:22株Cryptococcus sp:14株R.glutinis:1株5种基因型4种基因型2种基因型2种基因型0种基因型[53]TRRNASC+ISSR-MBH.uvarum:386株C.zemplinina:59株M.pulcherrima:22株Cryptococcus sp:14株R.glutinis:1株6种基因型7种基因型4种基因型3种基因型1种基因型AFLP限制性内切酶:EcoRⅠ和MseⅠ预扩增引物:EcoRⅠ-1p、MseⅠ-0选择性扩增引物:7对荧光标记的引物组合M.pulcherrima:43株L.thermotolerans:6株H.uvarum:4株T.delbrueckii:3株S.uvarum:6株4种基因型2种基因型2种基因型2种基因型2种基因型[55]限制性内切酶:EcoRⅠ和MseⅠ预扩增引物:EcoRⅠ-0和MseⅠ-C选择性扩增引物:EcoRⅠ-C和MseⅠ-ACH.uvarum:47株47种基因型[56]限制性内切酶:EcoRⅠ和MseⅠ预扩增引物:EcoRⅠ-0和MseⅠ-C选择性扩增引物:EcoRⅠ-C和MseⅠ-ACEcoRⅠ-C和MseⅠ-CH.uvarum:55株C.zemplinina:15株H.vineae:14株P.anomala:1株S.ludwigii:3株Z.bailii:1株11种基因型4种基因型6种基因型1种基因1种基因型1种基因型[57]SSRGTG5Z.lentus:36株16种基因型[60]GTG5C.zemplinina:36株17种基因型[61]12对特异性引物B.bruxellensis:23株4种基因型[62]RAPD和TRtRNARF2和R5T.delbrueckiiL.thermotoleransH.guilliermondiiH.osmophilaS.bacillaris未检测到基因差异2种基因型未检测到基因差异未检测到基因差异未检测到基因差异TRRNASC+SCAGT.delbrueckiiL.thermotoleransH.guilliermondiiH.osmophilaS.bacillaris未检测到基因差异2种基因型未检测到基因差异未检测到基因差异未检测到基因差异[51]TRRNASC+ISSR-MBT.delbrueckiiL.thermotoleransH.guilliermondiiH.osmophilaS.bacillaris2种基因型2种基因型未检测到基因差异未检测到基因差异未检测到基因差异
3 总结与展望
本研究系统综述了非酿酒酵母菌种鉴定及菌株分型分子技术的最新研究进展。通过对TRtRNA-PCR、RAPD和SSR等常用分子标记技术的原理、应用特点及优劣势的深入分析,发现当前技术体系存在以下关键问题:首先,所有现有技术均无法独立完成全面精确的鉴定与分型。其次,现有技术体系面临3个主要瓶颈:a)方法覆盖范围有限,主要集中于常见菌种鉴定,对稀有菌种缺乏特异性检测手段;b)标准化程度不足,实验室间技术方案差异导致结果难以比较;c)分辨率与重复性难以兼顾,ITS1-5.8S-ITS2区域和26S rDNA D1/D2区域的测序技术适用于物种鉴定,但菌株分型灵敏度低,而RAPD等高分辨率技术又因标准化不足导致重复性差。
基于上述问题,本文提出以下建议:a)应将基于培养和不依赖培养的分子技术视为互补策略,通过多种技术的联合应用来提高鉴定可靠性;b)需要重点开发新型通用引物,并结合高通量测序技术(如全基因组测序)来提升分型效率和准确性;c)应加强分型结果与菌株发酵特性(如产酶能力、代谢产物)的关联研究。这些研究方向的推进将显著提升非酿酒酵母的资源开发水平和酿造应用潜力,为该领域的科研创新和产业升级奠定坚实基础。
[1] DRUMONDE-NEVES J, FERNANDES T, LIMA T, et al.Learning from 80 years of studies:A comprehensive catalogue of non-Saccharomyces yeasts associated with viticulture and winemaking[J].FEMS Yeast Research, 2021, 21(3):foab017.
[2] 李玥玥, 王燕荣.非酿酒酵母对葡萄酒品质影响研究进展[J].农产品加工, 2024(19):85-88;93.LI Y Y, WANG Y R.Research progress on the effect of non-Saccharomyces cerevisiae on wine quality[J].Farm Products Processing, 2024(19):85-88;93.
[3] WANG X, FAN G H, PENG Y Y, et al.Mechanisms and effects of non-Saccharomyces yeast fermentation on the aromatic profile of wine[J].Journal of Food Composition and Analysis, 2023, 124:105660.
[4] 王春晓, 俞俊竹, 周文亚, 等.非酿酒酵母属酵母的葡萄酒发酵应用研究进展[J].中国农业科学, 2023, 56(3):529-548.WANG C X, YU J Z, ZHOU W Y, et al.Research progress on the application of non-Saccharomyces during wine fermentation[J].Scientia Agricultura Sinica, 2023, 56(3):529-548.
[5] 战吉宬, 曹梦竹, 游义琳, 等.非酿酒酵母在葡萄酒酿造中的应用[J].中国农业科学, 2020, 53(19):4057-4069.ZHAN J C, CAO M Z, YOU Y L, et al.Research advance on the application of non-Saccharomyces in winemaking[J].Scientia Agricultura Sinica, 2020, 53(19):4057-4069.
[6] HAN X Y, QING X, YANG S Y, et al.Study on the diversity of non-Saccharomyces yeasts in Chinese wine regions and their potential in improving wine aroma by β-glucosidase activity analyses[J].Food Chemistry, 2021, 360:129886.
[7] 李海峰, 李砷, 牟志勇, 等.非酿酒酵母在酒类酿造过程中的微生物相互作用及功能特性研究进展[J].食品与发酵工业, 2024, 50(7):313-323.LI H F, LI S, MU Z Y, et al.Research progress on microbial interaction and functional characteristics of non-Saccharomyces yeasts in wine brewing process[J].Food and Fermentation Industries, 2024, 50(7):313-323.
[8] LIU S X, LOU Y, LI Y X, et al.Aroma characteristics of volatile compounds brought by variations in microbes in winemaking[J].Food Chemistry, 2023, 420:136075.
[9] MEDINA K, BOIDO E, FARI A L, et al.Increased flavour diversity of Chardonnay wines by spontaneous fermentation and co-fermentation with Hanseniaspora vineae[J].Food Chemistry, 2013, 141(3):2513-2521.
A L, et al.Increased flavour diversity of Chardonnay wines by spontaneous fermentation and co-fermentation with Hanseniaspora vineae[J].Food Chemistry, 2013, 141(3):2513-2521.
[10] YARROW D.Chapter 11 Methods for the isolation, maintenance and identification of yeasts[J].The Yeasts, 1998:77-100.
[11] HOLBAN A M, GRUMEZESCU A.Biotechnological Progress and Beverage Consumption[M].London:Academic Press, 2020.
[12] ZHANG J W, PLOWMAN J E, TIAN B, et al.Application of MALDI-TOF analysis to reveal diversity and dynamics of winemaking yeast species in wild-fermented, organically produced, New Zealand Pinot Noir wine[J].Food Microbiology, 2021, 99:103824.
[13] IVEY M L, PHISTER T G.Detection and identification of microorganisms in wine:A review of molecular techniques[J].Journal of Industrial Microbiology &Biotechnology, 2011, 38(10):1619-1634.
[14] ESTEVE-ZARZOSO B, BELLOCH C, URUBURU F, et al.Identification of yeasts by RFLP analysis of the 5.8S rRNA gene and the two ribosomal internal transcribed spacers[J].International Journal of Systematic and Evolutionary Microbiology, 1999, 49(1):329-337.
[15] KURTZMAN C P, ROBNETT C J.Identification and phylogeny of ascomycetous yeasts from analysis of nuclear large subunit (26S) ribosomal DNA partial sequences[J].Antonie Van Leeuwenhoek, 1998, 73(4):331-371.
[16] ZHANG J J, SHANG Y M, CHEN J Y, et al.Diversity of non-Saccharomyces yeasts of grape berry surfaces from representative Cabernet Sauvignon vineyards in Henan Province, China[J].FEMS Microbiology Letters, 2021, 368(20):fnab142.
[17] BEYENE E, TEFERA A T, MULETA D, et al.Molecular identification and performance evaluation of wild yeasts from different Ethiopian fermented products[J].Journal of Food Science and Technology, 2020, 57(9):3436-3444.
[18] MATEUS D, SOUSA S, COIMBRA C, et al.Identification and characterization of non-Saccharomyces species isolated from port wine spontaneous fermentations[J].Foods, 2020, 9(2):120.
[19] BARQUET M, MART N V, MEDINA K, et al.Tandem repeat-tRNA (TRtRNA) PCR method for the molecular typing of non-Saccharomyces subspecies[J].Applied Microbiology and Biotechnology, 2012, 93(2):807-814.
N V, MEDINA K, et al.Tandem repeat-tRNA (TRtRNA) PCR method for the molecular typing of non-Saccharomyces subspecies[J].Applied Microbiology and Biotechnology, 2012, 93(2):807-814.
[20] FERN NDEZ ESPINAR M T, MARTORELL P, DE LLANOS R, et al. Molecular Methods to Identify and Characterize Yeasts in Foods and Beverages[M]. Yeasts in Food and Beverages. Berlin, Heidelberg: Springer, 2006: 55-82.
NDEZ ESPINAR M T, MARTORELL P, DE LLANOS R, et al. Molecular Methods to Identify and Characterize Yeasts in Foods and Beverages[M]. Yeasts in Food and Beverages. Berlin, Heidelberg: Springer, 2006: 55-82.
[21] FENG C T, DU X, WEE J,et al.Microbial and chemical analysis of non-Saccharomyces yeasts from chambourcin hybrid grapes for potential use in winemaking[J].Fermentation, 2021, 7(1):15.
[22] VOCE S, IACUMIN L, COMUZZO P,et al.Characterization of non-Saccharomyces yeast strains isolated from grape juice and pomace:Production of polysaccharides and antioxidant molecules after growth and autolysis[J].Fermentation, 2022, 8(9):450.
[23] ZABUKOVEC P, ![]() F.Isolation and identification of indigenous wine yeasts and their use in alcoholic fermentation[J].Food Technology and Biotechnology, 2020, 58(3):337-347.
F.Isolation and identification of indigenous wine yeasts and their use in alcoholic fermentation[J].Food Technology and Biotechnology, 2020, 58(3):337-347.
[24] ONETTO C A, WARD C M, VARELA C, et al.Genetic and phenotypic diversity of wine-associated Hanseniaspora species[J].FEMS Yeast Research, 2025,25:foaf031.
[25] CORBU V M, CSUTAK O.Molecular and physiological diversity of indigenous yeasts isolated from spontaneously fermented wine wort from ilfov county, Romania[J].Microorganisms, 2022, 11(1):37.
[26] MATEO J J, GARCER P, MAICAS S,et al.Unusual non-Saccharomyces yeasts isolated from unripened grapes without antifungal treatments[J].Fermentation, 2020, 6(2):41.
P, MAICAS S,et al.Unusual non-Saccharomyces yeasts isolated from unripened grapes without antifungal treatments[J].Fermentation, 2020, 6(2):41.
[27] L PEZ-ENR
PEZ-ENR QUEZ L, VILA-CRESPO J, RODR
QUEZ L, VILA-CRESPO J, RODR GUEZ-NOGALES J M, et al.Non-Saccharomyces yeasts from organic vineyards as spontaneous fermentation agents[J].Foods, 2023, 12(19):3644.
GUEZ-NOGALES J M, et al.Non-Saccharomyces yeasts from organic vineyards as spontaneous fermentation agents[J].Foods, 2023, 12(19):3644.
[28] MIRANDA A, PEREIRA V, JARDIM H, et al.Impact of non-Saccharomyces yeast fermentation in Madeira wine chemical composition[J].Processes, 2023, 11(2):482.
[29] LEE S B, PARK H D.Isolation and investigation of potential non-Saccharomyces yeasts to improve the volatile terpene compounds in Korean Muscat bailey a wine[J].Microorganisms, 2020, 8(10):1552.
[30] ZOTT K, CLAISSE O, LUCAS P, et al.Characterization of the yeast ecosystem in grape must and wine using real-time PCR[J].Food Microbiology, 2010, 27(5):559-567.
[31] WANG X F, GLAWE D A, WELLER D M, et al.Real-time PCR assays for the quantification of native yeast DNA in grape berry and fermentation extracts[J].Journal of Microbiological Methods, 2020, 168:105794.
[32] MITINA I, GRAJDIERU C, STURZA R, et al.The Brettanomyces bruxellensis contamination of wines:A case study of Moldovan micro-winery[J].Beverages, 2024, 11(1):3.
[33] COCOLIN L, BISSON L F, MILLS D A.Direct profiling of the yeast dynamics in wine fermentations[J].FEMS Microbiology Letters, 2000, 189(1):81-87.
[34] URSO R, RANTSIOU K, DOLCI P, et al.Yeast biodiversity and dynamics during sweet wine production as determined by molecular methods[J].FEMS Yeast Research, 2008, 8(7):1053-1062.
[35] LLEIX J, MART
J, MART N V, PORTILLO M D C, et al.Comparison of fermentation and wines produced by inoculation of Hanseniaspora vineae and Saccharomyces cerevisiae[J].Frontiers in Microbiology, 2016, 7:338.
N V, PORTILLO M D C, et al.Comparison of fermentation and wines produced by inoculation of Hanseniaspora vineae and Saccharomyces cerevisiae[J].Frontiers in Microbiology, 2016, 7:338.
[36] ![]() M, PU
M, PU K
K ROV
ROV A, ŽENI
A, ŽENI OV
OV K.Novel insights into microbial community dynamics during the fermentation of Central European ice wine[J].International Journal of Food Microbiology, 2018, 266:42-51.
K.Novel insights into microbial community dynamics during the fermentation of Central European ice wine[J].International Journal of Food Microbiology, 2018, 266:42-51.
[37] FERN NDEZ-GONZ
NDEZ-GONZ LEZ M, ESPINOSA J C, ÜBEDA J F, et al.Yeasts present during wine fermentation:Comparative analysis of conventional plating and PCR-TTGE[J].Systematic and Applied Microbiology, 2001, 24(4):634-638.
LEZ M, ESPINOSA J C, ÜBEDA J F, et al.Yeasts present during wine fermentation:Comparative analysis of conventional plating and PCR-TTGE[J].Systematic and Applied Microbiology, 2001, 24(4):634-638.
[38] ESTEVE-ZARZOSO B, PERIS-TOR N M J, RAM
N M J, RAM N D, et al.Molecular characterisation of Hanseniaspora species[J].Antonie Van Leeuwenhoek, 2001, 80(1):85-92.
N D, et al.Molecular characterisation of Hanseniaspora species[J].Antonie Van Leeuwenhoek, 2001, 80(1):85-92.
[39] ESTEVE-ZARZOSO B, ZORMAN T, BELLOCH C, et al.Molecular characterisation of the species of the genus Zygosaccharomyces[J].Systematic and Applied Microbiology, 2003, 26(3):404-411.
[40] MIOT-SERTIER C, LONVAUD-FUNEL A.Development of a molecular method for the typing of Brettanomyces bruxellensis (Dekkera bruxellensis) at the strain level[J].Journal of Applied Microbiology, 2007, 102(2):555-562.
[41] RENAULT P, MIOT-SERTIER C, MARULLO P, et al.Genetic characterization and phenotypic variability in Torulaspora delbrueckii species:Potential applications in the wine industry[J].International Journal of Food Microbiology, 2009, 134(3):201-210.
[42] QUEROL A, BARRIO E, HUERTA T, et al.Molecular monitoring of wine fermentations conducted by active dry yeast strains[J].Applied and Environmental Microbiology, 1992, 58(9):2948-2953.
[43] AGNOLUCCI M, VIGENTINI I, CAPURSO G, et al.Genetic diversity and physiological traits of Brettanomyces bruxellensis strains isolated from Tuscan Sangiovese wines[J].International Journal of Food Microbiology, 2009, 130(3):238-244.
[44] MARTORELL P, BARATA A, MALFEITO-FERREIRA M, et al.Molecular typing of the yeast species Dekkera bruxellensis and Pichia guilliermondii recovered from wine related sources[J].International Journal of Food Microbiology, 2006, 106(1):79-84.
[45] CSOMA H,  CS-SZAB
CS-SZAB L, PAPP L A, et al.Application of different markers and data-analysis tools to the examination of biodiversity can lead to different results:A case study with Starmerella bacillaris (synonym Candida zemplinina) strains[J].FEMS Yeast Research, 2018, 18(5):foy021.
L, PAPP L A, et al.Application of different markers and data-analysis tools to the examination of biodiversity can lead to different results:A case study with Starmerella bacillaris (synonym Candida zemplinina) strains[J].FEMS Yeast Research, 2018, 18(5):foy021.
[46] BINATI R L, INNOCENTE G, GATTO V, et al.Exploring the diversity of a collection of native non-Saccharomyces yeasts to develop co-starter cultures for winemaking[J].Food Research International, 2019, 122:432-442.
[47] CORBU V, CSUTAK O.Biodiversity studies on Pichia kudriavzevii from romanian spontaneous fermented products[J].AgroLife Scientific Journal, 2020, 9(1):1-12.
[48] G-POBLETE C, PE A-MORENO I C, MARCOS ANTONIO DE MORAIS J Jr, et al.Biodiversity among Brettanomyces bruxellensis strains isolated from different wine regions of Chile:Key factors revealed about its tolerance to sulphite[J].Microorganisms, 2020, 8(4):557.
A-MORENO I C, MARCOS ANTONIO DE MORAIS J Jr, et al.Biodiversity among Brettanomyces bruxellensis strains isolated from different wine regions of Chile:Key factors revealed about its tolerance to sulphite[J].Microorganisms, 2020, 8(4):557.
[49] ESCRIBANO-VIANA R, GONZ LEZ-ARENZANA L, GARIJO P, et al.Selection process of a mixed inoculum of non-Saccharomyces yeasts isolated in the D.O.Ca.Rioja[J].Fermentation, 2021, 7(3):148.
LEZ-ARENZANA L, GARIJO P, et al.Selection process of a mixed inoculum of non-Saccharomyces yeasts isolated in the D.O.Ca.Rioja[J].Fermentation, 2021, 7(3):148.
[50] ALLAHYARI N.Molecular identification of wild non-Saccharomyces yeasts from wine by PCR-RFLP and strain differentiation by RAPD[D].Ankara:Middle East Technical University, 2020.
[51] SGOUROS G, CHALVANTZI I, MALLOUCHOS A, et al.Biodiversity and enological potential of non-Saccharomyces yeasts from Nemean vineyards[J].Fermentation, 2018, 4(2):32.
[52] NISIOTOU A, GYFTOGIANNI E, BANILAS G,et al.Evaluation of different molecular markers for genotyping non-Saccharomyces wine yeast species[J].Microbiology Research, 2022, 13(3):643-654.
[53] LI R R, FENG D P, WANG H, et al.Genetic diversity of non-Saccharomyces yeasts associated with spontaneous fermentation of Cabernet Sauvignon wines from Ningxia, China[J].Frontiers in Microbiology, 2023, 14:1253969.
[54] DE BARROS LOPES M, RAINIERI S, HENSCHKE P A, et al.AFLP fingerprinting for analysis of yeast genetic variation[J].International Journal of Systematic Bacteriology, 1999, 49(Pt 2):915-924.
[55] BASELGA I, ZAFRA O, PÉREZ LAGO E, et al.An AFLP based method for the detection and identification of indigenous yeast in complex must samples without a microbiological culture[J].International Journal of Food Microbiology, 2017, 241:89-97.
[56] ALBERTIN W, SETATI M E, MIOT-SERTIER C, et al.Hanseniaspora uvarum from winemaking environments show spatial and temporal genetic clustering[J].Frontiers in Microbiology, 2015, 6:1569.
[57] ESTEVE-ZARZOSO B, HIERRO N, MAS A, et al.A new simplified AFLP method for wine yeast strain typing[J].LWT-Food Science and Technology, 2010, 43(10):1480-1484.
[58] BANILAS G, SGOUROS G, NISIOTOU A.Development of microsatellite markers for Lachancea thermotolerans typing and population structure of wine-associated isolates[J].Microbiological Research, 2016, 193:1-10.
[59] VICENTE J, NAVASCUÉS E, BENITO S, et al.Microsatellite typing of Lachancea thermotolerans for wine fermentation monitoring[J].International Journal of Food Microbiology, 2023, 394:110186.
[60] CSOMA H, ACS-SZABO L, PAPP L A, et al.Characterization of Zygosaccharomyces lentus yeast in Hungarian botrytized wines[J].Microorganisms, 2023, 11(4):852.
[61] PFLIEGLER W P, HORV TH E, K
TH E, K LLAI Z, et al.Diversity of Candida zemplinina isolates inferred from RAPD, micro/minisatellite and physiological analysis[J].Microbiological Research, 2014, 169(5-6):402-410.
LLAI Z, et al.Diversity of Candida zemplinina isolates inferred from RAPD, micro/minisatellite and physiological analysis[J].Microbiological Research, 2014, 169(5-6):402-410.
[62] DIMOPOULOU M, HATZIKAMARI M, MASNEUF-POMAREDE I, et al.Sulfur dioxide response of Brettanomyces bruxellensis strains isolated from Greek wine[J].Food Microbiology, 2019, 78:155-163.
[63] 田进, 吴成, 杨金仙, 等.葡萄酒有孢汉逊酵母属分子指纹图谱分析[J].菌物学报, 2020, 39(4):755-765.TIAN J, WU C, YANG J X, et al.The molecular fingerprinting analysis of Hanseniaspora in wine[J].Mycosystema, 2020, 39(4):755-765.