随着人们健康意识的增强,虾类产品因其高蛋白、低脂肪的优点而广受欢迎。为最大程度保证虾体的新鲜程度,多采用低温保存运输的方式[1]。目前,在短途冰鲜运输多采用冰袋泡沫箱的方式达到保鲜的作用,运输期间可能存在运输时间较长,无法及时更换冰袋,导致贮存环境温度逐渐升高等问题,从而造成肌原纤维蛋白(myofibrillar proteins,MPs)的分解氧化进程加快,导致虾肉的品质发生相应变化。
南美白对虾(Litopenaeus vannamei,LV),又名白皮虾,是我国重要的养殖虾种[2]。哈氏仿对虾(Parapenaeopsis hardwickii,PH),又名滑皮虾,主要分布在我国黄海南部、东海和南海以西[3]。虾肉组织水分含量较高,易促进蛋白质的氧化变性,使虾肉品质降低[4]。MPs是肌肉蛋白质的重要组成部分,是主要由肌球蛋白、肌动蛋白和少量调节性结构蛋白等组成的蛋白质群[5],其结构性质与虾肉的品质密切相关。
当前,陈钰等[6]发现在4 ℃贮存条件下,LV品质不断降低,推断在该条件下的货架期为6 d。叶洲琳等[7]发现在冷藏期间PH肌肉的水分含量不断下降,肌原纤维间隙不断增大,虾肉劣变程度加深。王美婧[8]发现在短期冷藏过程中,肌原纤维蛋白发生了降解,蛋白质二级结构出现改变。然而以上研究主要局限于单一的LV和PH中MPs的贮存过程变化,对两者的MPs在不同贮存条件下两者产生的差异研究较少。因此,本实验以LV和PH的MPs为对象,阐明不同贮存环境对2种虾MPs的分子损伤程度,为针对南美白对虾和哈氏仿对虾的差异化冷藏保鲜技术开发提供理论支持。
1 材料与方法
1.1 材料与试剂
新鲜LV(体长10~12 cm)、新鲜PH(体长6~8 cm),浙江舟山国际水产城,将其置于保温箱中,采用碎冰均匀覆盖,30 min内运回实验室。
氯化钠、氯化镁、氯化钾、乙二胺四乙酸、磷酸氢二钠、磷酸二氢钠、磷酸二氢钾、溴酚蓝(分析纯),国药集团化学试剂有限公司;溴化钾(光谱纯),上海阿拉丁生化科技股份有限公司;总巯基试剂盒、总蛋白试剂盒、羰基试剂盒,南京建成生物工程研究所。
1.2 仪器与设备
TU-1810紫外可见分光光度计,北京普析通用仪器有限责任公司;NicoletiS50傅里叶红外光谱,美国赛默飞公司;WAVE-Ⅱ纳米粒度及Zeta电位分析仪,大昌洋行(上海)有限公司;BX43共聚焦显微拉曼光谱仪,崛场仪器有限公司;WIX-EP300基础电泳,伟克斯科技(北京)有限公司。
1.3 实验方法
1.3.1 分组及贮存环境
将LV和PH的MPs分为冷藏组和模拟运输贮存组。冷藏组环境为稳定4 ℃;模拟运输贮存环境为将冰袋放于-20 ℃冰箱中预冷,后使用冰袋对泡沫箱(长36 cm,宽26 cm,高22.5 cm)内部进行填充,将MPs溶液完全覆盖,将泡沫箱置于25 ℃稳定的环境下,每日记录箱内温度变化,贮存时间均为0~4 d。每日取样进行指标测定。
1.3.2 MPs提取
参照LI等[9]的方法提取MPs,略作修改。新鲜虾去除虾壳和虾线,绞肉机搅碎为肉糜。取虾肉糜,加入5倍体积提取缓冲液(6.1 mmol/L Na2HPO4,3.9 mmol/L NaH2PO4,0.1 mol/L NaCl,1 mmol/L EDTA,2 mmol/L MgCl2,pH值为7.0)混合匀浆(10 000 r/min,30 s)并离心(8 000 r/min,15 min,4 ℃),弃上清液,保留沉淀,重复上述操作3次。在沉淀加入5倍体积的0.1 mol/L NaCl,使用与上述相同条件均质离心2次,保留沉淀。将磷酸盐缓冲液(50 mmol/L PBS含0.42 mmol/L Na2HPO4,0.08 mol/L KH2PO4,0.6 mol/L NaCl,pH值为7.0)与沉淀物混合匀浆,静置提取2 h,离心(8 000 r/min,20 min,4 ℃)后使用3层纱布过滤,全程均在冰上操作,维持4 ℃温度,获得MPs溶液。
1.3.3 表面疏水性的测定
参考WANG等[10]的方法,取5 mg/mL的MPs溶液1 mL,空白对照组采用PBS 1 mL,加入200 μL溴酚蓝溶液(1.0 mg/mL,去离子水溶解),室温下充分混匀10 min后离心(10 000 r/min,15 min),取上清液进行10倍稀释,于595 nm处测定吸光度。表面疏水性以溴酚蓝结合量表示,计算如公式(1)所示:
溴酚蓝结合量![]()
(1)
式中:A1为空白样品吸光度;A2为测试样品吸光度。
1.3.4 总巯基含量测定
使用总巯基试剂盒进行测定,具体操作依据说明书进行。
1.3.5 羰基含量测定
使用羰基试剂盒进行测定,具体操作依据说明书进行。
1.3.6 粒径
参考WEI等[11]的方法略作修改。使用PBS调整MPs溶液质量浓度为2 mg/mL,采用纳米粒度仪测定粒径比例分布及平均粒径。聚焦时间60 s,折射率1.333%。
1.3.7 蛋白质二级结构测定
参照LI等[12]的方法,稍作修改。将MPs溶液进行冻干。精准称取1 mg样品与100 mg溴化钾,将二者充分混合研磨压片。室温下使用傅里叶红外光谱仪扫描压片谱带。仪器设置:范围为0~3 000 cm-1,分辨率为4 cm-1,扫描次数64次。
1.3.8 拉曼光谱
参照DIGVIJAY等[13]的方法,略作修改。通过激光显微拉曼光谱仪分析冷藏条件和模拟运输贮存条件0~4 d过程中,LV和PH的MPs二级结构组成变化情况。测试参数为:选用532 nm激光器,光谱扫描范围为2 800~3 100 cm-1,衰减片0.1%,扫描时间30 s,重复次数6次。
1.3.9 蛋白质三级结构测定
使用WANG等[14]的实验方法并略作修改。将肌纤维蛋白溶液稀释至0.5 mg/mL置于石英比色皿中,在荧光分光光度计中扫描,发射波长为280 nm,光谱范围为320 ~ 360 nm,激发和发射狭缝宽度均为5 nm,PMT电压为650 V,扫描速率1 000 nm/min。
1.3.10 SDS-PAGE
按照李晓等[15]的方法进行。采用预制凝胶(4%~12%),恒定电压模式,初始电压为60 V,后加大电压至120 V直至结束。
1.4 数据分析
所有数据来自3次重复的独立试验。使用SPSS Statistics 27、LabSpec 6和Origin 2022进行处理对数据进行统计分析,并通过单因素方差分析(analysis of variance,ANOVA)和邓肯检验(Duncan)确定平均值之间的显著性差异(P<0.05)。
2 结果与分析
2.1 模拟运输贮存温度变化
在模拟运输贮存的0、1、2、3、4 d中箱内温度分别为-19.7、0.7、7.1、20.2、24.5 ℃,在第2天时超过4 ℃冷藏组温度,在4 d逐渐与外部温度25 ℃趋于一致。综合短途运输时间以及泡沫箱内温度变化,本实验采用0~4 d贮存进行实验。
2.2 表面疏水性
表面疏水性可评判蛋白质分子内部疏水性氨基酸残基暴露程度,常以溴酚蓝结合量来表示[16]。由图1可知,LV和PH中溴酚蓝结合量存在较大差异。随着贮存时间的延长,2种虾的MPs表面疏水性均呈不断上升的趋势。在4 ℃冷藏4 d后,LV和PH中MPs的溴酚蓝结合量较初始分别上升了8.45 μg和16.49 μg。同时,在模拟运输贮存条件下,两者溴酚蓝结合量分别上升了11.50 μg和28.31 μg。这是由于随着贮存时间的延长,MPs结构展开,疏水性氨基酸残基暴露,与溴酚蓝结合点位增加,使得疏水性上升。而在第1天时,模拟运输贮存组的疏水性低于冷藏组,这是因为在模拟运输贮存过程中,第1天的温度显著低于4 ℃,MPs较为完整。在第0天时,PH组溴酚蓝结合量显著小于LV组,这可能是PH的MPs表面疏水基团较少。
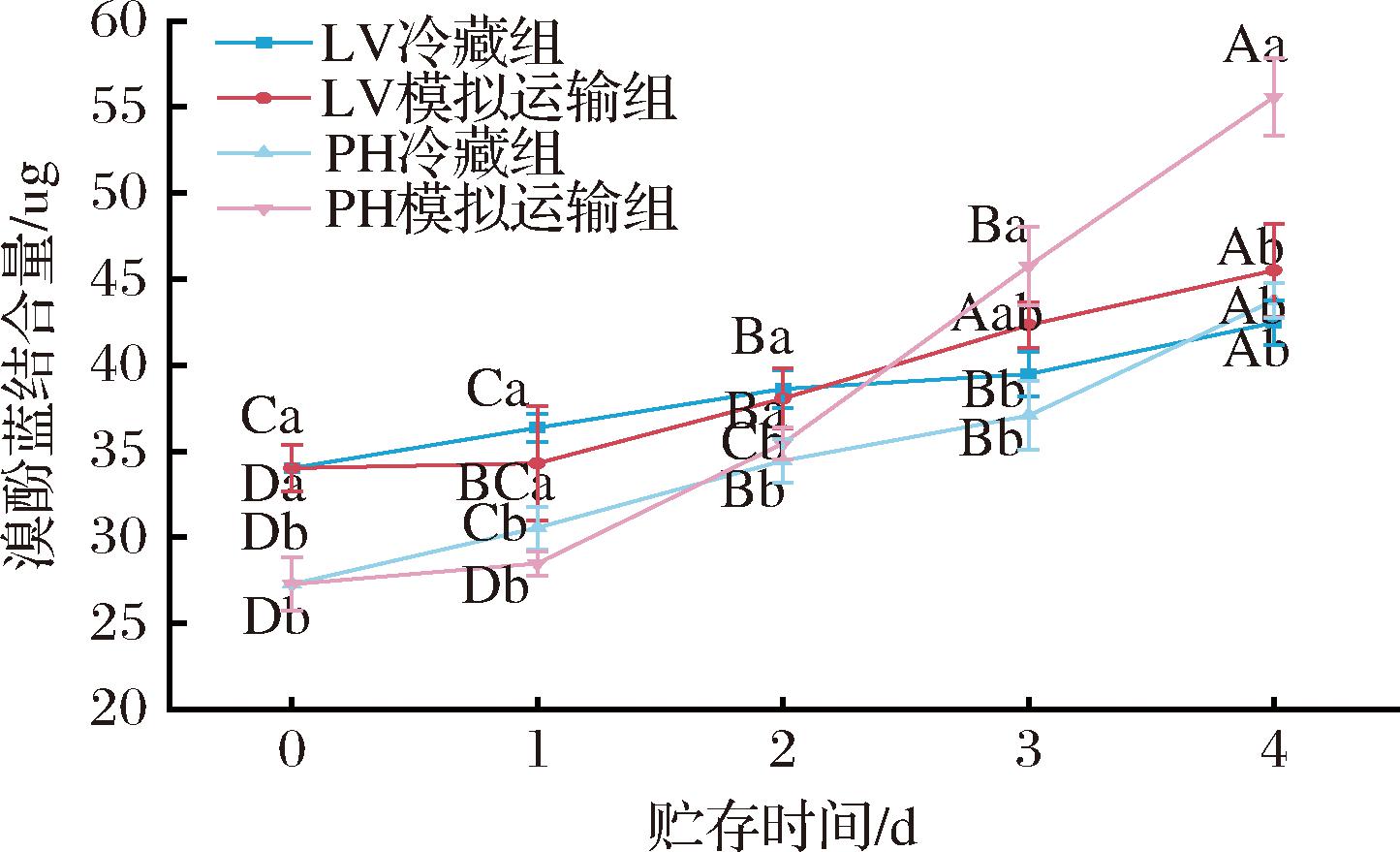
图1 贮存条件对LV和PH的MPs表面疏水性的影响
Fig.1 Effects of storage conditions on the surface hydrophobicity of LV and PH MPs
注:不同大写字母代表组内差异显著(P<0.05),不同小写字母代表组间差异显著(P<0.05)(下同)。
2.3 MPs总巯基含量
总巯基含量包括MPs表面和内部的巯基,总巯基含量越低说明蛋白质氧化程度越高[17]。由图2可知,随冷藏的延长,总巯基含量不断下降。经过4 d的贮存,在冷藏组和模拟运输贮存组中,LV的MPs总巯基含量较初始下分别下降了7.01%和12.92%;PH的MPs总巯基含量分别下降了10.29%和14.72%。其中模拟运输贮存组的下降幅度更加剧烈,可能是温度不断上升,加速了MPs的分解,暴露了更多的巯基点位,同时也加速了氧化的进程,促进了二硫键的形成,进一步使巯基含量下降造成的。其中PH的MPs总巯基初始值明显低于LV,在4 d的贮存时间中,其下降速度也明显高于LV组,推测PH的MPs可能具有更松散或更易展开的构象(如肌球蛋白头部区域更灵活),导致游离巯基更易暴露于氧化环境。两者在0 d时总巯基含量差异较大还可能与2种虾的物种差异和生存环境相关。林洪等[18]发现,养殖虾的各项稳定性指标均逊于海捕虾,这与本实验的研究结果一致。
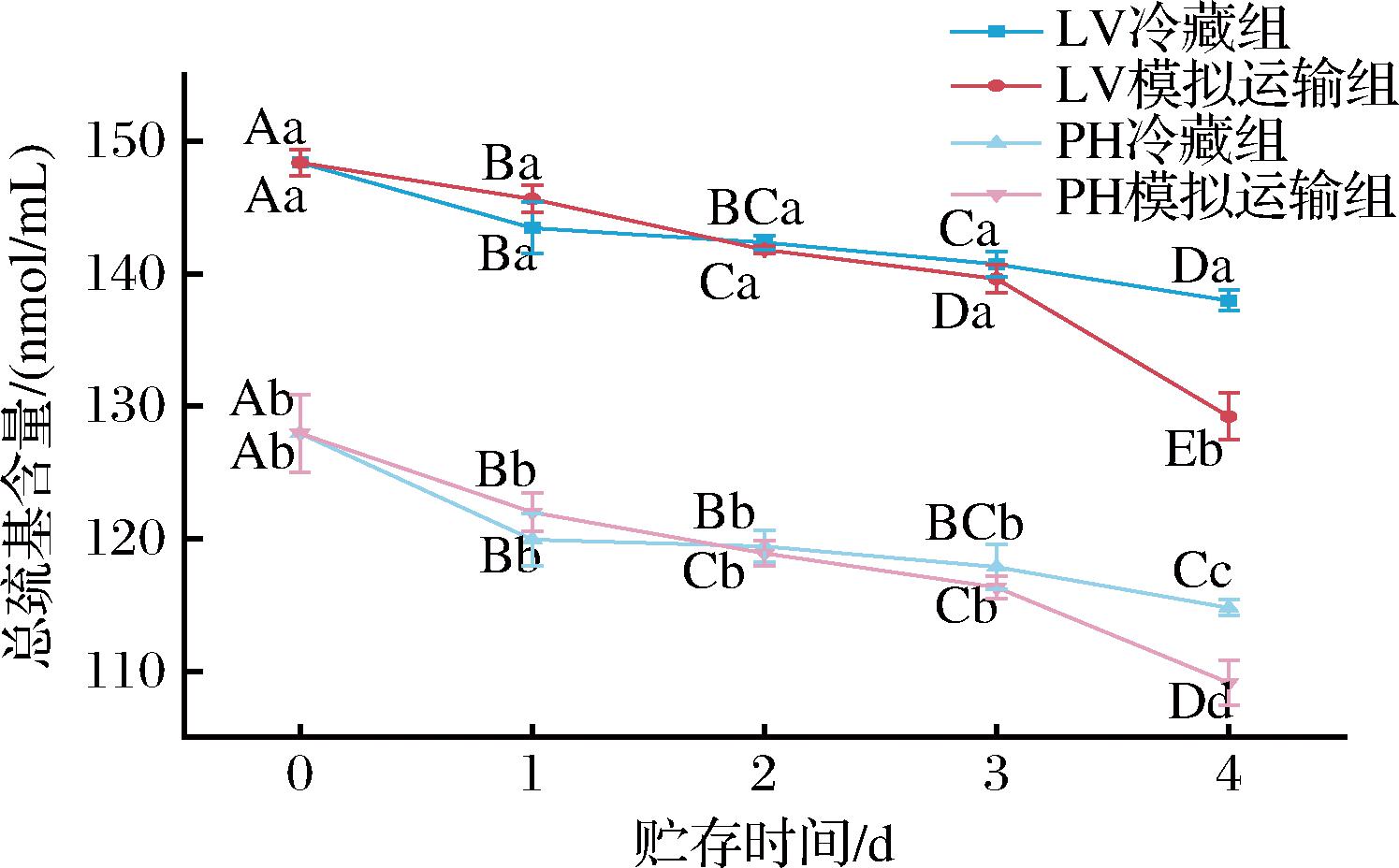
图2 贮存条件对LV和PH的MPs总巯基含量的影响
Fig.2 Effects of storage conditions on total sulfhydryl content of LV and PH MPs
2.4 MPs羰基含量
蛋白质羰基一般来源为蛋白质侧链氨基酸残基受到氧化损伤,因此羰基含量一般可作为判断蛋白质氧化程度的重要指标[19]。由图3可知,在0~4 d的贮存过程中,LV和PH的MPs羰基含量均呈现增加趋势。在冷藏组中,LV和PH的MPs羰基含量分别增加了0.43 nmol/mL和0.70 nmol/mL;在模拟运输贮存组中,两者羰基含量分别增加了0.76 nmol/mL和1.08 nmol/mL。模拟贮存组羰基含量增加幅度大于冷藏组,这一差异很可能是较高的温度促进了体系中活性氧自由基攻击MPs肽链,引发氧化反应并促进疏水性基团的暴露,而暴露的疏水性基团更易受到自由基的攻击,使MPs发生了更为剧烈的氧化损伤,最终导致其羰基衍生物的生成量和积累速率高于冷藏组。在贮存期间,PH的MPs羰基增加速率明显高于LV,推测可能是因为PH的MPs含有更多易被氧化的氨基酸(如赖氨酸、精氨酸、脯氨酸),其侧链易受活性氧攻击生成羰基化合物[4]。
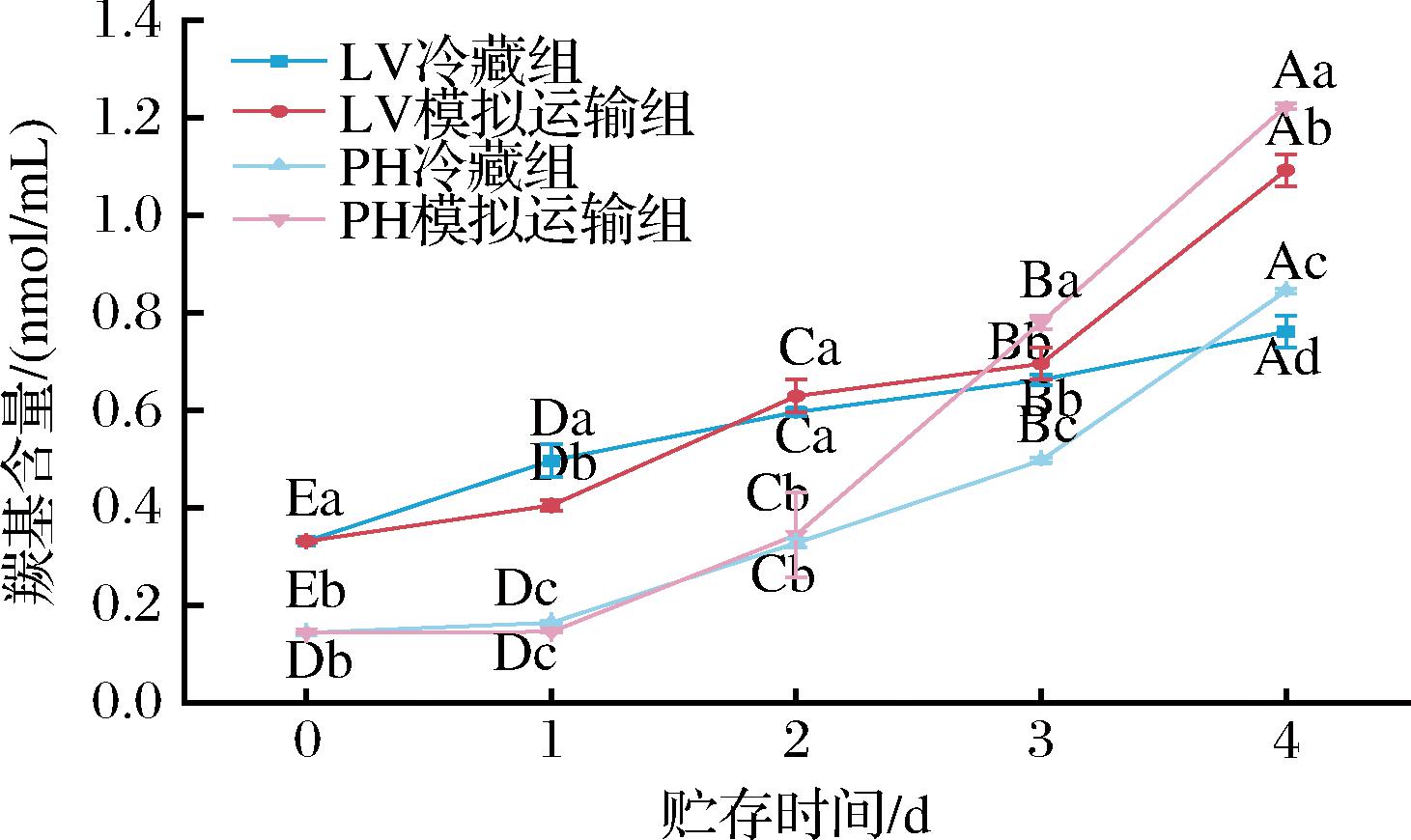
图3 贮存条件对LV和PH的MPs羰基含量的影响
Fig.3 Effect of storage conditions on carbonyl content of LV and PH MPs
2.5 粒径分布
随着贮存时间的延长,MPs的氧化和变性导致聚集体的形成,因此粒径分布和平均粒径可以表征MPs聚集程度[20]。由图4-A可知,可看出PH的MPs比LV的MPs的颗粒小。随着贮存时间的延长,2种虾的MPs粒径逐渐增大,其中模拟运输组的粒径增加幅度大于冷藏组。在图4-B显示PH的MPs大分子颗粒占比高于LV的MPs,表明PH的MPs更容易聚集。在0~4 d的贮存时间中,MPs的粒径峰逐渐右移,且最后一天模拟运输贮存组的大分子(>4 000 nm)占比高于冷藏组,原因是随着冷藏时间的延长,模拟运输贮存组的温度组间上升,MPs表面疏水性逐渐增加,从而絮凝形成聚集体,使得大分子颗粒占比增加。在贮存第1天时,冷藏组图谱出现粒径峰左移的趋势,这是由于MPs分解,小分子增加造成的。后续PH组的粒径峰偏移情况快于LV组,这可能是由于PH的颗粒较小,可能其更容易暴露内部基团,促进MPs聚集导致的。
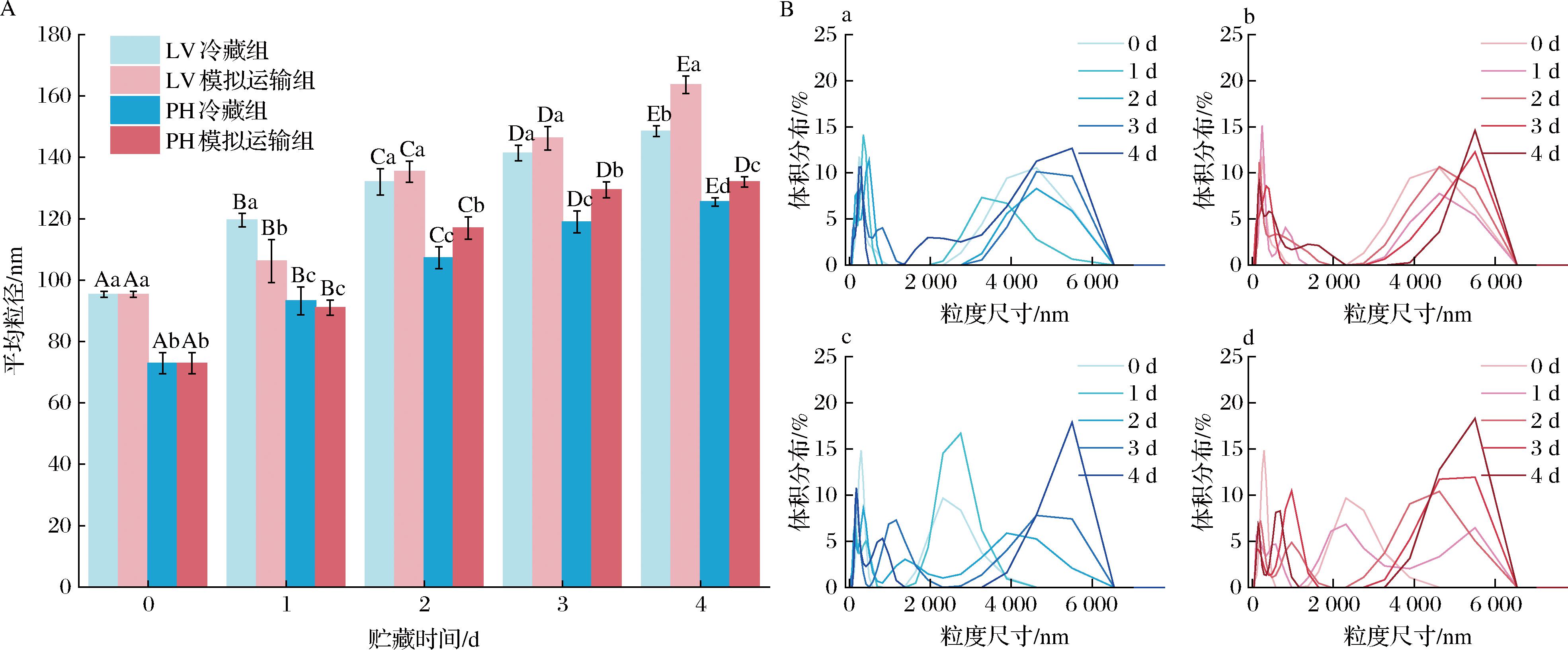
A-平均粒径图,B-粒径分布图(a-LV冷藏组;b-LV模拟运输贮存组;c-PH冷藏组;d-PH模拟运输贮存组)
图4 贮存条件对LV和PH的MPs粒径分布和平均粒径的影响
Fig.4 Effect of storage conditions on particle size distribution and mean particle size of LV and PH MPs
2.6 MPs二级结构
如图5所示,1 600~1 700 cm-1[1 550~1 660 cm-1(α-螺旋)、1 600~1 640 cm-1(β-折叠)、1 660~1 700 cm-1(β-转角)和1 640~1 650 cm-1(无规则卷曲)]是蛋白质最突出和敏感的振动带,与蛋白质的二级结构相关[21]。在2种虾中,LV冷藏组和模拟运输贮存组的α-螺旋分别降低了4.71%和4.91%,PH降低了10.76%和18.41%;LV冷藏组和模拟运输贮存组的β-折叠分别增加了7.69%和8.42%,PH组分别增加了14.03%和15.27%,由此得出,随时间的延长,模拟运输贮存组环境对MPs的影响大于冷藏组环境,推测是由于模拟运输贮存组的贮存温度不断上升,使得MPs分解,暴露出更多的氢键由疏水相互作用重排,进而在分子聚集过程中重新连接形成β-折叠使其含量上升,而MPs表面疏水性与α-螺旋呈负相关,其含量变化表明分子内部的疏水性位点暴露,导致疏水性增强,这与前文表面疏水性研究结果一致。在不同贮存条件下,海捕虾种(PH组)MPs的二级结构(如α-螺旋和β-折叠)所呈现的变化程度显著高于养殖虾种(LV组)。LV组(养殖虾)与PH组(海捕虾)分属不同虾种,其长期适应的生态环境、运动模式、能量代谢以及生长策略等存在显著区别。这些根本性的生物学差异,直接导致了其肌肉组织中MPs的组成本质不同,从而使海捕虾种(PH组)的MPs表现出相对更低的稳定性。
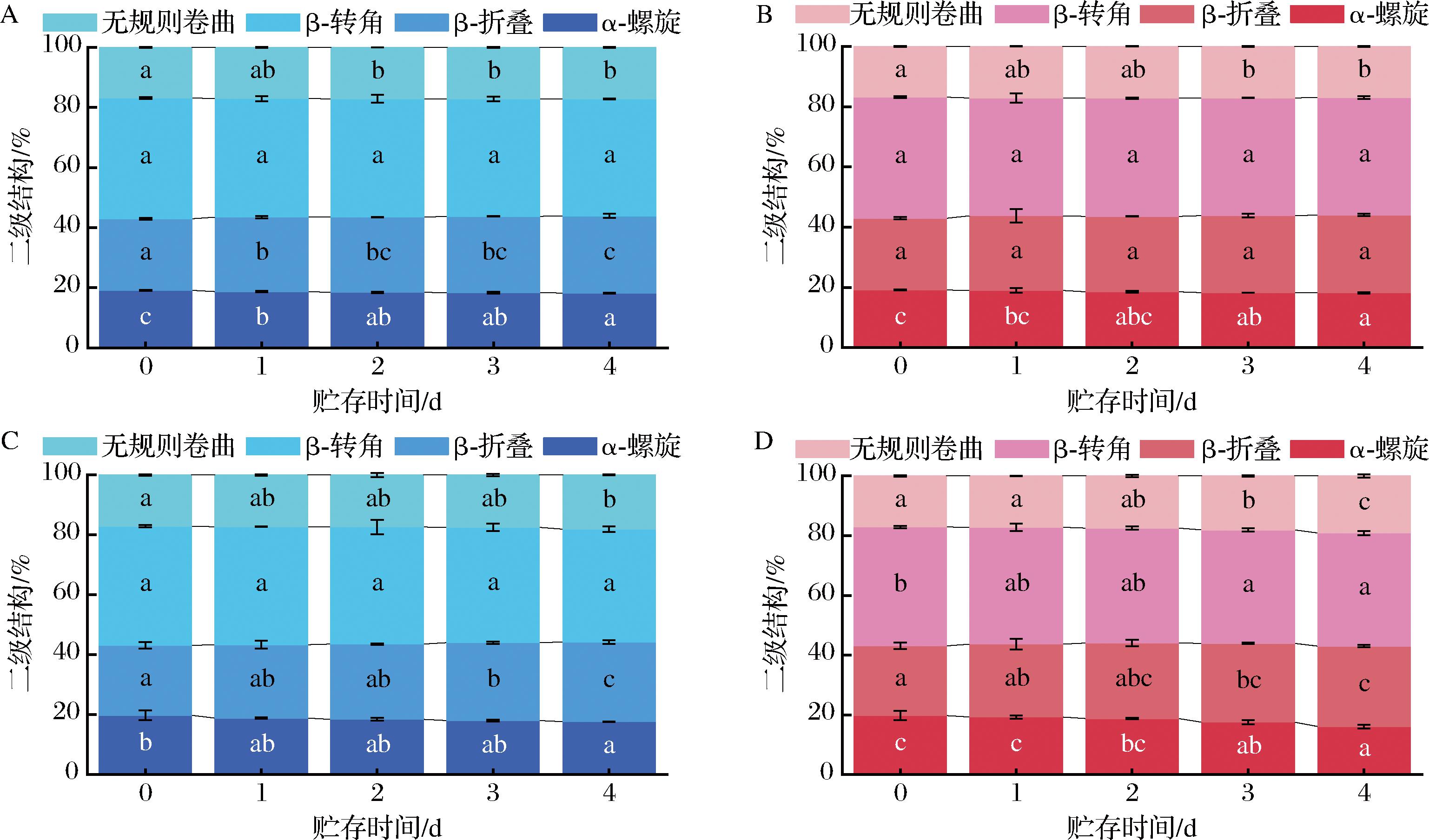
A-LV冷藏组;B-LV模拟运输贮存组;C-PH冷藏组;D-PH模拟运输贮存组
图5 贮存条件对LV和PH的MPs二级结构的影响
Fig.5 Effects of storage conditions on the secondary structure of LV and PH MPs
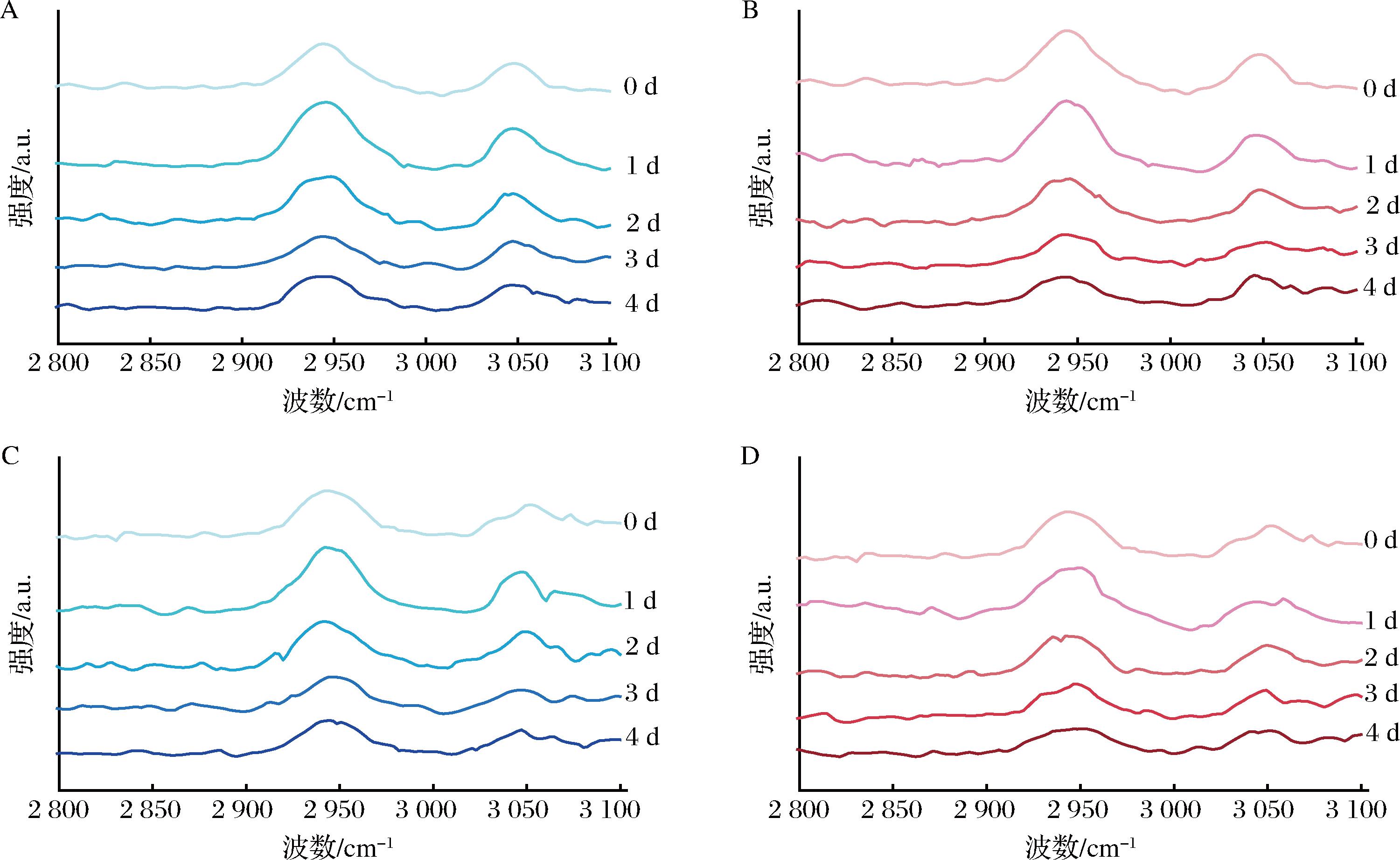
A-LV冷藏组;B-LV模拟运输贮存组;C-PH冷藏组;D-PH模拟运输贮存组
图6 贮存条件对LV和PH的MPs拉曼光谱的影响
Fig.6 Effects of storage conditions on raman spectra of LV and PH MPs
2.7 C—H特征峰
拉曼光谱与红外光谱互为互补关系。在拉曼光谱中甲基和亚甲基的不对称伸缩振动峰位通常在2 900~3 000 cm-1,主要来源于蛋白质疏水侧链中的脂肪族结构[22]。苯丙氨酸和酪氨酸的芳香环C—H振动峰位在3 000~3 100 cm-1。在图6中,所有组别的峰值随贮存时间的延长呈现先增加后持续减少的趋势。而在第1天时,所有峰值比第0天略有增加,可能是MPs的二级结构部分展开,原本包埋的疏水侧链暴露,这导致脂肪族C—H键和芳香族C—H键的振动信号增强,表现出峰强度升高,后续下降可能是由于随着贮存时间的延长使得MPs变性程度加深,α-螺旋结构含量减少,β-折叠结构可增加,MPs具有的特定的、相对有序的结构被破坏,C—H键的振动减弱,导致特征峰强度下降,这与HERRERO等[23]的研究结果类似。模拟运输贮存组的峰强变化程度比冷藏组的较多,原因是模拟运输贮存组的贮存温度随时间延长温度逐渐升高,使MPs分子的运动和聚集行为更为频繁。
2.8 MPs三级结构
内源性荧光主要来源于蛋白质中存在的色氨酸、酪氨酸和苯丙氨酸残基。色氨酸残基对周围微环境的变化高度敏感,因此在研究蛋白质三级结构变化方面具有重要价值[24]。图7显示了不同贮存条件对MPs内源荧光强度的影响。在第1天时,模拟运输贮存组的荧光强度高于冷藏组,原因是当天模拟运输贮存组的温度低于冷藏组,MPs相对完整。随着贮存时间的延长,荧光强度逐渐下降,表明蛋白质结构部分展开,使氨基酸残基和更多的发色团暴露于水环境中,导致荧光淬灭,从而引起荧光强度的下降。另外随着贮存时间的延长,疏水基团逐渐增加,疏水相互作用会使MPs逐渐聚集,使得发色基团被掩埋,进一步使MPs的荧光强度降低。
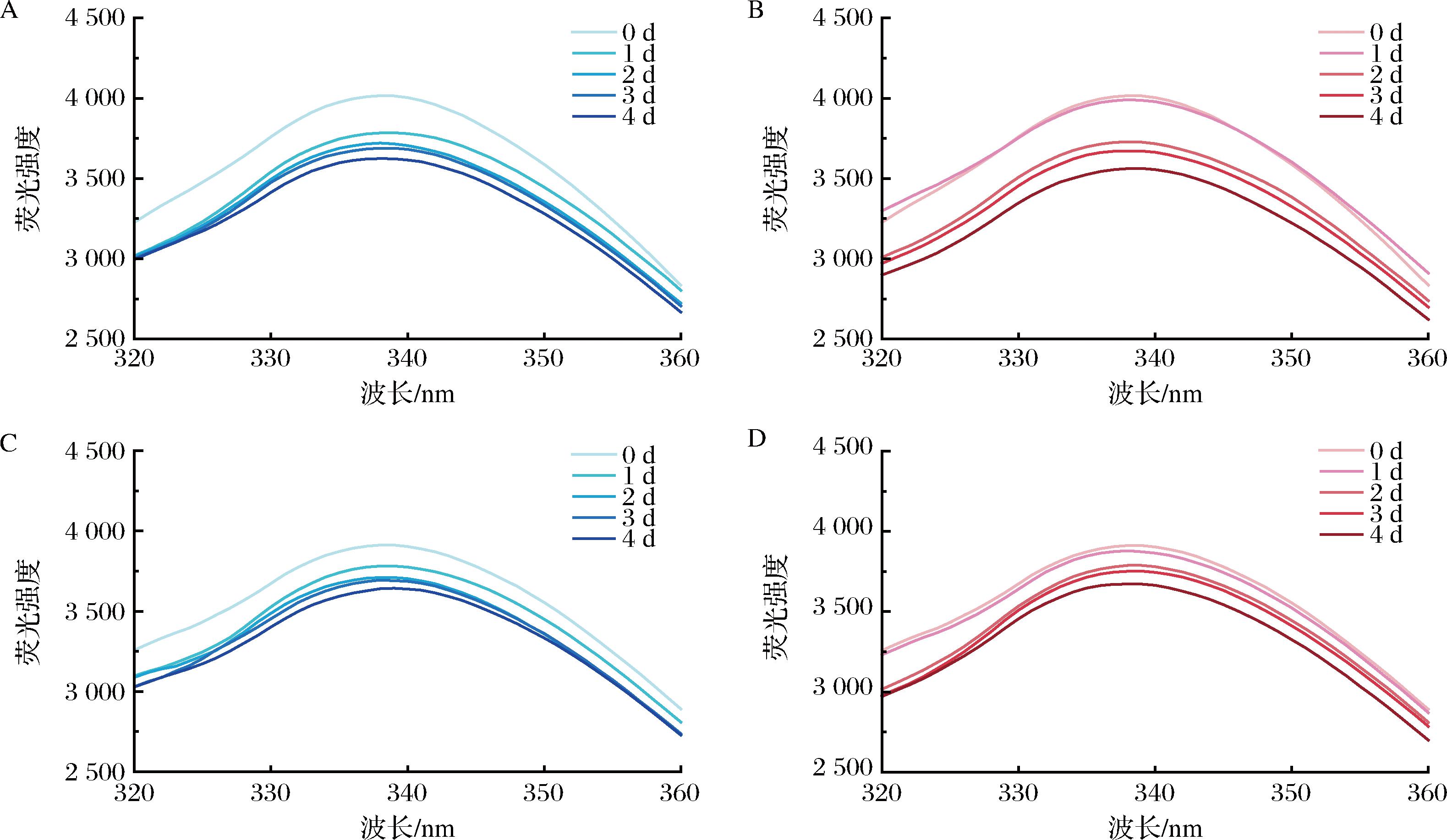
A-LV冷藏组;B-LV模拟运输贮存组;C-PH冷藏组;D-PH模拟运输贮存组
图7 贮存条件对LV和PH的MPs的内源性荧光光谱的影响
Fig.7 Effects of storage conditions on the endogenous fluorescence spectra of LV and PH MPs
2.9 SDS-PAGE蛋白分析
MPs分子高蛋白分子质量条带的模糊、弱化、消失、扩展以和低分子条带的出现或加深,是其降解的外在表现[25]。因此电泳条带的变化可以用来反映MPs的聚集和降解程度。由图8可看出,LV和PH冷藏组的电泳条带总体无太大变化,这表明冷藏期间MPs未出现明显的分解。而模拟运输贮存组第4天时LV组肌动蛋白条带颜色变浅,同时在100~135 kDa出现了新的条带,证明第4天时该组别MPs出现了降解和聚集。PH组随着贮存时间的延长,在模拟运输贮存条件下也出现了条带变浅,并且以肌动蛋白条带颜色变浅最为明显,证明在该条件下发生了MPs分子展开,肽键断裂等过程。
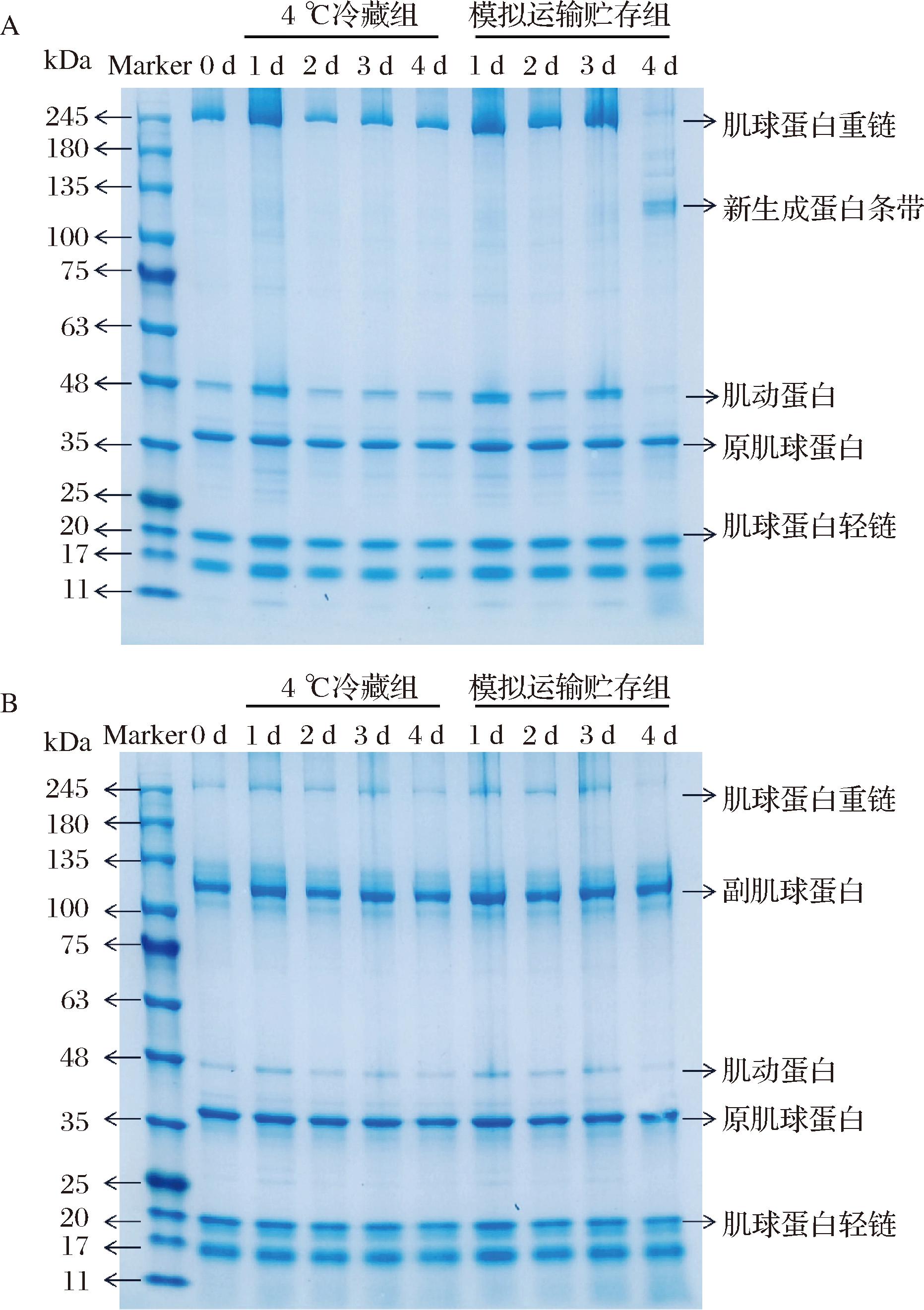
A-LV组;B-PH组
图8 贮存条件对LV和PH的MPs分子条带的影响
Fig.8 Effects of storage conditions on molecular bands of MPs in LV and PH
3 结论
本研究系统探究了4 ℃冷藏条件与模拟运输贮存条件对LV和PH的MPs的差异性和稳定性的影响。通过分析MPs理化指标(表面疏水性、总巯基含量、羰基含量、粒径、二三级结构及SDS-PAGE),发现在2种贮存条件下第4天时2种虾的MPs变性程度差异显著(P<0.05)。结果表明,LV的MPs稳定性显著高于PH(P<0.05),模拟运输贮存条件对MPs的破坏程度高于冷藏条件。因此在短期的虾类运输过程中,建议每24 h更换一次冰袋,控制运输环境温度维持在4 ℃以下并缩短运输时间,以减少对虾类MPs的破坏进而保持虾类的品质。
[1] 李肖婵, 林琳, 郑静静, 等.不同复合包装材料对即食小龙虾品质的影响[J].中国调味品, 2020, 45(3):118-124.LI X C, LIN L, ZHENG J J, et al.Effect of different compound packaging materials on the quality of ready-to-eat crayfish[J].China Condiment, 2020, 45(3):118-124.
[2] 武天昕.琼胶寡糖对冻藏南美白对虾的品质保障作用及影响机制[D].舟山:浙江海洋大学, 2022.WU T X.Effect and influence mechanism of jonesin oligosacc harides on quality assurance of frozen Penaeus vannamei[J].Zhoushan:Zhejiang Ocean University, 2022.
[3] 乔毅, 沈辉, 蒋葛, 等.我国哈氏仿对虾资源分布、保护及开发利用现状[J].浙江海洋大学学报(自然科学版), 2022, 41(6):550-557.QIAO Y, SHEN H, JIANG G, et al.Current situation of distribution, protection, development and utilization of Parapenaeopsis hardwickii in China[J].Journal of Zhejiang Ocean University (Natural Science), 2022, 41(6):550-557.
[4] 王潇, 张继光, 徐坤华, 等.3种海捕虾肌肉营养成分分析与品质评价[J].食品与发酵工业, 2014, 40(8):209-214.WANG X, ZHANG J G, XU K H, et al.Analysis and quality evaluation of nutrition in the muscle of three kinds of marine shrimps[J].Food and Fermentation Industries, 2014, 40(8):209-214.
[5] 李亚丽, 许玉娟, 徐幸莲.多酚对肌原纤维蛋白结构与功能特性的影响研究进展[J].食品与发酵工业, 2021, 47(19):296-306.LI Y L, XU Y J, XU X L.Research progress on the effect of polyphenols on the structural and functional properties of myofibrillar protein[J].Food and Fermentation Industries, 2021, 47(19):296-306.
[6] 陈钰, 庞文媛, 周三女, 等.不同贮藏温度对南美白对虾品质的影响[J].粮食与油脂, 2024, 37(2):85-89.CHEN Y, PANG W Y, ZHOU S N, et al.Effects of different storage temperatures on the quality of Litopenaeus vannamei[J].Grain and Oil, 2024, 37(2):85-89.
[7] 叶洲琳, 周婷, 水珊珊, 等.冷藏哈氏仿对虾肌肉品质和微生物群落组成变化[J].现代食品科技, 2025,41(8):131-139.YE Z L, ZHOU T, SHUI S S, et al.Changes in sword prawn muscle quality and microbial community (Parapenaeopsis hardwickii) during chilled storage[J].Modern Food Science and Technology, 2025,41(8):131-139.
[8] 王美婧.短期冷藏过程中乌鳢肌原纤维蛋白变化及其应用研究[D].杭州:浙江工商大学, 2020.WANG M J.Changes of myofibrillar protein in snakehead during short-term refrigeration and its application[D].Hangzhou:Zhejiang Gongshang University, 2020.
[9] LI J, DAI Z C, CHEN Z H, et al.Improved gelling and emulsifying properties of myofibrillar protein from frozen shrimp (Litopenaeus vannamei) by high-intensity ultrasound[J].Food Hydrocolloids, 2023, 135:108188.
[10] WANG H H, SONG Y Y, LIU Z Q, et al.Effects of iron-catalyzed and metmyoglobin oxidizing systems on biochemical properties of yak muscle myofibrillar protein[J].Meat Science, 2020, 166:108041.
[11] WEI L, CAO L W, XIONG S B, et al.Effects of pH on self-assembly of silver carp myosin at low temperature[J].Food Bioscience, 2019, 30:100420.
[12] LI K, FU L, ZHAO Y Y, et al.Use of high-intensity ultrasound to improve emulsifying properties of chicken myofibrillar protein and enhance the rheological properties and stability of the emulsion[J].Food Hydrocolloids, 2020, 98:105275.
[13] DIGVIJAY, KELLY A L, LAMICHHANE P.Ice crystallization and structural changes in cheese during freezing and frozen storage:Implications for functional properties[J].Critical Reviews in Food Science and Nutrition, 2025, 65(3):527-550.
[14] WANG Z M, HE Z F, EMARA A M, et al.Effects of malondialdehyde as a byproduct of lipid oxidation on protein oxidation in rabbit meat[J].Food Chemistry, 2019, 288:405-412.
[15] 李晓, 王颖, 刘洪军, 等.0 ℃贮藏下南美白对虾品质变化研究[J].核农学报, 2020, 34(12):2734-2741.LI X, WANG Y, LIU H J, et al.Quality changes of pacific white shrimp (Litopenaeus vannamei) during 0 ℃ storage[J].Journal of Nuclear Agricultural Sciences, 2020, 34(12):2734-2741.
[16] 董智铭, 姜萩婉, 蒋泽临, 等.超声时间对牛肉干品质及其肌原纤维蛋白结构的影响[J].食品工业科技, 2023, 44(20):36-42.DONG Z M, JIANG Q W, JIANG Z L, et al.Effect of ultrasonic time on quality characteristics and myofibrillar protein structure of beef jerky[J].Science and Technology of Food Industry, 2023, 44(20):36-42.
[17] LI Y, LI X, WANG J Z, et al.Effects of oxidation on water distribution and physicochemical properties of porcine myofibrillar protein gel[J].Food Biophysics, 2014, 9(2):169-178.
[18] 林洪, 姜凤英, KHALIDJAMIL, 等.养殖和海捕对虾加热后蛋白特性变化的比较研究[J].水产学报, 1998,22(2):48-52.LIN H, JIANG F Y, KHALIDJAMIL, et al.Comparative studies on changes of actomyosin in cultured and wild prawns by thermal treatment[J].Journal of Fisheries of China, 1998,22(2):48-52.
[19] 郑文雄, 杨榕琳, 水珊珊, 等.热加工对3种带鱼肌球蛋白功能特性的影响[J].食品科学, 2024, 45(7):211-217.ZHENG W X, YANG R L, SHUI S S, et al.Effect of heat processing on the functional properties of myosin in three kinds of hairtail[J].Food Science, 2024, 45(7):211-217.
[20] MI H B, LIANG S Y, LI Z H, et al.Effect of corn starch on the structure, physicochemical and gel properties of hairtail (Trichiurus haumela) myosin[J].International Journal of Food Science and Technology, 2021, 56(6):2843-2852.
[21] SUN J, HUANG Y Q, LIU T M, et al.Evaluation of crossing-linking sites of egg white protein-polyphenol conjugates:Fabricated using a conventional and ultrasound-assisted free radical technique[J].Food Chemistry, 2022, 386:132606.
[22] LEELAPONGWATTANA K, BENJAKUL S, VISESSANGUAN W, et al.Raman spectroscopic analysis and rheological measurements on natural actomyosin from haddock (Melanogrammus aeglefinus) during refrigerated (4 ℃) and frozen (-10 ℃) storage in the presence of trimethylamine-N-oxide demethylase from kidney of lizardfish (Saurida tumbil)[J].Food Chemistry, 2008, 106(3):1253-1263.
[23] HERRERO A M, CARMONA P, L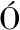 PEZ-L
PEZ-L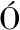 PEZ I, et al.Raman spectroscopic evaluation of meat batter structural changes induced by thermal treatment and salt addition[J].Journal of Agricultural and Food Chemistry, 2008, 56(16):7119-7124.
PEZ I, et al.Raman spectroscopic evaluation of meat batter structural changes induced by thermal treatment and salt addition[J].Journal of Agricultural and Food Chemistry, 2008, 56(16):7119-7124.
[24] YU L, LEI Y Z, MA Y, et al.A comprehensive review of fluorescence correlation spectroscopy[J].Frontiers in Physics, 2021, 9:644450.
[25] 朱迎春, 马俪珍, 党晓燕, 等.不同天然保鲜液对气调包装冰温贮藏鲶鱼片品质的影响[J].农业工程学报, 2017, 33(1):292-300.ZHU Y C, MA L Z, DANG X Y, et al.Effects of different natural preservative on catfish (Clarias gariepinus) fillet quality during storage with combination of super-chilling and high-CO2 packaging[J].Transactions of the Chinese Society of Agricultural Engineering, 2017, 33(1):292-300.