当前全球生物安全形势日趋严峻,据估计,全球每年发生15亿例微生物感染病例,导致460万人死亡[1],如2017年法国沙门氏菌污染、2018年荷兰奶粉阪崎肠杆菌污染以及后来的法国奶酪大肠杆菌污染等,给人们带来严重的生命财产损失。随着食源性疾病在各国频繁爆发,食品安全问题受到广泛重视。食源性疾病主要是由致病细菌引起,如大肠杆菌、沙门氏菌、单增李斯特菌、金黄色葡萄球菌、霍乱志贺氏菌、小肠结肠炎耶尔森菌、罗诺杆菌和空肠弯曲杆菌等[2],当人们误食被食源性致病菌污染的食物时,可能会产生呕吐、腹泻甚至死亡[3]。因此,需要准确快速检测食品中的致病菌以确保食品安全和人类健康。
目前用于食源性致病菌的检测方法包括传统培养法[4]、酶联免疫法[5](enzyme linked immunosorbent assay, ELISA)和PCR[6]技术等,这些方法检测耗时长、流程烦琐,且需要昂贵的仪器和专业的操作人员,在一定程度上限制了现场检测。纳米材料在食源性致病菌检测中的应用可以替代传统检测方法中的诸多弊端,具有操作简便、节省人力物力、准确性高等优点,因此在食品检测、生物医学和农业等方面有广泛的研究和发展[7-9]。
纳米科学始于20世纪80年代,纳米技术则是运用原子或分子层级操控来创造新型物质的科技领域。按照尺寸的不同,纳米材料大致分为4种类型:纳米颗粒(零维)、纳米纤维(一维)、纳米薄膜(二维)以及纳米块材(三维)。所有尺寸均为纳米级的纳米材料,即尺度低于100 nm的纳米材料被称为零维纳米材料,其主要研究对象集中在1~100 nm尺寸范围内[10-11]。这类材料因具有突出的电学、光学、磁学、化学和力学性能而备受瞩目[12-13]。举例来说,如金纳米颗粒受益于其表面等离子体共振效应,能够显著增强光学信号,从而大幅提高检测灵敏度;量子点因其尺寸与发射波长之间的关系,能够实现多色荧光编码,从而提供高灵敏度的检测手段;碳纳米管由于其具备高比表面积、出色的电导性能和良好的生物相容性,特别适合应用于构建电化学和光学传感器来检测食源性致病菌。本文概述了金属纳米颗粒、无机非金属纳米颗粒以及碳基纳米材料这三大类主流纳米材料的检测原理、性能特点及技术优势,综述了近5年来各纳米材料在食源性致病菌检测领域的最新研究进展,重点总结了各材料在实际应用中的局限性,并对未来发展趋势提出了见解,以期为该领域的进一步研究提供思路和一定的理论依据。
1 金属纳米材料
1.1 金纳米颗粒(aurum nanoparticles, AuNPs)
AuNPs具有特定的局域表面等离子体共振(localized surface plasmon resonance, LSPR)效应,当其聚集状态改变时,会引发溶液颜色的显著变化[14]。通过将AuNPs表面修饰特定的识别分子(如抗体、核酸适配体等),使其与食源性致病菌特异性结合,导致AuNPs聚集,产生颜色变化,实现对细菌的直观、快速检测[15]。例如,YAN等[16]通过用噬菌体T156功能化半胱胺(cysteamine,CS)稳定的金纳米颗粒(CS-AuNPs)获得沙门氏菌的纳米探针(CS-AuNPs@phage-T156),利用比色法检测食源性沙门氏菌。结果在目标沙门氏菌存在下,CS-AuNPs@phage-T156特异性识别并吸附在沙门氏菌表面,诱导金纳米颗粒聚集,颜色由红色变为紫色,实现视觉检测(图1),该方法的检出限为12 CFU/mL。GUO等[17]采用由微小Au纳米线组成的巨型Au囊泡来检测副溶血性弧菌,Au囊泡可以与被抗体功能化载玻片捕获的副溶血性弧菌结合,并进一步被银染成灰色。与检出限(limit of detection, LOD)为1 000 CFU/mL的Au纳米球相比,基于Au纳米线的银染法在比色法中的LOD为10 CFU/mL。HUA等[18]通过卵黄免疫球蛋白与脲酶标记金纳米棒,选择性地与金黄色葡萄球菌结合。在金黄色葡萄球菌存在的情况下,它会与纳米棒和磁珠结合,整个复合物会与上清液磁分离。在这种情况下,酚酞试纸会呈白色,结果为阳性。在没有金黄色葡萄球菌存在的情况下,纳米棒会留在上清液中并将尿素催化成![]() 和OH-,这导致pH值增加,酚酞试纸颜色从白色变为粉红色,结果为阴性。该方法的LOD为476 CFU/mL,无需仪器即可在20 min内完成,适合现场检测。此外,该生物传感器不受单核细胞增生李斯特菌、鼠伤寒沙门氏菌、大肠杆菌O157:H7和副溶血性弧菌等几种常见食源性病原体的干扰,对金黄色葡萄球菌具有高度特异性。YANG等[19]利用AuNPs和多壁碳纳米管(multiwalled carbon nanotube,MWCNT),研制了一种基于智能手机的比色传感器,通过智能手机RGB分析监测AuNPs的颜色变化来指示不同浓度的大肠杆菌O157:H7,对在牛奶中样品中大肠杆菌O157:H7的检测达到良好的灵敏度和特异性,LOD为5.24×102 CFU/mL。
和OH-,这导致pH值增加,酚酞试纸颜色从白色变为粉红色,结果为阴性。该方法的LOD为476 CFU/mL,无需仪器即可在20 min内完成,适合现场检测。此外,该生物传感器不受单核细胞增生李斯特菌、鼠伤寒沙门氏菌、大肠杆菌O157:H7和副溶血性弧菌等几种常见食源性病原体的干扰,对金黄色葡萄球菌具有高度特异性。YANG等[19]利用AuNPs和多壁碳纳米管(multiwalled carbon nanotube,MWCNT),研制了一种基于智能手机的比色传感器,通过智能手机RGB分析监测AuNPs的颜色变化来指示不同浓度的大肠杆菌O157:H7,对在牛奶中样品中大肠杆菌O157:H7的检测达到良好的灵敏度和特异性,LOD为5.24×102 CFU/mL。
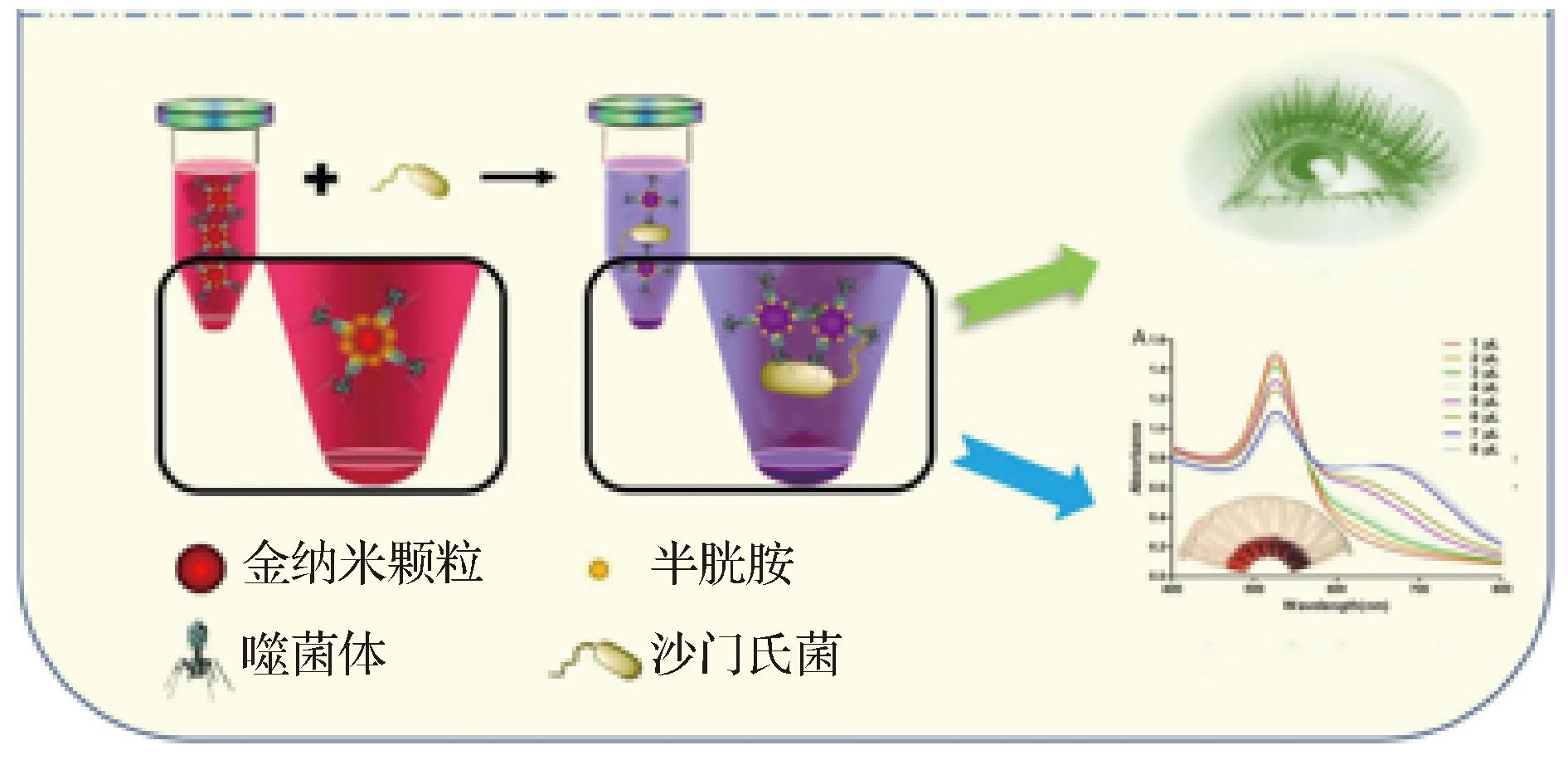
图1 基于CS-AuNPs@phage-T156介导的比色检测原理[16]
Fig.1 Based on the colorimetric detection principle mediated by CS-AuNPs@phage-T156[16]
除了颜色变化外,AuNPs可作为表面增强拉曼散射(surface-enhanced raman spectroscopy, SERS)基底,通过吸附特定标记分子或直接与食源性致病菌相互作用,增强其拉曼散射信号,实现对细菌的高灵敏度检测[20]。ZENG等[21]开发了一种基于AuNPs衬底的固相高灵敏度SERS平台,通过对样品中的4种病原体进行检测,验证了SERS分析的有效性和灵敏性,并结合主成分分析(principal component analysis,PCA)和层次聚类分析(hierarchical cluster analysis,HCA)进一步实现了病原体的分离和鉴定,说明该方法可以有效地用于病原菌的识别,对促进食源性病原体的快速检测和食品安全具有巨大的前景。
AuNPs在食源性致病菌检测中具有高灵敏度、多样化的检测模式、便捷操作和良好生物相容性等优点,但同时也面临纳米颗粒聚集[22]、表面修饰复杂性、成本与标准化以及环境影响等问题。为解决这些问题,今后应更加关注优化AuNPs的表面修饰、提高其生物相容性和稳定性,以及探索更经济的制备方法等。
1.2 银纳米颗粒(argentum nanoparticles, AgNPs)
AgNPs因其微小的粒径、超大的表面积和生物相容性而被认为对包括细菌、病毒在内的各种病原体具有显著的抗菌作用[23]。已经有研究证明AgNPs对一些食源性细菌具有杀菌活性,例如大肠杆菌、金黄色葡萄球菌[24]、铜绿假单胞菌、肠沙门氏菌、蜡样芽孢杆菌[25]以及单增李斯特菌[26]。BEGUM等[27]通过测定最低抑菌浓度(minimal inhibitory concentration, MIC)来评估4种不同类型的AgNPs对生长在水稻中的大肠杆菌O157:H7和鼠伤寒沙门氏菌的抗菌作用。研究结果显示,这些AgNPs展现出显著的抗菌效能,其MIC仅为62.5×10-6。ZHU等[28]提出了一种Au@Ag@MPBA标签辅助SERS系统,用于筛选食源性病原体。首先通过在Au核上原位形成Ag壳层来合成金和银核壳纳米颗粒(Au@AgNPs)作为SERS底物,并利用4-巯基苯硼酸(4-mercaptophenylboronic acid,4-MPBA)作为拉曼报告分子和细菌识别元件对Au@AgNPs进行功能化。基于细菌抑制盐诱导聚集的检测机制,通过鉴定4-MPBA的拉曼信号变化间接检测病原菌,构建了标记SERS方法(图2),对鱼类样品中人工污染的金黄色葡萄球菌、大肠杆菌和副溶血性弧菌进行检测,根据病原体的对数浓度绘制标签的SERS强度(56~56×105CFU/mL)的检测灵敏度为16 CFU/mL,因此该系统在实际环境中提供了一种快速、灵敏的病原菌筛选方法。
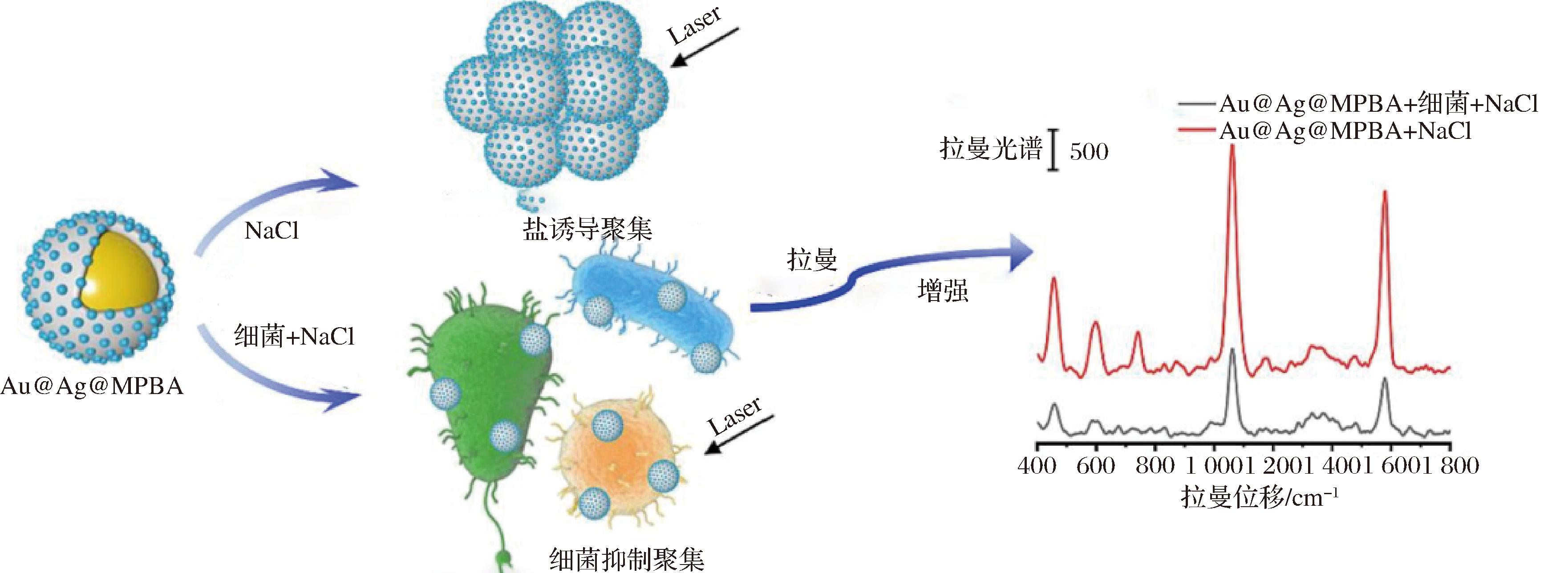
图2 建立的细菌抑制盐诱导聚集的病原体(金黄色葡萄球菌、大肠杆菌和副溶血性弧菌)检测的SERS平台示意图[28]
Fig.2 Schematic illustration of the established bacteria inhibiting salt-induced aggregation SERS-platform for pathogens (Staphylococcus aureus, Escherichia coli, and Vibrio parahaemolyticus) detection[28]
尽管AgNPs在抗菌、检测等方面展现出诸多优势,但由于其对某些生物体具有一定的毒性作用[29],在食源性致病菌检测领域的实际应用受到了一定的限制。在AgNPs颗粒应用方面,应结合其他新技术进一步提高其检测的灵敏度、特异性及多重靶标检测。通过优化AgNPs的表面修饰技术,开发更具特异性的识别分子,如新型适配体或抗体,提高其与食源性致病菌的结合特异性,减少非特异性结合,同时结合先进的信号放大技术,如SERS、电化学信号放大等,进一步提高检测灵敏度,实现对更低浓度致病菌的检测。利用AgNPs可多功能化修饰的特点,将多种不同的识别分子固定在其表面,实现对多种食源性致病菌的同时检测,提高检测效率,满足复杂食品样品中多菌检测的需求。
1.3 金属有机框架(metal-organic frameworks, MOFs)
MOFs是一类高度有序的三维网状多孔晶体材料,其结构特征是由无机金属离子或金属簇与有机配体通过配位键相互连接而成,因其比表面积大、结构稳定、孔径可调而备受关注[30]。含有不同金属和有机配体成分的MOFs通过其结构的多样性、功能的可调控性,展现出丰富的催化性、电化学性和光学活性[31]。图3展示了基于MOF的纳米复合材料的分类[32]。LI等[33]成功构建了基于脲酶包封的MOFs的免疫测定,以pH计为读数灵敏检测食源性病原体的方法。首先由脲酶包封以沸石咪唑酸盐框架-90(ZIF-90)作为的MOF模型,形成U@ZIF-90,这一过程放大了检测信号,然后U@ZIF-90偶联猪IgG抗体形成U@ZIF-90/IgG,建立了以便携式pH计为读数的ELISA检测金黄色葡萄球菌的方法,具有较高的灵敏度和选择性(图4)。结果表明,该酶联免疫吸附试验对金黄色葡萄球菌的LOD为1.96 CFU/mL,线性响应范围为10~109 CFU/mL。随后,GUO等[34]开发的生物传感器创新性地结合了PtNPs@MOFs复合材料的催化性能、氧气的生成、CaO的化学反应以及智能手机热传感器的便捷检测手段,构建了一种新型的细菌检测系统,该系统在1 h内对沙门氏菌LOD低至93 CFU/mL。
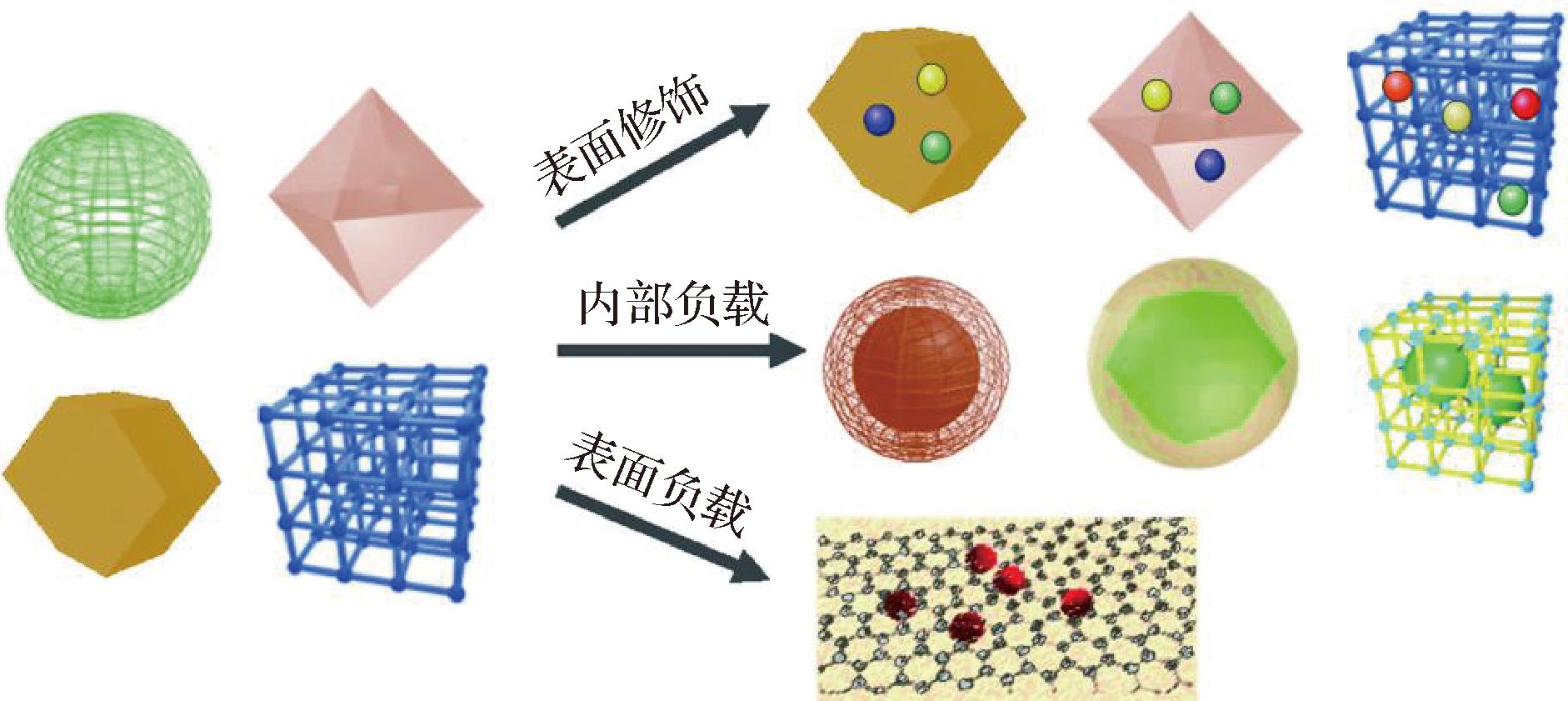
图3 基于MOF的纳米复合材料的设计示意图[32]
Fig.3 Design diagram of MOF-based nanocomposites[32]
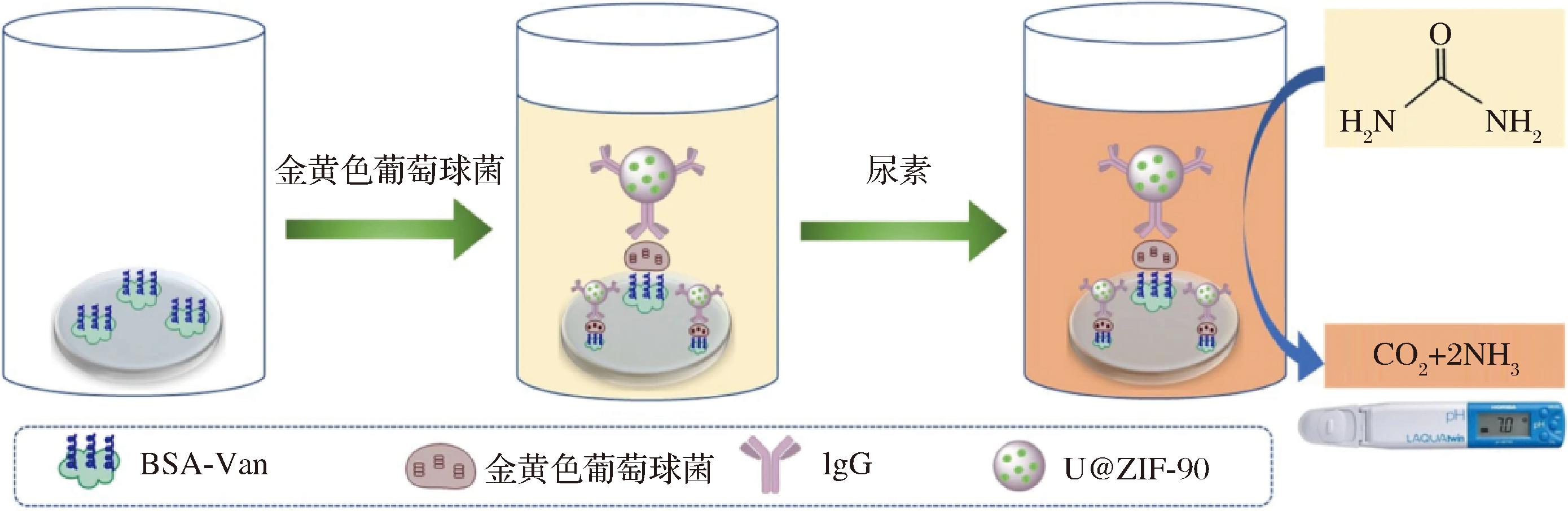
图4 基于U@ZIF-90/IgG构建用于金黄色葡萄球菌检测的ELISA图[33]
Fig.4 Illustration of the construction of ELISA based on U@ZIF-90/IgG for S.aureus detection[33]
注:Van:vancomycin(万古霉素)。
MOFs作为一种新兴微孔材料,在食源性致病菌检测领域展现出了巨大的潜力。然而,要实现其广泛应用还需克服与合成、稳定性和工艺适应性相关的一些挑战。
2 无机非金属纳米材料
2.1 量子点(quantum dots, QDs)
QDs是一种无机荧光半导体纳米晶体,其直径通常为1~10 nm[35],每个纳米颗粒由大约100~10 000个原子组成,能够发射跨越紫外至红外波段的光线,且其发射强度之高足以实现亚细胞水平的精确检测[36]。基于量子效应,量子点在受到光激发时会发生荧光现象,即光致发光(photoluminescence, PL),其原理如图5所示。
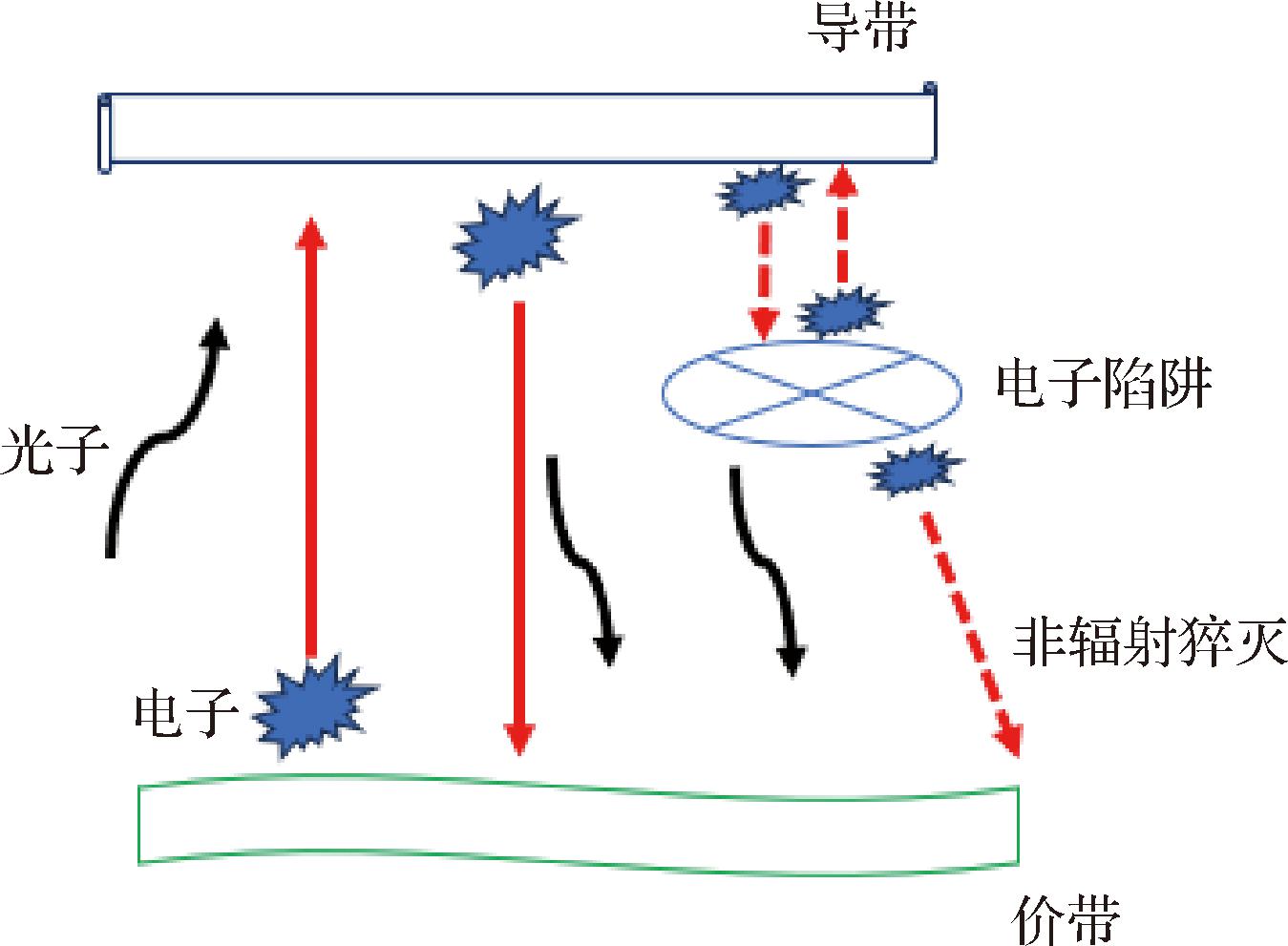
图5 量子点光致发光原理图
Fig.5 Schematic diagram of quantum dots photoluminescence
量子点之所以备受瞩目,主要因其具备以下优点:卓越的光稳定性、高量子产率、宽广的吸收光谱、显著的大消光系数以及宽泛的激发光谱。尤为重要的是,通过精确调控量子点的尺寸和化学成分,可以灵活调整其发射光谱[37]。这意味着,仅需使用单一激发光源,即可激活不同发射波长的量子点,从而实现对多种致病菌的同时定量检测,显著增强了检测的便携性和灵敏度。
HU等[38]开发了一种量子点纳米珠生物传感器用来快速筛选和定量检测沙门氏菌。通过在聚合物纳米球表面逐层组装量子点来制备的量子点纳米珠,不仅继承了高分子纳米球易于操作的特性和胶体稳定性,而且表现出优异的荧光特质。利用量子点纳米珠作为信号报告器,成功设计了一种灵敏、特异、准确的沙门氏菌侧流免疫检测方法。该传感器在缓冲液中LOD为5×103 CFU/mL,在肉汤中LOD为5×104 CFU/mL,对沙门氏菌的检测灵敏度是商用侧流免疫层析法检测(lateral flow immunochromatography assay,LFIA)的4~40倍。ZHANG等[39]制备了碳点适配体复合物,用于定量鉴定蛋壳和自来水溶液中的鼠伤寒沙门氏菌,检测范围为103~105 CFU/mL,LOD为50 CFU/mL。ANGELOPOULOU等[40]利用3D打印技术构建了一种电化学免疫传感器,结合夹心免疫测定法、Cd/Se ZnS QDs标记以及阳极溶出伏安法(anodic stripping voltammetry, ASV),对新鲜鸡肉中鼠伤寒沙门氏菌进行快速、灵敏、特异性定量检测(图6),该方法能在25 min检测到低至5 CFU/mL的鼠伤寒沙门氏菌。
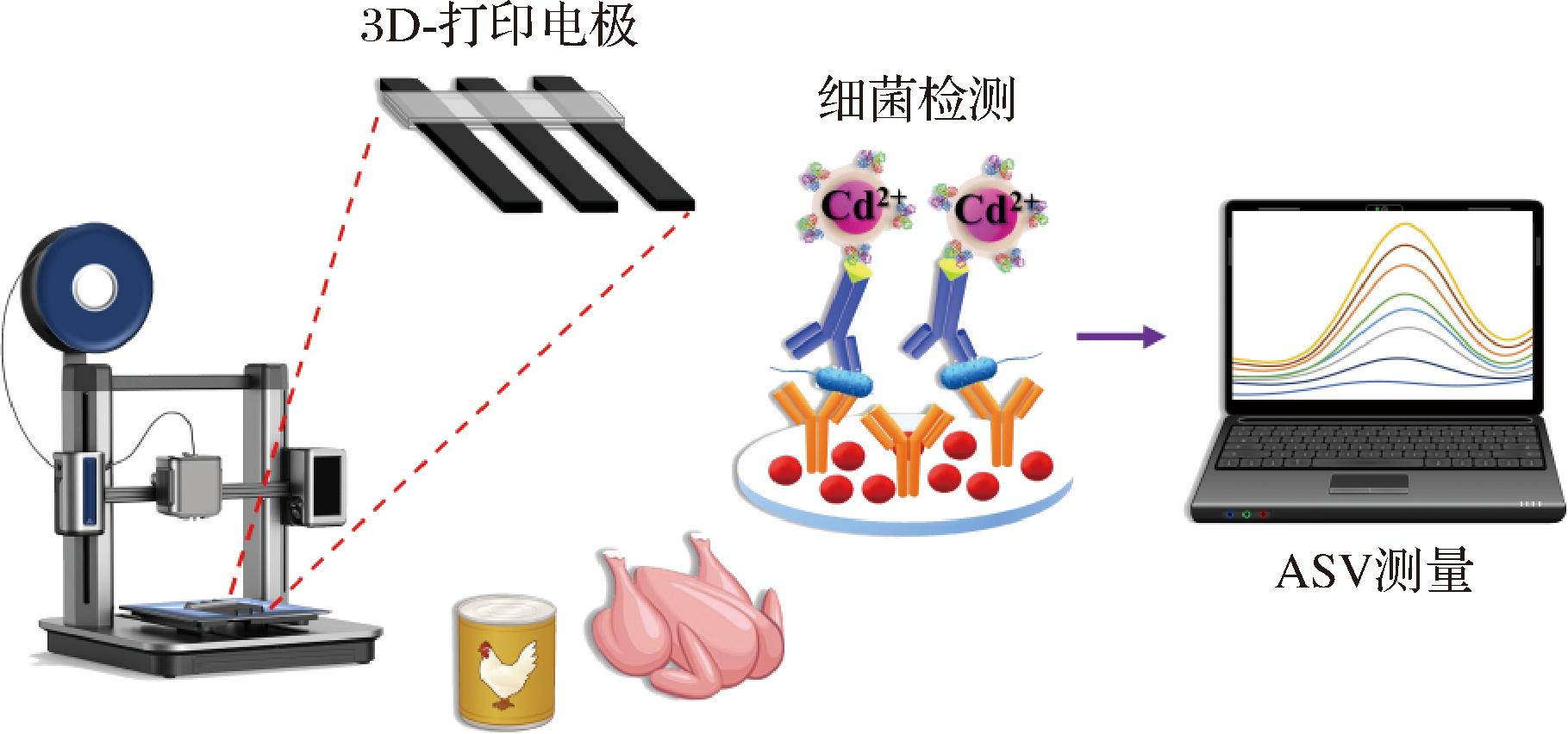
图6 基于Cd/Se ZnS QDs标记的分析示意图[40]
Fig.6 Analysis schematic based on Cd/Se ZnS QDs labeling[40]
QDs作为一类具有高荧光强度、良好光稳定性和荧光波长可调谐性的纳米材料,在荧光标记、生物成像、光电子器件和食源性致病菌检测等多个领域具有显著优势。然而,制备高质量量子点通常需要依赖于包含镉、铟、硒等昂贵金属元素或稀有元素碲在内的原材料,这些原料成本高昂,构成了量子点制备过程中的主要经济负担。因此,尽管量子点性能优越,但其在大规模应用和商业化进程中面临的首要挑战就是如何降低成本,尤其是寻找价格适宜且环境友好的替代材料,以实现QDs的可持续发展和广泛应用。
2.2 荧光二氧化硅纳米粒子(fluorescent silica nanoparticles, FSiNPs)
二氧化硅是一种典型的无机非金属化合物,当其直径小于100 nm时,就构成了无机非金属纳米材料的一种。FSiNPs是指表面或内部经过特定修饰,使其具有荧光性质的二氧化硅纳米颗粒。这种纳米材料通常通过在二氧化硅纳米粒子表面或内部引入荧光基团,或通过调控其尺寸、形状和表面性质,实现对特定波长光的吸收和随后的荧光发射。FSiNPs因其具有高表面积[41]、生物相容性、可生物降解、高量子产率、高光稳定性[42]以及显著的生物分子结合能力[43]等优异特性,可以实现对病原菌的高效分离和检测。SIFANA等[44]构建了一种基于FSiNPs的生物传感技术,其利用含有Van的识别方法来检测耐甲氧西林金黄色葡萄球菌(methicillin-resistant Staphylococcus aureus, MRSA)。该检测原理是基于FSiNPs-Van在特定激发波长下的荧光猝灭效应,当FSiNPs-Van与MRSA结合时,Van与MRSA的特异性相互作用,导致原本的荧光强度大幅降低。这种生物传感器的响应时间非常快,只需要20 min即可完成对MRSA的检测,与浓度为10~106 CFU/mL的MRSA呈现良好的线性关系,其检测极限低至1 CFU/mL,表明该探针具有极高的灵敏度和实用性。HORMSOMBUT等[45]将介孔二氧化硅纳米颗粒(mesoporous silica nanoparticles,MSNs)与荧光素、链亲和素和7种检测抗体-生物素结合,形成荧光素掺杂的介孔二氧化硅纳米颗粒与检测抗体(MSNs-flu-sa-abs)结合的复合物,可以同时检测7种食源性致病菌。结果显示,这7种病原菌在缓冲液和食品样品中的LOD均为102 CFU/mL,抗体适体阵列的荧光强度定量可低至20~34 CFU/g。碳点本质上是发光纳米材料,由于其高光稳定性和荧光特性,在生物传感技术中具有许多潜在的应用,而二氧化硅因其独特性质增强了碳点的荧光强度。SONG等[46]利用碳纳米点杂交二氧化硅纳米球(carbon nanodot-hybridized silica nanospheres,CSN)辅助免疫分析法进行大肠杆菌O157:H7的检测(图7),结果发现其检出限为2.4 CFU/mL,证实了该方法的灵敏性和实用性。
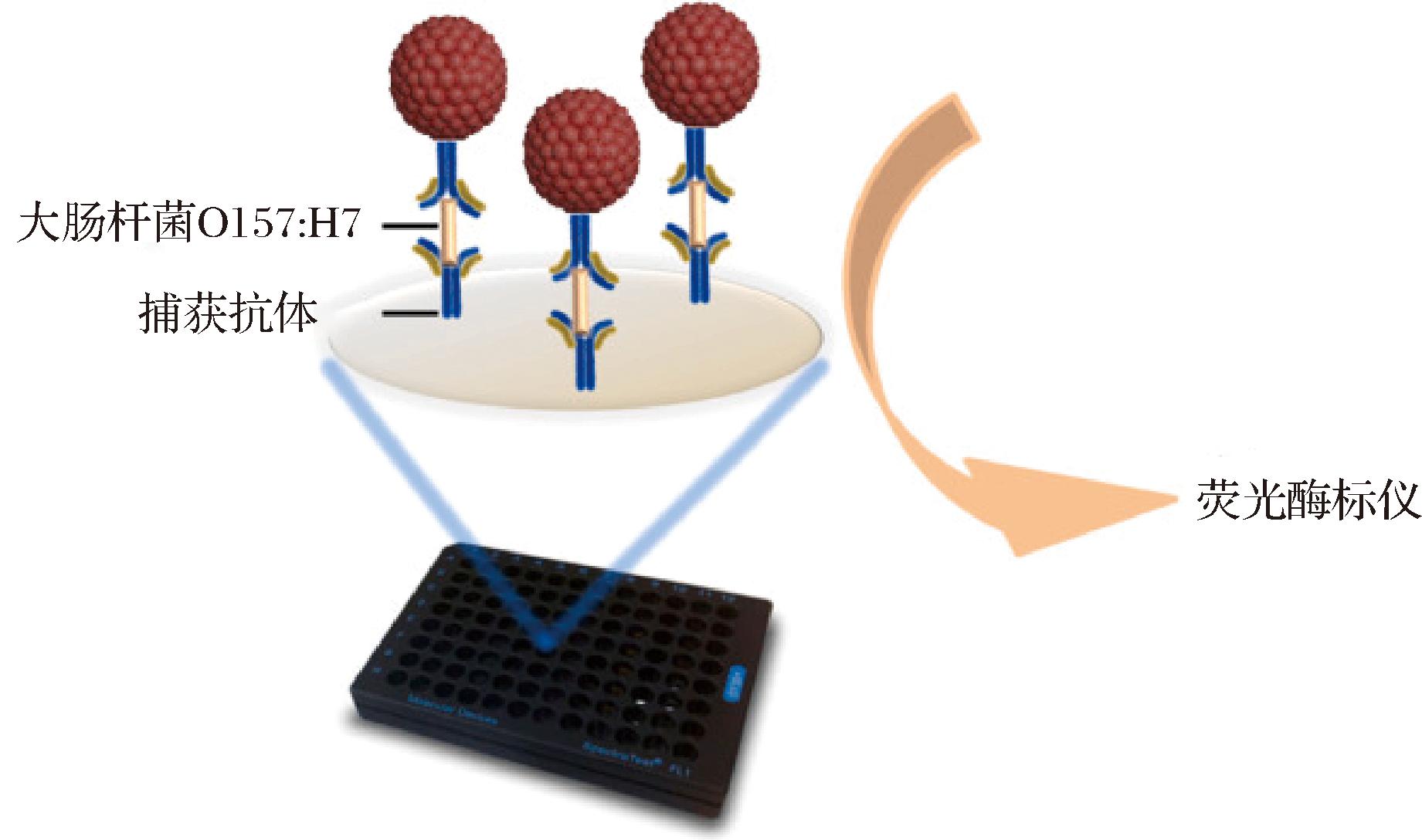
图7 在免疫测定中使用荧光CSN检测大肠杆菌O157:H7的示意图[46]
Fig.7 Schematic diagram of the detection of E.coli O157:H7 using fluorescent CSN in immunoassays[46]
FSiNPs在食源性致病菌检测方面的应用虽已取得显著成果,但仍需不断优化纳米材料的合成与修饰方法,以应对实际应用中面临的挑战,最大限度地发挥其在快速、准确检测食源性致病菌方面的优势。
3 碳基纳米材料
3.1 碳纳米管(carbon nanotube,CNT)
CNTs是一种以碳为主要成分的新型管状材料,具有纳米级管状结构、较强的非极性C—C键和纯sp2杂化碳键,表面积高达50~200 m2/g。因其独特的结构和性能,对于有害物质的吸附能力较强。CNTs由石墨烯卷曲而成的同轴一维纳米管材料,包括单壁碳纳米管(single-walled carbon nanotubes, SWCNT)和MWCNT,层间距约为0.34 nm,管径为2~20 nm[47]。 SWCNT是将单层石墨烯卷成无缝的分子圆筒,这种CNT的直径分布范围相对较小,缺陷较少,具有较高的均匀一致性,整体的结构比较稳定[48]。MWCNT由2层或多层卷曲石墨烯片组成,其直径通常为2~30 nm,有的甚至超过100 nm[49]。
基于CNT的独特结构及性质,研究者通过对其进行修饰改性或更换适配体,可制备出用于食源性致病菌检测性能优良的CNT复合材料来识别或量化病原体,检测灵敏且耗时短,适合现场检测。YANG等[50]基于羰基铁粉(carbonyl iron powder,CIP)和MWCNT结合,开发了CIP@MWCNT新型荧光适配体传感器用以检测牛奶中的大肠杆菌O157:H5,LOD为3.1×102 CFU/mL(图8)。该传感器具有特异性高、重现性好、稳定性强的特点,为有效合成纳米复合材料和乳制品行业食源性病原体的敏感检测提供了新的可能性。HAN等[51]提出了一种微流控SWCNT场效应晶体管生物传感器,用于连续无标记地检测金黄色葡萄球菌,采用电液聚焦对细菌进行校准,并进一步采用电泳对细菌进行浓缩,以提高分析的灵敏度,该方法LOD为150 CFU/mL。机器学习具有很强的自学习能力,在解决多参数非线性问题方面具有优势。XU等[52]构建了一个基于MWCNTs/AuNPs的电化学阻抗谱(electrochemical impedance spectroscopy,EIS)生物传感器,并使用机器学习模型进行大肠杆菌检测。MWCNTs/AuNPs可以改善传感器的电化学性能。并且本研究主要是通过计算机自动制定多个EIS参数来确定细菌浓度与EIS结果之间的关系。由于该方法具有自主学习的能力,因此基于机器学习的EIS生物传感器应该更能适应各种传感器。更重要的是,随着更多EIS数据维度的探索,可以大大提高大肠杆菌检测的准确性。
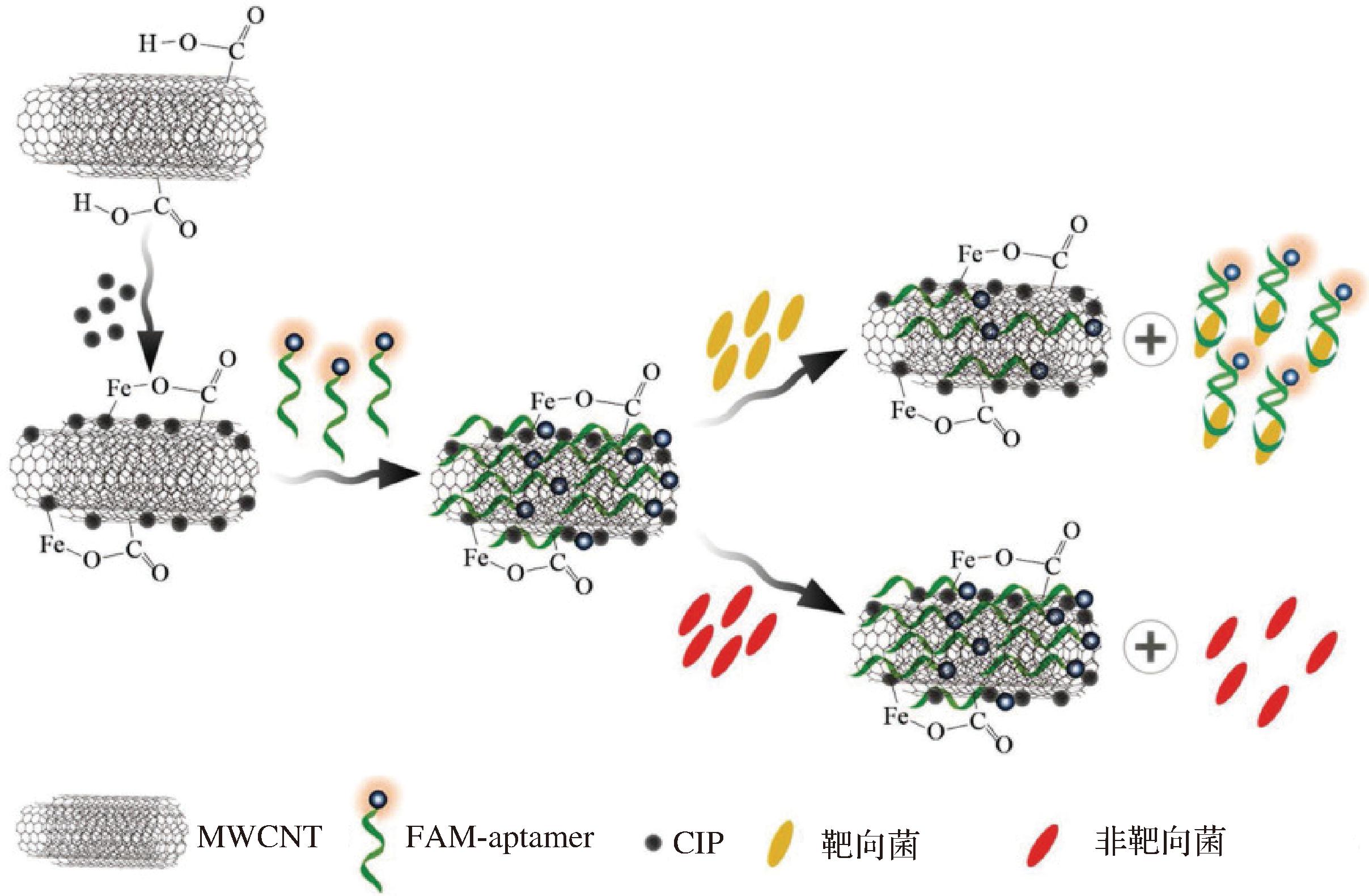
图8 用于检测大肠杆菌O157:H7的基于CIP@MWCNT适配体传感器的示意图[50]
Fig.8 Schematic illustration of the CIP@MWCNT-based aptasensor for the detection of Escherichia coli O157:H7[50]
CNT因其独特的管状结构和出色的物理化学性质,在生物传感领域引起了广泛关注和广泛应用。然而,尽管制备方法相对成熟,但CNT的种类繁多,包括SWCNT和MWCNT等,每种类型的性能各异,且在实际应用中,往往需要高度纯净的产品以确保其在生物传感中的性能稳定性及检测结果的准确性。
3.2 石墨烯(graphene, GR)
GR是一种由单层碳原子紧密堆积形成的2D蜂窝状晶格结构,每个碳原子通过sp2杂化与相邻的3个碳原子形成蜂窝状六角形网格。基于GR的纳米材料有氧化石墨烯、还原氧化石墨烯、功能化石墨烯等,因其优异的导电性和导热性而成为电化学应用领域中一种有吸引力的纳米材料[53]。GR的表面积高达2 630 m2/g,这一数值远超过CNTs的比表面积。这种巨大的比表面积意味着在单位质量或体积的GR材料上,存在着极其丰富的表面活性位点,能够与待测目标物质充分接触,从而显著提高传感器检测的线性范围和灵敏度[54],为食品安全检测提供了一种高效、灵敏的传感平台。FENG等[55]利用Fe3O4@graphene修饰电极构建了检测沙门氏菌的电化学免疫传感器。首先,将Fe3O4和GR混合在壳聚糖溶液中,超声后形成均匀的混合溶液,用于修饰玻碳电极(glassy carbon electrode,GCE)。接下来,利用电沉积技术将AuNPs沉积在Fe3O4@graphene纳米复合材料上,然后通过稳定的Au-NH2键将单克隆抗体固定在AuNPs上。最后,免疫传感器通过抗原-抗体反应捕获沙门氏菌(图9)。由于GR优异的导电性和机械稳定性以及Fe3O4的大比表面积,Fe3O4@graphene纳米复合材料表现出优异的电信号,大大提高了免疫传感器的灵敏度。在优化的实验条件下,沙门氏菌浓度在2.4×102~2.4×107 CFU/mL呈良好的线性关系,免疫传感器的LOD为2.4×102 CFU/mL。SHI等[56]开发了一种基于石墨烯气凝胶的生物传感系统,凭借其独特的一步水热合成工艺、高特异性抗体修饰、多孔结构设计以及电阻和电化学阻抗谱双重监测手段,实现了对大肠杆菌的高特异性和高灵敏度检测,为食源性致病菌的快速、准确检测提供了新的技术手段。
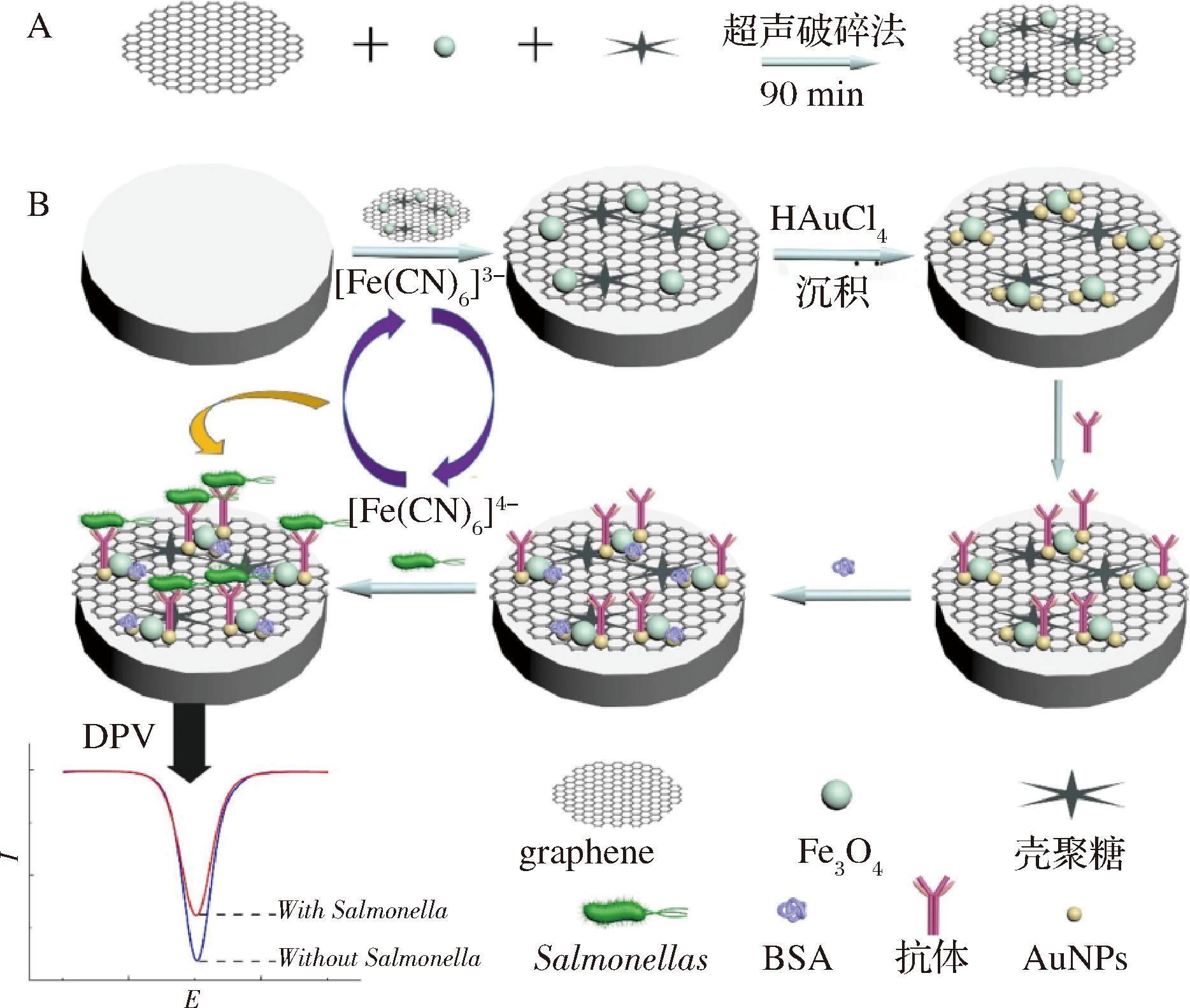
A-Fe3O4@graphene的合成路径; B-C基于Fe3O4@graphene的电化学免疫传感器的构建过程
图9 基于Fe3O4@graphene的电化学免疫传感器的示意图[55]
Fig.9 Schematic diagram of electrochemical immunosensor based on Fe3O4@graphene[55]
注:DPV:different pulse voltammetry(差分脉冲伏安法)。
GR作为前沿纳米材料,具有良好的电流密度、化学惰性和生物相容性,已在食源性致病菌检测中展现出明显优势,但由于范德华相互作用的层间效应和GR薄片的堆积,导致GR的比表面积减小,使得电化学性能不理想。将其与其他材料共同制备复合材料,既克服了上述缺点,又具有其他材料的优异性能,为电化学生物传感器提供了一种非常可靠的电极材料,实现了食源性病原体的快速、灵敏、准确检测。
4 不同纳米材料在食源性致病菌检测应用的优缺点比较
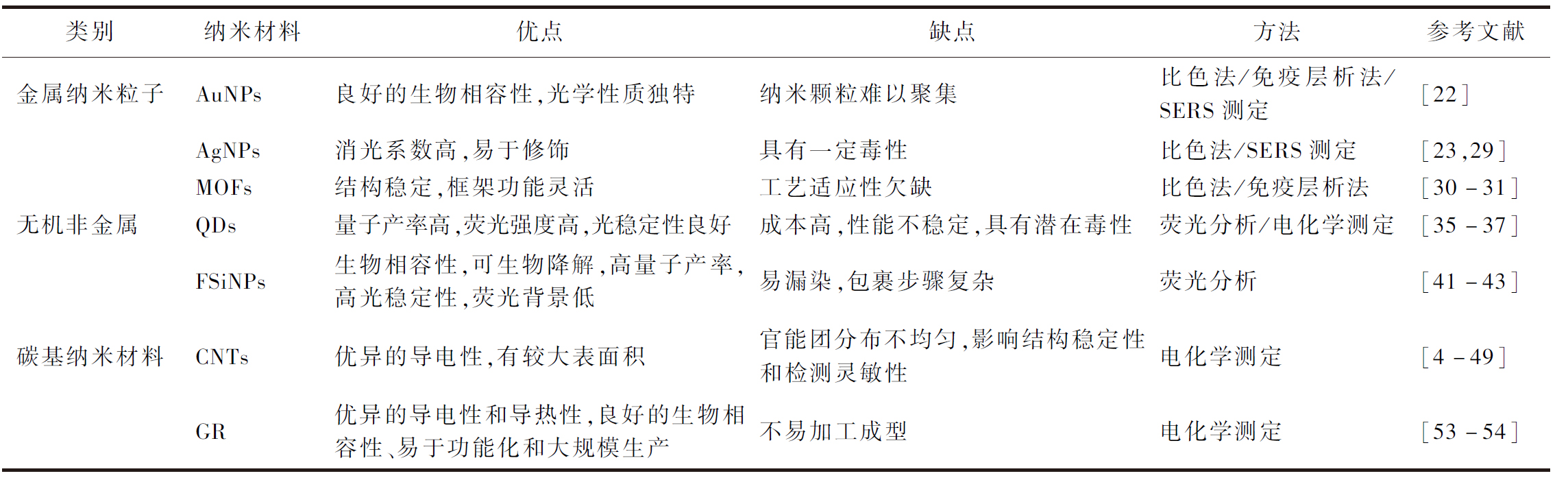
不同纳米材料在食源性致病菌检测应用中具有其各自的性能特点及应用场景,详见表1。金属纳米材料主要用于比色分析和SERS测定,AuNPs是其中应用前景较好的材料,具有独特的光学性质和良好的生物相容性,但容易出现难以聚集纳米颗粒的问题,AgNPs易于修饰但具有一定的毒性作用,MOFs结构稳定、框架灵活但离实际应用还有很长的一段路要走。无机非金属纳米材料通常用于荧光分析与SERS测定,其中QDs具有良好的光稳定性与高荧光强度,但是成本较高且具有潜在毒性,FSiNPs因其具有生物相容性,高量子产率,以及显著的生物分子结合能力可以高效、准确地检测食源性致病菌,相较QDs具有明显的信号放大作用,但包裹步骤复杂,易出现漏染现象。碳基纳米材料主要用于电化学测定,以其独特的结构特性、表面化学特性、电学和光学特性被广泛应用,但制备高度纯净的产品仍然较为困难。
表1 不同纳米材料在食源性致病菌检测中的总结
Table 1 Summary of different nanomaterials in the detection of foodborne pathogens
5 总结与展望
随着人们食品安全意识的逐步增强,影响食品安全的因素越来越受到关注,食源性疾病是食品安全的主要问题,世界卫生组织将食源性疾病定义为:“凡是通过摄食进入人体的,使人体患感染性或中毒性的疾病”。因此,在从农场到餐桌的过程中,检测和控制食物中的病原体非常重要。虽然现有的纳米材料在一定程度上能满足对食源性致病菌的检测,但也存在一些不足。金属纳米颗粒(如金、银等)主要在于生物安全性问题;量子点等无机非金属纳米材料含有重金属元素,对人体有害;碳基纳米材料的表面往往存在官能团分布不均匀的问题,这可能影响其与生物分子(如抗体、核酸等)的均匀、稳定结合,降低检测的特异性和灵敏度。
综上,不同纳米材料在食源性致病菌检测中展现出不同优缺点,在实际应用中还需进一步完善。针对金属纳米颗粒可以研发低毒或无毒的替代品,或者通过表面修饰增加其生物稳定性,降低毒性效应;对于含有重金属元素无机非金属纳米材料,应研发不含或少含重金属的新型纳米材料,同时改进合成方法,确保批次间质量和性能的稳定性;对于碳基纳米材料,应继续深入研究其表面功能化技术,发展更为简便且高效的生物分子固定和靶向识别策略,以提高检测的特异性和灵敏度。基于碳材料的电化学生物传感器在食源性致病菌检测中显示出许多优势,但是要使生物传感器商业化仍然面临许多挑战:a)如何通过简单经济的合成方法制备具有优异电化学传感性能的碳纳米材料?b)如何保证用于食源性致病菌检测的电化学生物传感器的稳定性和结构重现性?c)如何实现碳纳米材料和生物元素的完美固定是电化学生物传感器检测性能的另一个问题。d)如何构建电化学生物传感器实现样品中多种食源性致病菌的同时检测?e)如何制备微型化电化学生物传感器,实现食源性致病菌的现场检测?随着该领域的不断发展,上述挑战也将得到有效解决。更重要的是,基于纳米材料的电化学生物传感器在食源性致病菌检测中的实际应用将会大大提高,并有望逐步商业化。
另外,纳米材料的开发也应努力降低材料的制备成本,简化制备工艺,提高纳米材料的规模化生产能力,同时尽量减少对环境的影响。未来发展方向应着重研发新型纳米材料、优化功能化策略、提高检出限值和响应速度,以及探索其在实际检测系统中的应用集成。通过多学科交叉研究,有望开发出更智能、便捷、绿色的纳米技术用于食源性致病菌的实时、现场检测,从而更好地保障食品安全和公共健康。
[1] RENNER L D, ZAN J D, HU L, et al. Detection of ESKAPE bacterial pathogens at the point of care using isothermal DNA-based assays in a portable degas-actuated microfluidic diagnostic assay platform[J]. Applied and Environmental Microbiology, 2017, 83(4): e02449-16.
[2] KUMAR A, MALINEE M, DHIMAN A, et al. Advanced Biosensors for Health Care Applications[M]. Amsterdam: Elsevier, 2019: 45-69.
[3] TACK D M, MARDER E P, GRIFFIN P M, et al. Preliminary incidence and trends of infections with pathogens transmitted commonly through food: Foodborne Diseases Active Surveillance Network, 10 U.S. sites, 2015-2018[J]. American Journal of Transplantation, 2019, 19(6):1859-1863.
[4] HAMEED S, XIE L J, YING Y B. Conventional and emerging detection techniques for pathogenic bacteria in food science: A review[J]. Trends in Food Science &Technology, 2018, 81:61-73.
[5] WU L, LI G H, XU X, et al. Application of nano-ELISA in food analysis: Recent advances and challenges[J]. TrAC Trends in Analytical Chemistry, 2019, 113:140-156.
[6] LEE S H, PARK S M, KIM B N, et al. Emerging ultrafast nucleic acid amplification technologies for next-generation molecular diagnostics[J]. Biosensors and Bioelectronics, 2019, 141:111448.
[7] 吴文静. 电化学分析法在食品安全检测中的应用探讨[J]. 科技经济导刊,2020, 28(3): 80.WU W J. Application of electrochemical analysis in food safety detection[J]. Technology and Economic Guide, 2020, 28(3): 80.
[8] 丁永玲. 量子点复合材料及应用于药物载体和金属离子检测的研究[D]. 济南: 山东大学, 2017.DING Y L. Application and study on quantum dots composites for drug carriers and metal lon detection[D]. Jinan: Shandong Univiersity, 2017.
[9] 袁建霞, 张秋菊, 胡小鹿, 等. 农业传感器国际竞争态势与研究前沿分析[J]. 现代农业科技, 2019(14):233-235; 237.YUAN J X, ZHANG Q J, HU X L, et al. Analysis on international competition situation and research fronts of agricultural sensor[J]. Modern Agricultural Science and Technology, 2019(14):233-235; 237.
[10] PAVLICEK A, PART F, ROSE G, et al. A European nano-registry as a reliable database for quantitative risk assessment of nanomaterials? A comparison of national approaches[J]. NanoImpact, 2021, 21:100276.
[11] BOVERHOF D R, BRAMANTE C M, BUTALA J H, et al. Comparative assessment of nanomaterial definitions and safety evaluation considerations[J]. Regulatory Toxicology and Pharmacology, 2015, 73(1):137-150.
[12] SALEH T A. Nanomaterials: Classification, properties, and environmental toxicities[J]. Environmental Technology &Innovation, 2020, 20:101067.
[13] SHEN Y Z, ZHANG Y Y, GAO Z F, et al. Recent advances in nanotechnology for simultaneous detection of multiple pathogenic bacteria[J]. Nano Today, 2021, 38:101121.
[14] SUN R M, ZOU H J, ZHANG Y, et al. Vancomycin recognition and induced-aggregation of the Au nanoparticles through freeze-thaw for foodborne pathogen Staphylococcus aureus detection[J]. Analytica Chimica Acta, 2022, 1190:339253.
[15] ZHANG H, MA X Y, LIU Y, et al. Gold nanoparticles enhanced SERS aptasensor for the simultaneous detection of Salmonella typhimurium and Staphylococcus aureus[J]. Biosensors and Bioelectronics, 2015, 74:872-877.
[16] YAN Y, WANG X R, LU Y Y, et al. Visualization and quantitative detection of foodborne Salmonella typhimurium by functionalizing cysteamine (CS) stabilized gold nanoparticles (CS-AuNPs@phage)[J]. European Food Research and Technology, 2024, 250(11):2797-2808.
[17] GUO R Y, HUANG F C, CAI G Z, et al. A colorimetric immunosensor for determination of foodborne bacteria using rotating immunomagnetic separation, gold nanorod indication, and click chemistry amplification[J]. Microchimica Acta, 2020, 187(4):197.
[18] HUA Z, YU T, LIU D H, et al. Recent advances in gold nanoparticles-based biosensors for food safety detection[J]. Biosensors and Bioelectronics, 2021, 179:113076.
[19] YANG T, WANG Z H, SONG Y, et al. A novel smartphone-based colorimetric aptasensor for on-site detection of Escherichia coli O157∶H7 in milk[J]. Journal of Dairy Science, 2021, 104(8):8506-8516.
[20] 成汉文. 高灵敏SERS基底的制备及其在芽孢杆菌检测中的应用[D]. 长沙: 湖南大学, 2013.CHENG H W. Highly-sensitive SERS substrates for detection of bacterial spores[D]. Changsha: Hunan University, 2013.
[21] ZENG P, GUAN Q, ZHANG Q Q, et al. SERS detection of foodborne pathogens in beverage with Au nanostars[J]. Microchimica Acta, 2023, 191(1):28.
[22] 周静, 田风玉, 焦必宁, 等. 基于纳米材料的可视化比色检测技术在食源性致病菌检测中的应用研究进展[J]. 食品与发酵工业, 2019, 45(11):259-267.ZHOU J, TIAN F Y, JIAO B N, et al. Applications of visual colorimetric detection methods based on nanomaterials in detecting foodborne pathogens[J]. Food and Fermentation Industries, 2019, 45(11):259-267.
[23] FRANCI G, FALANGA A, GALDIERO S, et al. Silver nanoparticles as potential antibacterial agents[J]. Molecules, 2015, 20(5):8856-8874.
[24] NANDA A, SARAVANAN M. Biosynthesis of silver nanoparticles from Staphylococcus aureus and its antimicrobial activity against MRSA and MRSE[J]. Nanomedicine: Nanotechnology, Biology and Medicine, 2009, 5(4):452-456.
[25] VALDÉS A, GARCIA-SERNA E, MART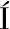 NEZ-ABAD A, et al. Gelatin-based antimicrobial films incorporating pomegranate (Punica granatum L.) seed juice by-product[J]. Molecules, 2019, 25(1): 166.
NEZ-ABAD A, et al. Gelatin-based antimicrobial films incorporating pomegranate (Punica granatum L.) seed juice by-product[J]. Molecules, 2019, 25(1): 166.
[26] MORSY M K, KHALAF H H, SHAROBA A M, et al. Incorporation of essential oils and nanoparticles in pullulan films to control foodborne pathogens on meat and poultry products[J]. Journal of Food Science, 2014, 79(4): M675-M684.
[27] BEGUM T, FOLLETT P A, MAHMUD J, et al. Silver nanoparticles-essential oils combined treatments to enhance the antibacterial and antifungal properties against foodborne pathogens and spoilage microorganisms[J]. Microbial Pathogenesis, 2022, 164:105411.
[28] ZHU A F, LI H Q, ALI S, et al. Au@Ag@MPBA tags assisted surface-enhanced Raman spectroscopy for pathogens detection based on bacteria inhibiting salt-induced aggregation[J]. Microchemical Journal, 2024, 196:109630.
[29] DU J, TANG J H, XU S D, et al. Parental transfer of perfluorooctane sulfonate and ZnO nanoparticles chronic co-exposure and inhibition of growth in F1 offspring[J]. Regulatory Toxicology and Pharmacology, 2018, 98:41-49.
[30] AHMADI M, AYYOUBZADEH S M, GHORBANI-BIDKORBEH F, et al. An investigation of affecting factors on MOF characteristics for biomedical applications: A systematic review[J]. Heliyon, 2021, 7(4): e06914.
[31] CHENG W W, TANG X Z, ZHANG Y, et al. Applications of metal-organic framework (MOF)-based sensors for food safety: Enhancing mechanisms and recent advances[J]. Trends in Food Science &Technology, 2021, 112:268-282.
[32] 张静. 基于金属有机骨架材料的生物传感器在食源性致病菌和毒素检测中的应用[J]. 化学通报, 2022, 85(11):1322-1329.ZHANG J. Application of metal-organic frameworks-based biosensors in the detection of foodborne pathogenic bacteria and toxins[J]. Chemistry, 2022, 85(11):1322-1329.
[33] LI S H, XIE H Q, XIE F M, et al. Immunoassay based on urease-encapsulated metal-organic framework for sensitive detection of foodborne pathogen with pH meter as a readout[J]. Microchimica Acta, 2022, 189(9):358.
[34] GUO R Y, XUE L, CAI G Z, et al. Fe-MIL-88NH2 metal-organic framework nanocubes decorated with Pt nanoparticles for the detection of Salmonella[J]. ACS Applied Nano Materials, 2021, 4(5):5115-5122.
[35] E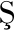 REF D, VINCENT C. Evaluation of the potential genotoxicity of quantum dots. a review[J]. Aspects of Nanotechnology, 2017, 1(1): 1-19.
REF D, VINCENT C. Evaluation of the potential genotoxicity of quantum dots. a review[J]. Aspects of Nanotechnology, 2017, 1(1): 1-19.
[36] QU W J, ZUO W B, LI N, et al. Design of multifunctional liposome-quantum dot hybrid nanocarriers and their biomedical application[J]. Journal of Drug Targeting, 2017, 25(8):661-672.
[37] 杨欣煜, 沈宝星, 杨雪娇, 等. 纳米材料在食源性致病菌检测的研究进展[J]. 食品安全质量检测学报, 2022, 13(19):6320-6326. YANG X Y, SHEN B X, YANG X J, et al. Recent advances in detection for foodborne pathogens with nanomaterials[J]. Journal of Food Safety &Quality, 2022, 13(19):6320-6326.
[38] HU J, TANG F, JIANG Y Z, et al. Rapid screening and quantitative detection of Salmonella using a quantum dot nanobead-based biosensor[J]. Analyst, 2020, 145(6):2184-2190.
[39] ZHANG H W, LIU Y S, YAO S, et al. A multicolor sensing system for simultaneous detection of four foodborne pathogenic bacteria based on Fe3O4/MnO2 nanocomposites and the etching of gold nanorods[J]. Food and Chemical Toxicology, 2021, 149:112035.
[40] ANGELOPOULOU M, KOURTI D, MERTIRI M, et al. A 3D-printed electrochemical immunosensor employing Cd/Se ZnS QDs as labels for the rapid and ultrasensitive detection of Salmonella typhimurium in poultry samples[J]. Chemosensors, 2023, 11(9): 475.
[41] SIFANA N O, JENIE S N A. Fabrication and characterization of FITC-modified naturalbased silica nanoparticles using sol-gel method[J]. IOP Conference Series: Earth and Environmental Science, 2022, 963(1):012025.
[42] AISYIYAH JENIE S N, KUSUMASTUTI Y, KRISMASTUTI F S H, et al. Rapid fluorescence quenching detection of Escherichia coli using natural silica-based nanoparticles[J]. Sensors, 2021, 21(3): 881.
[43] ANANDA P D, TILLEKARATNE A, HETTIARACHCHI C, et al. Sensitive detection of E. coli using bioconjugated fluorescent silica nanoparticles[J]. Applied Surface Science Advances, 2021, 6:100159.
[44] SIFANA N O, SEPTIANI N L W, SEPTAMA A W, et al. Detection of methicillin-resistant Staphylococcus Aureus using vancomycin conjugated silica-based fluorescent nanoprobe[J]. Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, 2024, 307:123643.
[45] HORMSOMBUT T, MEKJINDA N, KALASIN S, et al. Mesoporous silica nanoparticles-enhanced microarray technology for highly sensitive simultaneous detection of multiplex foodborne pathogens[J]. ACS Applied Bio Materials, 2024, 7(4):2367-2377.
[46] SONG Y, OSTERMEYER G P, DU D, et al. Carbon nanodot-hybridized silica nanospheres assisted immunoassay for sensitive detection of Escherichia coli[J]. Sensors and Actuators B: Chemical, 2021, 349:130730.
[47] 刘腾飞, 杨代凤, 毛健, 等. 碳纳米管材料在食品安全分析中的应用[J]. 化工进展, 2018, 37(10):3699-3725.LIU T F, YANG D F, MAO J, et al. Review on the application of carbon nanotubes in food safety analysis[J]. Chemical Industry and Engineering Progress, 2018, 37(10):3699-3725.
[48] 黄佳佳, 江东文, 杨昭, 等. 多壁碳纳米管固相萃取技术及其在食品安全检测中的应用[J]. 食品工业科技, 2016, 37(14):368-374; 384.HUANG J J, JIANG D W, YANG Z, et al. Solid-phase extraction technique based on multi-walled carbon nanotubes and its application in food safety detection[J]. Science and Technology of Food Industry, 2016, 37(14):368-374; 384.
[49] ALIM S, VEJAYAN J, YUSOFF M M, et al. Recent uses of carbon nanotubes &gold nanoparticles in electrochemistry with application in biosensing: A review[J]. Biosensors &Bioelectronics, 2018, 121:125-136.
[50] YANG T, YANG X Y, GUO X J, et al. A novel fluorometric aptasensor based on carbon nanocomposite for sensitive detection of Escherichia coli O157∶H7 in milk[J]. Journal of Dairy Science, 2020, 103(9):7879-7889.
[51] HAN C H, JANG J. Integrated microfluidic platform with electrohydrodynamic focusing and a carbon-nanotube-based field-effect transistor immunosensor for continuous, selective, and label-free quantification of bacteria[J]. Lab on a Chip, 2021, 21(1):184-195.
[52] XU Y, LI C, JIANG Y, et al. Electrochemical impedance spectroscopic detection of E.coli with machine learning[J]. Journal of the Electrochemical Society, 2020, 167(4):047508.
[53] YAMADA K, KIM C T, KIM J H, et al. Single walled carbon nanotube-based junction biosensor for detection of Escherichia coli[J]. PLoS One, 2014, 9(9): e105767.
[54] PUMERA M. Graphene-based nanomaterials and their electrochemistry[J]. Chemical Society Reviews, 2010, 39(11):4146-4157.
[55] FENG K W, LI T, YE C Z, et al. A novel electrochemical immunosensor based on Fe(3)O(4)@graphene nanocomposite modified glassy carbon electrode for rapid detection of Salmonella in milk[J]. Journal of Dairy Science, 2022, 105(3):2108-2118.
[56] SHI C Y, TANG Y N, YANG H Y, et al. Capture and detection of Escherichia coli with graphene aerogels[J]. Journal of Materials Chemistry B, 2022, 10(40):8211-8217.