鱼糜作为工业化鱼糜制品的主要原材料,其制备过程包括鱼肉切片、去骨、洗涤、脱水、精制,并与冷冻保护剂混合后冷冻加工[1]。鱼糜制品则以新鲜鱼肉或冷冻鱼糜为基料,通过斩拌、擂溃、成型及热诱导凝胶化等工序加工而成,属高蛋白、低脂肪食品。油炸是鱼糜制品常见的熟制方法,虽可赋予产品良好风味与质地,但在氧气、高温及水分条件下易诱发脂质氧化,导致蛋白质变性及营养价值下降[2],同时高温过程还可能生成如杂环胺等有害化合物[3]。空气煎炸作为传统油炸的替代技术,旨在显著降低油脂含量,并通过促进食品快速脱水以形成酥脆表层[4]。然而,经此技术加工的食品常呈现硬度偏高、咀嚼适口性欠佳的问题。表面涂油处理可有效调节其质构特性,使口感近似油炸食品的感官特性。但液态油涂层因其高流动性易致分布不均,致使油脂局部聚集与过度渗透,进而影响产品整体品质。高内相乳液(high internal phase emulsion,HIPEs)凭借其优异的黏弹性、自支撑性及稳定性,在食品领域展现出作为涂层替代液态油的应用潜力。
HIPEs定义为内相体积分数超过74%的乳液体系[5]。在食品领域,HIPEs可将液态油转化为固态形式而无需氢化[6],为改善食品质地、营养与风味提供了创新技术途径。生物源固体颗粒是HIPEs的常用稳定剂。蛋白质虽具备高表面活性与优异的界面吸附动力学特性,但其乳化稳定性易受温度、pH及离子强度影响而导致HIPEs失稳[7]。多糖可通过在水相中形成厚空间位阻层并提供静电斥力以抑制液滴聚集,但其乳化能力与表面活性有限[8]。研究表明,单一蛋白质或多糖作为稳定剂的局限性可通过复合使用得以克服。纤维素纳米晶(cellulose nanocrystals,CNC)是通过化学、物理或生物酶处理去除纤维素无定形区域后获得的高度结晶棒状或针状纳米颗粒[9],因其高长径比、良好生物相容性、低成本及易得性,被广泛用作Pickering乳液稳定剂[10]。然而,CNC表面富含羟基所赋予的强亲水性,使其不足以稳定HIPEs。鉴于CNC与蛋白质的优良相容性,可利用酪蛋白(casein,CA)进行复合。CA主要由αs1-、αs2-、β-和κ-酪蛋白组成,是一类具有高表面活性的线性两亲性大分子[11]。其柔性构象与两亲性赋予其快速扩散至油水界面的能力,并在油滴周围形成界面膜[12]。作为一种新兴非热加工技术,超声处理可通过空化效应(即微观气泡形成与剧烈溃灭产生强局部剪切力)改变物质的物理、结构和功能特性,导致样品降解与解聚[13]。前人研究表明,超声处理可进一步优化蛋白质-多糖复合颗粒的理化性质,从而提升其稳定乳液的能力[14]。此外,鉴于抗氧化剂对脂质氧化及美拉德反应的调控作用,在超声处理的CA-CNC(ultrasonically treated casein-cellulose nanocrystals,U-CA-CNC ,简称UCC)稳定剂中添加抗氧化剂可能进一步提升HIPEs性能,最终改善煎炸鱼糜制品品质。葡萄籽提取物(grape seed extract,GSE)是从酿酒葡萄种子中提取的多酚类物质,富含四聚花青素、原花青素等酚类化合物,是一种天然强效抗氧化剂。
本研究通过调控UCC稳定剂比例并引入GSE,构建了具有梯度黏度的功能性HIPEs涂层。系统评价了该涂层对空气煎炸鱼糜制品质构参数、色泽、挥发性风味物质及有害物质(杂环胺)生成量的影响,以确定最佳配方比例。
1 材料与方法
1.1 材料与试剂
金龙鱼大豆油,大连当地超市;酪蛋白,上海阿拉丁生化科技有限公司;GSE,亳州亦言生物科技有限公司。鲢鱼鱼糜,洪湖市井力水产食品股份有限公司。氢氧化钠、浓硫酸(分析级),天津市大茂化学试剂厂;浓盐酸、氯化钠(分析级),天津科密欧化学试剂有限公司;三氯乙酸、2-硫代巴比妥酸(thiobarbituric acid,TBA)(分析级),国药集团化学试剂有限公司;正己烷、无水硫酸镁(均为分析级)、冰乙酸(HPLC)、微晶纤维素,上海麦克林生化科技股份有限公司;乙腈(HPLC),美国Sigma-Aldrich公司;D3-2-氨基-3,4,8-三甲基咪唑并[4,5-f]喹喔啉(2-amino-3,4,8-trimethylimidazo[4,5-*f*]quinoxaline-d3, D3-4,8-DiMeIQx)(色谱纯),Toronto Research Chemicals;2-氨基-3,4,8-三甲基咪唑并[4,5-f]喹喔啉(2-amino-3,4,8-trimethylimidazo[4,5-*f*]quinoxaline, 4,8-DiMeIQx)(色谱纯),Toronto Research Chemicals;2-氨基-3,7,8-三甲基咪唑并 [4,5-f] 喹喔啉(2-amino-3,7,8-trimethylimidazo[4,5-*f*]quinoxaline, 7,8-DiMeIQx)(色谱纯),Toronto Research Chemicals;2-氨基-3-甲基咪唑并[4,5-f]喹啉(2-amino-3-methylimidazo[4,5-*f*]quinoline, IQ)(色谱纯),Toronto Research Chemicals;2-氨基-1-甲基-6-苯基-咪唑并[4,5-b]吡啶(2-amino-1-methyl-6-phenylimidazo[4,5-*b*]pyridine, PhIP)(色谱纯),Toronto Research Chemicals;2-氨基-3,8-二甲基咪唑并[4,5-f] 喹喔啉(2-amino-3,8-dimethylimidazo[4,5-*f*]quinoxaline, MeIQx)(色谱纯),Toronto Research Chemicals。
1.2 仪器与设备
HD9257空气炸锅,荷兰皇家飞利浦电子公司;JY99-IIIDN超声波细胞破碎仪,宁波新芝生物科技股份有限公司;T25匀浆机,德国IKA公司;DHR-2 流变仪,美国TA公司;TA.XT.plus质构仪,英国Stable Micro Systems公司;Ultra Scan Pro测色仪,美国Hunter Lab公司;Infinite F200 PRO荧光酶标仪,瑞士Tecan公司;A200电子顺磁共振波谱仪(electron spin resonance,ESR),德国Bruker Bio Spin公司;Centri Vap真空冷冻离心浓缩仪,美国LABCONCO公司;5500 QTRAP液相质谱联用仪,美国AB SCIEX公司。
1.3 实验方法
1.3.1 不同CA与CNC质量比稳定HIPEs的制备
纳米纤维素晶的提取方法是根据REVOL等[15]的硫酸水解法稍加修改。将微晶纤维素(microcrystalline cellulose,MCC)粉末与9 mol/L的H2SO4溶液按照料液比1∶15(g∶mL)的比例在一定条件下(400 r/min,55 ℃)水解1 h,反应后得到淡黄色液体,加入10倍体积冷去离子水以停止反应,4 ℃静置12 h,弃去上层液体,以8 000 r/min,10 min重复离心3次,回收白色沉淀,加去离子水得到白色悬浮液,将悬浮液置于分子截留量为1 000 Da的透析袋中透析除去多余的酸,得到CNC溶液,随后将其质量浓度调整为40 g/L。将纳米纤维素晶溶液分别与不同质量的CA粉末混合,在800 r/min转速下搅拌1 h,然后用1 mol/L NaOH将pH值调至中性,得到不同比例(0.25∶1、0.5∶1和1∶1,质量比)的CA-CNC复合溶液。用超声波细胞破碎仪对CA-CNC溶液进行超声波处理。将钛探针(直径25 mm)插入20 mL样品溶液中,深度为10 mm。将样品置于800 W的超声波中,持续30 min,开1 s,关1 s,获得UCC(0.25∶1、0.5∶1和1∶1)复合溶液。随后在不同质量比的UCC复合溶液中分别添加10 g/L的GSE,制得U-CA-CNC-GSE(0.25∶1、0.5∶1和1∶1)复合溶液(简称UCCG)。
以大豆油为油相,将上述6种溶液各取5 mL分别与15 mL大豆油混合。使用匀浆机在8 000 r/min转速下对UCC和UCCG系列溶液进行高速匀浆2 min,制备得到高内相乳液。
1.3.2 不同CA与CNC质量比稳定HIPEs的表征
1.3.2.1 流变特性
按照LIU等[16]的方法,使用流变仪测量HIPEs的流变特性。取适量样品放入到流变仪底座平台上,选用40 mm平板于(25.0±0.1) ℃下测量流变学性质。通过改变剪切速率(范围为1~100 s-1)测定悬浮液的表观黏度。对于动态流变测量,首先固定1 Hz 频率,通过改变应变(0.01%~100%)来确定线性黏弹区。随后,在恒定应变下,0.1~10 Hz频率扫描测定悬浮液动态流变行为。
1.3.2.2 氧化稳定性
根据WANG等[17]的方法,测量硫代巴比妥酸反应物(thiobarbituric acid reactive substances,TBARS)值监测次级氧化产物以表示HIPEs的氧化稳定性。具体如下:取0.2 g乳液与1.8 mL去离子水和4.0 mL TBA溶液混合,通过将30 g三氯乙酸、0.75 g TBA、4.17 mL 12 mol/L HCl与196 mL去离子水混合来制备。将所得混合物在沸水浴中加热15 min,用自来水冲洗并冷却至室温,最后将混合物在4 000 r/min下离心15 min。取上清液后立即在532 nm处测量吸光度,使用标准曲线法计算丙二醛浓度。
1.3.3 空气煎炸不同CA与CNC质量比稳定HIPEs涂层鱼糜片的制备
鲢鱼鱼糜解冻,水分控制在(80.0±1.0)%,搅拌斩1 min,添加1%(质量分数)盐,再搅拌1 min,制作成长3 cm、宽3 cm、厚0.5 cm的鱼糜片备用。将大豆油、与大豆油具有相同油含量的不同黏度的高内相乳液以及其添加GSE的对照组分别均匀涂抹在鱼糜片上,在160 ℃下空气煎炸12 min。
1.3.4 空气煎炸不同CA与CNC质量比稳定HIPEs涂层鱼糜片的质构
根据罗晓林等[18]的方法,采用质构仪结合物理性能测试仪测定不同涂油条件下(不涂油、涂大豆油、涂高内相乳)分别在温度140、160 ℃空气油炸6、12 min的鱼糜片的硬度、弹性、咀嚼性和内聚性。将空气煎炸鱼糜片切成1 cm(宽)×1 cm(长)×0.3 cm(高)的长方体进行测试,选择P/50 TPA探头;根据探头与样品面的接触情况设置下降距离为10 mm;其中试验前、中、后速度都设置为1 mm/s;实验返回速度设置为15.00 mm/s;对样品进行应变50%的压缩;经5.0 s后循环压缩。
1.3.5 空气煎炸不同CA与CNC质量比稳定HIPEs涂层鱼糜片的色泽
用测色仪检测鱼糜片的色度参数。将不同涂油条件下(不涂油、涂液体油、涂高内相乳)的鱼糜片分别在温度140、160 ℃下空气油炸6、12 min,测定其色度。在检测前对测色仪进行色度校正:选用标准的黑白板分别放置在0.39英寸孔径的镜头前进行校正。校正后将空气煎炸鱼糜片的平整表面贴至镜头上检测样品色度值。白色指数(white index,WI)计算如公式(1)所示:
WI=100-[(100-L*)2+a*2+b*2]1/2
(1)
式中:L*表示亮度;a*表示绿色到红色;b*表示蓝色到黄色;WI表示白色指数。
1.3.6 空气煎炸不同CA与CNC质量比稳定HIPEs涂层鱼糜片的脂质氧化
根据姜化彬等[19]的方法稍作修改,称取样品5 g于50 mL离心管中,加入45 mL 100 g/L三氯乙酸,静置1 h,然后在8 000 r/min、4 ℃条件下离心10 min,取上清液5 mL于离心管,加5 mL 0.02 mol/L TBA在95 ℃水浴加热反应30 min,取出用流动水冷却,于532 nm波长处测定吸光度。TBARS值的测定以丙二醛(malondialdehyde,MDA)为标准品,结果以每千克样品中MDA的毫克数来表示,记为mg MDA/kg。
1.3.7 空气煎炸不同CA与CNC质量比稳定HIPEs涂层鱼糜片的自由基测定
将制备好的鱼糜制品切碎放入真空冷冻干燥机中,将冻干好的样品研磨成粉,采用电子顺磁共振波谱仪(electron spin resonance,ESR)对自由基含量进行测定。测定条件参考李德阳[20]测定自由基含量的方法。
1.3.8 空气煎炸不同CA与CNC质量比稳定HIPEs涂层鱼糜片的杂环胺测定
1.3.8.1 杂环胺的提取
根据GAO等[21]的方法,称取(2.0±0.1) g已剪碎的样品,加入5 mL去离子水和5 mL乙腈溶液,并加入200 μL 1 μg/mL的D3-4,8-DiMeIQx内标。使用匀浆机以8 000 r/min均化30 s,并在超声浴中放置15 min。取出后加入2.5 mL正己烷,2 g无水硫酸镁和0.25 g氯化钠,并剧烈涡旋振荡2 min,从而使样品与所加试剂充分混合作用。在3 040×g离心10 min 实现三相分离后,收集乙腈层,并添加正己烷去除脂质。脱脂后的溶液使用真空冷冻离心浓缩仪进行干燥后,用400 μL 50%(体积分数)乙腈水溶液重新溶解,并使用离心机在20 000×g、4 ℃下离心10 min 后取上层清液,进行超高效液相色谱串联质谱检测。所有测定均重复3次。
添加正己烷进行除脂:实现三相分离后,向分离后的2 mL乙腈层添加2.5 mL正己烷,涡旋振荡2 min,然后使用离心机在20 000×g、4 ℃条件下离心10 min,吸取离心后的上层清液进行后续制备及分析。
1.3.8.2 标准曲线
配制1.00、10.00、20.00、50.00、100.00、200.00 ng/mL 6个质量浓度的混合标准品溶液进行检测,每个浓度均重复3次。以标准品浓度为横坐标,以待测分析物与内标的峰面积比值为纵坐标绘制标准曲线,得到各待测分析物的相关系数(R2)。在正离子模式下,选用D3-4,8-DiMeIQx为内标校正5种杂环胺。
1.3.8.3 杂环胺的检测分析
采用超高效液相色谱法串联三重四极杆质谱仪对热加工样品中的5种杂环胺进行检测分析。使用ZORBAX Stable Bond C18色谱柱(4.6 mm×150 mm,5 μm)分离目标待测物。流动相A为水溶液(含0.1% 乙酸),流动相B为乙腈溶液(含0.1%乙酸)。采用线性梯度洗脱:0~1.5 min,1% B;1.5~16.5 min,99% B;16.6~20 min,1% B。进样流速设定为0.3 mL/min;柱温设定为40 ℃;自动进样器温度设定为4 ℃;洗针液为80%(体积分数)乙腈-水溶液;进样量设定为1 μL。三重四极杆质谱仪采用正离子模式,在多反应监测(multiple reaction monitoring, MRM)模式下进行检测。电喷雾电离(electro spray ionization,ESI)源参数设置为:入口电位10 V;喷雾电压5 500 V;气帘气35 psi;离子化温度600 ℃;雾化气和辅助加热气60 psi。采用高纯氮气作为气帘气和碰撞气。
1.4 数据统计分析
所有实验均重复3次。对数据进行方差分析(ANOVA),并通过最小显著性差异(least significant difference,LSD)检验检测实验平均值之间的差异,显著性水平定为P<0.05。采用Origin 2022和Excel绘图。
2 结果与分析
2.1 不同CA与CNC质量比稳定HIPEs的表征
2.1.1 流变特性
流变特性表征了高内相乳液HIPEs的黏弹性及表观黏度,后者显著影响HIPEs的涂抹性与稳定性。如图1-A、图1-B所示,所有HIPEs的储能模量(G′)均高于损耗模量(G″),表明其均呈现凝胶状结构特征。随着CA-CNC比例的增加,HIPEs的G′值增大。这可能源于CA含量增加促进了CA-CNC间氢键与疏水相互作用的形成,从而增强了界面膜稳定性[6]。同时,附着于不同油水界面的复合颗粒间氢键作用增强,导致乳液液滴间产生强氢键作用,进一步稳定了液滴结构。此外,UCCG稳定的HIPEs其G′值均高于对应的UCC样品。该趋势与表观黏度的变化规律一致(图1-C)。当剪切速率从0.1 s-1增至100 s-1时,6种HIPEs的表观黏度均下降,表明均具有剪切稀化特性。HIPEs的表观黏度随CA-CNC比例增加而升高,此现象与WONG等[22]的研究结果相符,该研究证实大豆分离蛋白-纳米纤维素(soy protein isolate-CNC,SPI-CNC)体系中SPI含量的增加同样会提高HIPEs的表观黏度。值得注意的是,添加GSE的UCCG 稳定的HIPEs,其表观黏度高于未添加GSE的对应组。这可能是由于GSE的引入增强了GSE与UCC间的分子间相互作用,主要为氢键与静电相互作用,其中静电作用占主导地位[23]。这种分子间相互作用的增强可以赋予复合颗粒在油水界面形成更稳定的界面膜,防止乳滴的聚集。同时,乳滴间增强的静电斥力限制了其运动。上述2种机制的协同效应促使HIPEs形成高度密堆积的液滴结构,最终导致表观黏度升高。
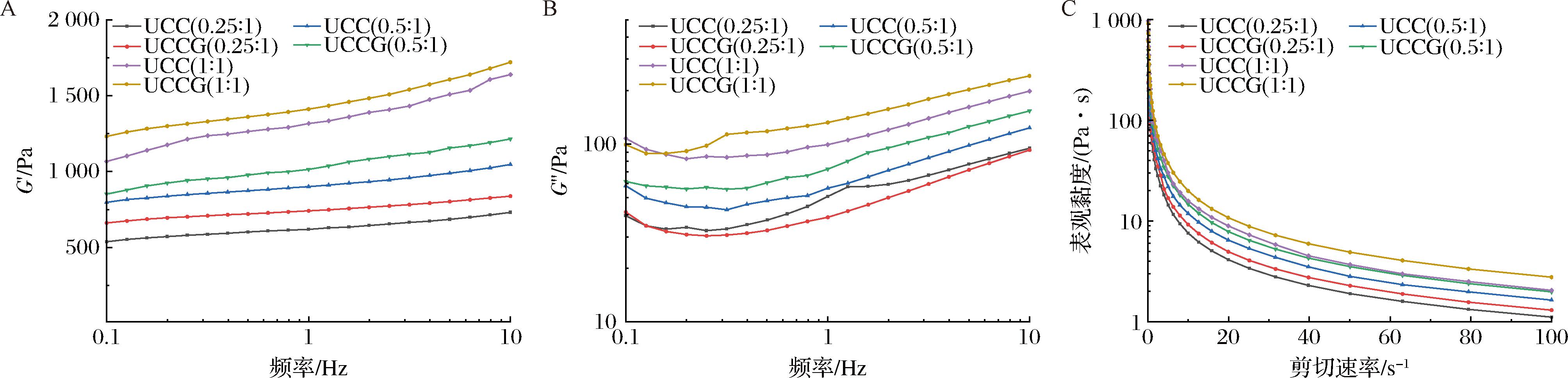
A-G′;B-G″;C-表观黏度
图1 HIPEs的G′、G″和表观黏度
Fig.1 The storage modulus (G′), loss modulus (G″) and apparent viscosity of HIPEs
2.1.2 氧化稳定性
如图2所示,随着UCC比例增加,其稳定的HIPEs的TBARS显著降低。相较于UCC(0.25∶1),UCC(1∶1)的TBARS值下降尤为显著。这一现象可能源于CA含量增加强化了CA与CNC间的氢键作用,促使复合颗粒在油水界面形成更致密有序的排列结构,进而构建出稳定性更高的界面膜[6]。增强的界面屏障效应可有效阻隔油相与氧化因子(如氧分子及自由基)的接触,从而抑制脂质的次级氧化[24]。此外,此外,添加GSE的UCCG体系亦呈现相似的TBARS值变化趋势,即随CA占比提高,脂质氧化程度逐渐减弱。值得注意的是,在相同CA添加比例下,UCC与其对应UCCG稳定的HIPEs间,TBARS值未呈现显著差异。综合而言,CA与CNC通过分子间作用力(氢键及疏水相互作用)形成的致密界面膜本身已具备优异的氧阻隔性能。这种物理屏障作用可能主导了抗氧化效应,导致外源添加的GSE的贡献未达统计学显著水平。
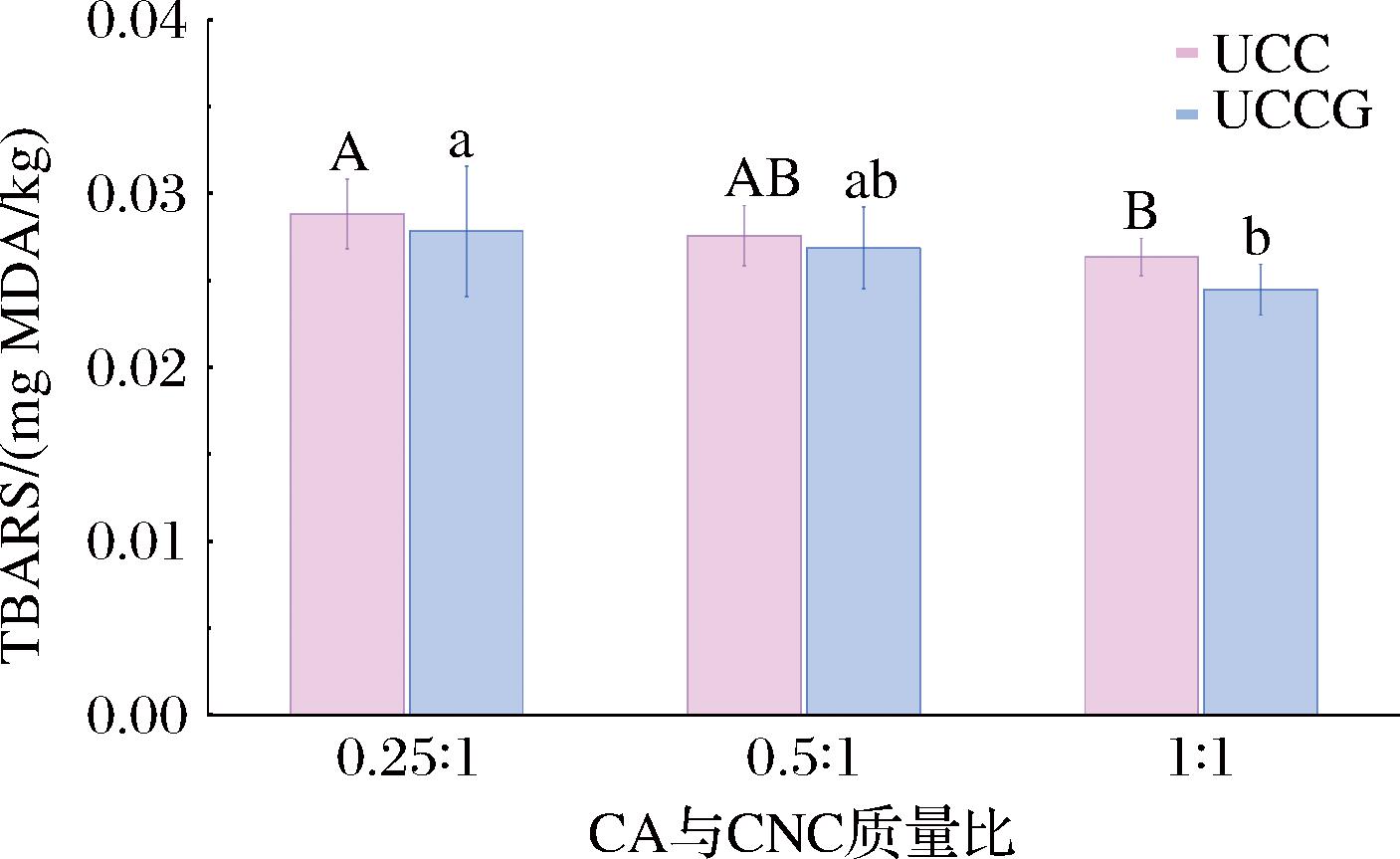
图2 HIPEs的次级氧化产物含量
Fig.2 The content of secondary oxidant products of HIPEs
注:不同大写字母表示不同CA与CNC质量比稳定的HIPEs间差异显著(P<0.05);小写字母表示其相应添加GSE对照组间差异显著(P<0.05)(下同)。
2.2 空气煎炸鱼糜片的质构特性
煎炸食品的质构特性是决定煎炸鱼糜品质及消费者接受度的关键指标。如图3-A和图3-C所示,大豆油样品的硬度和咀嚼性显著高于所有HIPEs样品,而其弹性与内聚性则与HIPEs样品无显著差异(图3-B和图3-D)。这种差异可能源于大豆油较高的流动性,导致其难以在鱼糜片表面形成均匀覆盖层,从而加速水分流失并增加硬度。在HIPEs涂层样品中,随着CA比例的增加,UCC系列样品的硬度显著降低,其中UCC(1∶1)的硬度最低。此现象可归因于UCC中CA比例上升增强了CA与CNC间的氢键相互作用,促使复合颗粒在油水界面形成更致密、有序的排列结构,进而构建出稳定性更高的界面膜[6]。该结构有利于形成高密度堆积的稳定乳液液滴,从而提升HIPEs的黏度和稳定性。在煎炸过程中,此类稳定的HIPEs能形成更均匀的保护层,有效减少水分蒸发并维持鱼糜内部结构,最终降低硬度。值得注意的是,UCCG系列样品的硬度和咀嚼性随CA比例增加未呈现显著变化。
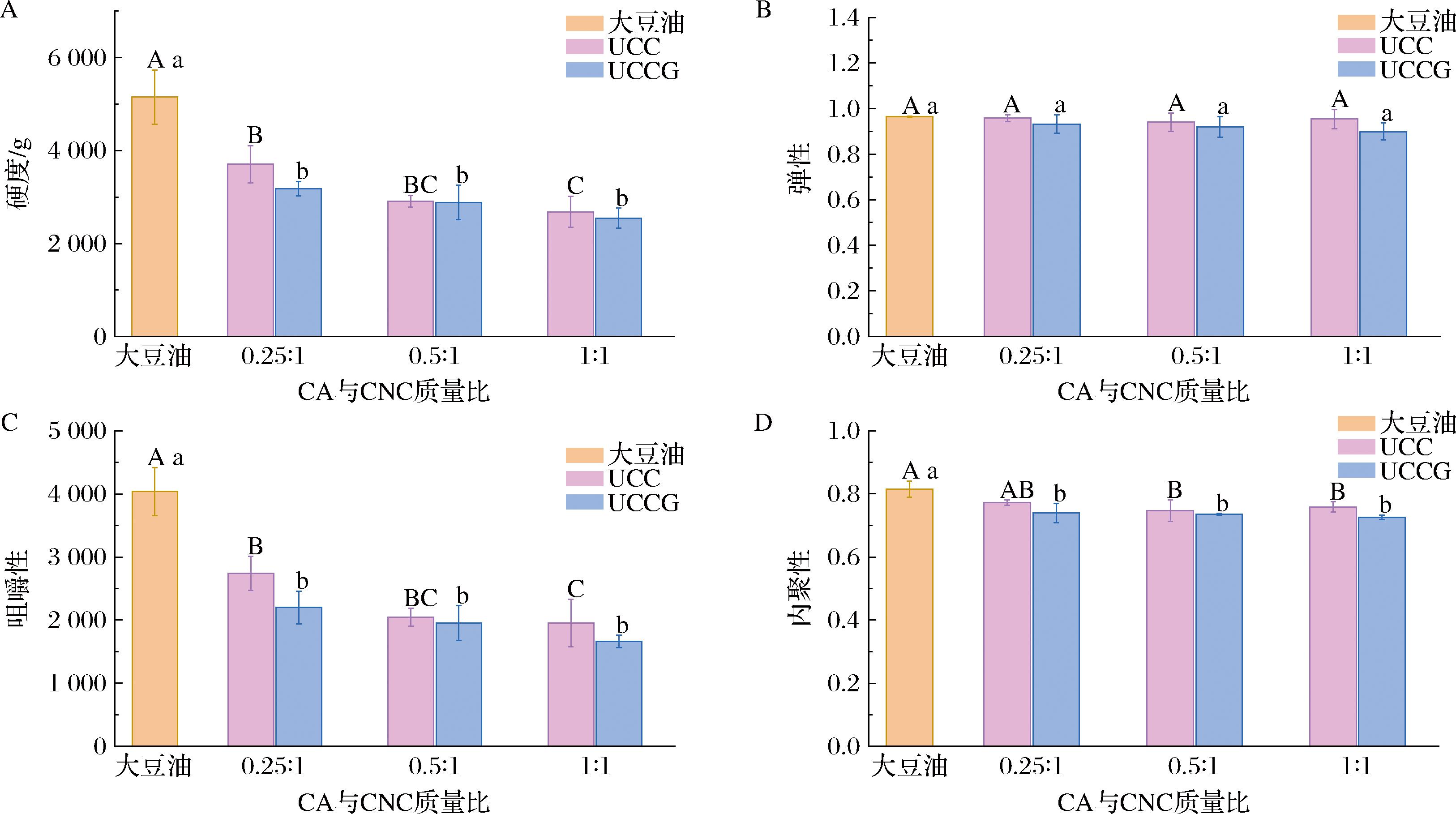
A-硬度;B-弹性;C-咀嚼性;D-内聚性
图3 不同CA与CNC质量比稳定HIPEs涂层空气煎炸鱼糜片的硬度、弹性、咀嚼性、内聚性
Fig.3 Hardness, elasticity, chewiness, and cohesiveness of air-fried surimi fillets coated with HIPEs stabilized with different CA to CNC mass ratios
2.3 空气煎炸鱼糜片的色泽
煎炸食品均匀的金黄色泽是评价其感官品质的重要指标,其中L*是煎炸食品的主要因素,被普遍认为是消费者在评估产品可接受性时评价的第一质量属性。图4显示了不同黏度HIPEs涂层对空气煎炸鱼糜颜色的影响。大豆油组的L*值最小,而表征褐变程度的黄蓝色b*值则最大。这一现象主要归因于油相的高流动性:在热加工过程中,油膜难以形成连续阻隔层,致使样品表面局部区域与氧气直接接触。结合样品外观,大豆油涂层制品表面呈现暗沉色泽,且存在明显的中心-边缘色差,这可能是由于氧气介导的美拉德反应、焦糖化反应及油脂中磷脂的降解等褐变反应协同作用所致[25]。在HIPEs体系中,UCC(0.5∶1)和UCC(1∶1)的L*值相比于UCC(0.25∶1)显著增加,这是因为UCC比例的上升增加了CA与CNC之间的氢键作用,促使复合颗粒在油水界面形成更为致密有序的排列结构,构建出具有更高稳定性的界面膜,从而形成更稳定的高密度堆积的乳滴,导致HIPEs黏度和热稳定性随之增加,使得在煎炸过程中更好地黏附于样品表面形成物理屏障,阻止了氧气的接触,减少了褐变物质的沉积,提高亮度,这与外观图反映的结果一致。而UCC体系中b*值无明显差异。值得注意的是,UCCG虽呈现与UCC相同的L*、b*变化趋势,但相比于对应的UCC,其L*相对下降且b*略有上升。从外观图也可以看到UCCG相比于UCC色泽略深。这可能使由于HIPEs中添加了GSE,GSE主要由原花青素和少量没食子酸、儿茶素等单体多酚组成[26]。ZHOU等[27]报告称,茶多酚(表没食子儿茶素没食子酸酯及其二聚体)在高温下可分解成没食子酸并聚合成色素。因此,推测GSE在高温下可能会发生氧化和聚合过程,导致它们转化为黄褐色,从而加深鱼糜片的表面颜色。综上所述,UCC(0.5∶1)和UCCG(0.5∶1)能够展现出较为理想的煎炸色泽的特征。
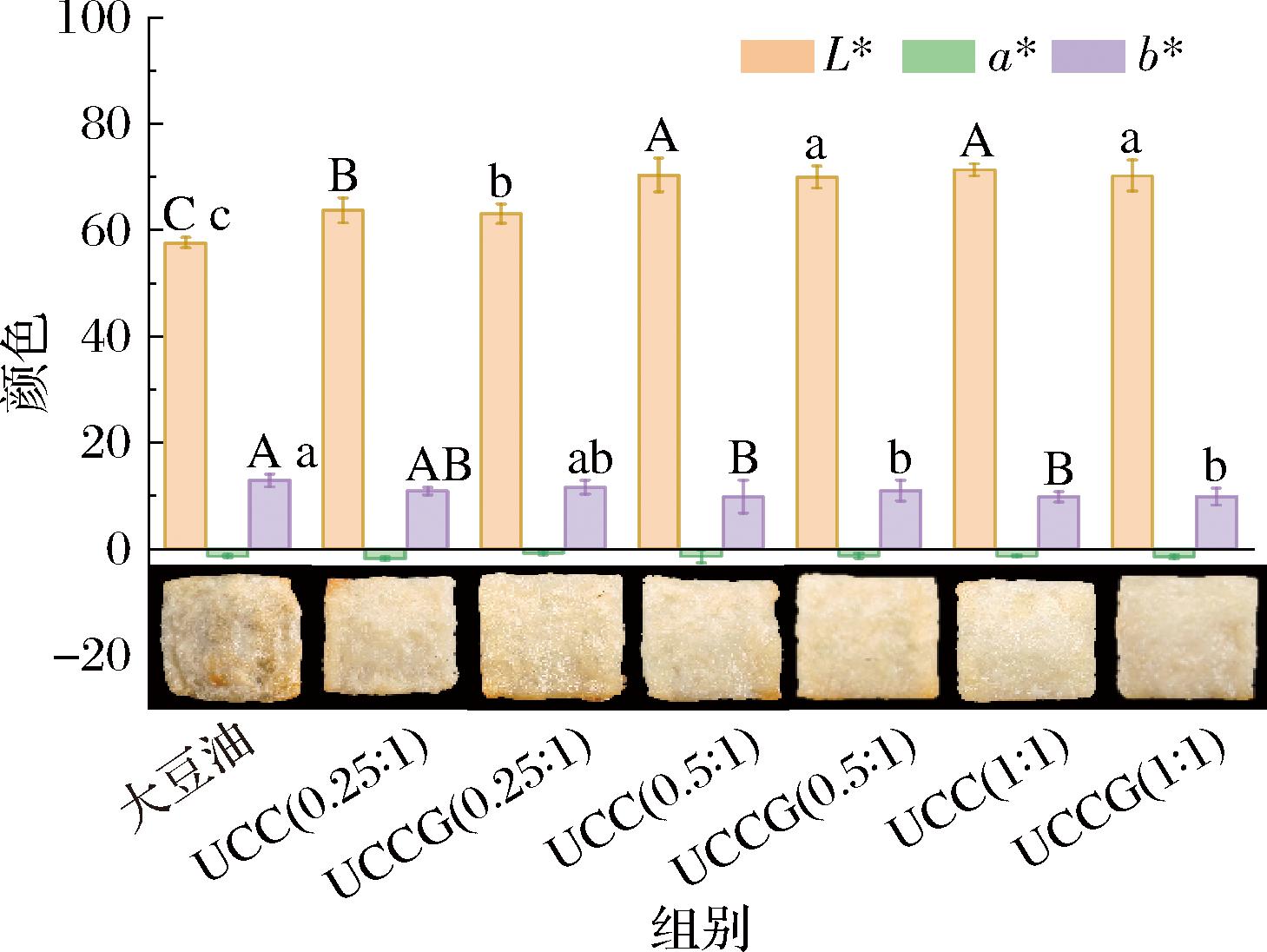
图4 不同CA与CNC质量比稳定HIPEs涂层空气煎炸鱼糜片的色泽
Fig.4 Color of air-fried surimi fillets coated with HIPEs stabilized with different CA to CNC mass ratios
2.4 空气煎炸鱼糜片的脂质氧化
如图5所示,相比于Oil,UCC对脂质氧化的抑制效果显著提升。在UCC体系中,TBARS值随CA比例增加呈现下降趋势,其中UCC(0.5∶1)和UCC(1∶1)表现出最优抗氧化性能。这是由于CA与CNC之间增强的氢键作用使复合颗粒更好在油水界面形成稳定界面膜,同时高比例的CA可在界面膜中的CA-CNC之间提供更多的氢键[6],这可能会加强乳液液滴的界面膜和乳液液滴之间的相互作用,限制乳液液滴的迁移,从而形成更稳定且高度紧密堆积的乳滴,这种拓扑排列防止氧气穿透HIPEs接触鱼糜片,有效抑制了脂质氧化。在UCCG体系中,虽然添加GSE后TBARS值较对应UCC略有降低,但统计学分析显示差异不显著。这可能是因为CA与CNC通过强氢键和疏水作用构建的刚性界面膜主导了HIPEs涂层的稳定性,而引入的GSE主要通过较弱的静电相互作用与复合颗粒结合[23]。由于氢键作用的结合能显著高于静电相互作用,GSE的介入未能实质性改变界面膜的力学特性。
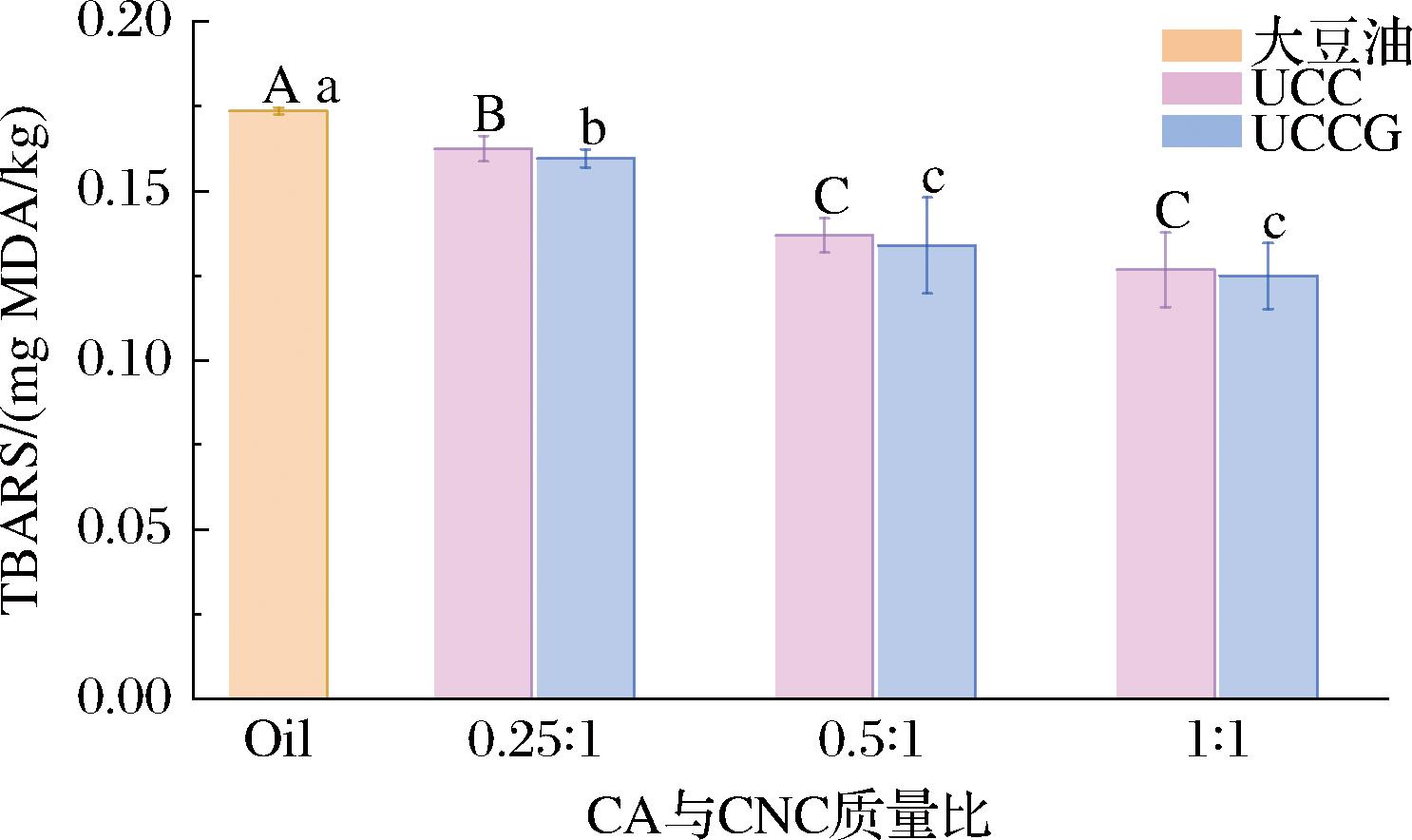
图5 不同CA与CNC质量比稳定HIPEs涂层空气煎炸鱼糜片的脂肪氧化
Fig.5 Lipid oxidation in air-fried surimi fillets coated with HIPEs of stabilized with different CA to CNC mass ratios
2.5 空气煎炸鱼糜片的自由基测定
如图6-A所示,通过电子顺磁共振光谱分析发现,大豆油组在3 470~3 545 G磁场范围内表现出显著的自由基信号,表明其自由基含量最高。图6-B~图6-D表明,在UCC体系中,自由基的含量UCC(0.25∶1)>UCC(0.5∶1)>UCC(1∶1),这一结果与上述脂质氧化产物的积累规律高度吻合。由图6可以看出,由UCC稳定的HIPEs作为涂层随着CA比例的增加,能够显著减少自由基的产生,HIPEs的抗氧化效果归因于其凝胶层对氧气的隔绝,而高比例的CA致使HIPEs的黏度显著上升且稳定性增加,其致密的凝胶网络结构可有效阻隔氧气渗透,同时增强乳液在鱼糜片表面的黏附均匀性,抑制了自由基链式反应的引发与传播。在UCCG体系中,自由基含量UCCG(0.25∶1)>UCCG(0.5∶1)>UCCG(1∶1),但相比于对应UCC,UCCG的自由基含量轻微下降,这是因为GSE通过静电相互作用与CA交联[23],形成更致密的界面膜结构,提升HIPEs稳定性,进一步抑制了自由基的生成。
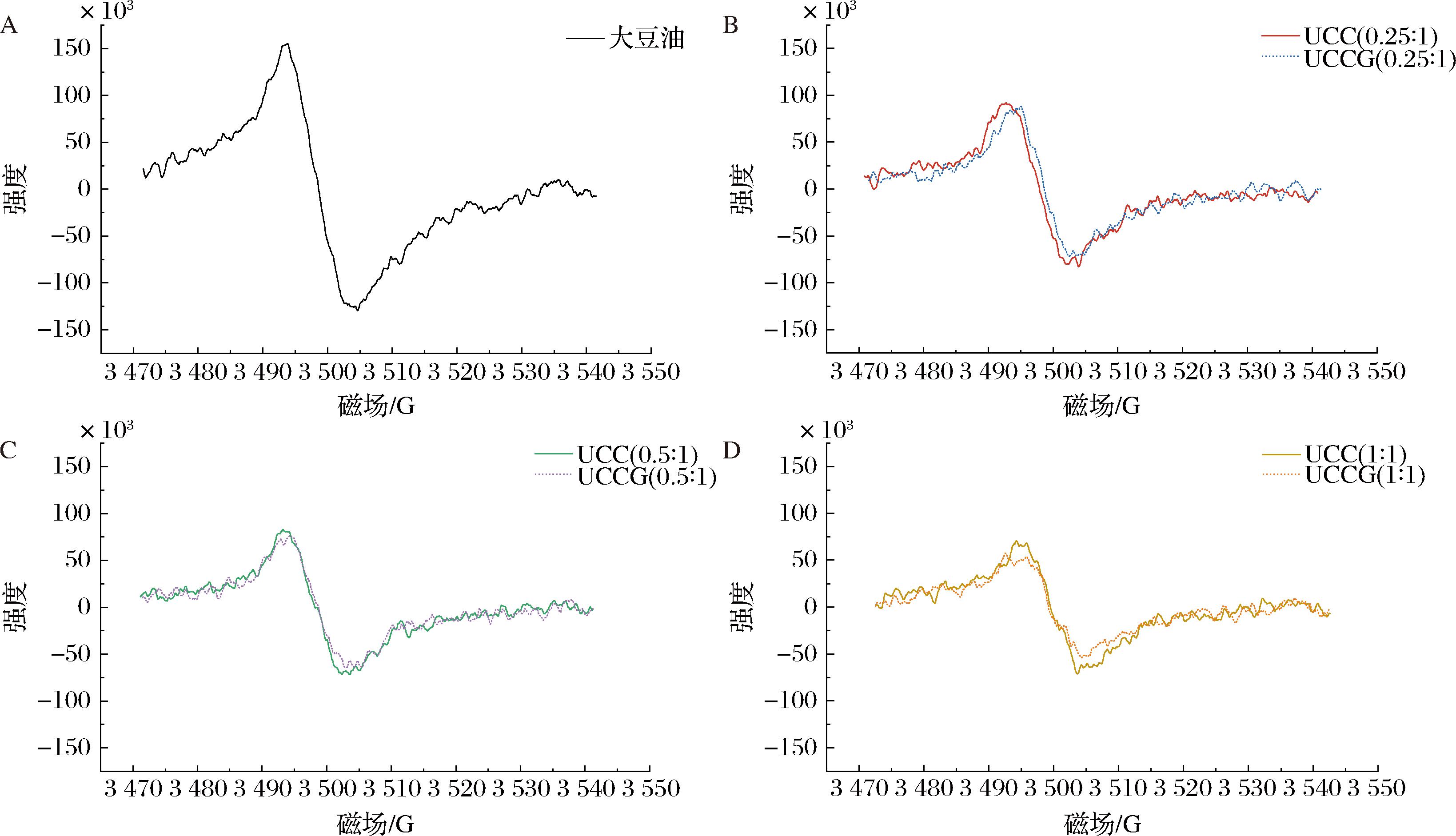
A-大豆油;B-UCC(0.25∶1)和UCCG(0.25∶1);C-UCC(0.5∶1)和UCCG(0.5∶1);D-UCC(1∶1)和UCCG(1∶1)
图6 不同CA与CNC质量比稳定HIPEs涂层空气煎炸鱼糜片的ESR光谱
Fig.6 ESR spectra of air-fried surimi fillets coated with HIPEs stabilized with different CA to CNC mass ratios
2.6 空气煎炸鱼糜片的杂环胺含量
为探究不同黏度HIPEs涂层对鱼糜片杂环胺生成的影响,采用HPLC-MS/MS进行目标物定量分析。本研究对用于检测5种杂环胺方法的线性范围、相关系数和标准曲线进行了验证,各分析参数如表1所示。考虑到待测物的极性和信号响应的差异,本研究选择了D3-4,8-DiMeIQx来校正目标化合物,所有待测物均配制成质量浓度为1.00、5.00、10.00、20.00、50.00、100.00、200.00 ng/mL的混标溶液,在此范围内建立并评估标准曲线。使用标准曲线通过线性回归分析选择每种分析物合适的线性范围并优化相关系数(R2)。结果显示所有目标分析物均在其线性范围内均显示出良好的线性,且R2≥0.99。
表1 待测物的线性范围,相关系数和标准曲线
Table 1 The liner range, correlation coefficient, and calibration curves of analytes
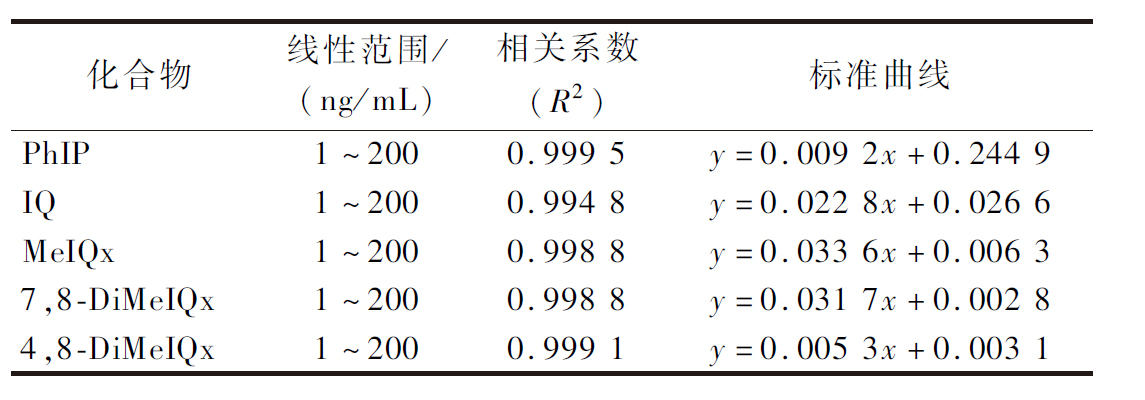
化合物线性范围/(ng/mL)相关系数(R2)标准曲线PhIP1^2000.999 5y=0.009 2x+0.244 9IQ1^2000.994 8y=0.022 8x+0.026 6MeIQx1^2000.998 8y=0.033 6x+0.006 37,8-DiMeIQx1^2000.998 8y=0.031 7x+0.002 84,8-DiMeIQx1^2000.999 1y=0.005 3x+0.003 1
如图7-A所示,由于在高温下鱼糜的肌酸、氨基酸和碳水化合物等前体物较易通过美拉德反应产生氨基咪唑氮杂芳烃类杂环胺[28],因此5种杂环胺均被检测到。其中,PhIP的生成量显著高于其他化合物,其次是4,8-DiMeIQx,IQ、7,8-DiMeIQx和MeIQx生成的含量较少。大豆油样品中PhIP含量显著高于HIPEs样品,这可能源于油脂氧化过程中产生的不饱和脂肪酸衍生物,特别是2,4-二烯醛和2-烯醛等活性羰基化合物,其作为关键前体物质直接参与了PhIP的合成路径[29]。在UCCG中,PhIP和4,8-DiMeIQx的生成量较对应的UCC呈现持平或下降。食品中杂环胺的形成与美拉德反应中不稳定自由基的产生有关,而含有抗氧化剂成分的物质能够有效的清除这些自由基,从而达到抑制杂环胺生成的效果。孙思远[30]研究表明添加茶多酚显著抑制空气油炸鲐鱼4,8-DiMeIQx的产生。如图7-B所示,大豆油样品的杂环胺累积量显著高于其他实验组,UCC/UCCG(0.25∶1、0.5∶1)、UCC(1∶1)无显著差异,而UCCG-1含量最小,这可能源于高浓度CA对HIPEs界面膜的强化作用与GSE抗氧化体系的协同调控机制。当CA-CNC比例增强使,形成致密界面膜,显著提高HIPEs的流变稳定性。与此同时,GSE中高含量表没食子儿茶素没食子酸酯通过清除羟自由基。UCCG复合体系通过双重作用机制,使美拉德反应中活性羰基化合物生成量减少,最终导致杂环胺前体物浓度下降。
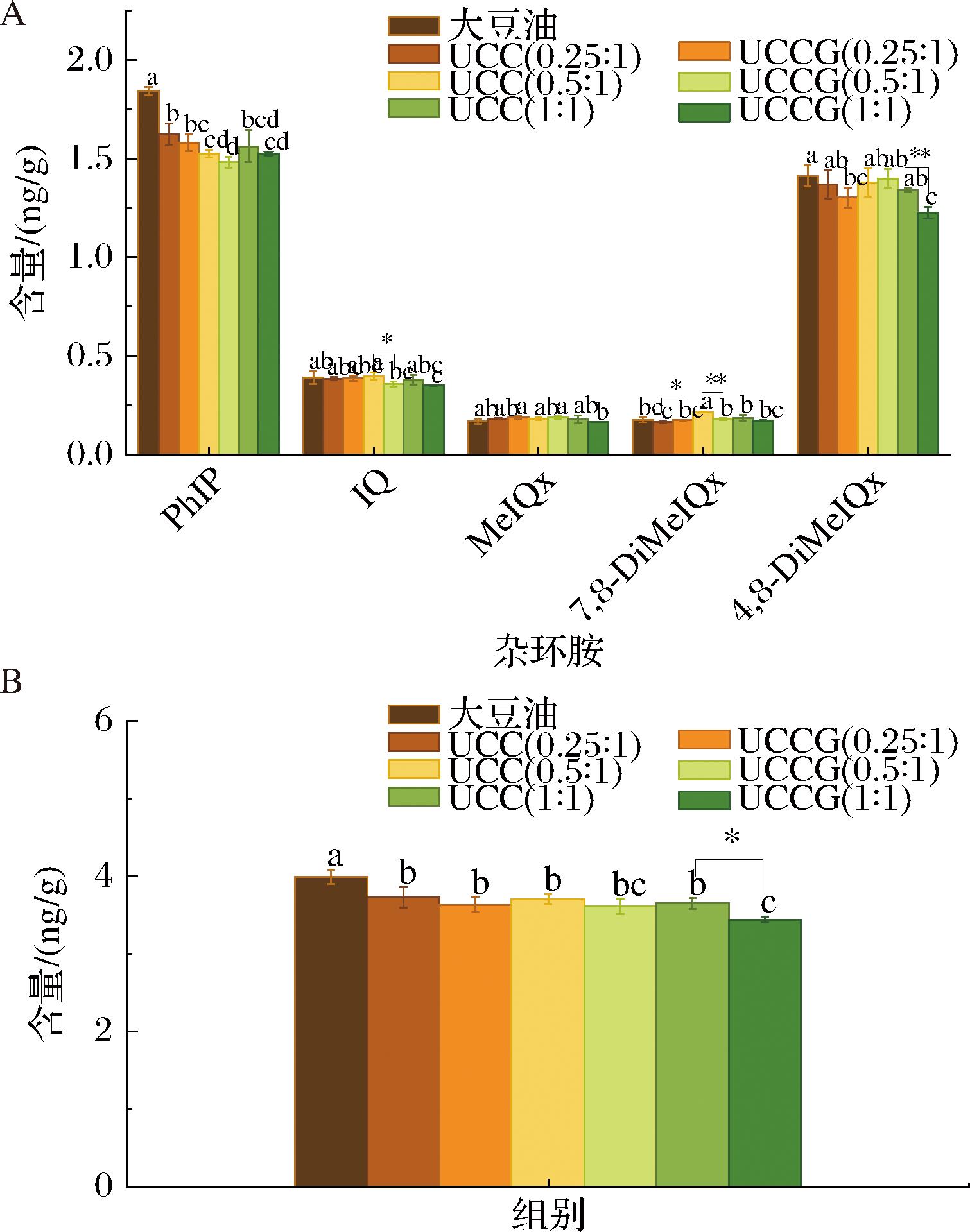
A-不同种类杂环胺的含量;B-总含量
图7 不同CA与CNC质量比稳定HIPEs涂层空气煎炸鱼糜片的不同种类杂环胺的含量和总含量
Fig.7 Content of different types of heterocyclic amines and total heterocyclic amines of air-fried surimi fillets coated with HIPEs stabilized with different CA to CNC mass ratios
注:*表示P<0.05,**表示P<0.01。
3 结论与讨论
本研究制备不同黏度HIPEs涂层,系统评估了其对空气煎炸鱼糜制品品质的影响。结果表明,在色泽方面,UCC(0.5∶1)和UCCG(0.5∶1)样品呈现明亮且均匀的金黄色,既无褐色物质积累,又符合油炸食品的典型色泽特征。在质构方面,UCC/UCCG(≤0.5)的硬度与咀嚼性与大豆油组最为接近,表明其质构特性模拟大豆油组效果最佳。在抗氧化性方面,UCC/UCCG(≥0.5)显著抑制了脂质氧化,自由基含量随CA比例升高呈梯度下降趋势;而UCCG体系因GSE的加入,其自由基清除效率提升。在危害物抑制方面,UCCG(1∶1)得益于高CA比例强化界面膜与GSE抗氧化活性的协同效应,其杂环胺总量最低。综上,UCCG(0.5∶1)涂层显著改善了鱼糜制品的质构和色泽,并有效抑制了加工过程中脂质氧化和杂环胺的生成,实现了对鱼糜制品低危害、高品质的多目标优化,为开发健康煎炸食品提供了创新性的理论依据与技术支撑。
[1] ZHANG S J, ZHANG L Z, YIN T, et al.Exploring the versatility of carbohydrates in surimi and surimi products:Novel applications and future perspectives[J].Journal of the Science of Food and Agriculture, 2024, 104(4):1874-1883.
[2] POKORNY J.Substrate influence on the frying process[J].Grasas Aceites, 1998, 49(3-4):265-270.
[3] DONG L, QIU C Y, WANG R C, et al.Effects of air frying on French fries:The indication role of physicochemical properties on the formation of Maillard hazards, and the changes of starch digestibility[J].Frontiers in Nutrition, 2022, 9:889901.
[4] 张贵会,欧阳辉,黄榆,等.空气油炸与微波处理对南瓜籽品质的影响[J].食品与机械,2022,38(12):190-198.ZHANG G H, OUYANG H, HUANG Y, et al.Effects of air-frying and microwave treatment on the quality of pumpkin seed kernels[J].Food &Machinery,2022,38(12):190-198.
[5] BAGO RODRIGUEZ A M, BINKS B P.High internal phase pickering emulsions[J].Current Opinion in Colloid &Interface Science, 2022, 57:101556.
[6] LIU Z, LIN D H, SHEN R, et al.Bacterial cellulose nanofibers improved the emulsifying capacity of soy protein isolate as a stabilizer for Pickering high internal-phase emulsions[J].Food Hydrocolloids, 2021, 112:106279.
[7] CHEN H, JI A G, QIU S, et al.Covalent conjugation of bovine serum album and sugar beet pectin through Maillard reaction/laccase catalysis to improve the emulsifying properties[J].Food Hydrocolloids, 2018, 76:173-183.
[8] ASHAOLU T J, ZHAO G H.Fabricating a Pickering stabilizer from okara dietary fibre particulates by conjugating with soy protein isolate via Maillard reaction[J].Foods, 2020, 9(2):143.
[9] KARGARZADEH H, MARIANO M, GOPAKUMAR D, et al.Advances in cellulose nanomaterials[J].Cellulose, 2018, 25(4):2151-2189.
[10] LI X Y, SUN P H, FU L, et al.Surface modification of cellulose nanocrystals by physically adsorbing lactoferrin as Pickering stabilizers:Emulsion stabilization and in vitro lipid digestion[J].Food Structure, 2023, 37:100331.
[11] XU G R, WANG C N, YAO P.Stable emulsion produced from casein and soy polysaccharide compacted complex for protection and oral delivery of curcumin[J].Food Hydrocolloids, 2017, 71:108-117.
[12] ABD EL-SALAM M H, EL-SHIBINY S.Preparation and potential applications of casein-polysaccharide conjugates:A review[J].Journal of the Science of Food and Agriculture, 2020, 100(5):1852-1859.
[13] TIAN L L, ROOS Y H, BILIADERIS C G, et al.Effect of ultrasound on the interactions and physicochemical properties of the whey protein isolate-tremella fuciformis polysaccharide system[J].Food Hydrocolloids, 2024, 157:110375.
[14] YANG J, HUANG F H, HUANG Q D, et al.Physical and emulsifying properties of pea protein:Influence of combined physical modification by flaxseed gum and ultrasonic treatment[J].Food Science and Human Wellness, 2023, 12(2):431-441.
[15] REVOL J F, BRADFORD H, GIASSON J, et al.Helicoidal self-ordering of cellulose microfibrils in aqueous suspension[J].International Journal of Biological Macromolecules, 1992, 14(3):170-172.
[16] LIU Y H, FU D W, BI A Q, et al.Development of a high internal phase emulsion of Antarctic krill oil diluted by soybean oil using casein as a co-emulsifier[J].Foods, 2021, 10(5):917.
[17] WANG X Q, SHEN Z Y, HAO R Y, et al.Nanocellulose prepared from shiitake mushroom (Lentinus edodes) stipe by high pressure homogenization and the gel-like emulsions stabilized by them[J].International Journal of Biological Macromolecules, 2025, 300:140210.
[18] 罗晓林,潘锦锋,徐献兵.香菇风味高内相乳/液体油涂层应用下空气油炸鱿鱼的品质特征比较[J].现代食品科技,2022,38(12):51-58.LUO X L, PAN J F, XU X B.Comparison of quality characteristics of air-fried squid with application of shiitake-flavored high internal phase emulsion/liquid oil coating[J] Modern Food Science and Technology,2022,38(12):51-58.
[19] 姜化彬,李文钊,王绍顺,等.鸡腿在油炸过程中的品质变化规律研究[J].食品研究与开发,2017,38(11):17-20;157.JIANG H B, LI W Z, WANG S S, et al.Study on the quality change of chicken in frying process[J].Food Research and Development,2017,38(11):17-20;157.
[20] 李德阳.虾类加工和贮藏过程中品质变化机制及调控研究[D].大连:大连工业大学,2020.LI D Y.Research on the mechanism and regulation of quality changes in shrimp during processing and storage [D].Dalian:Dalian Polytechnic University,2020.
[21] GAO J X, QIN L, WEN S Y, et al.Simultaneous determination of acrylamide, 5-hydroxymethylfurfural, and heterocyclic aromatic amines in thermally processed foods by ultrahigh-performance liquid chromatography coupled with a Q exactive HF-X mass spectrometer[J].Journal of Agricultural and Food Chemistry, 2021, 69(7):2325-2336.
[22] WONG S K, LOW L E, SUPRAMANIAM J, et al.Physical stability and rheological behavior of Pickering emulsions stabilized by protein-polysaccharide hybrid nanoconjugates[J].Nanotechnology Reviews, 2021, 10(1):1293-1305.
[23] WANG C, WEI M, ZHU H P, et al.Development of porous materials via protein/polysaccharides/polyphenols nanoparticles stabilized Pickering high internal phase emulsions for adsorption of pb2+ and cu2+ ions[J].Food Chemistry, 2024, 445:138796.
[24] NIE C L, BU X P, MA S H, et al.Pickering emulsions synergistically stabilized by cellulose nanocrystals and peanut protein isolate[J].LWT, 2022, 167:113884.
[25] SHI H N, QIN R K, WU R L, et al.Effect of cryoprotectants on the formation of advanced glycation end products and acrylamide in fried fish cakes[J].Food Bioscience, 2021, 44:101433.
[26] GUO Y C, HUANG J C, CHEN Y R, et al.Effect of grape seed extract combined with modified atmosphere packaging on the quality of roast chicken[J].Poultry Science, 2020, 99(3):1598-1605.
[27] ZHOU J, WU Y, LONG P P, et al.LC-MS-based metabolomics reveals the chemical changes of polyphenols during high-temperature roasting of large-leaf yellow tea[J].Journal of Agricultural and Food Chemistry, 2019, 67(19):5405-5412.
[28] TORIBIO F, BUSQUETS R, PUIGNOU L, et al.Heterocyclic amines in griddled beef steak analysed using a single extract clean-up procedure[J].Food and Chemical Toxicology, 2007, 45(4):667-675.
[29] ZAMORA R, ALC N E, HIDALGO F J.Effect of lipid oxidation products on the formation of 2-amino-1-methyl-6-phenylimidazo [4, 5-b] pyridine (PhIP) in model systems[J].Food Chemistry, 2012, 135(4):2569-2574.
N E, HIDALGO F J.Effect of lipid oxidation products on the formation of 2-amino-1-methyl-6-phenylimidazo [4, 5-b] pyridine (PhIP) in model systems[J].Food Chemistry, 2012, 135(4):2569-2574.
[30] 孙思远.不同空气油炸条件对鲐鱼品质及安全性的影响研究[D].烟台:烟台大学, 2020.SUN S Y.Research on the effects of different air frying conditions on the quality and safety of mackerel [D] Yantai:Yantai University,2020.