铁蛋白是广泛存在于植物、动物和微生物中的高度保守的铁贮存蛋白,通常一个铁蛋白分子内腔中可以携带大约4 500个铁原子[1],并且它可以通过小肠中受体介导的内吞作用被吸收,近年来被认为是一种潜在的新型天然铁补充剂[2]。Holoferritin由铁蛋白纳米笼和铁核共同组成,其中,铁蛋白纳米笼是呈现外径约12 nm、内径约8 nm的中空笼形结构,由24个亚基通过F432点对称自组装形成菱形十二面体构型[3]。每个铁蛋白亚基N端都含有一个亚铁氧化酶中心,可以将Fe2+快速转化为Fe3+,并沉积形成含2 000~4 500个铁原子矿化核,具有调节铁代谢平衡和消除亚铁毒性的双重功能[4]。
目前,Holoferritin的制备主要包括动/植物提取途径、体外合成途径和生物合成途径。其中,由动、植物源中提取的Holoferritin,依赖复杂的细胞表达、破碎、提取以及层析等纯化步骤提取蛋白,存在细胞破碎效率低、纯化损失高等缺陷[3]。体外合成法则通过控制外部条件(如溶液pH值、温度等)合成Holoferritin的内部铁芯结构,虽然可以实现对铁含量的自由调控,但受限于铁/铁蛋白负载比,当其负载比大于1 000时,易引发铁蛋白的聚集和沉淀[5]。Holoferritin的生物合成途径,主要通过调节亚铁离子在微生物体内的生物合成,进而依赖细胞蛋白表达、提取和纯化等步骤,最终实现Holoferritin的制备。此途径虽可在一定程度上弥补上述2种合成途径的不足,但仍受限于复杂的层析纯化流程,存在纯化效率较低、蛋白损失严重的问题[6]。综上所述,现行Holoferritin的制备方法面临的主要瓶颈包括:a)多步复杂的纯化步骤导致蛋白产率损失,阻碍蛋白规模化生产;b)铁核负载效率与蛋白稳定之间的矛盾性。
因此,本研究基于铁离子胁迫诱导微生物细胞生物合成Holoferritin体系,系统探究了Holoferritin的高效制备、纯化工艺,并分析了该工艺条件对Holoferritin结构和性质的影响,以期为Holoferritin的高效制备奠定理论基础和技术支撑。
1 材料与方法
1.1 材料与试剂
胰蛋白胨、酵母提取物,重庆润晨生物科技有限公司;氨苄青霉素(≥99.8%)、异丙基-β-D-硫代半乳糖苷(isopropyl-β-D-thiogalactopyranoside,IPTG≥99.0%)、全能核酸酶(250 u/μL),上海源叶生物科技有限公司;硫酸铵,天津希恩思生化科技有限公司;硫酸亚铁,山东科源生化有限公司。本实验中使用的其他化学试剂均为分析纯。
1.2 仪器与设备
JA3003B电子天平,上海精天电子仪器有限公司;Heraeus Multifuge X3R高速冷冻离心机,美国赛默飞世尔科技公司;JY92-IIN超声波细胞粉碎机、SCIENTZ-10 ND冷冻干燥机,新芝生物;HH-4数显恒温搅拌水浴锅,上海新诺仪器设备有限公司;UV-6100紫外可见分光光度计,上海元析仪器有限公司;JASCO J-1500圆二色谱仪,日本JASCO公司;Spectrum 100傅里叶变换红外光谱仪,美国珀金埃尔默公司;Zetasizer Nano ZS90纳米粒度仪,英国马尔文仪器有限公司;Jem-1400 plus透射电子显微镜,日本电子株式会社。
1.3 实验方法
1.3.1 表达载体的活化与培养
将编码日本囊对虾铁蛋白的cDNA(LOC122256452)经亚克隆插入至大肠杆菌pET-3a表达载体,构建重组质粒。通过定点突变、PCR和酶切处理将其转化至大肠杆菌DH5α中筛选阳性克隆,并进行DNA测序鉴定。将确认突变的重组质粒转入大肠杆菌BL21(DE3)受体细胞中,经二次测序确保其变异准确性后进行大规模蛋白表达[7]。
将细胞置于5 mL含有氨苄青霉素的LB培养基中培养活化,随后接种至500 mL LB培养基上,置于37 ℃下培养至光密度达到0.6。向培养基中同时加入原浓度为200 μL的IPTG溶液和终浓度40 mmol/L的硫酸亚铁溶液,于37 ℃培养8 h,诱导大肠杆菌细胞合成表达Holoferritin。8 000 r/min的转速下离心收集细胞,用25 mmol/L Tris-HCl缓冲液(pH 8.0)洗涤重悬[8]。
1.3.2 Holoferritin的分离与纯化
将收集的细胞在冰浴条件下进行超声细胞破碎20 min(功率325 W,超声3 s,间隔2 s),离心(10 000 r/min,4 ℃,10 min)去除细胞碎片。向上清液中分别添加体积分数为0.005%、0.010%、0.015%的核酸酶,置于37 ℃下搅拌孵育1 h。而后,将溶液置于65 ℃下加热20 min,灭活核酸酶并使热敏蛋白变性,离心(10 000 r/min,4 ℃,10 min)收集上清液。用质量浓度为106~143 g/L的硫酸铵对溶液进行复合处理6 h,离心(10 000 r/min,4 ℃,20 min)收集沉淀的目标蛋白,用25 mmol/L Tris-HCl缓冲液(pH 8.0)复溶并透析3次(8 h/次)。
此外,设置未进行核酸酶处理的Holoferritin作为对照组,按上述步骤处理后,对其采用阴离子交换色谱层析进一步提纯;收集纯化后的蛋白溶液用25 mmol/L Tris-HCl缓冲液(pH 8.0)透析3次(8 h/次)。
1.3.3 核酸的检测
对Holoferritin进行核酸杂质的鉴定,使用质量分数为1%的琼脂糖凝胶对未经核酸酶处理和经不同浓度核酸酶处理的Holoferritin样品进行电泳检测[9],分别取3.5 μL的样品与marker进样,于120 V,25 min的条件下进行恒压电泳。电泳完成后进行染色并在凝胶成像系统下观察、拍照分析。
1.3.4 Holoferritin纯度的鉴定
对上述Holoferritin样品进行十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(sodium dodecyl sulfate polyacrylamide gel electrophoresis,SDS-PAGE)和非变性聚丙烯酰胺凝胶电泳(native polyacrylamide gel electrophoresis,Native-PAGE)分析,以测定其蛋白纯度及亚基的分子质量[8,10]。SDS-PAGE选择丙烯酰胺质量浓度为50 g/L的浓缩胶和120 g/L的分离胶,Native-PAGE选择质量浓度为80 g/L的聚丙烯酰胺梯度凝胶,两者均在80 V运行30 min后转为120 V进行恒压电泳,电泳结束后进一步用考马斯亮蓝R-250染色观察。
1.3.5 Holoferritin结构表征
1.3.5.1 紫外-可见光谱测定
对Holoferritin进行紫外光谱表征,使用紫外-可见分光光度计进行光谱扫描,波长扫描范围为200~500 nm[11]。
1.3.5.2 圆二色谱测定
取质量浓度为0.125 mg/mL的Holoferritin溶液进行圆二色谱扫描,使用1 mm的石英比色皿(光程1 mm)分别装载背景溶液和样品进行测试。波长扫描范围为190~260 nm,扫描速率50 nm/min,采样间隔0.1 s。利用CDNN软件分析α-螺旋、β-折叠、β-转角和无规则卷曲的相对含量[12-13]。
1.3.5.3 傅里叶变换红外光谱测定
将纯化后的样品冷冻干燥成粉末,使用傅里叶变换红外光谱仪进行测定。通过32次扫描,确定其在600~4 000 cm-1区域的吸收特征。所有测量均重复3次[14]。
1.3.5.4 粒径与ζ-电位测定
对Holoferritin进行粒径尺寸分布及电位表征,将Holoferritin用25 mmol/L Tris-HCl缓冲液(pH 8.0)稀释至浓度为0.5 μmol/L,使用马尔文粒度仪测量其粒径分布和ζ-电位[15]。探测器角度为90°,激光波长为633 nm,平衡时间设置为2 min,共运行11次,测量3次,所有样品都在路径长度为10 mm的比色皿中进行测定和分析,分析模型为马尔文软件通用模型(标准分辨率),ζ-电位的分析模型设置为马尔文软件的自动模式。所有值均在25 ℃条件下重复3次测定。
1.3.5.5 透射电子显微镜分析
采用透射电子显微镜对样品进行透射电镜分析。样品制备过程如下[16]:将5 μL样品浇铸在覆有薄层无定形碳的铜网格上1 min,使目标颗粒在其表面被吸收,用滤纸将多余的蛋白质溶液清除,然后在室温下干燥数分钟。用质量浓度为20 g/L的磷钨酸溶液对铜网格进行30 s负染色,并用滤纸去除多余的溶液。进行电镜观察,采集图像分析。
1.4 数据分析与处理
所有实验至少独立进行3次,数据结果以“平均值±标准差”表示,采用SPSS 26进行显著性分析(P<0.05),利用Origin 2025软件对数据进行分析及绘图。
2 结果与分析
2.1 Holoferritin的提取与鉴定
2.1.1 琼脂糖凝胶电泳分析
为探究此制备工艺对宿主残留核酸的去除效果,本研究分别设置了未添加核酸酶处理且未进行阴离子交换色谱层析的Holoferritin作为对照组,与添加不等量核酸酶处理纯化的Holoferritin作为实验组。对两者进行琼脂糖凝胶电泳分析[13],结果如图1所示,对照组样品中呈现明显的核酸特征条带,而经不同浓度核酸酶处理的所有实验组均未检测到核酸残留。结果表明,在设定的浓度范围内,核酸酶能有效降解并去除Holoferritin中残留的核酸。值得注意的是,此制备策略即使未添加阴离子交换色谱纯化步骤,仅通过超声细胞破碎、核酸酶处理、热变性除杂和硫酸铵梯度沉淀步骤即可实现残留核酸的有效清除,初步证实其在简化Holoferritin纯化流程、缩短其制备周期和提高产物纯度等方面具有显著优势。
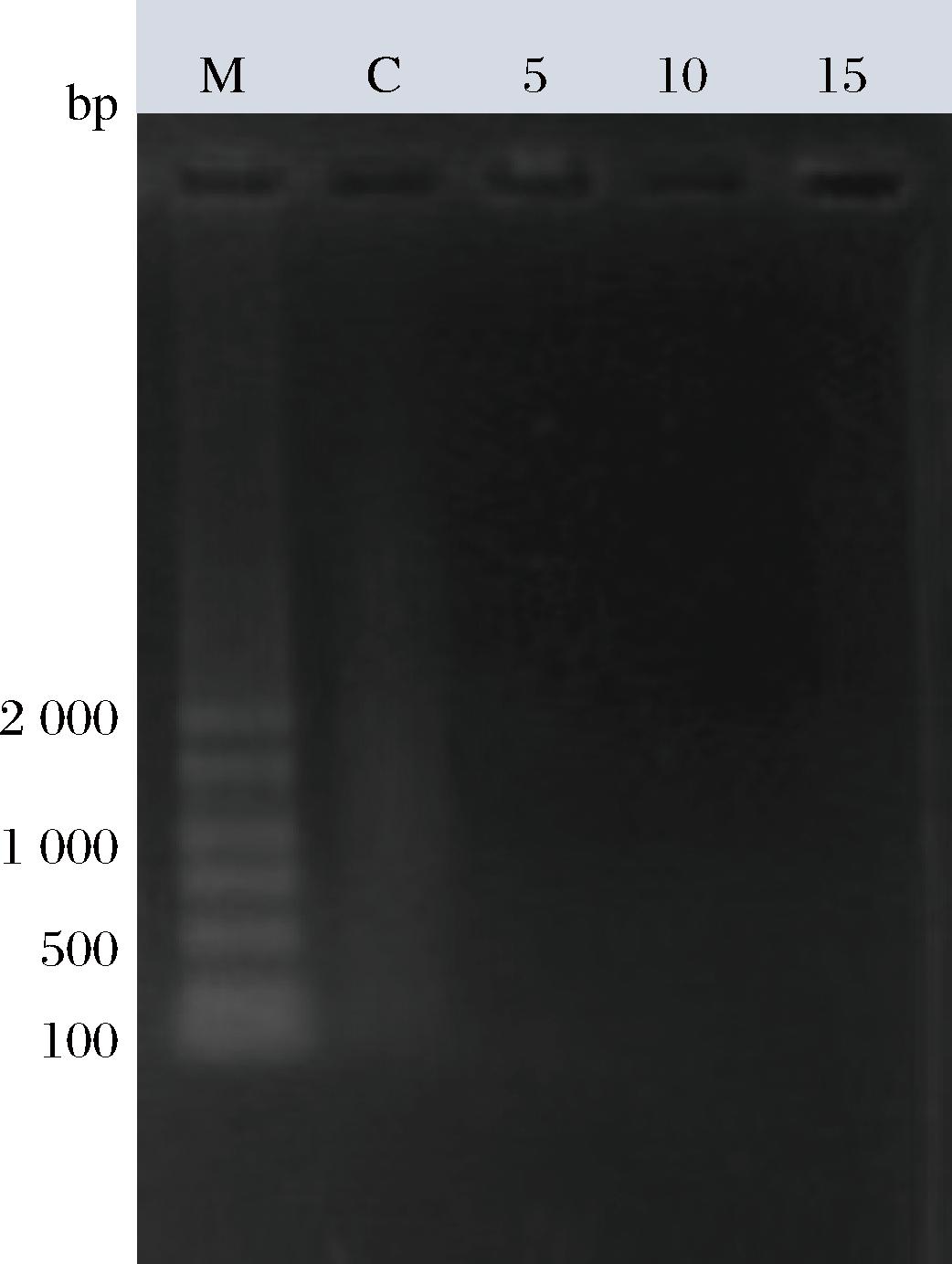
图1 Holoferritin的琼脂糖凝胶电泳结果
Fig.1 The results of the agarose gel electrophoresis for Holoferritin
注:M,蛋白质标志物及其对应分子质量;C,未进行纯化的Holoferritin; 5,添加0.005%核酸酶处理的Holoferritin;10,添加0.010%核酸酶处理的Holoferritin;15,添加0.015%核酸酶处理的Holoferritin(下同)。
2.1.2 SDS-PAGE和Native-PAGE电泳分析
将前述实验组与对照组的Holoferritin样品进行SDS-PAGE和Native-PAGE电泳分析。结果如图2所示,所有样品的SDS-PAGE在19 kDa处均呈现单一且均匀的条带(图2-a),与Holoferritin亚基的理论分子质量吻合;而Native-PAGE则检测到分子质量约为440 kDa的清晰条带(图2-b),对应Holoferritin完整的寡聚体结构[8]。2项电泳结果均未出现杂蛋白弥散条带或自身蛋白降解条带,表明上述制备工艺可有效获取结构完整的高纯度Holoferritin。因此,采用核酸酶处理、加热、硫酸铵沉淀即可获得高纯度Holoferritin,且不需要柱层析纯化步骤,有效减少纯化过程Holoferritin的损失和缩短纯化周期。
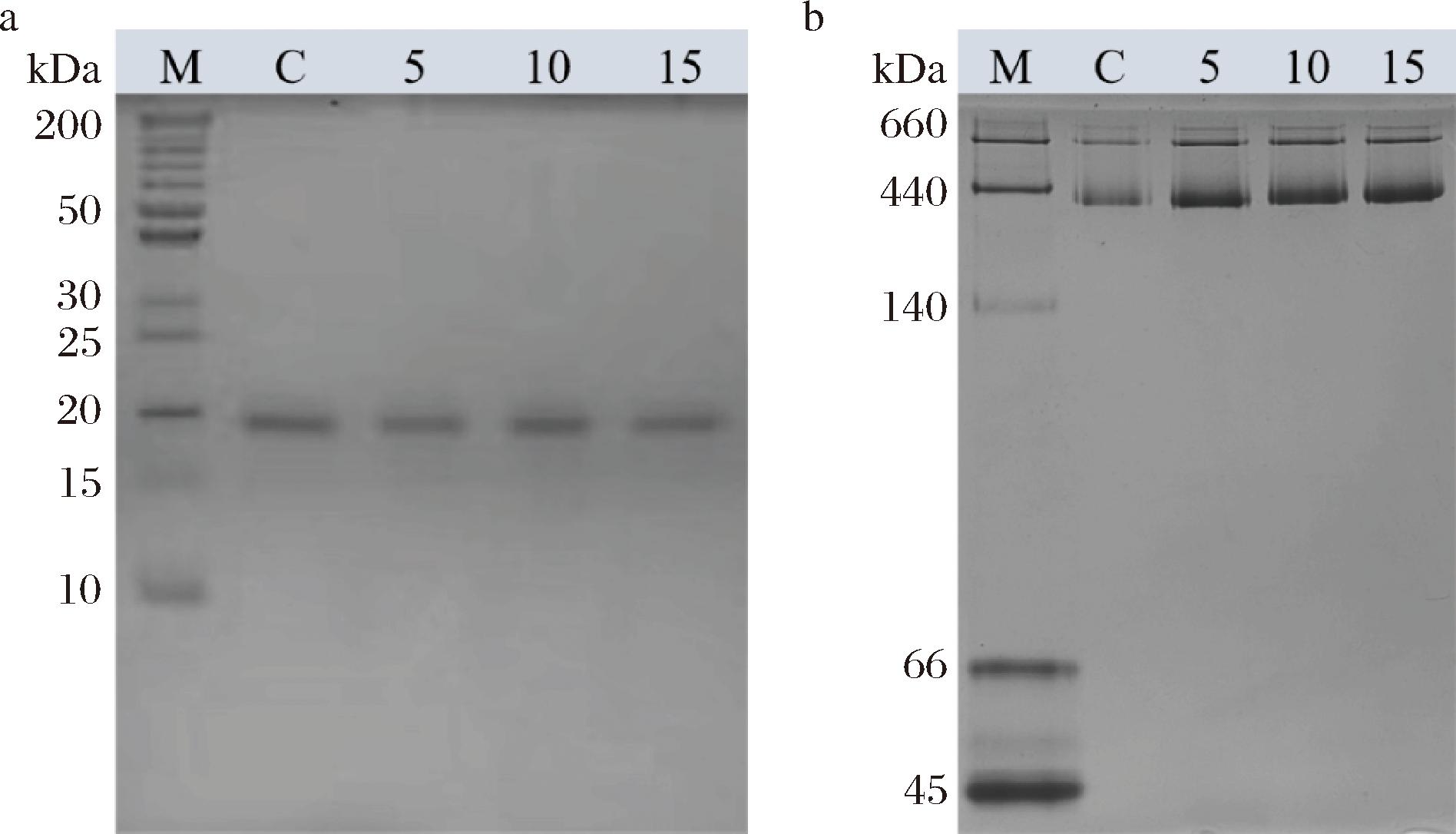
a-Holoferritin的SDS-PAGE结果;b-Holoferritin的Native-PAGE结果
图2 Holoferritin的SDS-PAGE和Native-PAGE电泳分析结果
Fig.2 The results of SDS-PAGE and Native-PAGE electrophoresis analysis of Holoferritin
上述结果表明,添加0.005%核酸酶处理即可使样品中宿主残留的核酸完全去除,且提取的Holoferritin为电泳条带单一的高纯度蛋白。因此,本研究后续将经阴离子交换色谱柱层析(未添加核酸酶处理)的Holoferritin样品作为对照组(Holoferritin,Holo),添加0.005%核酸酶处理纯化(未经阴离子交换色谱柱层析)的Holoferritin样品作为实验组(Holoferritin-enzyme treatment,Holo-ET)。定量测定两者的蛋白质回收率发现,本研究提出的制备工艺可以将Holoferritin的回收率由(69.8±2.03)%提升至(88.2±2.54)%,同时将纯化周期由72 h压缩至48 h,显著提升Holoferritin的制备效率。后续,本研究将通过对比分析两者的结构特征,阐明该制备工艺对Holoferritin结构的影响。
2.2 Holoferritin的结构分析
2.2.1 紫外-可见光谱分析
为探究此制备工艺对Holoferritin蛋白结构的影响,本研究通过紫外-可见吸收光谱对样品进行表征。如图3所示,由于铁芯纳米颗粒的成功合成,样品在200~400 nm范围内展现出宽谱带强吸收[17],且最大吸收波长相较于不含铁核的铁蛋白发生显著红移[14]。值得注意的是,实验组与对照组的光谱图线基本一致,两者在280 nm处(色氨酸/酪氨酸特征吸收带)及铁核相关吸收区域均未出现显著位移或强度差异[18]。上述结果说明,核酸酶的加入未改变样品中芳香族氨基酸的微环境及其共轭电子体系,进一步证实该制备工艺在去除核酸杂质的同时,仍能够保持Holoferritin完整的结构特性。
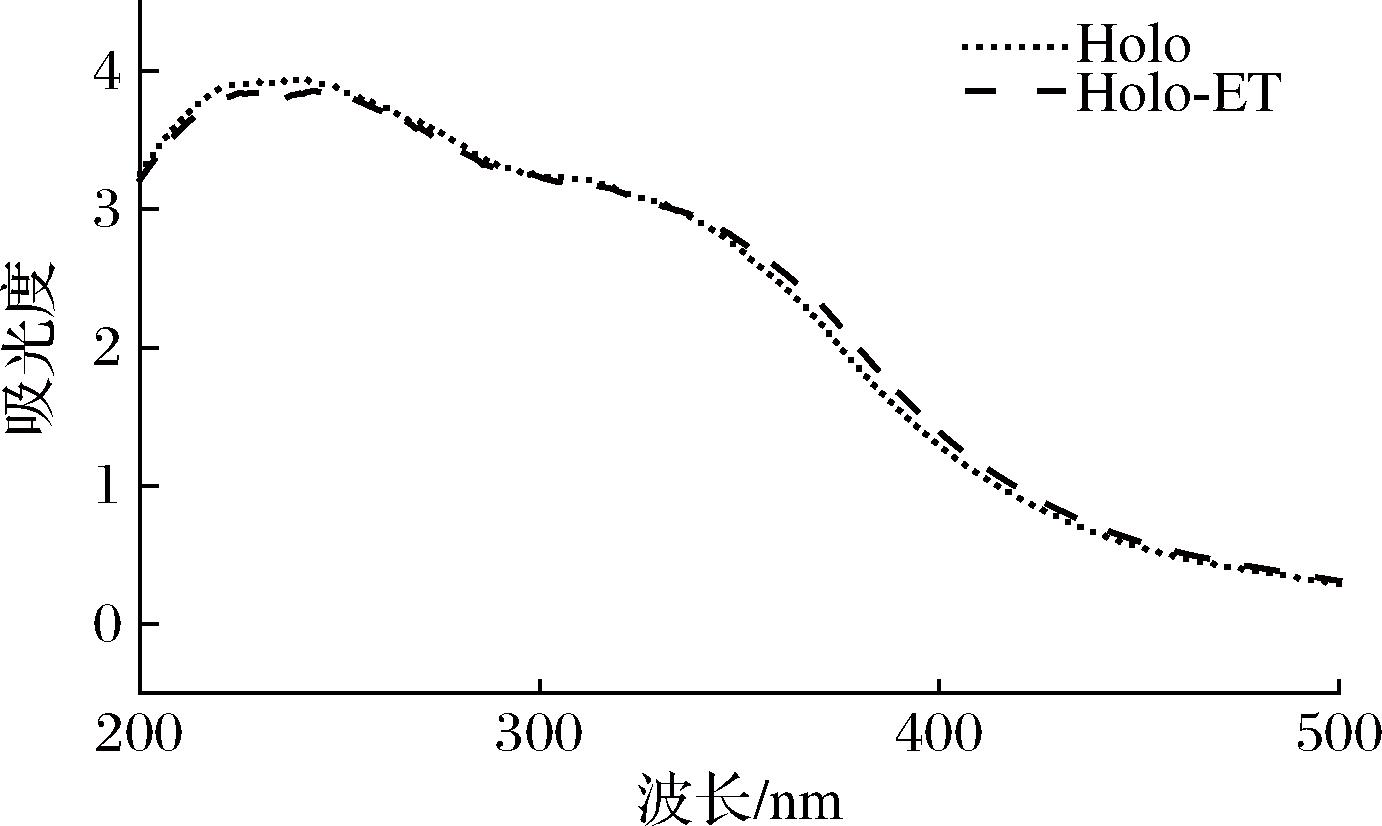
图3 对照组和实验组Holoferritin的紫外-可见光谱分析结果
Fig.3 UV-VIS spectra analysis results of Holoferritin in the control group and experimental group
2.2.2 圆二色谱结果分析
本研究在190~260 nm波长范围内扫描了Holoferritin的圆二色光谱,以分析此制备工艺对其蛋白二级结构的影响,结果如图4所示。与文献报道一致[19-20],Holoferritin的圆二色光谱在208、222 nm处呈现2个典型α-螺旋结构的负吸收峰。通过CDNN软件对光谱数据进行拟合分析,结果表明,Holoferritin的二级结构主要以α-螺旋为主(约88.38%),此外,还包含β-折叠(约3.01%)、β-转角(约5.21%)和无规则卷曲(约3.51%)结构。对比发现,实验组样品圆二光谱的关键吸收峰位(208、222 nm)及峰强度均未发生明显偏移。上述结果表明,Holoferritin具有高度稳定的二级结构,本研究使用的制备工艺几乎不会引起Holoferritin蛋白二级结构的改变。
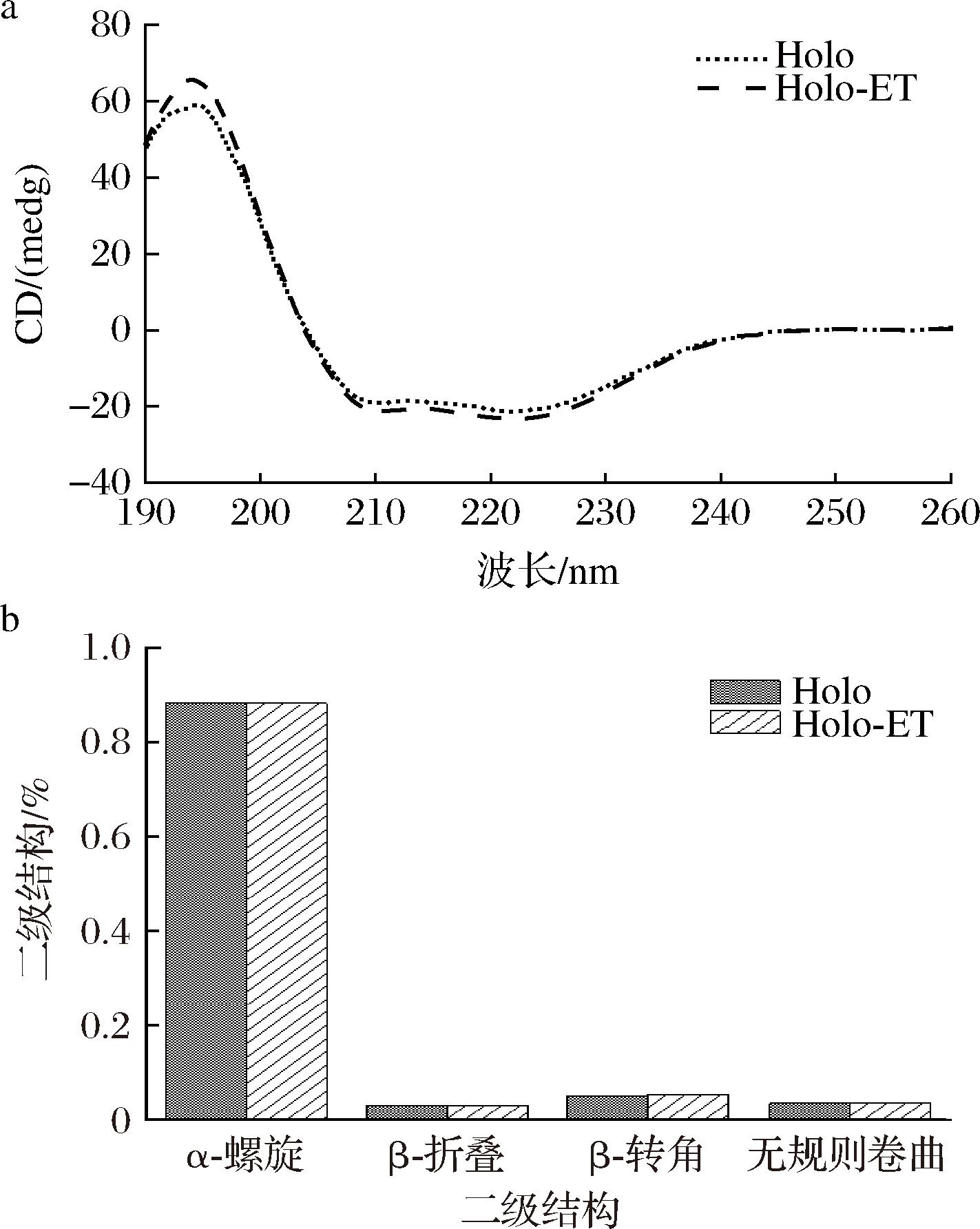
a-对照组和实验组Holoferritin的CD光谱;b-对照组和实验组Holoferritin的二级结构含量
图4 对照组和实验组Holoferritin的圆二色光谱结果
Fig.4 CD spectra of Holoferritin in the control group and experimental group
2.2.3 傅里叶变换红外光谱分析
为阐明此制备工艺对蛋白结构的影响机制,本研究采用傅里叶变换红外光谱对其结构进行表征。如图5所示,对照组Holoferritin在1 638、1 550 cm-1处分别呈现属于酰胺Ⅰ带(1 600~1 700 cm-1)和酰胺Ⅱ带(1 500~1 600 cm-1)的特征吸收峰[21]及C![]() O伸缩振动、N—H面内弯曲振动和C—N伸缩振动[22-23]。值得注意的是,实验组样品在1 642、1 546 cm-1处表现出与对照组基本一致的特征峰。上述结果表明,两者均具备铁蛋白结构的振动特征,此制备工艺未影响Holoferritin独特的蛋白质结构,且其稳定的结构可能由α-螺旋主链中C
O伸缩振动、N—H面内弯曲振动和C—N伸缩振动[22-23]。值得注意的是,实验组样品在1 642、1 546 cm-1处表现出与对照组基本一致的特征峰。上述结果表明,两者均具备铁蛋白结构的振动特征,此制备工艺未影响Holoferritin独特的蛋白质结构,且其稳定的结构可能由α-螺旋主链中C![]() O与N—H基团间形成的氢键网络维持[24],该相互作用可有效保证蛋白质结构的完整性。
O与N—H基团间形成的氢键网络维持[24],该相互作用可有效保证蛋白质结构的完整性。
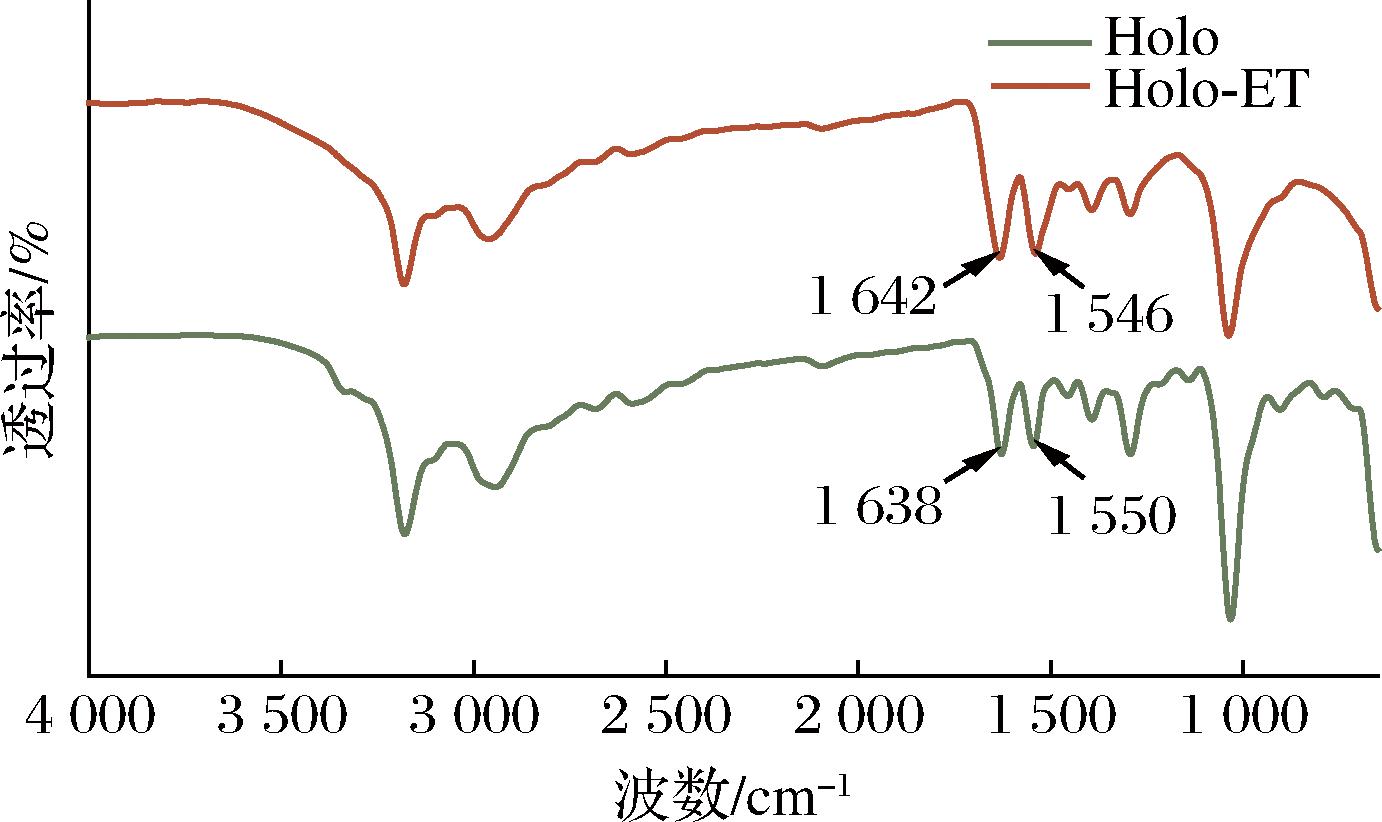
图5 对照组和实验组Holoferritin的傅里叶变换红外光谱结果
Fig.5 FTIR spectra results of Holoferritin in the control group and experimental group
2.2.4 粒径及ζ-电位结果分析
为探究此制备工艺对Holoferritin蛋白颗粒理化性质的影响,本研究采用马尔文粒度仪对其流体动力学直径及表面电荷特性进行表征。结果如图6-a和图6-b所示,对照组与实验组的粒径尺寸分布结果均呈现单峰分布特征,其平均流体动力学直径约12 nm,表明蛋白颗粒在溶液中保持优异的单分散性,该数值与文献报道结果一致[8]。进一步测定颗粒的ζ-电位值发现(图3-c),对照组与实验组的表面电荷值分别为(-13.3±0.36)、(-13.3±0.42) mV,两者无显著差异(P >0.05,n=3),表明此制备工艺不会改变Holoferritin表面电荷的分布[6]。值得注意的是,当Holoferritin的表面电荷值为5 mV时,蛋白会产生聚集,而本研究对照组与实验组的表面电荷均远低于5 mV,表明铁蛋白颗粒具有极大的单分散性[14]。上述结果表明,在既定的核酸酶处理浓度下,此制备工艺既不改变Holoferritin纳米颗粒的组装状态,也不影响其表面电荷分布特性,进一步验证了此工艺能够有效维持Holoferritin蛋白结构的完整性。
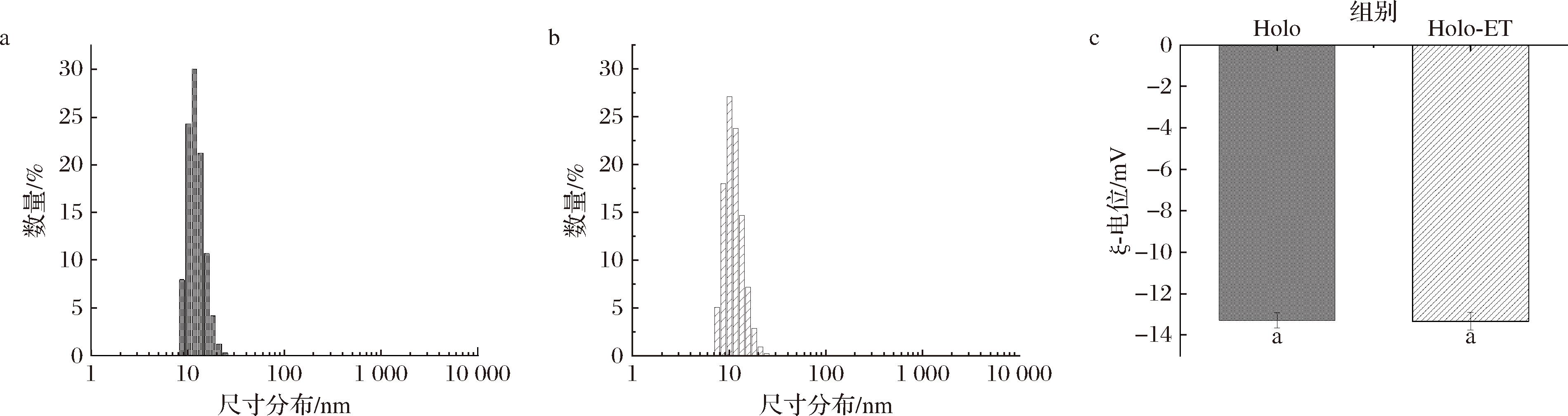
a-对照组Holoferritin的粒径尺寸分布;b-实验组Holoferritin的粒径尺寸分布;c-对照组和实验组Holoferritin的ζ-电位结果
图6 对照组和实验组Holoferritin的粒径尺寸分布和ζ-电位结果
Fig.6 The size distribution and the Zeta potential results of Holoferritin in the control group and the experimental group
2.2.5 透射电子显微镜结果分析
为了探究此制备工艺是否会对Holoferritin的结构完整性产生影响,本研究采用透射电子显微镜对样品形貌进行表征。如图7所示,未经负染处理的实验组与对照组样品中(图7-a、图7-c)均可观察到直径约4 nm的黑色单分散颗粒,该尺寸与Holoferritin内源性铁核(Fe3O4)的典型尺寸高度一致[25],表明铁芯纳米颗粒在蛋白空腔内成功矿化。进一步采用质量浓度为20 g/L的磷钨酸对Holoferritin进行负染色(图7-b、图7-d),两者均呈现出清晰的蛋白纳米笼结构,其直径约12 nm,且黑色铁芯颗粒被包裹于蛋白空腔内部,结果与文献报道一致[6,8]。值得注意的是,实验组样品(图7-c、图7-d)在未染色及负染色条件下均显示出与对照组一致的纳米结构特征,未观察到蛋白纳米笼破裂或铁芯泄露、聚集等异常现象。上述结果表明,此纯化策略对Holoferritin的蛋白微观结构和结构完整性无显著影响。
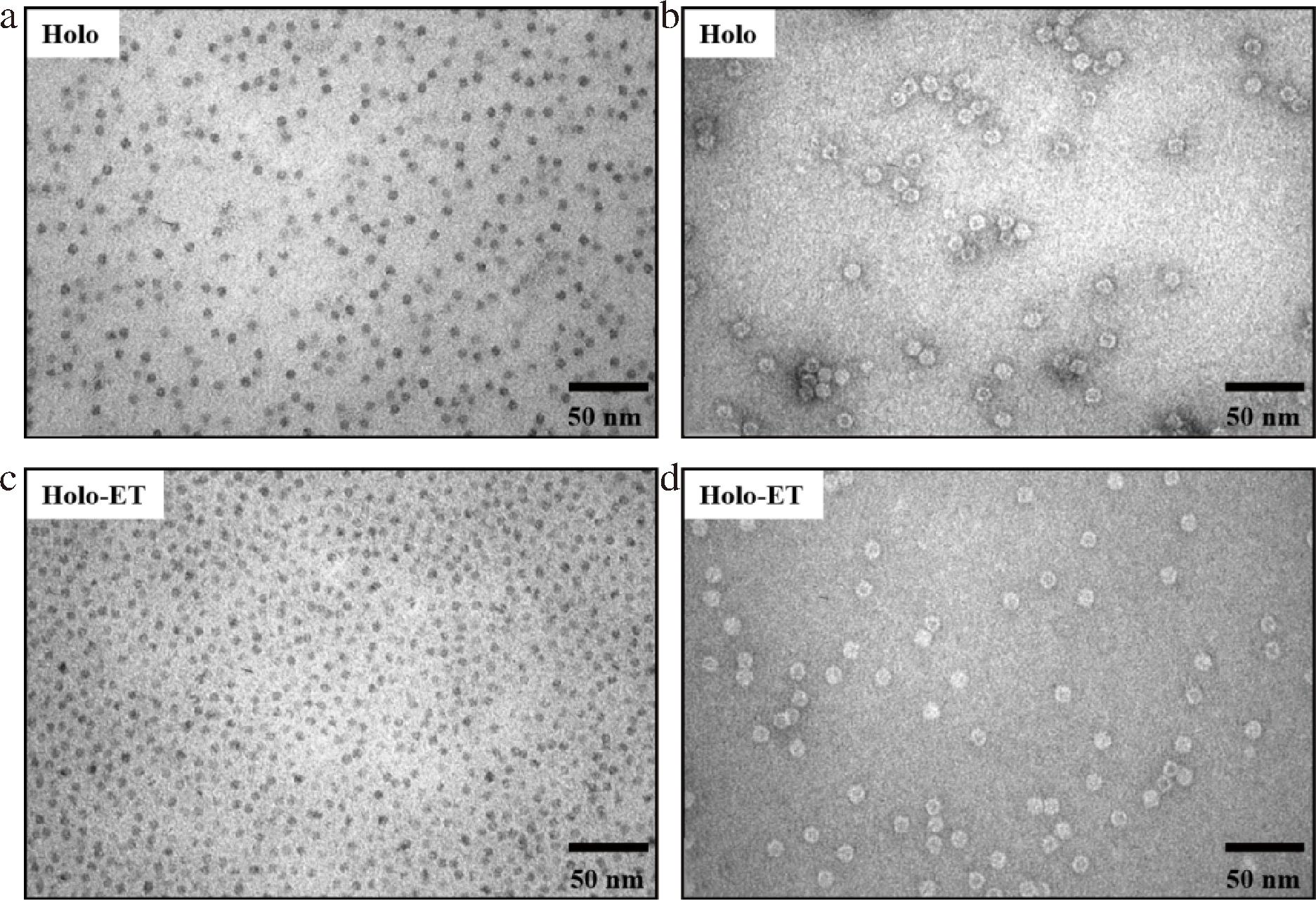
a-未经负染处理的对照组Holoferritin;b-经负染处理的对照组Holoferritin;c-未经负染处理的实验组Holoferritin;d-经负染处理的实验组Holoferritin
图7 对照组和实验组Holoferritin的透射电子显微镜结果
Fig.7 TEM images of Holoferritin in the control group and experimental group
3 结论与讨论
本研究基于生物合成途径提取Holoferritin的基本方案,整合核酸酶处理工艺,构建了一种简单高效的Holoferritin制备工艺。通过研究发现,相较于传统生物合成途径制备工艺,本研究核酸酶处理工艺的优化,实现了宿主残留核酸的有效清除,同时能够将Holoferritin的回收率由(69.8±2.03)%提升至(88.2±2.54)%,将纯化周期由72 h压缩至48 h,简化了层析纯化步骤,显著提升蛋白制备效率。值得注意的是,此策略显著的工艺优化效果,主要依赖于其采用广谱性全能核酸酶替代传统层析纯化步骤。该酶不具备碱基识别特异性,能够降解Holoferritin提取过程中宿主残留的所有形式的DNA及RNA,最终有效降低核酸残留、改善蛋白纯化工艺、提高蛋白产量,且不会对Holoferritin蛋白结构产生破坏。基于此,本研究通过紫外-可见光谱、圆二色谱和傅里叶变换红外光谱等蛋白结构表征发现,此制备工艺不仅能够保持Holoferritin特有的α-螺旋占主体的二级结构,还能够维持其由蛋白质纳米笼包裹铁芯的完整结构。本研究基于生物合成途径的Holoferritin高效制备和纯化工艺,能够为规模化制备Holoferritin提供理论指导。
[1] MONTEMIGLIO L C, TESTI C, CECI P, et al.Cryo-EM structure of the human ferritin-transferrin receptor 1 complex[J].Nature Communications, 2019, 10:1121.
[2] LI H, XIA X Y, TAN X Y, et al.Advancements of nature nanocage protein:Preparation, identification and multiple applications of ferritins[J].Critical Reviews in Food Science and Nutrition, 2022, 62(25):7117-7128.
[3] WU Y, MING T H, HUO C H, et al.Crystallographic characterization of a marine invertebrate ferritin from the sea cucumber Apostichopus japonicus[J].FEBS Open Bio, 2022, 12(3):664-674.
[4] CHEN H, TAN X Y, HAN X E, et al.Ferritin nanocage based delivery vehicles:From single-, co- to compartmentalized- encapsulation of bioactive or nutraceutical compounds[J].Biotechnology Advances, 2022, 61:108037.
[5] LV C Y, ZHAO G H, LÖNNERDAL B.Bioavailability of iron from plant and animal ferritins[J].The Journal of Nutritional Biochemistry, 2015, 26 (5):532-540.
[6] CHEN H, XIE J, HU M J, et al.In vivo biosynthesis of nutritional holoferritin nanoparticles:Preparation, characterization, iron content analysis, and synthetic pathway[J].Food Chemistry, 2023, 414:135692.
[7] CHEN H Z, CHU H C, JIANG Q, et al.Irf6 participates in sevoflurane-induced perioperative neurocognitive disorder via modulating M2, but not M1 polarization of microglia[J].Brain Research Bulletin, 2021, 177:1-11.
[8] CHEN H, DAI H J, ZHU H K, et al.Construction of dual-compartmental micro-droplet via shrimp ferritin nanocages stabilized Pickering emulsions for co-encapsulation of hydrophobic/hydrophilic bioactive compounds[J].Food Hydrocolloids, 2022, 126:107443.
[9] ZHANG Y, DENG Z A, LOU D D, et al.High-efficiency separation of extracellular vesicles from lipoproteins in plasma by agarose gel electrophoresis[J].Analytical Chemistry, 2020, 92 (11):7493-7499.
[10] JIANG B, CHEN X H, SUN G M, et al.A natural drug entry channel in the ferritin nanocage[J].Nano Today, 2020, 35:100948.
[11] MOGLIA I, SANTIAGO M, OLIVERA-NAPPA 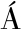 , et al.An optimized low-cost protocol for standardized production of iron-free apoferritin nanocages with high protein recovery and suitable conformation for nanotechnological applications[J].Journal of Inorganic Biochemistry, 2018, 183:184-190.
, et al.An optimized low-cost protocol for standardized production of iron-free apoferritin nanocages with high protein recovery and suitable conformation for nanotechnological applications[J].Journal of Inorganic Biochemistry, 2018, 183:184-190.
[12] 肖宇, 续晓琪, 张涛, 等.鸽蛋卵转铁蛋白的纯化鉴定、理化特性及消化产物抗氧化性研究[J].食品与发酵工业, 2024, 50(23):123-131.XIAO Y, XU X Q, ZHANG T, et al.Purification, identification, physicochemical properties and antioxidant activity of the digestion products of ovotransferrin from pigeon egg[J].Food and Fermentation Industries, 2024, 50(23):123-131.
[13] 王舸楠, 马文瑞, 全莉, 等.酿酒葡萄DNA的提取方法[J].食品与发酵工业, 2018, 44(12):118-122.WANG G N, MA W R, QUAN L, et al.Optimization of genomic DNA extraction from grapes[J].Food and Fermentation Industries, 2018, 44(12):118-122.
[14] ZHOU K, ZANG J C, CHEN H, et al.On-axis alignment of protein nanocage assemblies from 2D to 3D through the aromatic stacking interactions of amino acid residues[J].ACS Nano, 2018,12(11):11323-11332.
[15] CHEN H, HAN X E, FU Y, et al.Compartmentalized chitooligosaccharide/ferritin particles for controlled co-encapsulation of curcumin and rutin[J].Carbohydrate Polymers, 2022, 290:119484.
[16] GAO J L, TAN X Y, WANG H X, et al.Chitooligosaccharide facilitated the co-stabilization of ferritin-based dual-compartmental Pickering emulsions:The effect and contribution of chitooligosaccharide molecular weight[J].Food Hydrocolloids, 2024, 152:109895.
[17] CAZACU N, CHILOM C G, IFTIMIE S, et al.Biogenic ferrihydrite nanoparticles produced by Klebsiella oxytoca:Characterization, physicochemical properties and bovine serum albumin interactions[J].Nanomaterials, 2022, 12(2):249.
[18] 刘文营. 鹰嘴豆铁蛋白的分离纯化表征及性质分析[D].石河子:石河子大学, 2011.LIU W Y.Isolation, purification, characterization and property analysis of chickpea ferritin[D].Shihezi:Shihezi University, 2011.
[19] ZHANG C X, TAN X Y, LV C Y, et al.Shrimp ferritin greatly improves the physical and chemical stability of astaxanthin[J].Journal of Food Science, 2021, 86(12):5295-5306.
[20] WANG Q Q, ZHOU K, NING Y, et al.Effect of the structure of gallic acid and its derivatives on their interaction with plant ferritin[J].Food Chemistry, 2016, 213:260-267.
[21] CHEN H, HU M J, TAN X Y, et al.Facile approach to fabricate stable multi-chamber colloid particles for compartmentalized encapsulation and reaction control of incompatible molecules[J].Chemical Engineering Journal, 2023, 475:146029.
[22] 杨凡, 朱玲, 吴港城, 等.紫檀芪纳米复合物的构建及稳定性研究[J].食品与发酵工业, 2021, 47(12):128-132.YANG F, ZHU L, WU G C, et al.The fabrication and stability of the pterostilbene nano complex[J].Food and Fermentation Industries, 2021, 47(12):128-132.
[23] LI X Q, LI M T, ZHANG T T, et al.Enzymatic and nonenzymatic conjugates of lactoferrin and(-)-epigallocatechin gallate:Formation,structure, functionality, and allergenicity[J].Journal of Agricultural and Food Chemistry, 2021, 69(22):6291-6302.
[24] 马贵红,赖龙昕,李蝶,等.饱和硫酸铵纯化重组日本囊对虾铁蛋白[J].食品与发酵工业,2022,48(16):138-143.MA G H, LAI L X, LI D, et al.Purification of recombinant Marsupenaeus japonicus ferritin by saturated ammonium sulfate[J].Food and Fermentation Industries, 2022, 48(16):138-143.
[25] LI M X, LIU G H, WANG K X, et al.Metal ion-responsive nanocarrier derived from phosphonated Calix [4] arenes for delivering dauricine specifically to sites of brain injury in a mouse model of intracerebral hemorrhage[J].Journal of Nanobiotechnology, 2020, 18(1):61.