酱油是一种传统的发酵豆制品,起源于亚洲国家,以其独特的鲜味和香气享誉全球。在发酵过程中,大豆中的蛋白质被分解成各种氨基酸、多肽和挥发性有机化合物[1]。随着酱油在世界范围内越来越受欢迎,确保其安全并提升其风味保持高质量已成为关键问题。
酱油中的一个主要安全问题是生物胺(包括酪胺、组胺等)的积累,其是通过氨基酸脱羧形成的低分子量氮化合物[2]。过量摄入组胺和酪胺会引发过敏反应,导致头痛、胃肠道不适等症状,甚至严重中毒。为应对健康问题,一些国家已开始对食品中的生物胺含量进行监管。根据LI等[3]的研究,商业酱油的生物胺含量可能为45.6~611.3 mg/L,大大超过安全阈值。因此,需要有效方法来降低酱油中的生物胺含量。目前已有部分研究证明接种合适的发酵剂能够降低酱油中的生物胺,如GUO等[4]证明,接种葡萄球菌和酵母发酵6个月后,总生物胺含量减少了31.51%。但目前广泛商业应用的发酵剂仍然很少。此外,由于酱油的微生物环境复杂,需要进一步研究发酵剂在这种条件下的表现及其对微生物群落和整体质量的影响。
酱油作为一种调味品,风味也是酱油质量的关键因素,因此有必要评估新型发酵剂对酱油产生的影响。谷氨酰胺酶(glutaminase,GLS)是一种能够催化谷氨酰胺水解生成谷氨酸的关键酶,广泛存在于微生物及动植物组织中,在酱油酿造中,该酶通过分解大豆蛋白中的谷氨酰胺,显著提升游离谷氨酸含量,从而增强酱油的鲜味特征[5]。目前有部分关于菌株发酵剂对于酱油风味影响的研究,如嗜盐四联球菌(Tetragenococcus halophilus)产生的有机酸会使发酵环境酸化,促进芳香族化合物的形成[6]。但是目前关于酶与菌株耦合发酵对于酱油风味影响的研究十分有限,酱油中微生物生态系统复杂,酶菌耦合发酵剂在酱油中的应用需要进一步研究,以充分了解新型发酵剂对酱油风味的影响及其机制。
本研究旨在筛选合适的酶菌耦合发酵剂,以降低发酵酱油的生物胺含量,增强酱油的风味,从而提高酱油的整体品质。将3种酱油中常见菌株[T.halophilus、植物乳植杆菌(Lactiplantibacillus plantarum)、鲁氏接合酵母(Zygosaccharomyces rouxii)]分别与谷氨酰胺酶进行单菌或混菌耦合发酵,研究不同发酵剂对于酱油理化指标、游离氨基酸含量、生物胺含量及风味指标的影响。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株与原料
T.halophilus C17、Z.rouxii L1从酱油酱醪中筛选,L.plantarum H11从发酵食品中筛选,并通过耐盐驯化[7]。上述菌株均保藏于大连工业大学国家海洋食品工程技术研究中心。
谷氨酰胺酶,安琪酵母股份有限公司;黄豆,依兰县三姓生态农业有限公司;小麦,漯河市源锦坊商贸有限公司;食用盐,中盐集团;酱油曲精(米曲霉),沂水锦润生物科技有限公司。
1.1.2 主要试剂
MRS肉汤/琼脂培养基、酵母提取物蛋白胨葡萄糖(yeast extract peptone dextrose, YPD)肉汤/琼脂培养基、胰酪胨大豆肉汤(tryptic soy broth,TSB)培养基、胰酪胨大豆琼脂(tryptic soy agar,TSA)培养基,青岛海博生物技术有限公司;氯化钠、氢氧化钠、碳酸氢钠、甲醛,天津市大茂化学试剂厂;3,5-二硝基水杨酸(3,5-dinitrosalicylic acid reagent, DNS)试剂,北京索莱宝科技有限公司;氨水,上海阿拉丁生化科技股份有限公司;甲醇、乙腈,美国Spectaum公司;丹磺酰氯、生物胺标准品(色胺、β-苯乙胺、腐胺、尸胺、组胺、酪胺、亚精胺、精胺),上海麦克林生化科技股份有限公司。
1.2 仪器与设备
AB2004-N电子分析天平、FE28-Standard pH计,梅特勒-托利多仪器(上海)有限公司;BJ-2CD超净工作台、BSC-1300IIA2生物安全柜,日本AIRTECH公司;PEN33电子鼻,德国AIRSENSE公司;TS-5000Z电子舌,北京盈盛恒泰科技有限责任公司;Micro 17R冷冻高速离心机,美国Thermo Scientific公司;LRH-150生化培养箱,上海一恒科学仪器有限公司;LC-16高效液相色谱仪,日本Shimaduz公司;LA8080氨基酸自动分析仪,日立高新科学公司;FlavourSpec气相色谱离子迁移谱联用仪,海能未来技术集团股份有限公司。
1.3 实验方法
1.3.1 酱油大曲与酱醪的制备
参考GUO等[4]的发酵工艺,并做出修改,将灭菌后的大豆与小麦按照质量比7∶3混合,并向其中加入总质量0.2%的酱油曲精(米曲霉),酱油在制曲的过程中将温度保持在30 ℃,湿度为50%,分别在第16、24、36 h进行翻曲,每次翻曲时将上层纱布用清水浸湿再重新铺盖保持曲的湿度,经过48 h制成大曲。将制成的曲与230 g/L的盐水混合加入到玻璃容器中,并放置在恒温30 ℃的室内进行180 d发酵。在第1天将总质量0.01%的谷氨酰胺酶接种到酱醪中,分别在第15、30、60、90、120、150、180 d取样观测其各项指标的变化。本研究每个实验组的体积均为10 L,每组均设置3组平行。
1.3.2 接种发酵剂的制备
T.halophilus采用加100 g/L氯化钠的TSB/TSA培养基,L.plantarum采用MRS肉汤/琼脂培养基,Z.rouxii 采用YPD肉汤/琼脂培养基进行培养传代,T.halophilus和L.plantarum在第15天,Z.rouxii在第30天接种于发酵罐中,最终使发酵罐中各菌株浓度均为108 CFU/g。
1.3.3 理化指标的测定
pH值用pH计测定,根据GB 12456—2021《食品安全国家标准 食品中总酸的测定(含第1号修改单)》中酸度计法测定总酸含量;氨基酸态氮含量根据GB 5009.234—2016《食品安全国家标准 食品中铵盐的测定》中甲醛滴定法测定;挥发性盐基氮含量采用GB 5009.228—2016《食品安全国家标准 食品中挥发性盐基氮的测定》中微量扩散法测定;还原糖含量采用[8]。
1.3.4 游离氨基酸含量检测
参考PEI等[9]的制样和测定方法,使用自动氨基酸分析仪测定游离氨基酸含量。
1.3.5 生物胺含量检测
采用丹磺酰氯衍生化,然后进行高效液相色谱分析,具体方法如YANG等[10]所述。
1.3.6 电子鼻电子舌测定
电子舌测定按照HE等[11]方法评估发酵完成时酱油的感官质量。电子鼻将2 mL酱油样品加入20 mL顶空瓶中,然后在60 ℃平衡20 min。随后,将电子鼻探头插入顶空瓶进行检测[12]。
1.3.7 挥发性化合物测定
采用离子迁移色谱对酱油中挥发性化合物进行快速检测,将3 mL酱油转移到20 mL顶空进样瓶中,然后在进样前以500 r/min和60 ℃孵育10 min。分析时间30 min,采用MXT-WAX柱,柱温60 ℃,N2作为载气/漂移气体,离子迁移谱温度45 ℃,进样针温度85 ℃[13]。
1.4 数据统计分析
利用Excel 2019、在线作图网站Chiplot(www.chiplot.online)及Origin 2021软件进行数据分析及可视化;采用t检验评估相关热图的显著性,而交互式Mantel相关性热图使用Mantel统计和排列检验来评估相关性。利用SPSS 27软件进行方差分析和显著性分析(P<0.05)。
2 结果与分析
2.1 理化指标测定结果
2.1.1 pH值、总酸和挥发性盐基氮含量的变化
在酱油的质量控制与安全性评估中,pH值、总酸和挥发性盐基氮含量是3个关键理化指标,其检测具有重要的科学意义。
pH值是表征酱油酸碱度的重要参数,其动态变化直接影响决定发酵过程的稳定性和风味物质形成[14]。如图1-a所示,无论是否接种菌株,各实验组间pH值差异均较小。酱醪初始pH值约为5.80,呈先下降后平稳趋势,在发酵终点pH值稳定在5.22~5.34,该结果与市售酱油pH值范围(4.50~5.50)一致[3],表明本研究发酵体系的pH变化符合酱油工业化生产的典型特征。
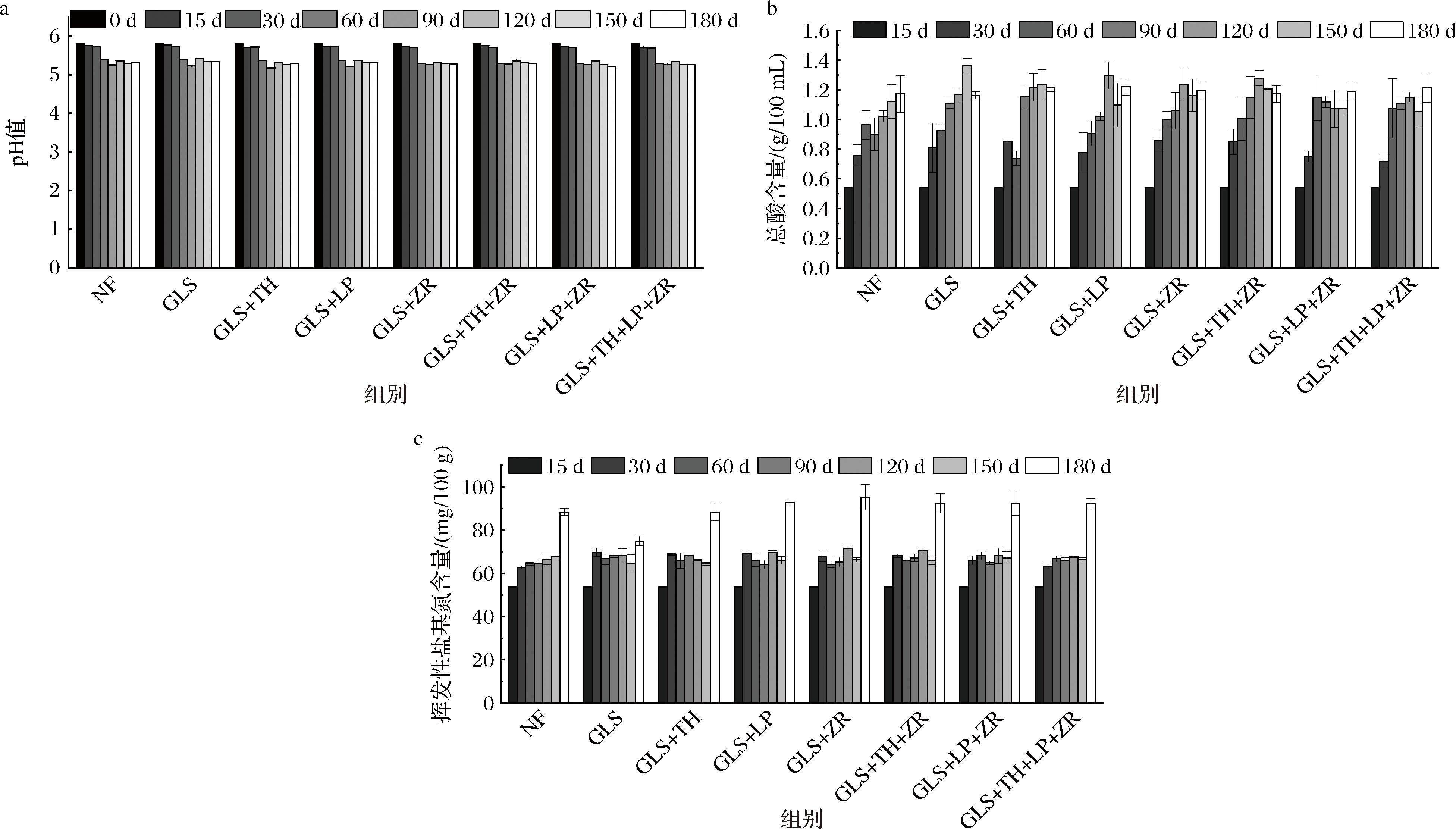
a-pH值;b-总酸含量;c-挥发性盐基氮含量
图1 酱油发酵过程中pH值、总酸含量、挥发性盐基氮含量变化
Fig.1 The changes of pH value, total acid content, and total volatile basic nitrogen content during the fermentation process of eight groups of soy sauce
注:NF-自然发酵组;GLS-谷氨酰胺酶;TH-T.halophilus C17,LP-L.plantarum H11;ZR-Z.rouxii L1(下同)。
总酸含量是评价酱油发酵过程中是否发生酸败的核心指标之一。如图1-b所示,本批发酵酱油总酸含量在前期快速上升,中后期缓慢增长,这可能是由于乳酸菌等细菌在发酵前期产生了酸性物质,而发酵中后期营养物质被大量消耗,乳酸菌代谢受到制约。发酵终点时,总酸含量为1.16~1.22 g/100 mL,表明酱油未发生杂菌污染导致的异常酸败现象。此外,总酸含量与生物胺前体物质的积累呈负相关[15],本研究中较低的总酸水平可能通过限制前体氨基酸的生成,间接影响生物胺的最终含量。
挥发性盐基氮是评估酱油发酵进程与新鲜度的关键指标,它与腐败菌的代谢和内源性酶的活性有关。因此,生产工艺中需精准监控挥发性盐基氮水平以保障产品质量。本研究中,酱醪发酵终点挥发性盐基氮含量为74.96~96.66 mg/100 g(图1-c)。根据酱醪密度(1.15 g/cm3)换算为体积浓度后,对应挥发性盐基氮值为86.20~111.16 mg/100 mL,经长期发酵后的酱油挥发性盐基氮含量为150~200 mg/100 mL[16],本批酱油的挥发性盐基氮含量较低,这可能是因为发酵剂抑制了腐败菌的生长,使挥发性盐基氮保持在较低的水平。
2.1.2 氨基酸态氮含量和还原糖含量变化
氨基酸态氮是酱油中以氨基酸形式存在的氮元素的总量,直接反映酱油的鲜味和品质。氨基酸态氮含量越高,酱油的鲜味可能越浓郁,口感更醇厚。根据GB 18186—2000《酿造酱油》基于氨基酸态氮含量将酱油分为特级、一级、二级、三级。特级酱油的氨基酸态氮含量≥0.8 g/100 mL;一级酱油≥0.7 g/100 mL。如图2-a所示,随着发酵时间的延长,氨基酸态氮含量持续增加。其中,酶菌耦合组(接种谷氨酰胺酶且复合2种以上菌株)的氨基酸态氮终值符合特级酱油标准;其余5组达到一级标准。这可能是因为酵母释放蛋白酶协同乳酸菌的肽酶,进一步降解大豆多肽为小分子氨基酸[17],同时谷氨酰胺酶催化谷氨酰胺转化为谷氨酸,共同提升氨基酸态氮含量。
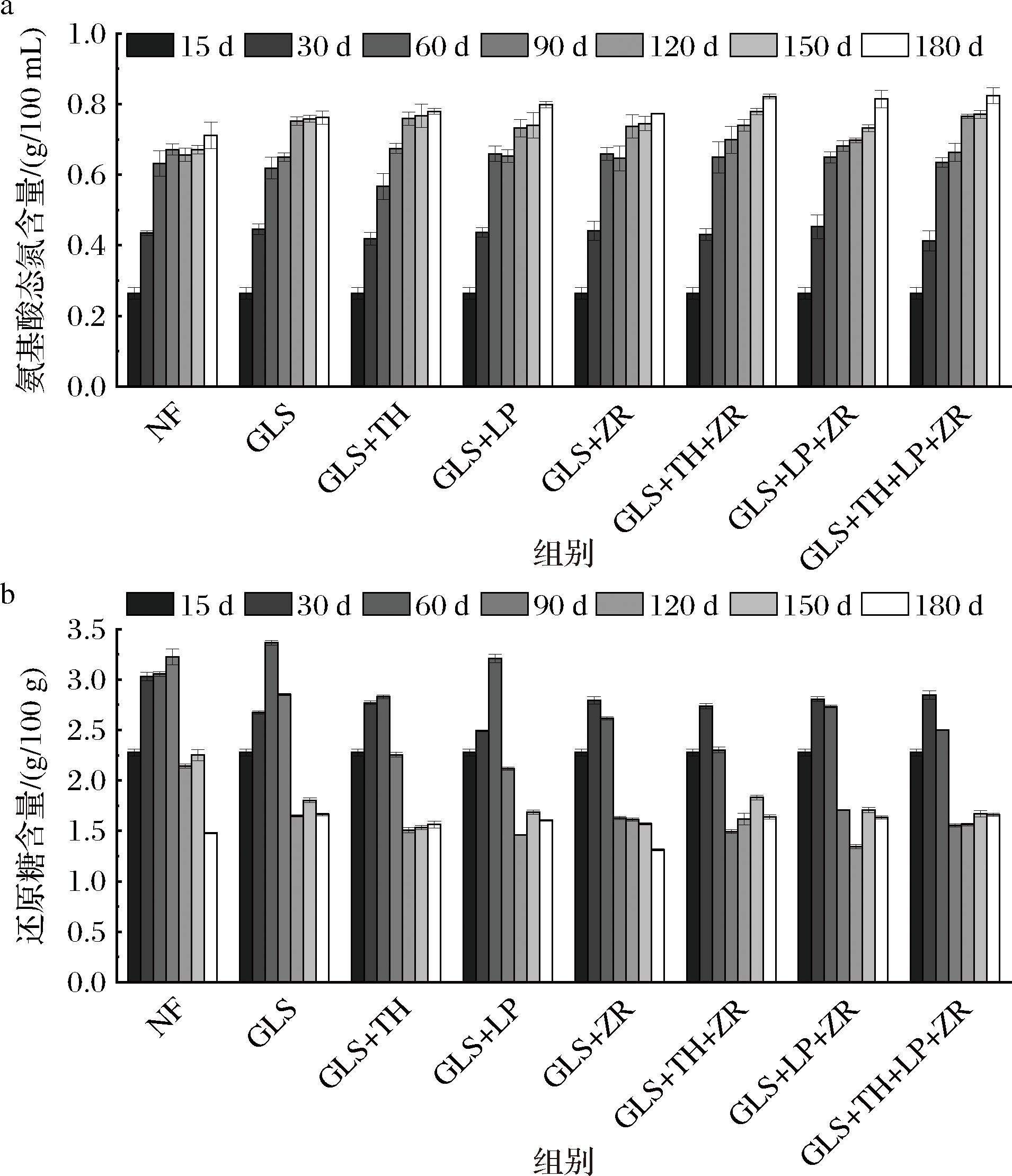
a-氨基酸态氮含量;b-还原糖含量
图2 酱油发酵过程中氨基酸态氮含量,还原糖含量变化
Fig.2 The changes in amino acid nitrogen content and reducing sugar content during the fermentation process of eight groups of soy sauce
还原糖是酱油发酵体系中微生物代谢的初级底物,其直接影响美拉德反应进程、挥发性风味物质合成。合理控制糖分水平对提升酱油风味、色泽及营养价值具有重要实践意义。如图2-b所示,本研究中的酱油还原糖含量呈先升后降的趋势,这可能是因为前期大曲中淀粉酶活力和糖化酶活力都较高,能使原料快速水解生成还原糖,之后由于高盐环境使得酶活性受到抑制,生成还原糖速度降低[18]。
2.2 酶菌耦合发酵对酱油游离氨基酸含量的影响
游离氨基酸含量是酱油品质的核心评价指标,其数值直接影响酱油的鲜味强度、营养价值及工艺稳定性。8组酱油经过180 d发酵后游离氨基酸含量如图3 所示,添加发酵剂的组别游离氨基酸含量均显著高于自然发酵组,这说明谷氨酰胺酶对于发酵酱油的游离氨基酸提升有着很好的效果。
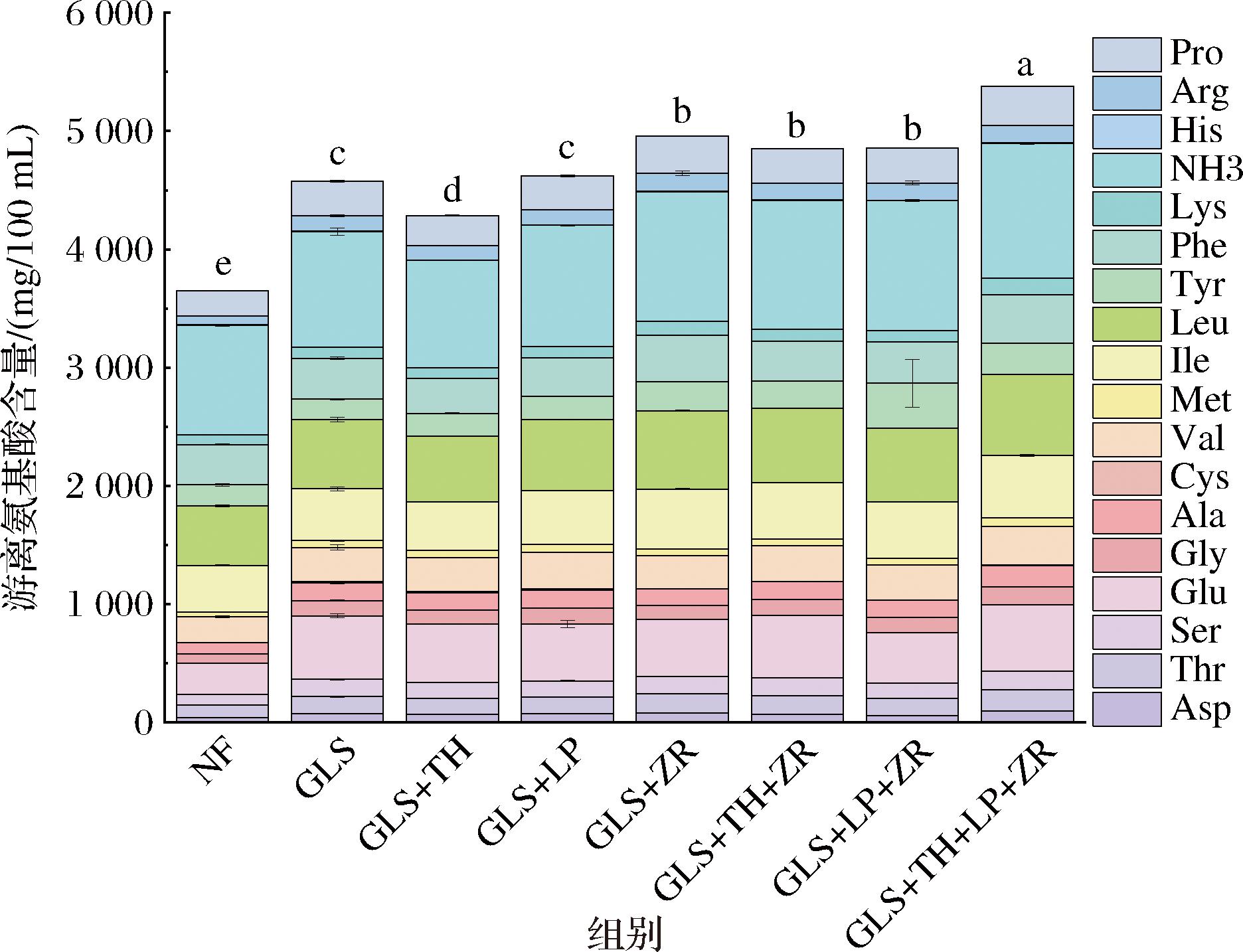
图3 酱油发酵终点游离氨基酸含量对比
Fig.3 Comparison of free amino acid contents at the end of fermentation in eight groups of soy sauce
注:不同小写字母表示差异显著(P<0.05)(下同)。
在单菌与谷氨酰胺酶耦合的组别中,接种Z.rouxii L1的组别游离氨基酸含量显著高于L.plantarum H11组和T.halophilus C17组。接种Z.rouxii L1发酵组别中游离氨基酸提升很可能是因为Z.rouxii具有谷氨酰胺酶、苏氨酸合酶以及二氨基庚二酸脱羧酶等氨基酸合成酶基因[19-20],这些关键酶通过催化底物转化,从而促进游离氨基酸含量的上升。
此外,接种2种菌株的组合游离氨基酸含量与只接种Z.rouxii L1的组合并无显著差异,而接种3种菌株与谷氨酰胺酶组的游离氨基酸含量显著高于其他各组,其游离氨基酸总量比自然发酵组提高了47.46%,这可能是因为乳酸菌会自溶产生丙酮酸等物质,这些成分会被酵母菌利用加快酵母菌的繁殖[21],而酵母菌的酶解作用会使蛋白质剧烈降解,促使大量游离氨基酸产生[22]。
酱油中主要的呈味氨基酸是谷氨酸、天冬氨酸、丙氨酸与甘氨酸,这4种氨基酸在只添加谷氨酰胺酶的组别较自然发酵组分别提升了103.95%、84.85%、60.07%、62.01%,并且添加谷氨酰胺酶、T.halophilus C17、L.plantarum H1和Z.rouxii L1的组别提升了113.07%、148.96%、87.35%、88.82%,这表明谷氨酰胺酶可显著提升风味氨基酸的含量,而菌株发酵剂与谷氨酰胺酶的耦合进一步高效促进了风味氨基酸的富集。
2.3 酶菌耦合发酵对酱油中生物胺的抑制效果研究
生物胺是酱油生产过程中潜在的安全隐患,这类物质由氨基酸脱羧作用形成,属于含游离氨基的低分子量含氮化合物。如图4所示,各组的总生物胺含量均在前期呈逐渐上升的趋势,在中后期呈逐渐下降的趋势,在整个发酵周期,苯乙胺、腐胺和酪胺占主导地位,其浓度动态变化与总生物胺浓度趋势高度一致。
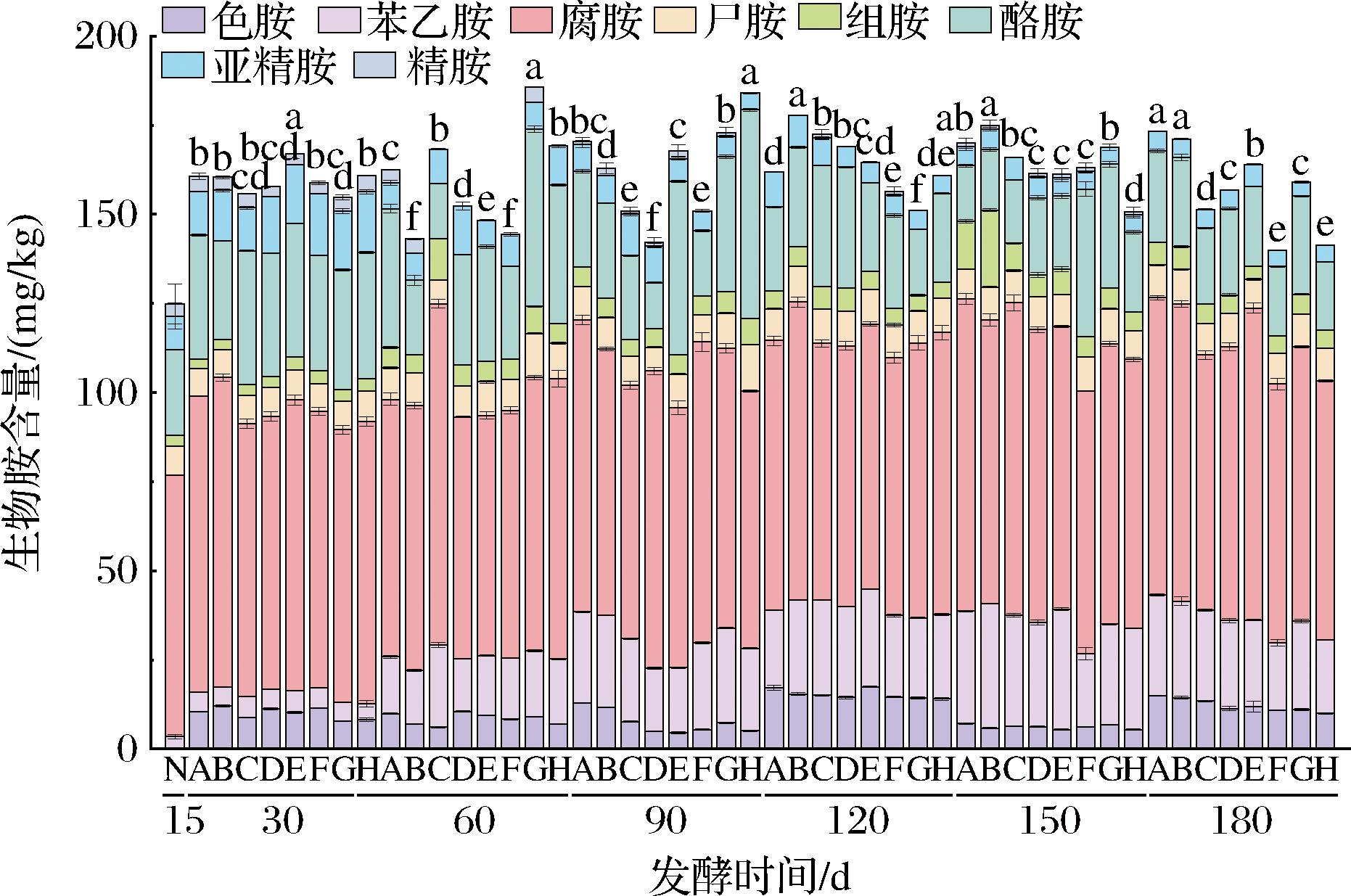
图4 八组酱油发酵过程中生物胺含量变化
Fig.4 The changes of biogenic amine content during the fermentation process of eight groups of soy sauce
注:N-15 d非接种对照组;A-自然发酵组;B-GLS组;C-GLS+TH组; D-GLS+LP组;E-GLS+ZR组;F-GLS+TH+ZR组; G-GLS+LP+ZR;H-GLS+TH+LP+ZR组(下同)。
在发酵终点时,各组生物胺含量为139.99~173.30 mg/kg,所有组别的生物胺含量均低于200 mg/kg,这表明本实验酱油的发酵条件良好,并未引发腐败菌异常生长。总体对比各组之间生物胺含量,添加菌株发酵剂的组别总生物胺含量均显著低于自然发酵组,表现较为突出的组别是添加T.halophilus C17的3组,分别比自然发酵组低21.87、33.31、31.87 mg/kg,对比单菌发酵组的生物胺含量可发现,接种T.halophilus C17的组别生物胺含量显著低于其余2组,表明T.halophilus C17在发酵酱油中具有良好的生物胺降解能力。这一效果可能与其能够产生成胺氧化酶有关,从而促进生物胺的降解[23]。
在混菌发酵组中,生物胺去除效果最显著的是接种谷氨酰胺酶、T.halophilus C17和Z.rouxii L1的组别。另1个组别(接种谷氨酰胺酶、T.halophilus C17、L.plantarum H11和Z.rouxii L1)与前者在生物胺含量上无显著差异。而接种谷氨酰胺酶、L.plantarum H11和Z.rouxii L1的组别生物胺含量显著高于另外2组。这一结果可能归因于T.halophilus C17本身具有一定降低生物胺的能力,且乳酸菌可促进包括Z.rouxii在内的多种酵母的生长[6],通过Uniprot等生物信息学数据库分析发现,Z.rouxii含有多铜氧化酶和单胺氧化酶等与胺降解相关的酶基因,这些酶可通过催化生物胺的氧化脱氨反应来降解生物胺。因此,T.halophilus C17与Z.rouxii可能通过协同作用抑制酱油中生物胺的积累。
对比各组在发酵终点的单种生物胺含量可发现,Z.rouxii L1单菌发酵组的腐胺含量高于其他组,但其组胺与尸胺含量均为最低水平。相比之下,T.halophilus C17单菌组的腐胺含量则低于Z.rouxii L1单菌组及自然发酵组。值得注意的是,T.halophilus C17与Z.rouxii L1混合接种组的苯乙胺含量和总胺均为最低,表明两菌株通过协同效应实现代谢互补,从而更有效地抑制生物胺积累。此外,L.plantarum H11的引入使色胺与酪胺含量下降。
2.4 酱油风味品质测定与分析
2.4.1 酶菌耦合发酵对酱油气味及挥发性化合物的影响
如图5-a所示,各组酱油在W5S(氮氧化物)、W2S(醇类/醛类)、W1W(无机硫化物)、W1S(甲基类)和W1C(芳香成分)传感器上响应值较高,这说明本批酱油经过180 d的发酵,酱油可能会产生部分无机硫化物,但与此同时也产生了较多的芳香类化合物的气味。
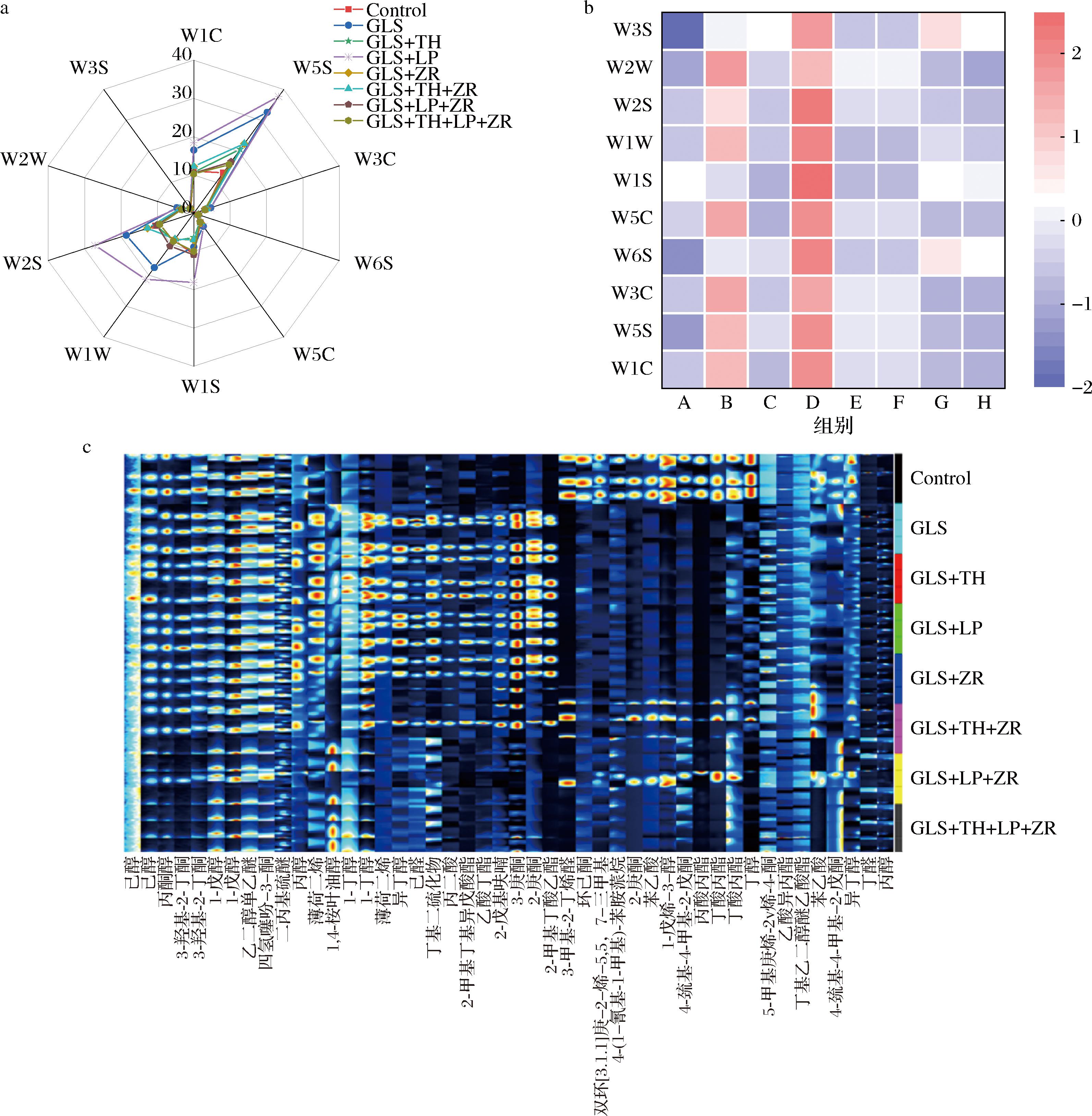
a-电子鼻雷达图;b-电子鼻数据Z值归一化热图;c-各组发酵终点挥发性化合物对比
图5 八组酱油发酵终点气味及挥发性化合物对比
Fig.5 Comparison of odor and volatile compounds at the end of soy sauce fermentation in eight groups
如图5-b所示,谷氨酰胺酶组及谷氨酰胺酶与L.plantarum H11耦合发酵组在W1C(芳香硫化物)、W5S(氮氧化物)、W3C(氨类)、W5C(短链烷烃)、W1W(无机硫化物)、W2S(醇类/醛类)及W2W(有机硫化物)传感器上的响应值均高于其他组别,其中接种谷氨酰胺酶及L.plantarum的组别在10个电极上的响应值均高于其他组,这说明添加谷氨酰胺酶和L.plantarum的组别具有最丰富的气味,这可能是因为乳酸菌具有一定的产谷氨酰胺酶的能力[24],而谷氨酰胺酶通过催化谷氨酰胺水解直接生成谷氨酸(鲜味氨基酸)及醇类、醛类、酮类化合物,从而增强芳香特征[5]。
在挥发性物质指纹图谱中,色阶从蓝色(低浓度)到红色(高浓度)直观反映物质丰度差异[25]。如图5-c所示,添加谷氨酰胺酶的组别新增12种风味物质,包括3种酯类、3种醇类、1种醛类、1种烯类、2种酮类以及丙二酸和2-戊基呋喃。其中,2-戊基呋喃呈现青草香与发酵豆香特征,这种化合物可能是由亚油酸产生的单线态氧化化合物,谷氨酰胺酶会促进谷氨酸的生成,而谷氨酸与还原糖进行美拉德反应从而产生呋喃类化合物[26],同时嗜盐四联球菌和鲁氏接合酵母也可以促进其产生[27]。值得注意的是,酶菌耦合复合发酵剂降低了不良挥发性成分的丰度。例如环己酮与1-戊烯-3-醇,后者具有蘑菇土腥味和青草腥味,是脂质氧化的产物会破坏酱油的新鲜度。由此可见,酶菌耦合发酵提升了酱油的正面风味化合物丰度,降低了负面风味化合物丰度,从而使酱油的风味和品质得到改善。综上,结合电子鼻检测结果与挥发性化合物结果,添加谷氨酰胺酶使化合物种类有所增加从而使酱油的气味更加丰富,尤其是L.plantarum H11与谷氨酰胺酶的添加使酱油的气味最为丰富。
2.4.2 酶菌耦合发酵对酱油滋味的影响及其与氨基酸组成的关联分析
酱油滋味是多种呈味物质共同作用的结果,酱油中呈味物质主要有鲜味氨基酸、总酸、苦味氨基酸、盐分等,在不同程度上影响酱油的鲜味、酸味、苦味、咸味、甜味[28]。如图6-a所示,各组酱油在鲜味,咸味和苦味电极上响应值较高,鲜味氨基酸含量较高使酱油的鲜味较为明显,而其咸味较高可能是因为酱油本身的含盐量较高(在17%左右),且食盐中存在微量的氯化镁、硫酸钠等,这可能使酱油中具有一定的苦味。
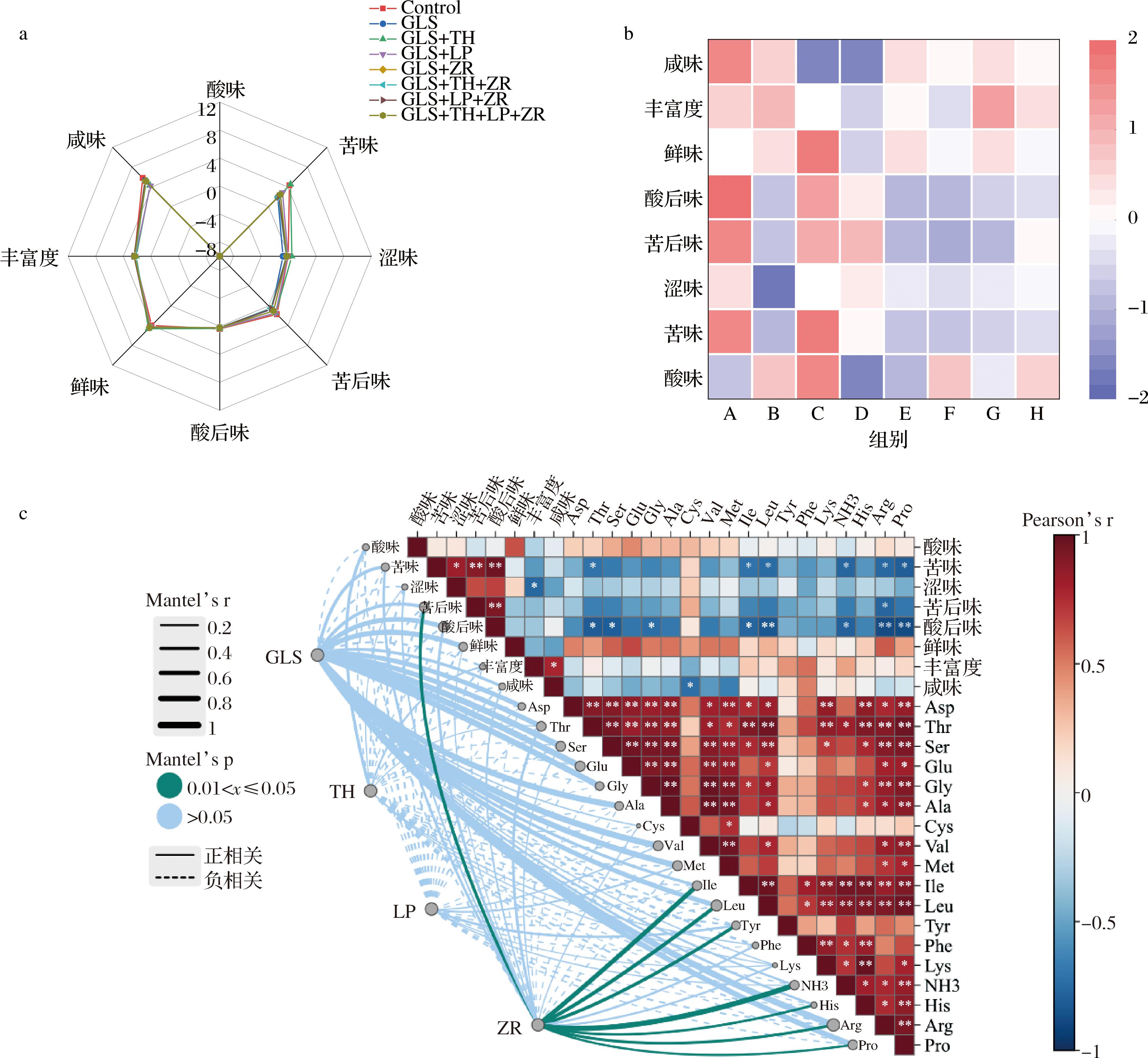
a-电子舌雷达图;b-电子舌数据Z值归一化热图;c-发酵剂与游离氨基酸、电子舌相关性分析
图6 发酵剂对酱油滋味的影响
Fig.6 The influence of starter cultures on the taste of soy sauce
注:*表示P<0.05;**表示P<0.01。
将电子舌各组数据进行Z值归一化处理能够能加清晰地体现各组之间的滋味差别。如图6-b所示,自然发酵组(A组)的苦味、酸后味、苦后味及咸味电极响应值最高,而鲜味电极响应值最低。谷氨酰胺酶组(B组)鲜味、丰富度、甜味电极响应值相对提升,接种谷氨酰胺酶、鲁氏接合酵母与谷氨酰胺酶耦合发酵的组别(G组)综合味觉评价最高,其鲜味、丰富度等正面味觉电极响应值提升,而苦味、涩味等负面味觉电极的响应值降低,这说明这种耦合发酵剂组合可以提升酱油的滋味。这可能是因为酶菌耦合发酵剂提升了酱油中的鲜味氨基酸和氨基酸态氮的含量。
游离氨基酸含量与电子舌均是体现酱油滋味的重要指标,进行相关性分析以便于直观观测接种发酵剂对于酱油滋味的影响。如图6-c所示,除半胱氨酸外所有游离氨基酸均与苦味、涩味、苦后味和涩味残留程度等负面电极响应值呈负相关,而相反的是,除苯丙氨酸外所有游离氨基酸均与鲜味呈正相关,这说明大部分游离氨基酸含量的上升会抑制酱油的负面滋味,同时也会提升正面滋味。
此外,谷氨酰胺酶与除酪氨酸、苯丙氨酸外的游离氨基酸均呈正相关,Z.rouxii L1与12种氨基酸呈正相关,谷氨酰胺酶和Z.rouxii L1提升了酱油中游离氨基酸的含量,这与前文得出的结论相同,其他2种菌株可能通过促进微生物群落变化从而间接改良酱油的滋味。
3 结论
发酵剂是酱油发酵的关键因素,对酱油的安全性和质量有着重要的影响。本研究表明,酶与多菌耦合发酵可使氨基酸态氮含量均达到特级酱油标准,并且3种菌共同与谷氨酰胺酶耦合时游离氨基酸含量显著上升,嗜盐四联球菌C17的接种对于生物胺有着很好的抑制效果,其中接种谷氨酰胺酶、嗜盐四联球菌C17和鲁氏接合酵母L1的组别抑制效果最好,此外酶菌耦合发酵丰富了酱油的香气和滋味,降低了不良的挥发性风味成分。针对复杂微生物群落的酱油发酵体系,未来应进一步开展新型功能发酵剂的筛选,并系统探索接种剂量、菌种组合及时序接种对微生物群落演替以及酱油品质与功能的影响。以上研究对于深入阐明酱油发酵品质的形成机制,提升工业生产中酱油发酵产品的质量具有重要意义。
[1] ZHANG W, XIAO Z C, GU Z M, et al.Fermentation-promoting effect of three salt-tolerant Staphylococcus and their co-fermentation flavor characteristics with Zygosaccharomyces rouxii in soy sauce brewing[J].Food Chemistry, 2024, 432:137245.
[2] ZHANG L L,XIONG S J, DU T H, et al.Exploring the core microorganisms and mechanisms responsible for biogenic amines production during soy sauce fermentation[J].Food Bioscience, 2024, 59:104236.
[3] LI J, HUANG H Z, FENG W, et al.Dynamic changes in biogenic amine content in the traditional brewing process of soy sauce[J].Journal of Food Protection, 2019, 82(9):1539-1545.
[4] GUO J, LUO W, FAN J, et al. Co-inoculation of Staphylococcus piscifermentans and salt-tolerant yeasts inhibited biogenic amines formation during soy sauce fermentation[J].Food Research International, 2020, 137:109436.
[5] 赵旭, 黄小玲, 崔春.谷氨酰胺酶在10 t规模酱油发酵中应用研究[J].中国调味品, 2024, 49(1):164-170.ZHAO X, HUANG X L, CUI C.Research on application of glutaminase in fermentation of 10 t scale of soy sauce[J].China Condiment, 2024, 49(1):164-170.
[6] QI Q, HUANG J, ZHOU R Q, et al.Abating biogenic amines and improving the flavor profile of Cantonese soy sauce via co-culturing Tetragenococcus halophilus and Zygosaccharomyces rouxii[J].Food Microbiology, 2022, 106:104056.
[7] HAN J, SUN Z X, CHEN Y X, et al.Adaptive laboratory evolution and mechanisms of salt tolerance in Lactiplantibacillus plantarum[J].Food Bioscience, 2025, 63:105811.
[8] DESHAVATH N N,MUKHERJEE G, GOUD V V, et al.Pitfalls in the 3, 5-dinitrosalicylic acid (DNS) assay for the reducing sugars:Interference of furfural and 5-hydroxymethylfurfural[J].International Journal of Biological Macromolecules, 2020, 156:180-185.
[9] PEI Q X, GUO B R, YUE Y, et al.Exploring the synergistic effect of Lactiplantibacillus plantarum 1-24-LJ and lipase on improving Quality, Flavor, and safety of Suanzharou[J].Food Research International, 2025, 200:115432.
[10] YANG J, LI Z H, LIN X P, et al.Impact of enzyme-microbe combined fermentation on the safety and quality of soy paste fermented with grass carp by-products[J].Foods, 2025, 14(1):106.
[11] HE Z,CHEN H Y, WANG X Y, et al.Effects of different temperatures on bacterial diversity and volatile flavor compounds during the fermentation of Suancai, a traditional fermented vegetable food from northeastern China[J].LWT, 2020, 118:108773.
[12] CHEN J, LIN B, ZHENG F J, et al.Characterization of the pure black tea wine fermentation process by electronic nose and tongue-based techniques with nutritional characteristics[J].ACS Omega, 2023, 8(13):12538-12547.
[13] LIU Z, LIU L X, HAN Q D, et al.Quality assessment of rose tea with different drying methods based on physicochemical properties, HS-SPME-GC-MS, and GC-IMS[J].Journal of Food Science, 2023, 88(4):1378-1391.
[14] QI W, HOU L H, GUO H L, et al.Effect of salt‐tolerant yeast of Candida versatilis and Zygosaccharomyces rouxii on the production of biogenic amines during soy sauce fermentation[J].Journal of the Science of Food and Agriculture, 2014, 94(8):1537-1542.
[15] LIU B, CAO Z N, QIN L H, et al.Investigation of the synthesis of biogenic amines and quality during high-salt liquid-state soy sauce fermentation[J].LWT, 2020, 133:109835.
[16] 程淑敏, 蓝翔, 徐莹, 等.生物胺降解菌在酱油中的应用[J].食品与发酵工业, 2019, 45(4):129-134.CHENG S M, LAN X, XU Y, et al.Biogenic amine degrading bacteria within soy sauce fermentation[J].Food and Fermentation Industries, 2019.45(4):129-134.
[17] REN Y M, LI L.The influence of protease hydrolysis of lactic acid bacteria on the fermentation induced soybean protein gel:Protein molecule, peptides and amino acids[J].Food Research International, 2022,156:111284.
[18] 张霖靖, 刘功良, 彭勃, 等.不同米曲霉在高盐稀态酱油中的发酵性能比较[J].食品与发酵工业, 2025, 51(3):137-146.ZHANG L J, LIU G L, PENG B, et al.Comparison of fermentation performance of different Aspergillus oryzae in high-salt liquid-state fermented soy sauce[J].Food and Fermentation Industries, 2025, 51(3):137-146.
[19] ZHANG L, ZHANG Z, HUANG J, et al.Co-culture of Tetragenococcus halophilus and Zygosaccharomyces rouxii to improve microbiota and metabolites in secondary fortified fermented soy sauce[J].Food Bioscience, 2024, 61:104850.
[20] KASHYAP P, SABU A, PANDEY A, et al.Extra-cellular L-glutaminase production by Zygosaccharomyces rouxii under solid-state fermentation[J].Process Biochemistry, 2002, 38(3):307-312.
[21] 闫彬. 一组乳酸菌与酵母菌共生关系和风味代谢产物的研究[D].呼和浩特:内蒙古农业大学, 2012.YAN B.Research on interactions and flavour metabolites between a strain of lactic acid bacteria and a strain of yeast[D].Hohhot:Inner Mongolia Agricultural University, 2012.
[22] 龚小会. 酵母产香特性及其对发酵肉制品风味品质的影响研究[D].贵阳:贵州大学, 2022.GONG X H.Research on aroma-producing properties of yeast and its effect on flavor quality of fermented meat products[D].Guiyang:Guizhou University, 2022.
[23] UDOMSIL N, RODTONG S, CHOI Y J, et al.Use of Tetragenococcus halophilus as a starter culture for flavor improvement in fish sauce fermentation[J].Journal of Agricultural and Food Chemistry, 2011, 59(15):8401-8408.
[24] WORAHARN S, LAILERD N, SIVAMARUTHI B S, et al.Screening and kinetics of glutaminase and glutamate decarboxylase producing lactic acid bacteria from fermented Thai foods[J].Food Science and Technology (Campinas), 2014, 34(4):793-799.
[25] WEN S Y, DONG N H, ZHANG Y J, et al.Metabolic profiling of wort fermented with water kefir grains and its effect on wort quality[J].Food Bioscience, 2024, 59:104181.
[26] LIU S Y, SUN H J, MA G, et al.Insights into flavor and key influencing factors of Maillard reaction products:A recent update[J].Frontiers in Nutrition, 2022, 9:973677.
[27] LEE K E, LEE S M, CHOI Y H, et al.Comparative volatile profiles in soy sauce according to inoculated microorganisms[J].Bioscience, Biotechnology, and Biochemistry, 2013, 77(11):2192-2200.
[28] 李露芳, 苏国万, 张佳男, 等.基于电子舌技术的酱油分析识别研究[J].中国食品学报, 2020, 20(9):265-274.LI L F, SU G W, ZHANG J N, et al.Studies on analysis and discrimination of soy sauce based on electronic tongue technology[J].Journal of Chinese Institute of Food Science and Technology, 2020, 20(9):265-274.