甲基萘醌(menaquinones,MK)是一类广泛存在于微生物细胞膜中的电子传递载体,在呼吸链氧化还原反应中发挥关键作用[1]。作为维生素K2的天然存在形式,其结构特征为2-甲基-1,4-萘醌母核连接长度不等的异戊二烯侧链,根据侧链异戊二烯单元数量(n)可分为MK-n系列。其中MK-4和MK-7被广泛应用于食品保健领域,与MK-4相比,MK-7因长效性和低剂量优势更适用于长期保健[2]。维生素K2可通过改善骨钙沉积和调节肠道菌群的作用从而维持骨骼健康发育,可用于预防骨质疏松症[3]。此外,对于心血管钙化、下肢痛性痉挛和部分神经退行性疾病,使用维生素K2也有一定的缓解和治疗效果[4-6]。需特别指出的是,MK-7存在顺反异构现象,仅全反式构型(all-trans)具有生物活性,而顺式构型无生理功能[7]。
枯草芽孢杆菌(Bacillus subtilis)作为维生素K2的优势生产菌株,具备以下特征:1)主要合成MK-7[8];2)不产内毒素;3)遗传操作体系成熟[9]。其MK-7生物合成途径可分为4大代谢模块(图1):甘油利用途径、莽草酸(shikimic acid,SA)途径、甲基赤藓醇磷酸(methylerythritol 4-phosphate,MEP)途径和MK途径[10]。然而,该合成体系存在多重限制因素:1)严格的代谢调控网络;2)前体供应不足;3)分支途径竞争;4)关键酶催化效率低下。针对这些瓶颈,研究者已采用多种代谢工程策略:HUANG等[11]通过改造MenD和MenA,提高酶的表达水平和蛋白稳定性,显著提高了MK-7产量;GAO等[12]构建了PhrC-RapC-SinR群体感应分子开关调控枯草芽孢杆菌MK-7合成,通过细胞密度实现对MK-7合成途径的动态调控。
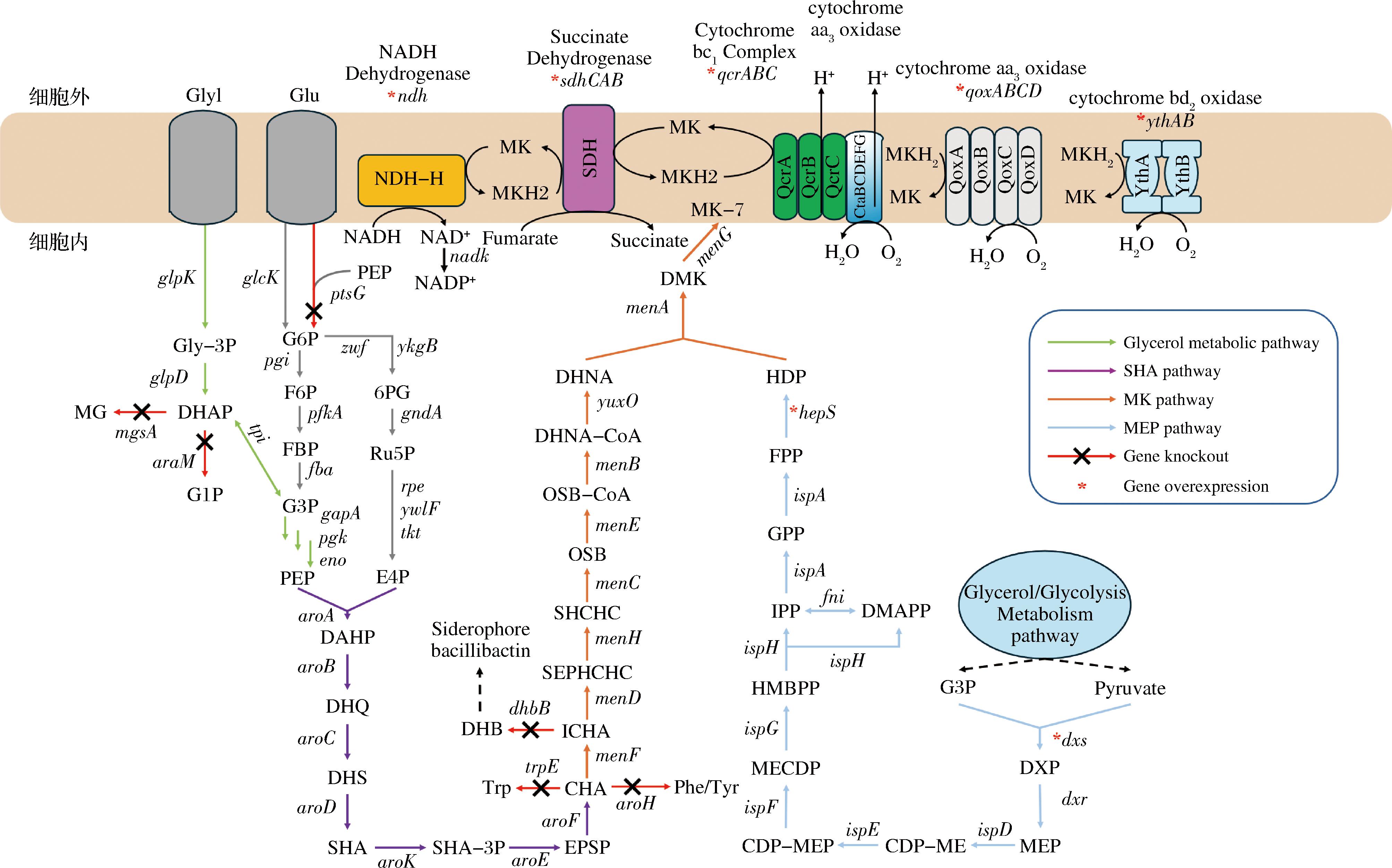
图1 枯草芽孢杆菌中MK-7合成途径
Fig.1 The MK-7 biosynthetic pathway in B.subtilis
注:Gly,甘油;Glu,葡萄糖;Fumarate,延胡索酸;Succinate,琥珀酸;Gly-3P,3-磷酸甘油;DHAP,磷酸二羟丙酮;G1P,1-磷酸甘油醛;MG,甲基乙二醛;G6P,6-磷酸葡萄糖;F6P,6-磷酸果糖;FBP,1,6-二磷酸果糖;G3P,3-磷酸甘油醛;6PG,葡萄糖酸-6-磷酸;Ru5P,5-磷酸核酮糖;PEP,磷酸烯醇丙酮酸;E4P,4-磷酸赤藓糖;DAHP,3-脱氧-阿拉伯-庚酮酸7-磷酸;DHQ,3-脱氢奎尼酸;DHS,3-脱氢莽草酸;SHA,莽草酸;SHA-3P,3-磷酸莽草酸;EPSP,烯醇丙酮酸磷酸莽草酸;CHA,分支酸;ICHA,异分支酸;DHB,2,3-二羟基苯甲酸;SEPHCHC,2-琥珀酰-5-烯醇丙酮酸-6-羟基-3-环己烯-1-羧酸;SHCHC,2-琥珀酰-6-羟基-2,4-环己二烯-1-羧酸;OSB,2-琥珀酰苯甲酸;OSB-CoA,2-琥珀酰苯甲酸-CoA;DHNA-CoA,1,4-二羟基-2-萘甲酸-CoA;DHNA,1,4-二羟基-2-萘甲酸;Pyruvate,丙酮酸;DXP,1-脱氧木糖-5-磷酸;MEP,甲基赤藓糖醇-4-焦磷酸;CDP-ME,4-(胞苷5′-焦磷酸)-2-碳-甲基赤藓糖醇;MECDP,2-磷酸-4-(胞苷5-焦磷酸)-2-碳-甲基赤藓糖醇;HMBPP,1-羟基-2-甲基-2-丁烯基4-焦磷酸;IPP,异戊烯基焦磷酸; DMAPP,二甲基烯丙基焦磷酸;GPP,香叶基焦磷酸;FPP,法尼基焦磷酸;HDP,庚丙烯基焦磷酸;DMK,2-去甲基甲萘醌;MK-7,七烯甲萘醌。
作为公认的食品安全级(generally recognized as safe,GRAS)微生物,枯草芽孢杆菌具有遗传背景清晰、操作工具完备等优势,是理想的代谢工程改造底盘。本研究以枯草芽孢杆菌为底盘菌株,通过敲除分支代谢途径、增强电子传递链、引入异源基因以及过表达关键基因的策略获得重组菌株S13,经3 L发酵罐规模验证,重组菌株的MK-7生产能力显著提升,为工业化生产奠定了重要基础。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株和引物
本研究所用菌株和质粒见表1,所用引物见表2。
表1 本研究所用菌株和质粒
Table 1 Plasmids and strains used in this study

菌株描述来源Escherichia coli DH5α商业感受态细胞南京诺唯赞生物科技股份有限公司B.subtilis 168Wild type实验室保存S01B.subtilis 168 ΔdhbB∷P43-menA本实验构建
续表1

菌株描述来源S02B.subtilis 168 ΔdhbB∷P43-menA ΔtrpE ΔaroH本实验构建S03B.subtilis 168 ΔdhbB∷P43-menA ΔtrpE ΔaroH ΔaraM本实验构建S04B.subtilis 168 ΔdhbB∷P43-menA ΔtrpE ΔaroH ΔmgsA本实验构建S05B.subtilis 168 ΔdhbB∷P43-menA ΔtrpE ΔaroH ΔptsG本实验构建S05-1B.subtilis 168 ΔdhbB∷P43-menA ΔtrpE ΔaroH ΔptsG ΔaraM本实验构建S05-2B.subtilis 168 ΔdhbB∷P43-menA ΔtrpE ΔaroH ΔptsG ΔmgsA本实验构建S06B.subtilis 168 ΔdhbB∷P43-menA ΔtrpE ΔaroH ΔptsG ilvC∷P43-nadK本实验构建S07B.subtilis 168 ΔdhbB∷P43-menA ΔtrpE ΔaroH ΔptsG ycsE∷P43-ndh本实验构建S08B.subtilis 168 ΔdhbB∷P43-menA ΔtrpE ΔaroH ΔptsG ycsE∷P43-ndh P43-qcrABC本实验构建S09B.subtilis 168 ΔdhbB∷P43-menA ΔtrpE ΔaroH ΔptsG ycsE∷P43-ndh P43-qoxABCD本实验构建S10B.subtilis 168 ΔdhbB∷P43-menA ΔtrpE ΔaroH ΔptsG ycsE∷P43-ndh P43-sdhCAB本实验构建S11B.subtilis 168 ΔdhbB∷P43-menA ΔtrpE ΔaroH ΔptsG ycsE∷P43-ndh P43-ythAB本实验构建S12B.subtilis 168 ΔdhbB∷P43-menA ΔtrpE ΔaroH ΔptsG ycsE∷P43-ndh lytC∷P43-AgtDxs本实验构建S13B.subtilis 168 ΔdhbB∷P43-menA ΔtrpE ΔaroH ΔptsG ycsE∷P43-ndh lytC∷P43-AgtDxs amyE∷P43-hepS本实验构建PDG148E.coli-B.subtilis shuttle vector, containing cre under the control of Pspac,Amp, Km实验室保存P7Z6Pmd18-T containing lox71-zeo-lox66 cassette实验室保存
表2 本研究所用引物
Table 2 Primers used in this study
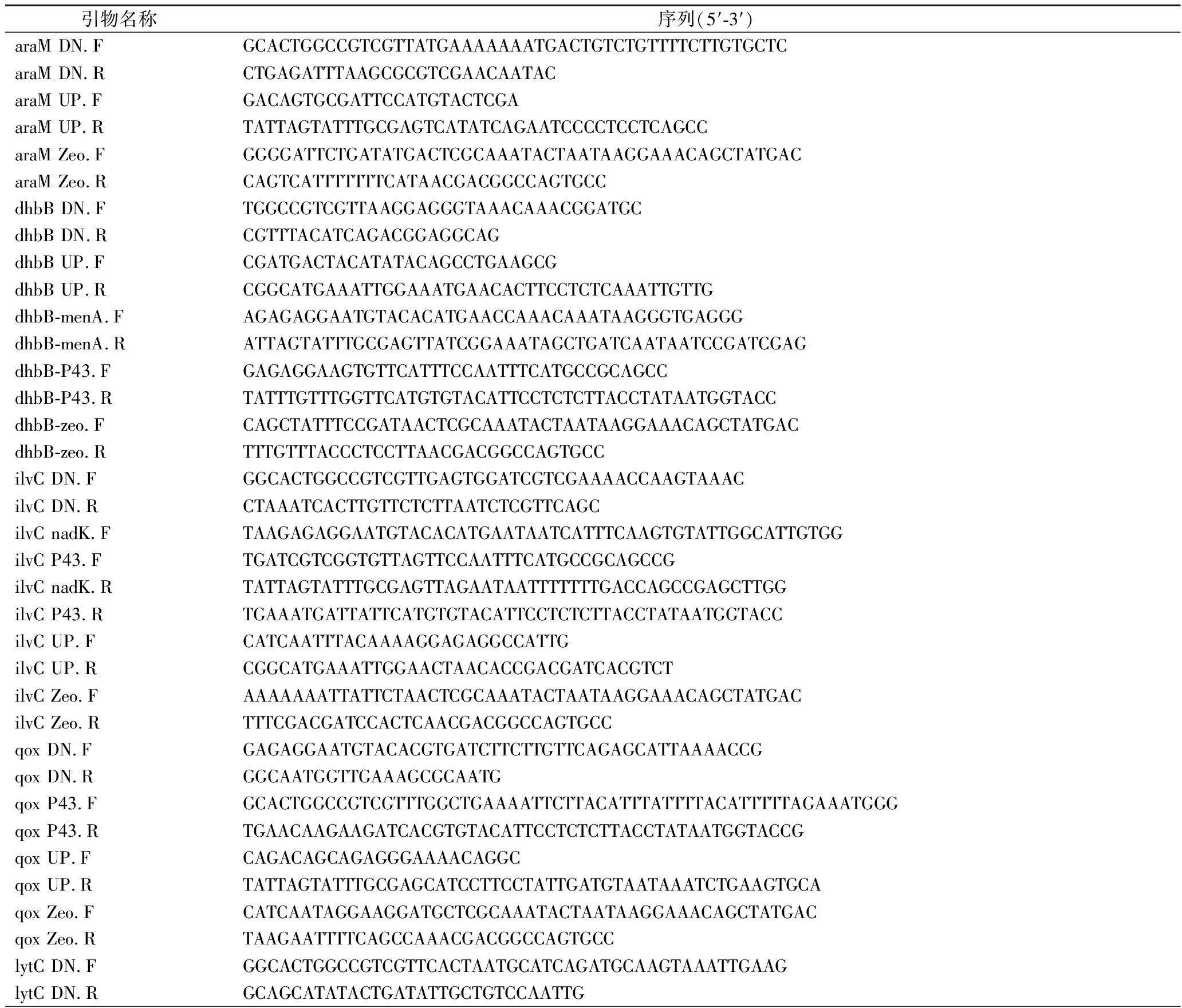
引物名称序列(5′-3′)araM DN.F GCACTGGCCGTCGTTATGAAAAAAATGACTGTCTGTTTTCTTGTGCTCaraM DN.R CTGAGATTTAAGCGCGTCGAACAATACaraM UP.F GACAGTGCGATTCCATGTACTCGAaraM UP.R TATTAGTATTTGCGAGTCATATCAGAATCCCCTCCTCAGCCaraM Zeo.FGGGGATTCTGATATGACTCGCAAATACTAATAAGGAAACAGCTATGAC araM Zeo.RCAGTCATTTTTTTCATAACGACGGCCAGTGCCdhbB DN.FTGGCCGTCGTTAAGGAGGGTAAACAAACGGATGCdhbB DN.RCGTTTACATCAGACGGAGGCAGdhbB UP.FCGATGACTACATATACAGCCTGAAGCGdhbB UP.RCGGCATGAAATTGGAAATGAACACTTCCTCTCAAATTGTTGdhbB-menA.FAGAGAGGAATGTACACATGAACCAAACAAATAAGGGTGAGGGdhbB-menA.RATTAGTATTTGCGAGTTATCGGAAATAGCTGATCAATAATCCGATCGAGdhbB-P43.F GAGAGGAAGTGTTCATTTCCAATTTCATGCCGCAGCCdhbB-P43.R TATTTGTTTGGTTCATGTGTACATTCCTCTCTTACCTATAATGGTACCdhbB-zeo.F CAGCTATTTCCGATAACTCGCAAATACTAATAAGGAAACAGCTATGACdhbB-zeo.R TTTGTTTACCCTCCTTAACGACGGCCAGTGCCilvC DN.FGGCACTGGCCGTCGTTGAGTGGATCGTCGAAAACCAAGTAAACilvC DN.RCTAAATCACTTGTTCTCTTAATCTCGTTCAGCilvC nadK.FTAAGAGAGGAATGTACACATGAATAATCATTTCAAGTGTATTGGCATTGTGGilvC P43.F TGATCGTCGGTGTTAGTTCCAATTTCATGCCGCAGCCGilvC nadK.RTATTAGTATTTGCGAGTTAGAATAATTTTTTTGACCAGCCGAGCTTGGilvC P43.R TGAAATGATTATTCATGTGTACATTCCTCTCTTACCTATAATGGTACCilvC UP.FCATCAATTTACAAAAGGAGAGGCCATTGilvC UP.RCGGCATGAAATTGGAACTAACACCGACGATCACGTCTilvC Zeo.F AAAAAAATTATTCTAACTCGCAAATACTAATAAGGAAACAGCTATGACilvC Zeo.R TTTCGACGATCCACTCAACGACGGCCAGTGCCqox DN.F GAGAGGAATGTACACGTGATCTTCTTGTTCAGAGCATTAAAACCGqox DN.R GGCAATGGTTGAAAGCGCAATGqox P43.FGCACTGGCCGTCGTTTGGCTGAAAATTCTTACATTTATTTTACATTTTTAGAAATGGGqox P43.RTGAACAAGAAGATCACGTGTACATTCCTCTCTTACCTATAATGGTACCGqox UP.F CAGACAGCAGAGGGAAAACAGGCqox UP.R TATTAGTATTTGCGAGCATCCTTCCTATTGATGTAATAAATCTGAAGTGCAqox Zeo.FCATCAATAGGAAGGATGCTCGCAAATACTAATAAGGAAACAGCTATGACqox Zeo.RTAAGAATTTTCAGCCAAACGACGGCCAGTGCClytC DN.F GGCACTGGCCGTCGTTCACTAATGCATCAGATGCAAGTAAATTGAAG lytC DN.R GCAGCATATACTGATATTGCTGTCCAATTG
续表2

引物名称序列(5′-3′)lytC dxs.FAGAGAGGAATGTACACATGCCGCAAACACCGTTACTGlytC dxs.RTATTAGTATTTGCGAGTCATTAGCCTGCAAAGCCCACGlytC P43.FGGGAGTTCCTATGCAGTTCCAATTTCATGCCGCAGCCGlytC P43.RCGGTGTTTGCGGCATGTGTACATTCCTCTCTTACCTATAATGGTACClytC UP.F GAAATGCCTGCTAGCTGGTCAClytC UP.R CGGCATGAAATTGGAACTGCATAGGAACTCCCACCAACAATTAlytC Zeo.FTTTGCAGGCTAATGACTCGCAAATACTAATAAGGAAACAGCTATGAClytC Zeo.RTCTGATGCATTAGTGAACGACGGCCAGTGCCsdh DN.F AGAGAGGAATGTACACATGTCTGGGAACAGAGAGTTTTATTTTCGsdh DN.R CAGGCGTCCGGTTAAACATGACmgsA DN.F GGCACTGGCCGTCGTTATGTATAATGCTGACGTTCTTGCTTTTGGmgsA DN.R GATATCCGTGCCATGCAAAGTGGTAAmgsA UP.F GACATACAGGCTGAAGTAGACCGmgsA UP.R ATTAGTATTTGCGAGCTAATCAATGATATTTTCTAAACCATACACAAGCTGATCmgsA Zeo.FAAATATCATTGATTAGCTCGCAAATACTAATAAGGAAACAGCTATGACmgsA Zeo.RCGTCAGCATTATACATAACGACGGCCAGTGCCptsG DN.F GGCACTGGCCGTCGTTGGGTGTTAGTACGCCGTGCTptsG DN.R GCCTGTAGCAGCTTTCGTTCCptsG UP.F GAGGTATTGAATGACAAAGGAGCTGAGptsG UP.R ATTAGTATTTGCGAGAAGAATTGACCTCCTCTTTTTACTAGTCTGACptsG Zeo.FAGGAGGTCAATTCTTCTCGCAAATACTAATAAGGAAACAGCTATGACptsG Zeo.RCGGCGTACTAACACCCAACGACGGCCAGTGCCycsE DN.F GCACTGGCCGTCGTTCAGCCTTAATGACATTGCGATGATCAAAGycsE DN.R GACACATCATGTCCTTGCTGAGAycsE ndh.FAGAGAGGAATGTACACATGTCAAAACATATTGTCATTCTAGGCGCycsE ndh.RTATTAGTATTTGCGAGTTAGTAAGCCAGGCTGAAAAGTCCTTTAATATGTycsE P43.FCATACGGACCATATTCTTCCAATTTCATGCCGCAGCCycsE P43.RCAATATGTTTTGACATGTGTACATTCCTCTCTTACCTATAATGGTACCycsE UP.F GCTTATAAGCTGATTAGTGAGAACGACTGGycsE UP.R CGGCATGAAATTGGAAGAATATGGTCCGTATGAAGCAGCTycsE Zeo.FCAGCCTGGCTTACTAACTCGCAAATACTAATAAGGAAACAGCTATGACycsE Zeo.RAATGTCATTAAGGCTGAACGACGGCCAGTGCC
1.1.2 主要试剂
大豆蛋白胨、酵母提取物、蛋白胨,OXOID公司;甘油、博来霉素,北京索莱宝科技有限公司;正己烷、异丙醇、MgSO4·7H2O、K2PHO4,上海麦克林生化科技股份有限公司;琼脂、NaCl,生工生物工程(上海)股份有限公司;柱式PCR胶回收试剂盒,Omega Bio-Tek公司;Phanta Max、2×Taq PCR Master Mix,南京诺唯赞生物科技股份有限公司。
1.1.3 培养基
LB培养基(g/L):酵母提取物 5,蛋白胨 10,NaCl 10;LB固体培养基:在LB培养基的基础上添加15~20 g/L琼脂粉末,121 ℃、20 min灭菌。
发酵培养基(g/L):甘油 30,大豆蛋白胨 60,酵母粉 5,MgSO4·7H2O 0.5,K2HPO4 3,121 ℃、20 min灭菌。
1.2 仪器与设备
恒温摇床,上海知楚仪器有限公司;UV-2600可见分光光度计,岛津企业管理(中国)有限公司;ST16冷冻离心机,赛默飞世尔科技有限公司;T200双槽梯度基因扩增仪、HD-2500多管漩涡混合仪,杭州佑宁仪器有限公司;恒温培养箱,上海跃进医疗器械厂;RVC 2-33 CD plus大型浓缩仪,德采实仪器设备(北京)有限公司;H-Class/QDa液质联用仪,沃特世公司;M-100葡萄糖-甘油生物传感器分析仪,深圳市西尔曼科技有限公司;3 L生物反应器,上海保兴生物设备工程有限公司。
1.3 实验方法
1.3.1 基因过表达
以过表达ndh为例,以B.subtilis 168基因组为扩增模板,使用ycsE UP F/R、ycsE DN F/R、ycsE P43 F/R进行PCR扩增,获得片段ycsE-UP、ycsE-DN和P43;以P7Z6为模板,使用引物ycsE Zeo F/R进行扩增,获得片段ycsE-Zeo。将上述4个片段纯化后按照yscE-UP、ycsE-Zeo、ycsE-P43、ycsE-DN的顺序进行组装并整合至B.subtilis 168基因组上完成ndh在ycsE位点的过表达。以重组菌株为宿主,转入pDG148质粒后使用IPTG诱导,引发lox71和lox66位点发生特异性重组,从而敲除博来霉素抗性筛选标记。随后通过连续传代培养促使pDG148质粒自然丢失,最终获得无筛选标记的重组菌株。
1.3.2 重组菌株的构建
使用SPIZIZEN[13]的转化方法进行重组菌株构建。
1.3.3 生物量测定
根据发酵时间的不同,选择合适的稀释倍数,使用分光光度计测定发酵液在600 nm处的吸光值。
1.3.4 菌株发酵
种子培养:甘油菌划线后挑取生长良好的单菌落接种于LB培养基中,37 ℃,220 r/min,培养12 h。摇瓶发酵:接种初始OD值为0.1,吸取相应体积的种子液接种于装有30 mL发酵培养基的三角瓶中,40 ℃,220 r/min,培养96 h。发酵罐培养:接种量10%,初始装液量1 L。转速与溶氧偶联,维持在20%~30%,通气量2 vvm,发酵温度40 ℃。使用含有400 g/L甘油的补料培养基维持甘油质量浓度在5~10 g/L,发酵过程中每12 h进行1次取样,测定生物量和MK-7产量。
1.3.5 MK-7萃取
取1 mL发酵液,加入1 mL 5%(体积分数)稀盐酸,混匀后沸水浴5 min,冷却至室温。加入4 mL萃取剂(正己烷∶异丙醇=2∶1,体积比,下同),在多管涡旋振荡仪上振荡30 min。将充分混匀的样品置于离心机中,4 000 r/min,10 min离心,吸取上层萃取液,放入10 mL离心管中进行真空浓缩。
1.3.6 MK-7检测与分析
取1 mL复溶液(甲醇∶乙腈=1∶3,体积比)加入浓缩产物后使用振荡仪混匀,使用0.22 μm有机滤头过滤至液相瓶中。检测条件:柱温40 ℃,进样量3 μL,检测波长270 nm。流动相为甲醇,流速0.7 mL/min。
1.4 数据处理
所有实验均独立重复3次,数据以“平均值±标准差”表示。采用GraphPad Prism 9.5软件进行显著性分析,显著性水平设定为:P<0.05(*),P<0.01(**),P<0.001(***),P<0.000 1(****)。
2 结果与讨论
2.1 分支代谢途径的改造
以B.subtilis 168作为底盘菌株,其合成MK-7的途径可以分为4个模块:甘油利用途径、SA途径、MK途径和MEP途径。这些途径中存在多个与MK-7竞争底物的分支途径,严重限制了MK-7的合成效率。可以通过系统改造分支途径的方法,增强目标代谢通量。
异分支酸作为关键节点代谢物,面临双重竞争:一方面由2-琥珀酰基-5-烯醇丙酮基-6-烃基-3-环己烯-1-羧酸酯合成酶(2-succinyl-5-enolpyruvyl-6-hydroxy-3-cyclohexene-1-carboxylate synthase,MenD)催化进入甲萘醌的生物合成[14];另一方面可被二氢-2,3二羟基苯甲酸合酶(dihydro-2,3 dihydroxybenzoate synthase,DhbB)催化,参与铁载体杆菌凝集素的合成[15]。本研究采用以下改造策略:敲除异分支酸-丙酮酸水解酶编码基因dhbB并整合MK-7合成关键酶基因menA,获得菌株S01;在S01的基础上对芳香族氨基酸合成途径中的2个关键基因—trpE(编码邻氨基苯甲酸合成酶)和aroH(编码分支酸变位酶)进行组合敲除,减少分支酸的竞争性消耗,获得菌株S02。
重组菌株S01产量为(11.98±0.93)mg/L,与对照组相比提升了53.3%;S02的产量为(21.50±0.64) mg/L,与S01相比,产量提升了79.4%(图2)。对于dhbB的敲除并未对生物量产生影响,但叠加敲除trpE和aroH导致生物量下降,但MK-7的合成效率仍显著提高,表明碳代谢流已有效导向目标途径。基于上述结果,S02被选为后续改造的底盘菌株。
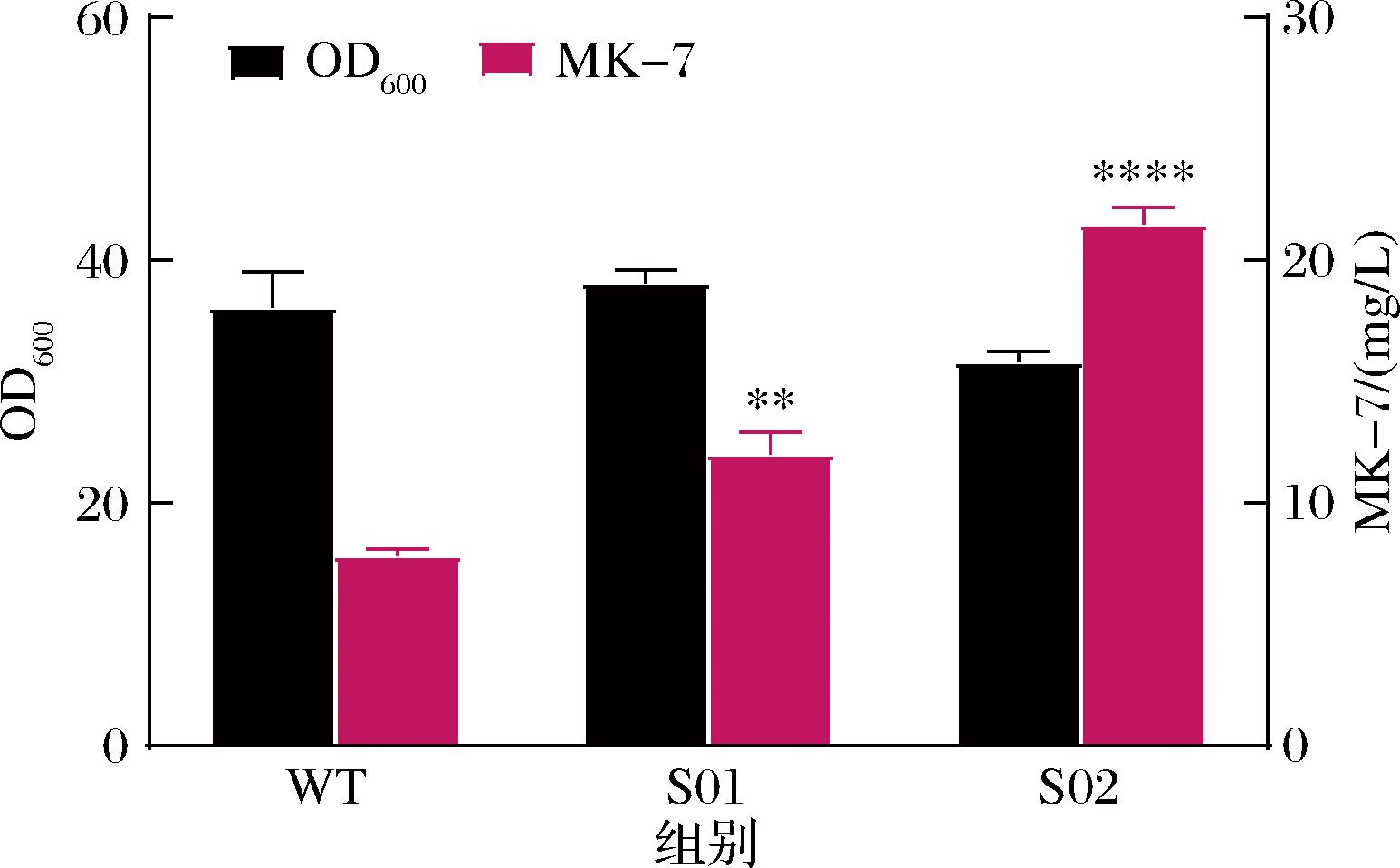
图2 铁载体杆菌凝集素和芳香族氨基酸合成分支途径改造
Fig.2 Modification of the branching pathway of siderophore bacillibactin and aromatic amino acid synthesis
注:**表示P<0.01;****表示P<0.000 1(下同)。
基于菌株S02,本研究进一步对碳代谢关键分流节点进行系统改造,以优化MK-7的生物合成效率。二羟丙酮磷酸(dihydroxyacetone phosphate,DHAP)作为甘油代谢途径的核心中间产物,同时为MEP途径和SA途径提供前体物质甘油醛-3-磷酸(Glyceraldehyde 3-phosphate,G3P)。然而,该代谢节点存在显著的分流竞争:araM基因编码的葡萄糖-1-磷酸(Glucose 1-phosphate,G1P)磷酸脱氢酶催化DHAP转化为磷酸甘油酸[16];mgsA基因编码的甲基乙二醛合酶催化DHAP生成甲基乙二醛。这些竞争途径显著降低了可用于MK-7合成的DHAP供给。此外,ptsG基因编码的磷酸酶转移系统(phosphotransferase system,PTS)葡萄糖转运蛋白在介导葡萄糖摄取过程中会消耗磷酸烯醇式丙酮酸(phosphoenolpyruvic acid,PEP)[17],从而与SA途径竞争这一重要前体物质。
在S02菌株基础上,本研究分别构建了araM、mgsA和ptsG的单基因敲除突变株。S03、S04和S05菌株的MK-7产量分别达到(26.29±1.02)、(26.15±0.48)、(39.37±2.51) mg/L(图3-a)。由此可见,敲除ptsG效果最为显著,阻断PEP消耗途径的同时还提高了菌体生物量。随后在S05(ΔptsG)菌株基础上,分别构建了mgsA和araM的双基因敲除菌株S05-1(ΔptsG ΔmgsA)和S05-2(ΔptsG ΔaraM)。S05-1和S05-2的MK-7产量分别为(39.58±1.47)和(39.03±1.45) mg/L,与S05单敲除菌株相比未呈现显著差异(图3-b)。基于上述研究结果,本研究选择S05作为后续改造的底盘菌株。
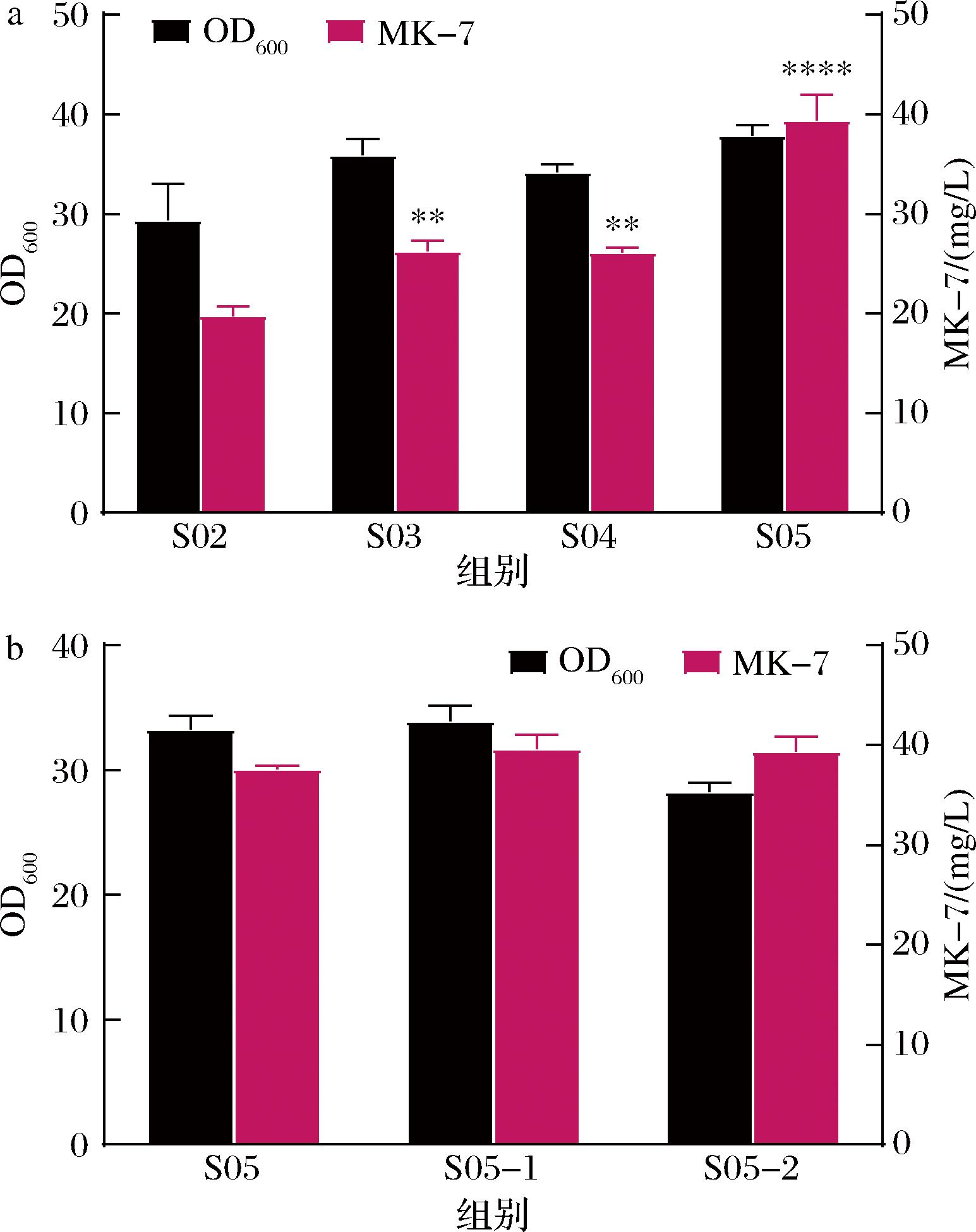
a-敲除araM、mgsA和ptsG后的对产物合成和细胞生长的影响;b-基于S05敲除araM和mgsA的发酵评价
图3 葡萄糖摄取和甘油利用分支代谢途径改造
Fig.3 Glucose uptake and glycerol are engineered using branched metabolic pathways
2.2 辅因子改造
在MK-7的合成过程中,涉及多种辅因子的消耗与再生,辅因子的平衡调控至关重要。根据DING等[18]的研究,每合成1 mol DMK-7需要消耗19 mol甘油和10 mol NADPH,同时会生成11 mol NADH。研究表明,MK-7的合成量与NADH的生成量呈正相关。当细胞内NADH/NADPH比例失衡时,会影响正常的生理代谢活动和产物合成。
为优化辅因子平衡,本研究采用2个策略:在ilvC位点过表达nadK(NAD激酶),促进NAD+向NADP+的转化,生成的NADP+参与三羧酸(tricarboxylic acid,TCA)循环,生成NADPH;在ycsE位点过表达ndh(NADH脱氢酶),强化电子传递效率(图4-a)。过表达nadK的菌株MK-7产量达到(44.56±2.11) mg/L;过表达ndh的菌株产量显著提升至(54.82±1.82) mg/L,较对照提高31%(图4-b)。此外,ndh过表达菌株的生物量也呈现显著增加。机制分析表明,ndh过表达促进了电子传递链的电子供应,提高了细胞呼吸链的活性,增强了对MK-7(作为电子载体)的需求。与此同时,该策略改善了细胞整体的代谢强度和能量生成效率,促进了菌株生长。
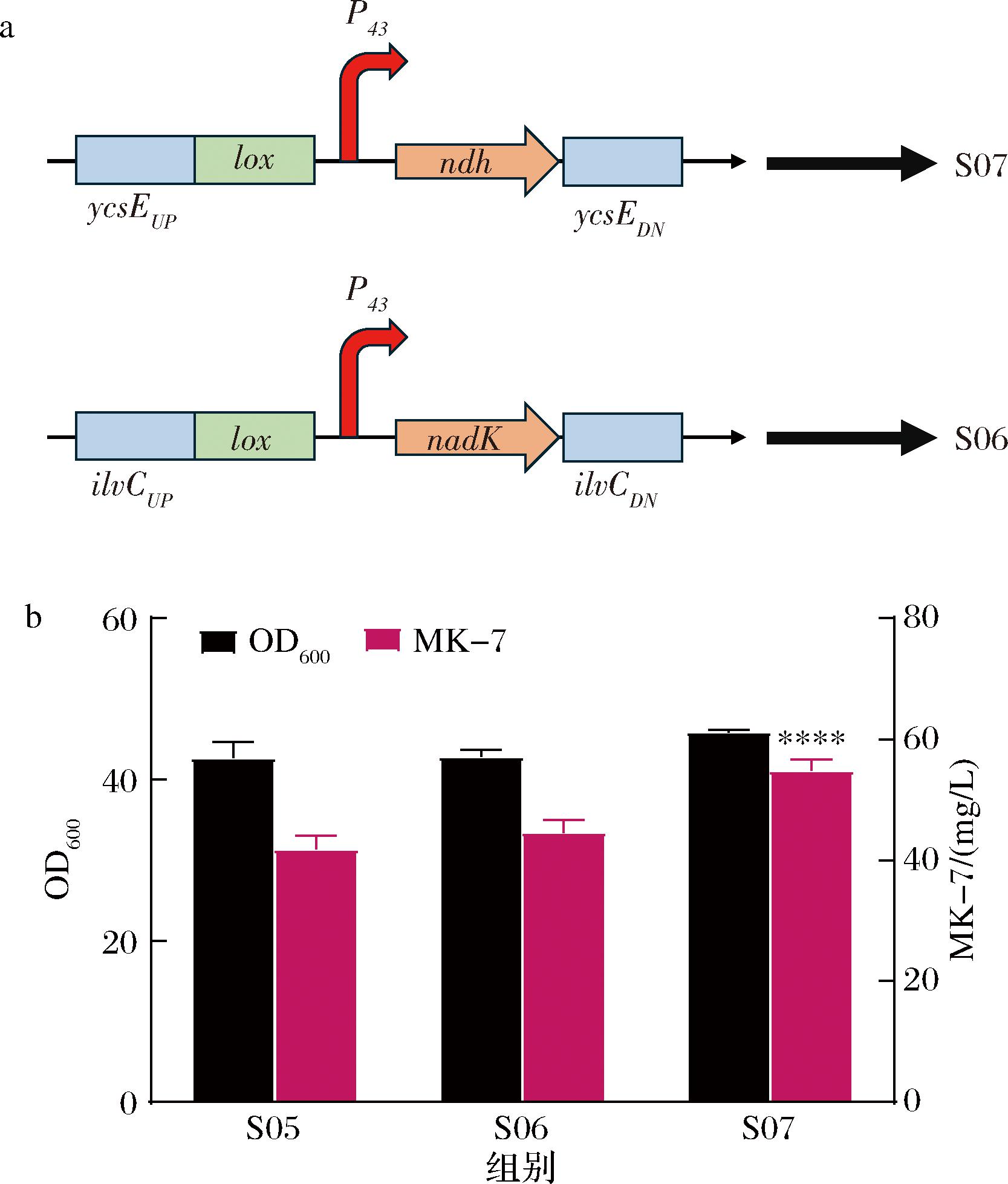
a-分别在ycsE位点和ilvC位点过表达ndh和nadK;b-过表达ndh和nadK对生长和产物合成的影响
图4 辅因子改造
Fig.4 Cofactor engineering
基于上述结果,选择S07菌株作为后续改造的底盘菌株。该策略不仅优化了辅因子平衡,还通过增强细胞呼吸链实现了代谢强度的提升,促进了MK-7的高效合成。
2.3 末端氧化呼吸酶的改造
MK-7在枯草芽孢杆菌的有氧呼吸链中发挥着关键作用。其电子传递机制表现为:NADH通过NADH脱氢酶(NADH dehydrogenase,NDH)脱氢,将H+传递给氧化态MK-7,使其还原为甲萘氢醌(2-Methyl-1,4-naphthoquinol,MKH2);随后MKH2作为电子载体通过末端氧化酶被重新氧化为MK-7,完成电子传递循环。在S07中,ndh的过表达提升了电子传递效率,促进了细胞的生长和产物的合成。在此基础上,本研究进一步对电子传递链进行系统改造。选取了4类与醌类电子传递相关的末端氧化酶基因进行过表达(图5-a):qcrABC(甲萘醌:细胞色素c氧化还原酶)、qoxABCD(细胞色素aa3醌氧化还原酶)、sdhCAB(琥珀酸脱氢酶)、ythAB(甲萘醌氧化酶)。
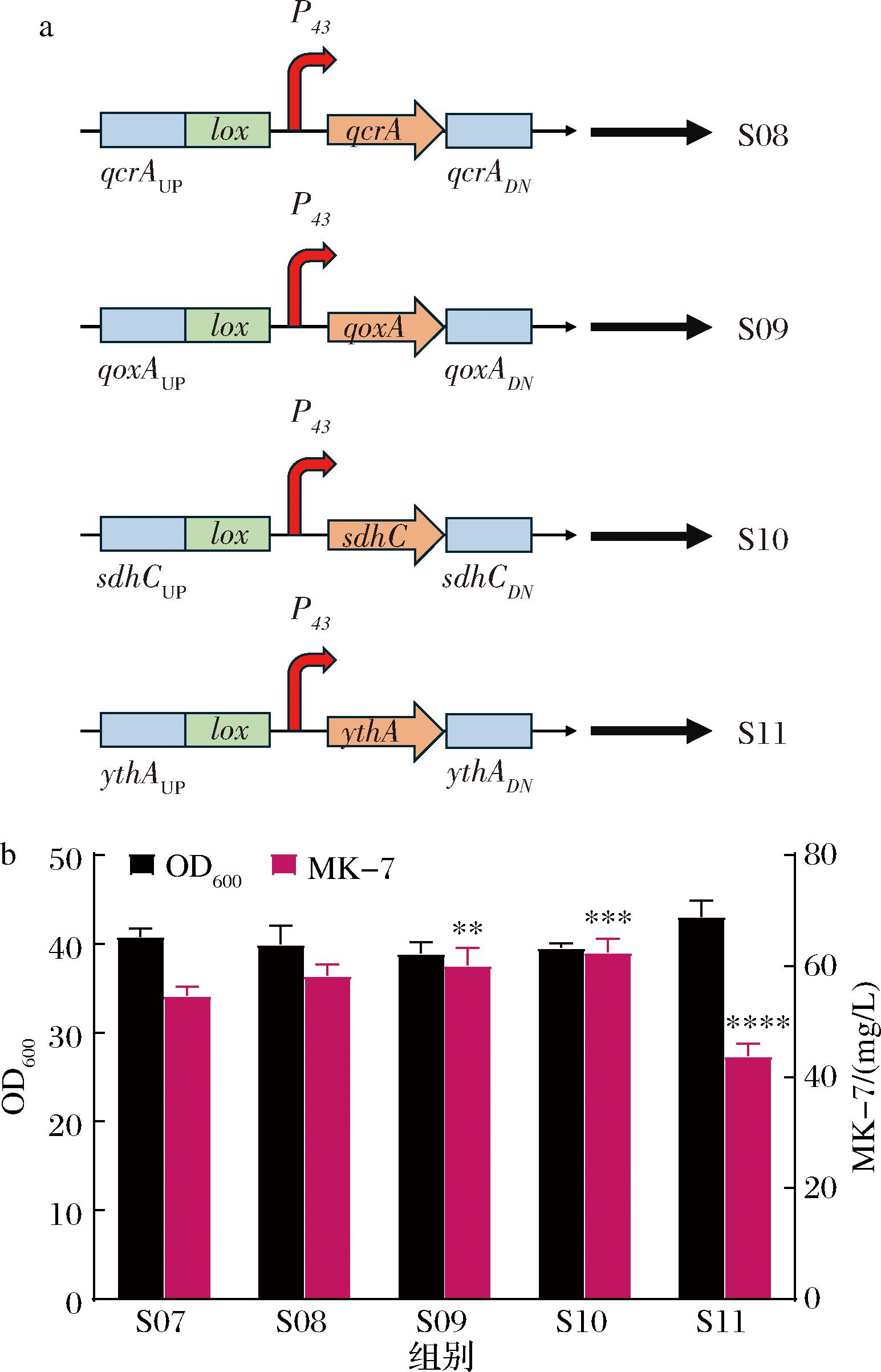
a-对末端氧化酶编码基因进行原位过表达;b-过表达末端氧化呼吸酶后对生长和生产的影响
图5 末端氧化呼吸酶改造
Fig.5 Modification of terminal oxidative respiratory enzymes
注:***表示P<0.001(下同)。
对sdhCAB进行过表达后,产量为(62.50±2.37) mg/L,与S07相比提升了14.6%,效果较为显著(图5-b);过表达ythAB导致产量出现了剧烈的下降,可能引发了电子传递失衡;qcrABC和qoxABCD的过表达对产量具有正向的积累作用,但效果有限,推测与其受到严格的调控相关。sdhCAB的促进作用可能源于:作为TCA循环关键酶,其过表达可能重塑了碳代谢流;增强了醌类电子传递效率;促进了NADH的再生循环。这也为后续的呼吸链工程改造提供了重要的参考。
2.4 MEP途径的改造
MEP途径不仅用于甲萘醌的异戊二烯侧链的生成,同时也被认为是MK-7生产的限制途径之一。其中的1-脱氧-D木酮糖-5-磷酸合成酶(1-deoxy-D-xylulose-5-phosphate synthase,DXS)是MEP途径的限速酶。其中,DXS活性受到中间产物IPP/DMAPP的反馈抑制调控[19]。此外,hepS也是MK-7合成的关键基因,GAO等[20]首次在大肠杆菌中过表达B.subtilis来源的hepT/hepS基因,构建了用于高效合成MK-7的工程化大肠杆菌。
基于此,以底盘菌株S10为基础,进行了以下基因改造:1)在lytC位点过表达根癌农杆菌(Agrobacterium tumefaciens)来源的dxs基因,获得重组菌株S12;2)在S12的基础上,进一步在amyE位点过表达内源hepS基因,获得工程菌株S13。发酵结果表明(图6),与S10相比,S12中异源dxs基因的过表达使MK-7产量提升至(79.24±3.07) mg/L,这表明引入异源dxs基因有效增强了MEP途径的通量,从而促进了MK-7的合成。在此基础上,S13通过过表达hepS基因,使MK-7产量进一步提高至(123.90±6.52) mg/L,这可能是由于hepS的过表达促进了法尼基焦磷酸(farnesyl pyrophosphate,FPP)向庚烯基焦磷酸(heptaprenyl diphosphate,HDP)的转化,增加了异戊二烯侧链的供应,从而显著提升了产物的合成效率。
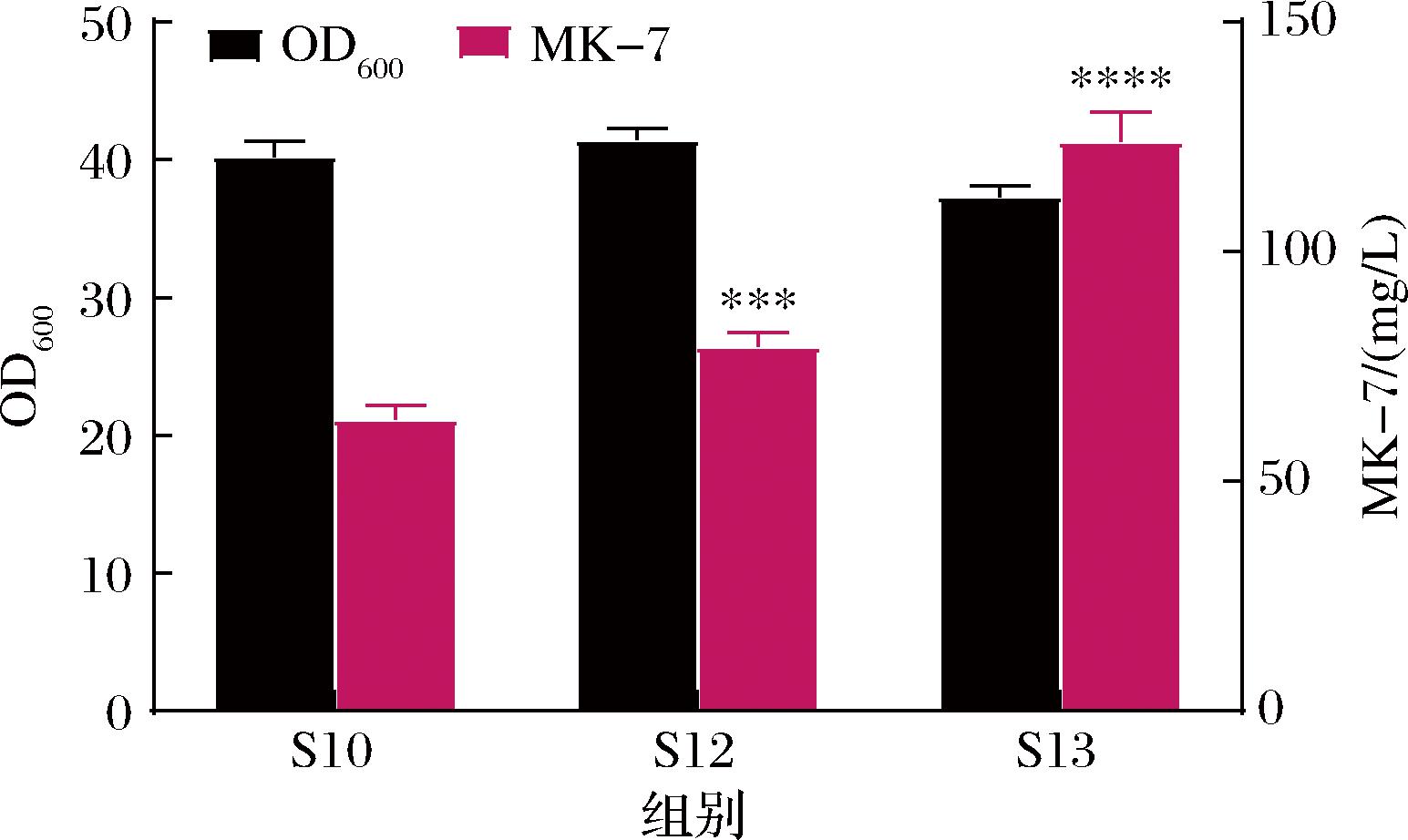
图6 MEP途径改造
Fig.6 Metabolic modification of MEP pathway
2.5 3 L发酵罐放大生产
在摇瓶培养的基础上,尝试对菌株S13进行3 L发酵罐放大生产,发酵时间96 h。产物的积累集中于发酵后期(48~96 h),有研究表明,枯草芽孢杆菌最适生长温度和最适生产温度并不一致[21],因此采用变温发酵策略—发酵前48 h采用37 ℃发酵,在49~96 h采用40 ℃发酵[22]。该策略可保证菌体能够在前期进行快速生长,中后期实现产物生成与积累。在分批补料培养条件下,甘油质量浓度控制在5~15 g/L,溶氧与转速偶联。由图7可见,随着发酵的进行,生物量呈现逐步提升的趋势,产物随着时间的增长会逐渐累积,发酵终止时为最高产量242.38 mg/L。
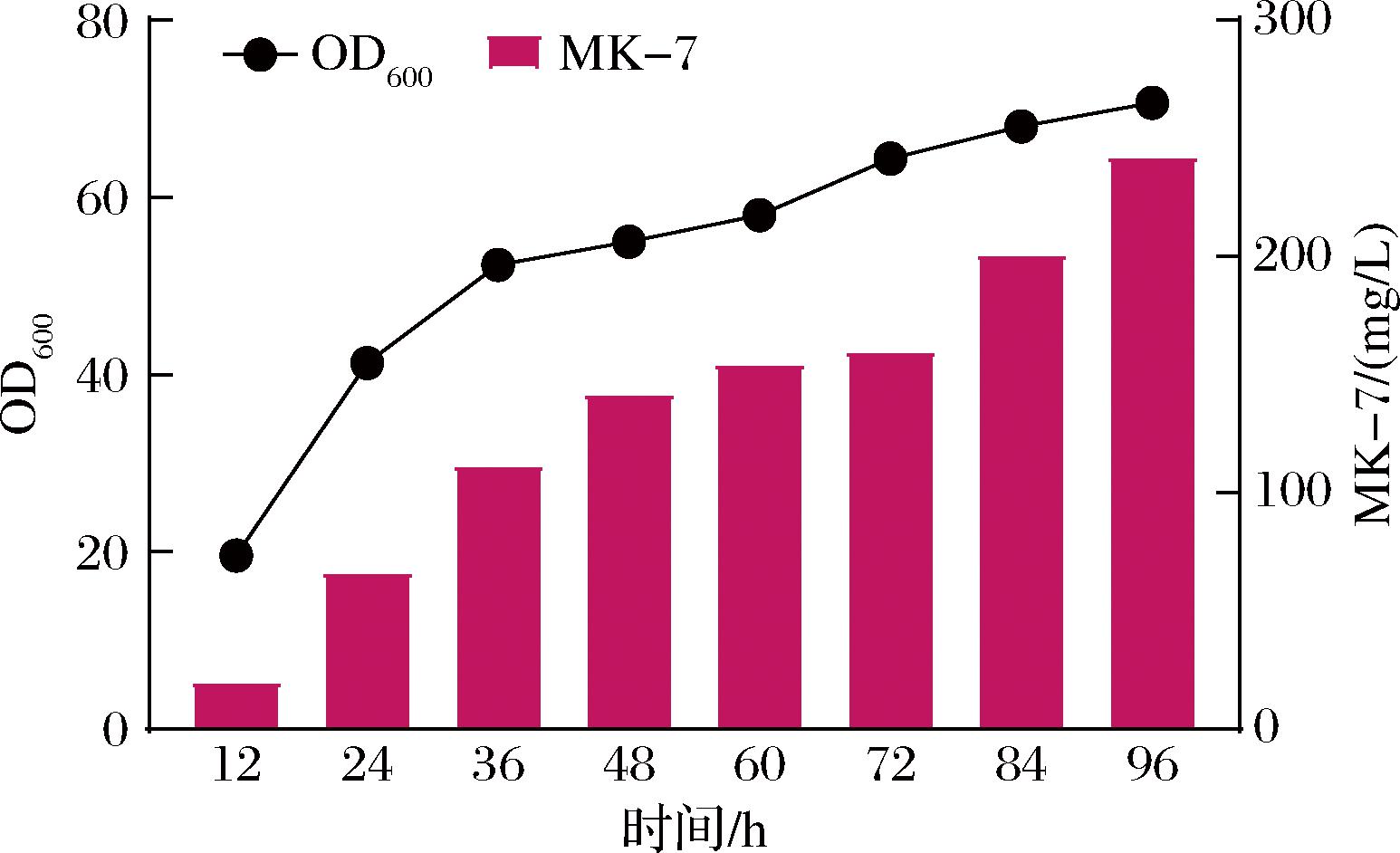
图7 3 L发酵罐放大生产
Fig.7 Scale-up production of 3 L fermenter
3 结论与讨论
MK-7被广泛应用于食品和医疗领域,其需求量逐年提升,因此利用微生物生产MK-7具有重要意义。在之前的研究中,多侧重于单方面的改造—MEP途径的强化、电子传递链的改造,而针对前体供应的改造较少。因此,本研究以B.subtilis 168为出发菌株,通过敲除分支代谢途径、增强电子传递链、引入异源基因以及过表达关键基因的策略,获得了高产菌株S13,其摇瓶发酵中MK-7产量达到(123.90±6.52) mg/L。随后在3 L发酵罐中对重组菌株进行放大生产,通过调整发酵温度和补料速率等参数,经96 h发酵后MK-7产量提升至242.38 mg/L。与之前的研究相比,该策略缩短了发酵周期,提高了枯草芽孢杆菌生产MK-7的效率。
近年来,随着对枯草芽孢杆菌研究的深入,越来越多的改造策略与工具被开发出来。后续研究可通过以下方面进一步提高MK-7产量:强化MK-7合成途径、敲除分支与降解途径、优化产物外排机制等策略,并结合培养基组分和发酵工艺参数的优化,进一步提升枯草芽孢杆菌生产MK-7的生产效率。
[1] KUROSU M, BEGARI E.Vitamin K2 in electron transport system:Are enzymes involved in vitamin K2 biosynthesis promising drug targets?[J].Molecules, 2010, 15(3):1531-1553.
[2] SATO T, INABA N, YAMASHITA T.MK-7 and its effects on bone quality and strength[J].Nutrients, 2020, 12(4):965.
[3] YUAN Y, SZETO I M, LI N, et al.Effects of menaquinone-7 on the bone health of growing rats under calcium restriction:New insights from microbiome-metabolomics[J].Nutrients, 2023, 15(15):3398.
[4] TAN J, ZHU R, LI Y, et al.Vitamin K2 in managing nocturnal leg cramps:A randomized clinical trial[J].JAMA Internal Medicine, 2024, 184(12):1443-1447.
[5] EMEKLI-ALTURFAN E, ALTURFAN A A.The emerging relationship between vitamin K and neurodegenerative diseases:A review of current evidence[J].Molecular Biology Reports, 2023, 50(1):815-828.
[6] HARIRI E, KASSIS N, ISKANDAR J P, et al.Vitamin K2-a neglected player in cardiovascular health:A narrative review[J].Open Heart, 2021, 8(2):e001715.
[7] LAL N, BERENJIAN A.Cis and trans isomers of the vitamin menaquinone-7:Which one is biologically significant?[J].Applied Microbiology and Biotechnology, 2020, 104(7):2765-2776.
[8] FANG Z W, WANG L, ZHAO G H, et al.A simple and efficient preparative procedure for menaquinone-7 from Bacillus subtilis (natto) using two-stage extraction followed by microporous resins[J].Process Biochemistry, 2019, 83:183-188.
[9] 康倩, 向梦洁, 张大伟.枯草芽孢杆菌在系统与合成生物技术中研究进展及工业应用[J].生物工程学报, 2021, 37(3):923-938.
KANG Q, XIANG M J, ZHANG D W.Research progress and industrial application of Bacillus subtilis in systematic and synthetic biotechnology[J].Chinese Journal of Biotechnology, 2021, 37(3):923-938.
[10] YANG S M, CAO Y X, SUN L M, et al.Modular pathway engineering of Bacillus subtilis to promote de novo biosynthesis of menaquinone-7[J].ACS Synthetic Biology, 2019, 8(1):70-81.
[11] HUANG W, LI J L, ZHU Q Y, et al.Increasing vitamin K2 synthesis in Bacillus subtilis by controlling the expression of MenD and stabilizing MenA[J].Journal of Agricultural and Food Chemistry, 2024, 72(41):22672-22681.
[12] GAO X L, LUO Y N, ADINKRA E K, et al.Engineering a PhrC-RapC-SinR quorum sensing molecular switch for dynamic fine-tuning of menaquinone-7 synthesis in Bacillus subtilis[J].Microbial Cell Factories, 2025, 24(1):88.
[13] SPIZIZEN J.Transformation of biochemically deficient strains of Bacillus subtilis by deoxyribonucleate[J].Proceedings of the National Academy of Sciences of the United States of America, 1958, 44(10):1072-1078.
[14] JOHNSTON J M, BULLOCH E M.Advances in menaquinone biosynthesis:Sublocalisation and allosteric regulation[J].Current Opinion in Structural Biology, 2020, 65:33-41.
[15] ROWLAND B M, TABER H W.Duplicate isochorismate synthase genes of Bacillus subtilis:Regulation and involvement in the biosyntheses of menaquinone and 2, 3-dihydroxybenzoate[J].Journal of Bacteriology, 1996, 178(3):854-861.
[16] GULDAN H, STERNER R, BABINGER P.Identification and characterization of a bacterial glycerol-1-phosphate dehydrogenase:Ni(2+)-dependent AraM from Bacillus subtilis[J].Biochemistry, 2008, 47(28):7376-7384.
[17] ZAGOREC M, POSTMA P W.Cloning and nucleotide sequence of the ptsG gene of Bacillus subtilis[J].Molecular and General Genetics MGG, 1992, 234(2):325-328.
[18] DING X M, ZHENG Z M, ZHAO G H, et al.Bottom-up synthetic biology approach for improving the efficiency of menaquinone-7 synthesis in Bacillus subtilis[J].Microbial Cell Factories, 2022, 21(1):101.
[19] DI X N, ORTEGA-ALARCON D, KAKUMANU R, et al.MEP pathway products allosterically promote monomerization of deoxy-D-xylulose-5-phosphate synthase to feedback-regulate their supply[J].Plant Communications, 2023, 4(3):100512.
[20] GAO Q X, CHEN H, WANG G Y, et al.Highly efficient production of menaquinone-7 from glucose by metabolically engineered Escherichia coli[J].ACS Synthetic Biology, 2021, 10(4):756-765.
[21] SATO T, YAMADA Y, OHTANI Y, et al.Production of menaquinone (vitamin K2)-7 by Bacillus subtilis[J].Journal of Bioscience and Bioengineering, 2001, 91(1):16-20.
[22] BERENJIAN A, CHAN N L, MAHANAMA R, et al.Effect of biofilm formation by Bacillus subtilis natto on menaquinone-7 biosynthesis[J].Molecular Biotechnology, 2013, 54(2):371-378.