黄嘌呤核苷,又名9-呋喃核糖-3,9-二氢-1H-嘌呤-2,6-二酮,简称黄苷,可通过水解反应生成黄嘌呤和核糖。作为非平衡细胞动力学分裂方式的抑制剂,黄苷既能实现骨髓间质干细胞的分裂方式由非平衡态向平衡态转变,又不影响其肝向分化的特性,有助于提高骨髓间质干细胞的体外增殖效率[1]。其次,黄苷还是咖啡碱合成途径中第一步反应的底物[2],所以在咖啡碱的生产过程中通常会添加一定浓度的黄苷,以得到更多的发酵产物。现在市场上以天然提取法和化学合成法来获得黄苷,但是都存在产率低且成本高的问题。近年来,微生物发酵法逐渐成为天然小分子产物大规模生产的重要方法。虽然细胞内嘌呤核苷的生物合成途径早已探明,但由于其合成路线长且途径受到强烈反馈抑制,目前尚未有发酵法生产黄苷的报道。
嘌呤核苷合成途径包括从头合成途径和补救途径。嘌呤核苷的全合成途径由磷酸戊糖(pentose phosphate,PP)途径生成的5-磷酸核糖焦磷酸(phosphoribosyl pyrophosphate,PRPP)出发,经多部反应生成次黄苷酸(inosine monophosphate,IMP),然后经IMP脱氢酶催化生成黄苷酸(xanthosine monophosphate,XMP),再由5′-核苷酸酶催化生成黄苷(图1);XMP也可由鸟嘌呤核苷酸合成酶催化生成鸟苷酸(guanosine monophosphate,GMP),进而生成鸟苷及下游产物[3];IMP也可在腺苷琥珀酸合成酶和腺苷琥珀酸裂解酶的催化作用下生成腺苷酸(adenosine monophosphate,AMP),进而生成腺苷及下游产物[4]。嘌呤核苷的全合成途径遇到阻碍时,生物体则需要借助补救合成途径实现嘌呤核苷的生成。在补救合成途径中,底物嘌呤碱基和PRPP在磷酸核糖转移酶的作用下相结合,形成特定的嘌呤核苷产物。
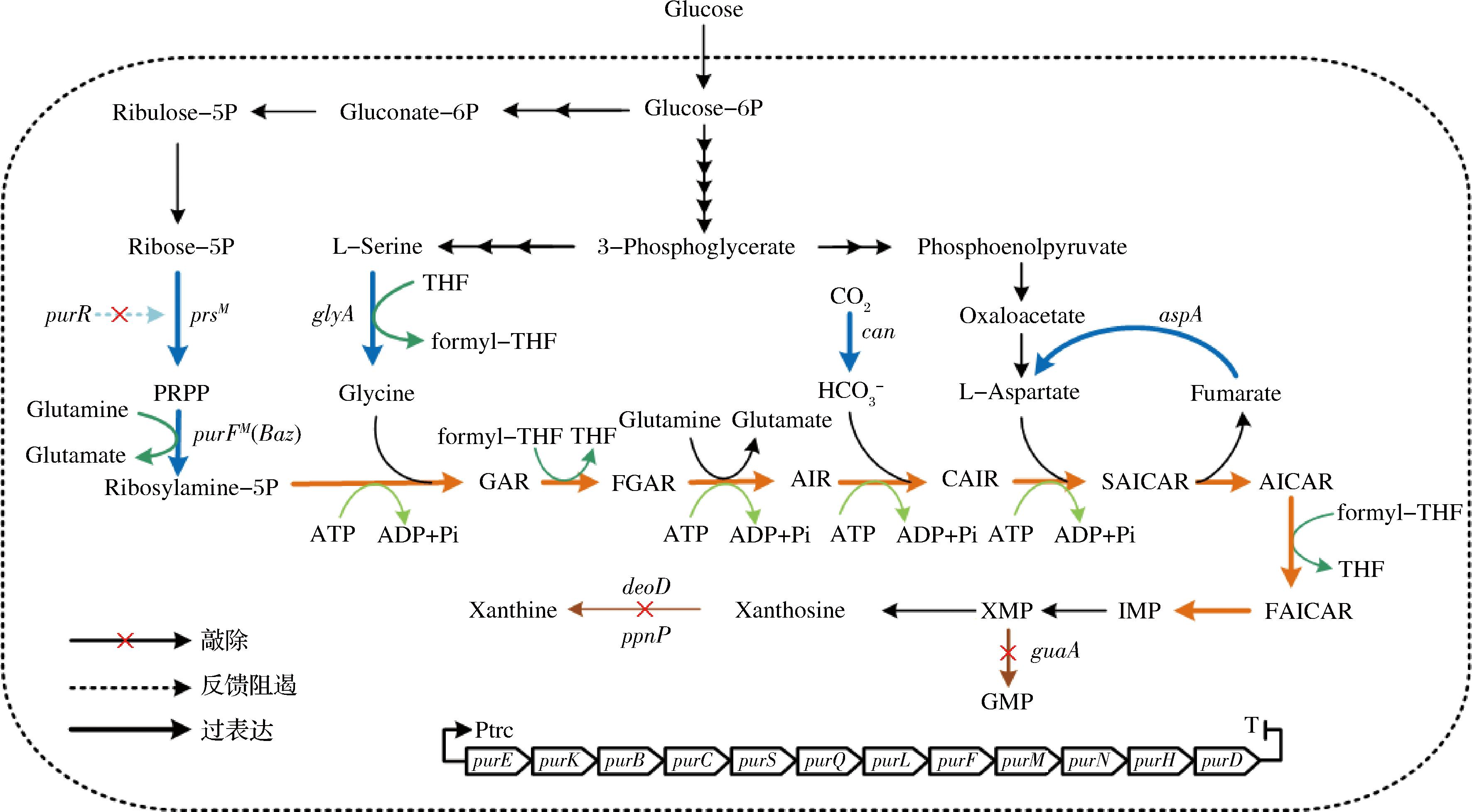
图1 黄苷生物合成途径和本研究的改造策略
Fig.1 Biosynthetic pathway of xanthosine and metabolic engineering strategies used in this study
注:Glucose,葡萄糖;Glucose-6P,6磷酸葡萄糖;Gluconate-6P,6磷酸葡糖酸;Ribulose-5P,5磷酸核酮糖;Ribose-5P,5磷酸核糖;Ribosylamine-5P,5磷酸核糖胺;Glutamine,谷氨酰胺;Glutamate,谷氨酸;3-Phosphoglycerate,3磷酸甘油酸;L-Serine,L-丝氨酸;Glycine,甘氨酸;Phosphoenolpyruvate,磷酸烯醇式丙酮酸;Oxaloacetate,草酰乙酸;L-Aspartate,L-天冬氨酸;Fumarate,富马酸;formyl-THF,甲酰基四氢叶酸;THF,四氢叶酸;purR,阻遏蛋白PurR编码基因;glyA,丝氨酸羟甲基转移酶编码基因;prsM,核糖磷酸二磷酸激酶突变体编码基因;purFM(Baz),来源于解淀粉芽胞杆菌氨基磷酸核糖基转移酶突变体编码基因;can,碳酸酐酶编码基因;aspA,天冬氨酸解氨酶编码基因;deoD,嘌呤核苷磷酸化酶编码基因;ppnP,嘌呤/嘧啶核苷磷酸化酶编码基因;guaA,GMP合成酶编码基因;purEKBCSQLFMNHD,嘌呤操纵子;GAR,甘氨酰胺核糖核苷酸;FGAR,甲酰甘氨酰胺核糖核苷酸;AIR,5-氨基咪唑核糖核苷酸;CAIR,5-氨基-4-羧基咪唑核糖核苷酸;SAICAR,N-琥珀酸-5-氨基咪唑-4-羧酰胺核糖核苷酸; AICAR,5-氨基咪唑-4-羧酰胺核糖核苷酸;FAICAR,5-甲酰胺基咪唑-4-羧酰胺核糖核苷酸;IMP,次黄苷酸;XMP,黄苷酸;GMP,鸟苷酸。
虽然目前没有微生物发酵法生产黄苷的报道,但是利用代谢工程手段构建肌苷、腺苷和鸟苷生产菌株已经有一些研究。综合来看,主要代谢改造策略包括强化嘌呤核苷的合成途径、加强前体物的供应、阻断和弱化竞争途径、切断产物分解途径等。(1)在代谢工程研究中常用强化合成路径的策略来促进目标产物的生成[5]。在芽孢杆菌中嘌呤核苷合成的关键基因以操纵子形式存在[6],引入天然操纵子结构增强嘌呤核苷合成的策略,该法既操作简便,同时保留了细菌长期进化形成的多酶表达的平衡系统。朱彦凯等[7]和梅漫莉[8]分别引入芽孢杆菌的嘌呤操纵子以提高肌苷和腺苷的含量。(2)增加嘌呤核苷合成前体物质的供应及进入嘌呤核苷合成途径的代谢反应,包括强化PRPP、甘氨酸、L-天冬氨酸、一碳单位以及CO2的合成。①PRPP的合成及进入嘌呤核苷途径的代谢:5′-磷酸核糖与ATP在PRPP合成酶的作用下生成PRPP,然而PRPP合成酶受到嘌呤核苷酸的反馈抑制。另外,PRPP合成酶编码基因prs,还有嘌呤核苷操纵子的基因,受到PurR蛋白的反馈阻遏[9]。此外,PRPP转酰胺酶受到AMP与GMP的共同反馈抑制,从而实现对嘌呤从头合成路径的精确调节[10]。MATSUI等[11]敲除了大肠杆菌(Escherichia coli)的purR基因后PRPP转酰胺酶活性提高了20%。ASAHARA等[12]敲除了枯草芽孢杆菌(Bacillus subtilis)purR基因,使嘌呤操纵子的转录强度提升了40%。SHIMAOKA等[13]在大肠杆菌中过表达了purFK326Q和prsD128A突变基因,使肌苷产量提升了72%。②前体物氨基酸合成:包括甘氨酸和L-天冬氨酸的供应。基因glyA编码的丝氨酸羟甲基转移酶催化L-丝氨酸生产甘氨酸,同时产生的5-10-亚甲基四氢叶酸是细胞新陈代谢一碳单位的重要提供者[14]。L-天冬氨酸解氨酶(由aspA基因编码)催化富马酸与氨发生加成反应,生成L-天冬氨酸。在嘌呤核苷合成的合成途径中,L-天冬氨酸将其氨基上的氮原子整合到嘌呤环中,促进嘌呤环的逐步构建。③CO2的固定:在嘌呤核苷合成途径中,CO2以![]() 的形式与5-氨基咪唑核糖核苷酸(5-aminoimidazole ribonucleotide,AIR)反应生成5-氨基-4-羧基咪唑核糖核苷酸(5-amino-4-carboxyl imidazolribonucleotide,CAIR)。潘富军等[15]研究表明碳酸酐酶可高效催化CO2生成
的形式与5-氨基咪唑核糖核苷酸(5-aminoimidazole ribonucleotide,AIR)反应生成5-氨基-4-羧基咪唑核糖核苷酸(5-amino-4-carboxyl imidazolribonucleotide,CAIR)。潘富军等[15]研究表明碳酸酐酶可高效催化CO2生成![]() 切断或弱化竞争途径是嘌呤核苷生产菌株构建中常用的手段之一。刘铁重[16]对大肠杆菌guaB基因进行弱化,使肌苷的产量提高了19%。(4)阻断产物分解途径也是代谢工程育种的重要策略。梅漫莉[8]通过敲除嘌呤核苷分解酶有效阻断了腺苷分解为腺嘌呤,徐庆阳等[17]通过敲除嘌呤核苷分解酶阻断了鸟苷的分解。同样,构建黄苷生产菌株也需要失活嘌呤核苷分解酶来阻断黄苷分解为黄嘌呤。
切断或弱化竞争途径是嘌呤核苷生产菌株构建中常用的手段之一。刘铁重[16]对大肠杆菌guaB基因进行弱化,使肌苷的产量提高了19%。(4)阻断产物分解途径也是代谢工程育种的重要策略。梅漫莉[8]通过敲除嘌呤核苷分解酶有效阻断了腺苷分解为腺嘌呤,徐庆阳等[17]通过敲除嘌呤核苷分解酶阻断了鸟苷的分解。同样,构建黄苷生产菌株也需要失活嘌呤核苷分解酶来阻断黄苷分解为黄嘌呤。
目前市场上以天然提取法和化学合成法来获得黄苷,但存在产率低且成本高的问题。开发发酵法生产黄苷为迫切需要解决的技术。近年来,系统生物学和基因编辑技术的不断发展,使得运用代谢工程理论对野生型菌株进行遗传改造获得高产菌株成为可能。本研究以野生型大肠杆菌W3110出发,通过引入解淀粉芽孢杆菌嘌呤操纵子,阻断生成GMP的分支途径,敲除purR解除PRPP合成酶和PRPP转酰胺酶表达的反馈阻遏效应,敲除黄苷到黄嘌呤的分解途径(图1),构建了1株无质粒的高产黄苷的工程菌株。
1 材料与方法
1.1 材料
1.1.1 菌株与质粒
本研究所用菌株与质粒见表1。
表1 本研究所用的菌株和质粒
Table 1 Strains and plasmids used in this study

续表1

菌株/质粒特征来源pGRB-rphpGRB derivative expressing gRNA targeting the rph pseudogene本研究pGRB-ycgHpGRB derivative expressing gRNA targeting the ycgH pseudogene本研究pGRB-yjiVpGRB derivative expressing gRNA targeting the yjiV pseudogene本研究pGRB-yghXpGRB derivative expressing gRNA targeting the yghX pseudogene本研究pGRB-ppnPpGRB derivative expressing gRNA targeting the ppnP gene本研究pGRB-deoDpGRB derivative expressing gRNA targeting the deoD gene本研究
1.1.2 培养基
LB液体培养基(g/L):酵母粉5,蛋白胨10,NaCl 10。
LB固体培养基(g/L):酵母粉5,蛋白胨10,NaCl 10,琼脂粉20。
2-酵母粉-胰蛋白胨(yeast extract-tryptone,YT)液体培养基(g/L):蛋白胨16,酵母粉10,NaCl 5。
SOC培养基(g/L):蛋白胨20,酵母粉5,NaCl 20,0.25 mmol/L KCl 10 mL,10 mmol/L MgCl2 20 mL,20 mmol/L葡萄糖20 mL。
其中LB液体培养基用于菌株的培养,LB固体培养基用于菌株的筛选(如有需要添加100 μg/mL奇霉素或者100 μg/mL氨苄青霉素);2-YT液体培养基用于感受态制备,制备过程中当OD值=0.1时加入0.2 mmol/L的IPTG溶液;SOC培养基用于电转化之后的复苏培养。
摇瓶种子培养基(g/L):葡萄糖30,酵母粉5,蛋白胨1,柠檬酸1.25,MgSO4·7H2O 1.5,KH2PO4 3.0,维生素B1 0.001,生物素0.001,鸟嘌呤0.2,苯酚红溶液2%(体积分数,下同)。
摇瓶发酵培养基(g/L):葡萄糖30,酵母粉3,蛋白胨1,柠檬酸2,MgSO4·7H2O 2,KH2PO4 6,FeSO4·7H2O 0.02,MnSO4 0.01,维生素B1 0.002,生物素0.002,鸟嘌呤0.2,苯酚红溶液2%。
斜面培养基(用于发酵罐菌种的活化)(g/L):牛肉膏10,葡萄糖5,NaCl 5,蛋白胨10,酵母粉5,鸟嘌呤0.1,琼脂粉25。
发酵罐种子培养基(g/L):葡萄糖30,酵母粉5,蛋白胨1,柠檬酸1.25,MgSO4·7H2O 1.5,KH2PO4 3.0,维生素B1 0.001,生物素0.001,鸟嘌呤0.2。
发酵罐发酵培养基(g/L):葡萄糖20,酵母粉3,蛋白胨1,柠檬酸2,MgSO4·7H2O 2,KH2PO4 6,FeSO4·7H2O 0.02,MnSO4 0.01,维生素B1 0.002,生物素 0.002,鸟嘌呤0.2。
1.1.3 主要试剂
Primer STAR HS DNA Polymerase,TaKaRa公司;2×Taq Master Mix、ClonExpress II(重组酶),诺唯赞生物科技有限公司;质粒提取试剂盒、DNA直接回收试剂盒、DNA凝胶回收试剂盒,美国Omega Bio-TeK公司;氨苄青霉素、奇霉素、阿拉伯糖、IPTG,上海源叶生物科技有限公司。
1.2 菌株构建方法
本研究对大肠杆菌的改造均在基因组水平进行,基因编辑技术采用LI等[18]报道的CRISPR/Cas9基因编辑方法。该方法为pREDCas9和pGRB双质粒系统:温敏型pREDCas9质粒包含Cas9表达框、IPTG诱导的Redαβγ重组酶表达元件和阿拉伯糖诱导的靶向并切割pGRB质粒的gRNA表达元件;pGRB质粒表达靶向基因组目标位点的gRNA。具体工作流程为首先将pREDCas9质粒导入菌株并制备感受态细胞,该过程添加IPTG诱导重组酶表达;然后将携带gRNA表达框的pGRB质粒和双链DNA片段一起电转入上述感受态细胞中,涂布平板培养基;其次通过菌落PCR筛选编辑菌株并测序确定;之后,将上述的菌株接入含有12 mmol/L阿拉伯糖的LB摇管中培养,消除pGRB质粒,然后在42 ℃培养消除pREDCas9质粒。表达gRNA的pGRB质粒构建:根据Cas-Designer在线工具(http://www.rgenome.net/cas-designer/)设计gRNA编码序列,两端添加与pGRB线性载体两测同源的序列,委托金唯智公司合成,利用ClonExpress II试剂盒完成质粒构建。双链DNA片段的构建通过重叠PCR完成。嘌呤操纵子purEKBCSQLFMNHD扩增于B.subtilis 168野生型菌株的基因组DNA,分5个片段依次进行基因组整合。本研究所用引物和编码gRNA的寡核苷酸序列见电子版增强出版附表1(https://doi.org/10.13995/jcnki.11-1802/ts.043150)。
1.3 菌株发酵实验
1.3.1 摇瓶发酵
菌株在37 ℃的LB摇管中培养12 h后,将菌液全部转移至装有30 mL种子培养基的摇瓶中,置于摇床在220 r/min、37 ℃下培养10 h,种子培养基以10%的接种量接种于发酵培养基中,相同条件下培养24 h。发酵培养基中添加了苯酚红指示剂,通过补加25%(体积分数)的氨水调控pH值稳定在7.0~7.2。当发酵培养基的颜色持续15 min不变时说明葡萄糖已耗尽,此时补加1 mL 600 g/L葡萄糖。
1.3.2 发酵罐发酵
种子培养:菌株在37 ℃的斜面培养基上培养超过12 h,使用无菌水将斜面上的菌体全部洗脱并接种于装有种子培养基的5 L发酵罐中(总体积为2 L),通过自动流加25%(体积分数)氨水溶液维持pH值在7.0左右;通过调节搅拌转速与通气量控制溶氧(dissolved oxygen,DO)在30%以上;培养温度恒定为37 ℃。
发酵阶段:当种子培养液OD值达到10左右时,保留20%的种子液,将发酵培养基加入发酵罐内(总体积3 L),通过自动添加25%(体积分数)氨水维持pH值在7.0左右,通过调节搅拌转速与通气量确保DO值在30%以上。当葡萄糖耗尽时,以800 g/L葡萄糖溶液进行补料,通过DO控制法来调节补糖速率。
1.4 分析方法
1.4.1 菌体生物量测定
采用分光光度计测定600 nm波长下的OD值,测量时需要稀释发酵液使OD值在0.2~0.8。
1.4.2 黄苷检测
摇瓶发酵周期为24 h,发酵结束后取样。在5 L发酵罐发酵过程中,每隔2 h取样。将菌液以12 000 r/min离心3 min。取上清液,进行适当稀释,然后经0.22 μm膜过滤。采用Thermo U3000高效液相色谱仪进行检测。色谱柱:Titank C18柱(250 mm×4.60 mm,5 μm);流动相:2%(体积分数)乙腈+0.5%(体积分数)三氟乙酸水溶液;柱温30 ℃;流速1 mL/min;紫外检测波长260 nm;进样量20 μL。
2 结果与分析
2.1 增强前体物甘氨酸、L-天冬氨酸和CO2供应
本实验以ΔlacI的大肠杆菌W3110(命名为XL0)为出发菌株进行改造。甘氨酸、L-天冬氨酸以及CO2是嘌呤核苷合成途径的前体物质,增强前体物的供应预期有助于提高嘌呤核苷的合成效率。为了增强前体物甘氨酸、L-天冬氨酸以及CO2的供应,依次过表达glyA基因(丝氨酸强甲基转移酶)、aspA基因(天冬氨酸酰化酶)和can基因(碳酸酐酶),得到菌株XL1、XL2、XL3。
2.2 敲除支路代谢途径
在嘌呤核苷的合成途径中,合成黄苷的前体XMP还可由鸟嘌呤核苷酸合成酶催化生成GMP,进而生成鸟苷及下游产物,影响黄苷的合成。为阻断XMP到GMP的支路代谢,在菌株XL3中敲除guaA基因获得菌株XL4。对菌株XL1、XL2、XL3、XL4进行摇瓶测试,并未在这些菌株的发酵液中检测到黄苷。
2.3 增强PRPP供应
PRPP是嘌呤核苷合成代谢的另一个重要前体,虽然前面强化了前体物甘氨酸、L-天冬氨酸以及CO2的供应,但菌株并未向胞外分泌黄苷,推测PRPP的供应可能为限制因素。PRPP合成酶受到嘌呤核苷酸的反馈抑制,通过过表达解除反馈抑制的PRPP合成酶的突变体基因prsEcoD128A[13],构建了菌株XL5。其次,PRPP合成酶基因prs受到PurR蛋白的反馈阻遏[9],我们敲除purR基因获得菌株XL6。
对XL4、XL5和XL6菌株进行摇瓶测试。经24 h发酵后,菌体生物量(OD值)和黄苷产量如图2所示。从图2可知,当过表达解除反馈抑制的PRPP合成酶后,菌株XL5胞外积累少量黄苷。在敲除purR后,黄苷产量达到1.05 g/L,为菌株XL5的20倍。菌株XL5已经过表达了解除反馈抑制的PRPP合成酶,尽管敲除purR基因可以解除本身prs基因的反馈阻遏,但是XL6菌株黄苷产量的大幅提升出乎我们的意料。由文献[9]可知除了prs基因,嘌呤核苷操纵子的基因也受到PurR蛋白的反馈阻遏。敲除purR后,嘌呤核苷操纵子基因(图1)的转录增强,这可能是导致XL6菌株黄苷产量大幅增加的主要原因。
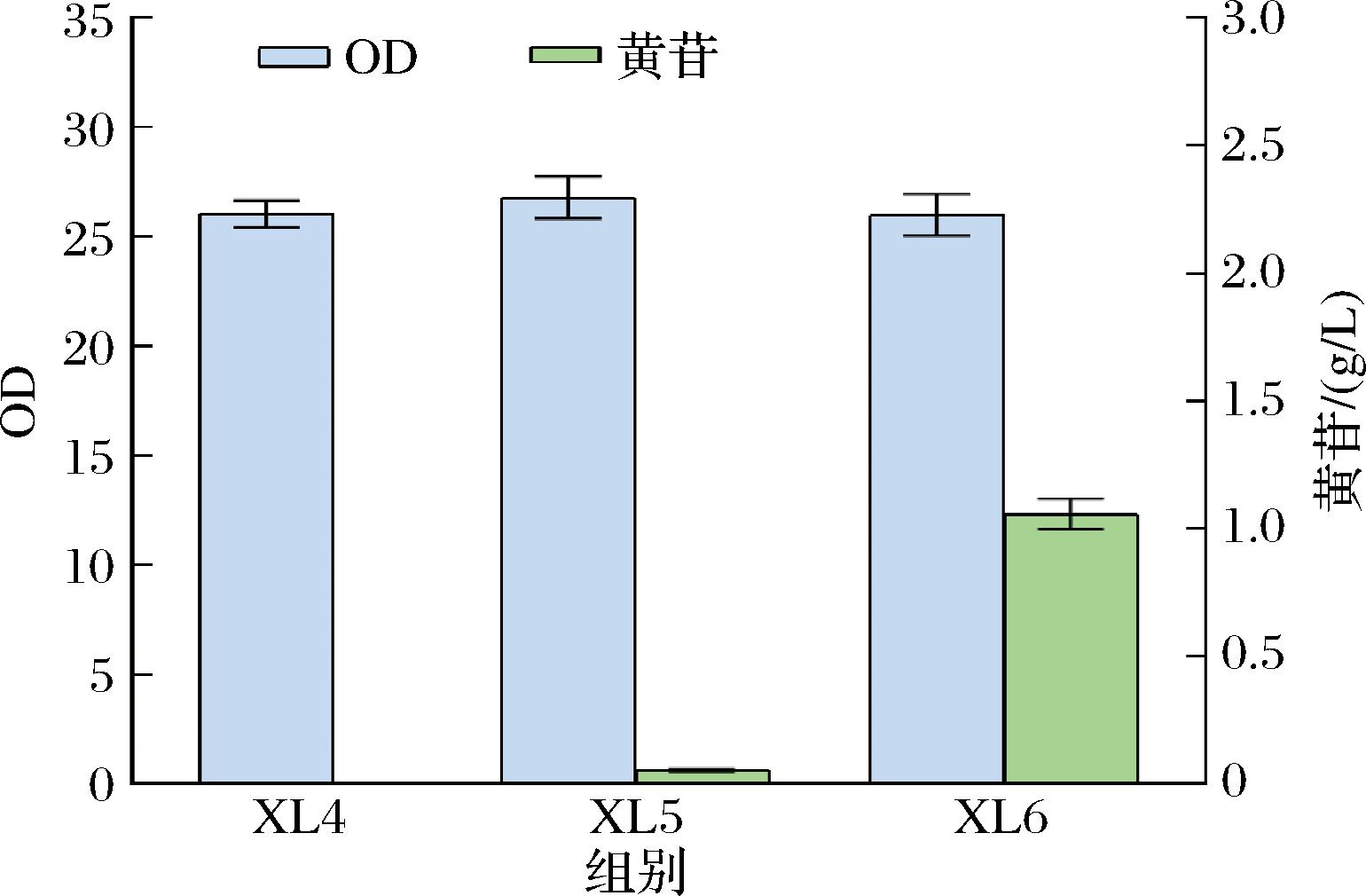
图2 摇瓶发酵XL4、XL5和XL6菌株的OD值和黄苷产量
Fig.2 The OD value and xanthosine production of strains XL4, XL5, and XL6 in shake-flask fermentation
PRPP转酰胺酶催化嘌呤核苷合成途径的第一步反应,其受到嘌呤核苷的反馈抑制,为嘌呤核苷从头合成的限速酶。SHIMAOKA等[13]发现purFBazK326Q突变体编码的PRPP转酰胺酶解除了嘌呤核苷的反馈抑制。我们过表达了解淀粉芽孢杆菌来源的purFBazK326Q,获得菌株XL7。其黄苷产量为1.43 g/L,较菌株XL6提升了36.19%(图3),说明该反应对嘌呤核苷的合成确实非常重要。由于PRPP是PRPP转酰胺酶催化的底物,接下来我们继续尝试增强其供应。PP途径中的核糖-5-磷酸是合成PRPP的直接前体。为增强PP途径的代谢流,我们在菌株XL7的基础上过表达6-磷酸葡萄糖脱氢酶编码基因zwf,得到菌株XL8。另外,PP途径的戊糖也可以通过转酮醇酶(tktA基因编码)催化果糖-6-磷酸和甘油醛-3-磷酸合成,我们进一步过表达tktA基因构建了菌株XL9。摇瓶发酵结果表明,在过表达基因zwf后,菌株XL8的黄苷产量达到1.92 g/L,较菌株XL7提高了34.27%,同时OD值也提高了13.28%。在过表达转酮醇酶基因tktA后,黄苷产量达到2.28 g/L,较XL8菌株提升了18.75%(图3)。这些结果表明通过增强PP途径和转酮醇酶进一步强化PRPP的供应,显著提高了黄苷的产量。
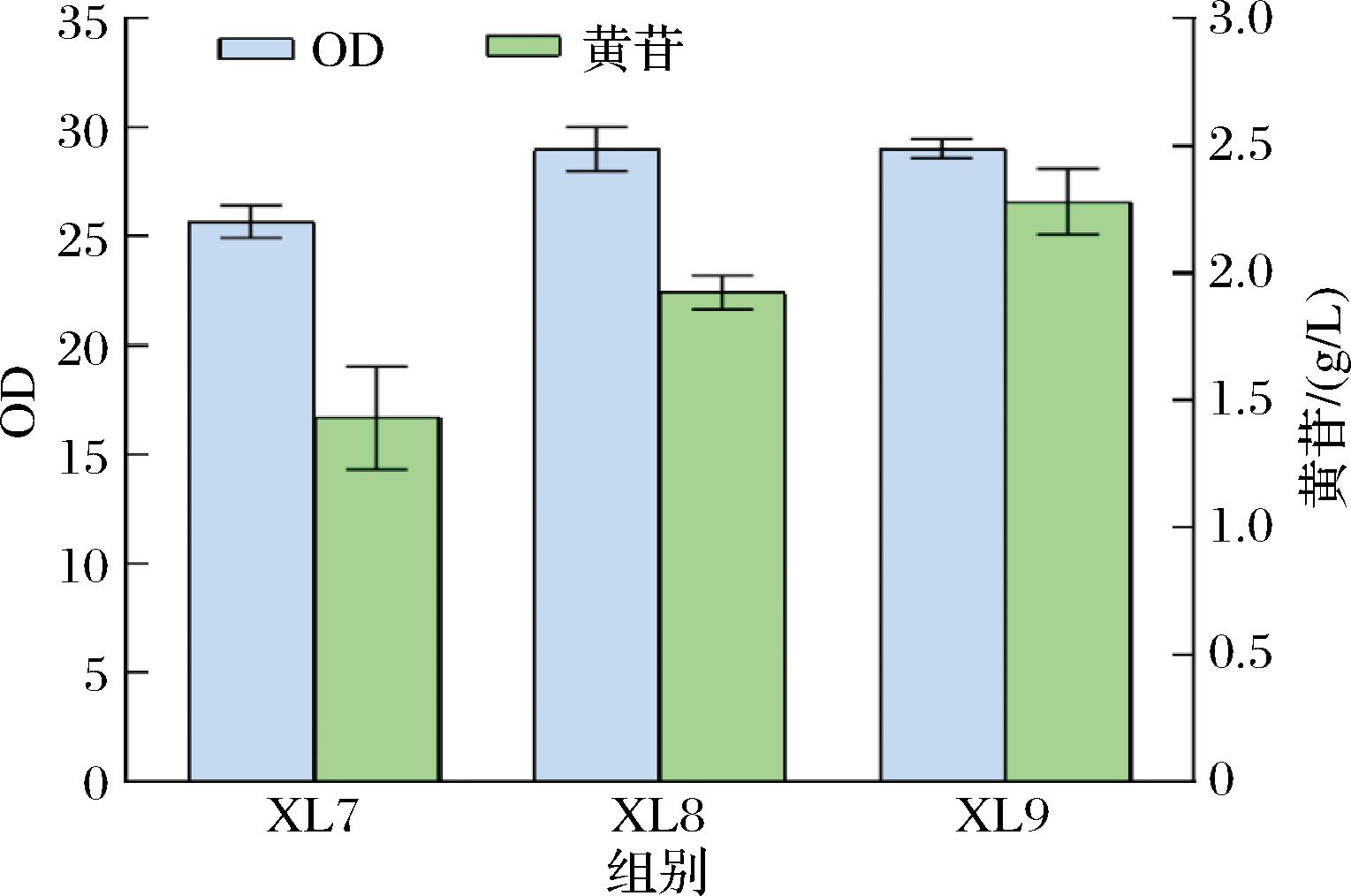
图3 摇瓶发酵XL7、XL8和XL9菌株的OD值和黄苷产量
Fig.3 The OD value and xanthosine production of XL7, XL8, and XL9 in shake-flask fermentation
2.4 强化嘌呤核苷合成途径
在芽孢杆菌中,嘌呤核苷合成的关键基因以天然操纵子的结构形式存在[6],引入天然操纵子结构增强嘌呤核苷合成的策略,既操作简便,同时保留了细菌长期进化形成的多酶表达平衡系统。我们引入B.subtilis 168菌株的嘌呤操纵子purEKBCSQLFMNHD,构建了菌株XL10。从摇瓶发酵结果可知,其黄苷产量为2.85 g/L,较XL9提升了25.00%(图4)。这与朱彦凯等[7]和梅漫莉[8]在肌苷和腺苷研究中的结果一致。
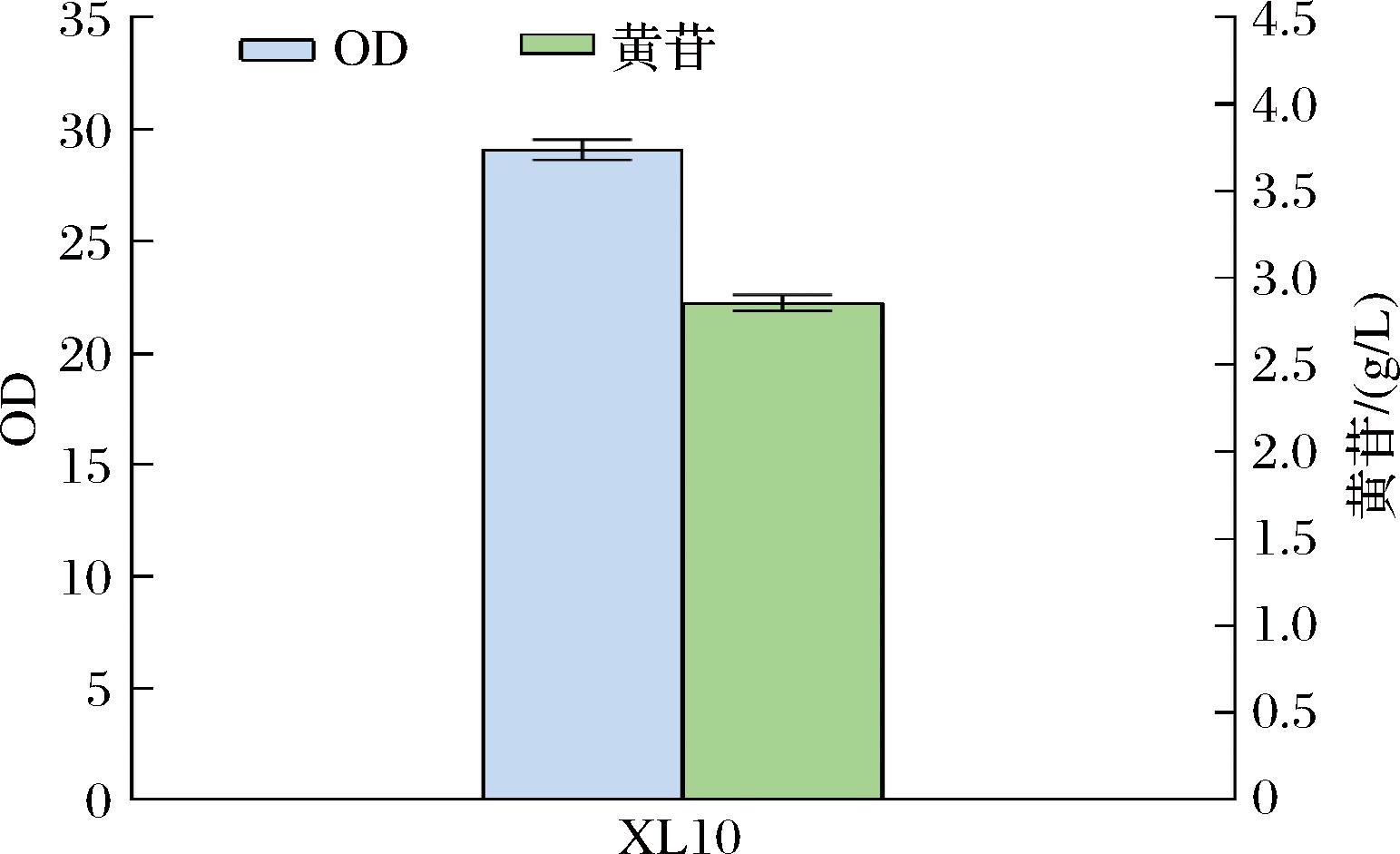
图4 摇瓶发酵XL10菌株的OD和黄苷产量
Fig.4 The OD and xanthosine production of XL10 in shake-flask fermentation
2.5 阻断黄苷分解途径
在大肠杆菌中,黄苷经嘌呤核苷分解酶和嘌呤核苷磷酸化酶分解为黄嘌呤。为阻断黄苷的分解途径,依次敲除嘌呤核苷分解酶编码基因ppnP和嘌呤核苷磷酸化酶基因deoD,获得菌株XL11和菌株XL12。
将菌株XL11和XL12进行摇瓶发酵,结果如图5所示,在敲除嘌呤核苷分解酶的编码基因ppnP后,黄苷产量为3.50 g/L,较XL10提升了22.82%;在敲除嘌呤核苷磷酸化酶基因deoD后,黄苷产量达到4.00 g/L,较XL11提升了14.29%。这表明了敲除deoD和ppnP基因减弱黄苷到黄嘌呤的分解,显著提高了黄苷的产量。
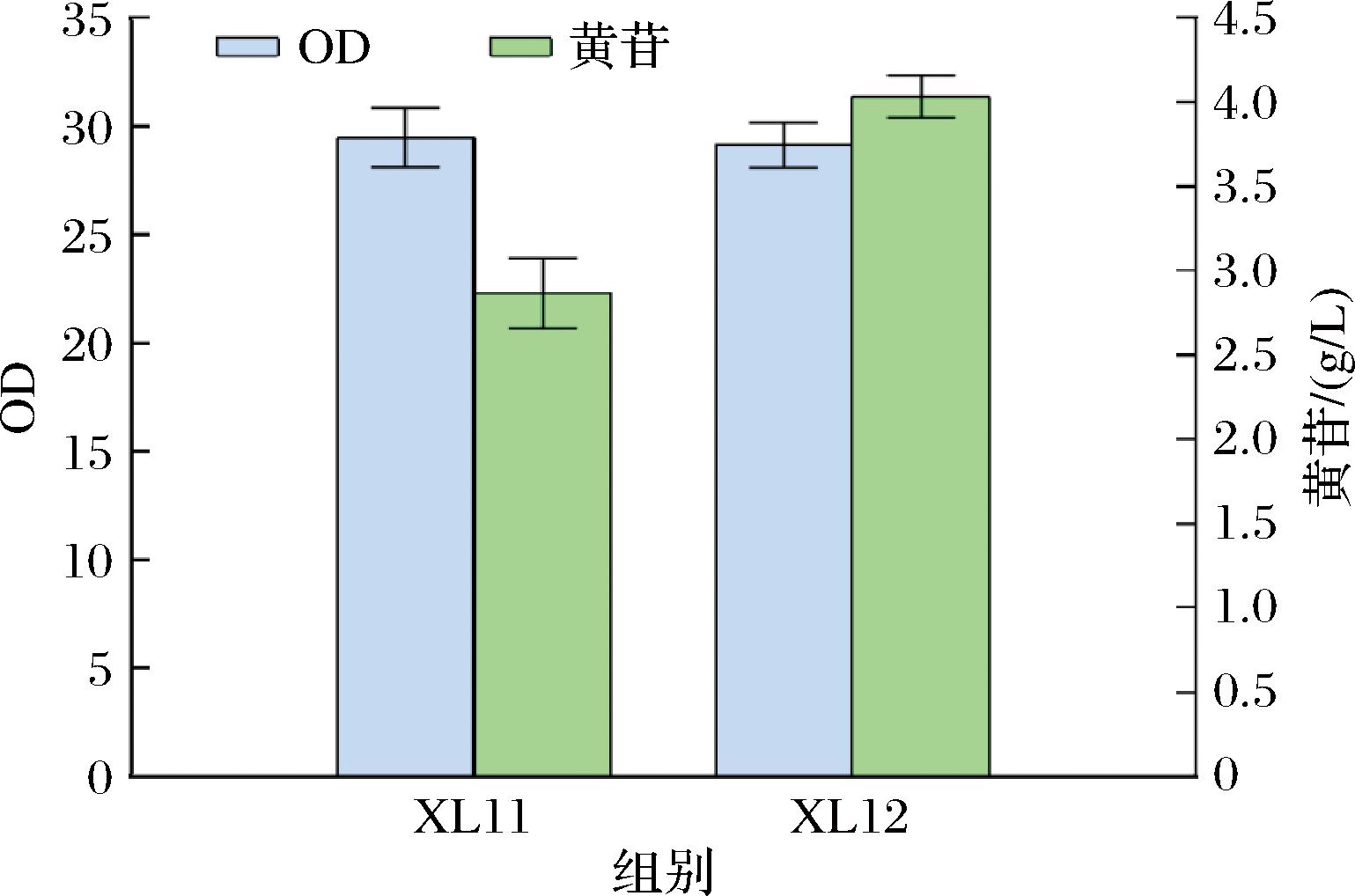
图5 摇瓶发酵XL11和XL12菌株的OD和黄苷产量
Fig.5 The OD and xanthosine production of XL11 and XL12 in shake-flask fermentation
2.6 5 L发酵罐测试
对XL12菌株进行5 L发酵罐测试。发酵初始葡萄糖质量浓度为20 g/L,发酵6.25 h时耗尽。之后采用DO控制策略维持葡萄糖质量浓度在2 g/L以下。如图6所示,发酵过程中通过控制通风速率和搅拌转速维持DO值在30%以上。菌株在发酵初期OD值稳定生长,至28 h时达到最高值60.5。黄苷的产量随着OD值的增长而不断增加,在26 h时达最高值10.25 g/L。
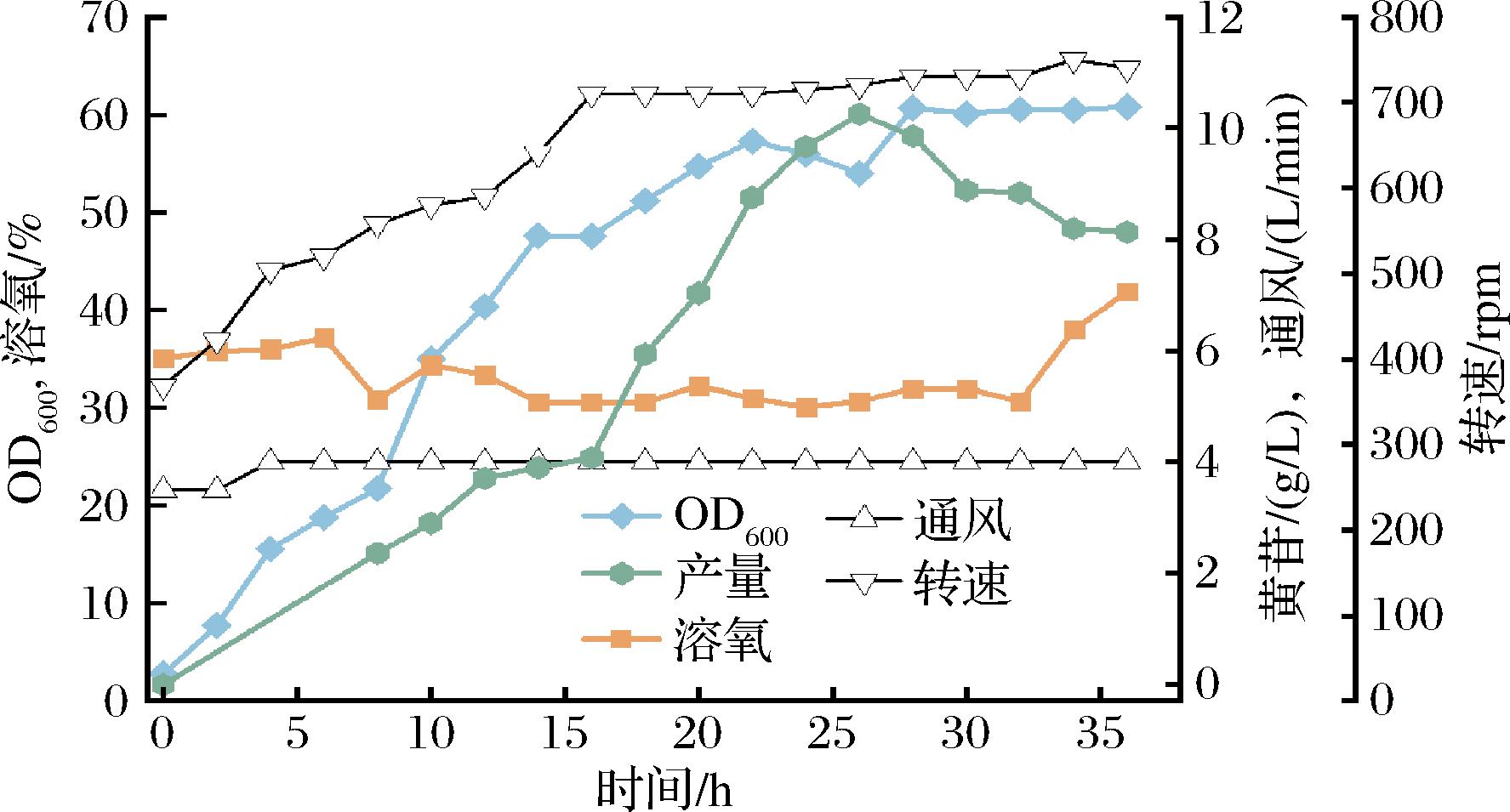
图6 5 L发酵罐验证菌株XL12的发酵性能
Fig.6 Fermentation performance of the strain XL12 in a 5 L bioreactor
3 结论
本研究通过系统性代谢工程改造,构建了1株高产黄苷的大肠杆菌工程菌株。通过加强前体物供给、解除反馈抑制、加强嘌呤核苷合成途径并阻断生成GMP的分支途径,逐步提高了大肠杆菌的黄苷产量。最终改造菌株XL12在5 L发酵罐中黄苷产量达到10.25 g/L。目前通过化学法进行黄苷的工业化生产,尚未见微生物发酵法生产黄苷的报道,但随着市场需求的增加,开发生物合成方法替代化学合成为未来的发展趋势。另外,目前已经采用发酵法生产其他嘌呤核苷如腺苷、肌苷和鸟苷,所用的菌株多为芽胞杆菌。与芽胞杆菌相比,大肠杆菌遗传背景更清楚、遗传工具更成熟,且所需培养基营养简单、发酵周期短,本研究采用大肠杆菌进行黄苷合成的研究。通常认为芽胞杆菌适合生产核苷类产品的原因是其具有较强的PP途径,本研究发现增强重要前体物PRPP的供给能够有效提升大肠杆菌的黄苷产量。本实验不足之处是为了阻断XMP到GMP的支路代谢,敲除了guaA基因失活GMP合成酶,使得菌株为鸟嘌呤营养缺陷型,在发酵过程中需要添加鸟嘌呤才能正常生长。后续可利用GMP合成酶的弱化突变体或者开发弱化表达策略,消除菌株对外源添加物的依赖,降低发酵成本。
[1] 刘芳, 陈少红, 刘青波, 等.黄嘌呤核苷促进骨髓间质干细胞体外快速扩增的实验研究[J].中国病理生理杂志, 2010, 26(12):2389-2393.
LIU F, CHEN S H, LIU Q B, et al.Rapid proliferation of bone marrow mesenchymal stem cells enhanced by xanthosine[J].Chinese Journal of Pathophysiology, 2010, 26(12):2389-2393.
[2] 闫振, 黄健垚, 高路, 等.茶树体内咖啡碱生物代谢研究进展[J].中国茶叶, 2020, 42(7):1-7.
YAN Z, HUANG J Y, GAO L, et al.Research progress of caffeine biological metabolism in tea plant[J].China Tea, 2020, 42(7):1-7.
[3] LIU M, FU Y X, GAO W J, et al.Highly efficient biosynthesis of hypoxanthine in Escherichia coli and transcriptome-based analysis of the purine metabolism[J].ACS Synthetic Biology, 2020, 9(3):525-535.
[4] 刘铁重, 高志强, 侯德欣, 等.大肠杆菌肌苷酸节点代谢优化高效合成肌苷[J].食品与发酵工业, 2024, 50(4):44-50.
LIU T Z, GAO Z Q, HOU D X, et al.Inosinic acid node metabolism optimization for efficient synthesis of inosine in Escherichia coli[J].Food and Fermentation Industries, 2024, 50(4):44-50.
[5] 邓爱华, 温廷益, 陈振翔, 等.发酵生产嘌呤核苷的重组菌及其构建方法与应用:中国, CN113583929A[P].2021-11-02.
DENG A H, WEN T Y, CHEN Z X, et al.Recombinant strain for fermentative production of purine nucleosides, construction method and application thereof:China, CN113583929A[P].2021-11-02.
[6] EBBOLE D J, ZALKIN H.Cloning and characterization of a 12-gene cluster from Bacillus subtilis encoding nine enzymes for de novo purine nucleotide synthesis[J].The Journal of Biological Chemistry, 1987, 262(17):8274-8287.
[7] 朱彦凯, 刘铁重, 伍法清, 等.代谢工程改造大肠杆菌生产肌苷[J].食品与发酵工业, 2022, 48(24):1-9.
ZHU Y K, LIU T Z, WU F Q, et al.Metabolic engineering of Escherichia coli for inosine production[J].Food and Fermentation Industries, 2022, 48(24):1-9.
[8] 梅漫莉. 腺苷工程菌的构建及其发酵过程控制[D].天津:天津科技大学, 2021.
MEI M L.Construction of adenosine engineering bacteria and its fermentation process control[D].Tianjin:Tianjin University of Science and Technology, 2021.
[9] RODIONOVA I A, GAO Y, SASTRY A, et al.Identification of a transcription factor, PunR, that regulates the purine and purine nucleoside transporter punC in E.coli[J].Communications Biology, 2021, 4:991.
[10] WILSON H R, TURNBOUGH C L Jr.Role of the purine repressor in the regulation of pyrimidine gene expression in Escherichia coli K-12[J].Journal of Bacteriology, 1990, 172(6):3208-3213.
[11] MATSUI H, KAWASAKI H, SHIMAOKA M, et al.Investigation of various genotype characteristics for inosine accumulation in Escherichia coli W3110[J].Bioscience, Biotechnology, and Biochemistry, 2001, 65(3):570-578.
[12] ASAHARA T, MORI Y, ZAKATAEVA N P, et al.Accumulation of gene-targeted Bacillus subtilis mutations that enhance fermentative inosine production[J].Applied Microbiology and Biotechnology, 2010, 87(6):2195-2207.
[13] SHIMAOKA M, TAKENAKA Y, KURAHASHI O, et al.Effect of amplification of desensitized purF and prs on inosine accumulation in Escherichia coli[J].Journal of Bioscience and Bioengineering, 2007, 103(3):255-261.
[14] 刘万红, 刘爱福.glyA基因及其编码的丝氨酸羟甲基转移酶[J].氨基酸和生物资源, 2001, 23(2):13-16;21.
LIU W H, LIU A F.GlyA gene and serine hydroxymethyltransferase encoded by GlyA gene[J].Amino Acids &Biotic Resources, 2001, 23(2):13-16;21.
[15] 潘富军, 周作明.碳酸酐酶固定化技术研究与应用进展[J].化学工程, 2014, 42(3):11-17;58.
PAN F J, ZHOU Z M.Research and application progress of carbonic anhydrase-immobilized technology[J].Chemical Engineering (China), 2014, 42(3):11-17;58.
[16] 刘铁重. 优化大肠杆菌中肌苷酸节点提升肌苷产量[D].天津:天津科技大学, 2023.
LIU T Z.Optimization of inosinic acid node in Escherichia coli to increase inosine production[D].Tianjin:Tianjin University of Science and Technology, 2023.
[17] 徐庆阳, 李良文, 陈志超, 等.一种鸟苷生产菌株及其构建方法与应用:中国, 202410465797.6[P].2024-07-09.
XU Q Y, LI L W, CHEN Z C, et al.A guanosine-producing strain and its construction method and application:China, 202410465797.6[P].2024-07-09.
[18] LI Y F, LIN Z Q, HUANG C, et al.Metabolic engineering of Escherichia coli using CRISPR-Cas9 meditated genome editing[J].Metabolic Engineering, 2015, 31:13-21.