特应性皮炎(atopic dermatitis,AD)是一种以慢性复发性湿疹样皮损、皮肤屏障功能障碍和剧烈瘙痒为特征的2型免疫相关炎症性皮肤病。AD不仅显著降低患者生存质量,更与过敏性鼻炎、哮喘等2型免疫相关疾病呈现显著临床共现性,提示其具有系统性免疫紊乱特征[1-3]。尽管AD的精确发病机制尚未完全阐明,但目前研究已揭示遗传易感性、免疫调节异常、表皮屏障缺陷、环境因素以及皮肤菌群紊乱等多因素共同参与疾病进程[4-6]。其中,皮肤微生物组失衡(如金黄色葡萄球菌异常定植伴随菌群多样性降低)已被证实可直接诱发皮肤免疫炎症反应[7]。
近年来研究热点逐步延伸至肠道微生物与AD的潜在关联。肠道菌群及其代谢产物不仅参与宿主免疫系统发育,更通过肠-皮肤轴发挥系统性免疫调节功能[8-10]。值得注意的是,婴幼儿期作为肠道菌群定植与功能成熟的关键窗口期,母乳喂养不足、环境微生物暴露缺乏、抗生素滥用等因素导致的菌群失衡,与儿童过敏性疾病(包括AD)发病率升高显著相关[11-12]。临床研究证实,AD患儿肠道菌群呈现特征性改变:双歧杆菌等有益菌丰度降低,肠杆菌等条件致病菌相对丰度升高,导致菌群稳态指数(有害菌/有益菌比率)显著失调[13-14]。
益生元作为不可消化的膳食成分,可通过选择性促进宿主有益菌增殖来改善肠道微生态平衡。相较于单一益生元,复合益生元作为多组分协同体系,能够通过多靶点作用选择性促进多种益生菌增殖,具体机制包括:调节肠道局部pH值、竞争性抑制病原体定植、提供特异性代谢底物等[15-18]。此外,益生元还可增强肠道上皮屏障完整性,降低微生物易位风险,同时通过调节树突状细胞成熟和T细胞分化等免疫机制,发挥系统性抗炎作用[19-20]。
本研究基于靶向调控原理,构建由低聚果糖(fructooligosaccharides,FOS)、低聚半乳糖(galactooligosaccharides,GOS)、低聚木糖(xylooligosaccharides,XOS)及菊粉组成的复合益生元体系。各组分通过差异化机制调控2型免疫反应:FOS通过选择性富集双歧杆菌属并促进丁酸合成,经组蛋白去乙酰化酶(histone deacetylase, HDAC)抑制通路阻遏Th2细胞分化[21];GOS介导调节性T细胞(regulatory T cells, Treg)扩增,重建Th2/Treg动态平衡[22]。进一步研究发现,XOS依赖阿克曼菌(Akkermansia muciniphila)与Toll样受体4(Toll like receptors, TLR4)信号互作,抑制树突状细胞成熟活化[21],而菊粉通过其代谢产物丙酸盐激活G蛋白偶联受体41(G protein-coupled receptors, GPR41),调控巨噬细胞IL-10/IL-33分泌平衡[23]。这些差异化作用模式的交叉整合提示,复合益生元可能通过多靶点协同产生“1+1>2”的免疫调节效应。
当前研究多局限于单一益生元的线性作用模式,而对复合体系中各组分间相互作用动力学(如代谢物交叉调控、菌群互养网络形成等)缺乏系统解析。借助多组学整合分析手段,全面揭示复合益生元的协同作用机制,将成为开发精准微生态干预策略的关键。
基于肠道微生物与AD的复杂关联网络,以及复合益生元在微生态调控方面的独特优势,本研究创新性采用复合益生元协同干预策略,系统评价其对AD小鼠模型的治疗效应。通过整合肠道菌群分析、皮肤病理评估和免疫指标检测,深入解析菌群-免疫-皮肤轴的调控机制。研究结果不仅为AD治疗提供新范式,还将深化对肠-皮肤轴互作机制的理解,为过敏性疾病微生态疗法的开发奠定理论基础。
1 材料与方法
1.1 材料与仪器
2,4-二硝基氟苯(2,4-dinitrofluorobenzene,DNFB)、富马酸酮替芬盐(阳性药物),美国Sigma-Aldrich公司;小鼠血清免疫球蛋白E(immunoglobulin E,IgE)、炎症因子检测试剂盒,美国R&D公司;BCA蛋白定量检测试剂盒、蛋白酶抑制剂,上海碧云天生物技术有限公司;橄榄油、丙酮、NaCl,国药集团化学试剂有限公司;FOS(纯度99%)、GOS(纯度70%)、XOS(纯度95%)、菊粉(纯度90%),上海博飞美科化学科技有限公司。
SX-300高压蒸汽灭菌锅,日本Tomy公司;GR60DA立式自动压力蒸汽灭菌器,致微(厦门)仪器有限公司;PANNORMIC MIDI数字切片扫描仪,匈牙利3DHistech有限公司。
1.2 实验动物设计
将40只6周龄、体重在18~20 g的SPF级雌性C57BL/6J小鼠随机分配为8组,每组5只,组别包括空白组、模型组、阳性药物组、FOS组、GOS组、XOS组、菊粉组和益生元组。实验用小鼠饲养于江南大学实验动物中心,饲养条件为室温维持在24~26 ℃,相对湿度控制在40%~70%,噪音水平不超过60 dB,光照强度为15~20 lx,并且维持12 h的昼夜循环。实验周期内,小鼠食用标准商业饲料,可自由进食和饮水。所有动物实验均获得江南大学动物福利与伦理管理委员会的审批,伦理审批编号为JN.No20230615c0960729[283]。
本实验共计28 d,前7天为适应期,从第8天开始每天进行干预,直至实验结束,干预方式如表1所示。
表1 动物分组信息
Table 1 Animal grouping information
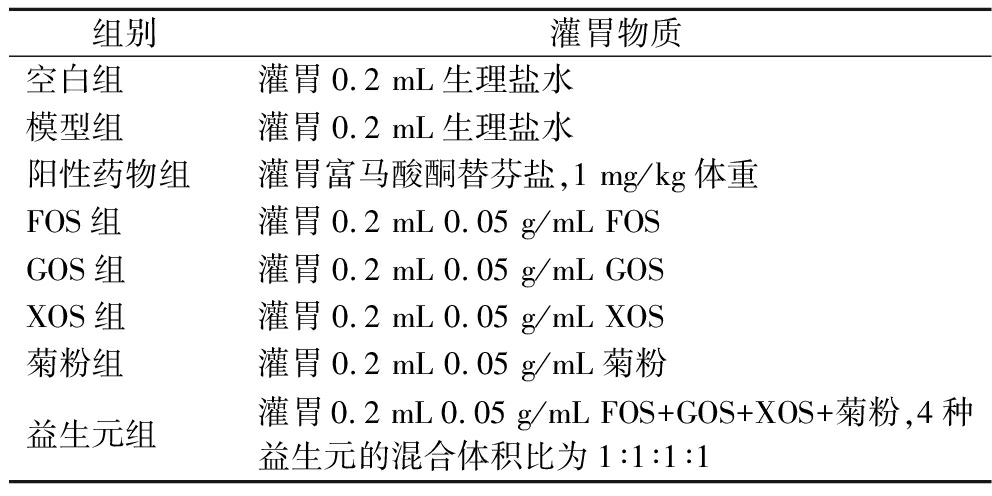
组别灌胃物质空白组灌胃0.2 mL生理盐水模型组灌胃0.2 mL生理盐水阳性药物组灌胃富马酸酮替芬盐,1 mg/kg体重FOS组灌胃0.2 mL 0.05 g/mL FOSGOS组灌胃0.2 mL 0.05 g/mL GOSXOS组灌胃0.2 mL 0.05 g/mL XOS菊粉组灌胃0.2 mL 0.05 g/mL菊粉益生元组灌胃0.2 mL 0.05 g/mL FOS+GOS+XOS+菊粉,4种益生元的混合体积比为1∶1∶1∶1
AD小鼠造模流程如图1所示,用剃毛器将小鼠背部皮肤毛发剃去。将DNFB与底物溶液(丙酮和橄榄油的体积比为4∶1)混合,制成致敏溶液(体积分数分别为0.5%和0.2%)。第15天,将25 μL体积分数为0.5% DNFB溶液涂于小鼠刮过毛的背部皮肤和左耳上。然后,在相同的地方用20 μL体积分数为0.2%DNFB溶液涂抹,在第19、22、25、28天诱导AD症状,空白组小鼠涂抹等量的基础液。当造模组小鼠背部皮损出现严重的结痂、脱落,其后转变为鳞屑、疤痕,同时造模组小鼠耳朵逐渐变硬,厚度增加,则证明AD模型造模成功[18],涂抹DNFB后,模型组和干预组小鼠均出现严重的AD样皮损症状,造模成功率为100%。第29天采用体积分数为1%~1.5%异氟烷吸入麻醉,对小鼠进行眼部静脉丛取血,取血后,辅以颈椎脱臼法处死小鼠,并对小鼠进行解剖收集样本。

图1 AD造模流程图
Fig.1 Atopic dermatitis modeling flow chart
1.3 小鼠耳朵厚度的测定
在实验第28天,用游标卡尺测量小鼠左耳厚度,并记录。
1.4 小鼠血清总IgE及炎症因子测定
取小鼠血清及皮肤组织制备匀浆样本,严格遵循
酶联免疫吸附测定试剂盒说明书进行操作。定量检测血清IgE水平,以及皮肤组织中IL-4、IL-5、IL-13、胸腺基质淋巴生成素(thymic stromal lymphopoietin,TSLP)和IFN-γ浓度。采用外标法建立标准曲线(R2≥0.99),通过酶标仪于450 nm波长下测定各孔吸光度值,依据标准曲线方程计算目标物浓度。
1.5 小鼠背部病理症状评价
实验动物经体积分数为1%~1.5%的异氟烷吸入麻醉后,无菌采集脱毛区域皮肤组织,立即置于体积分数为4%的多聚甲醛固定液中固定。经梯度乙醇脱水、二甲苯透明处理后,石蜡包埋制成组织块。使用旋转式切片机将样本连续切片(厚度5 μm),60 ℃烘片2 h后,进行苏木精-伊红(hematoxylin-eosin,HE)染色。由专业病理医师采用双盲法评估组织病理学特征。
1.6 小鼠背部皮肤肥大细胞浸润
将5 μm厚的切片经过烤片、系列酒精脱水之后,采用对肥大细胞颗粒进行特异性染色。每张切片于400倍光学显微镜下随机选取3个非重叠视野,统计单位面积(mm2)内特异性染色阳性细胞数,取平均值作为最终检测结果。
1.7 小鼠肠道菌群测定
按照DNA提取试剂盒操作说明,提取粪便菌群的DNA。使用引物(341F:5′-CCTAYGGGRBGCASCAG-3′, 806R:5′-GGACTACNNGGGTATCTAAT-3′)进行V3-V4区PCR扩增,PCR条件:1)95 ℃初始变性5 min;2)95 ℃变性30 s;3)52 ℃退火30 s;4)72 ℃延伸30 s,步骤2)~4)重复30个循环;5)72 ℃维持10 min;6)12 ℃维持10 min,同时设置1组以去离子无菌水为模板的阴性对照。通过凝胶电泳纯化DNA,用DNA凝胶回收试剂盒回收PCR产物(465 bp),所有纯化的DNA样本使用Illumina测序平台进行测序,最后用QIIME2中的DADA2包进行下机数据处理和质量控制。β-多样性使用未加权Unifrac距离(unweighted Unifrac distance)计算,并在联川生物云平台(https://www.omicstudio.cn/tool)上进行主坐标分析(principal coordinates analysis,PCoA)图的可视化。线性判别分析效应大小(linear discriminant analysis effect size,LEfSe)分析在微科盟生科云(https://www.bioincloud.tech)上进行,并基于线性判别分析(linear discriminant analysis,LDA)结果识别差异菌属/种。肠道菌群互作通过相关性网络(Spearman模型)在生科云网站上进行分析。
1.8 数据统计及分析
使用GraphPad Prismversion 8软件进行统计分析。采用单因素方差分析比较多组间的差异,然后采用新复极差法检验。结果以“平均值±标准差”表示。
2 结果与分析
2.1 益生元改善DNFB诱导的AD样症状
造模导致小鼠背部皮肤出现显著的AD皮损症状,通过HE切片病理染色发现,空白对照组皮肤组织表皮完整、结构清晰,并可见角化层,真皮层胶原纤维排列整齐,未见炎性细胞浸润(图2-a)。模型组皮肤组织损伤处结构不清、表皮缺失,可见大面积嗜酸性坏死物,角质层增厚,大量结缔组织、纤维细胞及成纤维细胞增生,并伴有较多坏死碎片、淋巴细胞及粒细胞浸润,相较于空白组,皮肤厚度显著增加(图2-c,n=5, P<0.001)。益生元组小鼠经一段时间干预后,皮肤厚度显著降低(n=5, P<0.001)、炎症细胞浸润明显改善。
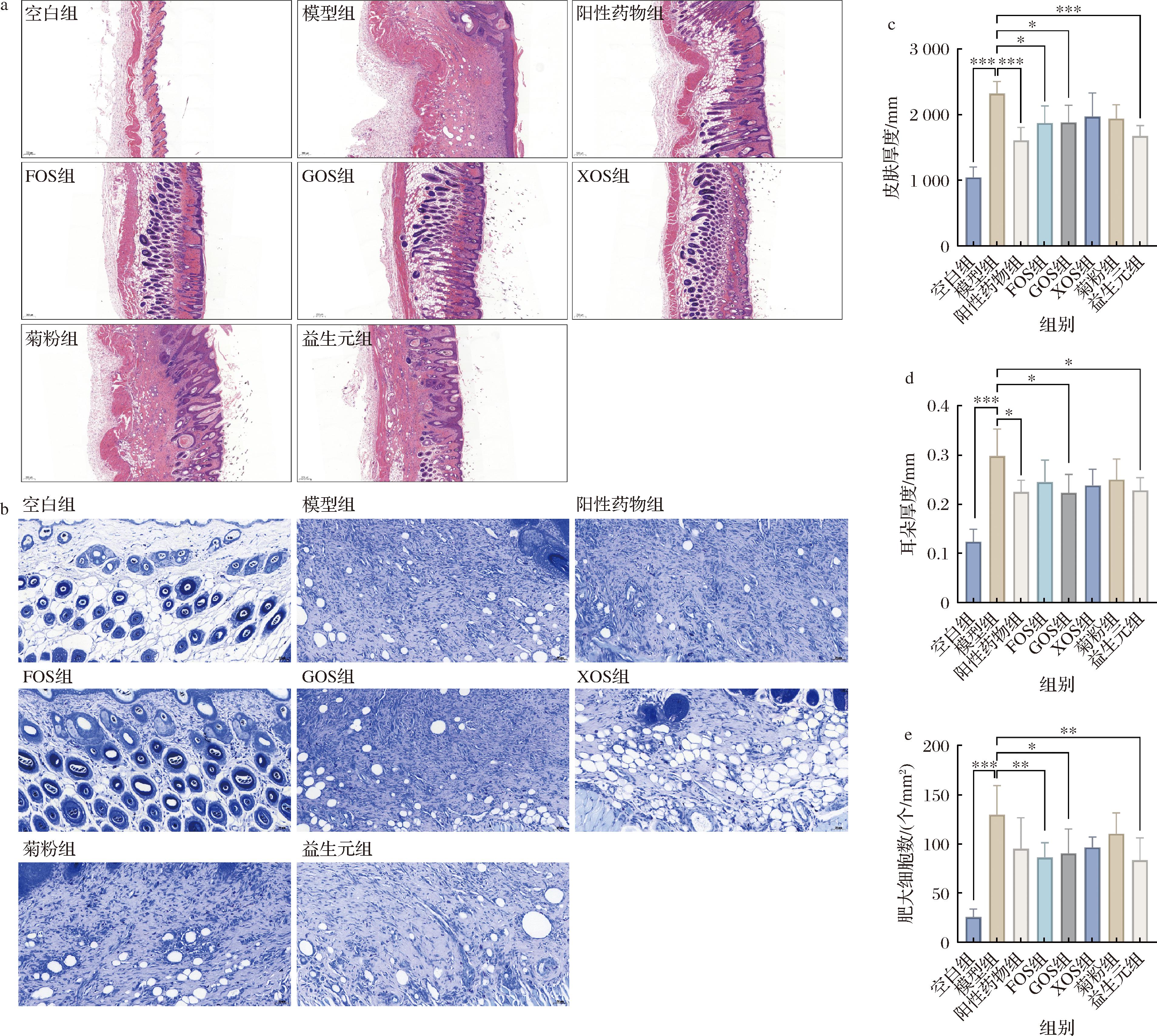
a-皮肤背部病理切片(×5);b-背部皮肤肥大细胞切片(×5);c-皮肤厚度;d-耳朵肿胀程度;e-肥大细胞浸润
图2 益生元对AD样症状的改善作用
Fig.2 Alleviation effects of probiotic formulations on AD-like symptoms
注:*表示与模型组有显著差异,*P<0.05,**P<0.01,***P<0.001(下同)。
DNFB的局部反复使用能够诱导小鼠皮肤出现AD的临床症状,小鼠耳朵厚度的变化反映了局部炎症浸润导致的耳朵肿胀程度。与空白组相比(图2-d),DNFB显著诱导小鼠耳朵厚度增加(n=5, P<0.001),而阳性药物组和各益生元干预组的小鼠耳朵肿胀程度均不同程度降低,其中,GOS益生元干预显著降低了小鼠耳朵厚度(n=5, P<0.05),表明益生元的摄入对于AD引起的耳部皮肤肿胀具有缓解作用。
肥大细胞在AD的发病机制中扮演着重要角色,不仅参与炎症和免疫反应,还可能在AD的瘙痒症状中发挥作用[19-20],因此,测定了AD小鼠皮肤组织中的肥大细胞数。如图2-b、2-e所示,相较于空白组,模型组小鼠背部皮损处出现了显著的肥大细胞炎症浸润的病理症状(n=5, P<0.001)。相比于模型组,阳性药物组和各益生元干预组的小鼠皮肤肥大细胞的炎症浸润均有一定程度的降低,其中,FOS组(n=5, P<0.01),GOS组(n=5, P<0.05),XOS组(n=5, P<0.01)具有显著性,改善小鼠皮肤肥大细胞浸润效果较好。以上结果表明,益生元干预显著抑制皮损处炎症细胞的浸润,且效果优于阳性药物。
2.2 益生元调节Th1/Th2免疫反应
在过敏性疾病的发病机制中,特别是肥大细胞激活和抗原提呈,IgE起到关键作用[24]。如图3-a所示,与空白对照组相比,模型组小鼠血清中总IgE水平显著增加。相比模型组,阳性药物和益生元干预均能降低小鼠血清中IgE水平,但不具有统计显著性。
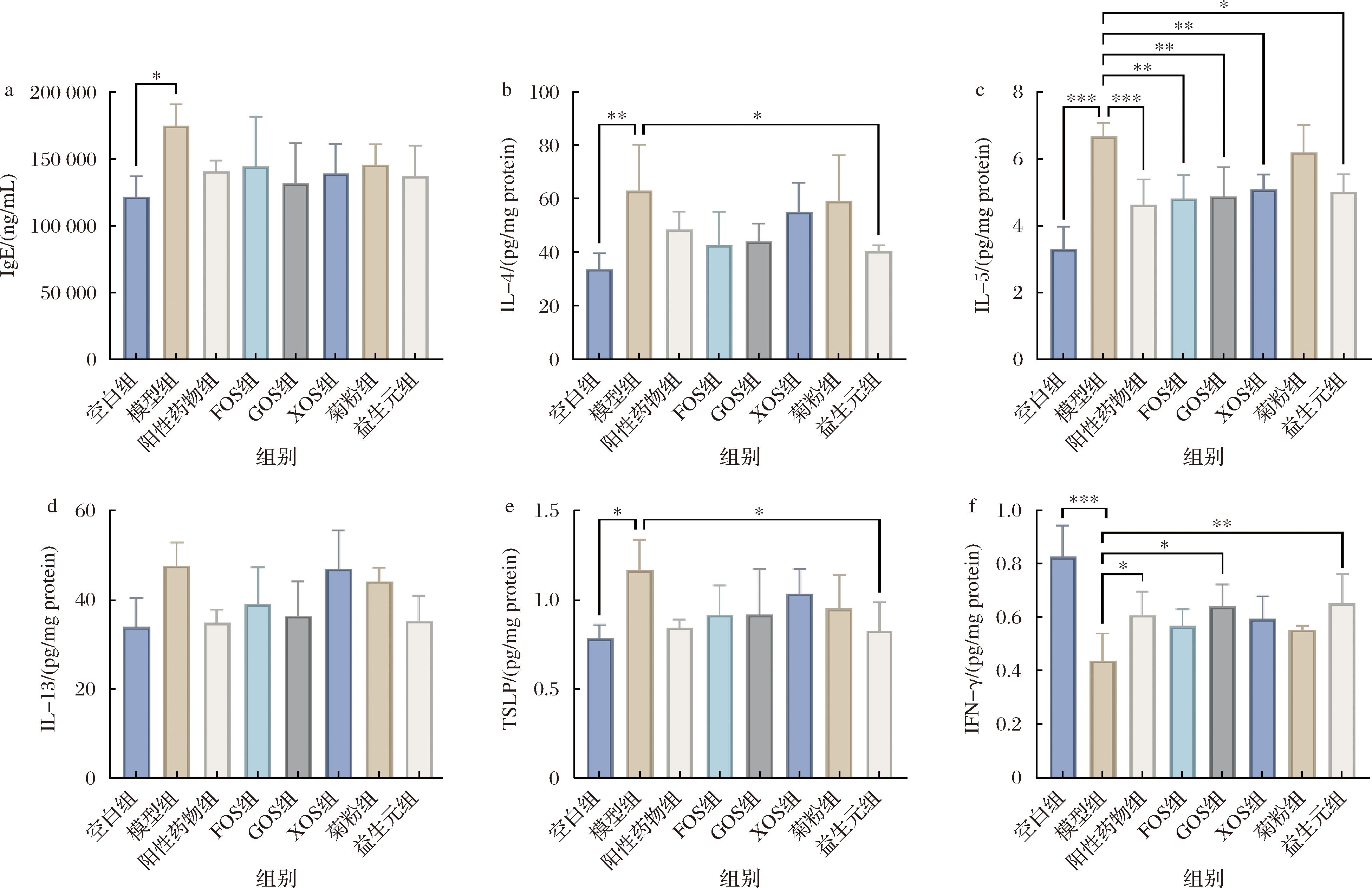
a-IgE;b-IL-4;c-IL-5;d-IL-13;e-TSLP;f-IFN-γ
图3 血清中总IgE水平和皮肤组织中炎症因子水平
Fig.3 Levels of total IgE in serum and inflammatory cytokines in mouse skin tissue
AD发生的核心免疫机制是Th2型免疫应答反应过度,Th2免疫细胞通过释放IL-4、IL-5和IL-13等细胞因子诱导IgE的合成以及炎症细胞的浸润,从而破坏正常的皮肤屏障,导致严重皮损的病理症状[25-26]。DNFB诱导的AD小鼠皮肤组织中的炎症因子IL-4显著增加(n=5, P<0.01),与模型组相比,干预各组均能降低IL-4水平,且益生元组具有较高显著性(n=5, P<0.05)(图3-b)。与空白组相比,模型组IL-5表达水平显著增加(n=5, P<0.001)。阳性药物和益生元干预不同程度降低了IL-5表达水平,尤其是FOS、GOS、XOS和益生元显著降低了IL-5的表达(图3-c)。与空白组相比,模型组小鼠皮肤组织中IL-13水平增加,在阳性药物和益生元干预后,小鼠皮肤组织中IL-13水平均有一定程度降低,但不具有统计显著性(图3-d)。TSLP是炎症反应的重要调节因子,能够刺激树突状细胞分化为Th2细胞,从而促进Th2型炎症反应[27]。与空白组相比,AD模型小鼠血清中的TSLP水平显著增加(n=5, P<0.05)。与模型组相比,阳性药物和益生元组小鼠血清中TSLP水平均有一定程度的降低,尤其是益生元组效果更为显著(n=5, P<0.05,图3-e)。
Th1型免疫反应相关的IFN-γ水平的提高有助于调节Th2型免疫偏移引起的Th1/Th2免疫失衡[26]。相比于空白组,模型组中观察到IFN-γ的浓度显著下降(n=5, P<0.001)。进一步分析发现,通过阳性药物,GOS和益生元的干预,能够有效增加小鼠组织中IFN-γ的水平,尤其是益生元组具有较高显著性(n=5, P<0.01,图3-f)。
2.3 益生元调节AD小鼠肠道菌群组成及结构
如图4-a~图4-c所示,与对照组相比,模型组小鼠的肠道微生物群落α-多样性指数降低,这可能指示了AD病理状态下微生物群落多样性的失衡。与模型组相比,益生元干预显著增加了Observed species指数(n=4, P<0.05)。此外,其他干预组也不同程度提高了Shannon指数、Evenness指数和Observed species指数,尽管这些变化没有达到统计学上的显著性。
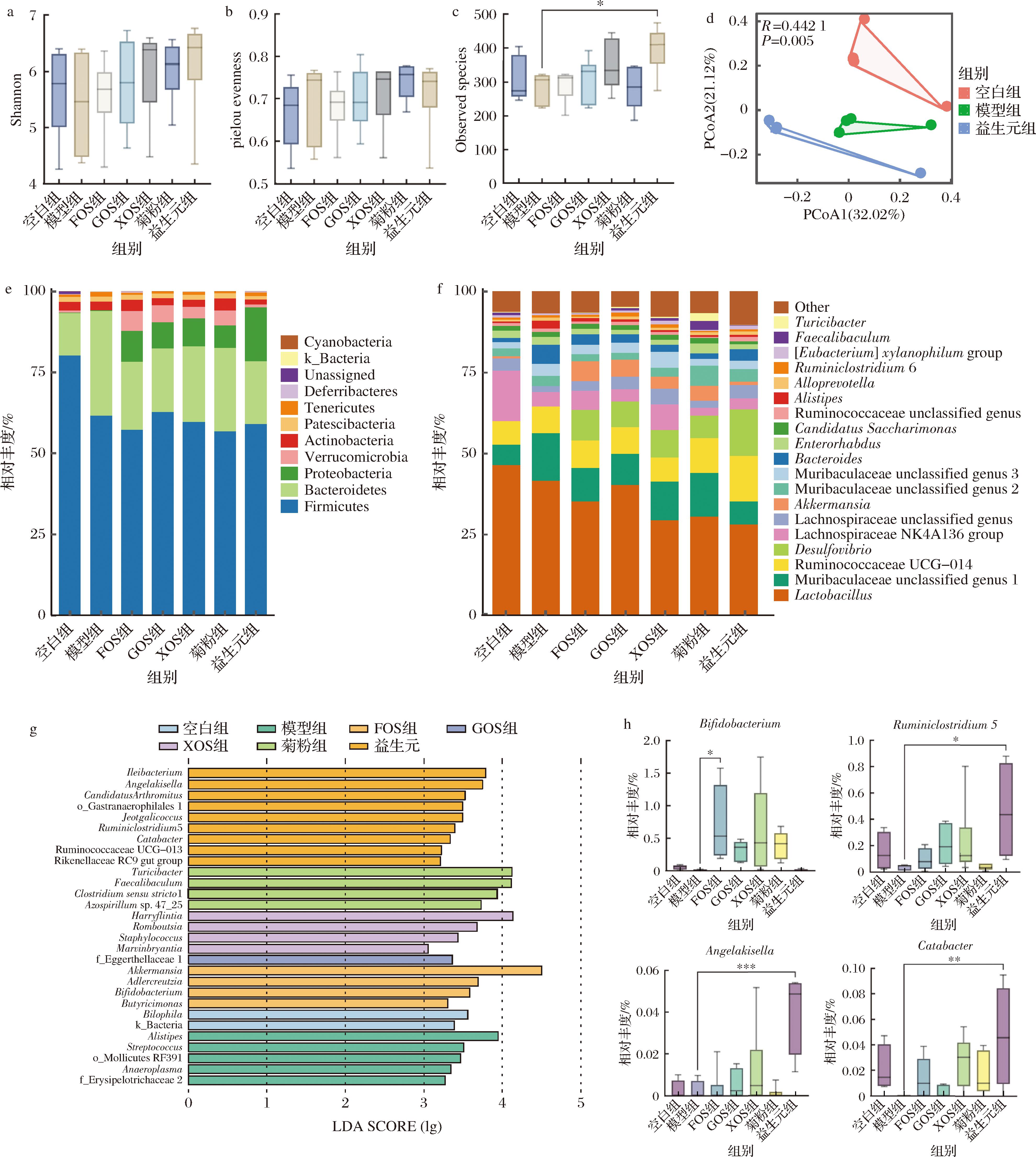
a-Shannon指数;b-Evenness指数;c-Observed species指数;d-PCoA结果;e-肠道菌群的门水平组成;f-肠道菌群的属水平组成;g-LEfSe分析结果;h-Bifidobacterium、Ruminiclostridium 5、Angelakisella和Catabacter的相对丰度
图4 益生元干预重塑了AD模型小鼠的肠道微生物组成(门水平和属水平)
Fig.4 Intervention with probiotic mixture restored the gut microbiota composition (in phylum-level and genus-level) of atopic dermatitis mice
为了研究益生元对肠道微生物群落结构的影响,通过PCoA评估了肠道微生物群落的β多样性。如图4-d所示,与对照组相比,AD模型组小鼠的肠道微生物群落出现了明显的变化。经过益生元干预后,小鼠的肠道微生物群落结构与AD模型组相比出现了显著的偏移。这些发现揭示了益生元在调节AD小鼠肠道微生物群落结构方面的显著效果。
如图4-e所示,小鼠肠道微生物群落在门分类层面上以厚壁菌门(Firmicutes)和拟杆菌门(Bacteroidetes)为主。相较于对照组,DNFB诱导的AD模型小鼠中厚壁菌门相对丰度增加,疣微菌门(Verrucomicrobia)的相对丰度下降,而益生元的补充降低了厚壁菌门相对丰度,提高了疣微菌门丰度。此外,各个益生元组均在不同程度上促进了变形菌门(Proteobacteria)的增长。如图4-f所示,在属水平上,与空白组相比,DNFB诱导的AD小鼠肠道中Akkermansia和Lachnospiraceae科的相对丰度减少,而各益生元干预组均不同程度增加了Akkermansia和Lachnospiraceae科的丰度。Akkermansia是潜在的益生菌,其丰度与肠道屏障功能和抗炎作用密切相关。此外,Lachnospiraceae与湿疹风险降低相关。因此,益生元的补充可能通过调整肠道微生物群的组成,调节免疫反应,进而减轻AD病理症状。
如图4-g~图4-h所示,LEfSe分析结果表明,相比于模型组,FOS干预显著富集了Bifidobacterium,益生元组显著富集了Angelakisella,Ruminiclostridium 5和Catabacter,其中Bifidobacterium能够通过调节免疫细胞的活性,增强机体的免疫功能。例如,Bifidobacterium animalis BB-12菌株可以显著提高Treg的数量,维持Th1/Th2平衡,从而增强机体的免疫反应[28]。Angelakisella在调节短链脂肪酸(short-chain fatty acids,SCFAs)产生和改善肥胖方面具有重要作用[29]。此外,Ruminiclostridium 5与胆汁酸谱的调节相关,研究发现其丰度的增加与次级胆汁酸和结合型胆汁酸的减少相关,这可能对肠道健康和整体代谢有益[30]。因此,益生元的补充可能通过调整肠道微生物群的组成和代谢,调节免疫反应,进而减轻AD病理症状。
如图5-a所示,在操作分类单元(operational taxonomic unit,OTU)水平上,PCoA结果表明,AD小鼠的肠道微生物群落结构组成与健康小鼠存在差异,值得注意的是,益生元干预显著改变了AD小鼠肠道微生物的结构和组成(n=4, P<0.01),表现出对肠道微生物群落的显著调节作用。如图5-b~图5-d所示,在OTU水平上,LEfSe分析结果表明,相比于模型组,益生元干预显著富集了s_Erysipelotrichaceae bacterium NYU-BL-F16、g_Angelakisella;s_uncultured bacterium等具有代谢调节作用和免疫调节作用的菌种[29, 31],这可能与AD小鼠免疫反应的改善密切相关。

a-基于OTU水平菌群丰度表的PCoA结果;b-基于OTU水平菌群丰度表的LEfSe分析结果;c-s_Erysipelotrichaceae bacterium NYU-BL-F16的相对丰度;d-g_Angelakisella s_uncultured bacterium的相对丰度
图5 益生元干预重塑了AD模型小鼠的肠道微生物组成(种水平)
Fig.5 Intervention with probiotic mixture restored the gut microbiota composition (in species-level) of atopic dermatitis mice
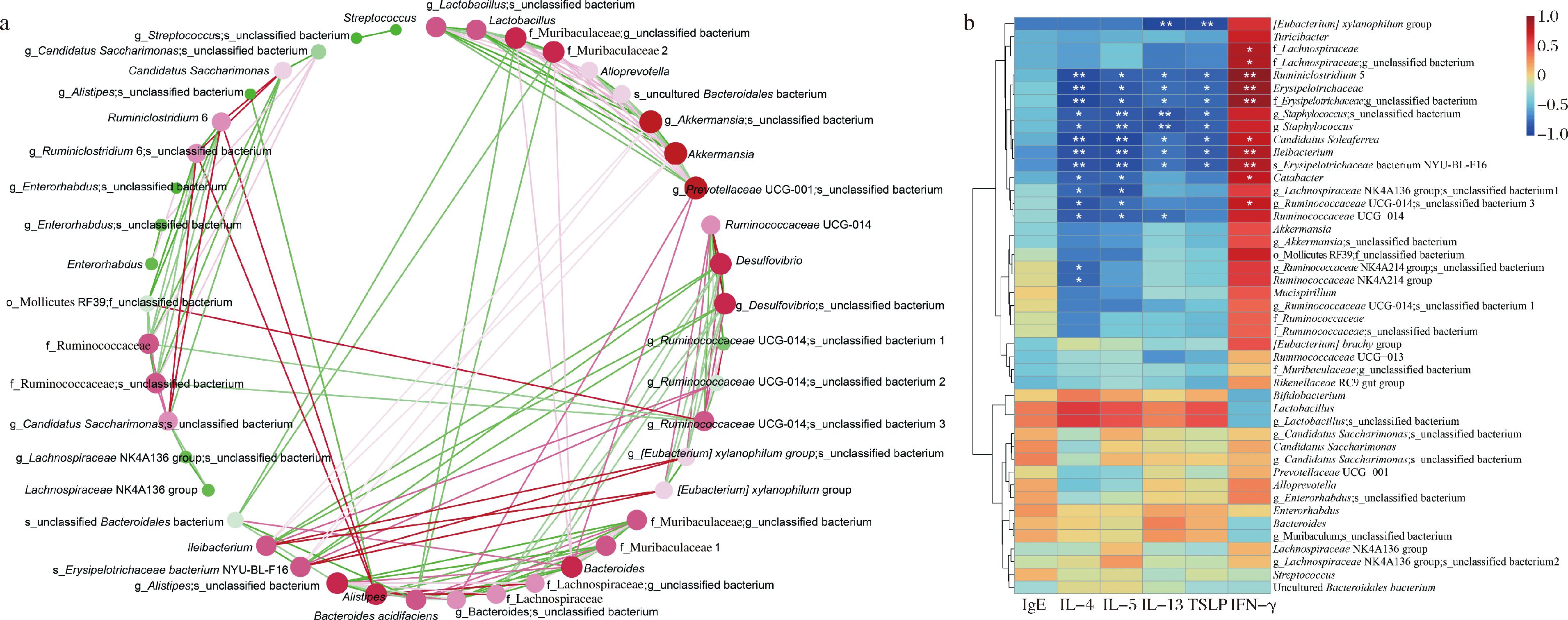
a-肠道菌群互作网络分析结果;b-肠道菌群与免疫炎症因子相关性分析
图6 益生元干预介导肠道菌群重塑后AD模型小鼠的肠道菌群-免疫关联性分析
Fig.6 Analysis of the gut microbiota-immune correlation in AD model mice after prebiotic intervention-mediated gut microbiota remodeling
注:图a中,节点表示45个关键微生物属,其大小与网络度值(degree)成正比;颜色对应门水平分类(红色:拟杆菌门;绿色:厚壁菌门;粉色:变形菌门);连接线粗细反映相关系数绝对值大小,红色连线表示显著正相关(P<0.05),绿色连线表示显著负相关(P<0.05)。
2.4 肠道菌群组成结构变化与免疫反应的联系
肠道菌群对宿主的影响与菌群之间的相互作用密切相关。因此,进一步进行了微生物网络分析,以整合和可视化肠道菌群之间的相互作用。如图6-a所示,在45个肠道微生物节点中,g_Lactobacillus;s_unclassified bacterium、f_Muribaculaceae unclassified bacterium、Desulfovibrio与肠道微生物群形成了8个连接,连接数最多。Lactobacillus casei可通过TLR/NF-κB信号通路调节Th1/Th2平衡,上调T-bet和GATA-3的mRNA水平,并增加CD4+T细胞数量[32]。此外,研究发现Muribaculaceae科能够通过内源性(如黏蛋白聚糖)和外源性多糖(如膳食纤维)发酵产生SCFAs,这些代谢产物可以调节肠道免疫细胞的活性,维持肠道屏障功能[33]。
为探究益生元干预引起的肠道细菌相对丰度的改变与炎症反应之间的相关性,进行了关联性分析(图6-b)。结果表明,Ruminiclostridium 5、Candidatus Saccharimonas和Ileibacterium与IL-4、IL-5、IL-13和TSLP水平呈显著负相关(n=4, P<0.05),与IFN-γ表达水平呈显著正相关(n=4, P<0.05)。f_Erysipelotrichaceae;g_unclassified bacterium和s_Erysipelotrichaceae bacterium NYU-BL-F16与IL-4、IL-5、IL-13和TSLP水平呈显著负相关(n=4,P<0.05),与IFN-γ的表达水平呈显著正相关(n=4, P<0.01),表明益生元可能通过改变肠道菌群组成和相对丰度调节了免疫炎症反应。
3 结论与讨论
本研究通过综合评估FOS、GOS、XOS、菊粉及其益生元组合对AD的缓解作用,揭示了益生元在改善AD症状方面的显著效果。实验结果表明,益生元不仅能显著缓解AD的皮肤病理症状(如表皮增生和炎性浸润减轻)和减少肥大细胞浸润,还能有效降低血清总IgE水平,并抑制异常的Th2型免疫反应(IL-4、IL-5升高,IFN-γ降低)。这些发现揭示了益生元通过调节免疫反应来减轻AD症状的潜力,对于开发新的AD治疗策略具有重要意义。
研究进一步揭示了益生元通过调节肠道菌群与免疫互作缓解AD的潜在机制。DNFB诱导的AD小鼠模型表现出Th2型免疫极化(IL-4、IL-5升高,IFN-γ降低)及肠道菌群失调(菌群多样性降低、厚壁菌门/疣微菌门比例失衡),而益生元干预显著逆转了上述病理特征。值得注意的是,益生元对Th2细胞因子的抑制作用与其富集特定功能菌群密切相关。例如,双歧杆菌属(Bifidobacterium)可能通过激活Treg增强免疫耐受[28],而Muribaculaceae科通过发酵产生SCFAs抑制炎症信号传导(如NF-κB通路)[33]。这些菌群的协同作用可能通过“代谢物-免疫”轴(如SCFAs调控GPR43/NF-κB通路)恢复Th1/Th2平衡,从而减轻皮肤炎症。
网络分析表明,关键菌群(如g_Lactobacillus;s_unclassified bacterium、Ruminiclostridium 5)与促炎因子(IL-4、IL-5)呈显著负相关,提示其可能通过调节胆汁酸代谢或免疫细胞活性影响炎症进程[30]。然而,益生元对血清总IgE和IL-13的调节作用未达统计学显著性,可能与干预时长或菌群代谢产物的局部效应有关。此外,AD模型组中阿克曼菌属(Akkermansia)丰度的降低与肠道屏障损伤一致,而益生元对其丰度的恢复可能通过减少肠源性抗原渗漏间接抑制全身炎症反应。
研究表明,肠道微生物群与AD的发病机理之间存在密切联系[34]。益生元干预能显著提升如Angelakisella、f_Muribaculaceae等潜在有益菌的相对丰度,优化AD小鼠的肠道菌群结构,并增加菌群多样性[29, 33]。本研究进一步证实,肠道微生物群的调节与AD症状的缓解密切相关。尽管观察到益生元能够改善肠道菌群结构、提高菌群多样性并调节免疫反应,但这些变化与AD症状缓解之间的直接因果关系尚未完全阐明。未来的研究需进一步探索益生元如何与肠道微生物相互作用,以及这些微生物代谢产物(如SCFAs)如何通过“代谢物-免疫”轴影响宿主的免疫系统,特别是针对AD相关的Th2型免疫异常。通过深入解析这些机制,可为开发靶向性益生元制剂提供理论基础,并优化其在AD治疗中的应用策略。
作者利益冲突公开声明:作者声明没有任何可能会影响本文所报告工作的已知经济利益或个人关系。
[1] SCHULER C F, TSOI L C, BILLI A C, et al.Genetic and immunological pathogenesis of atopic dermatitis[J].Journal of Investigative Dermatology, 2024, 144(5):954-968.
[2] ZHOU Y G, ZHOU Y, ZHANG S L, et al.Identification of novel hub genes and immune infiltration in atopic dermatitis using integrated bioinformatics analysis[J].Scientific Reports, 2024, 14:23054.
[3] MOHAMMAD S, KARIM M R, IQBAL S, et al.Atopic dermatitis:Pathophysiology, microbiota, and metabolome - A comprehensive review[J].Microbiological Research, 2024, 281:127595.
[4] ÖZDEMIR E, ÖKSÜZ L.Effect of Staphylococcus aureus colonization and immune defects on the pathogenesis of atopic dermatitis[J].Archives of Microbiology, 2024, 206(10):410.
[5] DING G A, YANG X Z, LI Y, et al.Gut microbiota regulates gut homeostasis, mucosal immunity and influences immune-related diseases[J].Molecular and Cellular Biochemistry, 2025, 480(4):1969-1981.
[6] D’AMELIO P, SASSI F.Gut microbiota, immune system, and bone[J].Calcified Tissue International, 2018, 102(4):415-425.
[7] CHEN J, YUE Y H, WANG L, et al.Altered gut microbiota correlated with systemic inflammation in children with Kawasaki disease[J].Scientific Reports, 2020, 10(1):14525.
[8] YAN X M, YAN J B, XIANG Q W, et al.Early-life gut microbiota in food allergic children and its impact on the development of allergic disease[J].Italian Journal of Pediatrics, 2023, 49(1):148.
[9] 邓梦路, 张婕, 盛文彬.肠道菌群在儿童过敏性疾病中的研究进展[J].临床儿科杂志, 2024, 42(8):741-746.
DENG M L, ZHANG J, SHENG W B.Research progress of gut microbiota in allergic diseases in children[J].Journal of Clinical Pediatrics, 2024, 42(8):741-746.
[10] DU B Q, SHAMA A, ZHANG Y, et al.Gut microbiota and plasma metabolites in pregnant mothers and infant atopic dermatitis:A multi-omics study[J].World Allergy Organization Journal, 2025, 18(1):101017.
[11] HOSKINSON C, DAI D L Y, DEL BEL K L, et al.Delayed gut microbiota maturation in the first year of life is a hallmark of pediatric allergic disease[J].Nature Communications, 2023, 14:4785.
[12] YOO S, JUNG S C, KWAK K, et al.The role of prebiotics in modulating gut microbiota:Implications for human health[J].International Journal of Molecular Sciences, 2024, 25(9):4834.
[13] ROBERFROID M, GIBSON G R, HOYLES L, et al.Prebiotic effects:Metabolic and health benefits[J].The British Journal of Nutrition, 2010, 104(Suppl 2):S1-S63.
[14] BOCK P M, MARTINS A F, SCHAAN B D.Understanding how pre- and probiotics affect the gut microbiome and metabolic health[J].American Journal of Physiology.Endocrinology and Metabolism, 2024, 327(1):E89-E102.
[15] KUMARI T, BAG K K, DAS A B, et al.Synergistic role of prebiotics and probiotics in gut microbiome health:Mechanisms and clinical applications[J].Food Bioengineering, 2024, 3(4):407-424.
[16] DE FREITAS PEDROSA L, DE VOS P, FABI J P.From structure to function:How prebiotic diversity shapes gut integrity and immune balance[J].Nutrients, 2024, 16(24):4286.
[17] ULLAH H, ARBAB S, TIAN Y L, et al.Crosstalk between gut microbiota and host immune system and its response to traumatic injury[J].Frontiers in Immunology, 2024, 15:1413485.
[18] 方志锋. 双歧杆菌缓解特应性皮炎的作用及机制研究[D].无锡:江南大学, 2020.
FANG Z F.The role and mechanism of Bifidobacterium in alleviating atopic dermatitis[D].Wuxi:Jiangnan University, 2020.
[19] PLUM T, FEYERABEND T B, RODEWALD H R.Beyond classical immunity:Mast cells as signal converters between tissues and neurons[J].Immunity, 2024, 57(12):2723-2736.
[20] KAWAKAMI T, ANDO T, KIMURA M, et al.Mast cells in atopic dermatitis[J].Current Opinion in Immunology, 2009, 21(6):666-678.
[21] HAIFER C, SAIKAL A, PARAMSOTHY R, et al.Response to faecal microbiota transplantation in ulcerative colitis is not sustained long term following induction therapy[J].Gut, 2021, 70(11):2210-2211.
[22] XIAO Y C, XU W N, SU W R.NLRP3 inflammasome:A likely target for the treatment of allergic diseases[J].Clinical &Experimental Allergy, 2018, 48(9):1080-1091.
[23] STOWER H.Training neuropathology[J].Nature Medicine, 2018, 24(6):702.
[24] CHEN M Y, SU Q, SHI Y G.Molecular mechanism of IgE-mediated FcεRI activation[J].Nature, 2025, 637(8045):453-460.
[25] 孔羽薇, 姚志荣.特应性皮炎相关细胞因子的研究进展[J].临床儿科杂志, 2019, 37(2):148-152.
KONG Y W, YAO Z R.Research progress on cytokines in atopic dermatitis[J].Journal of Clinical Pediatrics, 2019, 37(2):148-152.
[26] 罗静英, 黎小东, 李振洁, 等.特异性免疫治疗对特应性皮炎患者血清IL-4、IFN-γ的影响[J].岭南皮肤性病科杂志, 2009, 16(6):372-374.
LUO J Y, LI X D, LI Z J, et al.Effects of specific immunotherapy on the cytokines in atopic dermatitis[J].Southern China Journal of Dermato-Venereology, 2009, 16(6):372-374.
[27] LUO J L, ZHU Z, ZHAI Y M, et al.The role of TSLP in atopic dermatitis:From pathogenetic molecule to therapeutical target[J].Mediators of Inflammation, 2023, 2023(1):7697699.
[28] 张琳, 徐加英, 石羽杰, 等.双歧杆菌BB-12及其免疫调节功能的研究进展[J].上海预防医学, 2020, 32(7):600-605.
ZHANG L, XU J Y, SHI Y J, et al.Research progress on Bifidobacterium BB-12 and human immune regulation[J].Shanghai Journal of Preventive Medicine, 2020, 32(7):600-605.
[29] QIU X X, MACCHIETTO M G, LIU X T, et al.Identification of gut microbiota and microbial metabolites regulated by an antimicrobial peptide lipocalin 2 in high fat diet-induced obesity[J].International Journal of Obesity, 2021, 45(1):143-154.
[30] THOMPSON R S, GAFFNEY M, HOPKINS S, et al.Ruminiclostridium 5, Parabacteroides distasonis, and bile acid profile are modulated by prebiotic diet and associate with facilitated sleep/clock realignment after chronic disruption of rhythms[J].Brain, Behavior, and Immunity, 2021, 97:150-166.
[31] MAO J Z, WANG D X, LONG J Y, et al.Gut microbiome is associated with the clinical response to anti-PD-1 based immunotherapy in hepatobiliary cancers[J].Journal for Immunotherapy of Cancer, 2021, 9(12):e003334.
[32] 秦孟春, 张玲芳, 胡顺安, 等.乳酸菌的抗食物过敏及免疫调节特性的研究进展[J].中国酿造, 2024, 43(6):14-20.
QIN M C, ZHANG L F, HU S A, et al.Research progress on anti-food allergy and immunomodulatory properties of lactic acid bacteria[J].China Brewing, 2024, 43(6):14-20.
[33] XIE J, TIAN S M, LIU J, et al.Combination therapy with indigo and indirubin for ulcerative colitis via reinforcing intestinal barrier function[J].Oxidative Medicine and Cellular Longevity, 2023, 2023(1):2894695.
[34] YANG Z X, ZHU J L, LU W W, et al.Integrating artificial intelligence in exploring multiscale gut microbiota and diet relations for health promotion:A comprehensive review[J].Food Bioscience, 2024, 61:104541.