乳酸片球菌(Pediococcus acidilactici)属于片球菌属,是乳酸菌的重要成员之一,其分裂后通常成对或以聚集的形式呈现链状[1-2]。P.acidilactici常用于发酵蔬菜、肉类和发酵乳制品的生产。部分P.acidilactici菌株具有调节小鼠的肠道菌群从而缓解便秘[3]、缓解小鼠的特应性皮炎[4]、降低糖尿病大鼠的血糖水平和改善其胰腺β细胞功能[5]、提高断奶仔猪营养物质消化率和抗氧化能力[6]、预防高胆固醇血症[7]等益生特性。此外,部分P.acidilactici菌株还抑制白色念珠菌、鸡沙门氏菌等致病菌生长[8];作为抗氧化剂提高发酵产品的抗氧化性能[9];分泌出具有高DPPH自由基清除活性和良好抗生物膜能力的胞外多糖[10]等能力。P.acidilactici是一种拥有良好益生特性、功能活性全面的微生物,具有较高的经济价值。
关于P.acidilactici的基因组学研究从2009年第一株完成全基因组测序并上传到NCBI数据库的P.acidilactici 7_4开始,越来越多的P.acidilactici完成了基因组测序。2017年P.acidilactici S1完成测序,其基因组内含有多个编码酒精耐受酶相关基因[11]。2019年P.acidilactici LPBC161完成测序,其基因组内含有大量编码复杂多糖磷酸转移酶的特异基因[12]。2023年从比格犬肠道内分离出P.acidilactici GLP06并完成测序,其基因组内注释到8个CRISPR序列[13]。但目前对于P.acidilactici比较基因组学研究相对较少。RANJAN等[14]对P.acidilactici NRCC1完成测序,与P.acidilactici DSM 20284进行比较基因组学分析,发现P.acidilactici NRCC1具有23个特异性基因,且多数特异性基因与植物源多聚糖代谢能力有关。LI等[15]对NCBI数据库的41株P.acidilactici进行分析,发现P.acidilactici是一种非生态位特异性物种、来源广泛、代谢灵活、生态适应性强、功能多样、具有较高水平的遗传多样性。但是对猪源的P.acidilactici遗传背景知之甚少。通过对多个菌株的基因组进行测序和比较分析,可以更好地理解其遗传背景和功能基因组特征,这对于阐明P.acidilactici 的潜在应用价值具有重要意义[16-17]。
本研究从中国内蒙古自治区武川县种猪厂健康仔猪粪便分离鉴定的9株P.acidilactici进行基因组测序,结合NCBI数据库的275株P.acidilactici基因组信息进行分析,从基因组基本信息、遗传背景、功能基因方面进行比较基因组学分析,为了解该菌种的生境适应性进化提供数据支持。
1 材料与方法
1.1 样品的采集保存与分离纯化
采集内蒙古自治区呼和浩特市武川县的7份健康仔猪粪便样品于冻存管中,低温运输至实验室,保存在-80 ℃超低温冰箱中,用于样品的菌株分离。
在无菌条件下,称取7份粪便样品各1 g,分别加入9 mL无菌生理盐水(质量分数为0.85%),用涡旋振荡器充分振荡均匀,期间保证每份样品单独操作避免样品间相互污染。所得匀浆用9 mL无菌生理盐水进行10倍梯度稀释,直至10-6。将10-3、10-4和10-5稀释液各1 mL摇匀,涂抹在MRS(Oxoid,赛默飞世尔科技公司)琼脂和梭状芽胞杆菌的强化培养基(RCM+Vb;Sinopharm Chemical Reagent Co., Ltd.)[18]上。仔细观察菌落的形态,从平板中挑选具有不同形态特征的单个菌落,用平板划线法将其接种到MRS琼脂培养基上,培养24 h。重复上述过程以纯化菌落。选取形态特征、大小和颜色各异的单个菌落,接种到MRS液体培养基中。对培养物进行革兰氏染色,在BX50光学显微镜(OLYMPUS,日本)下观察染色玻片,记录细胞形态和排列。挑选出革兰氏阳性、分布均匀、形态单一的分离物,保存在-80 ℃冰箱中。
1.2 细菌菌株DNA提取和全基因组测序
使用Wizard®基因组DNA纯化试剂盒(Promega公司,美国威斯康星州麦迪逊市)对细菌基因组DNA进行提取。DNA提取完毕后,用NanoDrop分光光度计(NanoDrop Technologies, Inc.)测定OD260/280值,在1.8~2.0范围内为符合标准。同时,确保检测到的DNA含量超过20 ng/μL,且琼脂糖凝胶电泳合格。将符合要求的DNA发送到北京诺禾致源科技股份有限公司,对其进行基因组序列测定,测序平台是Illumina Novaseq平台(Illumina, Inc.),选取150 bp的DNA片段来构建Pair-end测序文库,数据平均覆盖度在500×左右。
在进行基因组组装的时候,首先要对原始reads展开质量控制,将低质量的数据和连接序列去掉,从而得到高质量的cleandata数据,再利用SOAP denovo(v2.04)[19],对每株菌的基因组进行组装拼接,并在reads的基础上进行单碱基校正。最后,调用GapCloser软件(http://sourceforge.net/proiects/soapdenovo2/files/GapCloser/)填充内部gap,完成基因组的组装拼接。
1.3 基因组来源
275株来源于NCBI RefSeq数据库(截至2024年10月12日)全基因组序列。利用checkM[20](V1.1.9)评估基因组质量,剔除其中基因组完整度<95%,污染度>5%的基因组。基本信息如电子版增强出版附表1(https://doi.org/10.13995/j.cnki.11-1802/ts.042154,下同)所示。
表1 九株分离鉴定的P.acidilactici 组装测序相关数据
Table 1 Data related to assembly sequencing of nine isolated and identified P.acidilactici strains
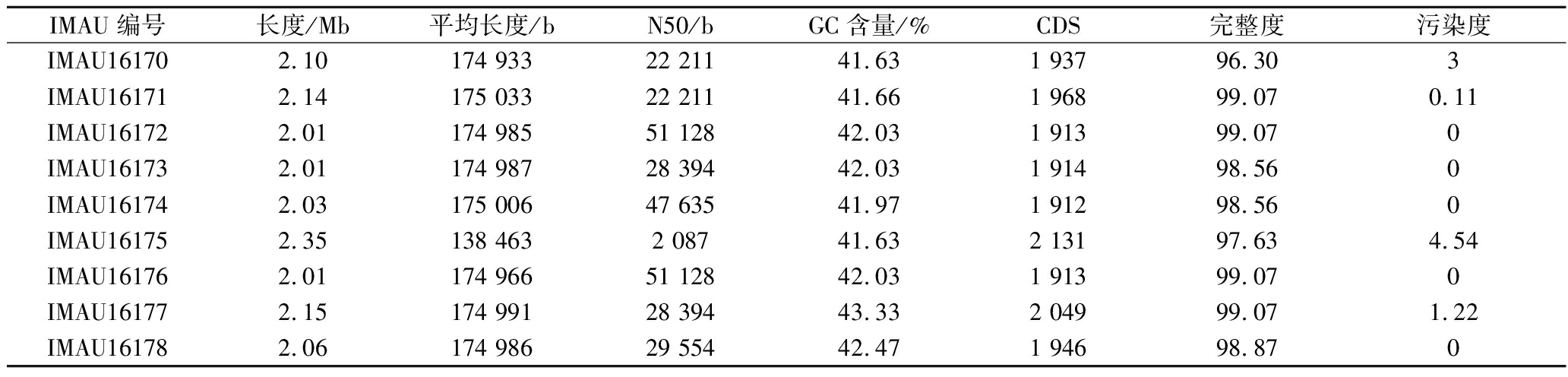
IMAU编号长度/Mb平均长度/bN50/bGC含量/%CDS完整度污染度IMAU161702.10174 93322 21141.631 93796.303IMAU161712.14175 03322 21141.661 96899.070.11IMAU161722.01174 98551 12842.031 91399.070IMAU161732.01174 98728 39442.031 91498.560IMAU161742.03175 00647 63541.971 91298.560IMAU161752.35138 4632 08741.632 13197.634.54IMAU161762.01174 96651 12842.031 91399.070IMAU161772.15174 99128 39443.332 04999.071.22IMAU161782.06174 98629 55442.471 94698.870
1.4 核-泛基因集与系统发育树构建
通过默认参数的Prokka[21]软件进行基因组注释,并使用roary[22]软件进行泛基因组和核心基因组分析,所有参数均为默认值。基于核心基因的系统发育树由Treebest软件(http://www.mybiosoftware.com/treebest)采用邻接法构建,bootstrap值1 000。使用Chiplot在线网站(https://www.chiplot.online/)对系统发育树进行可视化展示。
1.5 平均核苷酸一致性(average nucleotide identity,ANI)的计算
采用fastANI[23]进行乳酸片球菌基因组成对ANI值计算。用TBtools 软件计算并可视化ANI热图。
1.6 功能基因注释
1.6.1 蛋白质直系同源簇数据库(cluster of orthologous groups of protein,COG)注释
使用COG数据库[24]进行蛋白质同源序列比对完成功能注释。
1.6.2 碳水化合物活性酶(carbohydrate-active enzymes, CAZys)注释
使用CAZys数据库(http://csbl.bmb.uga.edu/dbCAN/)进行CAZys注释。
1.7 细菌素相关基因簇分析
使用BAGEL4(http://bagel4.molgenrug.nl/)对细菌素产生基因簇进行在线注释。
2 结果与分析
2.1 基因组基本特征分析
为了探究P.acidilactici 基因组特征,本研究完成了9株P.acidilactici 测序组装,其组装结果见表1,其基因组大小(2.09±0.10) Mb,GC含量为(42.08±0.54)%,编码序列(coding sequences,CDS)为(1 964±76)个。275株来源于NCBI RefSeq数据库P.acidilactici的基因组大小、GC含量、CDS数量进行了统计分析。结果显示275株P.acidilactici 基因组大小(2.01±0.08) Mb、GC含量为(42.12±0.16)%、编码序列(coding sequences,CDS)为(1 601±85)个。对测定的9株菌株与NCBI数据库中已有275株菌株基因组进行对比,GC含量与CDS数与NCBI菌株差异不显著(P>0.05),表明9株P.acidilactici 测序组装结果良好。
2.2 核-泛基因集与系统发育树分析
本研究对284株P.acidilactici 所构建的泛基因集进行分析发现,泛基因数量为10 618个。其中,核心基因(strains=100%)为675个,占泛基因集的6.35%;软核基因(95%≤strains<100%)为418个,占泛基因集的3.94%;壳基因(15%≤strains<95%)为1 397个,占泛基因集的13.16%;云基因为8 128个,占泛基因集的76.55%。284株P.acidilactici具有较低的核心基因占比和较高的云基因占比,表明P.acidilactici 具有高遗传多样性。
选择与P.acidilactici亲缘关系较近的模式菌株P.stilesii DSM 18001T和P.pentosaceus ATCC 33316 151T与284株菌共同构建泛基因集,基于286株菌的61个核心基因构建有外群系统发育树(附图1-A),分支的长度反映了进化亲缘关系的远近,结果发现所有P.acidilactici菌株与外群菌株均表现出较远的遗传距离,表明284株P.acidilactici为同一种。基于284株P.acidilactici泛基因集的675个核心基因构建无外群系统发育树(附图1-B),分支的长度反映了进化亲缘关系的远近,结果显示284株P.acidilactici分为2个遗传分支group1与group2,group1中包含了100株菌,group2中包含了184株菌。美国分离株中的75.51%位于group1;瑞士分离株的79.80%位于group2,且占group2总体的45.1%;中国分离株的86.96%位于group2。人源的菌株84%位于group1,且占group1总体的42%;动物源的菌株76.10%位于group2,且占group2总体的65.7%;植物源菌株的53.3%位于group1。系统发育树的结果发现,分离自瑞士菌株在group2上有聚集趋势,人源的菌株在group1上有聚集趋势,动物源的菌株在group2上有相对聚集趋势,表明菌株可能发生了生境适应性进化。
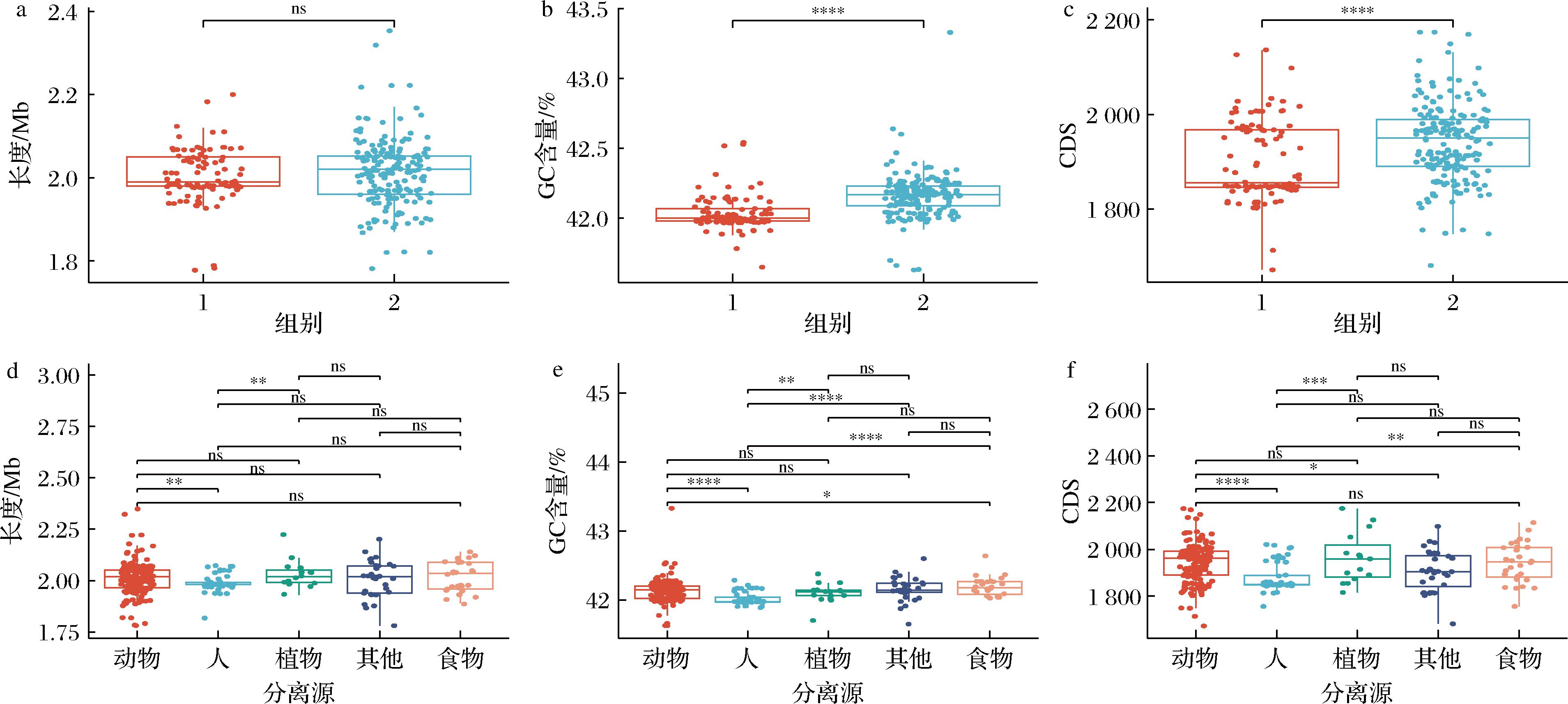
a-不同遗传分支基因组大小显著性差异分析;b-不同遗传分支GC含量显著性差异分析;c-不同遗传分支CDS数量显著性差异分析;d-不同分离源基因组大小显著性差异分析;e-不同分离源GC含量显著性差异分析;f-不同分离源CDS数量显著性差异分析
图1 284株P.acidilactici分组与不同分离源基因组大小、GC含量、CDS数量显著性差异分析
Fig.1 Comparative analysis of genome size, GC content, and number of coding sequences (CDSs) across different P.acidilactici groups and isolation sources
注:显著性水平:ns表示P>0.05;*表示P<0.05;**表示P<0.01;***表示P<0.001;****表示P<0.000 1(下同)。
本研究从仔猪体内分离的9株P.acidilactici均聚集于group2,与分离于啤酒的P.acidilactici BIO6314和分离于瑞士奶酪的FAM22235遗传距离较近。后续以所有动物体内分离株(45株)构建泛基因集,基于1 123个核心基因构建系统发育树,结果如附图1-C所示,发现分离于中国的猪源菌株都位于group2。且猪源菌株与从同为家畜的牛源菌株和鸡源菌株遗传距离较近。基于roary软件处理结果中的基因存在与缺失构建核-泛基因趋势如附图1-D所示,随着基因组数量持续增加,核心基因组逐渐趋于平稳,泛基因组仍有新基因被发现,这表明P.acidilactici 的泛基因组处于开放状态。
2.3 平均核苷酸同一性
ANI值可以在基因组水平上确定菌株间遗传序列的相似程度,通过计算平均核苷酸同一性定量分析284株P.acidilactici基因组之间的相似性。以ANI值96%作为边界数值[25],同一物种之间ANI值均大于96%。283株菌基因组与模式菌株P.acidilactici DSM 20284T的ANI值为(97.73±0.93)%,均大于96%,表明284株菌均为P.acidilactici。此外,如附图2所示,系统发育树的2个遗传分支与ANI热图中聚成两类的菌株一一对应,且分支内的ANI值高于分支间的ANI值。

a~k-不同遗传分支CAZys家族基因拷贝数显著性差异分析;l~t-不同分离源CAZys家族基因拷贝数显著性差异分析;u~y-猪源与其他动物体内分离菌株CAZys家族基因拷贝数显著性差异分析
图2 284株P.acidilactici 不同遗传分支不同分离源CAZys家族基因拷贝数显著性差异分析与45株动物体内分离株显著性差异分析
Fig.2 Comparative analysis of the copy number variation of CAZy family genes among different genetic lineages and isolation sources of P.acidilactici, including a subset of 45 strains isolated from animal hosts
2.4 不同组基因组特征差异分析
细菌的基因组特征可以反映其在自然界中的生态表现[26]。将284株P.acidilactici 按照系统发育树结果分成2组,将2组之间的基因组大小、GC含量、CDS数量进行显著性差异比较。结果如图1所示,2组之间基因组大小无显著差异(P>0.05),而group2菌株的GC含量与CDS数量显著高于group1(P<0.000 1)。
按照菌株不同分离源进行分组比较分析,发现人源P.acidilactici在基因组大小、GC含量、CDS数量均显著小于动物源与植物源菌株(P<0.001),而动物源与植物源无显著差异(P>0.05)。动物分离菌株中猪源菌株与其他动物源菌株在基因组大小、GC含量、CDS数量方面均无显著差异(P>0.05)。
2.5 碳水化合物利用能力分析
为进一步探究不同分离源P.acidilactici 生境适应性进化导致的功能基因组差异,对284株菌的CAZys注释结果进行分析。结果见附图3,共预测到74种CAZys。包括10种碳水化合物结合模块(carbohydrate-binding modules,CBMs)、10种碳水化合物酯酶家族(carbohydrate esterases,CEs)、37种糖苷水解酶家族(glycoside hydrolases,GHs)、12种糖基转移酶家族(glycosyl transferases,GTs)、4个辅助活性家族(auxiliary activities,AA)、1个多糖裂解酶家族(polysaccharide lyases,PL)。GT2、GH1、CBM50、GT4注释到的拷贝数最多,其中GT2和GT4与蔗糖等二糖、脂多糖、壳聚糖以及纤维素等碳水化合物的合成有关[27],CBM50与GH1分别与几丁质酶的合成和降解葡聚糖酶的相关酶有关[28]。
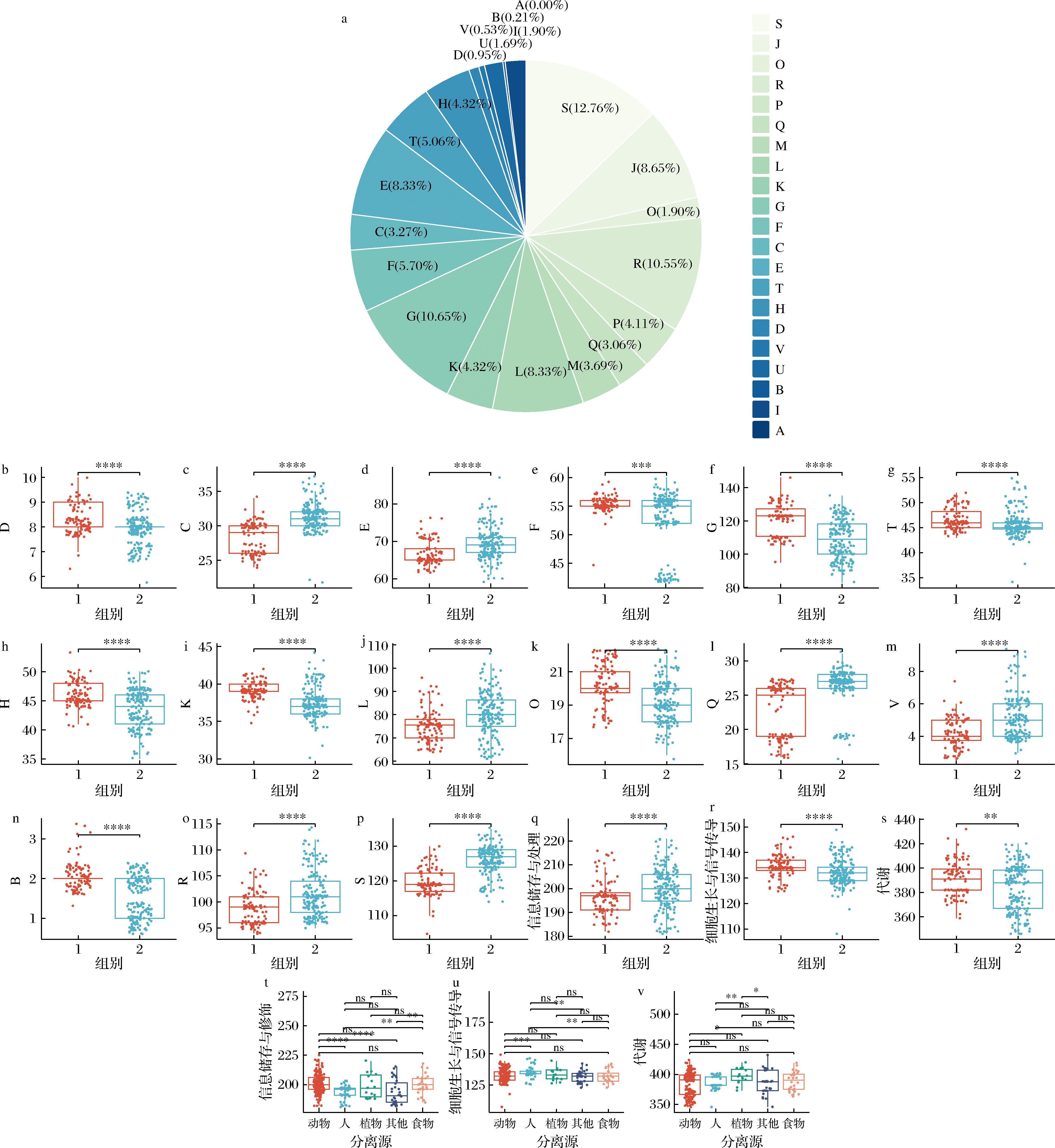
a-284株P.acidilactici COG功能基因拷贝数分类比例;b~p-不同遗传分支功能类别基因拷贝数显著性差异分析;q~s-不同遗传分支功能大类基因拷贝数显著性差异分析;t~v-不同分离源功能大类基因拷贝数显著性差异分析
图3 284株P.acidilactici不同COG功能分类比例与不同遗传分支COG功能类别与功能大类显著性差异分析与不同分离源功能大类显著性差异分析
Fig.3 Proportional distribution of P.acidilactici strains across different COG functional categories, along with a comparative analysis of COG functional classifications among different genetic lineages and isolation sources
对P.acidilactici两个遗传分支的注释结果进行比较发现,GT83只在group1中注释到,CBM54、CBM22、GH120、GT21、CBM32、AA3、GH35、CE4、GH70只在group2中注释到。对检出率100%的每个家族进行显著性差异分析,基于2个遗传分支菌株注释的CAZys家族基因拷贝数绘制箱线图,结果如图2(图2-a~图2-k),group1与group2中11个家族拷贝数存在显著差异(P<0.05)。其中CBM50、CE1、CE10、GH1、GH25、GH29、GT28的数量在group2中显著高于group1(P<0.05),CE6、GH31、GH43、GT2的数量group1显著高于group2(P<0.05)。
基于不同分离源菌株注释的CAZys家族基因拷贝数绘制箱线图,结果如图2(图2-l~图2-t)所示,9个家族(检出率100%)拷贝数存在显著差异(P<0.05)。人源的菌株在CE10与GH29的拷贝数显著少于动物与植物源菌株(P<0.05),GH2与CBM50的拷贝数显著少于动物源菌株(P<0.05),GT4与GT26的拷贝数显著多于动物源与植物源菌株(P<0.05),GH43与GH31拷贝数显著多于动物源菌株(P<0.05)。动物源菌株的GT4拷贝数显著多于植物源菌株(P<0.05),GT51拷贝数显著少于植物源菌株(P<0.05)。猪源菌株相比于其他动物体内分离菌,在GT2、GT4、GT26家族基因拷贝数上显著多于其他动物体内分离株(P<0.05)。CE10、GH43家族基因拷贝数上显著少于其他动物体内分离株(P>0.05)。
2.6 COG功能注释分析
对284株P.acidilactici进行了COG功能注释,基于注释结果中各族的基因拷贝数构建COG功能分类比例图。结果如图3-a所示,一共注释到21个功能分类,其中参与S族、G族、R族基因拷贝数占总比例最高。将几个具有相似功能家族的集合归为功能大类[26],即参与信息储存与处理基因的功能基因(J族、A族、K族、L族)占总体的21.32%;参与细胞生长过程与信号传导的功能基因,即(O族、M族、T族、D族、V族、U族、B族、Z族)占总体的14.03%;参与代谢的功能基因,即(P族、Q族、G族、F族、C族、E族、H族、I族)占总体的41.34%;剩余的S族与R族参与编码未知功能基因,分别为12.76%和10.55%。基于2个遗传分支菌株注释的COG功能基因拷贝数绘制箱线图,结果如图3(图3-b~图3-p)所示,其中group1菌株中K族、O族、T族、B族、D族、G族、H族、F族的拷贝数显著多于group2(P<0.05),group2菌株的L族、V族、C族、E族、Q族、S族、R族的拷贝数显著多于group1(P<0.05)。
基于不同遗传分支与不同分离源参与功能大类的基因拷贝绘制箱线图,结果如图3(图3-q~图3-v),group2在信息储存与处理功能基因拷贝数显著高于group1(P<0.000 1),动物源菌株显著多于人源菌株(P<0.000 1)。group1在细胞生长与信号传导功能基因的拷贝数显著高于group2(P<0.000 1),人源菌株显著多于动物源菌株(P<0.000 1)。group1在代谢功能基因的拷贝数显著高于group2(P<0.01),植物源菌株显著多于人源菌株(P<0.05)。猪源菌株相比于其他动物体内分离菌在COG功能注释大类上无显著差异(P>0.05)。
2.7 细菌素注释分析
将细菌素注释库比对结果转换为对应的细菌素基因簇相似片段在每个菌株基因组出现次数,基于此结果绘制热图,如附图4所示,在284株菌中鉴定出7种细菌素基因簇和1种假定细菌素基因簇。67株菌鉴定到1种细菌素基因簇,6株菌鉴定到2种细菌素基因簇。26.06%的P.acidilactici菌株注释到细菌素基因簇,59株菌(20.77%)中鉴定到Enterolysin A基因簇,其中P.acidilactici ACB04 包含2个Enterolysin A基因簇。11株菌(3.87%)中鉴定到Pediocin基因簇,3株菌(1.06%)中鉴定到了Bovicin基因簇,2株菌(0.70%)鉴定到了Penocin A基因簇。此外还鉴定到P.acidilactici携带Colicin B基因簇、Lanthipeptide_class_IV基因簇、Bacteriocin基因簇(0.35%)。
在2个遗传分支上,group1中19%的菌株注释到了细菌素基因簇,group2中29.9%的菌株注释到了细菌素基因簇。Penocin A基因簇只在group1中存在,且只在人源的菌株中存在。Bovicin基因簇、Colicin B基因簇、Lanthipeptide_class_IV基因簇、Bacteriocin基因簇只在group2中注释到。11株注释到Pediocin基因簇的菌株中除P.acidilactici 1001095A_150126_C3之外均位于group2。
45株动物体内分离的菌株中有20株(44.4%)菌注释到细菌素基因簇,包含8株鸡源菌株(40%),全部为enterolysin_A基因簇。7株牛源菌株(35%)中4株注释到enterolysin_A基因簇,3柱注释到Pediocin基因簇。3株(1.5%)猪源菌株分别注释到了enterolysin_A基因簇、Pediocin基因簇、Bacteriocin基因簇。1株(0.5%)獾源菌株和1株(0.5%)单峰驼源菌株均仅注释到enterolysin_A基因簇。16%人源菌株注释到细菌素基因簇,26.7%的植物来源菌株注释到细菌素基因簇。结果显示,动物源菌株具有更高的细菌素基因簇携带率,其可能是良好的益生菌来源。
3 讨论
益生菌通常应从同源宿主中分离和鉴定,以便更好地适应胃肠道更快地定植[29],发挥其益生特性。本研究对284株P.acidilactici基因组数据进行分析,探究其遗传背景进化历程,并对其功能基因进行注释。对泛核心基因集进行分析发现,P.acidilactici拥有开放的泛基因,表明其可能拥有高遗传多样性与较强的环境适应能力。这一结果与植物乳植杆菌和肺炎链球菌[30-31]相似。系统发育分析发现人源菌株与动物源菌株在整个发育树上有相对聚集趋势。动物源菌株聚集成了3个区域,可能是动物源菌株在适应不同环境过程中发生了适应性进化,导致了遗传上的差异和聚类。动物源菌株聚集的3个区域被人源菌株聚集隔开,且人源菌株聚集区域与其中一个动物源菌株聚集区域属于group1,可能暗示人源菌株和动物源菌株在进化过程中存在一定相互影响。植物源菌株穿插在动物源和人源菌株之间,可能是P.acidilactici的系统发育进化中植物源菌株与动物源、人源菌株间共享进化路径。植物源菌株可能在动物源和人源菌株的传播、演化过程中扮演了关键的桥梁角色。
对功能基因分析发现,P.acidilactici注释到的CAZys家族中多数都与利用植物源多糖有关[32],这与LI等[15]的研究结果一致。CBM54、CBM22、GH120等与来源于植物、乳中的碳水化合物的降解利用有关[33],GH35与GH70和乳糖半乳糖代谢利用有关[34]。人源菌株基因组中有关淀粉和蔗糖代谢的GT4、GH31的拷贝数显著多于动物源(P<0.05),动物源菌株基因组中有关纤维素降解的CE10的拷贝数显著多于人源菌株(P<0.000 1),且人源的菌株中88%的菌株分离自美国。这些结果表明菌株分解利用碳水化合物的基因拷贝数与其所处生存环境有关,可能与美国地区摄入的食物中淀粉蔗糖含量高、纤维素含量低有关[35]。
COG数据库的比对结果中显示,P.acidilactici参与代谢功能的基因比例最高,group1菌株在功能K族转录、O族翻译后修饰,蛋白质转换、T族信号转导上拷贝数显著多于group2,表明group1的菌株可能在对外界信号的接受和处理的功能潜力大。group2菌株在L族复制、重组与修复、V族防御机制、C族能量生产及保存、E族氨基酸转运及代谢上显著多于group1,表明group2可能在能量的生产与氨基酸代谢的功能潜力大。不同遗传分析出现组间差异的结果可能与生态位适应性进化有关。
相关研究发现,P.acidilactici所产生的细菌素具有改变小鼠肠道菌群[36]和抑制金黄色葡萄球菌[37]、鼠伤寒沙门氏菌[38]、粪肠球菌[39]等致病菌活性的能力。在细菌素注释结果中,74株菌注释到了细菌素。Enterolysin A细菌素对肠杆菌、枯草芽孢杆菌、金黄色葡萄球菌属等具有抑制作用[40]。通常由片球菌属产生Pediocin细菌素可以抑制食品乳制品中常见的腐败菌和病原菌的生长[41-42]。在李真真[11]研究中P.acidilactici所注释到的3种细菌素基因簇本研究均注释到。本研究发现动物源菌株细菌素基因簇携带率最高,表明动物源P.acidilactici是良好的益生菌来源。但需要注意的是,注释到的细菌素基因簇是否实际表达尚不得而知,这可能需要进一步的实验验证。
猪源菌株与其他动物体内分离株在基因组基本信息与COG功能大类上均无显著差异(P>0.05),但基因组中部分CAZys的家族拷贝数存在显著差异(P<0.05),在细菌素的结果中鸡、牛、猪分离株相比于其他动物体内分离株注释到了更多的细菌基因簇。可能是猪源菌株发生了生境适应性进化,导致与其他动物体内分离源菌株产生了差异。
4 结论
本研究分离的9株P.acidilactici 与NCBI数据库的275株进行比较基因组学分析,发现P.acidilactici拥有一个开放的泛基因组。284株P.acidilactici分为了2个遗传分支,本实验分离鉴定的9株P.acidilactici聚集于同一分支,GC含量与CDS数量与其他菌株无显著性差异,CAZys注释结果中CBM11、CBM58家族仅在9株P.acidilactici注释到,细菌素基因簇注释结果中,Bacteriocin细菌素基因簇相似片段仅在IMAU16171基因组中出现。人源菌株与动物源菌株在系统发育树上有相对聚集趋势。不同遗传分支表现出了不同的基因组特征,动物源P.acidilactici在基因组大小、GC含量、CDS数量均显著大于人源菌株(P<0.001)。动物源菌株中有关淀粉和蔗糖代谢的CAZys家族显著少于人源菌株(P<0.05),有关纤维素降解的CAZys家族则相反(P<0.000 1)。动物源菌株COG注释信息储存与处理的拷贝数显著多于人源菌株(P<0.000 1),细胞生长与信号传导的拷贝数则相反(P<0.000 1)。猪源菌株GT2、GT4、GT26拷贝数上显著多于其他动物体内分离株(P<0.05),CE10、GH43拷贝数上则相反(P<0.05)。此外,动物源菌株相比于其他分离源具有更高的细菌素基因簇携带率。以上结果表明P.acidilactici在不同生态环境下发生了适应性进化。本研究结果为探明P.acidilactici的生境适应性进化提供了数据支持。
[1] TIAN P J, CHEN Y, QIAN X, et al.Pediococcus acidilactici CCFM6432 mitigates chronic stress-induced anxiety and gut microbial abnormalities[J].Food &Function, 2021, 12(22):11241-11249.
[2] JANG H M, KIM J K, JOO M K, et al.Enterococcus faecium and Pediococcus acidilactici deteriorate Enterobacteriaceae-induced depression and colitis in mice[J].Scientific Reports, 2022, 12:9389.
[3] QIAO Y T, QIU Z C, TIAN F W, et al.Pediococcus acidilactici strains improve constipation symptoms and regulate intestinal flora in mice[J].Frontiers in Cellular and Infection Microbiology, 2021, 11:655258.
[4] JEONG D Y, RYU M S, YANG H J, et al.Pediococcus acidilactici intake decreases the clinical severity of atopic dermatitis along with increasing mucin production and improving the gut microbiome in Nc/Nga mice[J].Biomedicine &Pharmacotherapy, 2020, 129:110488.
[5] WIDODO W, KUSUMANINGRUM H R P, WIHADMADYATAMI H, et al.Milk fermented with Pediococcus acidilactici strain BE improves high blood glucose levels and pancreatic beta-cell function in diabetic rats[J].Food Science of Animal Resources, 2023, 43(1):170-183.
[6] DOWARAH R, VERMA A K, AGARWAL N, et al.Selection and characterization of probiotic lactic acid bacteria and its impact on growth, nutrient digestibility, health and antioxidant status in weaned piglets[J].PLoS One, 2018, 13(3):e0192978.
[7] LIM F T, LIM S M, RAMASAMY K.Pediococcus acidilactici LAB4 and Lactobacillus plantarum LAB12 assimilate cholesterol and modulate ABCA1, CD36, NPC1L1 and SCARB1 in vitro[J].Beneficial Microbes, 2017, 8(1):97-109.
[8] FENG J C, WANG L H, ZHOU L X, et al.Using in vitro immunomodulatory properties of lactic acid bacteria for selection of probiotics against Salmonella infection in broiler chicks[J].PLoS One, 2016, 11(1):e0147630.
[9] ALI A M M, GULLO M, RAI A K, et al.Bioconservation of iron and enhancement of antioxidant and antibacterial properties of chicken gizzard protein hydrolysate fermented by Pediococcus acidilactici ATTC 8042[J].Journal of the Science of Food and Agriculture, 2021, 101(7):2718-2726.
[10] BAI Y Y, LUO B L, ZHANG Y, et al.Exopolysaccharides produced by Pediococcus acidilactici MT41-11 isolated from camel milk:Structural characteristics and bioactive properties[J].International Journal of Biological Macromolecules, 2021, 185:1036-1049.
[11] 李真真. 乳酸片球菌JQⅡ-5的全基因组测序与比较基因组学分析[D].郑州:郑州大学, 2021.
LI Z Z.Complete genome sequencing and comparative genomic analysis of Pediococcus acidilactici JQⅡ-5[D].Zhengzhou:Zhengzhou University, 2021.
[12] MUYNARSK E S M, DE MELO PEREIRA G V, MESA D, et al.Draft genome sequence of Pediococcus acidilactici strain LPBC161, isolated from mature coffee cherries during natural fermentation[J].Microbiology Resource Announcements, 2019, 8(16):e00332-19.
[13] ZHAO M D, LIU K Y, ZHANG Y Y, et al.Probiotic characteristics and whole-genome sequence analysis of Pediococcus acidilactici isolated from the feces of adult beagles[J].Frontiers in Microbiology, 2023, 14:1179953.
[14] RANJAN R, PANDIT R J, DUGGIRALA S M, et al.Genome sequencing of Pediococcus acidilactici (NRCC1), a novel isolate from dromedary camel (Camelus dromedarius) rumen fluid[J].Annals of Microbiology, 2018, 68(2):103-110.
[15] LI Z Z, SONG Q, WANG M M, et al.Comparative genomics analysis of Pediococcus acidilactici species[J].Journal of Microbiology, 2021, 59(6):573-583.
[16] ALIKHAN N F, PETTY N K, BEN ZAKOUR N L, et al.BLAST Ring Image Generator (BRIG):Simple prokaryote genome comparisons[J].BMC Genomics, 2011, 12:402.
[17] RICHTER M, ROSSELL -M
-M RA R, OLIVER GLÖCKNER F, et al.JSpeciesWS:A web server for prokaryotic species circumscription based on pairwise genome comparison[J].Bioinformatics, 2016, 32(6):929-931.
RA R, OLIVER GLÖCKNER F, et al.JSpeciesWS:A web server for prokaryotic species circumscription based on pairwise genome comparison[J].Bioinformatics, 2016, 32(6):929-931.
[18] LI Y, GUO X Q, PENG Q T, et al.Culturomics:A promising approach for exploring bacterial diversity in natural fermented milk[J].Food Bioscience, 2024, 62:105383.
[19] LUO R B, LIU B H, XIE Y L, et al.SOAPdenovo2:An empirically improved memory-efficient short-read de novo assembler[J].GigaScience, 2012, 1(1):2047-217X-1-18.
[20] PARKS D H, IMELFORT M, SKENNERTON C T, et al.CheckM:Assessing the quality of microbial genomes recovered from isolates, single cells, and metagenomes[J].Genome Research, 2015, 25(7):1043-1055.
[21] SEEMANN T.Prokka:Rapid prokaryotic genome annotation[J].Bioinformatics, 2014, 30(14):2068-2069.
[22] PAGE A J, CUMMINS C A, HUNT M, et al.Roary:Rapid large-scale prokaryote pan genome analysis[J].Bioinformatics, 2015, 31(22):3691-3693.
[23] JAIN C, RODRIGUEZ-R L M, PHILLIPPY A M, et al.High throughput ANI analysis of 90K prokaryotic genomes reveals clear species boundaries[J].Nature Communications, 2018, 9:5114.
[24] TATUSOV R L, FEDOROVA N D, JACKSON J D, et al.The COG database:An updated version includes eukaryotes[J].BMC Bioinformatics, 2003, 4:41.
[25] CIUFO S, KANNAN S, SHARMA S, et al.Using average nucleotide identity to improve taxonomic assignments in prokaryotic genomes at the NCBI[J].International Journal of Systematic and Evolutionary Microbiology, 2018, 68(7):2386-2392.
[26] LI J H, MAU R L, DIJKSTRA P, et al.Predictive genomic traits for bacterial growth in culture versus actual growth in soil[J].The ISME Journal, 2019, 13(9):2162-2172.
[27] 刘旭. 植物乳植杆菌群体遗传学及功能基因组学研究[D].呼和浩特:内蒙古农业大学, 2023.
LIU X.Study on population geneties and functional genomic of Lactiplantibacillus plantarum[D].Hohhot:Inner Mongolia Agricultural University, 2021.
[28] 阎春兰, 余福燕, 王艺霏, 等.耐盐芽孢杆菌SF-18的生防潜能与基因组学分析[J].华中农业大学学报, 2024, 43(4):192-203.
YAN C L, YU F Y, WANG Y F, et al.Biocontrol potential and genomic analysis of salt tolerant bacterium Bacillus sp.SF-18[J].Journal of Huazhong Agricultural University, 2024, 43(4):192-203.
[29] ARGYRI A A, ZOUMPOPOULOU G, KARATZAS K G, et al.Selection of potential probiotic lactic acid bacteria from fermented olives by in vitro tests[J].Food Microbiology, 2013, 33(2):282-291.
[30] BAZINET A L.Pan-genome and phylogeny of Bacillus cereus sensu lato[J].BMC Evolutionary Biology, 2017, 17(1):176.
[31] 杨淑娟, 周金萍, 李海燕, 等.基于比较基因组学解析植物乳植杆菌ST的功能基因组[J].食品科学, 2023, 44(14):86-93.
YANG S J, ZHOU J P, LI H Y, et al.Comparative genomic analysis of functional genomics of Lactiplantibacillus plantarum ST[J].Food Science, 2023, 44(14):86-93.
[32] WARDMAN J F, BAINS R K, RAHFELD P, et al.Carbohydrate-active enzymes (CAZymes) in the gut microbiome[J].Nature Reviews Microbiology, 2022, 20(9):542-556.
[33] BORASTON A B, BOLAM D N, GILBERT H J, et al.Carbohydrate-binding modules:Fine-tuning polysaccharide recognition[J].The Biochemical Journal, 2004, 382(Pt 3):769-781.
[34] MENG X F, GANGOITI J, BAI Y X, et al.Structure-function relationships of family GH70 glucansucrase and 4, 6-α-glucanotransferase enzymes, and their evolutionary relationships with family GH13 enzymes[J].Cellular and Molecular Life Sciences, 2016, 73(14):2681-2706.
[35] AAKKO J, PIETIL S, TOIVONEN R, et al.A carbohydrate-active enzyme (CAZy) profile links successful metabolic specialization of Prevotella to its abundance in gut microbiota[J].Scientific Reports, 2020, 10:12411.
S, TOIVONEN R, et al.A carbohydrate-active enzyme (CAZy) profile links successful metabolic specialization of Prevotella to its abundance in gut microbiota[J].Scientific Reports, 2020, 10:12411.
[36] QIAO Y T, QIU Z C, TIAN F W, et al.Effect of bacteriocin-producing Pediococcus acidilactici strains on the immune system and intestinal flora of normal mice[J].Food Science and Human Wellness, 2022, 11(2):238-246.
[37] KIM J H, AHN H, LEE D, et al.Antibiofilm activity of crude bacteriocin JM01 produced by Pediococcus acidilactici against methicillin-resistant Staphylococcus aureus (MRSA)[J].International Journal of Food Science &Technology, 2023, 58(5):2580-2589.
[38] SEO H J, KANG S S.Inhibitory effect of bacteriocin produced by Pediococcus acidilactici on the biofilm formation of Salmonella Typhimurium[J].Food Control, 2020, 117:107361.
[39] YOON J W, KANG S S.In vitro antibiofilm and anti-inflammatory properties of bacteriocins produced by Pediococcus acidilactici against Enterococcus faecalis[J].Foodborne Pathogens and Disease, 2020, 17(12):764-771.
[40] WU Y J, PANG X X, WU Y S, et al.Enterocins:Classification, synthesis, antibacterial mechanisms and food applications[J].Molecules, 2022, 27(7):2258.
[41] NIETO-LOZANO J C, REGUERA-USEROS J I, DEL C PEL EZ-MART
EZ-MART NEZ M, et al.The effect of the pediocin PA-1 produced by Pediococcus acidilactici against Listeria monocytogenes and Clostridium perfringens in Spanish dry-fermented sausages and frankfurters[J].Food Control, 2010, 21(5):679-685.
NEZ M, et al.The effect of the pediocin PA-1 produced by Pediococcus acidilactici against Listeria monocytogenes and Clostridium perfringens in Spanish dry-fermented sausages and frankfurters[J].Food Control, 2010, 21(5):679-685.
[42] UEDA T, TATEGAKI A, HAMADA K, et al.Effects of Pediococcus acidilactici R037 on serum triglyceride levels in mice and rats after oral administration[J].Journal of Nutritional Science and Vitaminology, 2018, 64(1):41-47.