根据国际益生菌和益生元科学协会2021年发布的后生元共识声明[1],后生元是指对宿主健康有益的遗传背景明确的灭活微生物和/或菌体成分,包括或不包括其代谢产物。其主要成分包括灭活的菌体细胞、菌体成分及菌体代谢产物,其中菌体成分包括脂磷壁酸、肽聚糖、细胞表面蛋白等,菌体代谢产物包括胞外多糖、短链脂肪酸、蛋白质/多肽以及有机酸等。根据微生物的类型、菌株和代谢产物的不同,后生元的效果也不同[2]。已有研究表明[3-5],后生元在体内发挥预防和治疗双重作用,如免疫调节、预防感染、抗菌、抗氧化、抗肿瘤和减少食物过敏等作用,且在婴儿绞痛、成人特应性皮炎和腹泻等功能方向已进入临床研究阶段。除具有多种功效外,与益生菌相比,后生元还具有多种优势:一是具有更高的安全性,后生元对一些特殊人群如新生儿、肠道功能受损人群以及一些敏感人群同样适应,而且后生元不受抗生素的干扰抑制,没有传递耐药基因风险;二是具有更高的稳定性,不易受温度、pH等外界因素影响,且可以耐受高温、氧气等环境,具有更长的保质期,以及便于储存与运输;三是具有更广泛的作用靶点,不仅限于肠道,口腔、皮肤、泌尿生殖道及鼻咽等都可作为后生元的靶点,而且更易于被肠道吸收,提高利用率。因此,后生元被认为是天然的抗炎剂、抗氧化剂和抗菌剂等,被广泛应用于食品、药品等领域。
溃疡性结肠炎(ulcerative colitis, UC)是一种炎症性肠病,主要表现为肠道黏膜慢性及反复性炎症,主要症状是腹泻、腹痛、血便、疲劳和体重减轻[6]。目前UC症状主要依赖抗炎药物和免疫抑制剂等进行缓解,但长期使用易引发胃肠道不适、免疫抑制、感染风险增加等不良反应,因此,挖掘安全、有效、稳定的功能性成分用于UC的预防或辅助治疗成为当前研究的重要方向[7]。最近诸多研究提示肠道菌群失调和代谢物紊乱在UC发病机制中的核心作用,包括肠道微生物群多样性减少、厚壁菌门丰度降低以及拟杆菌门和放线菌门丰度增加等[7-8]。益生菌作为调节肠道微生态的热门功能性成分,在UC防治中的作用已有较多的研究与报道[9],长双歧杆菌长亚种(Bifidobacterium longum subsp. longum)作为人体肠道内的优势共生菌,其可通过下调促炎因子(如IL-6、TNF-α)、上调抗炎因子(如IL-10)、优化肠道菌群结构(如增加有益菌丰度、减少致病菌比例)等方式缓解UC症状[10]。然而,益生菌作为活菌产品,在肠道功能受损、部分免疫功能低下等人群中可能面临活菌感染风险,这很大程度上制约了其在预防或治疗结肠炎方面的应用[11-12]。
基于此,本研究以长双歧杆菌长亚种HSBL001制备的后生元为材料,在葡聚糖硫酸钠(dextran sulfate sodium, DSS)诱导的UC小鼠模型中,系统评价其对UC症状的改善作用,并结合宏基因组学与代谢组学技术揭示其潜在机制。
1 材料与方法
1.1 材料与试剂
长双歧杆菌长亚种HSBL001菌株保藏在中国普通微生物菌种保藏管理中心,编号为CGMCC No.31244;SPF级6~8周龄C57BL/6雄鼠,江苏华创信诺医药科技有限公司;SPF维持饲料、SPF玉米芯垫料,科澳协力饲料有限公司;DSS(分子质量36~50 kDa),美国MP Biomedicals公司;MRS培养基,青岛海博生物技术有限公司;乳酸标准品,美国Sigma公司;乙酸、琥珀酸标准品,上海麦克林生化科技股份有限公司;小鼠TNF-α、IL-6、IL-10 ELISA试剂盒,上海酶联生物科技有限公司;DNA提取试剂盒(QIAamp® Fast DNA Stool Mini Kit),德国Qiagen公司;文库制备试剂盒(TruSeq Nano DNA LT Sample Prepararion Kit),美国Illumina公司;苏木素染液,北京中杉金桥生物技术有限公司;苏木素返蓝液,武汉塞维尔生物科技有限公司;伊红染色液,北京索莱宝科技有限公司;4 %多聚甲醛溶液,Biosharp公司;二甲苯、无水乙醇、95%乙醇等其他化学试剂,西陇科学股份有限公司。
1.2 仪器与设备
HFsafe-1500LC生物安全柜,上海力康科学仪器有限公司;LDZF-50L-3立式蒸汽灭菌锅,上海申安医疗器械厂;ST1R Plus台式冷冻离心机,美国Thermo Fisher公司;DHG-9240A烘箱,上海一恒科学仪器有限公司;ZQZY-85BN恒温振荡培养箱,上海知楚仪器有限公司;FE28型pH计,瑞士梅特勒-托雷多集团;1260高效液相色谱仪,美国Agilent公司;发酵罐,江苏科海生物工程设备有限公司;EnSight多功能酶标仪,美国PerkinElmer公司;KD-TS3S1组织脱水机,浙江省金华市科迪仪器设备有限公司;HistoCore Arcadia石蜡包埋机、HistoCore BIOCUT切片机、HI1210摊片机,德国莱卡公司。
1.3 实验方法
1.3.1 长双歧杆菌长亚种HSBL001后生元制备
脱脂乳粉和豆粉用温水溶解,经过蛋白酶酶解后在蒸汽灭菌锅中杀菌灭酶30 min,冷却后接种长双歧杆菌长亚种HSBL001菌种,在厌氧条件下37 ℃、180 r/min发酵48 h。发酵结束后进行热灭活(85 ℃,30 min),过胶体磨后进行喷雾干燥得到长双歧杆菌长亚种HSBL001后生元。
1.3.2 有机酸含量检测
使用BIO-RAD Aminex® HPX-87H (300 mm×7.8 mm)色谱柱,流动相为5 mmol/L的H2SO4溶液,流速0.6 mL/min,柱温45 ℃,检测器波长为210 nm。样品适当稀释后,离心取上清液过0.22 μm滤膜后上机检测,根据标准曲线计算各有机酸含量。
1.3.3 动物实验
1.3.3.1 动物分组及给药
所有动物护理及实验程序均获得江中药业股份有限公司实验动物伦理委员会批准(批件号:20240903)。18只SPF级6周龄C57BL/6雄鼠(19 g~21 g),饲养在温度为 20~24 ℃的动物屏障中,适应性饲养7 d后进行随机分组(对照组、模型组、HSBL001组),每组6只。从第0天到第7天,对照组和模型组小鼠灌胃1 mL PBS,HSBL001组灌胃长双歧杆菌长亚种HSBL001后生元(1 g/kg BW),期间饮用纯水。从第8天到第14天,灌胃程序不变,模型组和HSBL001组饮用水换成2.5%(质量分数,下同)DSS溶液。第14天灌胃结束后禁食不禁水,在第15天摘眼球取血后立即处死小鼠,收集结肠组织、盲肠内容物和脾脏。
1.3.3.2 疾病活动指数(disease activity index, DAI)
DAI评分参考文献方法[7],按公式(1)计算:
(1)
体重下降评分(0为无减轻;1为1%~5%;2为5%~10%;3为10%~20%;4为>20%),直肠出血评分(0=粪便未见出血;1=粪便略微带血;2=粪便一些带血;3=粪便较多带血;4=粪便大量带血);粪便性状评分(0=正常粪便;1=轻微稀便;2=稀便;3=水样粪便;4=严重拉稀)。
1.3.3.3 炎症因子含量检测
采集的小鼠血液以3 500 r/min离心10 min后分装血清。小鼠血清中的TNF-α、IL-6 和 IL-10的含量根据ELISA试剂盒的说明,先绘制标准曲线,然后将血清稀释2倍后进行检测,单位为pg/mL。
1.3.3.4 苏木精-伊红(hematoxylin-eosin,HE)染色
小鼠解剖后取一段远端结肠组织,立即用0.04 g/mL多聚甲醛溶液固定。经石蜡包埋、切片及HE染色后,脱水封片再用显微镜进行观察拍照。
1.3.4 宏基因组测序分析
收集的小鼠盲肠内容物贮存在-80 ℃冰箱,解冻后使用DNA提取试剂盒提取小鼠粪便中总DNA,琼脂糖凝胶电泳和NanoDrop2000分光光度计检测 DNA的完整性和浓度测定。合格的DNA样本进行片段化处理,纯化后采用TruSeq Nano DNA LT Sample Prepararion Kit试剂盒进行文库构建。测序由上海欧易生物医学科技有限公司在llumina Novaseq 6000测序平台进行,并通过NR库对应的分类学信息数据库获得物种注释,然后使用物种对应的基因丰度综合计算该物种的丰度,原始数据在云平台https://cloud.oebiotech.com/上进行分析及可视化处理。
1.3.5 非靶向代谢组学分析
在低温下称取20 mg小鼠盲肠内容物至EP管中,加入2个均质珠小钢珠,并加入300 μL含有同位素标记内标(甲醇∶水=4∶1,体积比)的提取溶液中。将混合物涡旋30 s,在均质机中以45 Hz均质2 min,然后转移到冰水浴中超声波处理10 min,在-40 ℃下静置过夜。样品在4 ℃下以12 000 r/min离心20 min,收集上清液进行上机检测,所有样本的提取液等体积混合制备成质控样本(quality control,QC)。样品和QC使用液相色谱-质谱联用仪Waters ACQUITY UPLC I-Class plus/Thermo QE HF,ACQUITY UPLC HSS T3(100 mm×2.1 mm, 1.8 um)色谱柱,以A水(含体积分数为0.1%甲酸)、B乙腈为流动相进行检测分析。样品托盘保持在4 ℃,进样体积设置为2 μL。随后,对数据进行预处理、实验质量控制、代谢物鉴定分析、表达丰度分析、2组间比较分析。数据在云平台https://cloud.oebiotech.com/上进行分析及可视化处理。
1.4 数据处理
数据分析和绘图使用GraphPad Prism 8.3.0完成,对各组数据进行单因素方差分析(ANOVA)分析,采用图基(Tukey)检验方法,结果表示为“平均值±标准差”。P<0.05表示差异显著。
2 结果与分析
2.1 HSBL001理化指标及成分分析
长双歧杆菌长亚种HSBL001在脱脂乳-豆粉基质中能较好地增殖并积累代谢产物,如表1所示,发酵液活菌数为40.0×108 CFU/mL,进行热灭活并干燥后得到的后生元菌体数为285.7×108 cells/g。HSBL001后生元除了含有大量的灭活菌体外,还含有丰富的有机酸/短链脂肪酸等代谢产物,其酸度值为914.3 T,其中乳酸、乙酸和琥珀酸含量分别为42.44、32.27、19.36 g/kg。
T,其中乳酸、乙酸和琥珀酸含量分别为42.44、32.27、19.36 g/kg。
表1 HSBL001主要成分分析
Table 1 Main component analysis of HSBL001

项目数值菌体数/(×108 cells/g)285.7∗酸度/(°T)914.3乳酸/(g/kg)42.44乙酸/(g/kg)32.27琥珀酸/(g/kg)19.36
注:*表示根据发酵终点发酵液的活菌数估算的理论值,菌体数(×108 cells/g)=发酵液活菌数(×108 CFU/mL)/发酵液固形物含量,其中发酵液固形物含量为14%。
2.2 HSBL001对DSS诱导的结肠炎的影响
由图1可以看出,模型组小鼠具有典型的结肠炎症状,包括体重减轻、腹泻和便血(DAI评分升高),以及与对照组相比有显著的结肠长度缩短(P<0.01)、脾脏肿大的症状。经过HSBL001后生元干预后,不同程度的逆转了这些症状,从体重变化曲线(图1-a)看,HSBL001后生元组比DSS组体重降低量更少。DAI 评分(图1-b)与DSS相比有显著降低(P<0.01),DSS组在第14天DAI评分达到最高2.42±0.55,灌胃HSBL001后生元后,小鼠便血、水样粪便程度减少,DAI评分降低至1.46±0.50。结肠缩短是结肠炎的常见症状之一,主要由结肠充血、炎症和水肿引起,由图1-c可知,经DSS造模后,小鼠结肠长度缩短至(5.42±0.50) cm,HSBL001后生元组显著缓解了这一症状,使小鼠结肠长度恢复至(6.26±0.16) cm。此外,HSBL001后生元干预显著缓解了DSS诱导的脾肿大,降低了脾指数(图1-d),恢复小鼠免疫应答。对小鼠远端结肠组织进行HE染色,以评估小鼠结肠损伤程度,对照小鼠表现出正常的结肠形态,具有丰富的杯细胞、完整的黏膜和薄的肌肉层。经DSS处理后小鼠的结肠显示出明显的损伤,上皮表面呈溃烂弥散状,杯细胞消失,隐窝变形,固有肌层增厚的水肿和炎症细胞浸润的增强(图1-e)。对比DSS组,HSBL001后生元组在黏膜溃疡、隐窝损伤等方面具有明显改善。综合上述指征可以得出,HSBL001后生元可显著缓解DSS诱导的小鼠的结肠炎症状。
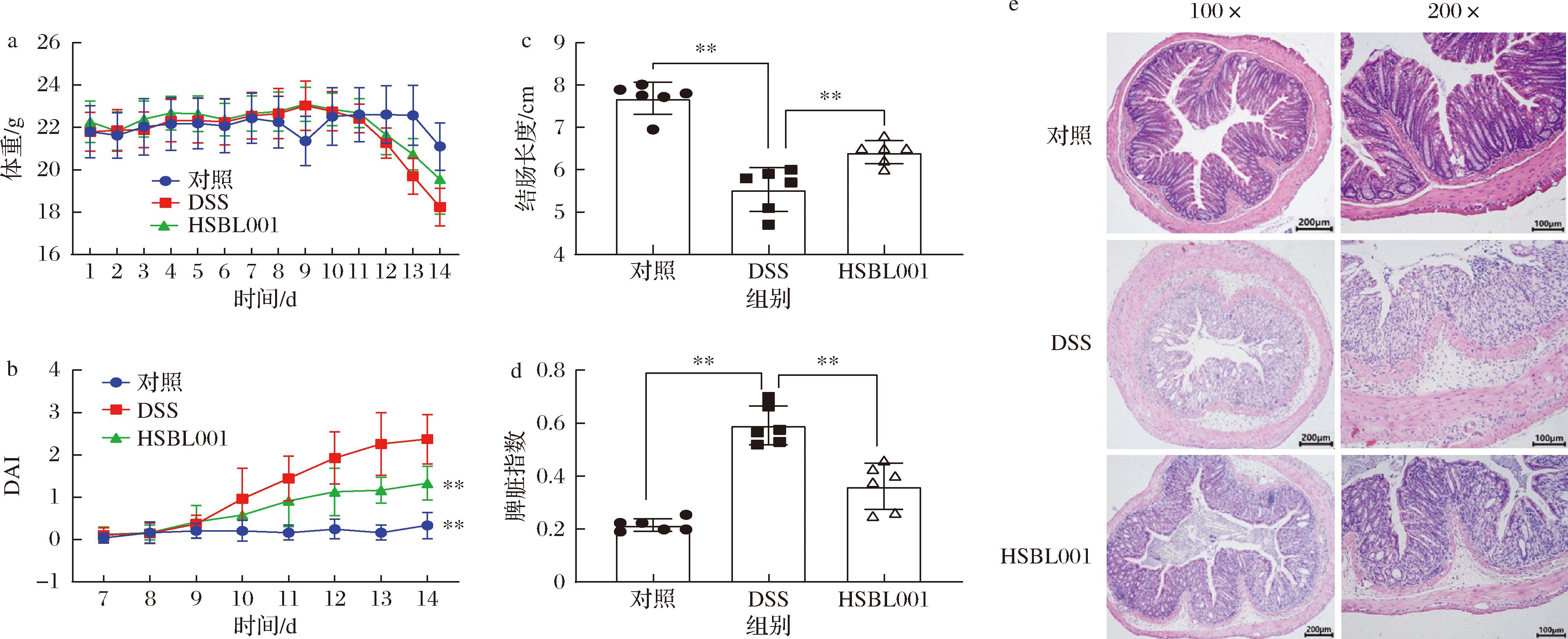
a-体重变化;b-DAI评分;c-结肠长度;d-脾脏指数;e-远端结肠组织HE染色分析结肠组织的病理变化
图1 HSBL001对DSS诱导的小鼠溃疡性结肠炎症状的影响
Fig.1 Effects of HSBL001 on symptoms of DSS-induced colitis in mice
注:与DSS组相比,ns表示无显著性差异,*P<0.05,**P<0.01(下同)。
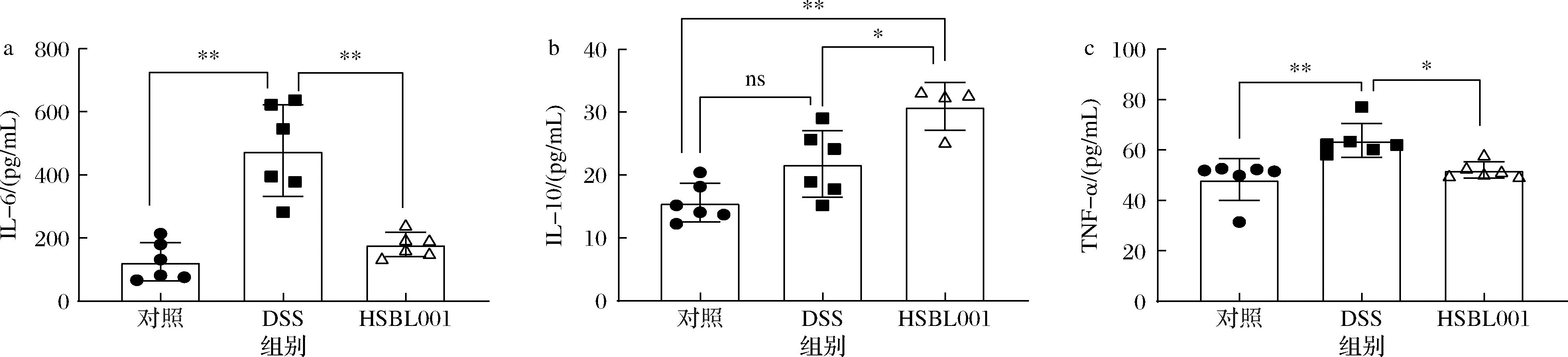
a-IL-6;b-IL-10;c-TNF-α
图2 HSBL001对小鼠血清中炎症因子水平的影响
Fig.2 Effects of HSBL001 on inflammatory factors in serum
2.3 HSBL001对小鼠血清中炎症因子水平的影响
通过ELISA试剂盒测定小鼠血清中的TNF-α、IL-6 和 IL-10的水平,如图2所示,DSS组与对照组相比,IL-6和TNF-α水平显著升高(P<0.001),分别升高2.83倍和0.32倍,而经HSBL001后生元干预后,与DSS组相比,这2种炎症因子的水平显著降低,使其含量恢复到了对照组水平。另外,HSBL001后生元还能显著提升抗炎因子IL-10的水平(P<0.05),说明HSBL001后生元具有较好的抗炎功效。
2.4 HSBL001对肠道菌群的影响
应用宏基因组测序分析HSBL001干预后对小鼠粪便肠道菌群的影响。对不同处理组之间的小鼠肠道菌群α多样性指数进行分析,DSS组Shannon指数升高,HSBL001干预后Shannon指数降低并趋于对照组,但组间无显著差异,表明HSBL001对肠道菌群的丰富度或均匀度有一定调节作用(图3-a)。利用Bray-Curtis距离算法进行主坐标分析(图3-b),结果显示,DSS组、HSBL001干预和对照组分别聚集在不同象限,3组小鼠之间的肠道菌群组成存在明显差异。本研究进一步从更精细的分类学水平上对肠道微生物群的变化进行分析,通过对菌群进行分类学注释,表明拟杆菌门(Bacteroidota)和厚壁菌门(Bacillota A、Bacillota)在所有组中占优势,占肠道微生物群总数的80%以上(图3-c),拟杆菌门/厚壁菌门比率的变化被视为肠道菌群失调的重要特征。与对照组相比,DSS组小鼠拟杆菌门明显减少以及厚壁菌门明显增加,但HSBL001干预后基本扭转这一变化,说明补充HSBL001能够调节DSS导致的肠道菌群失衡。为了进一步鉴定3组之间显著差异的微生物群类,本研究对3个处理组的差异菌群从门到属进行LEfSe分析(图3-d),将LDA 截止值设置为4共筛选得到28个显著改变的微生物群类,其中对照组有9个,DSS组有14个,HSBL001组有5个,对照组丰度差异较大的群类为鼠类杆菌科(f_Muribaculaceae)、拟杆菌目(o_Bacteroidales)、拟杆菌纲(c_Bacteroidia),DSS组丰度差异较大的菌群为梭状芽孢杆菌纲(c_Clostridia)、毛螺菌科(f_Lachnospiraceae)、毛螺旋菌目(o_Lachnospirales),HSBL001干预后丰度差异较大的菌群为拟杆菌科(f_Bacteroidaceae)、拟杆菌属(g_Bacteroides)和g_Odoribacter。对属级丰度进行差异筛选,前20个属进行了注释(图3-f),HSBL001后生元干预后,不仅能提高小鼠肠道中杜氏杆菌属(Duncaniella)、Alistipes、Odoribacter、普雷沃氏菌属(Prevotella)等属的丰度,还能逆转DSS造模引起Mucispirillum、Pelethomonas、Acetatifactor等属的丰富升高。

a-α多样性指数(Simpson和Shannon);b-β多样性分析;c-门水平差异群落分析;d-基于LefSe分析组间差异群落;e-种水平差异分析;f-属水平差异分析
图3 HSBL001对小鼠肠道微生物群的影响
Fig.3 Effects of HSBL001 on the gut functional microbial metagenome
此外,本研究筛选出在种水平上组间具有显著差异的物种,并进行Log10转换和均一化后对丰度TOP20绘制物种差异热图(图3-e)。结果表明,与对照组相比,DSS组的Paramuribaculum intestinale、Duncaniella dubosii、Duncaniella sp.001689575和Alistipes sp.002358415等菌丰度显著降低,而Mucispirillum schaedleri、Pumilibacter muris等菌的丰度显著升高,灌胃HSBL001后生元后显著逆转了上述菌的变化趋势,恢复了肠道稳态。另外,与DSS组相比,灌胃HSBL001后生元还能显著提高Bacteroides caecimuris、多形拟杆菌(Bacteroides thetaiotaomicron)等菌的丰度,这些菌的丰度变化可能与 HSBL001缓解结肠炎的机制有关。
2.5 HSBL001对小鼠粪便代谢组的影响
为了分析HSBL001对肠道代谢产物的影响,使用UPLC-MS/MS对小鼠粪便进行非靶向代谢组学分析。在3组样品中共鉴定出4 783种代谢物。在正离子模式下检测到2 352种代谢物,在负离子模式下检测到2 431种代谢物,鉴定出的前5种代谢物分别是羧酸及其衍生物、脂肪酰基类、类固醇和类固醇衍生物、异戊烯醇脂质和有机氧化合物,分别占总代谢物的18.80%、14.23%、11.57%、7.50%和7.40%。采用偏最小二乘法判别分析对照组、模型组以及HSBL001组之间的代谢物差异(图4-a),3组代谢物均表现出明显的聚类差异,表明模型组小鼠与正常小鼠以及与HSBL001干预之后代谢组学存在显著差异。从火山图(图4-b)和差异物热图(图4-c)可以看出,DSS诱导了718种代谢物的显著上调,以及1 303种代谢物的显著下调,其中牛磺胆酸、牛磺脱氧胆酸、牛磺熊去氧胆酸、熊去氧胆酸、脱氢石胆酸和甘氨脱氧胆酸等多种胆汁酸显著下调。结肠炎小鼠经HSBL001干预后,显著上调了95种代谢物,包括S-亚硝基谷胱甘肽、α-亚麻酸、肉豆蔻酰甘氨酸和7α-羟基-3-氧代胆甾-4-烯-27-酸等,以及显著下调了80种,包括3-羟基异戊酸、3-脱氧葡萄糖醛酮和N-乙酰葡糖胺醇等。随后,以HSBL001组与DSS组之间的差异代谢物进行通路富集分析,结果显示(图4-g)HSBL001主要涉及调节初级胆汁酸生物合成、鞘脂代谢、α-亚麻酸代谢等代谢通路。

a-偏最小二乘法判别分析;b-对照vs DSS的差异代谢物火山图;c-HSBL001 vs DSS的差异代谢物火山图;d-对照和DSS组差异代谢物聚类热图分析;e-HSBL001和DSS组差异代谢物聚类热图分析;f-α-亚麻酸、肉豆蔻酰甘氨酸、S-亚硝基谷胱甘肽和7α-羟基-3-氧代胆甾-4-烯-27-酸在3组小鼠中的丰度差异分析;g-差异代谢物KEGG通路富集分析
图4 HSBL001对小鼠粪便代谢组的影响
Fig.4 Effects of HSBL001 on the fecal metabolome of mice
2.6 HSBL001对小鼠粪便代谢物与菌群的相关性分析
利用Spearman相关性分析了HSBL001后生元干预对结肠炎小鼠微生物种水平变化与代谢物之间的潜在关联。如图5所示,(5Z)-13-羧基十三碳-5-烯酰基肉碱、7α-羟基-3-氧代胆甾-4-烯-27-酸、N-棕榈酰天冬酰胺和α-亚麻酸等多种代谢物与T.muris、啮齿粪杆菌(Faecalibaculum rodentium)、Paramuribaculum intestinale和Duncaniella sp.001689575等菌具有显著正相关性,与M.schaedleri等菌呈显著负相关。22-羟基维生素D3、甘氨酰酪氨酸、S-亚硝基谷胱甘肽和硫胺素等代谢物在结肠炎小鼠中的含量较低,而HSBL001后生元干预后显著升高,这与B.caecimuris和B.thetaiotaomicron等菌的丰度变化呈显著正相关(P<0.05)。
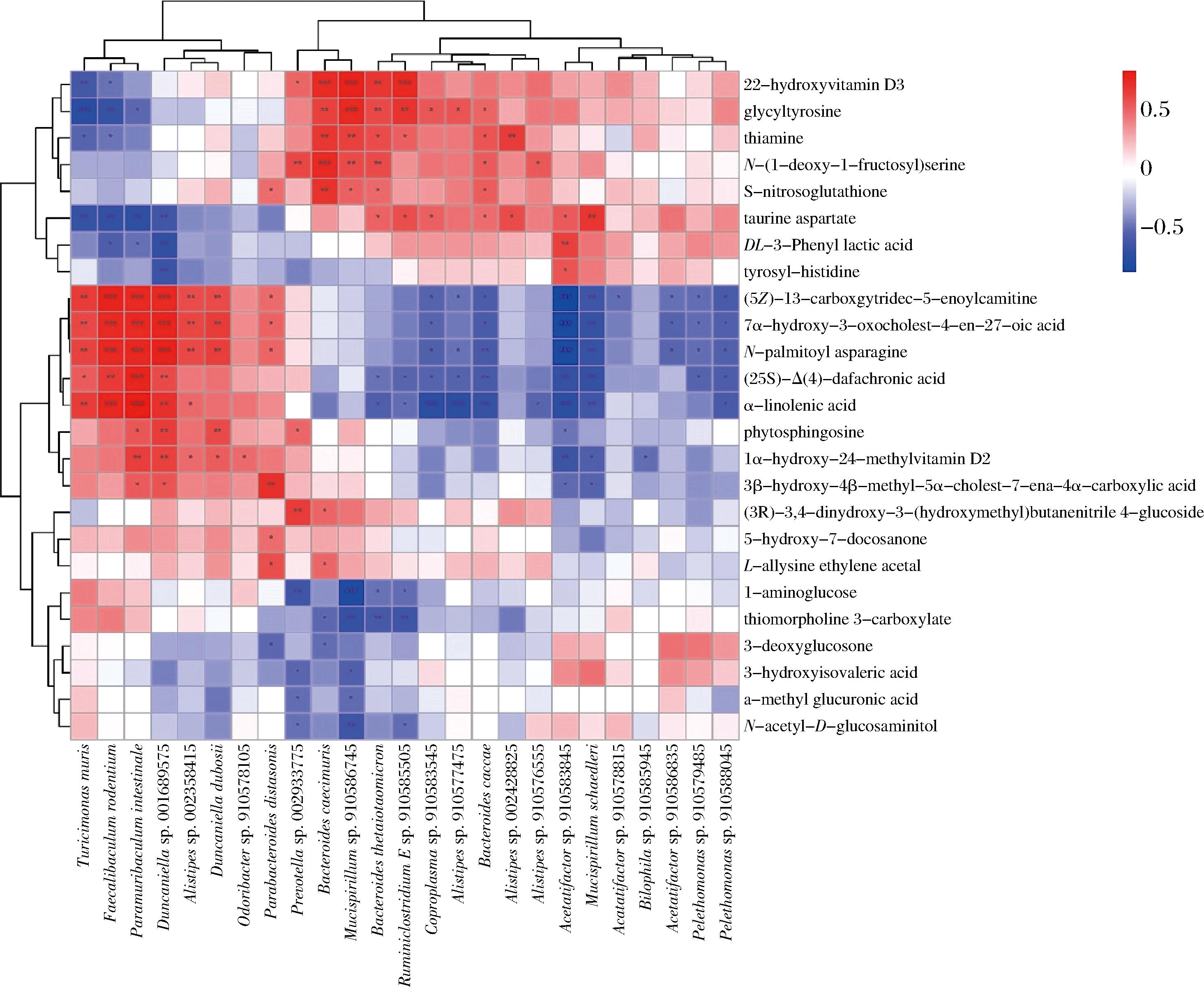
图5 代谢物与菌群的相关性分析
Fig.5 Heat map of the correlation between metabolites and microbiota composition
3 结论与讨论
后生元作为益生菌的替代品或补充剂,同样具有调节肠道菌群、维持肠道健康等功能[13],甚至在抗炎[9]、修复肠道屏障[14]、免疫调节[15]等方面功效活性要优于其活菌。后生元因其稳定性及安全性等优势,在缓解结肠炎方面也受到了广泛关注,ZHANG等[16]研究了不同剂量的鼠李糖乳酪杆菌1.0320后生元对DSS诱导结肠炎的缓解作用,数据表明后生元具有剂量依赖性的缓解结肠炎症状,包括降低DAI、改善结肠组织损伤、下调促炎因子分泌和降低氧化应激水平等。ZHANG等[17]比较了青春双歧杆菌B8589活菌和经热灭活后的后生元对DSS诱导的结肠炎的缓解作用,在2×109 CFU cells/d相当剂量下,后生元表现出更好的效果,包括在DAI评分、结肠长度和结肠组织损伤等方面均要略优于活菌,尤其是在调节肠道菌群方面(β多样性、属水平和种水平的菌群组成等)要显著强于活菌组。对于后生元发挥缓解结肠炎功效的成分方面也有较多研究,主要分为2类,第一类为菌体成分,如益生菌细胞膜的主要成分之一的脂壁酸,其参与细胞免疫等重要的细胞过程, PRADHAN等[18]对植物乳植杆菌MTCC 5690和发酵乳酪杆菌MTCC 5689中提取的脂壁酸,能够显著改善结肠炎小鼠的结肠长度、DAI评分等结肠炎症状,还能修复肠道屏障,改善肠道通透性。另一类是代谢产物,包括短链脂肪酸(乙酸、丁酸等)和有机酸(乳酸、琥珀酸等),丁酸在缓解炎症方面研究较充分, HAMER等[19]研究指出,每天用60 mL含有100 mmol/L丁酸钠灌肠能够改善缓解期UC患者的炎症水平和氧化应激,口服0.5%(质量分数)丁酸钠同样能够改善黏膜病变、调节炎症因子水平等指标来缓解结肠炎[20]。乙酸也具有缓解炎症和修复肠道屏障等功能,LAFFIN等[21]证明口服乙酸能够通过恢复肠道通透性显著改善DSS诱导的结肠炎,DELEU等[22]的研究表明,高浓度乙酸盐能够在UC患者的类器官来源的上皮单层培养物中发挥抗炎作用,并保护肠道屏障。乳酸是后生元中主要的代谢产物之一,其不仅能直接调节肠道的pH值,抑制有害菌的生长及促进益生菌的增殖来维持肠道环境的稳定,大量文献[23-24]证实乳酸还是一个重要的信号分子,在肠组织细胞表面,有特异的乳酸受体 GPR81(或HCA1),其可以通过GPR81 触发炎症、免疫相关等不同的信号通路,来缓解炎症、提高机体免疫力。琥珀酸是三羧酸循环的代谢中间体,也是益生菌代谢产生的主要有机酸成分之一, LIANG等[25]研究证明在饮食中补充琥珀酸可通过IL-4Rα/Hif-1α轴减轻DSS引起的结肠炎,在小鼠饮用水中添加300 mmol/L的琥珀酸,能够促进小鼠外周血、肠系膜淋巴结和结肠固有层中的髓细胞扩张,刺激2型免疫反应,减轻DSS引起的结肠炎。
长双歧杆菌长亚种HSBL001是双歧杆菌三联活菌肠溶胶囊(贝飞达)中的主要功能菌株之一,其在治疗/辅助治疗结肠炎方面已有广泛的研究及临床应用[26-28]。HSBL001后生元由长双歧杆菌长亚种HSBL001在脱脂乳-豆粉基质中发酵制得,除了含有大量的灭活菌体外(285.7×108 cells/g),还含有丰富的有机酸/短链脂肪酸等代谢产物,这种“菌体-代谢产物”复合体系相比于单一的灭活菌体类后生元,其功效及作用机制更广泛、多维度。DSS诱导的急性UC的症状与人类UC相似,是用来评价供试样品缓解结肠炎功效的可靠模型。本研究利用2.5% DSS溶液作为小鼠的唯一饮水,建立了小鼠UC模型,结肠炎小鼠经过HSBL001干预后,能够显著改善DSS诱导的结肠炎症状,DAI评分、结肠长度、脾脏指数等指标与DSS组相比均有显著的改善,HSBL001通过降低血清IL-6和TNF-α水平以及提高IL-10水平来降低机体炎症。其中IL-6和TNF-α代表促炎因子,是参与肠道炎症过程的主要细胞因子,IL-10代表抗炎因子,能抑制巨噬细胞/树突细胞活化,下调TNF-α、IL-6等促炎因子。
本研究结合宏基因组学和代谢组学,对HSBL001缓解结肠炎机制进行探究,对肠道菌群的分析结果显示,DSS造模以及HSBL001干预对小鼠肠道菌群α多样性没有显著改变。但是在β多样性方面有明显差异,HSBL001能够逆转DSS导致的拟杆菌门/厚壁菌门(F/B)比值失衡。拟杆菌门和厚壁菌门是肠道中的主要群落,占肠道微生物群的90%,F/B比值被广泛认为是正常的肠道稳态重要参考[7]。DSS增加了小鼠的F/B比值,而HSBL001降低了结肠炎小鼠的F/B比值,使其基本接近正常组小鼠,这提示HSBL001能够调节DSS诱导的小鼠肠道菌群失调。
通过对肠道菌群属水平和种水平的差异分析,HSBL001干预后能提高杜氏杆菌属(Duncaniella)、Paramuribaculum、Odoribacter、普雷沃氏菌属(Prevotella)等属的丰度,其中Duncaniella属中包括D.dubosii等多个种显著上调。Duncaniella是在正常小鼠肠道中丰度较高的一类菌群[29], CHANG等[30]研究表明Duncaniella属菌种对缓解DSS诱导的结肠炎有重要影响,通过分离培养该菌种,灌胃2×108 CFU的活菌同样能够较好地缓解结肠炎小鼠的症状。D.dubosii能够缓解结肠炎可能与其激活机体免疫力有关, KIM等[31]研究表明,D.dubosii干预提高了体内CD8 T细胞的水平,以及促进了其在体内的循环。本研究经相关性分析表明,D.dubosii与代谢物7α-羟基-3-氧代胆甾-4-烯-27-酸、N-棕榈酰基冬氨酸和植物鞘氨醇等含量呈显著正相关,7α-羟基-3-氧代胆甾-4-烯-27-酸为初级胆汁酸生物合成过程中的代谢物,提示D.dubosii可能对初级胆汁酸生物合成代谢通路有正向调节作用。F.rodentium是一种严格厌氧的革兰氏阳性杆菌,研究认为其是小鼠肠道中的有益菌,灌胃啮齿粪杆菌可以重建小鼠的肠道菌群,其代谢产生的短链脂肪酸能够调控蛋白质乙酰化来抑制肿瘤细胞生长[32],其还能通过“视黄酸-嗜酸性粒细胞-干扰素γ”轴来增加肠上皮细胞的周转率、促进隐窝增殖等发挥维持肠上皮稳态的作用[33]。有研究表明,啮齿粪杆菌生长过程中能积累组氨酸,利用啮齿粪杆菌干预的结肠炎小鼠通过组氨酸途径抑制巨噬细胞产生促炎细胞因子来改善小鼠结肠炎[34]。本研究发现HSBL001干预后啮齿粪杆菌丰度显著增加,且与7α-羟基-3-氧代胆甾-4-烯-27-酸、α-亚麻酸等多种代谢物有显著正相关,提示啮齿粪杆菌可能参与了初级胆汁酸生物合成及α-亚麻酸代谢通路,从而缓解DSS诱导的结肠炎症状。Paramuribaculum intestinale和T.muris是小鼠肠道中优势菌株,但其功能在文献中报道较少,有较多文献报道该菌在结肠炎恢复过程中起到积极作用[35-36],本研究得出类似结论,且菌株丰度与N-棕榈酰基冬氨酸、(5Z)-13-羧基十三碳-5-烯酰基肉碱等多种代谢物具有显著正相关性。
综上,长双歧杆菌长亚种HSBL001在脱脂乳-豆粉基质中发酵制得的包含菌体及代谢物的后生元,对DSS诱导的小鼠结肠炎症状具有较好的缓解作用,结合宏基因组学及代谢组学分析得出长双歧杆菌长亚种HSBL001后生元具有调节肠道菌群与代谢物平衡,增加D.dubosii、F.rodentium、B.caecimuris和B.thetaiotaomicron 等有益菌的丰度,同时提高S-亚硝基谷胱甘肽、α-亚麻酸和7α-羟基-3-氧代胆甾-4-烯-27-酸等化合物含量,调节初级胆汁酸生物合成和α-亚麻酸代谢等通路来缓解结肠炎症状,这为后生元的产业化应用提供了理论支持。
[1] 李娇, 李斌, 陈红贺, 等.流式细胞术定量检测后生元中灭活菌体的方法研究[J/OL].食品与发酵工业, 2025:1-10.(2025-08-19).DOI:10.13995/j.cnki.11-1802/ts.043295.
LI J, LI B, CHEN H H, et al.Study on quantitative detection of inactivated bacteria in Metazoa by flow cytometry[J/OL].Food and Fermentation Industries, 2025:1-10.(2025-08-19).DOI:10.13995/j.cnki.11-1802/ts.043295.
[2] SCOTT E, DE PAEPE K, VAN DE WIELE T.Postbiotics and their health modulatory biomolecules[J].Biomolecules, 2022, 12(11):1640.
[3] HERN NDEZ-GRANADOS M J, FRANCO-ROBLES E.Postbiotics in human health:Possible new functional ingredients?[J].Food Research International, 2020, 137:109660.
NDEZ-GRANADOS M J, FRANCO-ROBLES E.Postbiotics in human health:Possible new functional ingredients?[J].Food Research International, 2020, 137:109660.
[4] DE ALMEIDA C V, ANTIGA E, LULLI M.Oral and topical probiotics and postbiotics in skincare and dermatological therapy:A concise review[J].Microorganisms, 2023, 11(6):1420.
[5] GUO S, MA T, KWOK L Y, et al.Effects of postbiotics on chronic diarrhea in young adults:A randomized, double-blind, placebo-controlled crossover trial assessing clinical symptoms, gut microbiota, and metabolite profiles[J].Gut Microbes, 2024, 16(1):2395092.
[6] QU S W, FAN L N, QI Y D, et al.Akkermansia muciniphila alleviates dextran sulfate sodium (DSS)-induced acute colitis by NLRP3 activation[J].Microbiology Spectrum, 2021, 9(2):e00730-21.
[7] YU Z T, LI D G, SUN H X.Herba Origani alleviated DSS-induced ulcerative colitis in mice through remolding gut microbiota to regulate bile acid and short-chain fatty acid metabolisms[J].Biomedicine &Pharmacotherapy, 2023, 161:114409.
[8] GONG S M, SUN L Q, SUN Y J, et al.Integrated macrogenomics and metabolomics analysis of the effect of sea cucumber ovum hydrolysates on dextran sodium sulfate-induced colitis[J].Marine Drugs, 2025, 23(2):73.
[9] 张蓓.动物双歧杆菌乳亚种BX-186及其后生元对小鼠慢性炎症性肠病的影响[D].呼和浩特:内蒙古农业大学, 2024.
ZHANG B.Effects of Bifidobacterium animalis subsp.lactis BX-186 and its postbiotics on chronic IBD in mice[D].Hohhot:Inner Mongolia Agricultural University, 2024.
[10] YAO S Y, ZHAO Z X, WANG W J, et al.Bifidobacterium longum:Protection against inflammatory bowel disease[J].Journal of Immunology Research, 2021, 2021(1):8030297.
[11] HUANG F C, HUANG S C.The combined beneficial effects of postbiotic butyrate on active vitamin D3-orchestrated innate immunity to Salmonella colitis[J].Biomedicines, 2021, 9(10):1296.
[12] TSILINGIRI K, BARBOSA T, PENNA G, et al.Probiotic and postbiotic activity in health and disease:Comparison on a novel polarised ex-vivo organ culture model[J].Gut, 2012, 61(7):1007-1015.
[13] CHEN J R, ZHANG L F, JIAO Y H, et al.Lacticaseibacillus paracasei L21 and its postbiotics ameliorate ulcerative colitis through gut microbiota modulation, intestinal barrier restoration, and HIF1α/AhR-IL-22 axis activation:Combined in vitro and in vivo evidence[J].Nutrients, 2025, 17(15):2537.
[14] YE H L, LIU X L, GUAN K F, et al.Therapeutic potential of Lacticaseibacillus rhamnosus grx10 and its derived postbiotic through gut microbiota and MAPK/MLCK/MLC pathway-mediated intestinal barrier repairment in ulcerative colitis[J].Journal of Food Science, 2024, 89(12):10035-10052.
[15] 李欣媛. 马乳酒样乳杆菌ZW18鉴定及其后生元对免疫抑制小鼠的调节作用[D].天津:天津科技大学,2024.
LI X Y.Identification of Lactobacillus kefiranofaciens ZW18 and its postbiotic effect on immunosuppressed mice[D].Tianjin:Tianjin University of Science and Technology, 2024.
[16] ZHANG J, DUAN X L, CHEN X H, et al.Lactobacillus rhamnosus 1.0320 postbiotics ameliorate dextran sodium sulfate-induced colonic inflammation and oxidative stress by regulating the intestinal barrier and gut microbiota[J].Journal of Agricultural and Food Chemistry, 2024, 72(45):25078-25093.
[17] ZHANG T, ZHANG W Q, FENG C J, et al.Stronger gut microbiome modulatory effects by postbiotics than probiotics in a mouse colitis model[J].NPJ Science of Food, 2022, 6:53.
[18] PRADHAN D, GULATI G, AVADHANI R, et al.Postbiotic Lipoteichoic acid of probiotic Lactobacillus origin ameliorates inflammation in HT-29 cells and colitis mice[J].International Journal of Biological Macromolecules, 2023, 236:123962.
[19] HAMER H M, JONKERS D M A E, VANHOUTVIN S A L W, et al.Effect of butyrate enemas on inflammation and antioxidant status in the colonic mucosa of patients with ulcerative colitis in remission[J].Clinical Nutrition, 2010, 29(6):738-744.
[20] VIEIRA E L M, LEONEL A J, SAD A P, et al.Oral administration of sodium butyrate attenuates inflammation and mucosal lesion in experimental acute ulcerative colitis[J].The Journal of Nutritional Biochemistry, 2012, 23(5):430-436.
[21] LAFFIN M, FEDORAK R, ZALASKY A, et al.A high-sugar diet rapidly enhances susceptibility to colitis via depletion of luminal short-chain fatty acids in mice[J].Scientific Reports, 2019, 9:12294.
[22] DELEU S, ARNAUTS K, DEPREZ L, et al.High acetate concentration protects intestinal barrier and exerts anti-inflammatory effects in organoid-derived epithelial monolayer cultures from patients with ulcerative colitis[J].International Journal of Molecular Sciences, 2023, 24(1):768.
[23] WATANABE T, NISHIO H, TANIGAWA T, et al.Probiotic Lactobacillus casei strain Shirota prevents indomethacin-induced small intestinal injury:Involvement of lactic acid[J].American Journal of Physiology.Gastrointestinal and Liver Physiology, 2009, 297(3):G506-G513.
[24] HUANG Y P, ZHANG J L, DONG R J, et al.Lactate as a metabolite from probiotic Lactobacilli mitigates ethanol-induced gastric mucosal injury:An in vivo study[J].BMC Complementary Medicine and Therapies, 2021, 21(1):26.
[25] LIANG L Y, DANG B Y, OUYANG X M, et al.Dietary succinate supplementation alleviates DSS-induced colitis via the IL-4Rα/Hif-1α Axis[J].International Immunopharmacology, 2025, 152:114408.
[26] 李海霞.双歧杆菌三联活菌对溃疡性结肠炎患者的疗效[J].河南医学研究, 2020, 29(21):3944-3946.
LI H X.Efficacy of triple viable capsules dissolving at intestines in patients with ulcerative colitis[J].Henan Medical Research, 2020, 29(21):3944-3946.
[27] 吴克江. 美沙拉嗪肠溶片联合双歧杆菌三联活菌胶囊对溃疡性结肠炎患者的影响[J].中外医学研究, 2022, 20(35):18-21.
WU K J.Effect of mesalazine enteric coated tables combined with Lactobacillus and Enterococcus capsules on patients with ulcerative colitis[J].Chinese and Foreign Medical Research, 2022, 20(35):18-21.
[28] 孙成龙. 双歧杆菌三联活菌肠溶胶囊联合美沙拉嗪肠溶片治疗溃疡性结肠炎患者的效果分析[J].大医生, 2025, 10(12):40-42.
SUN C L.Effect analysis of Bifidobacterium triple live bacteria enteric-coated capsules combined with mesalazine enteric-coated tablets in the treatment of patients with ulcerative colitis[J].Doctor, 2025, 10(12):40-42.
[29] MIYAKE S, DING Y C, SOH M, et al.Cultivation and description of Duncaniella dubosii sp.nov., Duncaniella freteri sp.nov.and emended description of the species Duncaniella muris[J].International Journal of Systematic and Evolutionary Microbiology, 2020, 70(5):3105-3110.
[30] CHANG C S, LIAO Y C, HUANG C T, et al.Identification of a gut microbiota member that ameliorates DSS-induced colitis in intestinal barrier enhanced Dusp6-deficient mice[J].Cell Reports, 2021, 37(8):110016.
[31] KIM H C, KIM H J, LA J, et al.Gut microbiota dysbiosis induced by brain tumors modulates the efficacy of immunotherapy[J].Cell Reports, 2025, 44(7):115825.
[32] ZAGATO E, POZZI C, BERTOCCHI A, et al.Endogenous murine microbiota member Faecalibaculum rodentium and its human homologue protect from intestinal tumour growth[J].Nature Microbiology, 2020, 5(3):511-524.
[33] CAO Y G, BAE S, VILLARREAL J, et al.Faecalibaculum rodentium remodels retinoic acid signaling to govern eosinophil-dependent intestinal epithelial homeostasis[J].Cell Host &Microbe, 2022, 30(9):1295-1310.e8.
[34] ZENG W Y, WU J J, XIE H Y, et al.Enteral nutrition promotes the remission of colitis by gut bacteria-mediated histidine biosynthesis[J].eBioMedicine, 2024, 100:104959.
[35] 张颖.抗氧化乳酸菌对小鼠急性溃疡性结肠炎的预防作用及组学机制研究[D].兰州:兰州大学,2023
ZHANG Y.Preventive and alleviation of antioxidant lactic acid bacteria on acute ulcerative colitis in mice and its omics mechanism[D].Lanzhou:Lanzhou University, 2023.
[36] LI X F, HE N N, WANG H Y, et al.Therapeutic effect of Faecalibacterium longum CM04-06 on DSS-induced ulcerative colitis in mice[J].Journal of Applied Microbiology, 2025, 136(5):lxaf119.