植物乳植杆菌(Lactiplantibacillus plantarum)作为乳酸菌的重要成员,广泛存在于乳制品、蔬菜、肉制品等发酵食品中,能够在多种糖源上生长,以其环境适应性和碳源代谢多样性等特点而闻名[1]。碳水化合物是微生物生长和能量代谢的重要底物[2]。L.plantarum与大多数乳酸菌相比,具有更强的碳水化合物利用能力,对不同碳水化合物的各种环境具有广泛的适应性[3-5]。已有研究表明,L.plantarum的核心功能集中在碳水化合物代谢上,为菌株代谢多种糖类提供分子支持,并发现L.plantarum菌株使用碳水化合物的能力与碳水化合物代谢相关基因相关,包括编码糖苷酶和转运蛋白的基因[6]。L.plantarum生物体拥有一个由大量糖摄取和代谢相关基因组成的综合碳水化合物利用系统,这赋予了其强大的碳水化合物利用能力,其糖代谢相关基因的数量远远超过其他乳酸菌相关基因的数量[2-3]。
近年来的遗传学分析揭示了L.plantarum碳水化合物代谢基因的菌株特异性分布特征,反映了该物种在碳源利用方面的多样性[7]。碳水化合物活性酶数据库(carbohydrate-active enzymes database,CAZy)[8]能够注释一系列与碳水化合物代谢密切相关的酶类家族,主要分为6类:多糖裂合酶(polysaccharide lyase,PL)家族、糖基转移酶(glycosyl transferase,GT)家族、糖苷水解酶(glucoside hydrolase,GH)家族、碳水化合物酯酶(carbohydrate esterase,CE)家族、碳水化合物结合模块(carbohydrate binding module,CBM)家族以及辅助氧化还原酶(auxiliary activities,AA)家族[9]。在这个数据库中,酶家族,包括GH和GT,对于将复杂碳水化合物分解为微生物可利用的简单糖类至关重要[10]。GH家族负责聚糖的降解(水解糖苷键)[11],而GT家族催化糖基转移反应,参与聚糖的合成与修饰,糖基转移酶2(glycosyltransferase 2,GT2)主要转移β-糖苷键(如葡萄糖、甘露糖),糖基转移酶4(glycosyltransferase 4,GT4)主要转移α-糖苷键(如鼠李糖、水苏糖)[9]。
热带地区独特的气候环境,塑造了该地区特有菌群基因组特征[12]。LI等[13]分析445株不同地区的L.plantarum基因差异,发现相比于温带(荷兰)来源菌株,分离自热带地区(巴西)发酵木薯中菌株的基因组具有更高的单核苷酸多态性。SMITS等[14]的研究表明生活在坦桑尼亚热带部落的哈扎人肠道菌群基因组中聚糖代谢、支链氨基酸代谢等功能基因拷贝数显著高于美国人群。说明了热带与非热带地区来源菌株的功能和核心基因存在一定分化。
综上所述,L.plantarum展现出显著的碳水化合物利用能力,然而,相关酶与其在碳水化合物代谢中的作用以及发酵特性之间的关系尚未明确,本研究旨在探索其相关性。
1 材料与方法
1.1 实验试剂
实验所需的胰蛋白胨、酵母提取物、牛肉膏、L(+)鼠李糖、蔗糖,北京索莱宝科技公司;CaCl2、MgSO4·7H2O、NaCl、NaHCO3、FeSO4、KH2PO4,上海阿拉丁生化科技公司;果糖、木糖、麦芽糖、水苏糖、甘油,国药集团化学试剂公司。
1.2 实验菌株
实验所用的L.plantarum和干酪乳酪杆菌(Lactobacillus casei)均来自热带和非热带传统发酵食品中所分离筛选的菌株,鼠李糖乳酪杆菌(Lacticaseibacillus rhamnosus GG,LGG)为商业菌株。具体信息如表1所示。
表1 菌株信息表
Table 1 Strain information table

1.3 仪器设备
ZHJH-C1115B豪华型垂直流超净工作台,上海智城分析仪器制造有限公司;GRP-9160隔热式恒温培养箱,上海森信实验仪器有限公司;Micro21R高速冷冻离心机,赛默飞科技(中国)有限公司;TOMY SX-500高压蒸汽灭菌锅,日本Sanyo公司;磁力搅拌器,德国IKA公司;Bio-Rad S1000 PCR仪,美国Bio-Rad公司;FE28酸度计、AB104-N分析电子天平、ME3002E电子天平,梅特勒-托利多公司;CLARIOstar Plus微生物生长曲线检测系统,英国BMG LABTECH公司;T1-SAM倒置显微镜,尼康(日本)公司。
1.4 培养基及试剂配制
乳酸菌培养基(De man-rogosa-sharpe,MRS)(g/L):酵母粉5,胰蛋白胨10,无水葡萄糖20,无水乙酸钠2,七水合硫酸镁0.5,三水合磷酸氢二钾2.6,一水合硫酸锰0.25,柠檬酸氢二铵2,牛肉膏10,1 mL吐温-80,1 L去离子水;在上述液体培养基中加入琼脂粉至终浓度2 g/100 mL,混合制备得到MRS固体琼脂培养基,在115 ℃、20 min条件下高温灭菌。
1.5 CAZy基因注释
按照2%(体积分数)接种L.plantarum至MARS液体培养基培养12~18 h,6 000 r/min离心5 min,收集菌泥,利用Illumina HiSeq 4000平台测序,测序深度为1 G,测定菌株的全基因组草图。
使用Prokka软件对基因组序列进行基因注释,获得各菌株的注释文件,采用Roary软件结合MAFFT算法进行多序列比对分析[15]。
CAZy注释采用基于HMM(Hidden Markov Model)的HMMER 3.1软件包,结合dbCAN数据库中预先构建的特异性HMM[16],对热带和非热带来源的乳杆菌基因组中的功能酶系进行系统鉴定与分类注释。
1.6 不同糖源的利用
将经过分离筛选并已完成二次活化的L.plantarum菌株按2%(体积分数)比例,液接于MRS液体培养基中,置于37 ℃恒温培养,每隔1 h测定菌液在600 nm下的吸光度值,最终取样点为接种后24~48 h。
测定乳杆菌菌株对不同碳源的利用情况[17],分别以蔗糖、果糖、鼠李糖、木糖、麦芽糖、水苏糖作为MRS液体培养基(不含葡萄糖)的唯一碳源,将不含碳源的MRS液体培养基设置为对照组,加入溴甲酚紫指示剂,置于37 ℃恒温培养,每隔1 h测定菌液在600 nm下的吸光度值,最终取样点为接种后24 h,观察培养基变色情况,计算乳杆菌菌株在特定碳源培养基下生长的代时。
1.7 发酵皱皮小青椒及游离氨基酸测定
L.plantarum、L.rhamnosus在MRS固体培养基中进行2次划线分离,挑选代表性的单菌落转接至MRS液体培养基中培养至指数期。将新鲜的皱皮小青椒经过前处理后装入已灭菌的1 L烧杯中,用保鲜膜密封,进行超低温巴氏杀菌(60~65 ℃,30 min),杀菌结束后放入4 ℃冰箱降温;将活化的乳酸菌离心(6 000 r/min、3 min),洗涤3次后重悬于0.9%无菌生理盐水中,使其活菌数达到109 CFU/mL,随后,将激活菌株(2%,体积分数)分别接种在经过巴氏杀菌的皱皮小青椒,在30 ℃培养箱中进行好氧培养24 h,得到目标发酵皱皮小青椒。将发酵皱皮小青椒的发酵终点样品和起点样品,分别用于17种常见游离氨基酸含量的测定。测定方法参考SUN等[18]并稍作修改。
1.8 数据统计与分析
数据处理借助Origin 2024软件进行。进行数据的正态性分布检验、非参数统计分析。实验至少重复3次进行,结果以“平均数±标准差”表示,*P<0.05,**P<0.01,***P<0.001表示差异具有统计学意义,n.s.表示无统计学差异。
2 结果与分析
2.1 热带与非热带L.plantarum CAZy基因家族的鉴定与分类
通过比较6株热带与5株非热带来源的L.plantarum编码CAZy家族酶的基因,探讨地域因素对L.plantarum基因组功能进化的潜在影响。L.plantarumCAZy家族中各类别的基因家族分布如图1-a,GH和GT家族显著富集。值得注意的是,热带L.plantarum的GT家族基因平均含量(310±13)显著高于非热带菌株(296±5,P≤0.05,如图1-b)。上述研究表明地域因素可能通过驱动GT家族基因[19]扩张影响L.plantarum的碳水化合物代谢[20]功能进化。
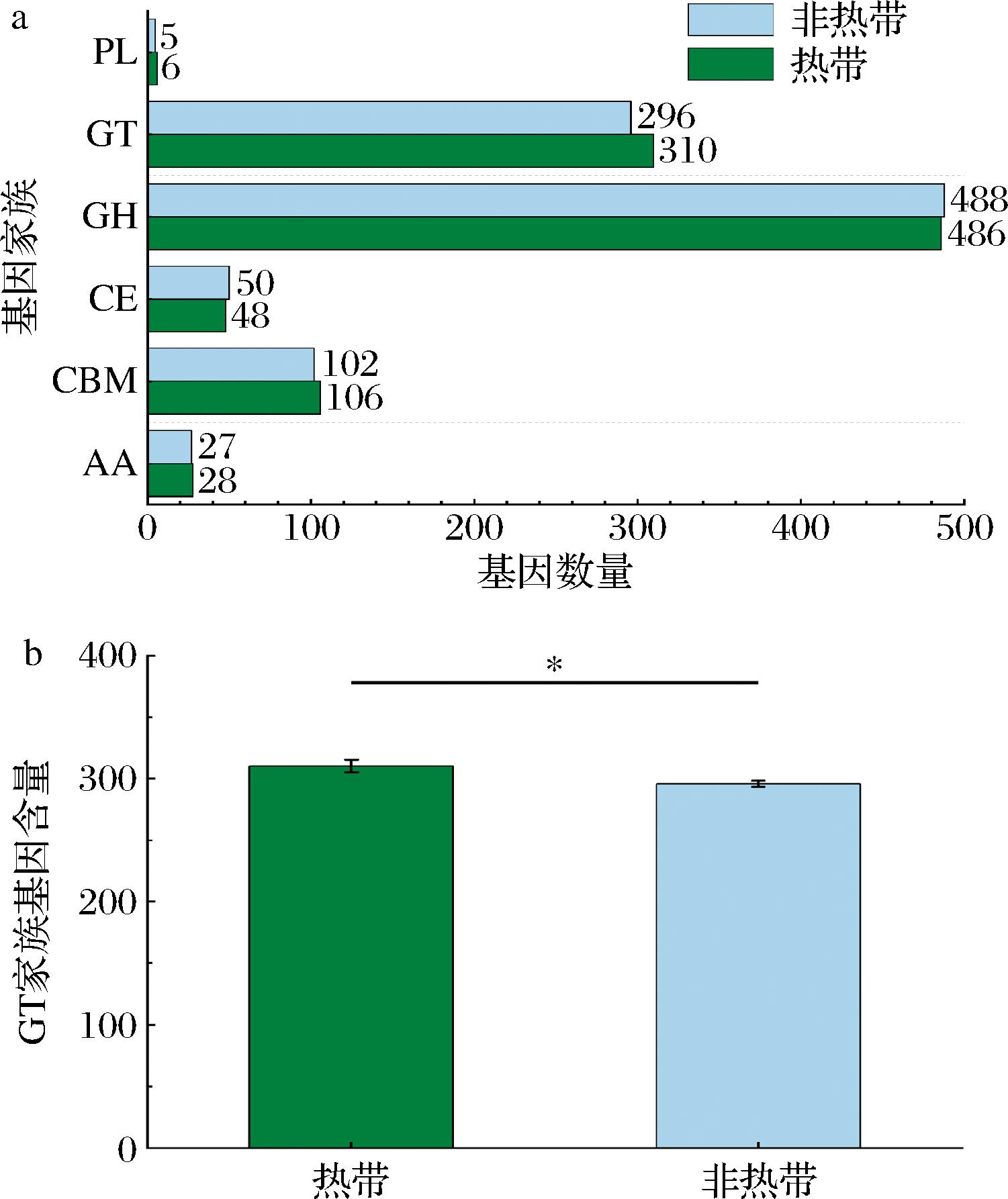
a-CAZy家族基因注释各类别直方图;b-GT家族基因平均含量
图1 热带与非热带地区L.plantarum菌株的CAZy注释结果
Fig.1 CAZy results of L.plantarum in tropical and nontropical regions
注:*表示P<0.05。
2.2 GT基因表达模式分析
比较8株热带与9株非热带来源的乳杆菌菌株的GT家族基因注释结果,如图2-a所示,热带和非热带来源的17株乳杆菌菌株基因组中共预测出58种编码的GT家族,GT家族中的GT2(糖基转移酶家族2)和GT4家族(糖基转移酶家族4)呈现显著富集。热带与非热带来源的L.plantarum均以GT2(平均101 vs.90,P≤0.01)和GT4(平均85 vs.79,P≤0.05)家族为核心CAZy组分,但热带菌株在两类家族中均表现出显著更高的基因丰度,如图2-b所示。结果表明热带与非热带来源的L.plantarum菌株间GT分布存在一定差异,揭示热带来源的L.plantarum可能进化出更复杂的碳水化合物代谢策略,以适应其生态环境中的特定碳源需求[21]。
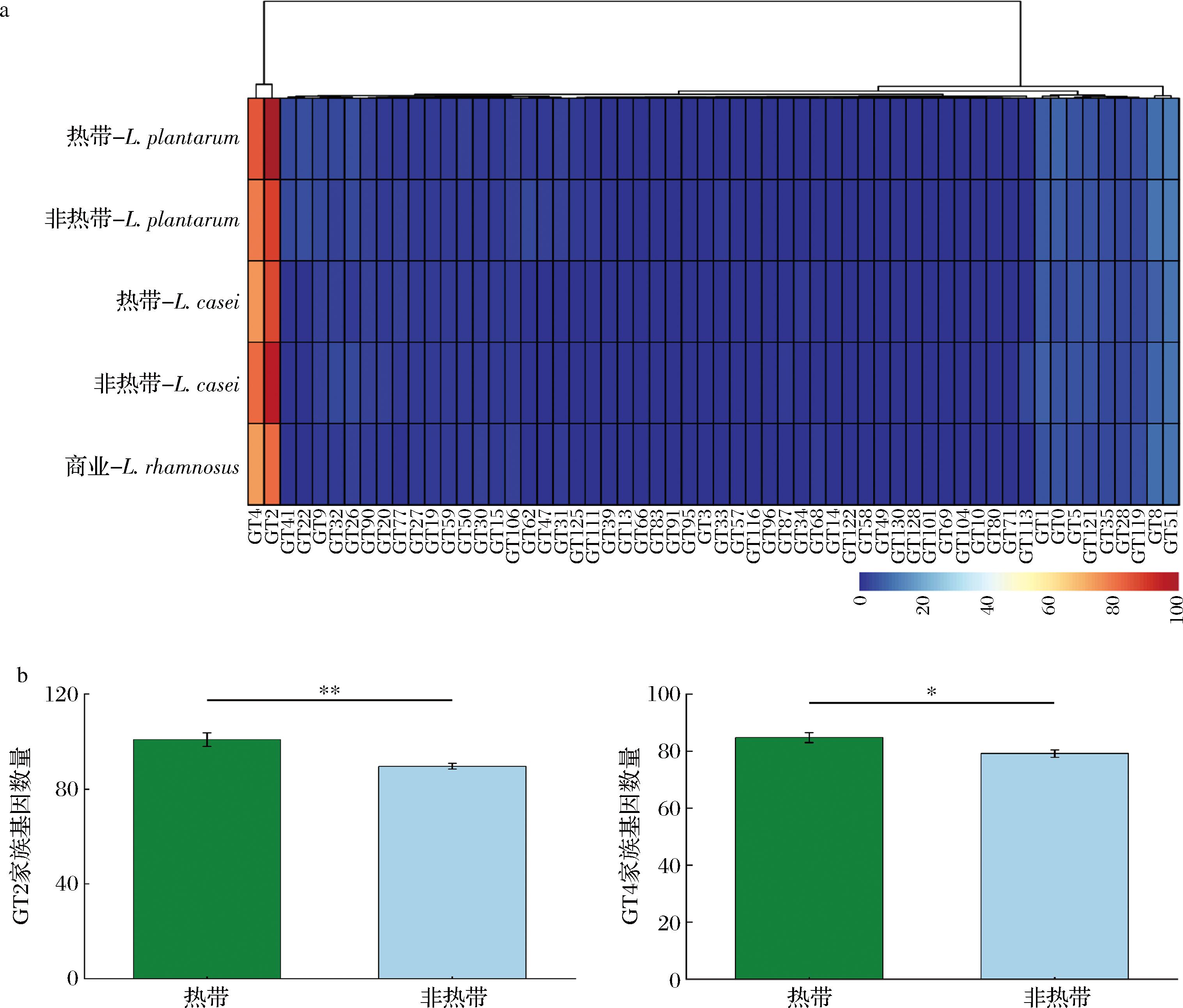
a-GT家族注释相关基因热图;b-植物乳植杆菌中GT2和GT4家族基因的平均含量
图2 热带与非热带地区乳杆菌菌株的GT家族注释结果
Fig.2 Results of GT families in Lactobacillus from tropical and nontropical regions
注:*表示P<0.05;**表示P<0.01。
2.3 热带与非热带来源的L.plantarum糖源利用差异
2.3.1 不同糖类条件下L.plantarum的生长特性
L.plantarum对蔗糖、果糖、鼠李糖、木糖、麦芽糖、水苏糖和葡萄糖等不同糖源的利用情况,能够反映其代谢多样性和底物特异性[22]。研究L.plantarum菌株在不同糖源环境中的生长特性,评估其环境适应性。通过分析其对不同糖源的利用效率,可以推断其糖代谢途径的完整性、关键酶的活性以及基因调控机制的差异[23-25]。
实验测定了4株热带与4株非热带来源的植物乳植杆菌在不同糖源的生长情况,基于在不同糖源中的代时评估其对不同糖源的利用情况。结果显示热
带来源的L.plantarum在以鼠李糖为唯一碳源时,代时(0.62±0.11) h显著低于非热带菌株[(1.35±0.27) h,P<0.05,图3-a];然而,在果糖[(1.42±0.09) vs (1.03±0.09) h,P<0.01,图3-b]和蔗糖[(1.43±0.06) vs (1.09±0.06) h,P<0.01,图3-c]作为唯一碳源时,其代时均显著高于非热带菌株。这表明热带菌株在稀有糖(如鼠李糖)的高效代谢中存在进化优势,而对常见糖类(蔗糖、果糖)的利用能力则弱于非热带菌株,提示菌株碳源代谢策略与其地理生态适应性存在显著关联。此外,热带与非热带来源的L.plantarum在木糖、麦芽糖、水苏糖和葡萄糖作为唯一碳源时,代时差异无统计学意义(P>0.05)。
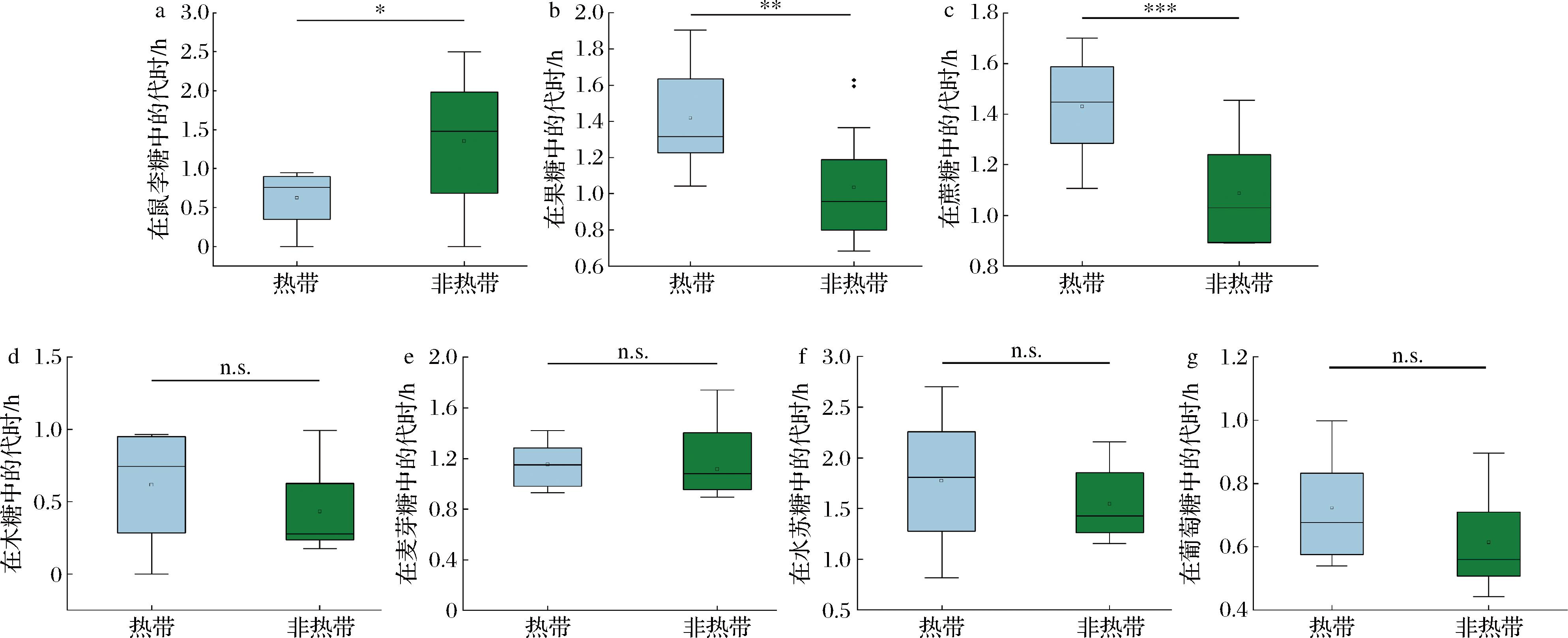
a-鼠李糖;b-果糖;c-蔗糖;d-木糖;e-麦芽糖;f-水苏糖;g-葡萄糖
图3 热带与非热带来源的L.plantarum对不同糖源的利用情况分析
Fig.3 Utilization of different glycogens by L.plantarum
注:*表示P<0.05;**表示P<0.01;***表示P<0.001,n.s.表示不显著(下同)。
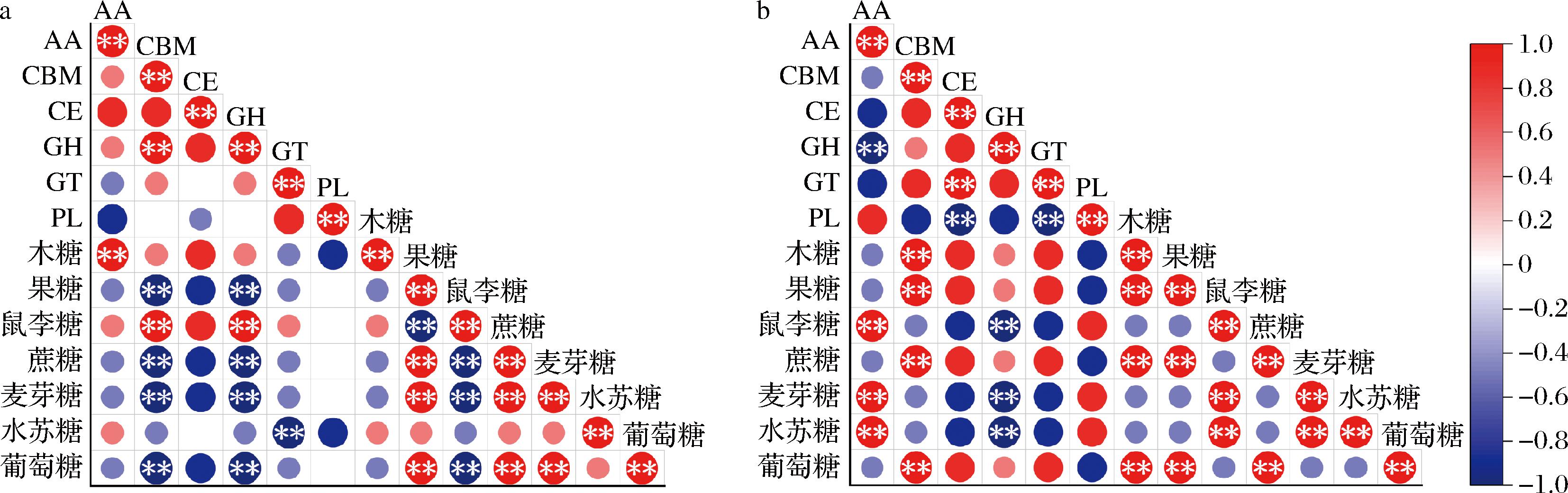
a-热带来源;b-非热带来源
图4 热带与非热带来源的L.plantarum对不同糖的代时与不同CAZy基因家族的相关性图
Fig.4 Correlation diagram of generation times of L.plantarum from tropical and nontropical regions with different sugars and different CAZy gene families
2.3.2 热带与非热带来源的L.plantarum的相关性分析
如图4-a显示3株热带来源的L.plantarum的辅助氧化还原酶(auxiliary activities,AA)家族与其在木糖中的代时显著正相关(P≤0.01),表明随着AA家族相关基因的数量增加,菌株在木糖中的代时会增加。碳水化合物结合模块(carbohydrate-binding module,CBM)家族和GH家族与其在葡萄糖、麦芽糖、蔗糖、果糖中的代时显著负相关(P≤0.01),与其在鼠李糖中的代时显著正相关(P≤0.01),表明随着热带来源菌株中的CBM家族和GH家族相关基因的数量增加,其在葡萄糖、麦芽糖、蔗糖、果糖中的代时会更短,但在鼠李糖中的代时会增加。GT家族与其在水苏糖中的代时显著负相关(P≤0.01),表明随着热带来源菌株中GT家族相关基因的数量增加,其在水苏糖中的代时会更短,菌株生长活性更强。
图4-b显示3株非热带来源的L.plantarum中的AA家族与其在水苏糖、麦芽糖、鼠李糖中的代时显著正相关(P≤0.01)。CBM家族与其在葡萄糖、蔗糖、果糖和木糖中的代时显著正相关(P≤0.01)。GH家族与其在水苏糖、麦芽糖、鼠李糖中的代时显著负相关(P≤0.01),表明随着非热带来源菌株中的GH家族相关基因的数量增加,其在水苏糖、麦芽糖、鼠李糖中的代时会更短,菌株的生长活性更强。
2.4 热带与非热带来源的L.plantarum所发酵青椒中的游离氨基酸含量差异
采用热带来源L.plantarumVHaN67M6、非热带来源L.plantarumVSCPC15M5及商业菌株LGG对青椒进行发酵,测定发酵终点17种常见游离氨基酸含量。结果表明,不同菌株发酵青椒的精氨酸(arginine,Arg)和丝氨酸(serine,Ser)含量存在显著差异。
精氨酸含量如图5-a所示,热带来源菌株发酵组的精氨酸含量最高[(5.15±0.11) mg/100 g],显著高于非热带来源菌株[(2.69±0.75 mg/100 g),P≤0.01]和LGG组[(2.10±0.36) mg/100 g,P≤0.001],而非热带来源菌株与LGG组间无显著差异(P>0.05)。
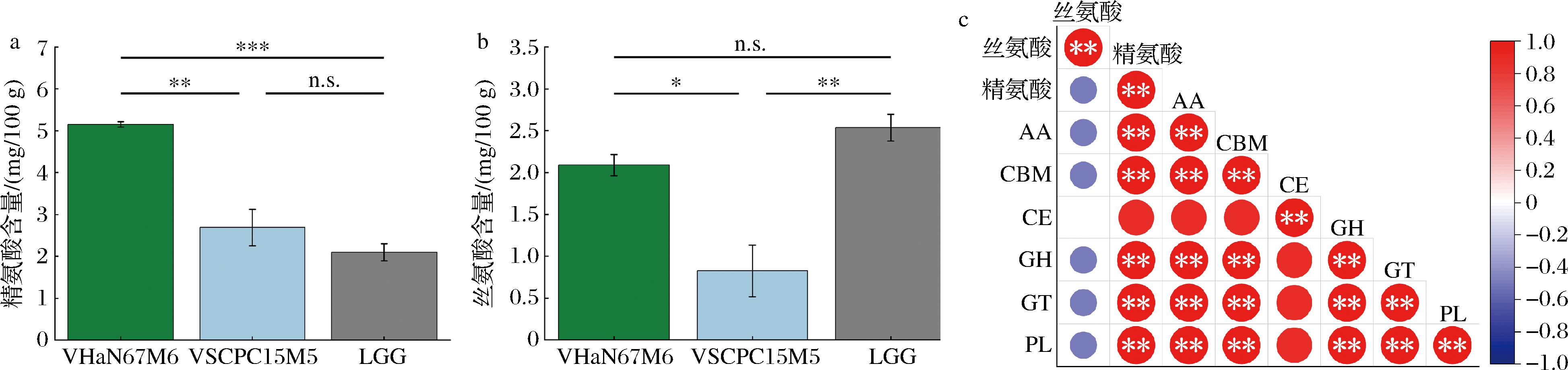
a-精氨酸含量;b-丝氨酸含量;c-氨基酸含量与CAZy基因各家族的相关性图
图5 热带与非热带来源的乳杆菌发酵青椒中的游离氨基酸分析
Fig.5 Analysis of free amino acids in green pepper fermented by Lactobacillus from tropical and nontropical regions
丝氨酸含量如图5-b所示,热带来源菌株发酵组的丝氨酸含量[(2.09±0.22) mg/100 g]显著高于非热带来源菌株[(0.83±0.53) mg/100 g,P≤0.05],而LGG组的丝氨酸含量[(2.54±0.28) mg/100 g]亦显著高于非热带来源菌株(P≤0.01)。热带来源菌株与LGG组间无显著差异(P>0.05)。
相关性分析结果表明,热带来源的菌株所发酵青椒中精氨酸含量与GH、GT、PL、CBM、AA基因显著正相关(P≤0.01),丝氨酸含量与CAZy各家族基因不具有统计学差异(P>0.05)。
上述结果表明,菌株的地理来源可能影响发酵过程中特定氨基酸的积累模式。值得注意的是,热带来源的L.plantarum在精氨酸和丝氨酸的积累方面表现出显著优势,暗示其代谢特征可能受地域适应性影响。
3 结论与讨论
本研究揭示了热带与非热带来源L.plantarum在碳水化合物代谢能力上的显著差异。热带菌株表现出更丰富的CAZy基因家族分布,主要体现在GT家族中GT2和GT4家族的基因丰度上。在糖源利用方面,热带菌株对鼠李糖的代谢效率显著优于非热带菌株,但对蔗糖和果糖的利用能力较弱;2组菌株对木糖、麦芽糖等常见糖源的利用能力无显著差异。相关性分析显示,热带菌株中GT家族基因与其在水苏糖中的代时呈显著负相关,说明GT基因的扩增可能直接增强了其对水苏糖的代谢能力。氨基酸测定结果显示菌株的地理来源可能影响发酵过程中特定氨基酸的积累,其中热带来源L.plantarum在精氨酸和丝氨酸的富集方面表现出显著优势,可能与其抗逆策略相关。揭示出高温高湿等热带气候条件可能筛选出依赖精氨酸(通过精氨酸脱亚胺酶途径产ATP/NO抗应激)和丝氨酸(维持膜流动性及热休克蛋白合成)的菌株。
综上,地域因素显著驱动了乳杆菌CAZy基因组的进化分化,为开发具有特定糖代谢能力的热带益生菌菌株提供了理论依据。未来研究可通过多组学联用(如转录组-代谢组)揭示GT基因调控网络及其与环境互作的分子机制。
[1] 王佳, 郑诗琪, 冯鑫, 等.植物乳植杆菌AR113利用碳源情况研究[J].食品与发酵工业, 2023, 49(11):1-6.
WANG J, ZHENG S Q, FENG X, et al.Research of carbon source utilization by Lactiplantibacillus plantarum AR113[J].Food and Fermentation Industries, 2023, 49(11):1-6.
[2] KLEEREBEZEM M, BOEKHORST J, VAN KRANENBURG R, et al.Complete genome sequence of Lactobacillus plantarum WCFS1[J].Proceedings of the National Academy of Sciences of the United States of America, 2003, 100(4):1990-1995.
[3] BUNTIN N, HONGPATTARAKERE T, RITARI J, et al.An inducible operon is involved in inulin utilization in Lactobacillus plantarum strains, as revealed by comparative proteogenomics and metabolic profiling[J].Applied and Environmental Microbiology, 2016, 83(2):e02402-16.
[4] FUHREN J, RÖSCH C, TEN NAPEL M, et al.Synbiotic matchmaking in Lactobacillus plantarum:Substrate screening and gene-trait matching to characterize strain-specific carbohydrate utilization[J].Applied and Environmental Microbiology, 2020, 86(18):e01081-20.
[5] SIEZEN R J, TZENEVA V A, CASTIONI A, et al.Phenotypic and genomic diversity of Lactobacillus plantarum strains isolated from various environmental niches[J].Environmental Microbiology, 2010, 12(3):758-773.
[6] MAO B Y, YIN R M, LI X S, et al.Comparative genomic analysis of Lactiplantibacillus plantarum isolated from different niches[J].Genes, 2021, 12(2):241.
[7] CUI Y H, WANG M H, ZHENG Y K, et al.The carbohydrate metabolism of Lactiplantibacillus plantarum[J].International Journal of Molecular Sciences, 2021, 22(24):13452.
[8] LOMBARD V, GOLACONDA RAMULU H, DRULA E, et al.The carbohydrate-active enzymes database (CAZy) in 2013[J].Nucleic Acids Research, 2014, 42(Database issue):D490-D495.
[9] WARDMAN J F, BAINS R K, RAHFELD P, et al.Carbohydrate-active enzymes (CAZymes) in the gut microbiome[J].Nature Reviews Microbiology, 2022, 20(9):542-556.
[10] ABOT A, ARNAL G, AUER L, et al.CAZyChip:Dynamic assessment of exploration of glycoside hydrolases in microbial ecosystems[J].BMC Genomics, 2016, 17(1):671.
[11] PENGTHAISONG S, PINIELLO B, DAVIES G J, et al.Reaction mechanism of glycoside hydrolase family 116 utilizes perpendicular protonation[J].ACS Catalysis, 2023, 13(9):5850-5863.
[12] HUANG L, WANG Y, ZHONG K Y, et al.In vitro characterization and identification of potential probiotic yeasts isolated from zaopocu, a traditional fermented dregs vinegar from Hainan Island[J].Probiotics and Antimicrobial Proteins, 2024.DOI:10.1007/s12602-024-10347-8.
[13] LI K N, WANG S J, LIU W J, et al.Comparative genomic analysis of 455 Lactiplantibacillus plantarum isolates:Habitat-specific genomes shaped by frequent recombination[J].Food Microbiology, 2022, 104:103989.
[14] SMITS S A, LEACH J, SONNENBURG E D, et al.Seasonal cycling in the gut microbiome of the Hadza hunter-gatherers of Tanzania[J].Science, 2017, 357(6353):802-806.
[15] RAPOPORT A E, TRIFONOV E N.“Anticipated” nucleosome positioning pattern in prokaryotes[J].Gene, 2011, 488(1-2):41-45.
[16] NGUYEN S T C, FREUND H L, KASANJIAN J, et al.Function, distribution, and annotation of characterized cellulases, xylanases, and chitinases from CAZy[J].Applied Microbiology and Biotechnology, 2018, 102(4):1629-1637.
[17] 李刘若兰. 人体肠道中长双歧杆菌占据属内丰度优势的机制解析及筛选方法开发[D].无锡:江南大学, 2023.
LI-LIU R L.Mechanism analysis and screening methoddevelopment of Bifidobacterium longum occupying of the abundance dominance within thegenus in the human gut[D].Wuxi:Jiangnan University, 2023.
[18] SUN X X, YU L L, XIAO M F, et al.Exploring core fermentation microorganisms, flavor compounds, and metabolic pathways in fermented rice and wheat foods[J].Food Chemistry, 2025, 463:141019.
[19] ADE C P, BEMM F, DICKSON J M J, et al.Family 34 glycosyltransferase (GT34) genes and proteins in Pinus radiata (Radiata pine) and Pinus taeda (loblolly pine)[J].The Plant Journal, 2014, 78(2):305-318.
[20] HICKS K G, CLUNTUN A A, SCHUBERT H L, et al.Protein-metabolite interactomics of carbohydrate metabolism reveal regulation of lactate dehydrogenase[J].Science, 2023, 379(6636):996-1003.
[21] NGOUÉNAM J R, MOMO KENFACK C H, FOKO KOUAM E M, et al.Lactic acid production ability of Lactobacillus sp.from four tropical fruits using their by-products as carbon source[J].Heliyon, 2021, 7(5):e07079.
[22] WU M M, ZHAO X, SHEN Y Q, et al.Efficient simultaneous utilization of glucose and xylose from corn straw by Sphingomonas sanxanigenens NX02 to produce microbial exopolysaccharide[J].Bioresource Technology, 2021, 319:124126.
[23] LUIS A S, JIN C S, PEREIRA G V, et al.A single sulfatase is required to access colonic mucin by a gut bacterium[J].Nature, 2021, 598(7880):332-337.
[24] XU B, LIU L H, LAI S J, et al.Directed evolution of Escherichia coli nissle 1917 to utilize allulose as sole carbon source[J].Small Methods, 2024, 8(8):2301385.
[25] ZHANG W Z, ZHANG J L, ZHAO X M, et al.Efficient production of ginsenoside Rh2 from xylose by remodeling metabolism in Saccharomyces cerevisiae[J].Chemical Engineering Journal, 2024, 494:153120.