黄芪味甘、性微温,是我国传统中药材[1],于2023年正式被国家卫健委列入药食同源物质目录。黄芪多糖(astragalus polysaccharides, APS)是黄芪的主要活性成分之一,较黄芪中其他物质含量占比也更高,具有调节免疫功能、降低血脂、抗炎、抗病毒和抗菌等多种益生作用[2]。许多研究证实了一些药食同源物质的主要活性成分——多糖类物质对益生菌的益生作用。如薛晨曦[3]优化并制备了APS合生元冻干粉剂,该粉剂能够改善犊牛的肠道健康并促进犊牛的生长。JING等[4]的研究表明,党参多糖可通过上调双歧杆菌和乳杆菌等与免疫呈正相关的菌群的生长,抑制脱硫弧菌和幽门螺杆菌等致病菌的生长,恢复结肠炎小鼠的肠道微生态平衡。WANG等[5]使用含有大豆多糖和海藻糖的复合冷冻保护剂可以使乳酸菌的存活率达到90.52%,与仅加入海藻糖或大豆多糖相比,增加了31.48%和36.47%。
益生菌通过提供额外的生物活性(抗癌、抗炎、抗氧化特性、植物化学物质等)并降低许多危及生命的疾病风险来保护宿主生理健康[6]。嗜酸乳杆菌被广泛认为具有益生作用,是最常推荐用于饮食用途的微生物之一,广泛应用于商业益生菌产品,包括奶酪、嗜酸性牛奶、酸奶和膳食补充剂等[7]。与其他益生菌相比,嗜酸乳杆菌对酸和胆盐的耐受性较好,这些特性有利于嗜酸乳杆菌在胃肠道的恶劣环境中存活[8]。益生菌对宿主的健康益处取决于它们的浓度,其数量达到一定的阈值,才能起到益生作用,益生菌产品的质量主要通过活菌的数量来评估[9]。因此,必须确保产品中嗜酸乳杆菌的活菌数量。
冷冻干燥(冻干)技术是乳酸菌发酵剂生产的一项主要技术,并被广泛应用,是最适合微生物产品生产和保存的方法之一[10]。但直接冻干菌体难以得到高存活率和强稳定性的乳酸菌产品,冻干时微生物极易受到细胞膜破坏、溶质损伤、蛋白质变性失活和细胞代谢异常等生理损伤,影响微生物的发酵效果[11]。冻干保护剂能够使乳酸菌在冻干时所处的环境发生变化,降低在冻干过程中环境变化对细胞造成的损害,使微生物的生理生化特征及生物活性得到最大程度的保护[12]。STEFANELLO等[13]研究发现同时使用海藻糖、蔗糖和脱脂牛奶可以为乳杆菌IAL 454提供有效保护,使其冻干存活率保持在83%~85%。
不同保护剂对冻干乳酸菌的存活有很大的影响。本研究在传统冻干保护剂成分中添加APS,通过嗜酸乳杆菌CICC 22162冻干菌粉的生长曲线、溶菌酶敏感性实验、NaCl敏感性实验、碱性磷酸酶(alkaline phosphatase, AKP)活性、乳酸脱氢酶(lactate dehydrogenase, LDH)活性和胞内磷酸化组蛋白(γ-H2AX)含量的测定,研究APS的添加对嗜酸乳杆菌冷冻干燥保护效果的影响,还通过体外胃肠消化和贮藏稳定性实验,为乳酸菌冻干保护剂的配比优化提供理论依据,为开发长效稳定的益生菌制剂提供创新解决方案。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株活化和保藏
嗜酸乳杆菌(Lactobacillus acidophilus),中国工业微生物菌种保藏管理中心,编号CICC 22162,按照冻干菌种产品说明书将菌种在MRS液体培养基中活化,继代培养3次后,4 ℃冰箱中保存在MRS琼脂培养基上备用。
1.1.2 实验材料
黄芪,甘肃普安制药股份有限公司;MRS肉汤培养基、MRS琼脂培养基,北京奥博星生物技术有限责任公司;脱脂乳粉,新西兰恒天然集团;乳清蛋白粉、山梨糖醇、海藻糖、胃蛋白酶(3 000 U/mg)、胰蛋白酶(250 U/mg)、PBS(0.1 mol/L,pH 7.0),上海源叶生物科技有限公司;葡萄糖标准品、考马斯亮蓝G-250,Sigma-Aldrich;牛血清白蛋白(bovine albumin,BSA)标准品,Thermo Fisher;95%乙醇、浓硫酸(≥98%),国药集团化学试剂有限公司;苯酚(≥99%),Alfa Aesar;H3PO4(85%),NaCl、NaOH、KH2PO4,天津市江天化工有限公司;AKP、LDH试剂盒,北京索莱宝科技有限公司;γ-H2AX试剂盒,上海抚生生物科技有限公司。
1.2 仪器与设备
Multiwave PRO微波消解仪,奥地利安东帕有限公司;SW-CJ-2FD超净工作台,苏州安泰空气技术有限公司;Cary 60紫外-可见分光光度计,安捷伦科技有限公司;ICS5000离子色谱,美国Thermo公司;1510酶标仪,赛默飞世尔仪器有限公司;H-1850R台式高速冷冻离心机,长沙湘仪离心机仪器有限公司;JA2003电子天平,上海舜宇恒平科学仪器有限公司;LDZF-75L-I立式高压蒸汽灭菌锅,上海申安医疗机械厂;DHP-9080B智能型恒温培养箱,上海琅玕实验设备有限公司;PHS-3CB型pH计,上海越平科学仪器有限公司;HNY-303恒温孵育摇床,天津欧诺仪器股份有限公司;Christ ALPHA 1-2 LD真空冷冻干燥机,上海甄明科学仪器有限公司。
1.3 实验方法
1.3.1 APS的提取纯化和单糖组分的测定
APS的提取:参照WANG等[14]的方法,黄芪粉碎过60目筛,利用前期优化的提取条件温度70 ℃、时间6 min、料液比1∶25(g∶mL),在微波消解仪(功率500 W)中制备多糖提取液,离心后取上清液,醇沉24 h离心后取其沉淀得到粗多糖。经过脱蛋白脱色的APS用蒸馏水再溶解,阴离子交换层析纯化得到APS纯化馏分,冻干备用。
APS纯度的测定:参照冉思琪[15]的方法,采用苯酚-硫酸法测定。
纯化APS中蛋白质的测定:参照段腊梅[16]的方法,采用Bradford法进行测定。
紫外全扫描检测:参照段腊梅[16]的方法,在200~400 nm内,用去离子水调配APS质量浓度为1 mg/mL,然后进行紫外吸收光谱扫描。
分子质量的测定:参照YANG等[17]的方法,利用高效凝胶渗透色谱(high-performance gel permeationchromatography, HPGPC)分析测定。
单糖组成测定:参照冉思琪[15]的方法,用高性能阴离子交换色谱(high performance anion exchange chromatography, HPAEC)法对多糖样品进行检测。
1.3.2 菌悬液的制备和活菌计数的测定
将嗜酸乳杆菌CICC 22162以3%的接种量接种,37 ℃恒温培养箱中培养24 h,培养结束将菌液收集到离心管,离心后弃去上清液,洗涤3次后将收获的菌泥重悬于无菌PBS后冻干。
冻干保护剂由8.30%(质量分数,下同)APS、16.00%脱脂乳粉、5.20%山梨糖醇和6.50%海藻糖组成,传统保护剂配方为16.00%脱脂乳粉、5.20%山梨糖醇和6.50%海藻糖(不含APS)。APS保护剂配方的优化通过单因素试验确定了APS、脱脂乳粉、半胱氨酸、谷氨酸钠、山梨醇、海藻糖和抗坏血酸等冷干保护剂适宜的添加量,利用Plackett-Burman设计和爬坡实验确定了对嗜酸乳杆菌冻干存活率有正向影响的4种保护剂APS、脱脂乳粉、山梨糖醇和海藻糖及其适合的添加量,最后采用Box-Behnken法建立了四因素三水平的数学模型,完成了嗜酸乳杆菌冻干保护剂配方的优化。将制备好的未添加保护剂(CK)、加入APS的复合冻干保护剂(A)和传统保护剂(B)的嗜酸乳杆菌冻干粉溶于无菌PBS中,按比例制备成菌悬液。
参照MARTINS等[18]的方法,略作修改。采用平板计数法测定嗜酸乳杆菌冻干后的存活率。用0.1 mol/L无菌PBS将冻干菌粉复原至其冻干前体积,将样品依次稀释10倍至适当浓度,吸取100 μL菌液均匀涂布于MRS固体培养基,每个稀释度作3个平行,37 ℃培养48 h后计数。冻干后嗜酸乳杆菌存活率的计算如公式(1)所示:
存活率![]()
(1)
式中:N1,冷冻干燥后冻干菌粉的活菌数,CFU/mL;N0,冷干前菌悬液的活菌数,CFU/mL。
1.3.3 生长曲线的绘制
参照文献[19]的方法,略作修改。按比例在MRS液体培养基中加入3%(体积分数)的菌悬液,每隔4 h用平板计数法进行菌落计数。以横坐标为培养时间,纵坐标轴为活菌数,绘制嗜酸乳杆菌CICC 22162的生长曲线。
1.3.4 扫描电镜观察
参照文献[20]的方法,将添加不同保护剂的冻干菌粉分别用导电胶固定于样品台,喷金后置于入场发射扫描电镜内,进行电镜观察并拍照。
1.3.5 细胞壁损伤评价实验
参照文献[21]的方法,略作修改。采用溶菌酶敏感性实验对菌株进行细胞壁损伤评价。实验采用嗜酸乳杆菌CICC 22162的溶菌酶亚致死浓度,溶菌酶添加质量浓度为60 μg/L。
1.3.6 细胞膜损伤评价实验
参照唐美[22]的方法,略作修改。采用NaCl敏感性实验对菌株进行细胞膜损伤评价。实验采用嗜酸乳杆菌CICC 22162的NaCl亚致死浓度,NaCl添加浓度为0.5 mol/L。
1.3.7 酶活力的测定
用试剂盒测定AKP的活力,比活力以每毫克蛋白质表示。用试剂盒测定LDH的活力,比活力以每毫克蛋白质表示。采用微生物γ-H2AX酶联免疫分析盒测定胞内γ-H2AX的含量。
1.3.8 体外肠胃模拟消化试验
模拟人工胃液[23-24]:用1 mol/L无菌盐酸溶液调节无菌水pH,冷却后加入2 g NaCl和10 g胃蛋白酶,用0.22 μm滤膜过滤,配制成1 L pH值为2.0的人工胃液。
模拟人工肠液:将6.8 g KH2PO4溶于250 mL水、190 mL 0.2 mol/L NaOH溶于400 mL水中,将溶液pH值调节至7.0,然后加入10 g胰蛋白酶,经0.22 μm滤膜除菌,制成1 L人工肠液备用。
取0.01 g冻干菌粉加入装有10 mL人工胃液的试管中,于37 ℃摇床振荡处理2 h;然后将胃消化液加入装有10 mL人工肠液的试管中,37 ℃摇床振荡处理2 h。从开始每隔1 h取消化液稀释于pH 7的PBS,进行活菌计数。嗜酸乳杆菌存活率的计算如公式(2)所示:
存活率![]()
(2)
式中:N1,经模拟胃液或肠液消化后的活菌数,CFU/mL;N0,加入模拟胃液第0 h时的嗜酸乳杆菌活菌数,,CFU/mL。
1.3.9 贮藏稳定性实验
参考CHEN等[25]的方法,略作修改。将3组冻干菌粉采用铝箔袋密封包装后,分别置于4 ℃(低温)冰箱和25 ℃(常温)恒温培养箱中,每隔15 d进行一次活菌数测定,测定到120 d。
1.4 数据处理
每组实验至少重复3次,使用SPSS 25软件对数据进行差异显著性。使用Origin 2021软件图表绘制。实验数值以“平均数±标准差”表示,当P<0.05时,认为平均值显著不同。
2 结果与分析
2.1 APS的提取纯化和单糖组分的测定
经过前期实验条件的优化,在提取温度70 ℃、时间6 min、料液比1∶25(g∶mL)时,多糖提取率达到7.63%。经纯化后APS纯度为(97.02±0.16)%,残留蛋白质含量为(0.45±0.05)%。该结果与紫外光谱扫描检测结果(图1-a)一致,在260 nm和280 nm处无显著吸收峰,表明脱蛋白和脱色步骤已有效去除蛋白质、核酸等杂质,与TANG等[26]的研究结果类似,也可以间接证明多糖组分纯度较高。
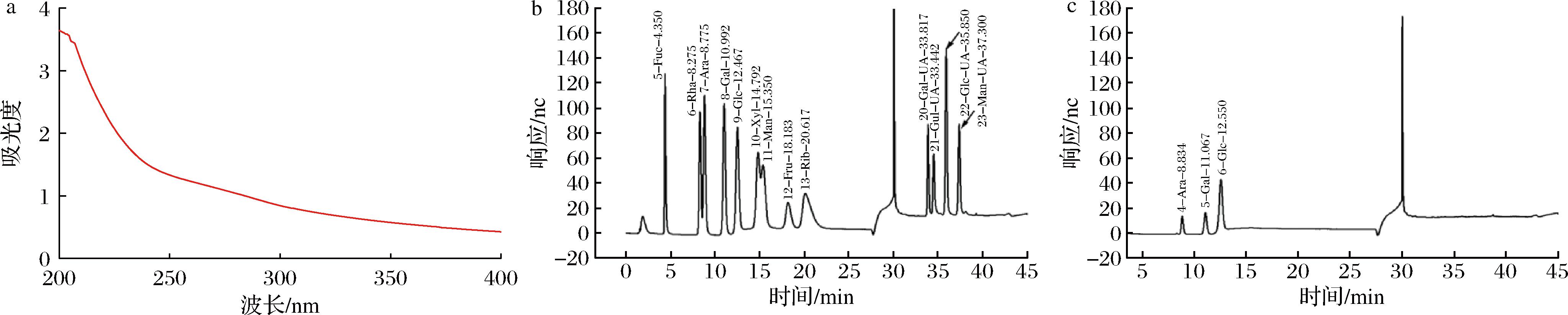
a-APS紫外吸收光谱;b-单糖标准品高效液相色谱图;c-黄芪纯化多糖高效液相色谱图
图1 APS紫外吸收光谱、单糖标准品高效液相色谱和黄芪纯化多糖高效液相色谱
Fig.1 Ultraviolet absorption spectrum of APS, HPLC chromatogram of monosaccharide standards and purified APS
通过标准样品HPGPC分析得到标准分子质量线性方程为:y=-0.237x+6.43;R2=0.991,根据APS保留时间10.496 min,利用标准品曲线,计算出APS的分子质量为8 754 Da。
多糖样品分析显示APS主要由阿拉伯糖、半乳糖和葡萄糖构成(摩尔比1∶1.25∶4.07),该组成特征与文献[14,27]报道的APS单糖成分相似。
2.2 APS和冻干保护剂对冻干菌粉的生长曲线的影响
未添加保护剂(CK)、加入APS的冻干保护剂(A)和添加传统保护剂(B)后嗜酸乳杆菌CICC 22162冻干存活率分别为36.52%、78.64%和85.02%。如图2所示,A组在培养中后期保持了最高的活菌水平,且稳定性优于B组和CK组。A组和B组生长现象大致相同,但是CK组的嗜酸乳杆菌延滞期较长,进入稳定期的时间比另外2组迟滞约4 h。结果说明,APS的加入可以有效唤醒嗜酸乳杆菌的生长,加快生长速率。3组嗜酸乳杆菌生长趋势和最终生物量趋向于一致,但添加传统冻干保护剂配方的菌株进入稳定期的时间有一定的迟滞,其最终生物量略低于添加了APS的冻干菌粉。需要注意的是,本研究中APS保护剂的活性成分含量较传统组高8.3%,可能贡献了部分效果提升。结果表明APS可能为嗜酸乳杆菌的初始生长提供了更多的碳源。
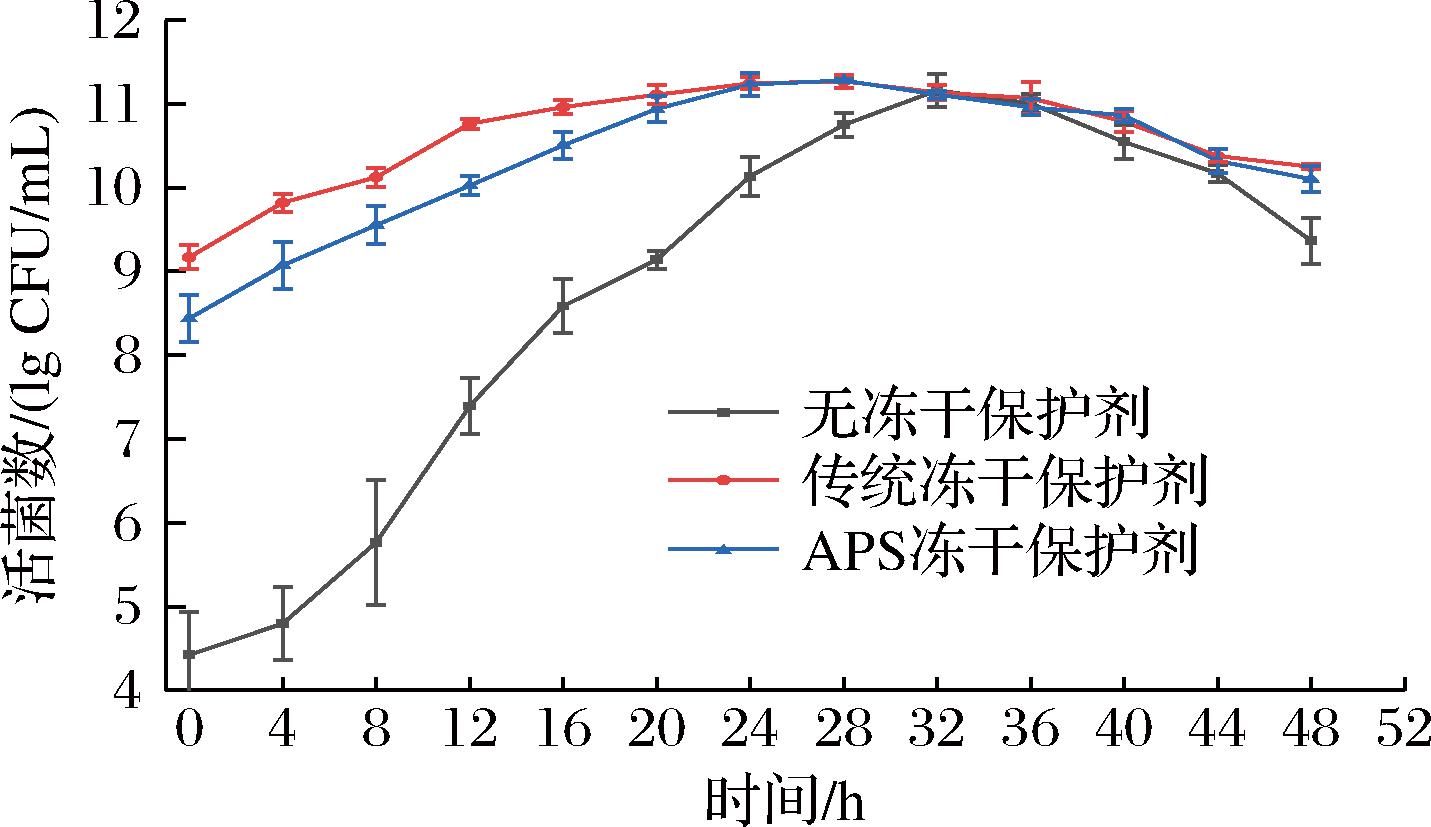
图2 嗜酸乳杆菌CICC 22162生长曲线
Fig.2 Growth curve of L. acidophilus CICC 22162
许多研究有类似结果,宋虹等[28]发现使用2种方法提取的大豆多糖做碳源有利于副干酪乳酪杆菌6244生长期的提前到来,由9.53 h缩短至4.08 h和4.69 h。李媛等[29]发现银耳多糖可以在德氏乳杆菌保加利亚亚种和唾液链球菌嗜热亚种进入对数生长期时,加快其生长速率,且生长速率与银耳多糖浓度呈正相关。
2.3 扫描电镜分析
将CK组、A组和B组冻干菌粉在场发射高分辨扫描电镜下放大5 000倍,观察菌粉的结构见图3。由图3-a可以看出正常冻干后嗜酸乳杆菌菌体纤细,杆状较长,排列杂乱;添加冻干保护剂后,嗜酸乳杆菌的杆状缩短变粗,多以单个分布,被冻干保护剂包裹(图3-b);而从图3-c可以看到APS保护剂组冻干菌粉嗜酸乳杆菌菌体呈短杆状,表面相对光滑,个体完整。

a-未添加保护剂;b-添加传统保护剂;c-加入APS的冻干保护剂
图3 嗜酸乳杆菌冻干菌粉扫描电镜图(5 000×)
Fig.3 SEM images of freeze-dried powder of L. acidophilus(5 000×)
冻干保护剂的添加使得菌体结构较为稳定且均匀,对菌体能形成完整的保护,使细胞免受低温的破坏,而且会使嗜酸乳杆菌冻干后的菌体形态由长杆状变成短杆状,由菌体纤细变成菌体粗壮。可能与嗜酸乳杆菌的防御机制有关,通过改变杆的长短、粗细,减少与外界环境的接触面积,从而抵抗外界不利环境变化的影响,维持细胞正常的生命活动。
2.4 细胞壁完整性表征分析
AKP作为定位于细胞壁-膜界面的关键酶,其胞外活力可灵敏反映壁结构完整性[30]。如图4-a所示,正常菌株组的AKP活力最低(1 978.67±61.67) U/g,代表了未冻干菌体的天然细胞壁-膜完整状态。未添加冻干保护剂组的AKP活力最高(7 396±160.10) U/g,显著高于其他组(P<0.05),表明冻干过程对细胞壁造成了严重破坏,与正常菌株组(1 978.67±61.67) U/g相比,活力升高了2.7倍,说明冻干导致了不可逆的损伤。相比之下,APS+保护剂组的AKP活力(3 450.33±95.83) U/g较无保护剂组降低了55.4%(P<0.05),证明APS能够显著减轻冻干对细胞壁的损伤。此外,APS组的AKP活力较传统保护剂组(4 082±85.02) U/g降低了15.5%,表明添加APS后保护效果优于传统保护剂,可能通过增强膜稳定性、增强细胞壁的机械强度或发挥抗氧化作用等机制实现。
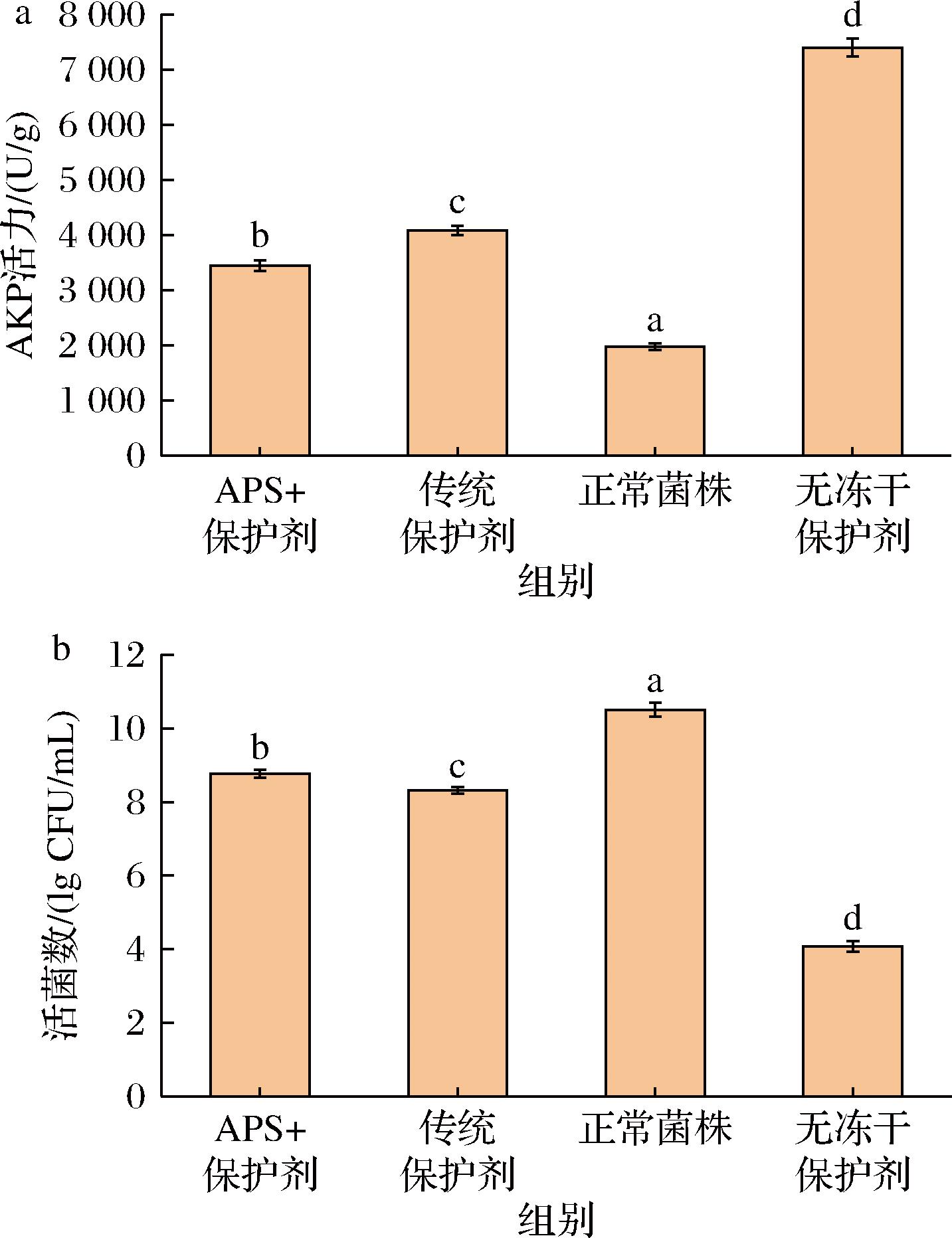
图4 冻干保护剂对冻干嗜酸乳杆菌细胞壁损伤的影响
Fig.4 Effect of freeze-drying protectant on cell wall damage of freeze-dried L. acidophilus
注:不同小写字母表示同一指标不同处理间差异显著(P<0.05)(下同)。
传统保护剂组AKP活力虽然显著优于无保护剂组(P<0.05),但其保护效果仍有限,提示传统保护剂(如海藻糖、脱脂乳粉等)在维持壁-膜完整性方面存在一定局限性。APS作为一种新型冻干保护剂,显著降低了AKP泄漏,其活力仅为传统保护剂的84.5%,表明其在维持细胞壁完整性方面具有显著优势。值得关注的是,APS中占比高的葡萄糖单元单糖组成分析显示APS含较多的葡萄糖单元,与TRIPATHI等[31]报道的β-葡聚糖增强乳酸菌细胞壁机械强度的机制相似,但APS分子构象还需通过后续结构表征进一步解析。
溶菌酶敏感性实验进一步验证了APS对嗜酸乳杆菌冻干菌粉的保护作用(图4-b)。溶菌酶能够降解细胞壁肽聚糖,导致细胞裂解,因此活菌数越多,表明细胞壁完整性越好,保护效果越显著。正常菌株的活菌数为(10.51±0.19) lg CFU/mL,APS组的活菌数降幅为1.73 lg CFU/mL,显著低于无冻干保护剂组的6.43 lg CFU/mL(P<0.05),表明APS能够有效维持细胞壁完整性,减少溶菌酶对细胞的破坏。与传统保护剂组(8.32±0.08) lg CFU/mL相比,APS组的活菌数降幅更低,说明其保护效果优于传统保护剂。综合来看,APS通过增强细胞壁稳定性,显著降低溶菌酶对细胞的敏感性,证明其在冻干过程中对细胞壁-膜结构的保护作用优于传统保护剂,表明APS是一种高效的冻干保护剂,能够显著提高嗜酸乳杆菌冻干菌粉的存活率和稳定性。APS组的菌体在冻干后呈现更完整的细胞形态(图3),且溶菌酶敏感度显著降低。结合已有研究,多糖类保护剂(如海藻糖)的冻干保护作用通常依赖玻璃化基质形成或物理屏障效应,而非化学修饰[32]。因此,APS可能通过类似机制(如包覆细胞壁或降低溶菌酶接触效率)提升菌体抗性。
2.5 LDH活力与细胞膜完整性分析
基于NaCl敏感性建立的细胞膜完整性评价体系显示(图5-a),正常菌株组的活菌数最高(9.79±0.03) lg CFU/mL,添加传统冻干保护剂和APS的冻干菌粉在NaCl选择培养基中的活菌数分别为(7.15±0.10) lg CFU/mL和(8.21±0.08) lg CFU/mL,均显著高于无冻干保护剂组的(3.53±0.30) lg CFU/mL(P<0.05),表明冻干保护剂可以一定程度上维持细胞膜完整性,减少NaCl对细胞的渗透压损伤[33]。
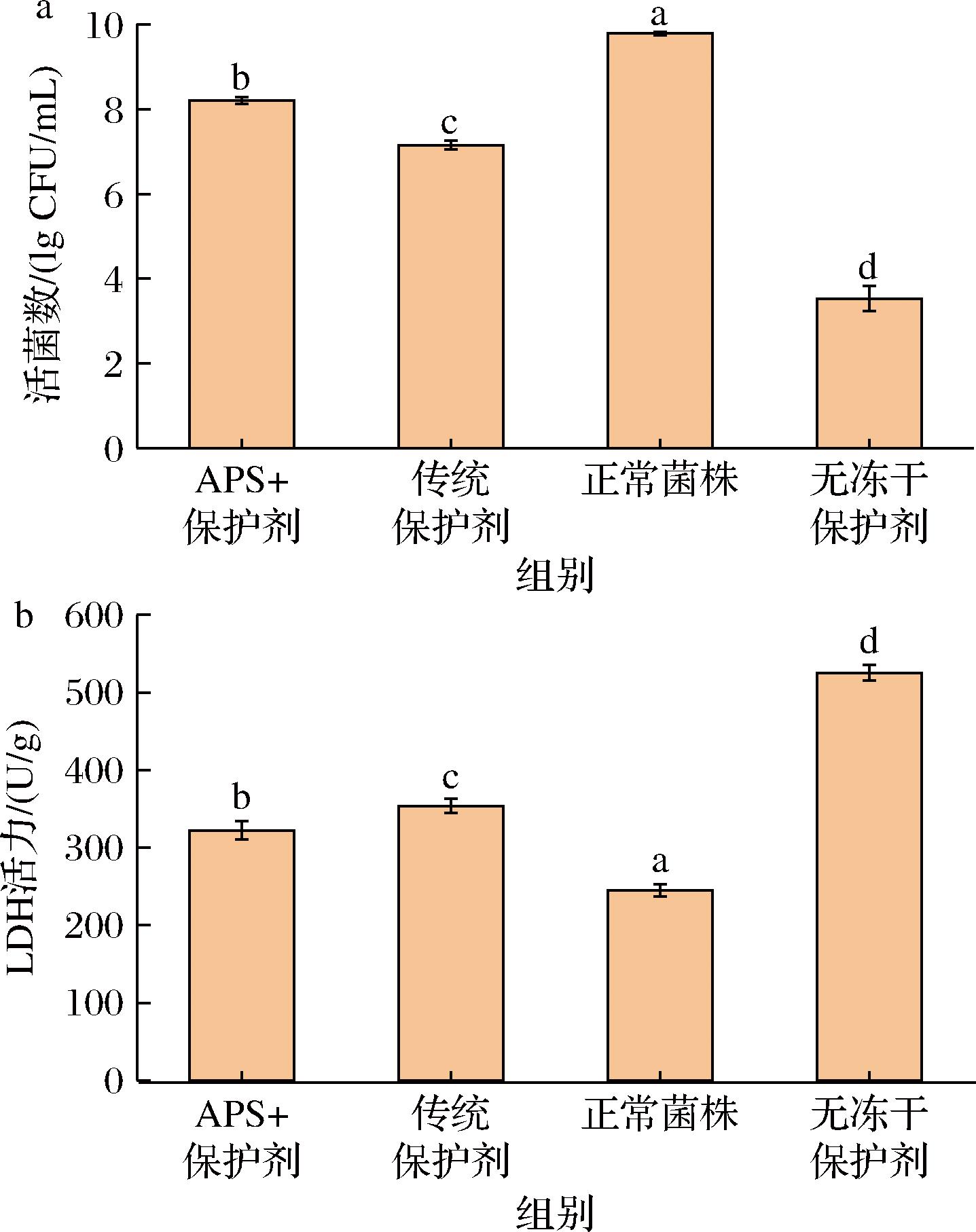
a-NaCl敏感性实验;b-LDH活力测定
图5 冻干保护剂对冻干嗜酸乳杆菌细胞膜损伤的影响
Fig.5 Effect of freeze-drying protectant on membrane damage of freeze-dried L. acidophilus
APS组的活菌数降幅较传统保护剂组提高了14.8%,说明APS在保护细胞膜完整性方面优于传统保护剂,可能通过增强膜稳定性或调节渗透压耐受性来实现。无冻干保护剂组的活菌数最低,表明冻干过程对细胞膜造成了严重损伤,导致细胞对NaCl的敏感性显著增加。说明APS能有效维持细胞膜屏障功能,提高嗜酸乳杆菌冻干菌粉的存活率和稳定性。GONG等[34]在保加利亚乳杆菌sp1.1喷雾干燥过程中发现细胞壁首先损伤,并不致命,而NaCl耐受性的降低,使得活细胞数急剧减少,表明细胞膜损伤是喷雾干燥过程中细胞死亡的原因。
LDH作为糖酵解途径的关键酶系(EC 1.1.1.27/28),其催化丙酮酸-乳酸转化的能力直接影响菌株能量代谢效率[35]。LDH活力与细胞膜完整性密切相关,活力值越高表明细胞膜损伤越严重。LDH活力检测显示(图5-b),无冻干保护剂组的LDH活力最高(525.33±10.21) U/g,显著高于其他组(P<0.05),表明冻干过程对细胞膜造成了严重破坏。相比之下,APS+保护剂组的LDH活力(322.33±11.95) U/g较无保护剂组降低了38.6%(P<0.05),证明APS能够显著减轻冻干对细胞膜的损伤。此外,APS组的LDH活力较传统保护剂组(354.00±9.63) U/g降低了8.9%,表明其保护效果优于传统保护剂,可能通过稳定细胞膜结构或减少冻干时冰晶的形成来实现。
传统保护剂组虽然显著优于无保护剂组(P<0.05),但其LDH活力仍较高,正常菌株组的LDH活力最低(245.00±7.79) U/g,表明传统保护剂在维持细胞膜完整性方面仍有一定局限性。APS可能通过多靶点保护机制维持壁-膜完整性,降低了胞内物质的泄漏,也可能通过影响细胞膜脂肪酸组成,提高菌株的细胞膜紧凑程度,维持细胞膜的流动性,使菌株细胞膜结构更加稳定[35]。
2.6 APS对嗜酸乳杆菌冷冻干燥DNA的影响
γ-H2AX是DNA双链断裂的敏感标记物,其表达水平与DNA损伤程度呈正相关[36]。由图6可知,无冻干保护剂组的γ-H2AX含量最高,为(8.63±0.23) pg/g,显著高于其他组(P<0.05),可能是冻干过程引发的氧化应激或机械损伤导致了严重的DNA断裂。而添加APS的保护组γ-H2AX含量为(5.85±0.11) pg/g较无保护剂组降低了32.2%(P<0.05),传统保护剂组的γ-H2AX含量(6.23±0.037) pg/g异常低于正常菌株组(4.63±0.05) pg/g。相比之下,APS组的γ-H2AX含量虽高于正常菌株,但更接近未冻干的天然状态,表明其保护作用更侧重于减少损伤而非干扰信息传递。结果证明,APS能够有效缓解DNA损伤,其机制可能涉及清除冻干过程中产生的自由基、减少氧化攻击或通过稳定染色质结构限制DNA链断裂[37]。
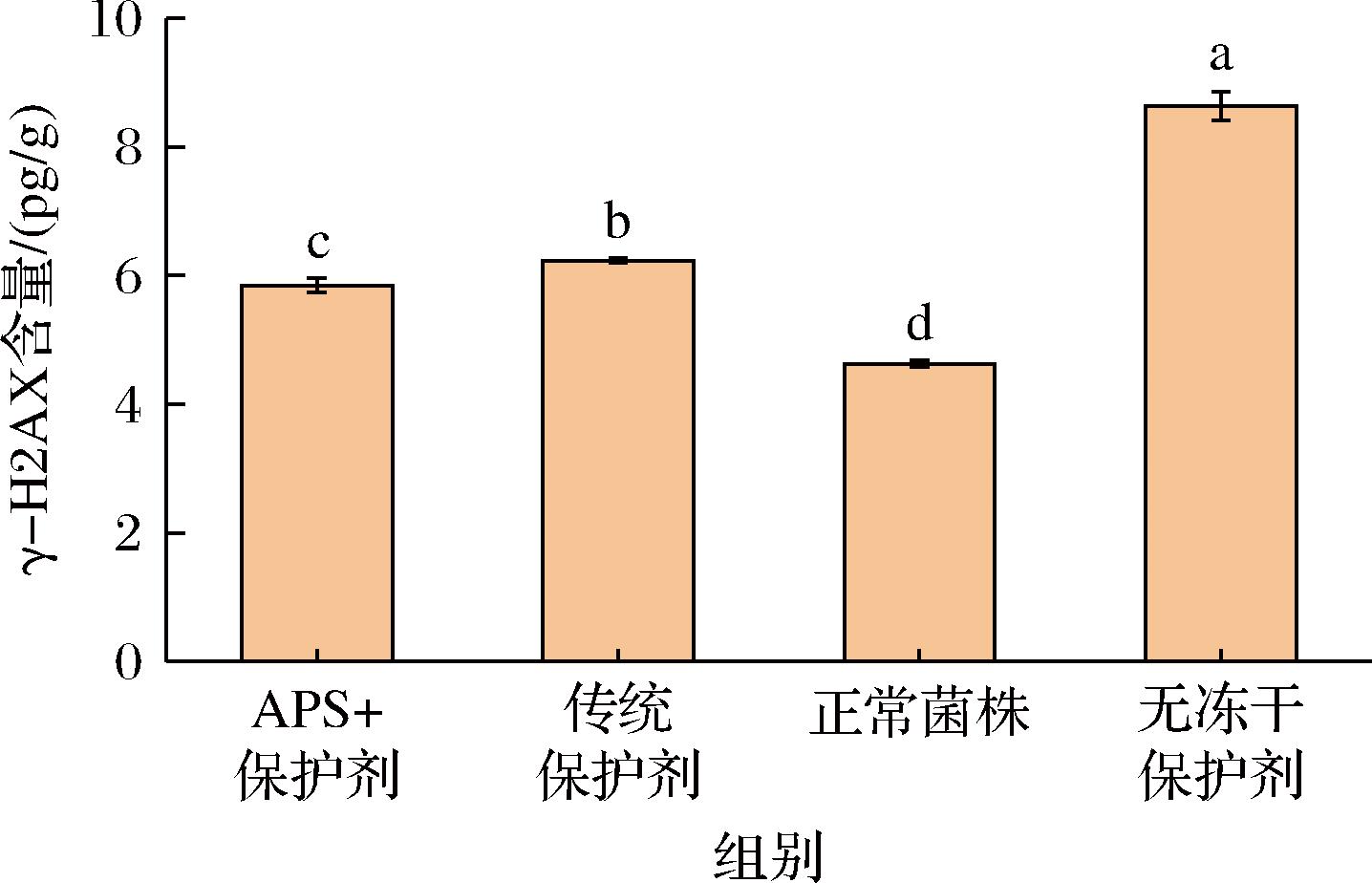
图6 冻干保护剂对冻干嗜酸乳杆菌DNA损伤的影响
Fig.6 Effect of freeze-drying protectants on DNA damage in freeze-dried L. acidophilus
2.7 APS对嗜酸乳杆菌胃肠消化耐受性的影响
如图7所示,APS对胃肠消化的保护作用显著优于传统保护剂和未加保护剂组。未加冻干保护剂的菌粉在胃液消化阶段(0~2 h)活菌数急剧下降,0 h初始活菌数为(10.42±0) lg CFU/mL,1 h后降至(7.36±0.36) lg CFU/mL,2 h后进一步降至(5.13±0.12) lg CFU/mL,表明胃液对冻干后的菌体造成了严重损伤;进入肠液消化阶段(2~4 h)后,活菌数持续衰减至(3.39±0.18) lg CFU/mL(3 h)和(2.15±0.08) lg CFU/mL(4 h),存活率仅为20.6%,未保护菌体在胃肠消化后几乎完全失活。相比之下,APS组的活菌数在胃液阶段仅轻微下降,0 h为(10.79±0) lg CFU/mL,1 h和2 h分别维持在(10.16±0.11) lg CFU/mL(降幅5.8%)和(9.71±0.13) lg CFU/mL(降幅10.0%),显著优于传统保护剂组同期活菌数。进入肠液消化后,APS组的活菌数仍稳定保持在(9.03±0.11) lg CFU/mL(3 h)和(8.77±0.09) lg CFU/mL(4 h),存活率达81.3%,传统保护剂组在肠液环境中保护效果明显减弱,3 h活菌数降至(8.24±0.09) lg CFU/mL,4 h进一步降至(7.81±0.07) lg CFU/mL。而传统保护剂组在2 h(肠液起始点)出现异常骤降,可能与其在酸碱环境切换时稳定性不足相关,而APS组在此阶段未出现显著波动,表明其保护机制具有酸碱适应性。
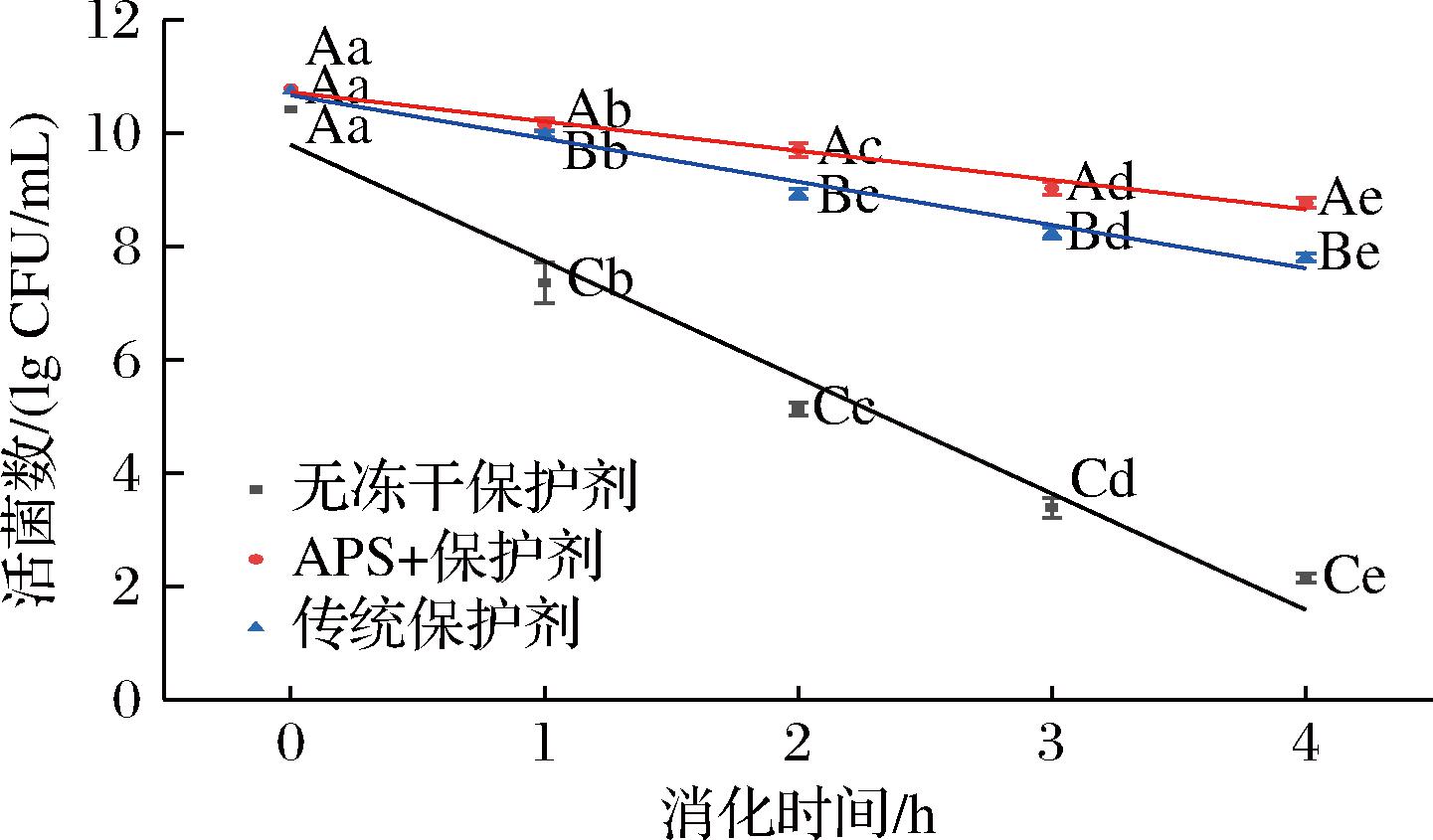
图7 冻干保护剂对冻干嗜酸乳杆菌胃肠消化耐变性的影响
Fig.7 Effect of freeze-drying protectant on the gastrointestinal digestive tolerance of freeze-dried L. acidophilus
注:大写字母表示不同处理组间差异显著,小写字母表示同一指标不同处理间差异显著(P<0.05)(下同)。
结果可知,APS可以显著提升嗜酸乳杆菌对胃酸(低pH)和肠液(胆盐、消化酶)的连续耐受性,为口服益生菌制剂的开发提供了更优的冻干保护参考。这种差异可能源于2类保护剂的作用靶点差异,传统保护剂(如海藻糖)主要通过玻璃化转变降低冰晶损伤[38],而APS除物理保护外,可能通过促进乳酸菌的生长和调控应激相关基因的表达增强菌体适应性[39]。这种生物活性保护机制使嗜酸乳杆菌在动态消化环境中展现出更强的抗逆性。
2.8 APS对嗜酸乳杆菌贮藏稳定性的影响
如图8所示,在4 ℃贮藏条件下,APS组的活菌数从初始的10.79 lg CFU/mL,经120 d仅下降至9.18 lg CFU/mL,平均衰减速率为0.013 lg CFU/(mL·d),显著低于传统保护剂组和无保护剂组。APS组在60 d后活菌数仍维持在10.02 lg CFU/mL以上,表明APS能有效抑制低温贮藏中的代谢性损伤。在常温贮藏(25 ℃)至120 d时,APS组活菌数从10.79 lg CFU/mL降至7.89 lg CFU/mL,而传统保护剂组从10.75 lg CFU/mL降至5.96 lg CFU/mL,无保护剂组从5.21 lg CFU/mL降至1.46 lg CFU/mL,衰退更快。
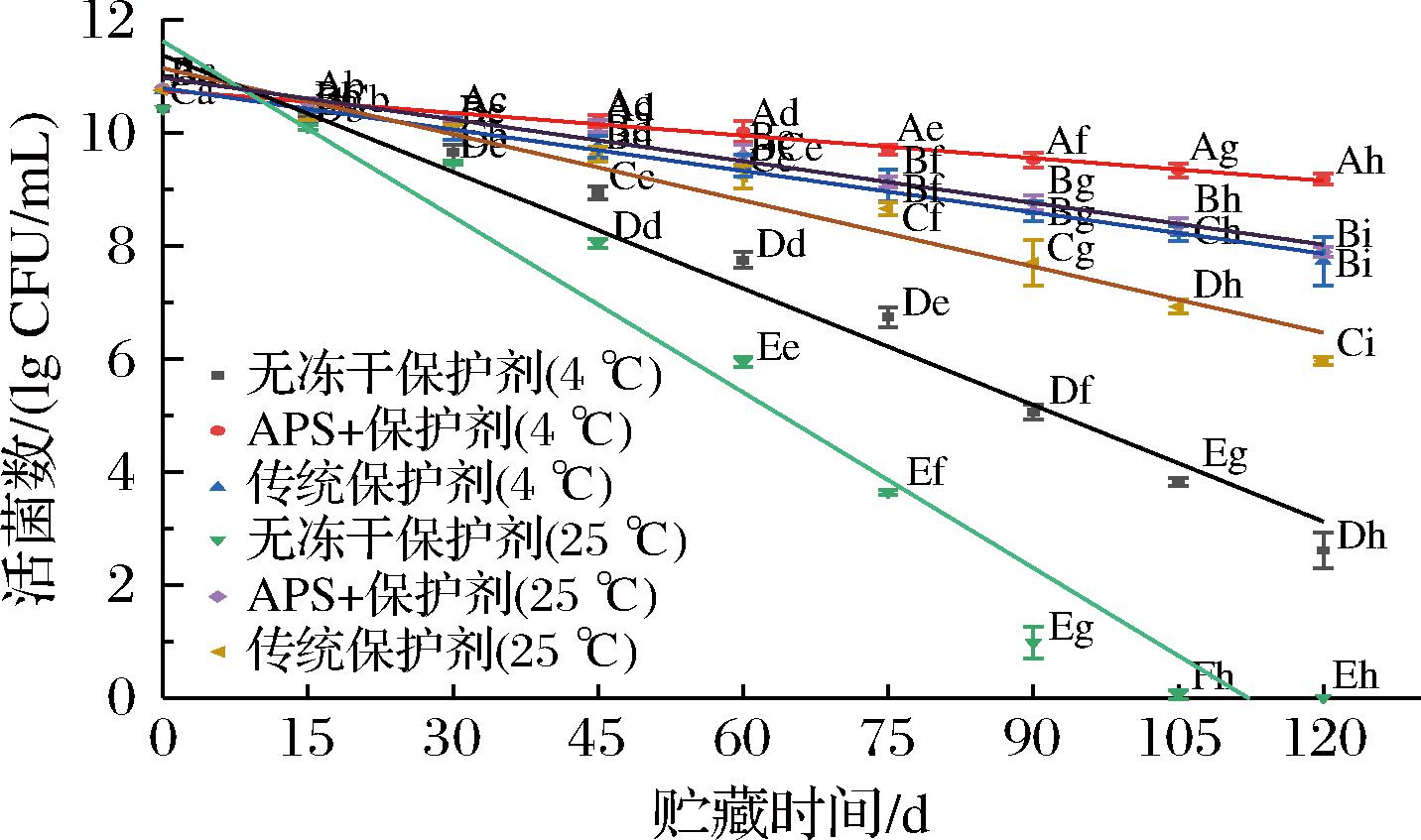
图8 冻干保护剂对嗜酸乳杆菌菌粉贮藏稳定性的影响
Fig.8 Effect of freeze-drying protectant on the storage stability of L. acidophilus powder
分析发现,APS组在2种温度下的衰减曲线均呈现“两阶段模式”。前45 d为缓慢衰退期,后期(45~120 d)进入稳定平台期,可能是通过形成多糖-膜复合物抑制细胞膜脂质过氧化,同时降低胞内酶泄漏导致的连锁损伤[37]。相比之下,传统保护剂组的单相线性衰减(R2>0.98)提示其仅通过物理隔离作用延缓损伤,无法阻断持续性代谢消耗。此差异在高温条件下被放大:APS组120 d活菌数(7.89 lg CFU/mL)仍高于传统保护剂组60 d水平(9.21 lg CFU/mL降至7.69 lg CFU/mL),证明其更适用于冷链不完善的贮藏场景。结果表明,与传统保护剂相比,APS的添加能更有效地维持嗜酸乳杆菌在贮藏期间的活菌数,特别是在常温(25 ℃)条件下。结果与GE等[40]利用4.2%海藻糖、2.0%甘露醇、11.9%脱脂乳和4.1%谷氨酸钠对乳酸乳球菌ZFM 559贮藏稳定性影响的结果一致。研究结果还表明,为了保持最佳的益生菌活性,应当尽可能缩短冻干粉的储存时间。后续的研究可以集中在APS发挥保护效应的具体作用机制或是探索最佳冻干菌粉的储存包装。
3 结论
本研究首次明确了APS与传统冻干保护剂对嗜酸乳杆菌CICC 22162冻干菌粉的协同增效作用。研究确定了APS特征性单糖组成(64.38%葡萄糖,19.81%半乳糖和15.81%阿拉伯糖),与冻干保护剂组合可以显著提高嗜酸乳杆菌冻干菌粉的生长速率,并改变了其冻干后的形态,增强其对不利环境的耐受性。在冻干过程中,APS复合保护剂通过提升菌体抗性,将菌体存活率提升至(85.02±1.25)%,较传统配方提高6.38%,并有效维持细胞壁完整性(溶菌酶敏感性降低14.8%)及膜稳定性(NaCl胁迫下活菌数降幅减少15.5%)。同时,APS通过对菌株细胞壁和细胞膜的保护作用,γ-H2AX流出降低32.2%,DNA氧化损伤减轻,多糖组分在表观调控中的潜在作用还有待探究。
冻干菌粉经APS保护后,胃肠消化存活率提升至81.3%(较传统保护剂组提高33.9%),且在4 ℃贮藏120 d后活菌数仍达9.18 lg CFU/mL,半衰期明显延长。本研究不仅为益生菌冻干保护剂的分子设计提供了理论依据(如单糖比例优化、膜靶向修饰),更开发出兼具高存活率(>85%)、强胃肠耐受性(胃液阶段存活率>90%)及长效稳定性(货架期≥4个月)的功能性菌粉,在功能性食品开发与肠道微生态制剂领域展现出双重应用价值。后续研究可以聚焦于APS结构和组分与菌体应激信号通路(如SOS响应、渗透压调节)的互作机制解析,以推动益生菌保护剂从经验复配向精准调控的范式转变。
[1] 姜辉, 顾胜龙, 张玉婷, 等.黄芪化学成分和药理作用研究进展[J].安徽中医药大学学报, 2020, 39(5):93-96.
JIANG H, GU S L, ZHANG Y T, et al.Research progress on chemical constituents and pharmacological effects of Astragalus membranaceus[J].Journal of Anhui University of Chinese Medicine, 2020, 39(5):93-96.
[2] LI C X, LIU Y, ZHANG Y Z, et al.Astragalus polysaccharide:A review of its immunomodulatory effect[J].Archives of Pharmacal Research, 2022, 45(6):367-389.
[3] 薛晨曦. 黄芪多糖合生元的制备与临床初步应用[D].长春:吉林大学, 2023.
XUE C X.Preparation and preliminary clinical application of astragalus polysaccharide synbiotics[D].Changchun:Jilin University, 2023.
[4] JING Y P, LI A P, LIU Z R, et al.Absorption of Codonopsis pilosula saponins by coexisting polysaccharides alleviates gut microbial dysbiosis with dextran sulfate sodium-induced colitis in model mice[J].BioMed Research International, 2018, 2018:1781036.
[5] WANG G Q, LUO L Y, DONG C, et al.Polysaccharides can improve the survival of Lactiplantibacillus plantarum subjected to freeze-drying[J].Journal of Dairy Science, 2021, 104(3):2606-2614.
[6] DONG Y S, LI M H, YUE X Q.Current research on probiotics and fermented products[J].Foods, 2024, 13(9):1406.
[7] MINJ J, CHANDRA P, PAUL C, et al.Bio-functional properties of probiotic Lactobacillus:Current applications and research perspectives[J].Critical Reviews in Food Science and Nutrition, 2021, 61(13):2207-2224.
[8] SHI Z H, LI X F, FAN X K, et al.The SlpX protein plays a crucial role in the intestinal juice tolerance of Lactobacillus acidophilus CICC6074[J].Food Bioscience, 2024, 59:103865.
[9] 周立光, 杨明喆, 冯会粉, 等.复合益生菌产品菌种鉴定及活菌定量检测方法[J].食品与发酵工业, 2022, 48(9):235-244.
ZHOU L G, YANG M Z, FENG H F, et al.Study on methods of species identification and quantitative detection of viable cells in composite probiotics products[J].Food and Fermentation Industries, 2022, 48(9):235-244.
[10] IBRAHIM I, AYARIGA J A, XU J H, et al.A comparative study of skimmed milk and cassava flour on the viability of freeze-dried lactic acid bacteria as starter cultures for yogurt fermentation[J].Foods, 2023, 12(6):1207.
[11] GAGNETEN M, PASSOT S, CENARD S, et al.Mechanistic study of the differences in lactic acid bacteria resistance to freeze- or spray-drying and storage[J].Applied Microbiology and Biotechnology, 2024, 108(1):361.
[12] LIU L, XIE S S, ZHU Y D, et al.Sodium carboxymethyl celluloses as a cryoprotectant for survival improvement of lactic acid bacterial strains subjected to freeze-drying[J].International Journal of Biological Macromolecules, 2024, 260:129468.
[13] STEFANELLO R F, NABESHIMA E H, IAMANAKA B T, et al.Survival and stability of Lactobacillus fermentum and Wickerhamomyces anomalus strains upon lyophilisation with different cryoprotectant agents[J].Food Research International, 2019, 115:90-94.
[14] WANG J, JIA J Y, SONG L, et al.Extraction, structure, and pharmacological activities of Astragalus polysaccharides[J].Applied Sciences, 2019, 9(1):122.
[15] 冉思琪. 黄芪多糖APS-1a的分离纯化、结构鉴定及促进肝细胞EPO分泌的研究[D].武汉:华中科技大学, 2020.
RAN S Q.Isolation, purification, structural characterization of polysaccharide APS-1a from Astragalus membranaceus and its activity of stimulating EPO secretion in HepG2 cell[D].Wuhan:Huazhong University of Science and Technology, 2020.
[16] 段腊梅. 苹果梨渣多糖结构表征及其与乳清蛋白相互作用研究[D].锦州:渤海大学, 2021.
DUAN L M.Structural characterization of polysaccharides from ‘Pingguo’ pear residue and their interactions with whey protein[D].Jinzhou:Bohai University, 2021.
[17] YANG W H, HAO J W, CHEN N D, et al.Development of a joint derivatization protocol for the unequivocal identification of the monosaccharide composition in four Dendrobium polysaccharides and free monosaccharide by GC-MS[J].Biomedical Chromatography, 2023, 37(12):e5743.
[18] MARTINS G N, GUERRERO S NCHEZ M, CARBONI A D, et al.Use of legume wastewater extracts on the storage stability of freeze-dried Lactiplantibacillus plantarum WCFS1[J].Food and Bioprocess Technology, 2025, 18(2):1707-1718.
NCHEZ M, CARBONI A D, et al.Use of legume wastewater extracts on the storage stability of freeze-dried Lactiplantibacillus plantarum WCFS1[J].Food and Bioprocess Technology, 2025, 18(2):1707-1718.
[19] BROMLEY A, PERRY J.Survival of probiotic Lactobacillus spp.during kombucha fermentation[J].Current Developments in Nutrition, 2022, 6:507.
[20] ALIZADEH BEHBAHANI B, JOOYANDEH H, VASIEE A, et al.Evaluation of anti-yeast metabolites produced by Lactobacillus strains and their potential application as bio-preservatives in traditional yogurt drink[J].LWT, 2023, 188:115428.
[21] EL OIRDI S, LAKHLIFI T, FRABERGER V, et al.Probiotic features of three lactic acid bacteria strains isolated from foods and characterization of their bioactive molecules[J].Microbiology, 2023, 92(6):881-891.
[22] 唐美. 卷曲乳杆菌发酵培养基优化及其抑菌物质的初步分离纯化和鉴定[D].长沙:中南大学, 2022.
TANG M.Optimization of fermentation medium of Lactobacillus crispatus and preliminary isolation, purification and identification of their antibacterial substances[D].Changsha:Central South University, 2022.
[23] 刘敏敏, 席茂盛, 李中媛, 等.植物乳杆菌CGMCC8198冻干菌粉的制备工艺优化[J].食品研究与开发, 2020, 41(21):9-14.
LIU M M, XI M S, LI Z Y, et al.Preparation process optimization of Lactobacillus plantarum CGMCC8198 lyophilized powder[J].Food Research and Development, 2020, 41(21):9-14.
[24] GARC A-CEJA A, MANI-L
A-CEJA A, MANI-L PEZ E, PALOU E, et al.Viability during refrigerated storage in selected food products and during simulated gastrointestinal conditions of individual and combined lactobacilli encapsulated in alginate or alginate-chitosan[J].LWT-Food Science and Technology, 2015, 63(1):482-489.
PEZ E, PALOU E, et al.Viability during refrigerated storage in selected food products and during simulated gastrointestinal conditions of individual and combined lactobacilli encapsulated in alginate or alginate-chitosan[J].LWT-Food Science and Technology, 2015, 63(1):482-489.
[25] CHEN B Y, WANG X Y, LI P Z, et al.Exploring the protective effects of freeze-dried Lactobacillus rhamnosus under optimized cryoprotectants formulation[J].LWT, 2023, 173:114295.
[26] TANG Z J, HUANG G L.Extraction, structure, and activity of polysaccharide from Radix astragali[J].Biomedicine &Pharmacotherapy, 2022, 150:113015.
[27] LI K, LI X Q, LI G X, et al.Relationship between the structure and immune activity of components from the active polysaccharides APS-II of astragali Radix by enzymolysis of endo α-1, 4-glucanase[J].Frontiers in Pharmacology, 2022, 13:839635.
[28] 宋虹, 陈晨, 张尊琴, 等.大豆种皮多糖对副干酪乳杆菌6244生长及肠道黏附性的影响[J].中国食品学报, 2025, 25(1):142-150.
SONG H, CHEN C, ZHANG Z Q, et al.Effects of soybean hull polysaccharides on the growth and adhesion of Lactobacillus paracasei 6244[J].Journal of Chinese Institute of Food Science and Technology, 2025, 25(1):142-150.
[29] 李媛, 谢玉东, 王媛媛.银耳多糖对椰浆酸奶感官品质及益生菌生长的影响[J].食品安全导刊, 2024(29):113-118.
LI Y, XIE Y D, WANG Y Y.Effect of Tremella fuciformis polysaccharides on sensory quality and probiotic growth of coconut milk yogurt[J].China Food Safety Magazine, 2024(29):113-118.
[30] WANG H, SHAO L L, SUN Y Y, et al.Recovery mechanisms of ohmic heating-induced sublethally injured Staphylococcus aureus: Changes in cellular structure and applications in pasteurized milk[J].Food Control, 2025, 171:111086.
[31] TRIPATHI A, LIVERANI E, TSYGANKOV A Y, et al.Iron alters the cell wall composition and intracellular lactate to affect Candida albicans susceptibility to antifungals and host immune response[J].Journal of Biological Chemistry, 2020, 295(29):10032-10044.
[32] 张玉华, 孟一, 凌沛学, 等.海藻糖和透明质酸对冻干双歧杆菌细胞的保护作用[J].食品科学, 2010, 31(7):236-241.
ZHANG Y H, MENG Y, LING P X, et al.Protective mechanisms of trehalose and hyaluronic acid on lyophilized Bifidobacterium longum[J].Food Science, 2010, 31(7):236-241.
[33] MOAYYEDI M, ESKANDARI M H, RAD A H E, et al.Effect of drying methods (electrospraying, freeze drying and spray drying) on survival and viability of microencapsulated Lactobacillus rhamnosus ATCC 7469[J].Journal of Functional Foods, 2018, 40:391-399.
[34] GONG P M, SUN J L, LIN K, et al.Changes process in the cellular structures and constituents of Lactobacillus bulgaricus sp1.1 during spray drying[J].LWT, 2019, 102:30-36.
[35] 鄂晶晶. 培养条件对植物乳植杆菌LIP-1冷冻干燥存活率的影响及其内在机制的研究[D].呼和浩特:内蒙古农业大学,2022.
E J J.Effect of culture conditions on Lactiplantibacillus plantarum LIP-1 freeze-drying survival rate and the internal mechanism of action[D].Hohhot:Inner Mongolia Agricultural University, 2022.
[36] 王依朝, 樊丽, 王红霞, 等.γH2AX、53BP1及RAD51焦点用于分析DNA双链断裂损伤[J].生物学杂志, 2020, 37(1):16-19.
WANG Y Z, FAN L, WANG H X, et al.γH2AX, 53BP1 and RAD51 foci analysis for monitoring DNA double-strand breaks[J].Journal of Biology, 2020, 37(1):16-19.
[37] 李明慧, 尚一娜, 霍麒文, 等.真空冷冻干燥对乳酸菌损伤机制的研究进展[J].食品科学, 2018, 39(19):273-279.
LI M H, SHANG Y N, HUO Q W, et al.Recent progress in understanding injury mechanisms of lactic acid bacteria during freeze-drying[J].Food Science, 2018, 39(19):273-279.
[38] WANG R X, E J J, YANG Y, et al.Trehalose enhances the resistance of Lactiplantibacillus plantarum LIP-1 to spray- and freeze-drying treatments by regulating amino acid metabolism[J].Food Bioscience, 2024, 60:104256.
[39] 邵匡振, 丁向萍, 张子恒, 等.中药益生元的研究进展[J].中国微生态学杂志, 2024, 36(7):838-842.
SHAO K Z, DING X P, ZHANG Z H, et al.Prebiotics in Chinese materia medica:Research progress[J].Chinese Journal of Microecology, 2024, 36(7):838-842.
[40] GE S T, HAN J R, SUN Q Y, et al.Optimization of cryoprotectants for improving the freeze-dried survival rate of potential probiotic Lactococcus lactis ZFM559 and evaluation of its storage stability[J].LWT, 2024, 198:116052.