食品安全是保障国民健康和社会稳定的重要前提,是维系民生福祉和促进经济可持续发展的重要基础。微生物污染是造成食品安全问题的关键因素,防控形势日益严峻。据统计,每年30%左右的食品在生产、运输等环节中损耗或变质,其中由微生物污染导致的经济损失高达食品总价值的10%[1-2]。蜡样芽孢杆菌(Bacillus cereus)是一种广泛存在于自然环境中的好氧或兼性厌氧芽孢杆菌,是引起食源性疾病的第五大原因,每年约有12%的食源性疾病由B.cereus污染引起,鞭毛和多层的芽孢结构使其具有能够运动、耐高温、耐紫外线、耐化学物质、耐干燥等特点[3-4]。B.cereus分泌的肠毒素、溶血素等毒力因子不仅能够污染食品引发食源性疾病,且其独特的芽孢结构对常规热处理及化学消毒剂具有较强的耐受性,这使B.cereus的清除变得极为困难[5-6]。目前常用的物理化学方法虽然能够杀死B.cereus,却面临着营养流失、风味改变、能耗成本高等问题,而防腐剂的使用使耐药性等问题日趋突出。因此,开发有效的控制B.cereus生长与繁殖的策略,以及预防其引发的食品安全问题是当前亟须解决的任务。
Temporins是从蛙类皮肤中分离出来的一类抗菌肽,也是从动物中分离出来的最短抗菌肽之一,具有抗菌、抗癌、抗真菌等生物活性[7]。AMPs作为先天免疫系统的关键效应分子,因其独特的抗菌机制和广谱抗菌活性而备受关注[8]。AMPs通过破坏细菌细胞膜完整性(如形成孔道或膜溶解)、干扰胞内靶标(如核酸与蛋白质合成)等多重作用模式,显著降低了细菌耐药性产生的风险[9-10]。AMPs的生物活性除抗菌作用外还被发现具有抗炎、抗癌、抗病毒、参与机体免疫调节、促进伤口愈合等生物特性[11-12]。天然AMPs存在着稳定性差的问题,这将会限制其在食品中的应用。Temporin L(FVQWFSKFLGRIL-NH2)是Temporins的一种,是含有13个氨基酸的C端酰胺化线性短肽,分子质量为1 640 Da,具有较好的溶解性,1996年Temporin L从欧洲林蛙(Rana temporaria)皮肤中分离得到,带有的正电荷更有利于其与细胞膜发生相互作用[13]。
AMPs的活性受结构特征、净电荷及疏水性等参数调控,而生物信息学是一种利用机器学习、能够高效分析AMPs关键理化参数与抗菌活性构效关系的重要工具[14]。因此,本研究利用生物信息学在线网站对Temporin L的理化性质、二级结构、跨膜区、毒性、两亲性等特性进行预测分析。同时还探究了Temporin L对B.cereus的抑菌活性,测定在不同紫外线照射时间、pH、温度、金属离子条件下的稳定性,从扫描电子显微镜和分子对接进一步揭示Temporin L对B.cereus的作用机制,以期能够为Temporin L的深入研究和抑菌机理提供新思路。
1 材料与方法
1.1 材料与试剂
1.1.1 菌种
蜡样芽孢杆菌YYZ-03由香肠中分离得到,并在苏州鸿讯生物科技有限公司进行16S rRNA鉴定,保存于河南农业大学。
Temporin L由吉尔生化有限公司合成;LB肉汤培养基、固体培养基,北京奥博星生物技术有限公司;卡那霉素溶液,大连美仑生物技术有限公司;CaCl2、NaCl、MgCl2、NaOH,国药集团化学试剂有限公司;KCl,天津市致远化学试剂有限公司;PBS,武汉普诺赛生命科技有限公司。
1.2 仪器与设备
SX-500高压灭菌锅,上海新朴仪器设备有限公司;CJ-2DF超净工作台,天津市泰斯特仪器有限公司;Synergy H1多功能酶标仪,美国伯腾仪器有限公司;S-3400扫描电子显微镜,日立科学仪器有限公司。
1.3 实验方法
1.3.1 Temporin L的生物信息学分析
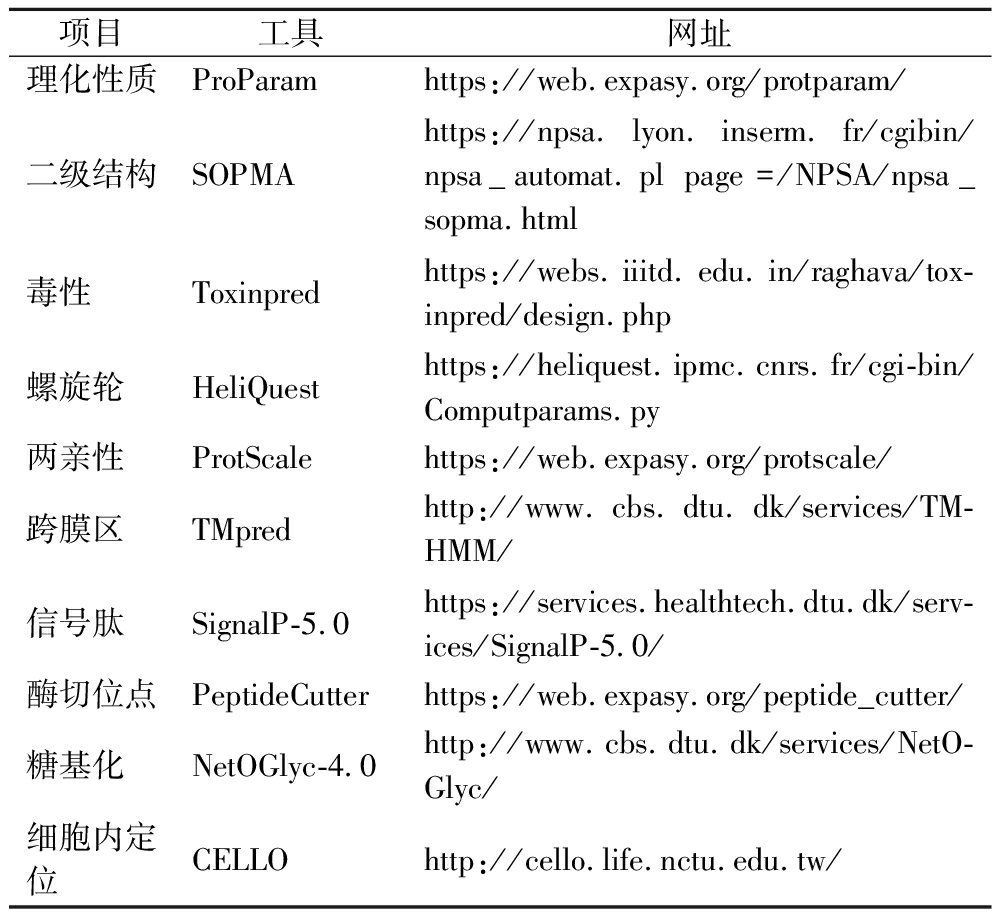
使用网络生物信息学软件对Temporin L的理化性质、两亲性、结构、酶切位点等进行预测,所需分析工具如表1所示。
表1 Temporin L生物信息学分析工具
Table 1 Bioinformatics analysis tools for Temporin L
项目工具网址理化性质ProParamhttps://web.expasy.org/protparam/二级结构SOPMAhttps://npsa.lyon.inserm.fr/cgibin/npsa_automat.pl page=/NPSA/npsa_sopma.html毒性Toxinpredhttps://webs.iiitd.edu.in/raghava/tox-inpred/design.php螺旋轮HeliQuesthttps://heliquest.ipmc.cnrs.fr/cgi-bin/Computparams.py两亲性ProtScalehttps://web.expasy.org/protscale/跨膜区TMpredhttp://www.cbs.dtu.dk/services/TM-HMM/信号肽SignalP-5.0https://services.healthtech.dtu.dk/serv-ices/SignalP-5.0/酶切位点PeptideCutterhttps://web.expasy.org/peptide_cutter/糖基化NetOGlyc-4.0http://www.cbs.dtu.dk/services/NetO-Glyc/细胞内定位CELLOhttp://cello.life.nctu.edu.tw/
1.3.2 Temporin L对蜡样芽孢杆菌的抑菌活性
根据肉汤微量法测定Temporin L对B.cereus的最小抑菌浓度(minimum inhibitory concentration,MIC)和最小杀菌浓度(minimum bactericidal concentration,MBC)。在96孔板每孔中加入100 μL LB肉汤,并用LB肉汤将Temporin L进行溶解,然后在96孔板中连续二倍稀释,最后每孔剩余含有Temporin L的100 μL溶液,肽浓度为0.5~128 μmol/L。将处于对数生长期的B.cereus用LB肉汤稀释至菌液浓度为1×106 CFU/mL,之后在96孔板每孔中加入100 μL菌液与肽溶液混合,置于37 ℃培养18 h。含有卡那霉素的为阳性对照。培养后96孔板中溶液为清澈的最低肽浓度为MIC。此外,取100 μL处理后的菌液进行涂布,过夜培养后没有菌落生长的最低浓度为MBC。
1.3.3 Temporin L的稳定性[15-16]
对紫外线的稳定性:将Temporin L溶液分别在紫外线下照射0、15、30、45、60 min之后按1.3.2节的实验方法进行测定,在37 ℃下孵育18 h后测定OD600nm,并读取MIC。未经过任何处理的肽为对照组,抑菌率为MIC浓度(未处理前)下处理组与对照组抑制百分比的比值。
对温度的稳定性:将Temporin L溶液分别在-20、4、20、40、60、80、100、121 ℃下维持30 min,以及在100 ℃分别加热0、15、30、45、60 min,当多肽温度恢复至室温后进行使用。之后按对紫外线稳定性的实验方法测定MIC和抑菌率。
对金属离子的稳定性:将Temporin L用不同金属离子溶液(CaCl2 20 mmol/L、FeCl3 4 mmol/L、MgCl2 1 mmol/L、KCl 4.5 mmol/L)及NaCl溶液(50、100、150、200 mmol/L)进行溶解,使用PBS进行溶解的Temporin L溶液为对照组。之后按对紫外线稳定性的实验方法测定MIC和抑菌率。
对pH的稳定性:使用1 mol/L盐酸和1 mol/L NaOH将Temporin L溶液分别调至pH值为2、4、6、8、10、12,使用PBS进行溶解的Temporin L溶液为对照组。之后按对紫外线稳定性的实验方法测定MIC和抑菌率。
1.3.4 微观结构观察
使用扫描电子显微镜对B.cereus的形态变化进行观察。使用Temporin L(0 MIC、0.5 MIC、MIC、2 MIC)处理重悬于PBS的B.cereus(1×108 CFU/mL),37 ℃下处理1 h。处理后的菌液低速离心,并用无菌PBS进行多次洗涤,除去多余杂质,在经过最后一次离心后去除上清液,加入预冷过的体积分数2.5%的戊二醛,并在4 ℃下固定2 h。将固定后的菌悬液离心(6 000 r/min、10 min、4 ℃)洗涤并重新溶解于无菌PBS中。之后依次加入体积分数为30%、50%、70%、80%、90%、100%乙醇,分别进行脱水干燥5 min,在100%乙醇时脱水2次。最后将样品进行冷冻干燥,在扫描电镜下进行观察。
1.3.5 分子对接
采用分子对接方法探究Temporin L对B.cereus靶点的作用机制。首先通过PDB数据库获取3U3W(DNA)和1AH7(磷脂酶C)的晶体结构[17],同时利用Chem 3D分子模拟软件构建Temporin L配体的三维结构并在MMFF94力场下进行几何优化。之后使用PyMol可视化系统对受体蛋白移除结晶水分子、补充氢原子以完善质子化状态;对配体分子进行加氢处理。采用AutoDock Tools将处理后的受体和配体分别转换为PDBQT格式文件,设置对接格点参数以覆盖酶的活性口袋区域。最后将分子对接过程在AutoDock Vina中进行,对接完成后运用PyMol进行可视化展示,并分析配体与靶点之间的氢键和疏水相互作用。
1.4 数据处理
独立进行的3次重复实验结果以“平均值±标准差”表示。使用SPSS 24.0软件对数据进行ANOVA方差分析,使用Origin 2021进行绘图。
2 结果与分析
2.1 Temporin L的生物信息学分析结果
使用ProParam在线网站对Temporin L的理化性质进行预测。Temporin L的氨基酸个数为13,分子质量为1 640.99 u,理论净电荷为11,呈碱性,含有2个正电荷(精氨酸+亮氨酸),不含有负电荷(天冬氨酸+谷氨酸)。Temporin L在哺乳动物细胞中的半衰期约为1.1 h,在酵母菌中为3 min,在大肠杆菌中为2 min,不稳定指数为24.05(<40),为稳定多肽,脂溶性指数为112.31,热稳定性较好,亲水性平均系数为0.823,为正数,总体呈疏水性。因此,Temporin L是一种小分子、带正电荷、稳定的疏水性多肽。
使用ProtScale对Temporin L的两亲性进行分析,由图1可知,Temporin L具有明显的两亲结构。除第4位和第8位氨基酸呈现亲水性外,其余氨基酸疏水性得分均大于0,呈现疏水性,总体为疏水性,这与理化性质预测结果相一致。其中最高疏水性得分为1.44,最低疏水性得分为-1.26。
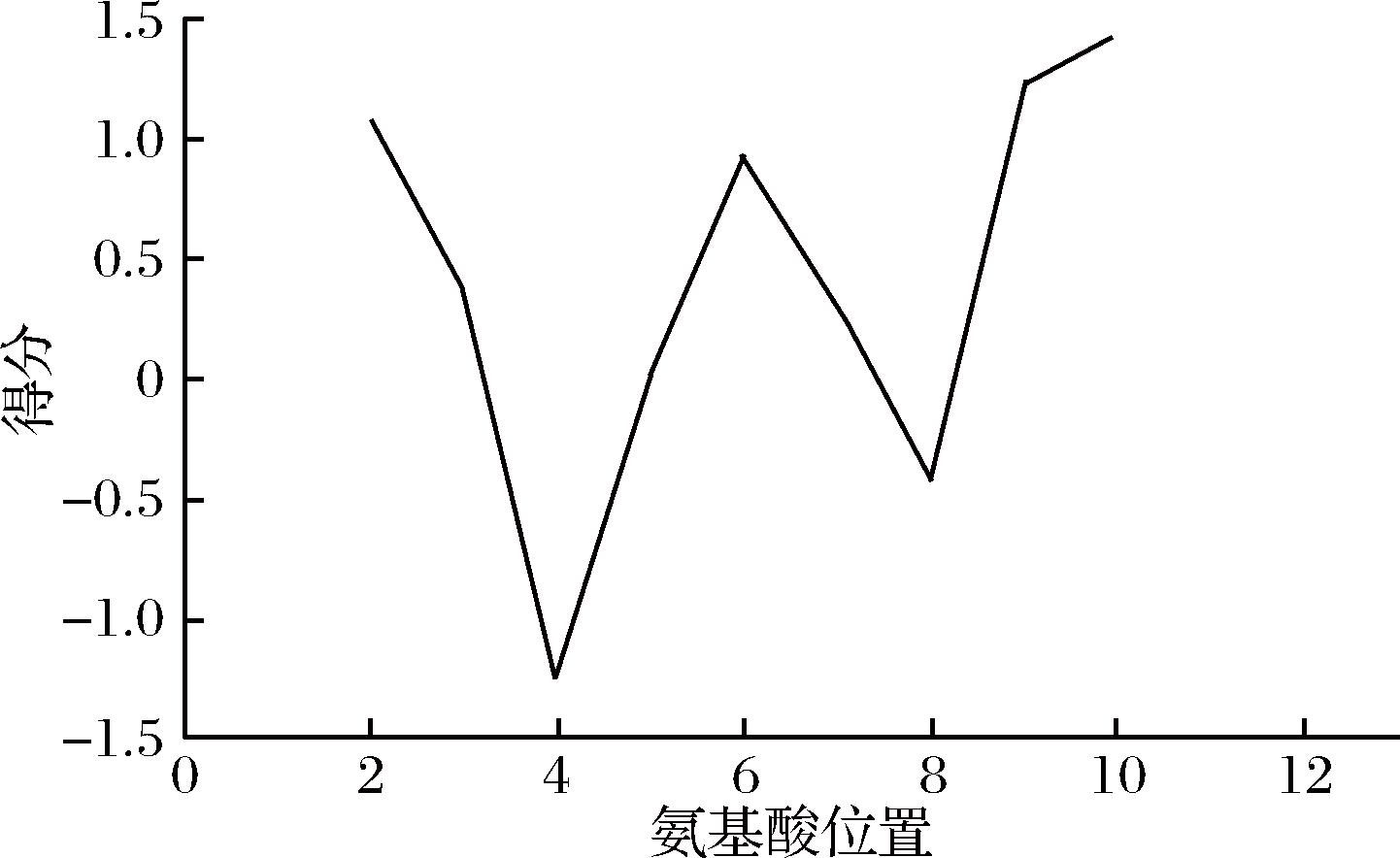
图1 Temporin L的两亲性预测
Fig.1 Amphiphilic prediction of Temporin L
注:纵坐标正值表示疏水性,负值表示亲水性。
图2-a螺旋轮投影中蓝色代表亲水性氨基酸,黄色代表疏水性氨基酸。通过螺旋轮投影可知Temporin L具有疏水和亲水2种氨基酸,具有较好的两亲性。同时Temporin L具有较多的疏水氨基酸,并且主要聚集在一边,因此整体更加倾向于疏水性,这与理化性质预测结果相一致。此外,由图2-b可知,Temporin L的二级结构包括2种,第5~12位氨基酸为延伸链,占总体的61.54%,其余38.46%为无规则卷曲。通过Toxinpred预测发现Temporin L不含毒性。综上,Temporin L是一种具有两亲性的无毒线性肽。
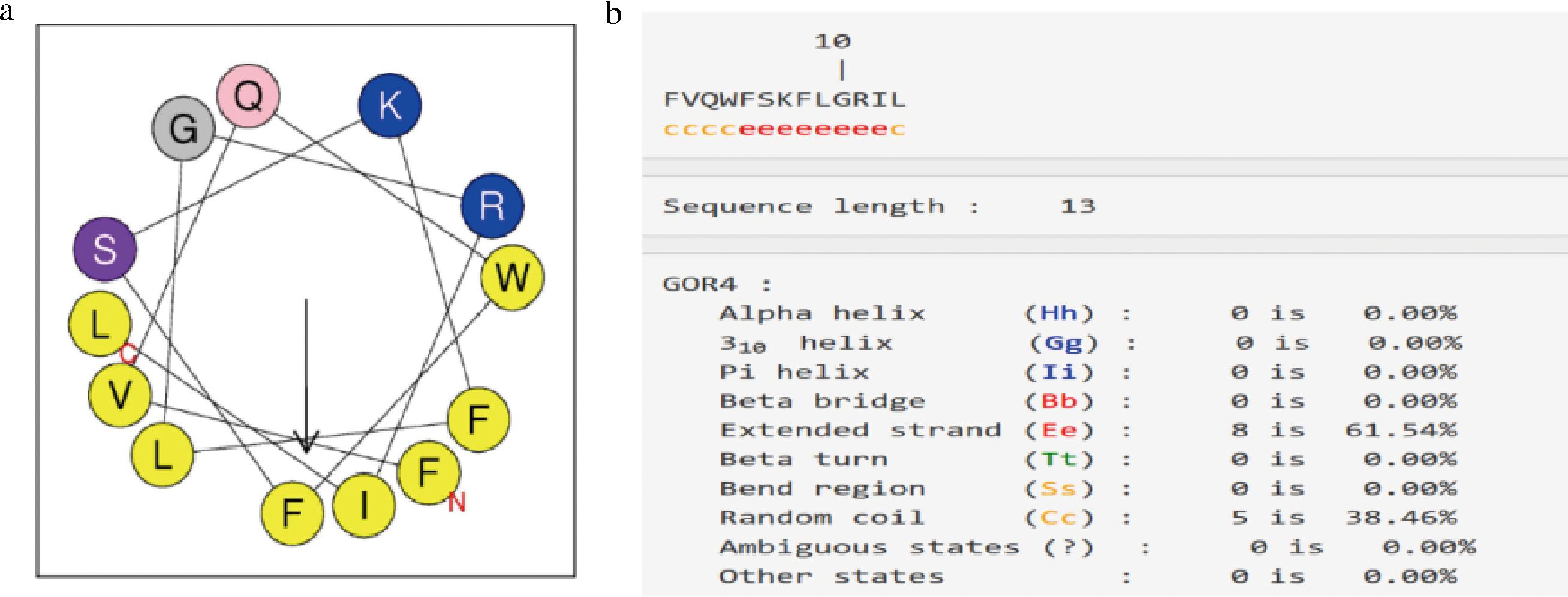
a-螺旋轮投影;b-二级结构预测
图2 Temporin L的螺旋轮投影和二级结构预测
Fig.2 Helical wheel projection and secondary structure prediction of Temporin L
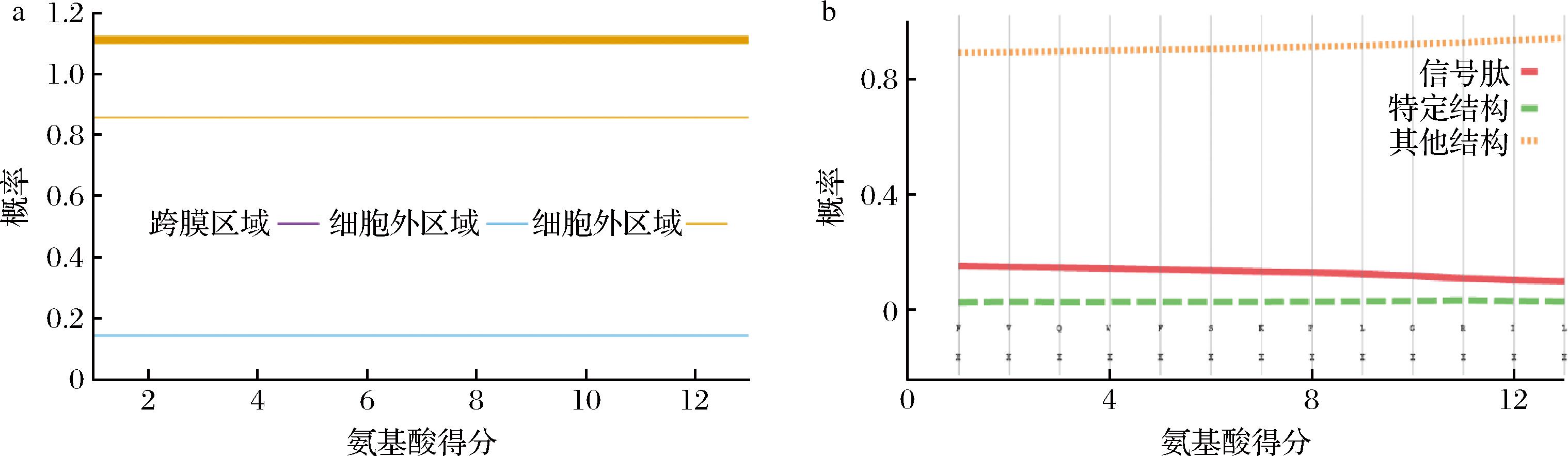
a-跨膜区预测;b-信号肽预测
图3 Temporin L的跨膜区和信号肽预测
Fig.3 Transmembrane domains and signal peptide prediction of Temporin L
跨膜区是膜蛋白中能够嵌入脂双层的疏水片段,多以α螺旋结构存在,长度一般为20~25个氨基酸,主要参与物质运输和细胞信号传递等生物学过程[18]。对Temporin L的跨膜区和信号肽预测分析可知Temporin L不存在跨膜区和信号肽(图3),推测该肽为膜外蛋白和非分泌蛋白,可能通过与细胞膜的相互作用来发挥抑菌机制。
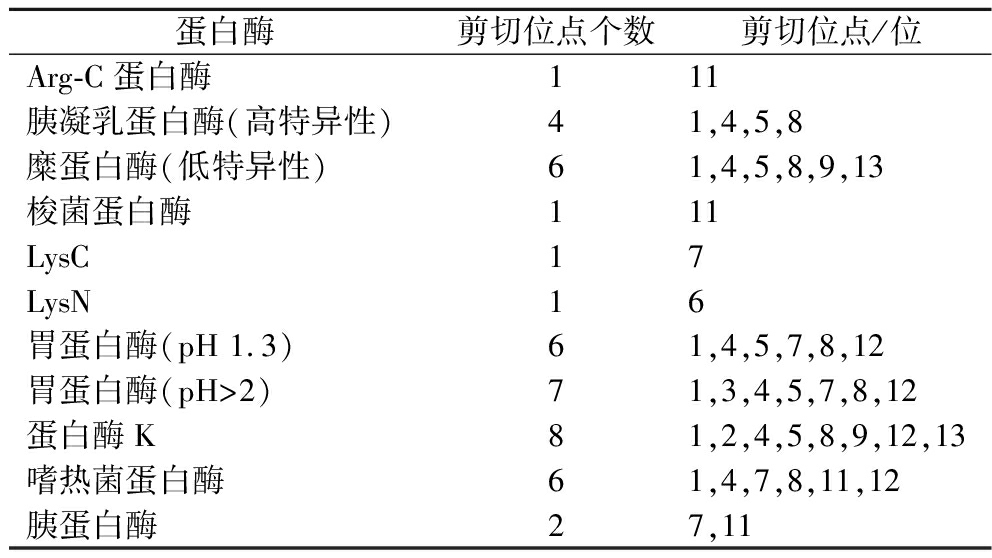
由表2可知,Arg-C蛋白酶、胰凝乳蛋白酶(高特异性)、蛋白酶K等11种蛋白酶均可对Temporin L进行剪切。除第10位氨基酸残基不是酶切位点外,其余氨基酸残基均是酶切位点。其中糜蛋白酶(低特异性)、胃蛋白酶(pH 1.3)、胃蛋白酶(pH>2)、蛋白酶K、嗜热菌蛋白酶可对6个及以上氨基酸残基位点进行酶切。同时,经过预测发现Temporin L不存在糖基化点,在细胞质中的得分最高为2.430(表3)。
表2 Temporin L的酶切位点
Table 2 Enzyme digestion site analysis of Temporin L
蛋白酶剪切位点个数剪切位点/位Arg-C蛋白酶111胰凝乳蛋白酶(高特异性)41,4,5,8糜蛋白酶(低特异性)61,4,5,8,9,13梭菌蛋白酶111LysC17LysN16胃蛋白酶(pH 1.3)61,4,5,7,8,12胃蛋白酶(pH>2)71,3,4,5,7,8,12蛋白酶K81,2,4,5,8,9,12,13嗜热菌蛋白酶61,4,7,8,11,12胰蛋白酶27,11
表3 Temporin L的细胞内定位结果
Table 3 Results of intracellular localization of Temporin L

定位位置可信度指数细胞质2.430周质1.067细胞外0.807
续表3

定位位置可信度指数细胞内膜0.482细胞外膜0.214
2.2 Temporin L对蜡样芽孢杆菌的抑菌活性
AMPs的抑菌效果可以通过MIC进行评价,MIC越小,抑菌作用越好。由图4可知,当Temporin L终浓度为8 μmol/L时孔洞中的菌溶液在18 h后仍为清澈透明,表明Temporin L对B.cereus具有抑制作用,并且MIC为8 μmol/L。之后将所有溶液进行平板计数,发现Temporin L浓度为16 μmol/L时平板上无任何菌落。因此,Temporin L对B.cereus具有抑制作用,MIC和MBC分别为8 μmol/L和16 μmol/L。

图4 Temporin L对蜡样芽孢杆菌的MIC
Fig.4 MIC of Temporin L against B.cereus
2.3 Temporin L的稳定性分析
如图5所示,Temporin L的抑菌活性在pH为4~10时与对照组相比没有显著变化(P>0.05)。但当pH值为2和12时抑菌活性有所下降,这可能是由于pH使多肽的净电荷发生略微改变,进而降低了抑菌效果。虽然Temporin L在强酸、强碱下有所下降,但抑菌效果仍能保持90%以上,说明Temporin L的抑菌活性不易受pH的影响。
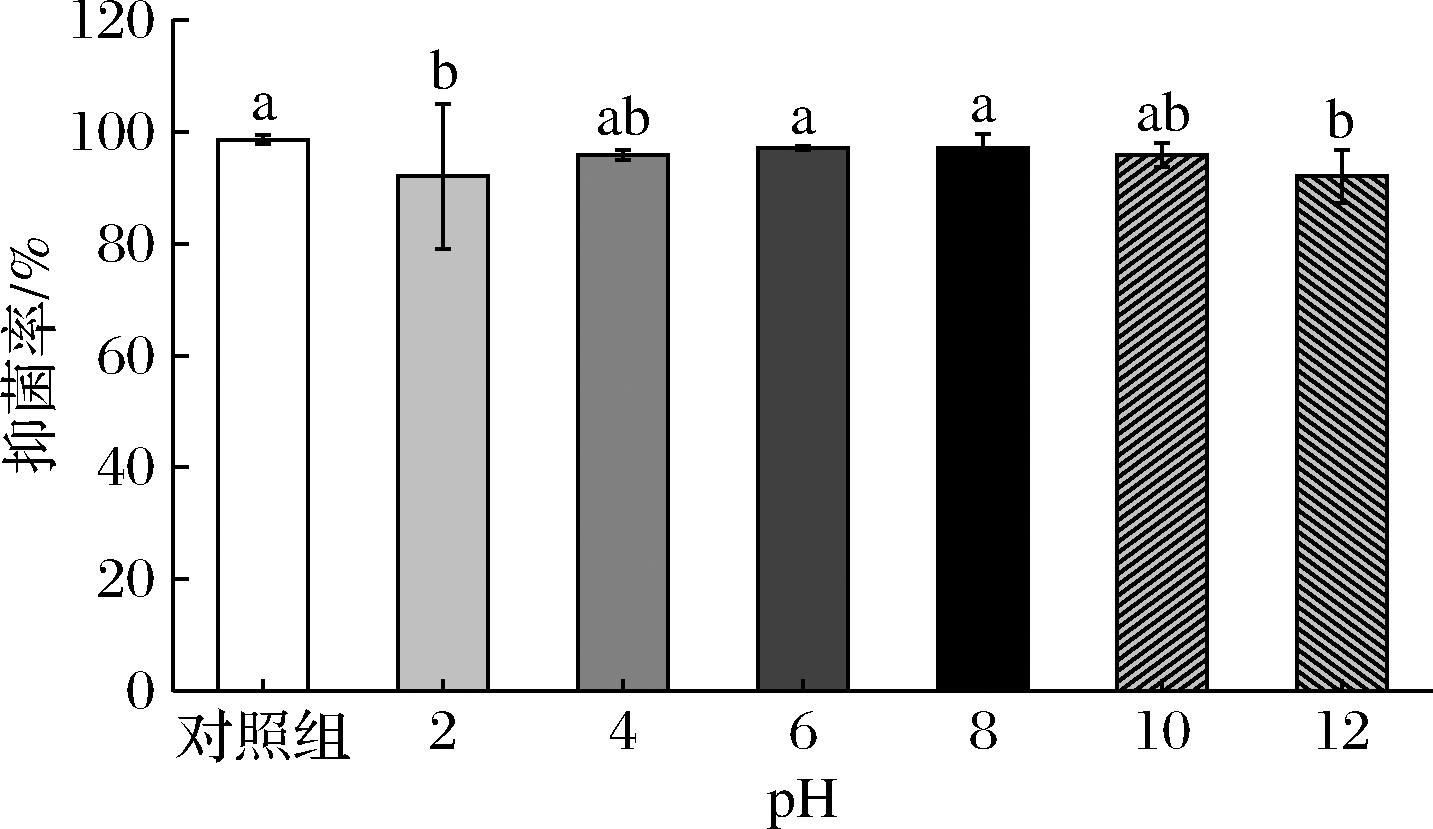
图5 Temporin L对pH的稳定性
Fig.5 Stability of Temporin L under different pH
注:不同小写字母表示差异显著(P<0.05)(下同)。
如图6-a所示,紫外线并未影响Temporin L对B.cereus的抑菌活性,即使在紫外线下照射60 min后,Temporin L的抑菌效果也未发生显著下降。如图6-b和图6-c所示。经过40、60、80、100 ℃加热30 min后,Temporin L的抑菌率与室温20 ℃的抑菌率相比几乎没有发生改变,并且低温保存更有利于Temporin L抑菌效果的发挥。经过121 ℃加热30 min 后Temporin L的抑菌效果有所降低(P<0.05),但仍能保持90%以上。延长Temporin L在100 ℃下的加热时间,结果显示,加热60 min抑菌效果仍未发生明显改变。因此,Temporin L具有较好的热稳定性,即使在100 ℃长时间加热也无明显影响。
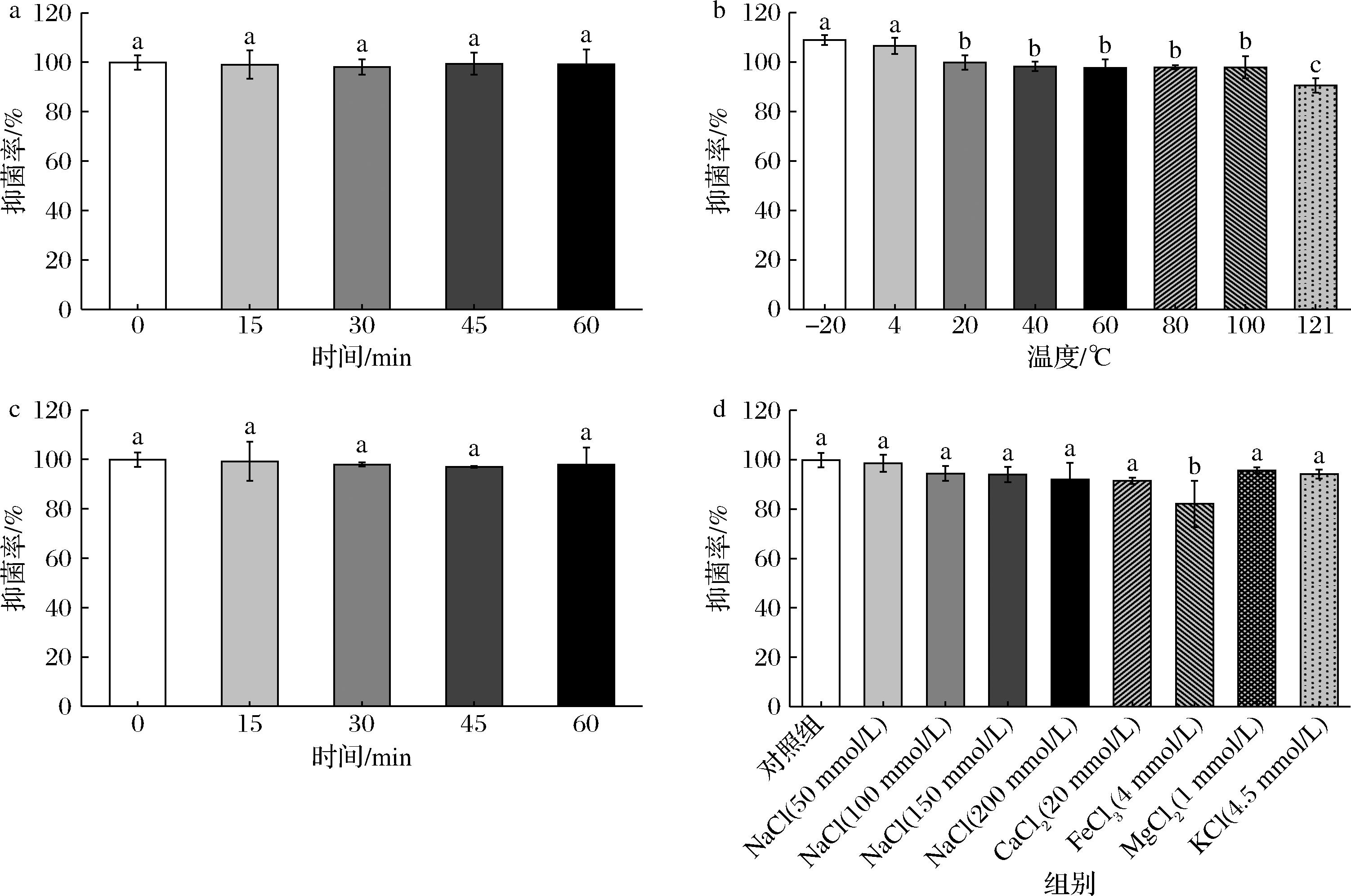
a-对紫外线的稳定性;b-对温度的稳定性;c-对100 ℃加热不同时间的稳定性;d-对金属离子的稳定性
图6 37 ℃下孵育18 h后Temporin L的抑菌率
Fig.6 Antibacterial rate of Temporin L after 18 h incubation at 37 ℃
由图6-d可知,在Fe3+存在时与对照组相比Temporin L对B.cereus的抑制作用显著下降(P<0.05)。然而在其他不同金属离子(Ca2+、Fe3+、Mg2+、K+、Na+)存在下,Temporin L对B.cereus的抑制作用基本没有发生改变。当Mg2+、K+、Na+(50、100、150 mmol/L)及高浓度的NaCl(200 mmol/L)存在时,Temporin L对B.cereus的抑菌活性保持94%以上。这些结果说明大多数的金属离子并不能使Temporin L对B.cereus的抑菌能力发生显著变化。
此外,通过肉汤微量法发现在不同条件处理后Temporin L对B.cereus的MIC未发生改变,即使在有Fe3+存在时仍保持为8 μmol/L。这些表明Temporin L拥有较好的稳定性,抑菌效果不随外部条件的改变而明显改变。
2.4 Temporin L对蜡样芽孢杆菌形态结构的影响
如图7所示,对照组B.cereus具有完整的细胞形态,表面清晰光滑,呈杆状,是正常菌体的生长状态。但是当被不同浓度的Temporin L处理1 h后B.cereus的形态发生不同变化,并且产生聚集现象。Temporin L在0.5 MIC时,B.cereus出现明显的皱缩,并且菌体聚集在一起。而暴露于MIC和2 MIC 后细菌形态严重变化,尤其在2 MIC下细胞全部严重萎缩,部分细菌表面出现孔洞,细胞壁变得模糊,胞内物质泄漏。此外,与Temporin L作用机制不同,部分AMPs虽然能使菌体凹陷,但表面仍可保持光滑[19]。
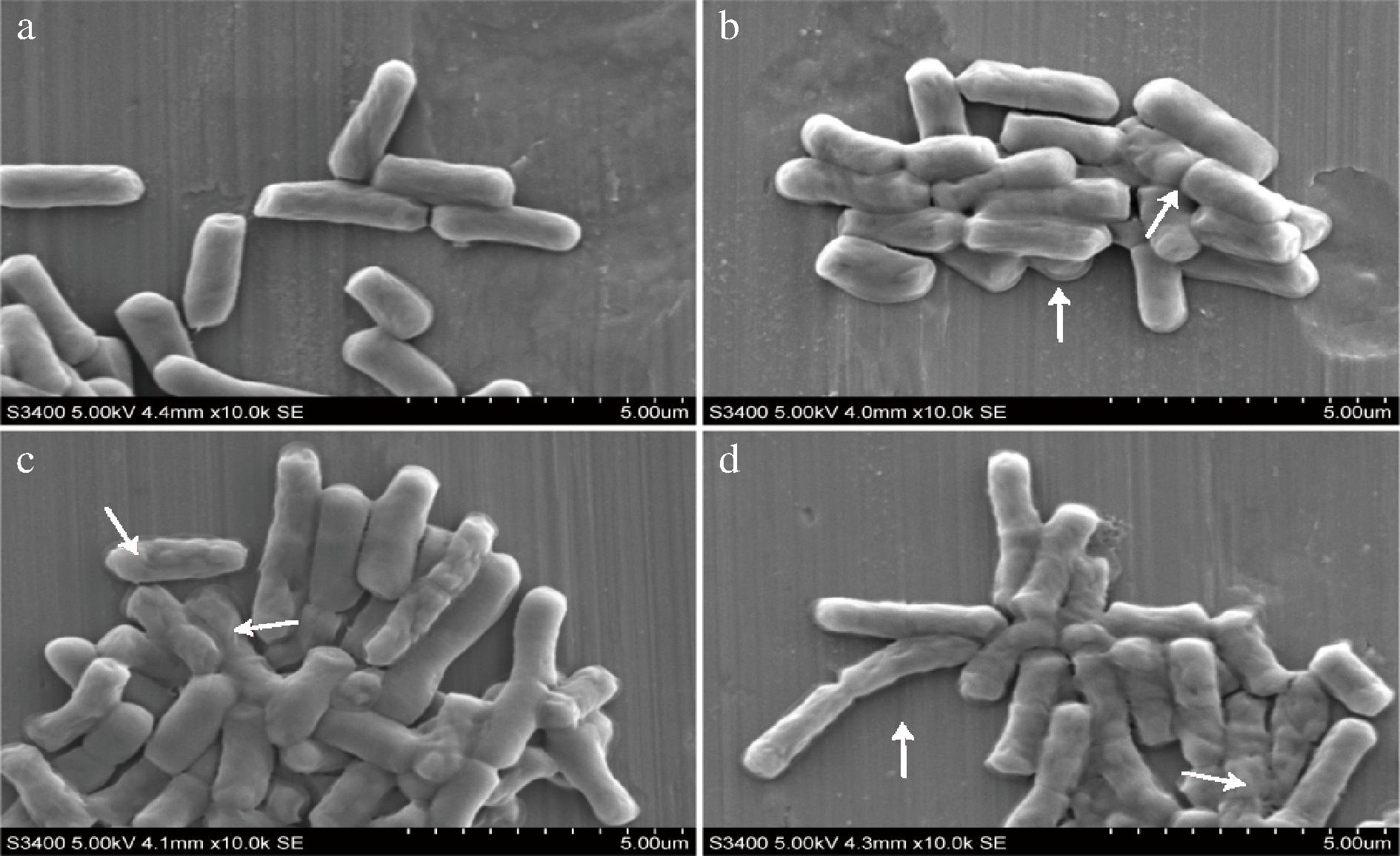
a-对照组;b-0.5 MIC;c-MIC;d-2 MIC
图7 Temporin L对蜡样芽孢杆菌形态的影响
Fig.7 Effects of Temporin L on morphology of B.cereus
2.5 分子对接
DNA和磷脂酶C是B.cereus 的重要靶点,对菌体的生存和繁殖至关重要[20]。如图8所示,Temporin L与DNA和磷脂酶C均可产生氢键,与磷脂酶C产生的氢键较多。此外,Temporin L与磷脂酶C多处还形成疏水作用,这使Temporin L与靶点具有较好的结合力。结合能的大小在分子识别和药物设计中具有重要指导价值。当相互作用的结合能呈现负值时,表明配体与生物大分子之间存在结合的倾向。同时数值越小两者形成稳定复合物的概率越高,分子间作用力越强,复合物结构越稳固[21]。经过分子对接,Temporin L与DNA和磷脂酶C的结合能分别为-5.6、-6.1 kcal/mol,均为负值,表明与靶点具有结合的可能,并且与磷脂酶C的结合可能性较大。
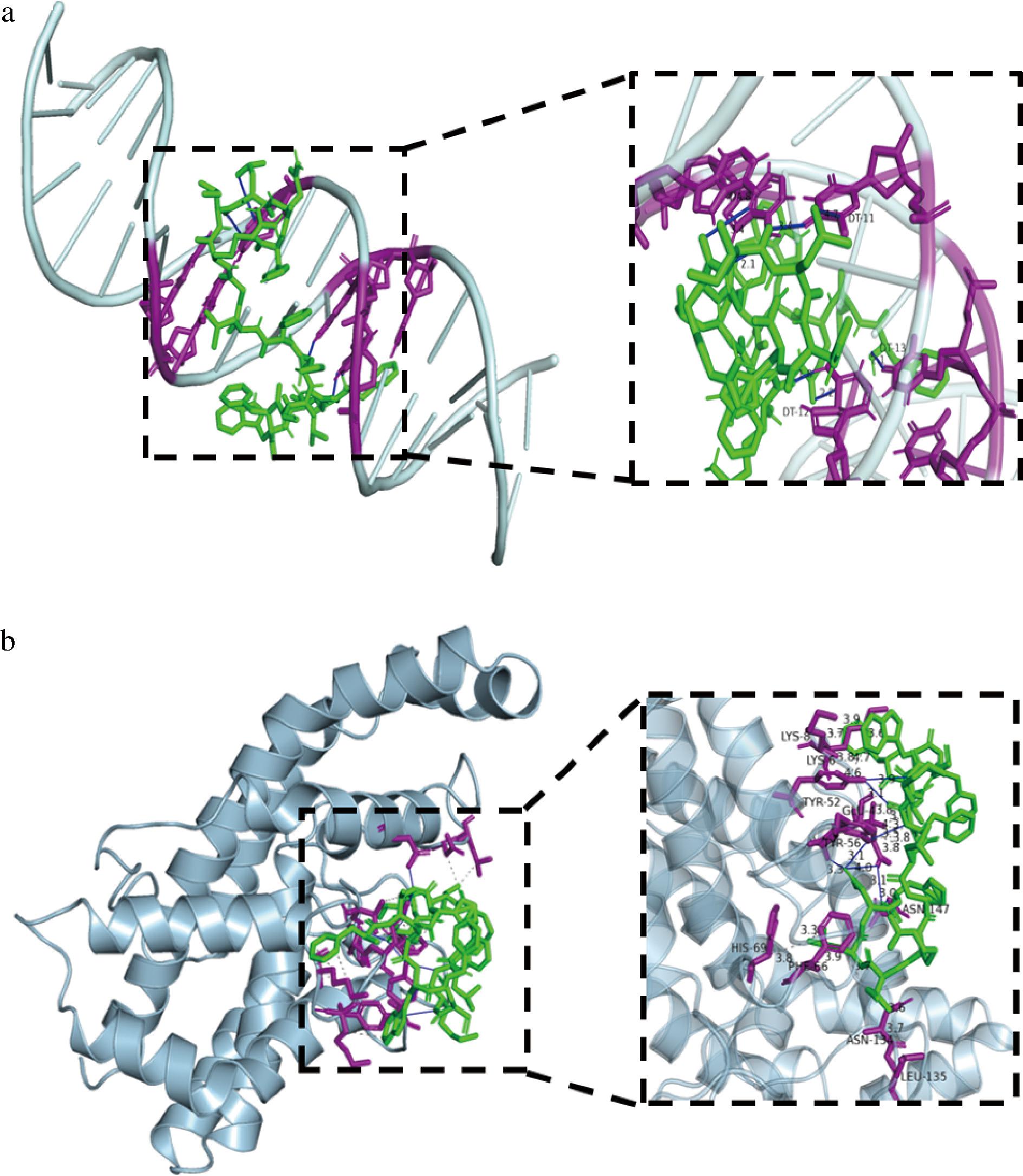
a-DNA;b-磷脂酶C
图8 Temporin L与DNA和磷脂酶C的分子对接模型
Fig.8 Molecular docking model of Temporin L with DNA and phospholipase C
注:图中绿色为Temporin L;紫色为靶点;蓝色实线表示氢键;灰色虚线表示疏水作用。
3 结论与讨论
食物腐烂是目前食品行业难以解决的重大问题,不仅会造成巨大的经济损失,还严重威胁食品供应链的稳定性与安全性。传统化学防腐剂虽能在一定程度上延缓食品变质、延长货架期,但不当使用或过量残留会引发胃黏膜损伤、机体免疫力下降等健康隐患,其应用局限性日益凸显。AMPs凭借高效的抑菌活性、优异的抗氧化能力以及天然来源赋予的低毒性优势,成为替代传统防腐剂的理想候选物;而阳离子氨基酸残基数量与疏水性更是决定其抑菌效能的核心基础。大量研究证实,AMPs在果蔬、肉制品、乳制品等多类食品的保鲜领域表现出显著成效,为解决食品腐烂问题、降低经济损耗提供了全新的技术路径。
AMPs的抑菌活性与净电荷数、疏水性、二级结构等理化性质和结构特性相关。带有阳离子的AMPs通过电荷的吸引与带有负电荷的细胞膜相互作用,而疏水性又为嵌入膜结构和破坏膜完整性提供了前提,α螺旋的结构更加快了对细菌的损伤作用。经预测发现Temporin L带有正电荷,总体呈现疏水性,具有较好的结构稳定性和热稳定性。此外,Temporin L含有疏水和亲水2种氨基酸,形成了典型的两亲结构,该特性更有利于使其溶于溶剂及与细菌相互作用。与许多发挥抗菌作用的AMPs二级结构不同,Temporin L的二级结构主要为延伸链,其余为无规则卷曲,该特殊结构避免了α螺旋结构AMPs因刚性过强导致的真核细胞非特异性损伤。虽然Temporin L不含跨膜区、信号肽、糖基化点,但可对多种蛋白酶进行剪切,这表明其在体内可能具备可控的代谢降解特性,降低了残留风险。Temporin L的理化特性与结构特性的相互协同,共同构成了 Temporin L 发挥抑菌活性的物质基础,通过肉汤微量法发现Temporin L能够较好地抑制B. cereus,并且MBC远低于Nisin(149 μmol/L)和BCP4(79.5 μmol/L),具有更好的抑菌作用,为其后续应用于食品防腐领域提供了关键的理论支撑[22]。
食品加工与贮存的复杂环境使AMPs的不稳定性成为制约产业化应用的核心瓶颈。高温的生产工艺容易破坏肽链维持构象的氢键、疏水作用等非共价键,导致活性中心构象改变;食品基质的pH波动会改变其带电性质与空间结构,在极端条件下甚至引发肽键水解;同时,食品中的蛋白质、脂肪、多糖等成分还可能与AMPs发生非特异性结合,包裹其活性位点,阻碍其与细菌的相互作用。而AMPs的抑菌机制以膜破坏作用为主,其作为阳离子肽,可通过电荷吸引快速结合带负电荷的细菌细胞膜,随后疏水区嵌入膜的疏水核心并伴随构象重排,最终通过形成跨膜孔道或诱导膜脂质紊乱,导致细菌内容物外泄而死亡;部分AMPs还可穿透细胞膜,靶向作用于细菌的核酸、核糖体等胞内靶点,干扰DNA复制、蛋白质合成等关键代谢过程,进一步发挥抑菌或杀菌效应。通过测定发现Temporin L在不同温度、pH、金属离子、紫外线下具有较好的稳定性,抑菌效果并未发生显著改变。已有研究表明,结构较为简单的AMPs抑菌活性主要由氨基酸序列决定,而温度和紫外线的变化并不会改变其一级结构,因此可维持稳定的抑菌效果[23]。然而,部分研究表明金属离子可通过自身所带的阳离子与细胞膜所带的负电荷结合,从而干扰多肽的抑菌效果。本研究中当Fe3+存在时抑菌活性显著下降,可能是Fe3+与细胞膜相互作用,从而降低了抑菌活性。此外,通过扫描电镜发现B. cereus经Temporin L处理后出现褶皱、凹陷、细胞壁模糊等现象,部分菌体还发生破裂、细胞质流出的情况,这是AMPs典型的膜结构破坏作用。而分子对接结果进一步表明Temporin L可通过靶向B. cereus的DNA和磷脂酶C形成氢键和疏水作用来抑制菌体的生长繁殖。
综上,本研究通过对Temporin L的深入研究发现其具有良好的生物特性,并且对B.cereus具有抑菌活性,能够通过破坏细菌形态和作用于多个靶点来发挥抑菌作用,为后续AMPs的设计和研发提供了信息学参考。
[1] ZHU Y L, WANG W, LI M, et al.Microbial diversity of meat products under spoilage and its controlling approaches[J].Frontiers in Nutrition, 2022, 9:1078201.
[2] 黄金凤. 油樟同分异构松油醇抑菌活性及高产途径研究[D].成都:西华大学, 2020.
HUANG J F.Antibacterial activity and high yield method of isomeric terpineol from Cinnamomum longepaniculatum[D].Chengdu:Xihua University, 2020.
[3] NING Y W, MA M G, ZHANG Y J, et al.Antibacterial mechanism of sucrose laurate against Bacillus cereus by attacking multiple targets and its application in milk beverage[J].Food Research International, 2022, 154:111018.
[4] LEONG S S, KOREL F, KING J H.Bacillus cereus:A review of “fried rice syndrome” causative agents[J].Microbial Pathogenesis, 2023, 185:106418.
[5] JOVANOVIC J, ORNELIS V F M, MADDER A, et al.Bacillus cereus food intoxication and toxicoinfection[J].Comprehensive Reviews in Food Science and Food Safety, 2021, 20(4):3719-3761.
[6] 白凤岚, 陈松, 罗梦幽, 等.食品中蜡样芽孢杆菌的分离及携带毒力基因的检测[J].现代食品科技, 2018, 34(10):247-252;204.
BAI F L, CHEN S, LUO M Y, et al.Identification and virulence genes detection of Bacillus cereus food isolates[J].Modern Food Science and Technology, 2018, 34(10):247-252;204.
[7] ROMERO S M, CARDILLO A B, MART NEZ CERON M C, et al.Temporins:An approach of potential pharmaceutic candidates[J].Surgical Infections, 2020, 21(4):309-322.
NEZ CERON M C, et al.Temporins:An approach of potential pharmaceutic candidates[J].Surgical Infections, 2020, 21(4):309-322.
[8] 苏琰, 李融.抗菌肽的食品保鲜应用及生物合成研究进展[J].食品与机械, 2024, 40(7):208-215.
SU Y, LI R.Advance on biosynthesis of antibacterial peptides and its application in food preservation[J].Food &Machinery, 2024, 40(7):208-215.
[9] LI X, ZUO S Y, WANG B, et al.Antimicrobial mechanisms and clinical application prospects of antimicrobial peptides[J].Molecules, 2022, 27(9):2675.
[10] MIAO H B, WANG L, WU Q, et al.Antimicrobial peptides:Mechanism, expressions, and optimization strategies[J].Probiotics and Antimicrobial Proteins, 2025, 17(2):857-872.
[11] PFALZGRAFF A, BRANDENBURG K, WEINDL G.Antimicrobial peptides and their therapeutic potential for bacterial skin infections and wounds[J].Frontiers in Pharmacology, 2018, 9:281.
[12] DA SILVA A M B, SILVA-GONÇALVES L C, OLIVEIRA F A, et al.Pro-necrotic activity of cationic mastoparan peptides in human glioblastoma multiforme cells via membranolytic action[J].Molecular Neurobiology, 2018, 55(7):5490-5504.
[13] BELLAVITA R, FALANGA A, MERLINO F, et al.Unveiling the mechanism of action of acylated temporin L analogues against multidrug-resistant Candida albicans[J].Journal of Enzyme Inhibition and Medicinal Chemistry, 2023, 38(1):36-50.
[14] 林志昊, 孔毅, 高美风.抗菌肽发现方法研究进展[J].药物生物技术, 2024, 31(5):573-577.
LIN Z H, KONG Y, GAO M F.Research progress of antimicrobial peptide discovery methods[J].Pharmaceutical Biotechnology, 2024, 31(5):573-577.
[15] ZHANG Y M, YANG L Y, YING J P, et al.A novel bacteriocin RSQ01 with antibacterial activity and its application and metabolomic mechanism in milk preservation[J].Food Control, 2023, 151:109823.
[16] OMIDBAKHSH AMIRI E, FARMANI J, RAFTANI AMIRI Z, et al.Antimicrobial activity, environmental sensitivity, mechanism of action, and food application of αs165-181 peptide[J].International Journal of Food Microbiology, 2021, 358:109403.
[17] 陶玮红, 林蓉, 梁铎, 等.源自发酵凡纳滨对虾的抗菌肽BCE3对蜡样芽孢杆菌的抑菌机制及其在米饭中的应用[J].微生物学报, 2024, 64(8):2768-2783.
TAO W H, LIN R, LIANG D, et al.The antimicrobial peptide BCE3 isolated from fermented Penaeus vannamei:Inhibition mechanism on Bacillus cereus and application in rice[J].Acta Microbiologica Sinica, 2024, 64(8):2768-2783.
[18] 杨红艳, 卢奎, 杜蘅, 等.天蚕素抗菌肽的生物信息学分析[J].河南工业大学学报(自然科学版), 2021, 42(4):58-67.
YANG H Y, LU K, DU H, et al.Bioinformatics analysis of cecropin antimicrobial peptides[J].Journal of Henan University of Technology (Natural Science Edition), 2021, 42(4):58-67.
[19] LI Y M, WANG M, LI Y Q, et al.Two novel antimicrobial peptides against vegetative cells, spores and biofilm of Bacillus cereus[J].Food Control, 2023, 149:109688.
[20] 李建明, 梁仁久, 肖健.磷脂酶C在HIV-1感染中作用的研究进展[J].中国艾滋病性病, 2021, 27(10):1166-1169.
LI J M, LIANG R J, XIAO J.Research progress of phospholipase C in HIV-1 infection[J].Chinese Journal of AIDS &STD, 2021, 27(10):1166-1169.
[21] MAHMUD S, BISWAS S, KUMAR PAUL G, et al.Antiviral peptides against the main protease of SARS-CoV-2:A molecular docking and dynamics study[J].Arabian Journal of Chemistry, 2021, 14(9):103315.
[22] TAO W H, LI W J, JIN R T, et al.BCP4:A novel antimicrobial peptide with potent efficacy against Bacillus cereus in rice porridge[J].International Journal of Food Microbiology, 2025, 429:111001.
[23] MOHAMMADI M, TAHERI B, MOMENZADEH N, et al.Identification and characterization of novel antimicrobial peptide from hippocampus comes by in silico and experimental studies[J].Marine Biotechnology, 2018, 20(6):718-728.