羟基肉桂酸(hydroxycinnamic acid,HCA)是一类广泛分布于多种植物中的酚酸类化合物,是木质素的主要成分,其代表化合物有咖啡酸、阿魏酸、对香豆酸和芥子酸[1]。羟基肉桂酸脱羧酶(hydroxycinnamic acid decarboxylase,HCDC)是一种广泛存在于微生物中的酶,可以催化HCA非氧化脱羧生成乙烯基酚[2]。目前报道的HCDC可按其作用的底物分为阿魏酸脱羧酶(ferulic acid decarboxylase,FDC)、对香豆酸脱羧酶(p-coumaric acid decarboxylase,PDC)和苯基丙烯酸脱羧酶(phenylacrylic acid decarboxylase,PAD1)[3]。4-乙烯基愈创木酚(4-vinylguaiacol,4-VG)是FDC最重要的催化产物[4],可以通过生物催化反应进一步改性,形成其他有价值的食用香精,包括乙酰香草醛、乙烯基愈创木酚和香兰素[5]。此外,4-VG可赋予葡萄酒、啤酒、苹果酒、白酒及酱油等发酵食品独特的香气属性[6]。同时,4-VG在制药和新兴材料行业也有较高的需求和应用,如抗真菌剂、抗氧化剂和滴眼液等[7]。
4-VG的制备方法主要有植物提取法[8]、化学合成法[9]以及生物合成法[10]。然而,植物提取法和化学合成法生产成本高、工艺复杂、产率低、环境不友好。生物合成法前体物质单一、条件温和、环境友好,具有广阔的应用前景,而且生物技术制备的香料被视为天然产品[11]。因此,利用FDC生物合成4-VG补充此类香料的生产途径具有重要的意义。目前关于HCDC的研究多数来源于芽孢杆菌(Bacillius)[12-13]、植物乳杆菌(Lactobacillus plantarum)[14]、布鲁克塞尔酒香酵母(Brettanomyces bruxellensis)[15-16]、曲霉菌属(Aspergillus)[17]。ZHOU等[18]将具有HCDC活性的异常威克汉姆酵母(Wickerhamomyces anomalus)应用在蓝莓酒的发酵中,最终使蓝莓酒的品质得到提高。然而,来源于W. anomalus的FDC异源表达研究极少。
本研究选取来源于W. anomalus的FDC基因在毕赤酵母宿主中进行异源表达,验证表达且具有HCDC活性后,进行后续的酶学性质及底物特异性研究,为工业上催化阿魏酸脱羧生成4-VG的方法提供有力参考依据。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株与质粒
Pichia pastoris GS115、Escherichia coli DH5α、表达载体pPIC9K,均由江南大学生物工程学院余晓斌教授课题组分享。
1.1.2 试剂
蛋白胨、酵母浸出粉、葡萄糖、NaCl、琼脂粉,上海博微生物科技有限公司;咖啡酸、阿魏酸、对香豆酸、芥子酸、氨苄青霉素钠,上海易恩化学技术有限公司;甲醇、乙腈,均为色谱纯,西格玛奥里奇(上海)贸易有限公司;无氨基酸酵母氮源、通用型DNA纯化回收试剂盒、SanPrep柱式质粒DNA小量抽提试剂盒,生工生物工程(上海)股份有限公司;5×PrimeSTAR Buffer、dNTP Mixture、PrimeSTAR HS DNA Polymerase,宝日医生物技术(北京)有限公司;DNA marker(15 000 bp)、Gene Green染料、考马斯亮蓝染料R-250、彩虹180广谱蛋白Marker(11~180 kDa),北京索莱宝科技有限公司;其余试剂均为国产分析纯。配制培养基与试剂所用的水均为分析纯水,由实验室提供。
1.1.3 培养基
LB液体培养基(g/L):蛋白胨10、酵母浸出粉5、NaCl 10,pH 7.2~7.4。
LB固体培养基(g/L):蛋白胨10、酵母浸出粉5、NaCl 10,琼脂粉20,pH 7.2~7.4。
酵母浸出粉胨葡萄糖(yeast extractpeptone dextrose,YPD)培养基(g/L):蛋白胨20、酵母浸出粉10、葡萄糖20。
最小葡萄糖(minimal dextrose,MD)培养基(g/L):琼脂糖20、无氨基酸酵母氮源13.4、葡萄糖20、生物素0.004。
含甘油的缓冲性完全培养基(buffered glycerol-complex medium,BMGY)(g/L):胰蛋白胨20、酵母浸出粉10、甘油1%(体积分数)、无氨基酸酵母氮源13.4、生物素0.004、K2HPO4 3、KH2PO4 11.8。
复合诱导表达培养基(buffered methanol-complex medium,BMMY)(g/L):胰蛋白胨20、酵母浸出粉10、甲醇0.5%(体积分数)、无氨基酸酵母氮源13.4、生物素0.04。
发酵基础盐培养基(fermentation basal salts medium,BSM)(g/L):CaSO4 0.93、K2SO4 18.2、MgSO4·7H2O 14.9、KOH 1.43、甘油40、H3PO4 2.67%(体积分数)。
1.2 仪器与设备
SPX-250B-Z生化培养箱、YXQ-75S11立式压力蒸汽灭菌器,上海博迅实业有限公司医疗设备厂;ZQPL-200立式全温振荡培养箱,天津市莱玻特瑞仪器设备有限公司;BEP-600电泳电源、蛋白电泳装置,北京伯兰特仪器设备有限公司;BL100蓝光透射仪,天根生化科技有限公司;电转仪,伯乐生命医学产品(上海)有限公司;9960D超声波清洗器,天津可贝尔有限公司;IMS-30全自动雪花制冰机,常熟市雪科电器有限公司;Agilent-LC 1260 infinity Ⅰ高效液相色谱仪,安捷伦科技公司;Essentia LC-16高效液相色谱仪,岛津仪器(苏州)有限公司。
1.3 实验方法
1.3.1 阿魏酸脱羧酶XM的蛋白质序列分析、分子对接及活性位点预测
通过美国国家生物技术信息中心(NCBI)数据库筛选出来源于W. anomalus的阿魏酸脱羧酶XM(登录号:XP_019037777.1)[19],运用ExPASY软件计算分子质量、等电点、半衰期、不稳定系数、亲疏水性分析等序列信息,使用SignalP-4.1、NetNGlyc-1.0 Server软件分别预测阿魏酸脱羧酶XM的信号肽及切割位点、糖基化位点,使用云深智药AI Lab(https://drug.ai.tencent.com/cn)预测阿魏酸脱羧酶XM的三维结构,借助AutoDockTools-1.5.7软件对阿魏酸脱羧酶XM与咖啡酸、阿魏酸、对香豆酸、芥子酸进行分子对接并预测关键氨基酸位点,使用PyMOL对结果可视化分析。
1.3.2 重组质粒的构建
阿魏酸脱羧酶XM基因序列由苏州金唯智生物科技有限公司合成,并在质粒pPIC9K的2个酶切位点EcoR Ⅰ和Not Ⅰ之间插入该段基因,获得的重组质粒命名为pPIC9K-XM。将重组质粒转化至E.coli DH5α,送上海生工生物有限公司进行测序验证。
1.3.3 重组蛋白诱导表达
将验证正确的重组菌接种在LB-Amp固体平板(含100 μg/mL氨苄青霉素钠)上37 ℃培养12~16 h后,挑取单菌落接种到50 mL LB-Amp液体培养基(含100 μg/mL氨苄青霉素钠)中,于37 ℃、180 r/min摇床充分振荡培养12~16 h,使用SanPrep柱式质粒DNA小量抽提试剂盒提取质粒DNA。将质粒DNA经Sac Ⅰ单酶切线性化,电击转化至毕赤酵母GS115感受态细胞中,将转化子涂布在选择性培养基MD平板上,培养4 d。获得的阳性转化子命名为GS115-pPIC9K-XM,将阳性转化子接种于装有15 mL BMGY培养基的250 mL摇瓶中,30 ℃、220 r/min培养24 h后,菌液经4 ℃,6 000×g离心5 min,弃上清液,再将菌体重悬于15 mL BMMY培养基中,在25 ℃、220 r/min连续培养,每隔24 h加入1%(体积分数)甲醇,诱导培养84 h,经4 ℃、6 000×g离心5 min后取上清液。将上清液进行SDS-PAGE分析,同时将20 μL上清液加入100 μL含有1 mg溴甲酚紫的5 mmol/L阿魏酸溶液中观察变色情况,溴甲酚紫的变色范围为pH 5.2(黄色)~6.8(紫红色),若阿魏酸被消耗,即FDC发生脱羧反应,生成碱性乙烯基酚,溶液将变成紫色,以此验证阿魏酸脱羧酶XM基因是否正确表达且具有HCDC活性。
1.3.4 GS115-pPIC9K-XM高密度产酶发酵获取粗酶液
将表达成功且具有HCDC活性的阳性转化子进行高密度产酶发酵,发酵方法和培养基的制备参照毕赤酵母发酵工艺指南。将GS115-pPIC9K-XM新鲜单克隆接种到50 mL YPD液体培养基中,于30 ℃、220 r/min摇床中培养36 h。然后,以10%(体积分数)接种量将培养液接种至50 mL YPD液体培养基中,于30 ℃、220 r/min摇床中培养36 h。最后将300 mL成熟种子液接种到装有3 L BSM的7 L发酵罐中,发酵罐的最终工作体积为3.3 L。在甘油补料发酵阶段,用14.9 mol/L的氨水将pH控制在5左右,温度控制在30 ℃,初始搅拌速度为500 r/min,无菌空气的通气比为1.5 VVM[空气体积/(培养基体积·min)];在分批培养阶段,当甘油消耗殆尽,即溶解氧(dissolved oxygen,DO)反弹时,开始流加50 g/100 mL甘油,设定补料速率关联DO,使DO始终控制在20%~30%,流加4~8 h。饥饿2 h后,缓慢添加甲醇,将pH调节至5.5,并将转速保持在700 r/min,控制DO>20%,诱导表达4 d,诱导后的菌液于4 ℃、6 000×g离心5 min所得上清液即为粗酶液。每隔12 h取样1次,经4 ℃、6 000×g离心5 min,取上清液进行SDS-PAGE分析,并测定其蛋白含量及酶活力。
1.3.5 重组蛋白的纯化
粗酶液置于截留相对分子质量为8 000~14 000的透析袋内,使用pH 7.5、0.2 mol/L Tris-HCl缓冲液透析,并于4 ℃保存。所得溶液使用Ni NTA Beads 6FF层析柱纯化,经不同咪唑浓度(50~500 mmol/L,pH 7.5)的NTA溶液洗脱,纯化后的酶液利用SDS-PAGE分析蛋白分子质量大小和纯化结果。
1.3.6 酶活力测定
将底物阿魏酸配制成50 mmol/L的溶液,用NaOH调节pH值至6.0。反应体系为1 mL,含有0.8 mL Na2HPO4-柠檬酸缓冲液(pH 6.0)、0.1 mL 50 mmol/L底物溶液、0.1 mL纯化后的酶液,40 ℃水浴反应15 min后加入2 mL甲醇终止反应。0.22 μm滤膜过滤后用HPLC进行测定。定义每分钟消耗1 μmol阿魏酸的酶量为1 IU,HCDC活力单位为IU/mg,计算如公式(1)所示:
HCDC活力![]()
(1)
式中:V1,酶促反应体系的最终体积,mL;X,根据标准曲线计算出的消耗的阿魏酸的含量,mmol/L;V2,所加纯化酶液的量,mL;T,酶促反应时间,min;n,酶液的稀释倍数。
HPLC检测条件:Agilent ZORBAX-C18色谱柱(4.6 × 250 mm,5 μm)。A相为0.1%(体积分数)甲酸水,B相为0.1%(体积分数)甲酸乙腈,柱温40 ℃,流速1.0 mL/min,进样量20 μL,检测时间60 min,检测波长310 nm。流动相采用梯度洗脱程序,具体条件如下:初始阶段(0 min),流动相由90%(体积分数)的A相和10%(体积分数)的B相组成;在15 min时,A相比例降至75%(体积分数),B相比例升至25%(体积分数);在20 min时,恢复至初始比例,即A相90%(体积分数),B相10%(体积分数)。
1.3.7 酶学性质
为测定重组酶最适反应温度,按照1.3.6节所述构建催化体系,纯化后的酶液在不同反应温度(10、20、30、40、50、60 ℃)下测定酶活力,相对酶活力的计算如公式(2)所示:
相对酶活力![]()
(2)
为测定重组酶热稳定性,按照1.3.6节所述构建催化体系,将纯化后的酶液置于上述不同反应温度条件下保温2 h[20],迅速加热或冷却至所对应的最适反应温度后,在最适反应温度及pH=6条件下测定酶活力,使用公式(2)计算相对酶活力。
为测定重组酶最适pH,配制pH 3.0~8.0的0.15 mol/L Na2HPO4-柠檬酸缓冲液。按照1.3.6节所述构建催化体系,纯化后的酶液在不同pH条件下测定酶活力,使用公式(2)计算相对酶活力。
为测定重组酶的pH稳定性,将纯化后的酶液分别置于上述不同pH值的缓冲液中,于4 ℃冷藏处理24 h后,在最适反应条件下测定酶活力,使用公式(2)计算相对酶活力。
1.3.8 不同化学物质及金属离子对酶活力的影响
测定浓度为1、5 mmol/L金属阳离子(Cu2+、Zn2+、Mg2+、Ca2+、Mn2+、Na+、Co2+、Fe3+和K+)和化学物质乙二胺四乙酸(ethylenediaminetetraacetic acid,EDTA)对酶活力的影响。将纯化后的酶液与各种金属离子及化合物在40 ℃下孵育15 min,然后在最适反应条件下测定酶活力。以未添加金属离子的催化活力为对照,其活力定义为100%。
1.3.9 底物特异性
以1~6 mmol/L的咖啡酸、阿魏酸、对香豆酸、芥子酸为底物,按照1.3.6节的方法测定重组酶活力,研究重组酶的底物特异性。将最适底物的最高酶活力设为100%,计算催化其他底物时的相对酶活力。
1.3.10 动力学参数
分别以咖啡酸、阿魏酸、对香豆酸、芥子酸为底物,在反应体系中添加不同浓度的底物溶液(0.1~5 mmol/L),在最适pH和最适温度下反应15 min,利用软件OriginPro 2018进行非线性回归拟合,计算Vmax、Km、Kcat。
1.3.11 4-VG的转化率
将底物阿魏酸配制成40 mmol/L的溶液,用NaOH调节pH值至6.0。反应体系为25 mL,含有20 mL Na2HPO4-柠檬酸缓冲液(pH 6.0)、2.5 mL 40 mmol/L阿魏酸溶液、2.5 mL纯化后的酶液,40 ℃水浴30、60、90、120 min后加入50 mL甲醇终止反应。0.22 μm滤膜过滤后用HPLC进行测定。4-VG转化率的计算如公式(3)所示:
转化率![]()
(3)
式中:m2,根据标准曲线计算出的4-VG含量,μg;M1,阿魏酸的摩尔质量,g/mol;M2,4-VG的摩尔质量,g/mol;m1,反应体系中阿魏酸的含量,μg。
检测波长为320 nm,其余HPLC检测条件同1.3.6节。流动相采用梯度洗脱程序,具体条件如下:初始阶段(0 min),流动相由90%(体积分数)的A相和10%(体积分数)的B相组成;在30 min时,A相比例降至80%(体积分数),B相比例升至20%(体积分数);在40 min时,A相比例降至70%(体积分数),B相比例升至30%(体积分数);在50 min时,A相比例降至60%(体积分数),B相比例升至40%(体积分数);在51~60 min时,恢复至初始比例,即A相90%(体积分数),B相10%(体积分数)。
1.4 数据处理
所有数据均采用Microsoft Excel和SPSS 22.0进行分析,实验结果表示为“平均值±标准差”。使用邓肯检验比较均值差异,所有实验结果均采用5%的显著性水平,采用OriginPro 2018软件对实验数据处理制图。
2 结果与分析
2.1 阿魏酸脱羧酶XM的蛋白质序列分析、分子对接及活性位点预测
为了探究阿魏酸脱羧酶XM的氨基酸残基、理论分子质量、等电点等基本信息,运用ExPASY ProtParam Tool软件进行了计算,阿魏酸脱羧酶XM由518个氨基酸残基组成,理论分子质量为58.1 kDa,理论等电点为5.83,在酵母中的半衰期>20 h,不稳定系数达到37.86。
为进一步探究阿魏酸脱羧酶XM序列信息,采用SignalP-4.1、NetNGlyc-1.0 Server、ExPASy ProtScale预测阿魏酸脱羧酶XM的信号肽、糖基化位点及分析其亲疏水性,结果显示,阿魏酸脱羧酶XM不存在信号肽(图1-a),可直接用于后续研究;阿魏酸脱羧酶XM为亲水性蛋白(图1-b),在底物溶液中能够保持较好的溶解性和稳定性,可提高催化效率;阿魏酸脱羧酶XM的4个潜在N-糖基化位点分别位于N17、N186、N251和N326(图1-c)。
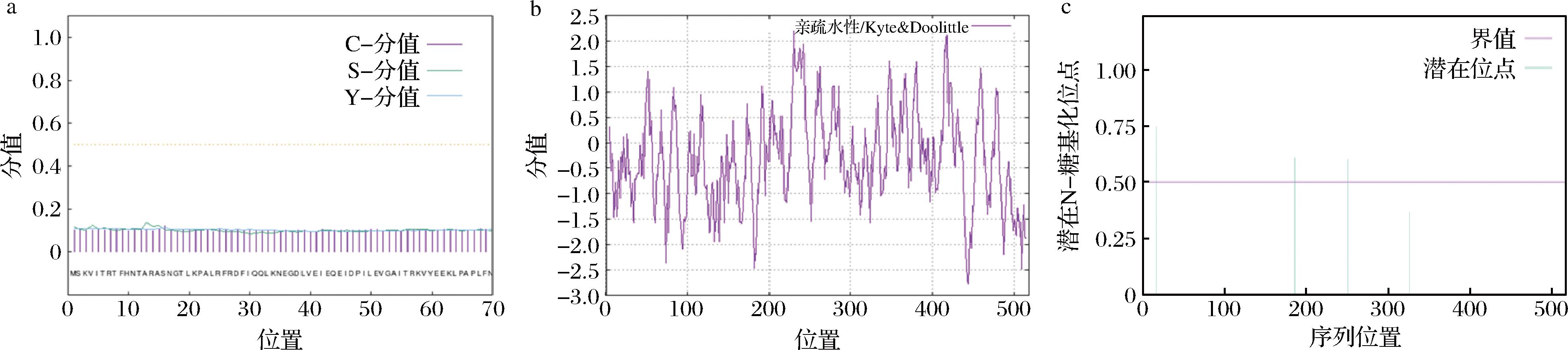
a-信号肽预测;b-亲疏水性分析(分值>0表示疏水性;分值<0表示亲水性);c-糖基化位点预测
图1 阿魏酸脱羧酶XM的蛋白质序列分析
Fig.1 Protein sequence analysis of ferulic acid decarboxylase XM
为进一步验证阿魏酸脱羧酶XM的三维结构与4种底物(咖啡酸、阿魏酸、对香豆酸、芥子酸)的亲和力大小,采用AutoDockTools-1.5.7软件进行分子对接,结果表明,阿魏酸脱羧酶XM上的TYR-305、PHE-299两种氨基酸与小分子底物咖啡酸结合形成3个氢键(图2-a);阿魏酸脱羧酶XM上的HIS-303、TYR-305、GLN-310三种氨基酸与阿魏酸结合形成5个氢键(图2-b);阿魏酸脱羧酶XM上的TYR-305、HIS-303两种氨基酸与小分子底物对香豆酸结合形成3个氢键(图2-c);阿魏酸脱羧酶XM上的GLU-252、HIS-209两种氨基酸与小分子底物芥子酸结合形成2个氢键(图2-d),这些氨基酸残基可能影响阿魏脱羧酶XM的功能。
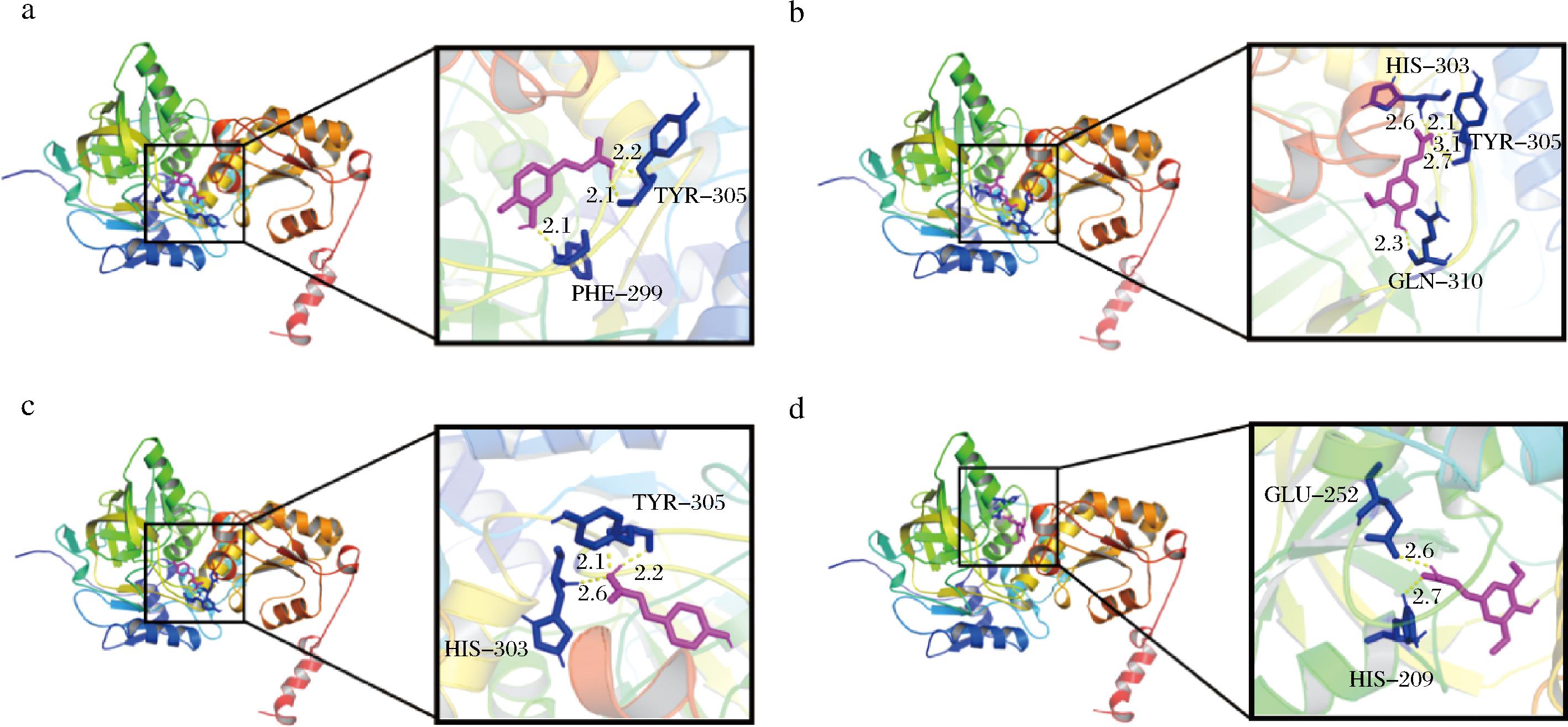
a-咖啡酸;b-阿魏酸;c-对香豆酸;d-芥子酸
图2 阿魏酸脱羧酶XM与不同底物的分子对接图
Fig.2 Molecular docking diagram of ferulic acid decarboxylase XM with different substrates
阿魏酸脱羧酶XM与咖啡酸、阿魏酸、对香豆酸、芥子酸的对接结合能分别是-6.9、-6.9、-6.6、-6.0 kcal/mol,结合能的绝对值越大,结合越稳定,因此,阿魏酸脱羧酶XM与咖啡酸和阿魏酸的结合更稳定。
2.2 重组蛋白的诱导表达
为研究阿魏酸脱羧酶XM在毕赤酵母系统中的表达,将阿魏酸脱羧酶XM同源重组到毕赤酵母表达宿主中,利用甲醇诱导表达84 h后经离心取上清液,SDS-PAGE分析结果如图3-a所示,与GS115-pPIC9K相比,凝胶上的GS115-pPIC9K-XM发酵上清液多出了一条分子质量为68 kDa的条带,与预测的分子质量相比,相差10 kDa左右,可能是羟基肉桂酸脱羧酶XM预测的糖基化位点有4个,糖基化程度更高更复杂造成的。
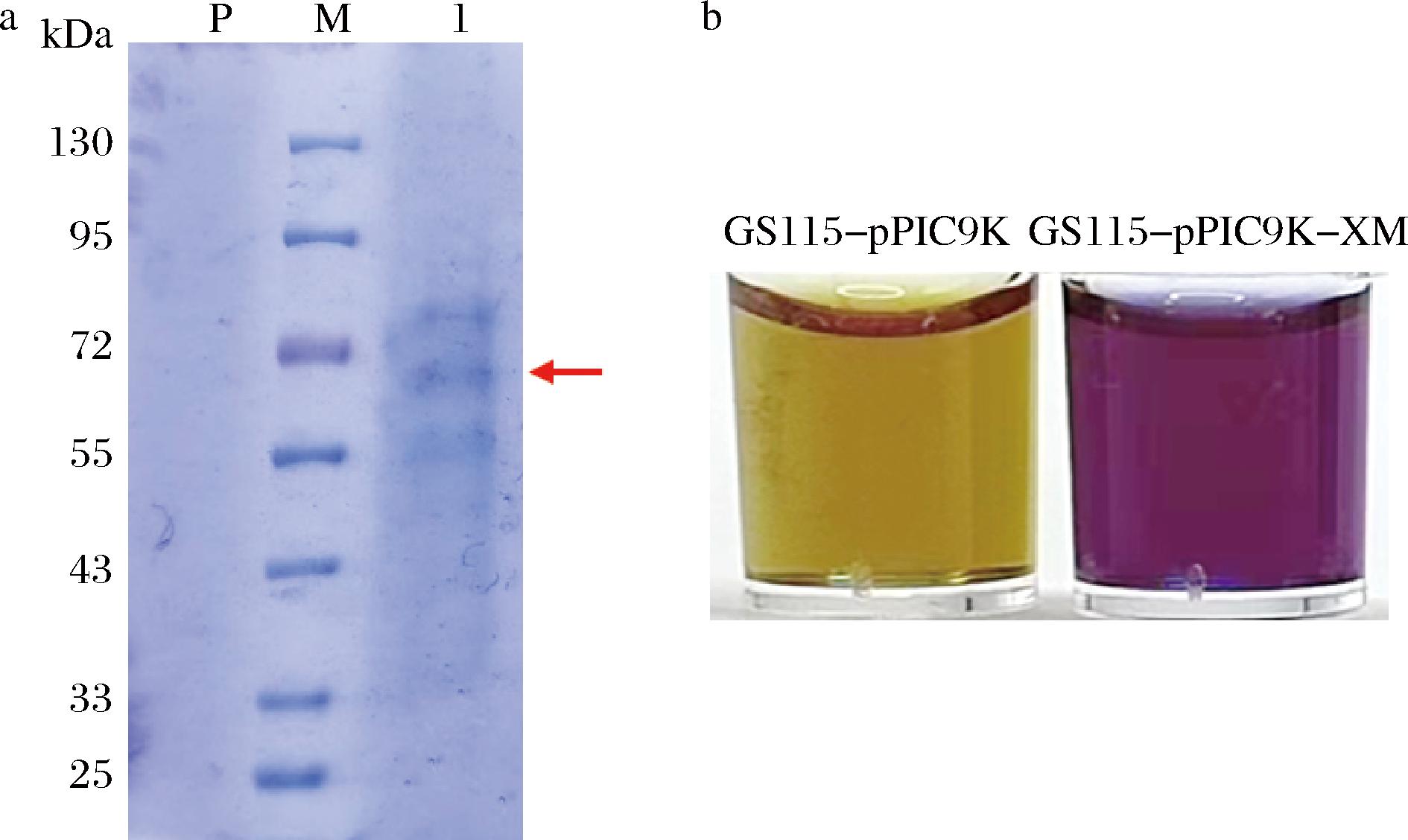
P-GS115-pPIC9K;M-蛋白质Marker;1-GS115-pPIC9K-XM。a-SDS-PAGE分析;b-上清液的HCDC活性验证
图3 诱导表达上清液的SDS-PAGE分析及活性验证
Fig.3 SDS-PAGE analysis and activity verification of induced expression supernatant
如图3-b所示,将100 μL GS115-pPIC9K-XM上清液加入到含有1 mg溴甲酚紫的100 μL 5 mmol/L阿魏酸溶液中,溶液变成紫色,而加入100 μL GS115-pPIC9K上清液未变色,由此说明GS115-pPIC9K-XM具有HCDC活性。
2.3 GS115-pPIC9K-XM的高密度发酵
为进一步增加目的蛋白表达量,将表达成功且具有HCDC活性的GS115-pPIC9K-XM进行高密度发酵,SDS-PAGE分析结果如图4-a所示,与GS115-pPIC9K相比,凝胶上的GS115-pPIC9K-XM发酵上清液有一条分子质量约为68 kDa的条带,与理论分子质量相差约10 kDa,可能是阿魏酸脱羧酶XM预测的糖基化造成的。发酵过程中参数变化分析结果如图4-b所示,GS115-pPIC9K-XM的细胞湿重随着高密度发酵时间的延长而增加,在高密度富集阶段,细胞生长迅速(在发酵36 h细胞湿重达到(147.10±2.81) g/L;在诱导阶段,细胞生长较缓,在发酵120 h(诱导表达84 h)细胞湿重最大达到(259.27±0.55) g/L),该阶段主要是重组酶的诱导表达,在诱导表达0~72 h时,随着诱导时间的延长,蛋白质含量和总酶活力也逐渐增加,在诱导72 h时,蛋白质含量达到最大值[(15.48±0.17) mg/mL],总酶活力也达到最大[(155.84±2.39) IU/mg]。GS115-pPIC9K-XM在摇瓶中和在发酵罐中诱导84 h后的总酶活力分别为(19.72±0.32) IU/mg和(136.39±2.94) IU/mg。高密度发酵比摇瓶发酵总酶活力提升了(116.67±2.62) IU/mg,与大肠杆菌重组酚酸脱羧酶活力(19.2 IU/mL)相比有显著提升[21]。
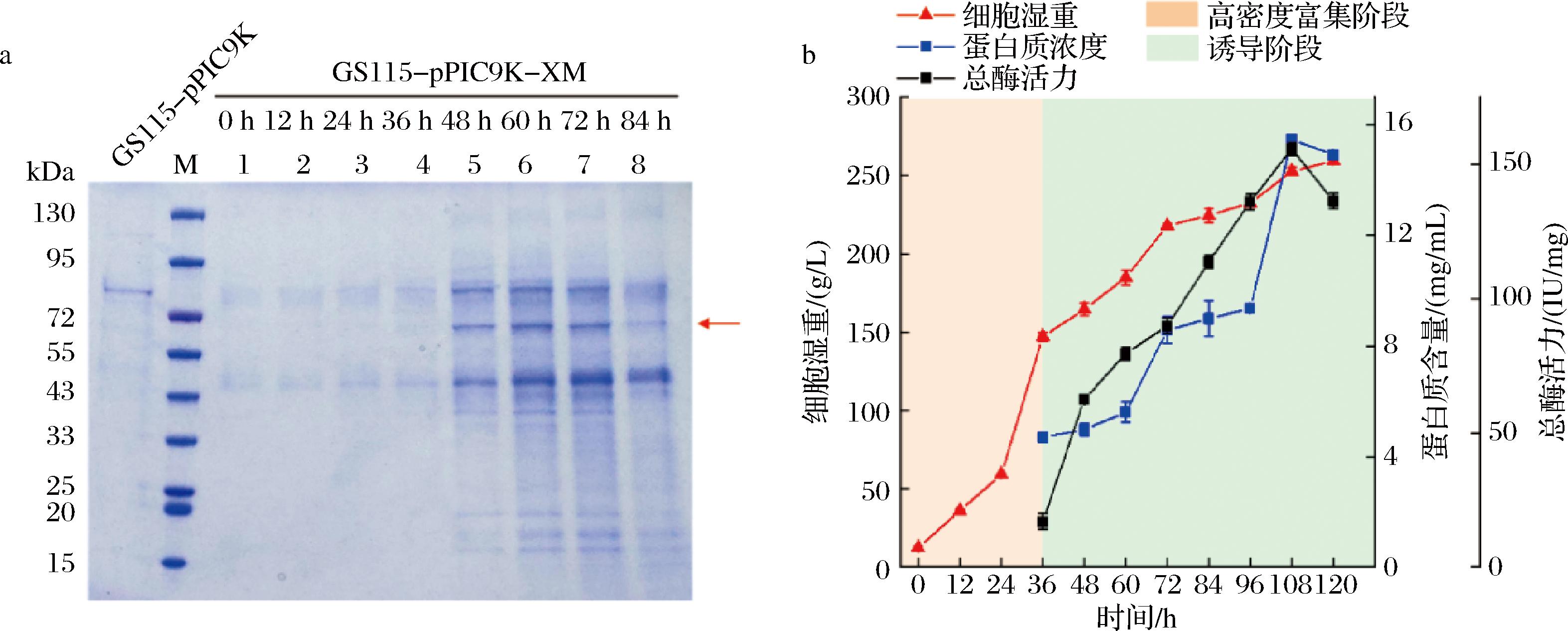
M-蛋白质Marker。a-高密度发酵上清液的SDS-PAGE分析;b-发酵过程中参数的变化
图4 高密度发酵上清液的SDS-PAGE分析及发酵过程中参数的变化
Fig.4 SDS-PAGE analysis of high-density fermentation supernatant and variation of parameters during high-density fermentation
如图5所示,将20 μL GS115-pPIC9K-XM高密度发酵上清液加入到100 μL含有1 mg溴甲酚紫的5 mmol/L阿魏酸溶液中,溶液变成紫色,而加入20 μL GS115-pPIC9K上清液未变色,由此说明GS115-pPIC9K-XM具有HCDC活力且比摇瓶发酵活力高。

图5 高密度发酵上清液的显色反应
Fig.5 Color development reaction of high-density fermentation supernatant
2.4 重组蛋白的纯化
重组酶通过Ni NTA Beads 6FF层析柱进行纯化,纯化后经SDS-PAGE分析验证,在55 kDa和72 kDa之间有一条约为68 kDa清晰的蛋白条带(图6),与理论分子质量(58.1 kDa)相差约10 kDa,可能是由于阿魏酸脱羧酶XM的糖基化造成。
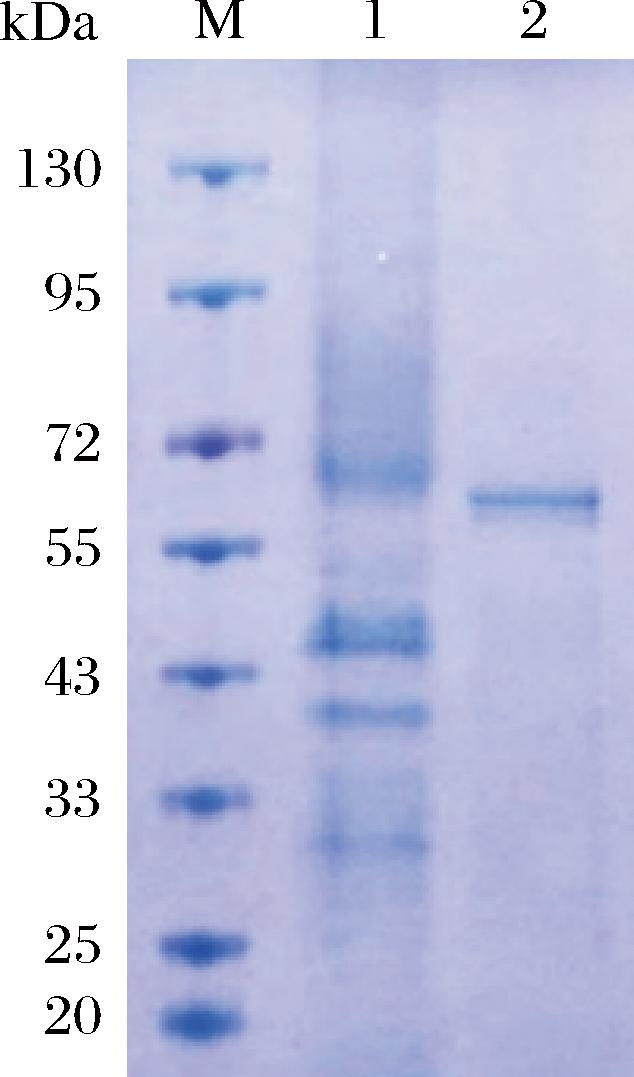
M-蛋白质Marker;1-粗酶液;2-纯化后的酶液。
图6 纯化蛋白的SDS-PAGE分析
Fig.6 SDS-PAGE analysis of the purified protein
2.5 酶学性质
如图7-a所示,重组酶在10~40 ℃内酶活力随着温度的升高而升高,在40 ℃后,酶活力随着温度的升高而逐渐降低,因此重组酶的最适反应温度为40 ℃,这与EDLIN等[22]研究结果一致,60 ℃时酶的蛋白结构可能被破坏,导致酶活力降低至20%以下。为探索重组酶的温度稳定性,测定在不同温度下孵育2 h后酶活力,结果如图7-b所示,在30~50 ℃内表现出良好的稳定性,相对酶活力达到60%以上。
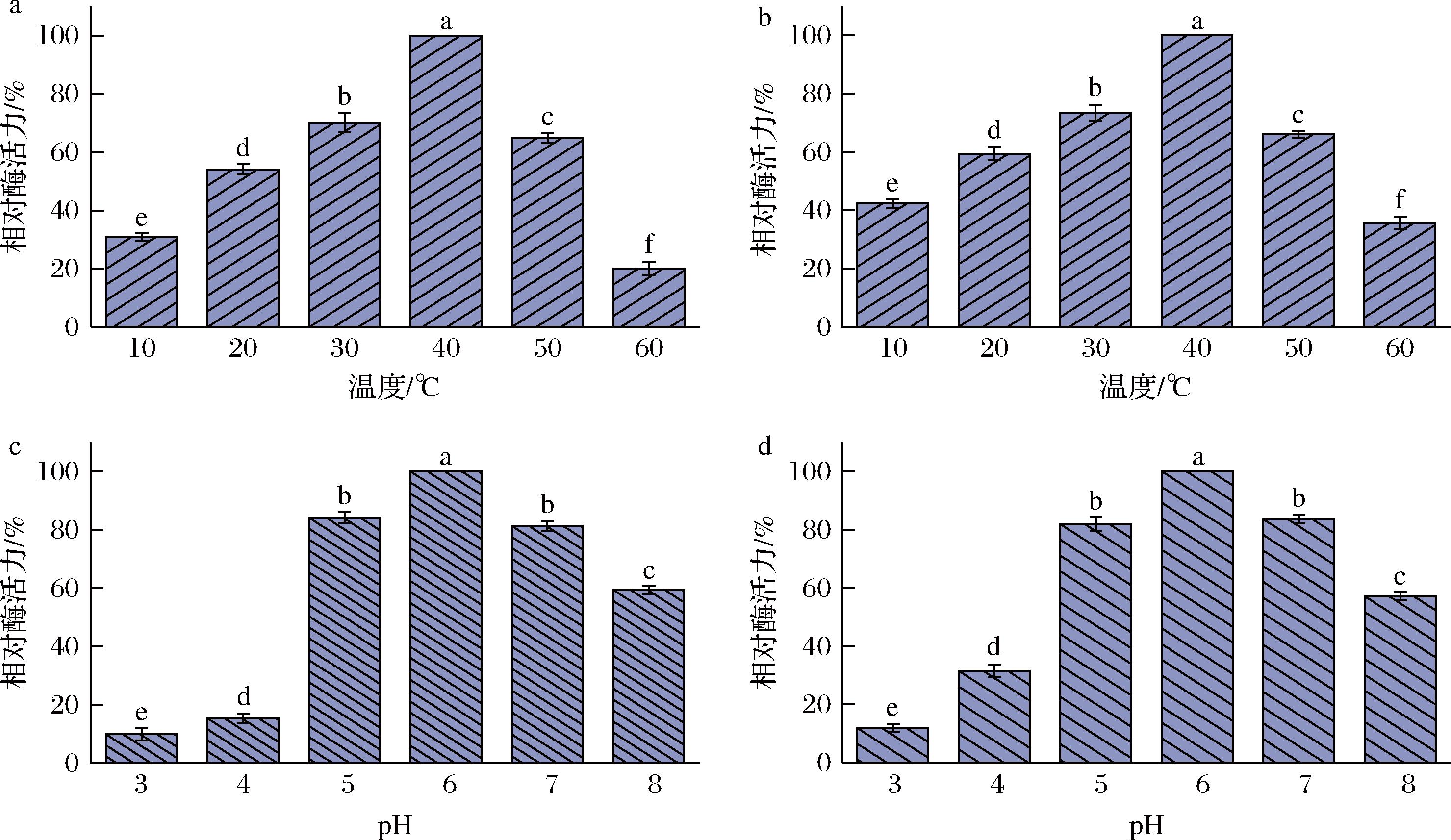
a-不同温度对重组酶活力的影响;b-重组酶的温度稳定性;c-不同pH对重组酶活力的影响;d-重组酶的pH稳定性
图7 不同温度、pH对重组酶活力的影响
Fig.7 Effect of different temperature and pH on the activity of recombinant enzymes
为研究重组酶的最适pH,测定了pH为3~8时的酶活力,结果如图7-c所示。在pH 3.0~6.0条件下,随着pH的升高,酶活力逐渐提升,重组酶的最适pH为6,这与前人的研究结果一致[23],pH=3时酶活力低至10%左右,pH=8时酶活力仍近50%。由此可见,重组酶在酸性条件下,酶活力较低。为了探究重组酶的pH稳定性,测定其在不同pH条件下、4 ℃放置24 h后的活力,结果如图7-d所示,重组酶在pH=6时酶活力最稳定,当pH<4时,相对酶活力低于30%,在pH 5~7时表现出较好的稳定性,相对酶活力达到80%以上,说明重组酶不耐强酸[4]。
2.6 不同化学物质和金属离子对酶活力的影响
由表1可以看出,Fe3+、EDTA对重组酶活力均有较明显的提升效果,Mg2+、Mn2+、Na+、Co2+对重组酶活力均有较大的抑制作用,可能是这些离子影响阿魏酸脱羧酶XM的活性中心结构[4]。Ca2+、K+在1 mmol/L浓度下对重组酶活力有抑制作用,而在5 mmol/L浓度下对重组酶活力影响较小,其余各金属离子对重组酶活力的影响均较小。
表1 不同化学物质和金属离子对重组酶活力的影响 单位:%
Table 1 Effects of different chemicals and metal ions on recombinant enzymes activity
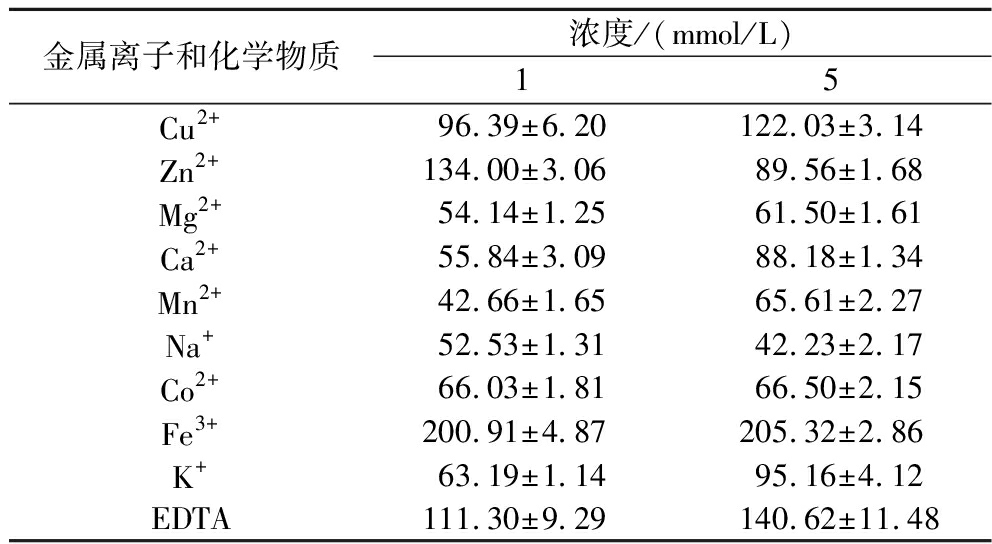
金属离子和化学物质浓度/(mmol/L)15Cu2+96.39±6.20122.03±3.14Zn2+134.00±3.0689.56±1.68Mg2+54.14±1.2561.50±1.61Ca2+55.84±3.0988.18±1.34Mn2+42.66±1.6565.61±2.27Na+52.53±1.3142.23±2.17Co2+66.03±1.8166.50±2.15Fe3+200.91±4.87205.32±2.86K+63.19±1.1495.16±4.12EDTA111.30±9.29140.62±11.48
注:以未添加金属离子时酶的催化活力为对照,该活力定义为100%。
2.7 底物特异性
如图8所示,重组酶对4 mmol/L浓度下的4种底物均表现出较强的催化分解能力,其中对阿魏酸的催化分解能力最强,其次是咖啡酸、对香豆酸、芥子酸,相对酶活力最高分别达到98.28%、96.82%、83.92%,这与2.1节的研究结果一致。在以1~6 mmol/L咖啡酸、阿魏酸、对香豆酸为底物时,相对酶活力均达到80%以上,说明重组酶对这3种酸的脱羧能力较好。
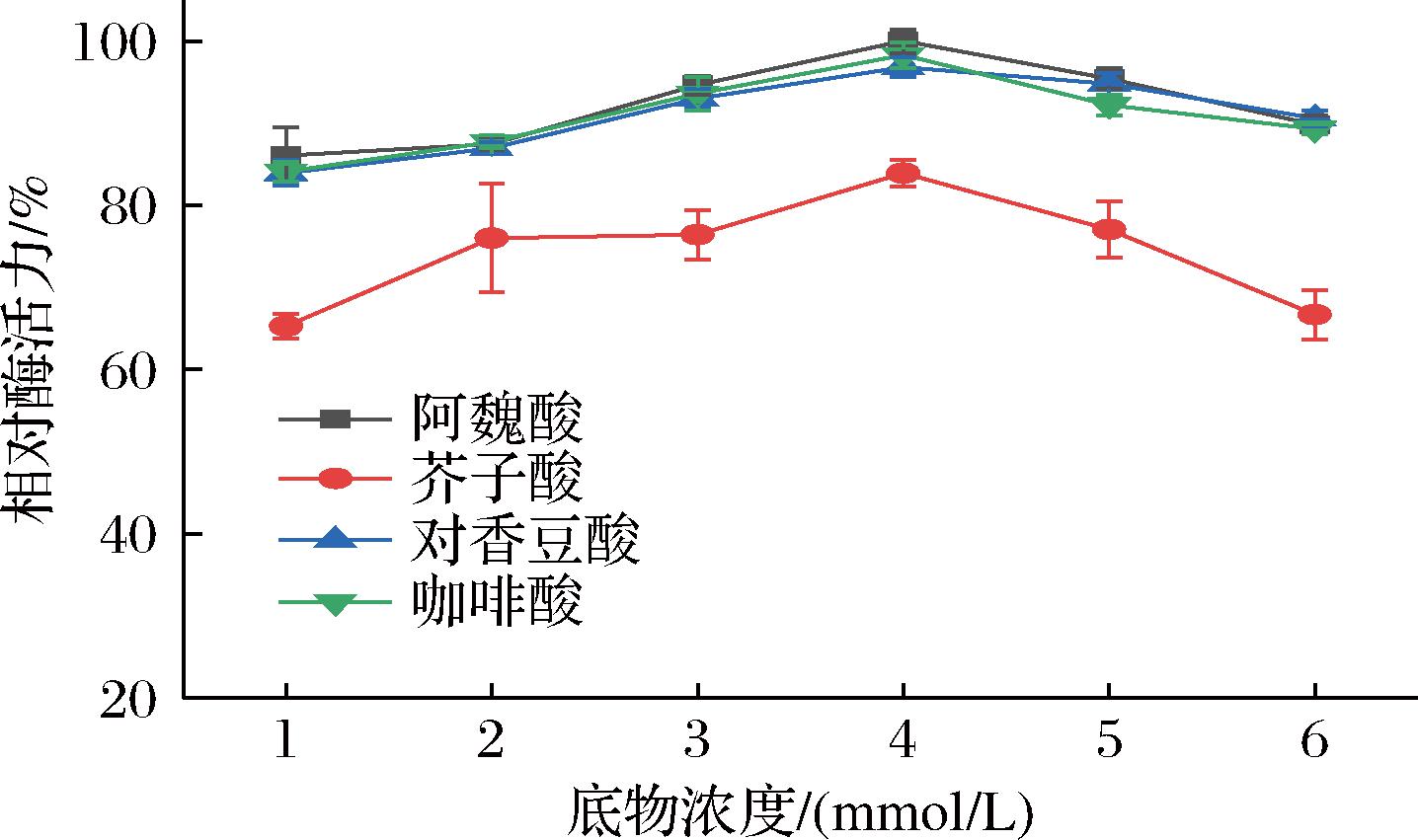
图8 不同底物浓度对重组酶活力的影响
Fig.8 Effect of different substrate concentrations on recombinant enzymes activity
2.8 动力学参数
Km值越小,重组酶与底物的亲和力越强;Kcat值越大,重组酶对底物的催化效率越好[24]。由表2可见,4种底物中重组酶与阿魏酸的亲和力最强,其次是咖啡酸、对香豆酸、芥子酸,重组酶对阿魏酸的催化效率最好。因此,重组酶的最适底物是阿魏酸,这与2.1节和2.7节的研究结果一致。
表2 重组酶对4种底物的动力学参数
Table 2 Kinetic parameters of recombinant enzymes for four substrates
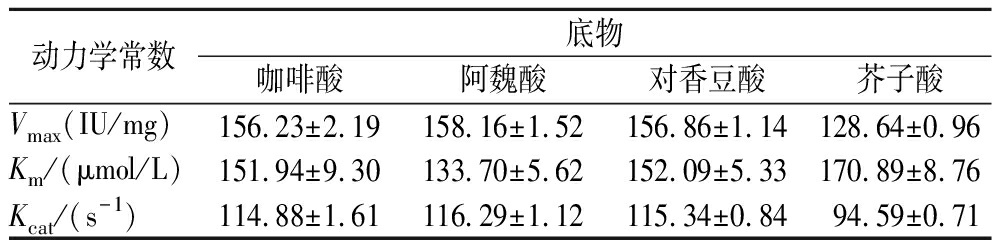
动力学常数底物咖啡酸阿魏酸对香豆酸芥子酸Vmax(IU/mg)156.23±2.19158.16±1.52156.86±1.14128.64±0.96Km/(μmol/L)151.94±9.30 133.70±5.62152.09±5.33170.89±8.76Kcat/(s-1)114.88±1.61116.29±1.12115.34±0.8494.59±0.71
2.9 4-VG的转化率
为进一步探究阿魏酸脱羧酶XM催化最适底物阿魏酸生成4-VG的效率,在1.3.6节酶活力测定的1 mL反应体系的基础上,将反应体系增大到25 mL,在最适反应温度40 ℃,最适pH 6.0以及底物最适浓度4 mmol/L的条件下测定产物4-VG的转化率。如图9-a所示,4-VG标准品的质量浓度为0.05~0.4 mg/mL,出峰时间为48.14 min左右。如图9-b所示,重组酶在反应时间30~120 min内,随着反应时间的延长,4-VG的转化率呈现下降趋势,在反应30 min时4-VG的转化率达到最高为85.71%,反应120 min时转化率仍达到70.96%。
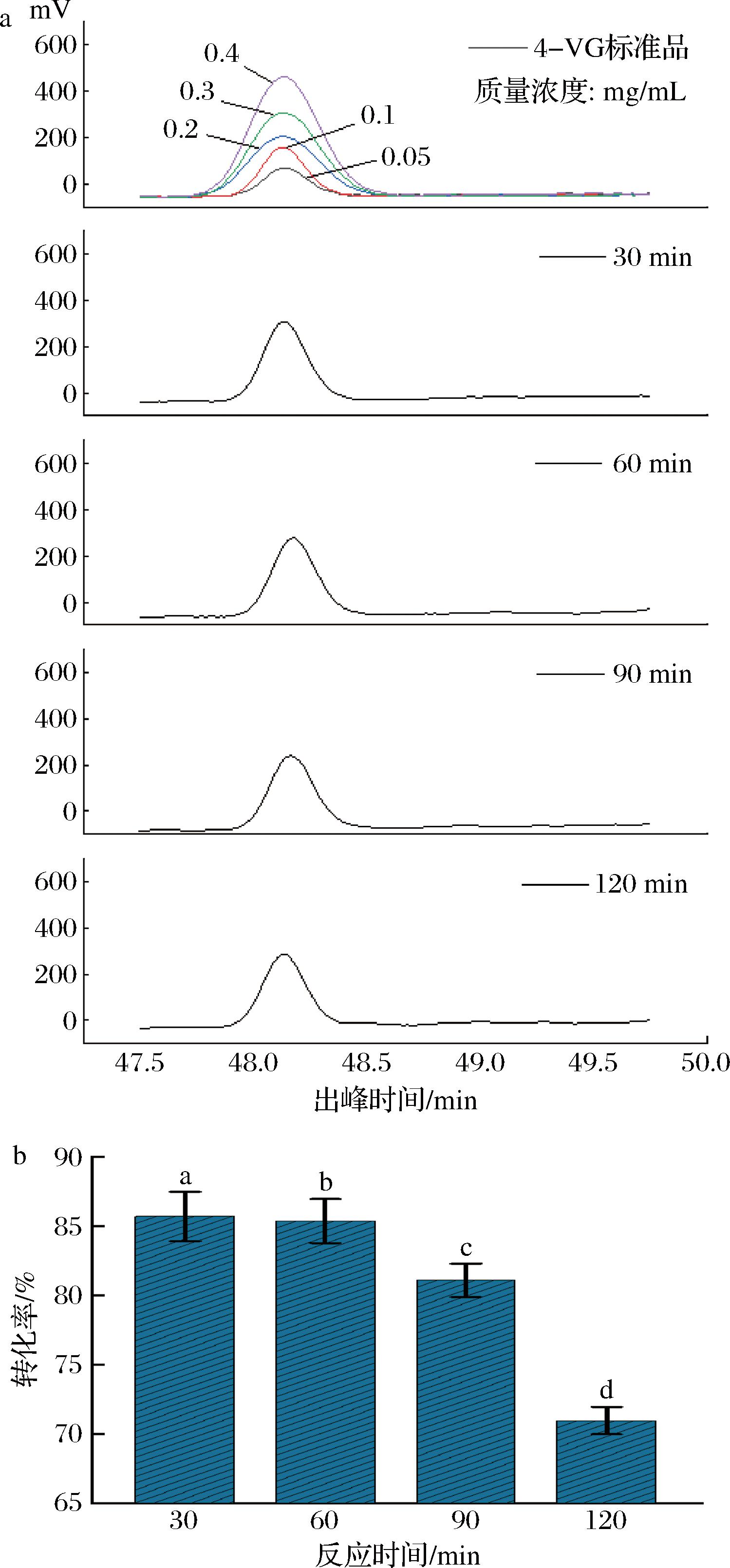
a-色谱图;b-转化率
图9 不同反应时间下4-VG的色谱图及其转化率
Fig.9 Chromatogram and conversion rate of 4-VG under different reaction time
3 结论
本研究将来源于W. anomalus的阿魏酸脱羧酶XM同源重组到毕赤酵母细胞内进行异源表达,随后进行高密度产酶发酵以提高FDC的表达量,SDS-PAGE分析验证了目的蛋白表达条带与理论分子质量一致,且酶液具有HCDC活性。纯化后的酶液通过酶学性质的研究发现,该重组酶的最适pH及最适温度分别为6.0、40 ℃。该酶在pH 5.0~7.0和 30~50 ℃时表现出良好的稳定,相对酶活力仍有60%以上,但是该酶不耐强酸,在以后研究中可通过固定化技术对阿魏酸脱羧酶XM的稳定性进行改造,以满足工业化生产的需求。Fe3+、EDTA对重组酶活力均有较明显的提升效果,而Mg2+、Mn2+、Na+、Co2+对重组酶活力均有较大的抑制作用。在底物浓度为4 mmol/L条件下,该重组酶对4种酸的脱羧能力最好,且该重组酶对阿魏酸的脱羧能力最强,其次是咖啡酸、对香豆酸和芥子酸。重组酶在40 ℃,pH=6.0和4 mmol/L阿魏酸条件下反应30 min后生成的4-VG转化率达到85.71%,且随着反应时间的延长,转化率降低。本研究通过异源表达及酶学性质手段对重组酶进行研究,为工业上生产制备4-VG提供一定的参考。
[1] HOA N T, NGOC VAN L T, VO Q V.The hydroperoxyl antiradical activity of natural hydroxycinnamic acid derivatives in physiological environments:The effects of pH values on rate constants[J].RSC Advances, 2022, 12(24):15115-15122.
[2] ROSIMIN A A, KIM K S.Production of volatile phenols by kimchi Lactobacillus plantarum isolates and factors influencing their phenolic acid decarboxylase gene expression profiles[J].Food Research International, 2015, 78:231-237.
[3] 陈阴竹, 覃池, 李琴, 等.微生物来源酚酸脱羧酶的研究进展[J].食品科学, 2024, 45(11):323-332.
CHEN Y Z, QIN C, LI Q, et al.Research progress in phenolic acid decarboxylase derived from microorganisms[J].Food Science, 2024, 45(11):323-332.
[4] ZHAO Y J, ZHU B F, ZHOU Z Y, et al.Cloning and characterization of phenolic acid decarboxylase responsible for aromatic volatile phenols production in Paocai based on metatranscriptomics[J].Food Bioscience, 2023, 55:102953.
[5] NI W J, ZHANG P Y, LONG L K, et al.Engineering and linker-mediated co-immobilization of carotenoid cleavage oxygenase with phenolic acid decarboxylase for efficiently converting ferulic acid into vanillin[J].Process Biochemistry, 2022, 122:67-77.
[6] PIZARRO C, PÉREZ-DEL-NOTARIO N, GONZ LEZ-S
LEZ-S IZ J M.Headspace solid-phase microextraction for direct determination of volatile phenols in cider[J].Journal of Separation Science, 2009, 32(21):3746-3754.
IZ J M.Headspace solid-phase microextraction for direct determination of volatile phenols in cider[J].Journal of Separation Science, 2009, 32(21):3746-3754.
[7] 徐李亮, 施罗欣洁, 李若赛, 等.羟基肉桂酸类化合物及其衍生物在阿尔茨海默病治疗中的研究进展[J].海峡药学, 2022, 34(8):78-82.
XU L L, SHI L, LI R S, et al.Progress of hydroxycinnamic acids and their derivatives in Alzheimer’s disease[J].Strait Pharmaceutical Journal, 2022, 34(8):78-82.
[8] 林炯明, 陈建军.从稻草生物油中提取4-乙基愈创木酚的方法:中国,CN1146985A[P].2014-04-09.
LIN J M, CHEN J J. A method for extracting 4-ethylguaiacol from rice straw bio-oil: China, CN102659534B[P]. 2014-04-09.
[9] 陈恩治, 金涛.4-乙基愈创木酚的合成[J].香料香精化妆品, 2010(3):30-32.
CHEN E Z, JIN T.Synthesis of 4-ethylguaiacol[J].Flavour Fragrance Cosmetics, 2010(3):30-32.
[10] 巩园园, 毛豪, 晋湘宜, 等.产4-乙烯基愈创木酚细菌的筛选及酚酸脱羧酶基因的克隆与表达[J].中国酿造, 2021, 40(7):160-164.
GONG Y Y, MAO H, JIN X Y, et al.Screening of 4-vinylguaiacol-producing bacteria and cloning and expression of phenolic acid decarboxylase gene[J].China Brewing, 2021, 40(7):160-164.
[11] HOU R R, WANG Y Z, YANG J, et al.Bioconversion of waste generated during ethanol production into value-added products for sustainable utilization of rice straw[J].Biochemical Engineering Journal, 2020, 164:107761.
[12] LI Q, XIA Y, ZHAO T, et al.Improving the catalytic characteristics of phenolic acid decarboxylase from Bacillus amyloliquefaciens by the engineering of N-terminus and C-terminus[J].BMC Biotechnology, 2021, 21(1):44.
[13] HU H F, LI L L, DING S J.An organic solvent-tolerant phenolic acid decarboxylase from Bacillus licheniformis for the efficient bioconversion of hydroxycinnamic acids to vinyl phenol derivatives[J].Applied Microbiology and Biotechnology, 2015, 99(12):5071-5081.
[14] OKCU G, AYHAN K, GUNES ALTUNTAS E, et al.Determination of phenolic acid decarboxylase produced by lactic acid bacteria isolated from shalgam ( algam) juice using green analytical chemistry method[J].LWT - Food Science and Technology, 2016, 66:615-621.
algam) juice using green analytical chemistry method[J].LWT - Food Science and Technology, 2016, 66:615-621.
[15] LAFORGUE R, LONVAUD-FUNEL A.Hydroxycinnamic acid decarboxylase activity of Brettanomyces bruxellensis involved in volatile phenol production:Relationship with cell viability[J].Food Microbiology, 2012, 32(2):230-234.
[16] GODOY L, MART NEZ C, CARRASCO N, et al.Purification and characterization of a p-coumarate decarboxylase and a vinylphenol reductase from Brettanomyces bruxellensis[J].International Journal of Food Microbiology, 2008, 127(1-2):6-11.
NEZ C, CARRASCO N, et al.Purification and characterization of a p-coumarate decarboxylase and a vinylphenol reductase from Brettanomyces bruxellensis[J].International Journal of Food Microbiology, 2008, 127(1-2):6-11.
[17] MAEDA M, MOTOSOKO M, TOKASHIKI T, et al.Phenolic acid decarboxylase of Aspergillus luchuensis plays a crucial role in 4-vinylguaiacol production during awamori brewing[J].Journal of Bioscience and Bioengineering, 2020, 130(4):352-359.
[18] ZHOU J L, TANG C Q, ZOU S L, et al.Enhancement of pyranoanthocyanin formation in blueberry wine with non-Saccharomyces yeasts[J].Food Chemistry, 2024, 438:137956.
[19] RILEY R, HARIDAS S, WOLFE K H, et al.Comparative genomics of biotechnologically important yeasts[J].Proceedings of the National Academy of Sciences of the United States of America, 2016, 113(35):9882-9887.
[20] 刘向歌, 赵子琪, 吴家葳, 等.海洋细菌假交替单胞菌DL-6来源β-N-乙酰己糖胺酶异源表达及酶学表征[J].食品科学, 2024, 45(16):68-76.
LIU X G, ZHAO Z Q, WU J W, et al.Heterologous expression and enzymatic characterization of β-N-acetylhexosaminidase from marine bacterium Pseudoalteromonas sp.DL-6[J].Food Science, 2024, 45(16):68-76.
[21] 任明杰, 王路路, 申纪辉, 等.解淀粉芽孢杆菌Q-426酚酸脱羧酶的克隆表达及酶学性质鉴定[J].中国生物工程杂志, 2022, 42(6):20-29.
REN M J, WANG L L, SHEN J H, et al.Cloning, expression and characterization of phenolic acid decarboxylase from Bacillus amyloliquefaciens Q-426[J].China Biotechnology, 2022, 42(6):20-29.
[22] EDLIN D A N, NARBAD A, GASSON M J, et al.Purification and characterization of hydroxycinnamate decarboxylase from Brettanomyces anomalus[J].Enzyme and Microbial Technology, 1998, 22(4):232-239.
[23] DENG H L, GU Q Y, YU X B, et al.Surface-displayed phenolic acid decarboxylase for increased vinylphenolic pyranoanthocyanins in blueberry wine[J].Current Research in Food Science, 2024, 8:100730.
[24] 王婉莹, 李志建, 李泽浩, 等.克雷伯杆菌烯还原酶基因的异源表达和性质研究[J].食品与发酵工业, 2025, 51(14):65-73.
WANG W Y, LI Z J, LI Z H, et al.Heterologous expression and characterization of Klebsiella sp.ene reductase gene[J].Food and Fermentation Industries, 2025, 51(14):65-73.