酱香型白酒作为中国白酒的杰出代表,凭借其卓越的品质和独特的风味,不仅在中国白酒市场占据举足轻重的地位,更承载着深厚的文化底蕴[1]。因此,深入研究其酿造机制,对于揭示传统固态发酵的科学奥秘,具有重要的理论及实际价值。高温大曲是酱香型白酒生产中的糖化剂、发酵剂和生香剂[2],是酱香型白酒生产的关键工艺环节,其复杂的微生物群落是形成独特风味物质的基础[3-5]。真核微生物,尤其是丝状真菌,是高温大曲菌群的重要组成部分,一直以来被认为主要是通过分泌丰富的淀粉酶和纤维素酶,为后续发酵提供必要的碳源和能量[6-7]。然而,尽管已有研究证实大曲中存在嗜热或耐热的丝状真菌,但作为优势菌群,其是否直接参与高温大曲的香气形成,以及具体的香气贡献特点和机制,目前尚缺乏深入系统的研究。这一认知的不足,不仅严重制约了我们对大曲培养机制的全面解析,也限制了通过优化微生物群落结构来提升白酒品质和风味的潜力。
近年来,随着分子生物学技术的快速发展[8],高通量测序是评估复杂样本中真菌多样性的有力工具[9]。多数研究者借助高通量测序技术对高温大曲的真菌群落组成[10]、理化性质[11]、空间特征[12]、演替规律[13]等进行了系统性探究。通过分析大数据之间的相关关系,大量研究者推测了丝状真菌的产香贡献,并取得了一些进展。例如,JIN等[14]利用高通量测序和顶空固相微萃取-气相色谱-质谱联用技术(headspace solid-phase microextraction-gas chromatography-mass spectrometry,HS-SPME-GC-MS)对酱香大曲样品进行微生物多样性和挥发性香气进行检测,结果表明曲霉(Aspergillus)与酯类和芳香族化合物的生成有直接关联。CAI等[7]利用高通量测序和电子传感研究了高温大曲中的真菌多样性、味道和香气特征,揭示了高温大曲的香气主要是受到毛霉属(Mucor)、曲霉属(Aspergillus)、嗜热真菌属(Thermomyces)和嗜热子囊菌属(Thermoascus)等优势真菌属的影响。ZHANG等[15]利用高通量测序和核磁共振探究优级大曲和普通大曲的微生物群落多样性和代谢物的差异,发现嗜热子囊菌属(Thermoascus)与丙氨酸呈高度负相关。然而,仅依靠高通量测序技术难以获得微生物的纯培养物[16],也无法详细阐述香气产生与丝状真菌发酵时间的因果关系。因此,需要结合可培养方法以及原位模拟发酵以进一步深入研究。
与此同时,通过可培养方法验证菌株功能性的研究取得了显著进展。例如,通过在选择性培养基上培养,研究人员从高温大曲中分离筛选出高产糖化酶的黑曲霉(Aspergillus niger)、高产酸性蛋白酶的米曲霉(Aspergillus oryzae)、高产酯化酶的红曲霉(Monascus purpureus)[17]。HUANG等[18]从高温大曲中分离鉴定出1种新的蛋白酶生产者(Aspergillus hennebergii),通过酶水解鉴定和定量了42种化合物,其中主要是酯类和芳香族化合物。何夷敏等[19]采用传统培养分离技术从大曲中筛选到产酶及产香性能优良的丝状真菌。邓灿[20]从高温大曲中筛选出1株宛氏拟青霉(Paecilomyces variotii PV3),并将其应用于大曲的实际生产,结果发现强化曲的液化力显著提升。这些研究展示了可培养方法在解析微生物功能方面的独特优势。然而,由于丝状真菌的细胞壁成分复杂[21]、生长速率差异很大[22]等难点,使其难以通过常规分离方法将其从原位体系中提取出来。目前,大多数研究都是根据丝状真菌的产酶特性进行选择性培养,鲜有研究结合高通量测序等组学技术和可培养方法,并通过原位验证风味化合物的合成潜力[23],这在很大程度上限制了对大曲产香微生物的认识以及对其发酵机制的深入理解。
本研究以酱香型白酒高温大曲主体丝状真菌为研究对象,旨在通过高通量测序和可培养方法,系统解析大曲培养过程中主体丝状真菌的种属关系及其形态学特征。同时,通过原位模拟发酵,深入探究主体丝状真菌的生长特性及其生香特征。本研究为高温大曲的微生物资源开发和工艺优化提供了有价值的参考。
1 材料与方法
1.1 样本采集
实验样品取自贵州省仁怀市茅台镇3家酱香型白酒酒厂,采集发酵第0、8、15、40天的曲样,每个发酵点取3份平行样本。取样后,大曲样品破碎混匀,低温运至实验室,分别贮存于4 ℃(用于微生物分离培养)和-80 ℃(用于高通量测序)。
1.2 主要试剂与仪器
PDA培养基、HCl、NaOH(分析纯),上海国药集团化学试剂有限公司;Takara裂解液,宝日医生物技术(北京)有限公司。
HWS-150恒温培养箱,上海森信实验仪器公司;气相色谱GC 7890B/质谱MS 5975、DB-FFAP色谱柱,美国Agilent公司;SPME自动进样系统,德国Gerstel公司;SU8220扫描电子显微镜,HITACHI公司。
1.3 高温大曲中主体丝状真菌的分离筛选与鉴定
称取5 g大曲样品,置于45 mL无菌PBS和玻璃珠的三角瓶中,30 ℃、200 r/min振荡30 min。用PBS稀释成10-3、10-4、10-5,每种稀释液的总体积为200 μL。在PDA培养基上30 ℃和50 ℃下培养3 d,选择表观形态大小不一样的微生物进行分离纯化。
使用Takara裂解液提取DNA,上清液作为模板,使用真菌的通用引物ITS1F和ITS4R扩增真菌的ITS序列,PCR扩增条件如下:95 ℃,5 min;95 ℃,15 s;55 ℃,15 s;72 ℃,15 s,32个循环;72 ℃,5 min;16 ℃,10 min。PCR产物由生工生物工程(上海)股份有限公司进行单向测序。测序结果通过NCBI BLAST进行同源性序列比对。
1.4 高温大曲主体丝状真菌生长特性
将纯培养物于固体PDA培养基中培养,使用3~5 mL无菌水将菌落洗脱,以制备菌悬液。
采用点植法将菌体接种于PDA培养基,分别于30、45、50、55、60 ℃下培养4 d,每天测量各菌株菌落的2个垂直直径,每个菌株设3个生物学重复。
用1 mol/L HCl溶液和NaOH溶液将PDA培养基pH值调至3.5、4.0、4.5和6.5,采用点植法将菌体接种到不同pH的培养基培养4 d,每天测量各菌株菌落的2个垂直直径,每个菌株设3个生物学重复。
在大曲培养过程中,不同阶段的温度和pH如下:入仓(30 ℃、pH 6.5)、一翻(60 ℃、pH 4.0)、二翻(50 ℃、pH 4.5)、拆仓(30 ℃、pH 6.5)。将菌体点植于PDA培养基上,分别置于在一翻、二翻、拆仓阶段的条件下培养4 d,每天测量各菌株菌落的2个垂直直径,每个菌株设3个生物学重复。
1.5 高温大曲主体丝状真菌的变温固态发酵
为了深入解析高温大曲主体丝状真菌的代谢潜力,提高大曲的质量和风味,本研究模拟大曲发酵过程中温度的变化,利用小麦固体培养基进行变温发酵。
小麦固体培养基的制备:将小麦作为原料,粉碎后加入95 ℃的水润粮5 h(过夜),加入高温淀粉酶,115 ℃灭菌30 min,温度降为60 ℃时,在无菌条件下加入糖化酶,搅拌混匀后置于60 ℃烘箱处理2 h,分装置于牛皮纸袋(模拟稻草)中备用。
菌株接种:将菌株接种于PDA液体培养基中震荡培养24 h即为种子液。实验组将种子液以5%的接种量接种至固体培养基中,空白组则将无菌水以5%的接种量接种至固体培养基中。
培养条件:在30、35、40、45、55 ℃和60 ℃条件下,于恒温培养箱中静置发酵24 h后更换1次发酵温度,共持续发酵7 d。
1.6 挥发性化合物测定
采用HS-SPME-GC-MS分析检测菌株发酵产物的挥发性风味物质。将5 g发酵样品于20 mL超纯水中,漩涡振荡10 min,冰浴超声30 min。4 ℃冰箱过夜放置后振荡10 min,8 000×g离心10 min,收集上清液备用。称取1.5 g NaCl于20 mL顶空瓶中,加入5 mL上清液,再以5 μL薄荷醇(质量浓度为100 mg/L)作为内标,迅速用带聚四氟乙烯垫片的空心铁盖密封,检测条件基于该实验室早些时候建立的方法[6]。
1.7 高通量测序、数据处理和分析
根据制造商的说明,使用E.Z.N.A.® soil DNA kit从大曲样本中提取基因组DNA,每个样本设3个生物学重复。以提取的DNA为模板,使用真菌通用引物ITS3F和ITS4R进行PCR扩增。对纯化后的PCR产物建库,利用Illumina Miseq PE300平台测序,使用fastp软件进行质控,FLASH软件进行拼接。基于默认参数,使用Qiime2的DADA2插件进行降噪处理。去除叶绿体和线粒体序列。将所有样本序列数抽平至6 000,平均序列覆盖度为99.09%。基于UNITE ITS基因数据库,置信度阈值为70%,使用Qiime2的Naive bayes分类器进行物种分类学分析。采用mothur软件算Alph多样性指标(Chao 1、Shannon指数等),并进行组间差异分析;使用主坐标分析结合PERMANOVA检验样本间微生物群落结构的相似性及差异显著性;用线性判别分析确定不同组间从门到属水平丰度显著差异的真菌类群。
1.8 数据分析和可视化
本研究中的可视化图使用Origin 2021软件和Illustrator 2020软件进行。
2 结果与分析
2.1 解析高温大曲主体丝状真菌
大曲培养过程是一个多菌种混合发酵,其微生物菌群结构复杂多样。为了确定高温大曲的真菌群落特征,本研究对A酒厂高温大曲不同发酵阶段(第0、8、15、40天)的大曲样本进行DNA提取并扩增子测序,将测序数据与公共数据库进行对比注释。将相对丰度>1%的真菌属定义为优势菌属,相对丰度<1%的菌属归为其他属。如图1-a所示,在大曲培养过程中共鉴定到19个优势菌属,其中12个为优势丝状真菌属,包括嗜热子囊菌属(Thermomyces,42.97%)、拟青霉属(Paecilomyces,16.58%)、曲霉属(Aspergillus,11.17%)、平囊菌属(Leiothecium,4.07%)、嗜热真菌属(Thermomyces,3.67%)、红曲霉属(Monascus,2.42%)等。此外,本研究结果还表明大曲培养阶段的真菌群落表现出稳定的演替规律,发酵初期以Paecilomyces为主,逐渐演替为Aspergillus(第8天)及Thermomyces和Thermoascus(第15~40天),与马叶胜等[12]研究结果一致。
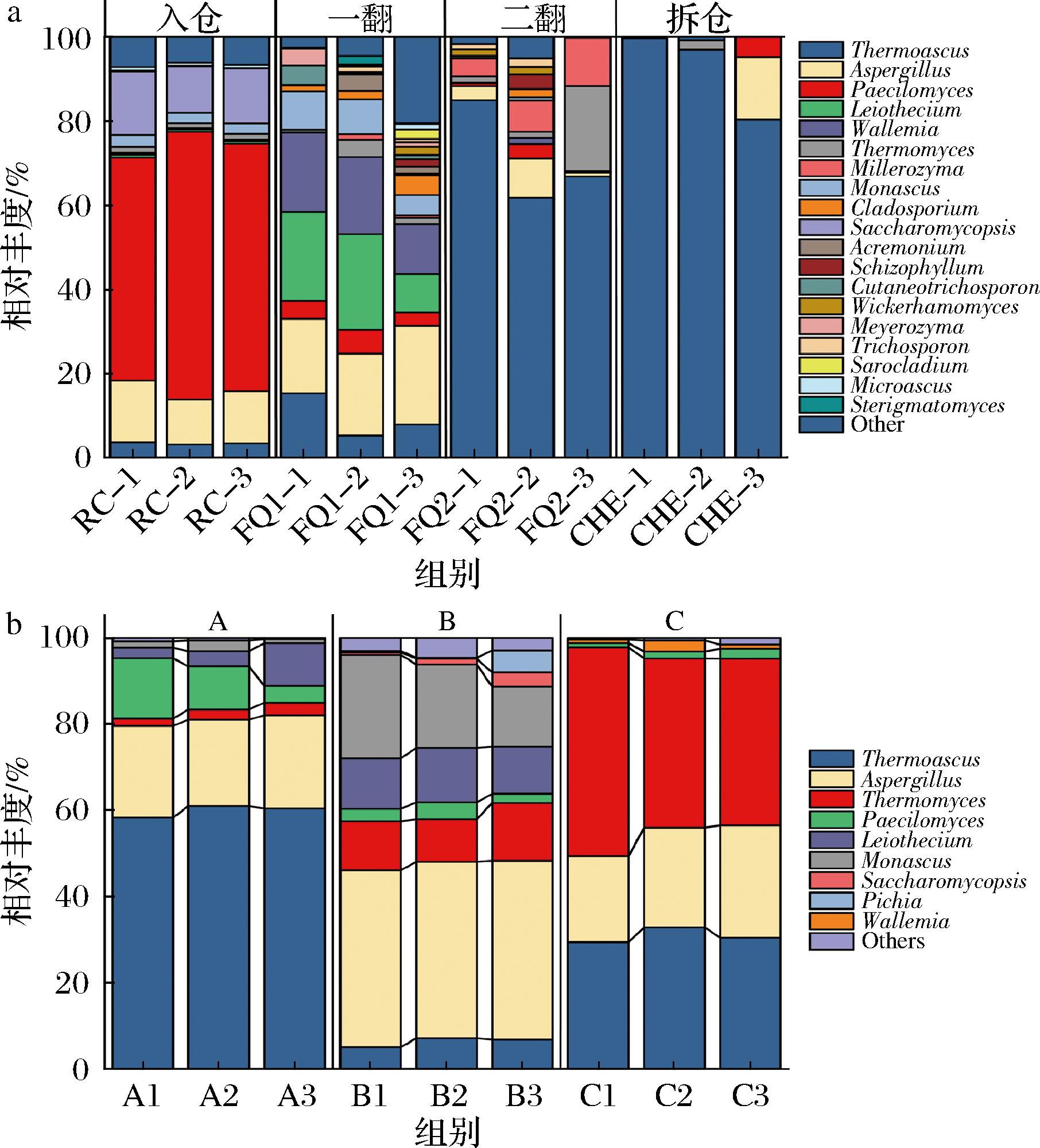
a-A酒厂高温大曲的不同发酵阶段;b-A、B、C这3个酒厂
图1 高温大曲真菌群落特征分析
Fig.1 Analysis of fungal community characteristics in high temperature Daqu
本研究进一步解析了包括A在内的3个酒厂母曲,结果如图1-b所示,共检测到9个优势菌属,其中6个优势丝状真菌属,分别为嗜热子囊菌属(Thermoascus,32.37%)、曲霉属(Aspergillus,28.41%)、嗜热真菌属(Thermomyces,18.65%)、拟青霉属(Paecilomyces,4.65%)、平囊菌属(Leiothecium,5.69%)、红曲霉属(Monascus,6.89%)。其中,Thermoascus、Thermomyces、Aspergillus和Paecilomyces在3个酒厂所有大曲样本中都出现,是高温大曲中的主体丝状真菌。这些菌属在所有大曲样本中的相对丰度范围为:Thermoascus(3.36%~92.37%)、Thermomyces(1.34%~42.11%)、Aspergillus(4.53%~41.19%)、Paecilomyces(1.41%~58.84%)。
2.2 高温大曲主体丝状真菌的分离鉴定
2.2.1 菌株的分离鉴定
本研究采用分离培养技术从高温大曲样品中分离培养到4种主体丝状真菌纯培养物。分别为疏棉状嗜热丝孢菌(Thermomyces lanuginosus)5株、坚脆嗜热子囊菌(Thermoascus crustaceus)18株、米曲霉(Aspergillus orayzae)2株、宛氏拟青霉(Paecilomyces variotii)3株。菌株的筛选培养基、培养条件、鉴定结果等如表1所示。
表1 主体丝状真菌的分离和鉴定结果
Table 1 Results of isolation and identification of dominant filamentous fungi
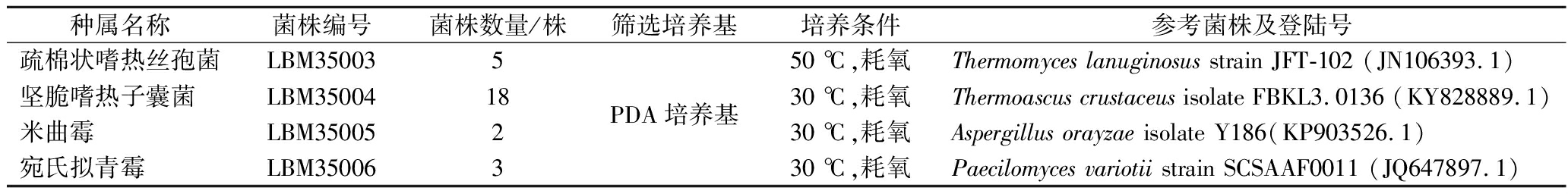
种属名称菌株编号菌株数量/株筛选培养基培养条件参考菌株及登陆号疏棉状嗜热丝孢菌LBM350035坚脆嗜热子囊菌LBM3500418米曲霉LBM350052宛氏拟青霉LBM350063PDA培养基50 ℃,耗氧Thermomyces lanuginosus strain JFT-102 (JN106393.1)30 ℃,耗氧Thermoascus crustaceus isolate FBKL3.0136 (KY828889.1)30 ℃,耗氧Aspergillus orayzae isolate Y186(KP903526.1)30 ℃,耗氧Paecilomyces variotii strain SCSAAF0011 (JQ647897.1)
2.2.2 菌株的形态学特征
本研究从PDA培养基上筛选出4株主体丝状真菌,通过形态观察和冷场发射扫描电子显微镜分析其生长特征和微观结构。如图2所示,这些真菌在形态和结构上存在显著差异:T.lanuginosus在50 ℃下培养3 d,菌落由白色絮状变为绿灰色至黑色,子囊果球形或近球形,菌丝结构清晰,孢子平均直径约10 μm。T.crustaceus生长迅速,菌落呈浅黄褐色,无渗出液和可溶性色素,具分枝和隔膜,闭囊壳球形。A.orayzae菌落初期为白色或浅黄色,后变为黄绿色,呈丝绒状,分生孢子球形或近球形,表面光滑,直径约3 μm,孢子梗细长直立。P.variotii菌落生长速度快,表面粉末状,由黄色变为棕绿色,分生孢子梗和小梗呈扫帚状分支,小梗细长且基部膨大弯曲,分生孢子呈棱形、瓜子形和椭圆形,表面光滑。这些结果表明,高温大曲中的真核微生物具有丰富的形态和结构多样性。

a-T.lanuginosus,500×;b-T.crustaceus,2 400×;c-A.orayzae,1 000×;d-P.variotii,600×
图2 主体丝状真菌的菌落形态图(左)和电子显微镜图(右)
Fig.2 The colony morphology (left) and electron microscopy image (right) of dominant filamentous fungi
2.3 非生物因素对高温大曲主体丝状真菌生长的影响
生物或非生物因素对微生物的生长、群落演替及代谢谱的形成具有显著影响[24-26]。主体丝状真菌在高温大曲中占据主体地位并发挥重要作用。本研究初步解析了非生物因素对主体丝状真菌生长和代谢的影响,揭示其在大曲培养中的生态适应机制,为解析微生物群落的演替规律提供重要依据。
在传统固态发酵过程中,温度对微生物群落性能至关重要[24,27]。为深入探究温度对高温大曲中主体丝状真菌生长的影响,本研究将4株主体丝状真菌置于不同温度下固体培养4 d,通过菌落直径评估其生长状态。如图3-a所示,30 ℃时4株菌都能生长,但60 ℃下无真菌生长。其中,T.lanuginosus在55 ℃生长良好,菌落直径达4.3 cm;P.variotii和T.crustaceus在50 ℃有微弱生长,直径分别为1.2、1.4 cm;A.orayzae 在45 ℃未能生长。这一结果表明在高温大曲第1次翻曲阶段时环境条件贫瘠,抑制部分菌株生长,同时筛选出耐高温特性的优势菌株,为微生物群落演替提供了重要依据。
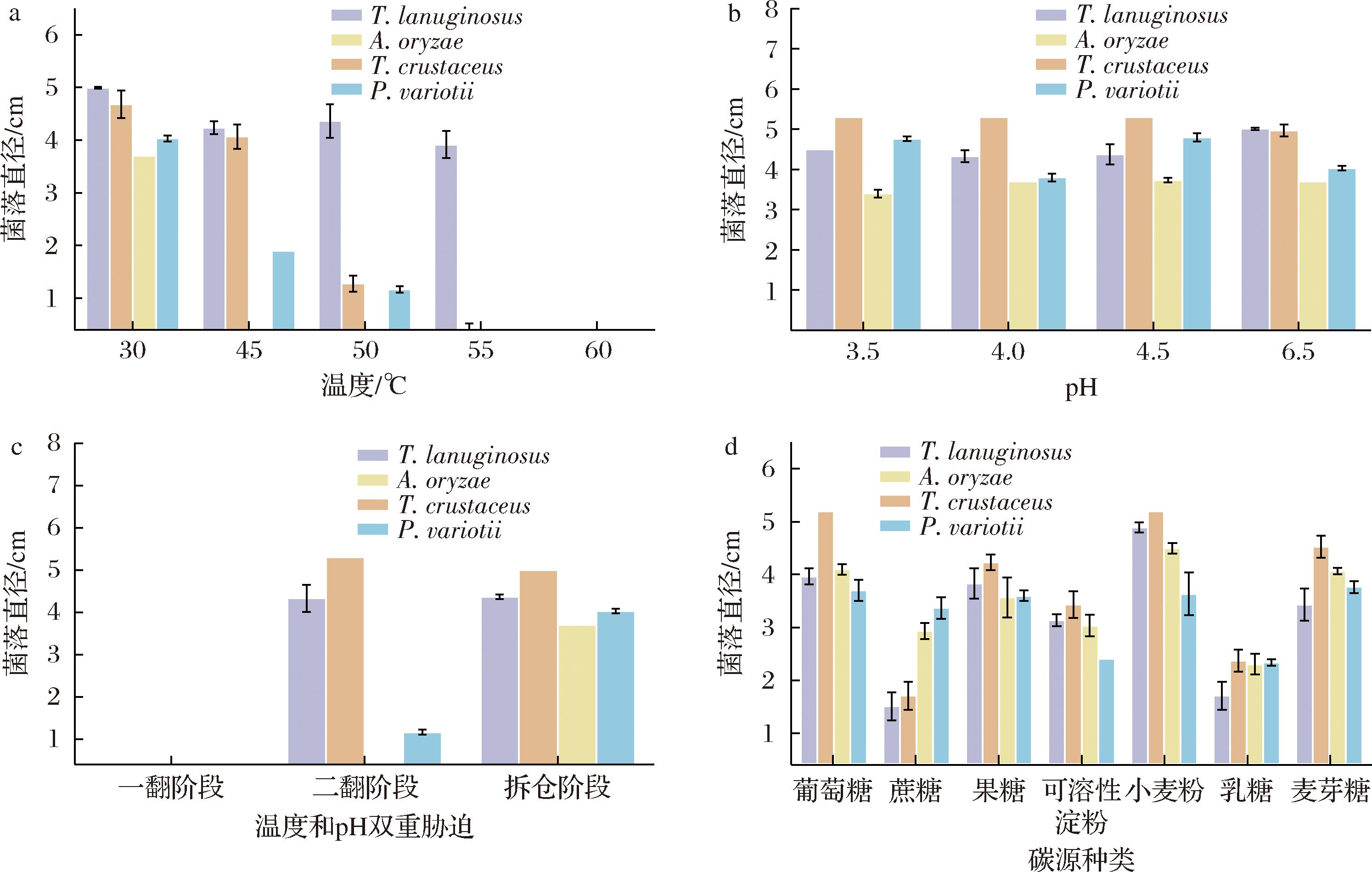
a-温度;b-pH;c-温度和pH双重胁迫;d-碳源种类
图3 非生物因素对高温大曲主体丝状真菌生长的影响
Fig.3 Influence of abiotic factors on the growth of dominant filamentous fungi in high temperature Daqu
注:图c中,一翻阶段:60 ℃,pH 4.0;二翻阶段:50 ℃,pH 4.5;拆仓阶段:30 ℃,pH 6.5。
pH对微生物的生长及产物合成具有重要影响[28]。本研究系统评估了4株主体丝状真菌在pH值为3.5~6.5的固体培养基中的生长情况。如图3-b所示,所有菌株均能在该pH范围内生长,表现出广泛的pH耐受性。这与大曲培养环境的低酸性特征密切相关[29]。这种广泛的pH适应性有助于维持微生物在复杂发酵环境中的稳定生长和代谢活性,保障大曲发酵过程中微生物群落演替及代谢产物的多样性。
在发酵过程中,监测关键微生物以及调控环境因素,将有效避免不利条件并提高发酵质量[30]。本研究模拟大曲培养的关键阶段(一翻、二翻和拆仓),设置了温度和pH双重胁迫条件。如图3-c所示,在一翻阶段(60 ℃、4.0)没有菌株生长。在二翻阶段(50 ℃、4.5),T.lanuginosus和T.crustaceus生长良好,菌落直径约5 cm,P.variotii生长缓慢,菌落直径为1.1 cm。所有菌株在拆仓阶段都能快速生长。这为T.lanuginosus和T.crustaceus在发酵后期成为优势菌株提供了有力的实验证据,同时也揭示了它们在复杂环境条件下的适应性和竞争力。
碳源是决定真菌代谢产物种类和含量的关键因素,进而决定了大曲风味的基础[31]。本研究探究了4株主体丝状真菌在不同碳源的固体培养基中的生长情况。如图3-d所示,所有菌株在不同碳源培养基中均能良好生长,且在小麦粉培养基中生长最旺盛,表明小麦粉是其最佳碳源。这揭示了这些真菌具有极高代谢灵活性,能够广泛利用多种碳源,为大曲风味的形成提供了丰富的基础。
2.4 高温大曲主体丝状真菌的代谢特征
大曲培养初期温度约30 ℃,后升至40 ℃以上,后期可达到50~60 ℃[32]。这一温度变化对微生物群落的演替和风味物质的形成具有重要影响[33]。为了深入解析主体丝状真菌在大曲培养过程中的生香特征,本研究通过变温固态发酵模拟大曲环境,采用HS-SPME-GC-MS方法系统分析发酵小麦的挥发性成分。
本研究一共检测到77种挥发性化合物,9种酯类、2种酮类、5种醛类、4种芳香族、5种呋喃类、7种醇类、8种酸类、6种酚类、6种吡嗪类以及21种其他类化合物,如电子增强出版附表1所示(https://doi.org/10.13995/j.cnki.11-1802/ts.043039)。如图4所示,T.crustaceus、T.lanuginosus和A.orayzae的总挥发性化合含量均高于空白组,P.variotii的总挥发性化合物含量低于空白组。吡嗪类化合物是所有菌株中主要挥发性化合物,其中T.crustaceus和T.lanuginosus的吡嗪类化合物含量最高,分别为8 618.60、6 616.96 μg/kg。A.orayzae的酯类和呋喃类化合物含量最高,分别为517.07、271.48 μg/kg。P.variotii的芳香族化合物含量最高,达到了1 370.75 μg/kg。
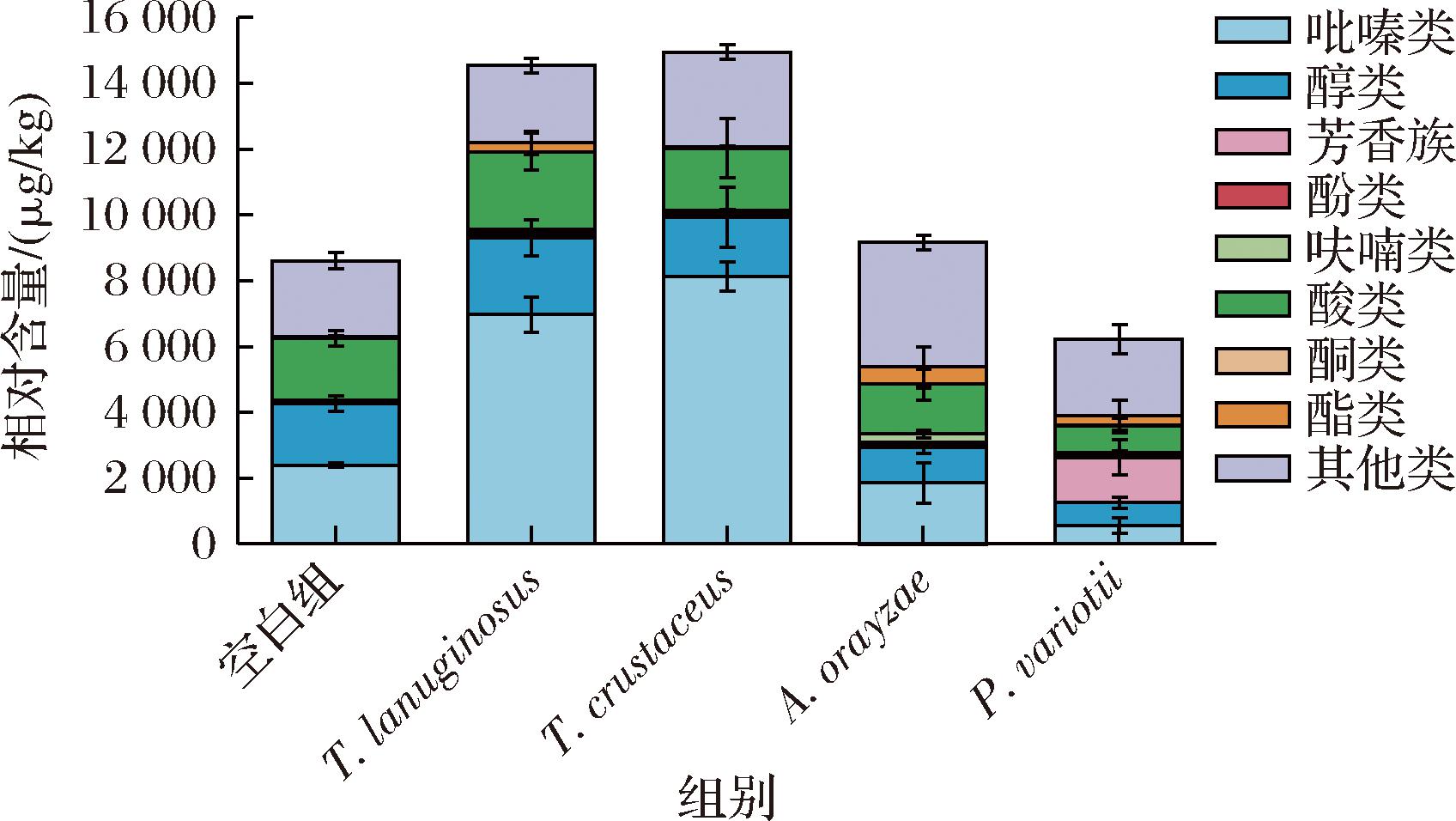
图4 主体丝状真菌的总挥发性化合物分析
Fig.4 Analysis of total volatile compounds of dominant filamentous fungi
吡嗪类物质是酱香型白酒的重要风味物质,因其有独特的烤香味和坚果味[34]。如图5-a所示,本研究中共检出6种吡嗪类物质,其中2-乙基-3,5-二甲基吡嗪和2,3,5,6-四甲基吡嗪含量最高,分别带有烘焙、焦糖杏仁、烤坚果和焦香味、坚果味。T.lanuginosus和T.crustaceus对这2类关键风味物质的合成优势尤为突出,发酵后产生浓郁的酱香味和焦香味。与空白组相比,T.crustaceus的2-乙基-3,5-二甲基吡嗪含量高达6 240.95 μg/kg,T.lanuginosus的为4 863.26 μg/kg。T.lanuginosus的2,3,5,6-四甲基吡嗪含量达到了1 799.50 μg/kg。研究发现,2,3,5,6-四甲基吡嗪、2,6-二甲基吡嗪和2,3,5-三甲基吡嗪等化合物在白酒中含量较高,且对风味的贡献显著[34]。这些物质在原位和体外样品中均被证实对大曲质量至关重要[35]。结果表明,嗜热真菌的吡嗪类化合物相对含量显著高于不嗜热真菌。在实际制曲过程中,除了嗜热真菌外,耐高温的芽孢杆菌也会产生吡嗪类物质[36]。例如,高温大曲中的芽孢杆菌在高温下能够发酵产生更多的2,3,5-三甲基吡嗪,其被认为是L-苏氨酸经L-苏氨酸脱氢酶催化合成的[37]。研究表明高温条件有利于美拉德反应的进行,这是吡嗪类化合物生成的主要途径[38]。因此,嗜热真菌在高温发酵环境中的优势生长特性,可能促使其大量合成吡嗪类化合物,从而提高发酵产物中的含量。这一发现揭示了嗜热真菌在大曲培养中的独特代谢潜力,为优化发酵工艺以增强酱香型白酒风味提供了重要的理论依据。
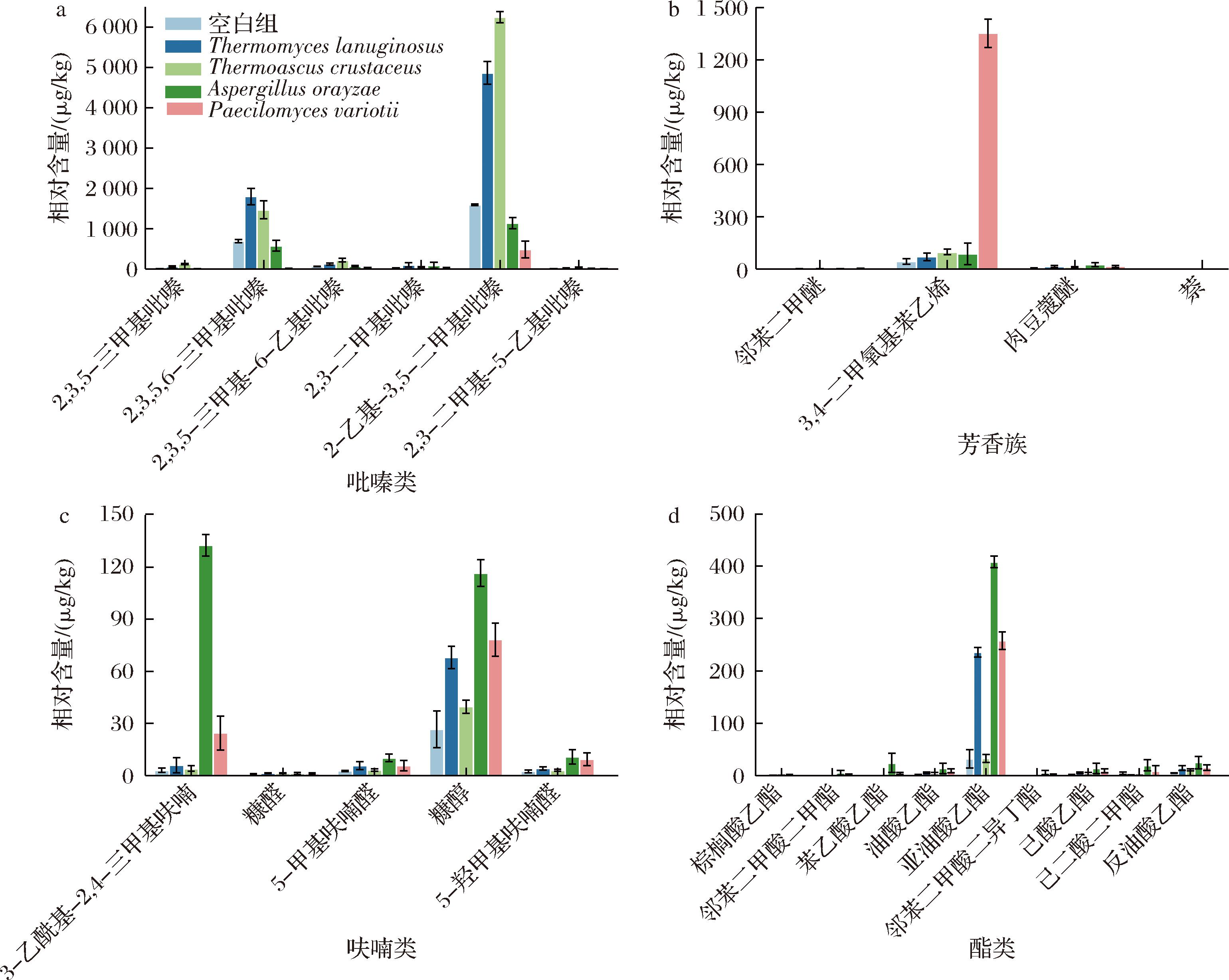
a-吡嗪类;b-芳香族;c-呋喃类;d-酯类
图5 主体丝状真菌的吡嗪类、芳香族、呋喃类和酯类化合物分析
Fig.5 Analysis of pyrazine, aromatic, furan, and ester compounds of dominant filamentous fungi
芳香族化合物在塑造酱香型白酒的风味方面有重要贡献[37]。如图4-b所示,在所有菌株中,Paecilomyces variotii合成芳香族类化合物的能力是最强的。本研究共检测到4种芳香族类化合物,其中3,4-二甲氧基苯乙烯相对含量最高。该化合物具有果皮、花朵、水果、杂草等风味特征,为酱香型白酒提供丰富的香气。值得注意的是,P.variotii产生的3,4-二甲氧基苯乙烯相对含量(1 352.93 μg/kg)显著高于其他主体菌株。这表明了P.variotii在酱香型白酒的风味形成过程中扮演着关键角色。
呋喃类和酯类化合物是酱香型白酒的特征化合物以及重要的呈香物质[39]。如图4-c、图4-d所示,A.orayzae合成呋喃类和酯类化合物的能力是最强的。呋喃类化合物具有较低的气味阈值和明显的特征,但现阶段对其风味贡献的研究相对较少,进一步从风味角度深入探究其功能显得尤为重要[40-41]。在本研究中,共检测到5种呋喃类化合物,其中,3-乙酰基-2,4-二甲基呋喃和糠醇的相对含量是最高的,糠醇具有咖啡、焦糖味、甜味、焦味等风味特征。A.orayzae的3-乙酰基-2,4-二甲基呋喃和糠醇相对含量高于其他主体菌株,分别为132.56、116.63 μg/kg。此外,A.orayzae合成亚油酸乙酯的能力显著强于其他主体菌株,其相对含量达到了408.09 μg/kg。亚油酸乙酯具有浓郁的果香味、脂肪香、甜香等风味特征,进一步丰富了酱香型白酒的风味复杂性。先前的研究也表明,以曲霉菌(Aspergillus)为核心的微生物群落主导了大曲中酯类物质合成的代谢网络[23, 42]。这些发现证实了曲霉菌(Aspergillus)在白酒酿造中的关键作用。
3 结论
本研究综合利用高通量测序、分离培养及原位模拟发酵,系统解析了大曲培养过程中主体丝状真菌的多样性及生香特征。研究结果表明,Thermoascus、Paecilomyces、Aspergillus、Thermomyces是高温大曲中的主体丝状真菌属。通过对这4种主体丝状真菌的分离鉴定以及形态学特征描述,揭示了不同菌株在温度、pH和碳源耐受性上的差异,并深入解析了它们在发酵过程中的生香特征。值得关注的是,T.lanuginosus和T.crustaceus在高温和低pH条件下表现出较强的适应性,且对高温大曲吡嗪类化合物的形成具有显著影响,P.variotii合成芳香族化合物的能力尤为突出,而A.orayzae合成呋喃类和酯类化合物能力尤为突出。本研究的发现不仅为高温大曲中主体丝状真菌的功能机制提供了理论依据,还为优化生产工艺和提升白酒品质提供了新思路和方法。未来的研究可进一步探索这些主体丝状真菌在白酒风味物质合成中的具体代谢途径及其调控机制。
[1] YANG L, FAN W L, XU Y.Qu-omics elucidates the formation and spatio-temporal differentiation mechanism underlying the microecology of high temperature Daqu[J].Food Chemistry, 2024, 438:137988.
[2] ZHENG X W, TABRIZI M R, ROBERT NOUT M J, et al.Daqu:A traditional Chinese liquor fermentation starter[J].Journal of the Institute of Brewing, 2011, 117(1):82-90.
[3] SHI W, CHAI L J, ZHAO H, et al.Deciphering the effects of different types of high-temperature Daqu on the fermentation process and flavor profiles of sauce-flavor Baijiu[J].Food Bioscience, 2024, 61:104917.
[4] LUO Y, WU L M, WU M Y, et al.Intelligent manufacturing challenges and directions of the Baijiu starter culture-Daqu industry:Microbiome and engineering perspectives[J].Trends in Food Science &Technology, 2024, 153:104724.
[5] DONG W W, YU X, WANG L Y, et al.Unveiling the microbiota of sauce-flavor Daqu and its relationships with flavors and color during maturation[J].Frontiers in Microbiology, 2024, 15:1345772.
[6] WANG X S, DU H, ZHANG Y, et al.Environmental microbiota drives microbial succession and metabolic profiles during Chinese liquor fermentation[J].Applied and Environmental Microbiology, 2018, 84(4):e02 369-17.
[7] CAI W C, XUE Y A, WANG Y R, et al.The fungal communities and flavor profiles in different types of high-temperature Daqu as revealed by high-throughput sequencing and electronic senses[J].Frontiers in Microbiology, 2021, 12:784651.
[8] SATAM H, JOSHI K, MANGROLIA U, et al.Next-generation sequencing technology:Current trends and advancements[J].Biology, 2023, 12(7):997.
[9] BHARTI R, GRIMM D G.Current challenges and best-practice protocols for microbiome analysis[J].Briefings in Bioinformatics, 2021, 22(1):178-193.
[10] ZHU Q, CHEN L Q, PU X X, et al.The differences in the composition of Maillard components between three kinds of sauce-flavor Daqu[J].Fermentation, 2023, 9(9):860.
[11] DENG L, MAO X, LIU D, et al.Comparative analysis of physicochemical properties and microbial composition in high-temperature Daqu with different colors[J].Frontiers in Microbiology, 2020, 11:588117.
[12] 马叶胜, 余苗, 王冕, 等.茅台镇8家酒企高温大曲的群落结构及其空间特征[J].轻工学报, 2023, 38(5):26-35.
MA Y S, YU M, WANG M, et al.Community structure and spatial characteristics of high-temperature Daqu in eight Baijiu companies in Maotai town[J].Journal of Light Industry, 2023, 38(5):26-35.
[13] GUAN T W, YANG H, OU M Y, et al.Storage period affecting dynamic succession of microbiota and quality changes of strong-flavor Baijiu Daqu[J].LWT, 2021, 139:110544.
[14] JIN Y, LI D Y, AI M, et al.Correlation between volatile profiles and microbial communities:A metabonomic approach to study Jiang-flavor liquor Daqu[J].Food Research International, 2019, 121:422-432.
[15] ZHANG Y D, DING F, SHEN Y, et al.Characteristics of the microbiota and metabolic profile of high-temperature Daqu with different grades[J].World Journal of Microbiology and Biotechnology, 2022, 38(8):137.
[16] 熊盈盈, 莫祯妮, 邱树毅, 等.未培养环境微生物培养方法的研究进展[J].微生物学通报, 2021, 48(5):1765-1779.
XIONG Y Y, MO Z N, QIU S Y, et al.Research progress on culture methods of uncultured environmental microorganisms[J].Microbiology China, 2021, 48(5):1765-1779.
[17] 贺奕森. 浓香型白酒大曲中霉菌的分离鉴定及应用[D].邯郸:河北工程大学, 2023.
HE Y S.Isolation, identification and application of mould in Daqu of Nongxiangxing Baijiu[D].Handan:Hebei University of Engineering, 2023.
[18] HUANG Y G, WU Q, XU Y.Isolation and identification of a black Aspergillus strain and the effect of its novel protease on the aroma of Moutai-flavoured liquor[J].Journal of the Institute of Brewing, 2014, 120(3):268-276.
[19] 何夷敏, 牟飞燕, 张维, 等.清香型白酒大曲中产酶产香霉菌的筛选、鉴定及耐受性研究[J].中国酿造, 2024, 43(11):58-63.
HE Y M, MOU F Y, ZHANG W, et al.Screening, identification and tolerance of enzyme and aroma-producing mold from light-flavor Baijiu Daqu[J].China Brewing, 2024, 43(11):58-63.
[20] 邓灿. 兼香型白酒不同品级高温大曲的特性分析及优势嗜热真菌功能研究[D].武汉:武汉轻工大学, 2022.
DENG C.Characteristics of high-temperature Daqu with different grades for Nongxiang-Jiangxiang Baijiu and the function of dominant thermophilic fungi[D].Wuhan:Wuhan Polytechnic University, 2022.
[21] BLATZER M, BEAUVAIS A, HENRISSAT B, et al.Revisiting Old Questions and New Approaches to Investigate the Fungal Cell Wall Construction[M].Fungal Cell Wall:An Armour and a Weapon for Human Fungal Pathogens, 2020.
[22] ANGULO V, BLEICHRODT R J, DIJKSTERHUIS J, et al.Enhancement of soil aggregation and physical properties through fungal amendments under varying moisture conditions[J].Environmental Microbiology, 2024, 26(5):e16627.
[23] ZHU M, DENG Z, TIE Y, et al.Unveiling the synthesis of aromatic compounds in sauce-flavor Daqu from the functional microorganisms to enzymes[J].Food Research International, 2024, 190:114628.
[24] WU S L, DU H, XU Y.Daqu microbiota adaptability to altered temperature determines the formation of characteristic compounds[J].International Journal of Food Microbiology, 2023, 385:109995.
[25] WEI J L, LU J, NIE Y, et al.Amino acids drive the deterministic assembly process of fungal community and affect the flavor metabolites in Baijiu fermentation[J].Microbiology Spectrum, 2023, 11(2):e0264022.
[26] ZHU M, ZHENG J, XIE J, et al.Effects of environmental factors on the microbial community changes during medium-high temperature Daqu manufacturing[J].Food Research International, 2022, 153:110955.
[27] YANG Y, NIU M S, YU H, et al.Exploring the contribution of temperature-adapted microbiota to enzyme profile of saccharification in Daqu using metagenomics and metaproteomics[J].LWT, 2024, 197:115916.
[28] 程爱芳, 邓政东, 陈文, 等.多粘类芽孢杆菌HD-1产纤维素酶的条件优化[J].食品工业科技, 2015, 36(10):173-177.
CHENG A F, DENG Z D, CHEN W, et al.Optimization of producing conditions of the cellulase from Paenibacillus polymyxa HD-1[J].Science and Technology of Food Industry, 2015, 36(10):173-177.
[29] 冯智伟, 郭松波, 孙朋朋, 等.酱香型白酒高温大曲贮曲过程理化性质与微生物演替规律分析[J].中国酿造, 2024, 43(9):44-49.
FENG Z W, GUO S B, SUN P P, et al.Analysis of physicochemical properties and microbial succession during storage process of high-temperature Daqu for sauce-flavor Baijiu[J].China Brewing, 2024, 43(9):44-49.
[30] WU S L, LU J, LI C W, et al.Pediococcus spp.- mediated competition interaction within Daqu microbiota determines the temperature formation and metabolic profiles[J].Applied and Environmental Microbiology, 2024, 90(4):e0179023.
[31] WANG Y, ZHOU W, TAO Y, et al.Profiling the global map of ester-producing metabolism and the response patterns of key genes to environmental factors during medium-high temperature Daqu production[J].Food Bioscience, 2024, 62:105462.
[32] 李涛, 万自然, 刘宇, 等.浓香型大曲生产过程中微生物及温度变化规律的研究分析[J].酿酒科技, 2023(2):53-56.
LI T, WAN Z R, LIU Y, et al.Change law of microorganisms and temperature during the production of Nongxiang Daqu[J].Liquor-Making Science &Technology, 2023(2):53-56.
[33] 薄涛, 吕娜, 杨凯环, 等.白酒大曲发酵过程中微生物群落及功能研究进展[J].食品科学, 2023, 44(19):385-393.
BO T, LÜ N, YANG K H, et al.Recent advances in understanding the composition and functions of microbial community in the fermentation of Baijiu Daqu[J]. Food Science, 2023, 44(19):385-393.
[34] YAN Y, CHEN S, NIE Y, et al.Quantitative analysis of pyrazines and their perceptual interactions in soy sauce aroma type Baijiu[J].Foods, 2021, 10(2):441.
[35] SHI W, CHAI L J, FANG G Y, et al.Spatial heterogeneity of the microbiome and metabolome profiles of high-temperature Daqu in the same workshop[J].Food Research International, 2022, 156:111298.
[36] 史洪丽, 余梦婷, 王世昕, 等.高温大曲中高产四甲基吡嗪芽孢杆菌的筛选及其在酒醅堆积中的应用[J].中国酿造, 2025, 44(3):59-65.
SHI H L, YU M T, WANG S X, et al.Screening of high yield tetramethylpyrazine Bacillus from high temperature Daqu and its application in the stacking of fermented grains[J].China Brewing, 2025, 44(3):59-65.
[37] 陈卓, 苏伟, 母应春, 等.洞酿酱香型白酒第三轮次酒醅发酵过程中微生物与挥发性风味物质相关性分析[J].中国酿造, 2024, 43(5):32-40.
CHEN Z, SU W, MU Y C, et al.Correlation analysis of microorganism and volatile flavor substance of the third round fermented grains of Dongniang sauce-flavor Baijiu during fermentation[J].China Brewing, 2024, 43(5):32-40.
[38] FAN W L, QIAN M C.Characterization of aroma compounds of Chinese “Wuliangye” and “Jiannanchun” liquors by aroma extract dilution analysis[J].Journal of Agricultural and Food Chemistry, 2006, 54(7):2695-2704.
[39] 何艳艳, 刘俊男, 李瑞杰, 等.酱香型白酒风味及其关键物质分析技术研究进展[J].中国酿造, 2024, 43(11):1-7.
HE Y Y, LIU J N, LI R J, et al.Research progress on the flavor and key substance analysis techniques of sauce-flavor Baijiu[J].China Brewing, 2024, 43(11):1-7.
[40] 杨亮, 何珺珺, 罗楚翔, 等.采用GC×GC-TOF-MS分析酱香型白酒缺陷酒挥发性风味物质[J].中国酿造, 2019, 38(8):67-72.
YANG L, HE J J, LUO C X, et al.Analysis of volatile flavor compounds from defective product of sauce-flavor Baijiu by GC × GC-TOF-MS[J].China Brewing, 2019, 38(8):67-72.
[41] WANG X X, FAN W L, XU Y.Comparison on aroma compounds in Chinese soy sauce and strong aroma type liquors by gas chromatography-olfactometry, chemical quantitative and odor activity values analysis[J].European Food Research and Technology, 2014, 239(5):813-825.
[42] WANG Y, QUAN S K, ZHAO Y J, et al.The active synergetic microbiota with Aspergillus as the core dominates the metabolic network of ester synthesis in medium-high temperature Daqu[J].Food Microbiology, 2023, 115:104336.