乳酸克鲁维酵母(Kluyveromyces lactis)是一种非常规酵母[1],被美国食品药品监督管理局认证为食品安全级(Generally Recognized As Safe,GRAS)微生物[2],其在有氧条件下不受克雷布斯效应(Crabtree effect)影响,能够实现更高的生物量积累[3]。因此,在工业生产中更具适用性。此外,该酵母在异源蛋白表达方面也表现出多项优势[4],包括强大的蛋白分泌能力、适度的糖基化修饰、高效的整合表达能力及优异的大规模发酵能力等,在合成生物学和代谢工程领域具有广泛应用前景[5]。
启动子是一段位于基因上游的DNA序列,能够与RNA聚合酶和转录因子结合,启动基因转录[6]。作为基因表达调控的关键元件,其活性直接影响目标基因的转录效率、蛋白表达水平及代谢途径的效率[7]。目前,乳糖诱导型启动子PLAC4是K.lactis中应用最广泛的启动子,此外,PPHO5、PADH4、PPDC1和PGAL7等内源启动子也已用于K.lactis中基因的表达调控[8]。然而,与酿酒酵母等常规酵母相比,K.lactis中已报道的内源启动子数量仍然有限[9],这限制了其在外源蛋白高效表达等生物合成中的应用。因此,筛选挖掘K.lactis高效内源启动子,对于构建高效微生物细胞工厂具有重要的意义[10]。
近年来,转录组学等高通量测序技术的发展为启动子的筛选和鉴定提供了新的工具[11]。通过微生物转录组分析可有效筛选出具有不同表达水平的启动子[12]。GAO等[13]基于酿酒酵母RNA-Seq数据,筛选了66个天然启动子并用于基因调控表达,使得(2S)-柚皮素的产量达到1.21 g/L。然而,天然启动子的强度和调控特性往往难以满足高效表达的需求,因此,启动子工程成为优化启动子元件的重要策略[14]。启动子工程是指通过理性设计或定向进化等方法对启动子序列进行改造,以提高其表达强度或优化其调控特性[15]。合成启动子通过重组核心启动子、上游激活序列(upstream activation sequence,UAS)[16]、增强子或转录因子结合位点,实现基因表达精确调控,是启动子工程的重要策略[17]。例如,BASSETT等[18]通过碳源响应元件筛选、合成启动子设计,构建了新型杂合启动子,并应用于β-胡萝卜素高效生物合成。LAI等[19]通过随机杂交和高通量筛选构建了一个梯度强度的启动子文库,并利用上游调控序列对PGAP1和PENO1启动子进行改造,实现了在毕赤酵母中基因表达的精细调控。
本研究基于K.lactis不同生长阶段的转录组分析,利用绿色荧光蛋白(green fluorescent protein,GFP)和乳糖酶作为报告基因,对K.lactis内源启动子进行筛选表征,获得了60个不同表达水平的内源启动子。通过启动子功能区域预测与截短实验,对6个强启动子的核心区域和UAS进行分析并构建杂合启动子,进一步提高转录表达水平。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株及质粒
本文所涉及到的K.lactis GG799、大肠杆菌(Escherichia coli) JM109、pUDP025质粒均为实验室保藏。
1.1.2 主要试剂
山梨醇、酵母粉、质粒抽提试剂盒、葡萄糖、PCR产物纯化试剂盒、蛋白胨、二硫代苏糖醇溶液、醋酸锂、氨苄青霉素、邻硝基苯酚-β-D-吡喃半乳糖苷(o-nitrophenyl-β-D-galactopyranoside,ONPG)、邻硝基苯酚(2-nitrophenol,ONP)、潮霉素B,生工生物工程(上海)股份有限公司;NaCl、MgSO4·7H2O、KH2PO4、K2HPO4、Tris-HCl溶液、乙二胺四乙酸二钠(ethylenediaminetetraacetic acid disodium salt,EDTA-2Na),上海国药集团;DNA Marker、2×Phanta Max Master Mix(Dye Plus),南京诺唯赞生物科技股份有限公司。
1.1.3 培养基及相关溶液
LB培养基(g/L):NaCl 10,蛋白胨10,酵母粉5。固体培养基中添加20的琼脂粉。主要用于质粒的构建。
YPD培养基(g/L):葡萄糖20、酵母粉10、蛋白胨20。固体培养基中添加20的琼脂粉。
酵母处理液:称取0.66 g醋酸锂、10 mL Tris-HCl溶液(pH 7.5)、109.3 g山梨醇溶于1 L去离子水,过滤除菌。
山梨醇溶液:称取72.87 g山梨醇溶于300 mL去离子水,定容至400 mL,115 ℃灭菌20 min备用。
PBS(pH 7.5):称取2.2 g Na2HPO4、0.2 g NaH2PO4、8.5 g NaCl,溶于900 mL去离子水,定容至1 L。
磷酸缓冲液(pH 6.5):称取KH2PO4 8.8 g和K2HPO4 8.0 g,0.25 g MgSO4·7H2O和18.6 mg EDTA-2Na于900 mL水中,定容至1 L;用盐酸或NaOH调节pH值至6.5±0.05。
Na2CO3终止剂:称取50 g Na2CO3和37.2 g EDTA-2Na于900 mL水中,将溶液定容至1 L,混合均匀,备用;
ONPG溶液:称取0.25 g ONPG,溶于80 mL磷酸缓冲液(pH 6.5),定容至100 mL。
ONP溶液:称取0.139 g ONP溶于10 mL体积分数95%乙醇溶液,定容至1 L,得到1 mmol/L的ONP标准溶液。
1.2 仪器和设备
BG-gdsAUTO凝胶成像分析系统,上海贝晶生物技术有限公司;Gene Pulser Xcell电转仪,伯乐生命医学产品(上海)有限公司;pH计,美国Ohaus公司;PCR仪、5804R台式高速冷冻离心机、5418高速离心机、移液枪、分析天平,德国Eppendorf公司;Synergy H1/Synergy2酶标仪,美国Biotek公司;DYY-6C型电泳仪,北京市六一仪器厂。
1.3 实验方法
1.3.1 启动子初筛
在YPD培养基中培养野生型菌株GG799,并在菌株生长的指数期(GG799_1)和稳定期(GG799_2)取样,对收集的酵母细胞送至生工生物工程(上海)有限公司进行RNA-Seq分析,进而基于样本中基因的TPM(transcripts per million)值筛选内源启动子。TPM是样本间基因表达水平估算的方法之一[20],通过TPM值,能够更可靠地比较不同样本之间的基因表达水平[21]。本研究对2组样本中所有基因的TPM值进行降序排列,去除重复基因及无注释基因后,选择排名靠前的60个基因进行后续评价。
1.3.2 质粒构建
本研究中所使用的主要菌株、质粒与引物如表1和表2所示。引物合成由生工生物工程(上海)有限公司完成,质粒测序由苏州金唯智生物科技有限公司完成。
表1 主要菌株和质粒
Table 1 Main strains and plasmids
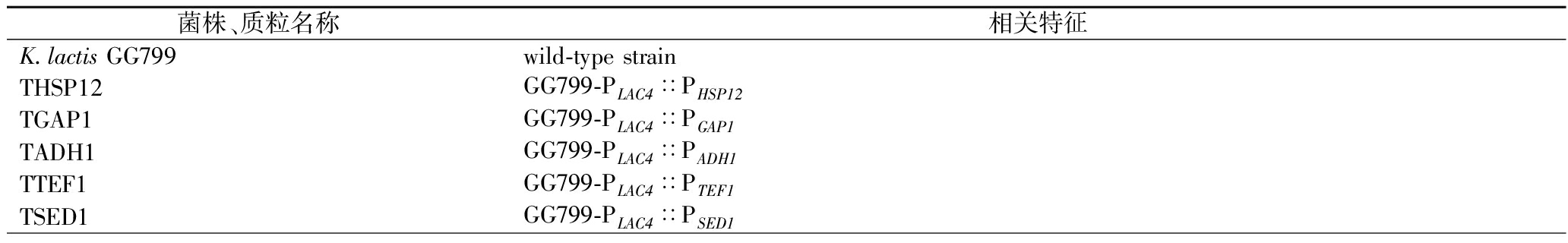
菌株、质粒名称相关特征K.lactis GG799wild-type strainTHSP12GG799-PLAC4∷PHSP12TGAP1GG799-PLAC4∷PGAP1TADH1GG799-PLAC4∷PADH1TTEF1GG799-PLAC4∷PTEF1TSED1GG799-PLAC4∷PSED1
续表1

菌株、质粒名称相关特征TSSA2GG799-PLAC4∷PSSA2ZX(X:Corresponding gene name)GG799 containing pUDP025-UX-CTEF1-GFPBXGG799 containing pUDP025-UX-UTEF1-CTEF1-GFPTZGAP1GG799-PLAC4∷UGAP1-CTEF1TZTEF1GG799-PLAC4∷UTEF1-CTEF1TBHSP12GG799-PLAC4∷UHSP12-UTEF1-CTEF1pUDP025-PHSP12Carrying PHSP12-GFP-TScPHO5pUDP025-PGAP1Carrying PGAP1-GFP-TScPHO5pUDP025-PADH1Carrying PADH1-GFP-TScPHO5pUDP025-PTEF1Carrying PTEF1-GFP-TScPHO5pUDP025-PSED1Carrying PSED1-GFP-TScPHO5pUDP025-PSSA2Carrying PSSA2-GFP-TScPHO5pT-DonorCarrying Donor DNApC9 sgR-PLAC4Cas9-sgRNA-PLAC4pUDP025-CHSP12From pUDP025-PHSP12, carrying CHSP12-GFP-TScPHO5(CHSP12:the core promoter sequence of PHSP12)pUDP025-CGAP1From pUDP025-PGAP1, carrying CGAP1-GFP-TScPHO5(CGAP1:the core promoter sequence of PGAP1)pUDP025-CADH1From pUDP025-PADH1, carrying CADH1-GFP-TScPHO5(CADH1:the core promoter sequence of PADH1)pUDP025-CTEF1From pUDP025-PTEF1, carrying CTEF1-GFP-TScPHO5(CTEF1:the core promoter sequence of PTEF1)pUDP025-CSED1From pUDP025-PSED1, carrying CSED1-GFP-TScPHO5(CSED1:the core promoter sequence of PSED1)pUDP025-CSSA2From pUDP025-PSSA2, carrying CSSA2-GFP-TScPHO5(CSSA2:the core promoter sequence of PSSA2)
表2 本研究涉及的主要引物
Table 2 Main primers involved in this study

引物名称引物序列 (5′~3′)PHSP12-FACCAGCCTAAGAATGTTCAAGACTTCCATCTTGTTCGGATTTGATAATGTCAPHSP12-RGTTCTTCTCCCTTACCCATTTTTATTATTAGTGTTTGTGTGTGTTTTGTATTGGATAACPGAP1-FACCAGCCTAAGAATGTTCAACGTAAAAACTAAAACGAGCCCCCACPGAP1-RAGTTCTTCTCCCTTACCCATTGTGTAATATTCTTTTTTTTTACTTGAAACTGTGAAGCPADH1-FACCAGCCTAAGAATGTTCAACCATTGGGTTTTTGTCCTCTTTTTAGGGPADH1-RTTCTTCTCCCTTACCCATTTTATCTTTTTTTAGTATAGAGTTTGTGTGTTTAAAGCTTGPTEF1-FACCAGCCTAAGAATGTTCAAGAGCCTGTCCAAGCAAATGCCPTEF1-RTCTTCTCCCTTACCCATTTTTAATGTTACTTCTCTTGCAGTTAGGGAACTATAATGTAAPSED1-FACCAGCCTAAGAATGTTCAAAACCAAAAGAGAGATCATGGAAATPSED1-RAGTTCTTCTCCCTTACCCATTTTTTGCAGTATTTCTTTATTGATGAACPSSA2-FACCAGCCTAAGAATGTTCAAAGATTTATTGACACTTTGGTATCCGACAACCPSSA2-RTTCTTCTCCCTTACCCATTATAATTTCGTTTGTATGTTATTTGATAATGTGGGGTTTCCpUDP025-GFP-FATGGGTAAGGGAGAAGAACTTTTCACTpUDP025-GFP-RTTGAACATTCTTAGGCTGGTCGAATCATTTDonor-Homology arm-L-FGCGCGGATCTTCCAGAGATACCAAAAACAAACAAGGAGAACTGTTCGDonor-Homology arm-L-RTCGCCCGCCTCACACDonor-PHSP12-FTATGTGTGTGAGGCGGGCGAGCTCAAAATATTTTCAAAGTTTTGCAGCCTCDonor-PHSP12-RAGGAATAAGGCAAGACATTTTTATTATTAGTGTTTGTGTGTGTTTTGTATTGGATAACCDonor-Homology arm-R-FATGTCTTGCCTTATTCCTGAGAATTTAAGGAACDonor-Homology arm-R-RGCACGCCTGCCGTTCGACGACCACTTGTCTGAAACCAACATGGT-Donor-FTCGTCGAACGGCAGGCT-Donor-RTATCTCTGGAAGATCCGCGCGCHSP12-FACCAGCCTAAGAATGTTCAAAACCAAAAAGTATATAAGCAGACTCTTCGAP1-FACCAGCCTAAGAATGTTCAAAATTTTGATATATAAAGGGTGGATCTTTTTCCADH1-FACCAGCCTAAGAATGTTCAAGGAATATGTATATAAACACCCGGTCCTEF1-FACCAGCCTAAGAATGTTCAAGAATTTTGAATATAAAAGGAGATCGAAAAAATTTCSED1-FACCAGCCTAAGAATGTTCAAGACTGAAAAGTATATAAGGCATTGGTCSSA2-FACCAGCCTAAGAATGTTCAAAATAGAATTATATAAAAAGAGACAGATTCAGTGApUDP025-C-RTTGAACATTCTTAGGCTGGTC
启动子筛选质粒的构建:将所筛启动子以GG799基因组为模板,采用表2中引物进行扩增后,连接到带有GFP的pUDP025质粒上构建重组载体。6个强启动子所转录基因的Gene ID及6个启动子序列的起始终止位点信息:PHSP12(Gene ID:2893432;656 256~657 623)、PGAP1(Gene ID:2894950;1 960 417~1 962 406)、PADH1(Gene ID:2895056;1 961 951~1 964 003)、PTEF1(Gene ID:2897093;787 497~789 873)、PSED1(Gene ID:2893936;116 315~117 800)、PSSA2(Gene ID:2893121;362 732~365 654)。
核心启动子筛选质粒的构建:以前期构建好的启动子筛选质粒为模板,保留包含SoftBerry网站预测的转录起始复合物(pre-initiation complex,PIC)结合序列及其下游序列,去除PIC结合序列上游的其余序列。6个核心启动子序列的起始终止位点信息:CHSP12(656 256~656 733)、CGAP1(1 960 417~1 961 625)、CADH1(1 962 766~1 964 003)、CTEF1(787 497~789 079)、CSED1(116 315~116 998)、CSSA2(363 396~365 654)。
截短启动子的构建:以前期构建好的启动子筛选质粒为模板,以每个启动子的5′端为起点,按照每100 bp的间隔进行截短,构建一系列截短启动子片段,设计引物进行质粒构建。经分析得到的6个启动子的UAS的起始终止位点信息:UHSP12(656 977~657 376)、UGAP1(1 962 107~1 962 306)、UADH1(1 962 151~1 962 450)、UTEF1(789 080~789 173;789 774~789 873)、USED1(117 101~117 400)、USSA2(363 232~363 331)。
启动子整合表达质粒的构建:包括带有Cas9蛋白的pUDP025质粒及带有供体DNA的T载质粒的构建。将sgRNA设计在引物同源臂上,以带有Cas9蛋白的pUDP025质粒为模板进行构建;以GG799基因组和启动子筛选质粒为模板,设计引物,通过同源重组将同源臂及启动子连接到T载质粒上进行测序及保存。
1.3.3 K.lactis感受态细胞的制备与转化
挑取GG799单菌落接种于3 mL YPD液体培养基中,置于30 ℃、220 r/min摇床培养12 h。按照1%接种量,将种子液接种至50 mL液体YPD培养基,在30 ℃、220 r/min条件下培养。当菌体浓度培养至OD600值达到0.8~1时,将菌液转移至50 mL无菌离心管,冰浴15 min后,于4 ℃、4 000 r/min离心5 min,弃上清液。接着,向沉淀中加入7 mL酵母处理液和40 μL 2 mol/L二硫代苏糖醇溶液,置于室温反应20 min后,于4 ℃、4 000 r/min离心5 min,弃上清液。然后,加入5 mL预冷的1 mol/L山梨醇溶液重悬菌体,于4 ℃、4 000 r/min离心5 min,弃上清液,此洗涤步骤重复一次。随后,在沉淀中加入1 mL 1 mol/L山梨醇溶液重悬菌体,取75 μL菌悬液分装至预冷的1.5 mL离心管中,然后加入质粒及同源片段,用移液枪轻轻吹打混匀,冰浴15 min。最后,将菌液吸取至预冷的2 mm电转杯中,在1.5 kV、200 Ω条件下电击5 ms后,用1 mL 1 mol/L山梨醇溶液将电转杯中菌液全部洗出至1.5 mL离心管中。转化结束,将离心管置于30 ℃、220 r/min摇床中培养1 h后涂布至带有潮霉素抗性的选择培养基平板上,接着将平板放置于30 ℃培养箱培养3~4 d后挑取单菌落进行验证。
1.3.4 培养条件及荧光检测
孔板初筛:将验证成功的重组菌株接种至96深孔板中,30 ℃、220 r/min培养24 h后,接着以5%的接种量取40 μL种子液转接至含有760 μL YPD培养基的96深孔板中,30 ℃、220 r/min 培养24 h后,取200 μL样品至黑色微孔板中,用酶标仪在激发波长为488 nm,发射波长为520 nm条件下测菌体荧光。
摇瓶培养:将重组菌株接种于3 mL YPD液体培养基中,在30 ℃、220 r/min的摇床中过夜培养。接着,取适量种子液转接于50 mL液体YPD培养基至菌液初始OD600值约为0.25,在条件为30 ℃、220 r/min的摇床中培养48 h后取样,弃上清液。随后,加入1 mL PBS(pH 7.5)重悬后离心,重复以上操作1次后用PBS重悬,并将菌液OD600值稀释至0.2~0.8。最后,取200 μL稀释菌液转移到黑色微孔板中,用酶标仪在激发波长为488 nm,发射波长为520 nm条件下测量GFP的荧光,并在600 nm条件下测量菌体浓度。GFP的相对强度用GFP荧光/OD600表示,以带有空质粒的重组菌株为阴性对照,每个样品至少有3个生物学重复。
1.3.5 乳糖酶粗酶液制备
取1 mL发酵48 h的发酵液,离心1 min后保留菌体,接着用1 mL的PBS(pH 7.5)将菌体重悬。随后取500 μL菌悬液至破碎管,加入0.5 mm玻璃珠,冰预30 min后,用FastPrep-24进行破碎。最后使用冷冻离心机在4 ℃、7 000 r/min下离心10 min,收集上清液即为胞内粗酶液。
1.3.6 乳糖酶活性测定方法
标准曲线绘制:取ONP溶液2、4、6、8、10、12、14 mL 于100 mL容量瓶中,加入25 mL Na2CO3溶液,用磷酸缓冲液(pH 6.5)定容至刻度,混匀,此时其中ONP的浓度分别为0.02、0.04、0.06、0.08、0.10、0.12、0.14 μmol/mL,420 nm处测量吸光值,以ONP浓度为X轴,吸光值为Y轴,绘制标准曲线y=4.294 53x,R2=0.999 98。取0.1 mL待测酶液,加入0.5 mL ONPG溶液,30 ℃水浴10 min后加入0.2 mL Na2CO3终止剂终止反应,在420 nm处测定吸光值。根据美国食品化学法典乳糖酶定义,1个中性乳糖酶单位为在30 ℃、pH 6.5条件下反应10 min,单位时间内释放1 μmol ONP的酶量。按公式(1)计算:
乳糖酶活力![]()
(1)
式中:ΔA420,反应体系的吸光值;A0,对照组的吸光值;V,反应体系总体积,mL;n,稀释倍数;K,标准曲线斜率;t,反应时间,min;V1,酶液体积,mL。
1.4 数据处理
实验数据结果以“平均值±标准差”表示。利用Origin 2024软件对数据进行统计和方差分析。
2 结果与分析
2.1 基于转录组分析筛选K.lactis内源启动子
为了扩展K.lactis的启动子库,本研究基于RNA-Seq分析获得60个TPM值较高的基因。为更清晰地展示这些基因在2个样本中的表达差异,将60个基因的TPM值进行标准化处理(图1)。结果显示,约1/3的基因呈现出较高的表达水平,其中,HSP12和GAP1的TPM值在2个样本中均显著高于其他基因,说明基因HSP12和GAP1的启动子在指数期和稳定期可能均具有较高的转录活性。为评价60个基因所对应启动子的转录水平,并便于后续基因表达盒的构建,将基因编码区上游1 000 bp的序列设定为K.lactis的启动子关联区域,并基于此构建了K.lactis内源启动子文库。
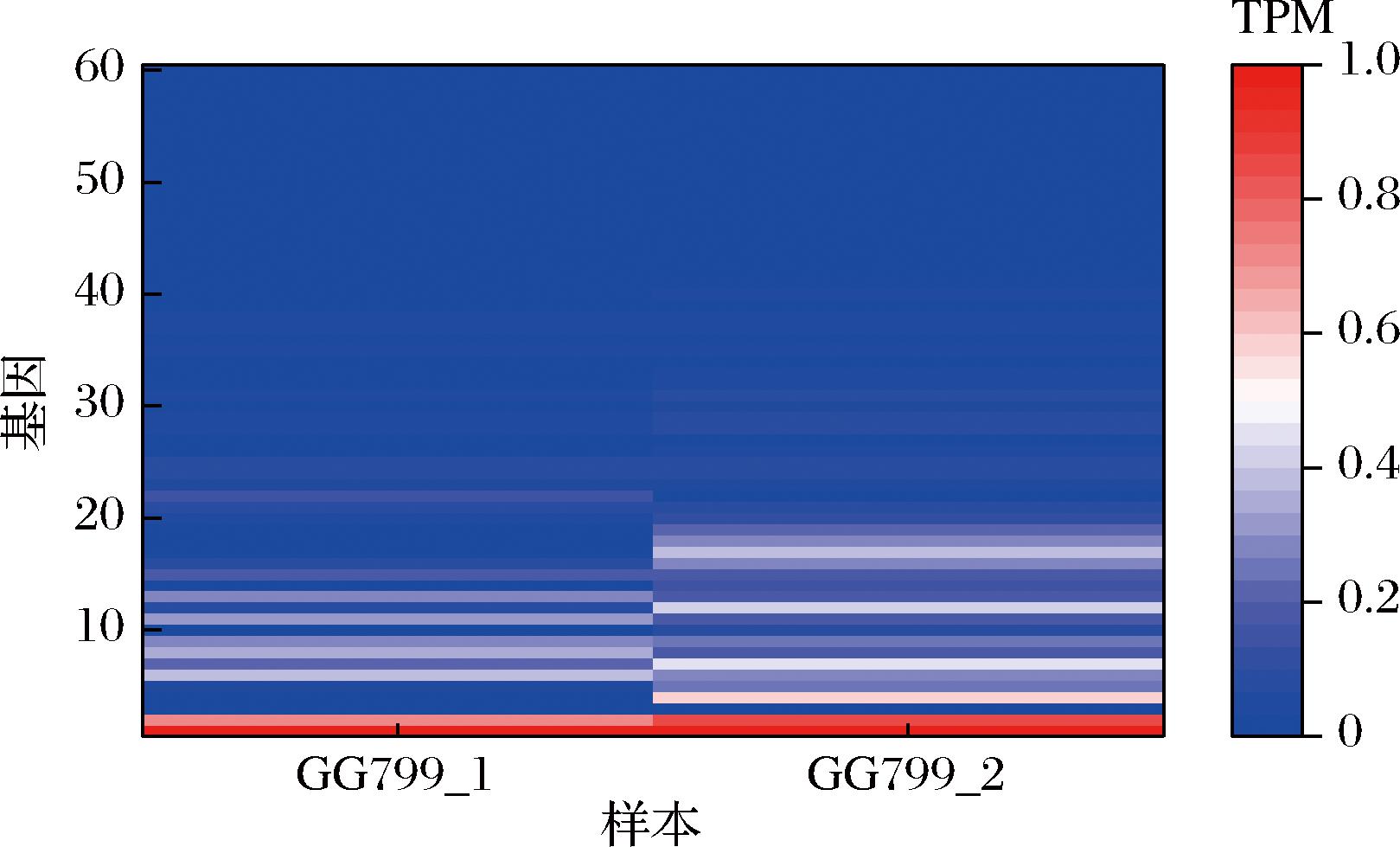
图1 基于TPM值的K.lactis内源启动子分析与筛选
Fig.1 Analysis and screening of endogenous promoters in K.lactis based on TPM value
2.2 内源启动子的荧光评价
为评估60个启动子的转录水平并筛选K.lactis的内源强启动子,首先利用GFP作为报告基因,在96孔板中对启动子表达水平进行初步表征。以酿酒酵母中广泛使用的强启动子PScTEF1作为对照,在发酵24 h后测定各启动子表达GFP的荧光强度。如图2-a所示,60个启动子的荧光强度存在显著差异,其中,有21个启动子的荧光强度高于异源启动子PScTEF1。
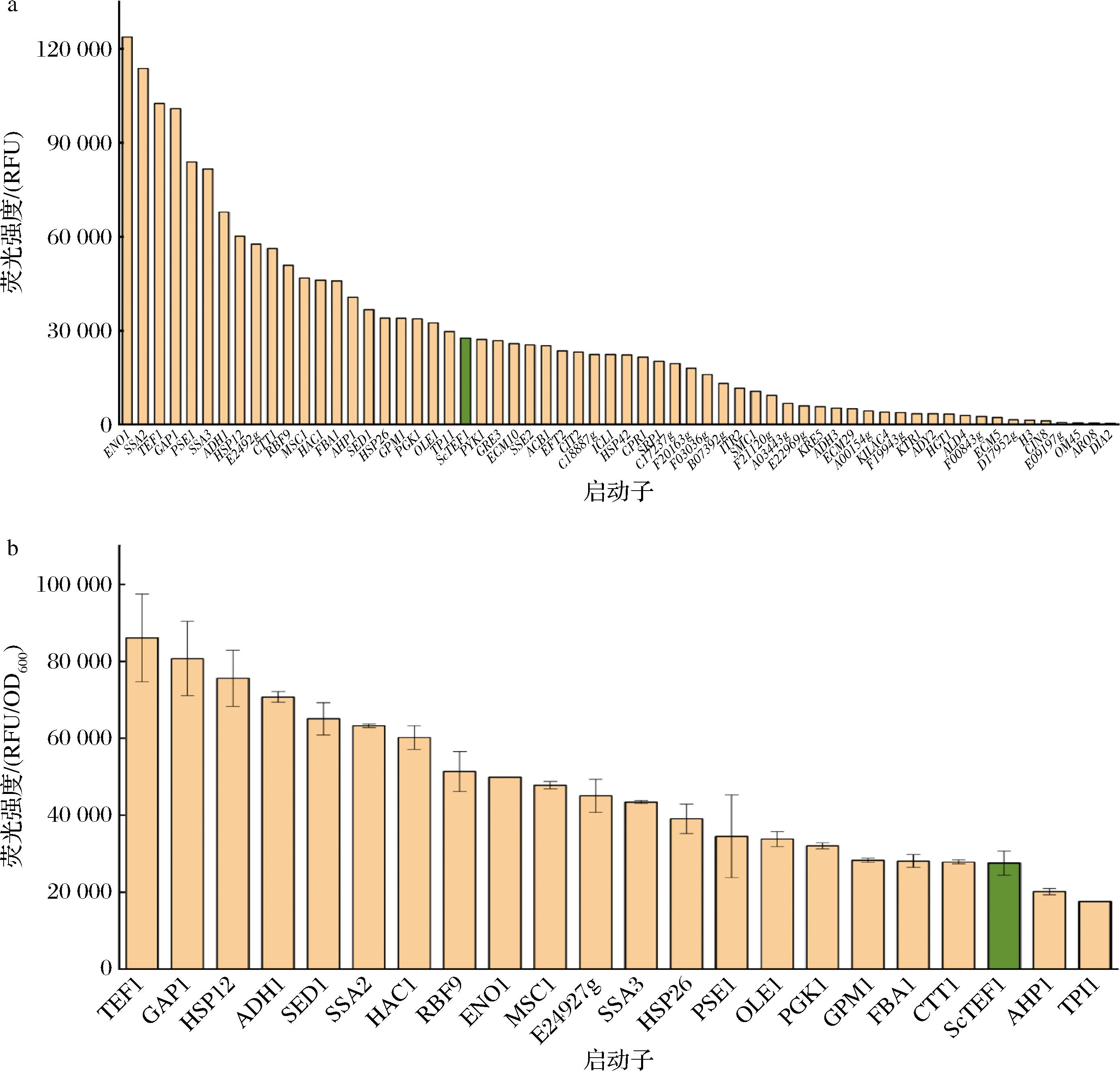
a-启动子孔板初筛;b-启动子摇瓶复筛
图2 内源启动子的荧光筛选
Fig.2 Fluorescent screening of endogenous promoters
为进一步验证筛选启动子的可靠性,对21个荧光强度较高的启动子进行摇瓶复筛(方法见1.3.4节)。结果显示,大多数启动子的荧光表达水平仍显著高于对照PScTEF1(图2-b),证实了初筛结果的稳定性。其中,6个启动子(PHSP12、PGAP1、PADH1、PTEF1、PSED1和PSSA2)表达的GFP荧光强度达到PScTEF1的2.3倍以上。因此,基于转录组数据筛选不同转录水平启动子具有可行性。
2.3 内源强启动子在乳糖酶表达中的应用
为评价启动子对不同基因的表达水平,选取K.lactis内源乳糖酶基因LAC4作为报告基因,并选择荧光强度最高的6个启动子(PHSP12、PGAP1、PADH1、PTEF1、PSED1和PSSA2)在基因组上进行替换整合,评价其对乳糖酶表达的影响。结果显示,启动子PHSP12、PGAP1、PADH1和PTEF1表达的乳糖酶活力分别是天然启动子PLAC4的5.2、3.4、2.3和2.2倍(图3)。其中,TPM值最高的基因HSP12与GAP1对应的启动子表达的乳糖酶活力最高,进一步证实了基于RNA-Seq分析筛选内源强启动子的有效性。但是,研究也发现同一启动子在质粒和基因组上的相对转录水平存在差异,这种差异可能源于基因组中周围基因的调控作用或染色质状态的差异,导致启动子在不同基因组位置中的转录活性发生变化[22]。
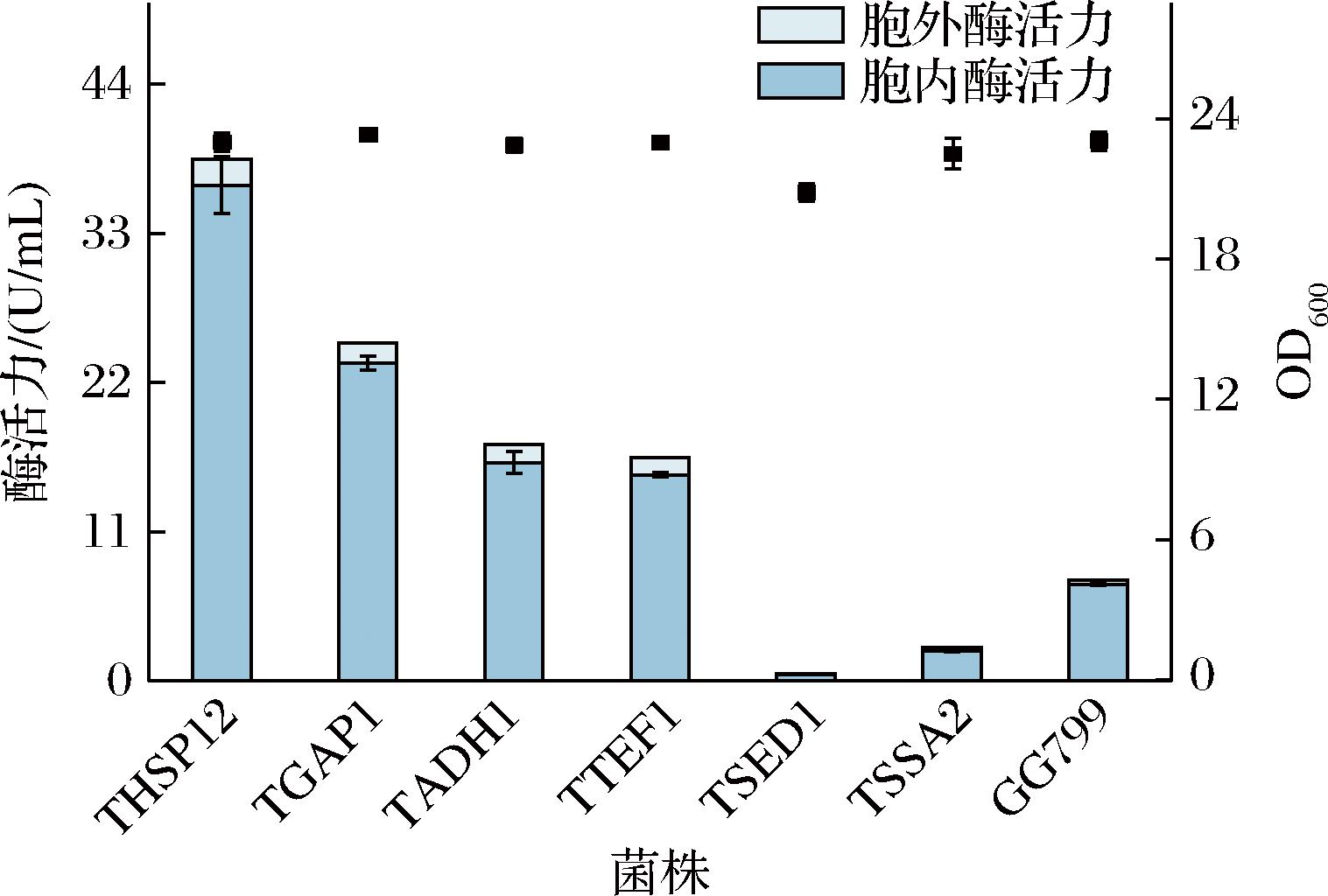
图3 重组菌株乳糖酶活力
Fig.3 Activity of lactase in recombinant strains
2.4 强启动子的核心启动子区域分析
酵母的启动子包含多个必要元件,如核心启动子区域、UAS、上游抑制序列等,以实现转录的精确调控。核心启动子是与RNA聚合酶Ⅱ和其他常见转录因子直接作用以形成PIC从而启动转录的核苷酸序列。UAS位于核心启动子的上游,主要为特定转录激活因子提供结合位点,是增强基因表达的启动子关键区域[23]。本研究将对前期筛选出的6个强启动子进行分区域分析及筛选,得到6个强启动子的功能元件(核心启动子及UAS)。
为分析6个强启动子的核心启动子区域,基于生物信息学软件对其核心启动子区域进行预测,确定了各启动子的TATA框及PIC结合序列(图4-a)。为系统评估核心启动子的转录起始效率,本研究将预测的PIC区域及其下游序列定义为核心启动子功能域(方法1.3.2节),并通过GFP报告基因进行转录活性定量分析。结果表明,不同核心启动子的驱动效率存在显著差异(图4-b)。其中,PTEF1来源的核心启动子CTEF1表现出最高转录活性,可作为后续杂合启动子构建的基础结构。
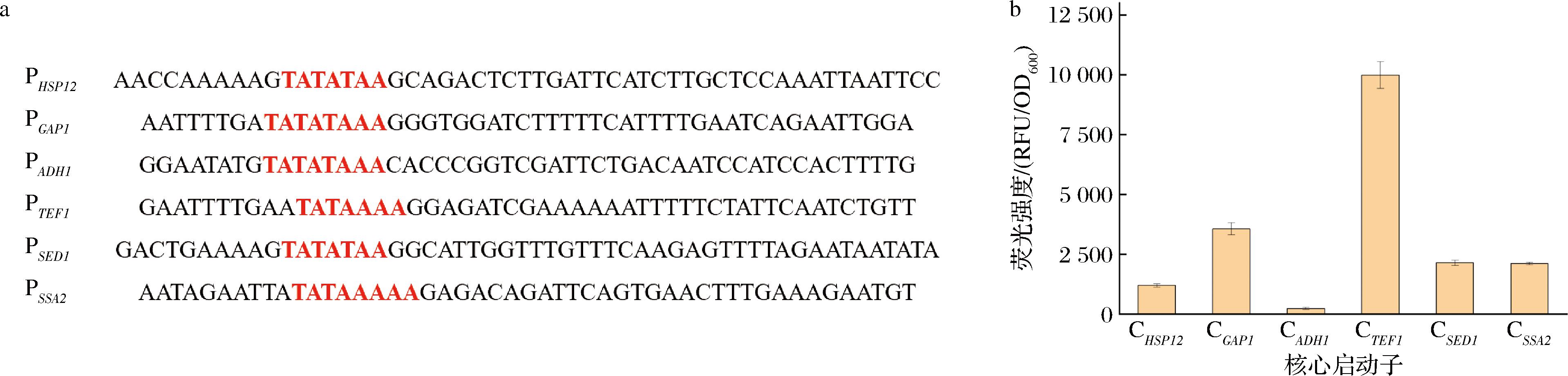
a-6个启动子的PIC结合序列;b-6个核心启动子在重组菌株中的荧光强度比较
图4 核心启动子分析
Fig.4 Analysis of core promoters
2.5 强启动子的UAS的定位
为进一步解析6个强启动子的UAS区域,采用将每个启动子逐步截短的方法对UAS进行定位。通过将6个强启动子分别从5′端向3′端方向,以每100 bp的间隔进行截短,获得6组不同长度的启动子序列,通过与GFP融合构建质粒进行验证。
从整体来看,随着启动子序列的逐步截短,各组GFP的荧光强度呈下降趋势。由此可推测,通过比较不同长度启动子驱动GFP表达所产生的荧光强度变化,可用于初步定位UAS所在的区域。以PSSA2为例(图5-f):以5′端为起点,截掉600 bp后的启动子JD-PSSA2-400所表达的GFP荧光强度较截掉500 bp后的启动子JD-PSSA2-500显著降低,且JD-PSSA2-500所表达的GFP荧光强度不低于截短前,表明在这100 bp内可能存在PSSA2的UAS。以上述方法分析6组截短启动子表达GFP的荧光强度变化,得到6个强启动子UAS的所在区间序列(序列见方法1.3.2节)。
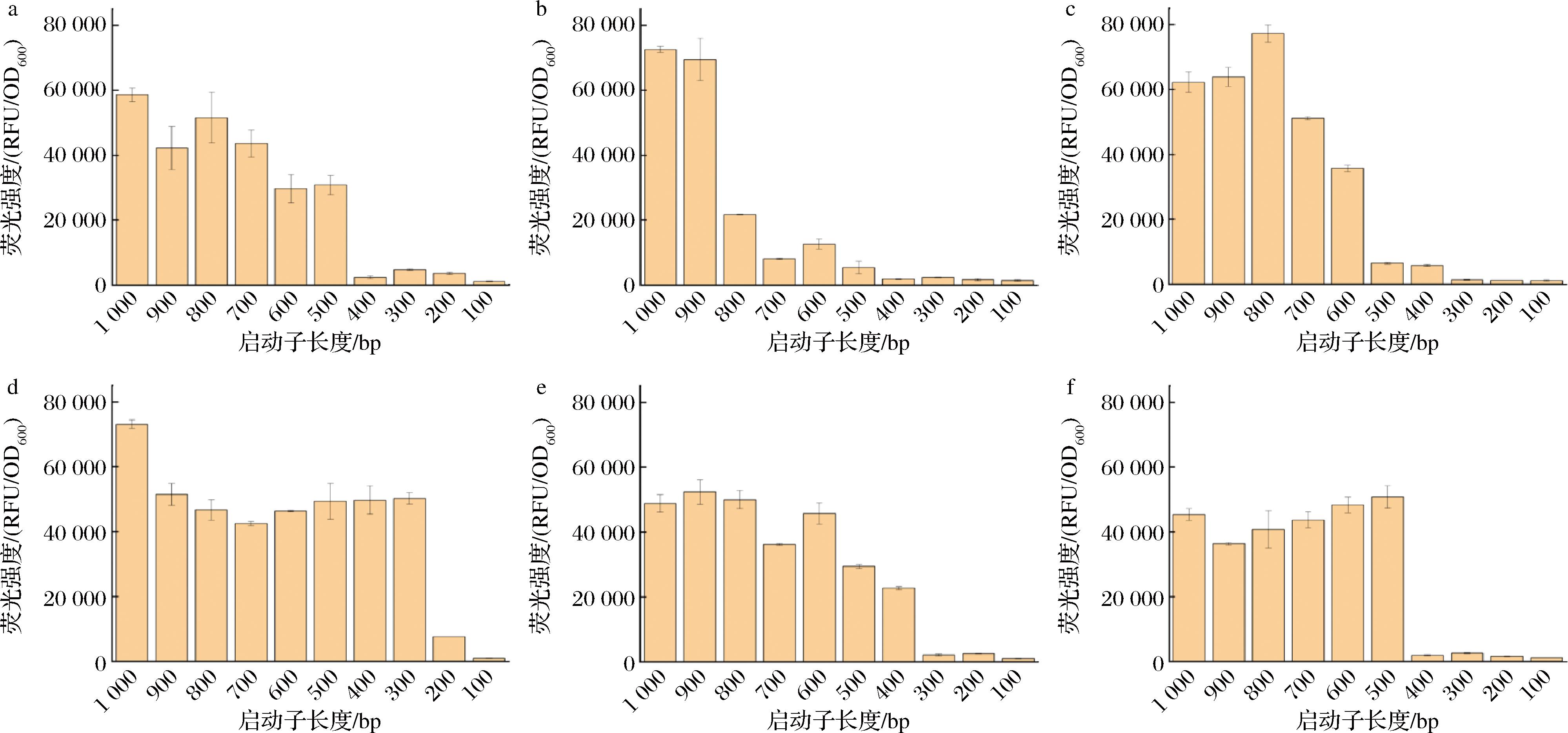
a-JD-PHSP12;b-JD-PGAP1;c-JD-PADH1;d-JD-PTEF1;e-JD-PSED1;f-JD-PSSA2
图5 不同截短启动子的荧光表达水平
Fig.5 Fluorescent expression levels of different truncated promoters
2.6 杂合启动子的构建与评价
将UAS与强核心启动子杂交以增强转录活性是合成生物学中的常见策略[23]。然而,本研究中筛选得到的UAS是否具有通用性仍需进一步探究。为验证UAS的增强作用是否依赖于其自身核心启动子,将各UAS分别与核心启动子CTEF1组合构建杂合启动子UASX-CTEF1(图6),并利用GFP进行评价。可以看到,6个杂合启动子所表达的荧光强度明显高于核心启动子CTEF1,证明6个UAS皆有较强的增强效果。这一结果表明,这些UAS区域对其自身核心启动子无严格依赖性,在K.lactis中可能具有一定的通用性,而非仅限于其自身的核心启动子。
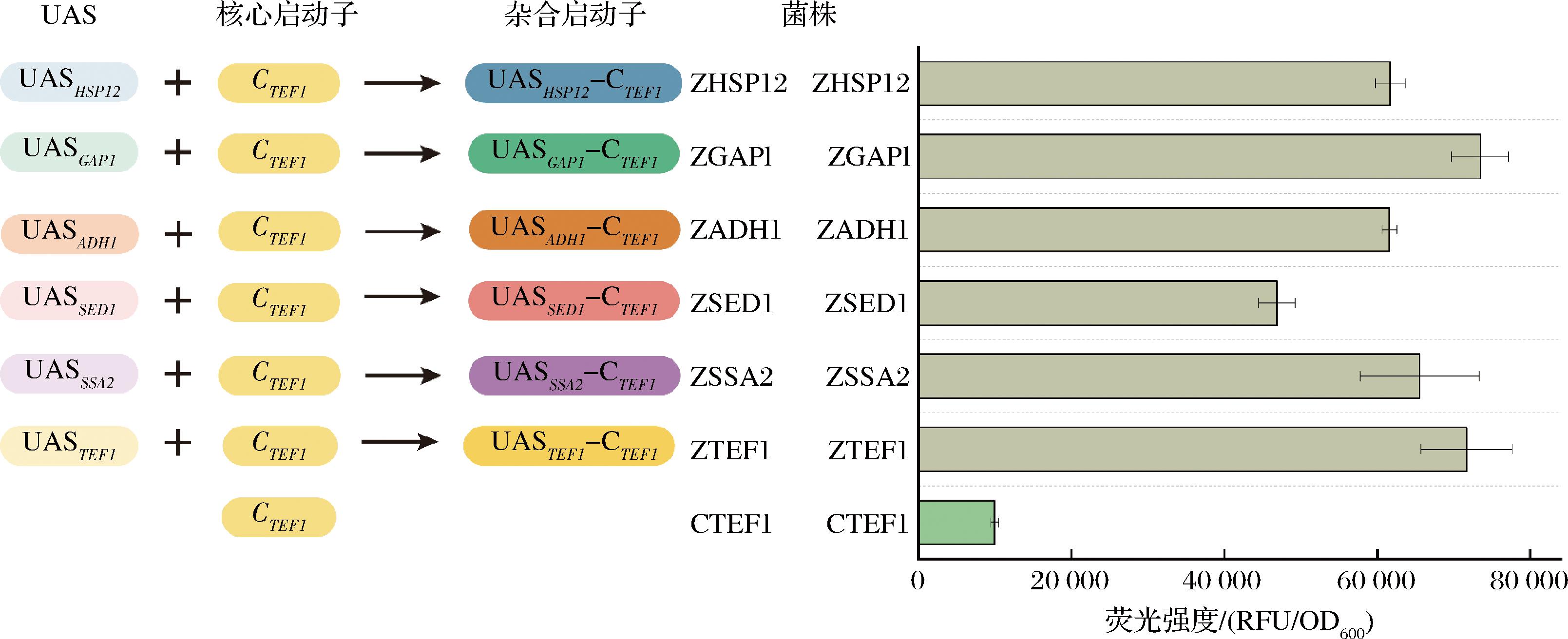
图6 杂合启动子构建示意图及荧光测定
Fig.6 Construction diagram and fluorescence determination of hybrid promoters
2.7 UAS串联杂合启动子的构建与评价
为进一步筛选表达水平更强的杂合启动子,本研究选择图6中表达荧光强度最强的2个杂合启动子UGAP1-CTEF1和UTEF1-CTEF1进行乳糖酶的表征。发现杂合启动子UTEF1-CTEF1表达乳糖酶的酶活力与内源启动子PTEF1的相近,是天然启动子PLAC4的2.2倍,因此获得了一个长度变短但表达水平基本保持不变的启动子UTEF1-CTEF1。
进一步选择启动子UTEF1-CTEF1作为UAS串联杂合启动子构建的基础结构,将每个UAS分别与启动子UTEF1-CTEF1组合构建UAS串联杂合启动子UX-UTEF1-CTEF1(图7-a),并利用GFP进一步评价。结果显示,杂合启动子UHSP12-UTEF1-CTEF1表达GFP的荧光强度是UTEF1-CTEF1的1.3倍(图7-b)。将其在基因组上用于乳糖酶的表达发现,杂合启动子UHSP12-UTEF1-CTEF1表达的乳糖酶活力较UTEF1-CTEF1提升1.8倍,较野生型GG799提升3.8倍(图7-c),进一步证明了所筛UAS的应用价值。虽然所构杂合启动子表达乳糖酶活力仍低于内源强启动子PHSP12,但后续可通过将所筛UAS与PHSP12串联或多UAS串联等不同组合方式进一步优化杂合启动子的表达水平。
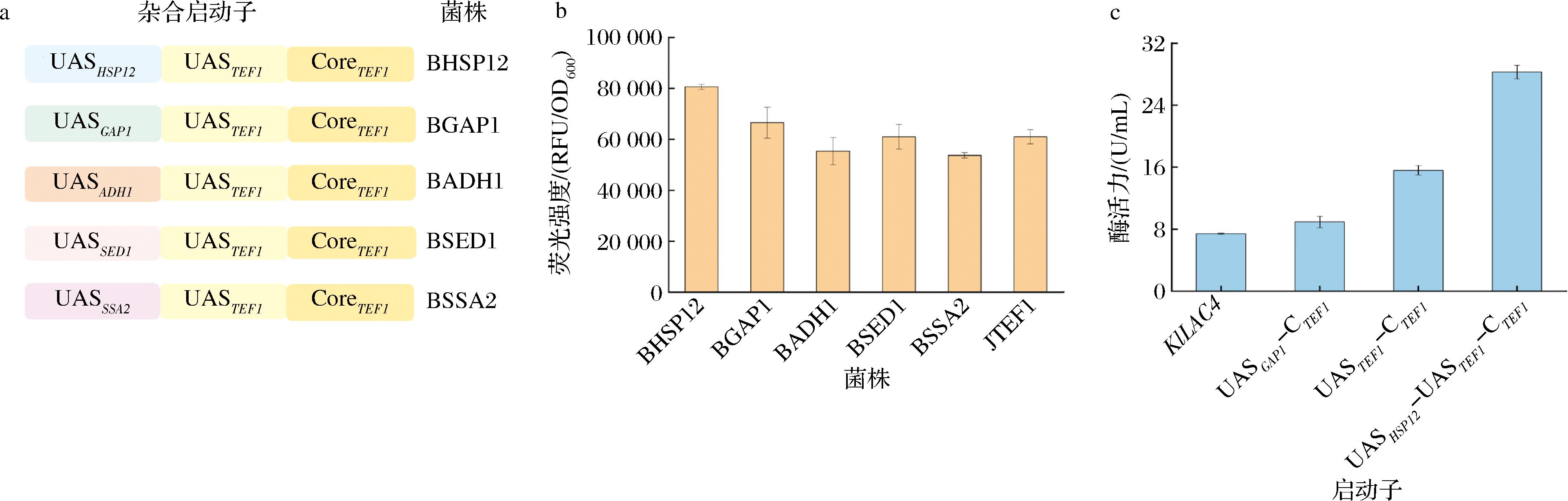
a-多UAS杂合启动子构建示意图;b-杂合启动子荧光强度;c-重组菌株乳糖酶活力
图7 杂合启动子的构建与评价
Fig.7 Construction and evaluation of hybrid promoters
3 结论与讨论
本研究通过转录组分析和荧光蛋白表达筛选,在K.lactis中系统筛选并表征了一批不同表达水平的内源启动子。通过启动子功能区域预测及截短实验,对荧光强度最高的6个启动子的核心启动子及UAS所在区域进行分析并构建杂合启动子。研究发现,大部分筛得的UAS具有通用性,而非严格依赖于自身的核心启动子,并且可通过优化UAS串联数量和顺序等方式进一步提高杂合启动子的表达水平。未来,随着高通量筛选技术和人工智能的不断进步,将更加高效和精准地筛选潜在启动子,设计更多的通用杂合启动子,为基因表达及高效细胞工厂构建提供更多的精细化调控元件。
[1] PATRA P, DAS M, KUNDU P, et al.Recent advances in systems and synthetic biology approaches for developing novel cell-factories in non-conventional yeasts[J].Biotechnology Advances, 2021, 47:107695.
[2] DE BRABANDER P, UITTERHAEGEN E, DELMULLE T, et al.Challenges and progress towards industrial recombinant protein production in yeasts:A review[J].Biotechnology Advances, 2023, 64:108121.
[3] SPOHNER S C, SCHAUM V, QUITMANN H, et al.Kluyveromyces lactis:An emerging tool in biotechnology[J].Journal of Biotechnology, 2016, 222:104-116.
[4] 刘波, 马清钧, 吴军.乳酸克鲁维酵母表达外源蛋白研究进展[J].生物技术通讯, 2007, 18(6):1039-1042.
LIU B, MA Q J, WU J.Advance in the production of heterologous proteins in the yeast Kluyveromyces lactis[J].Letters in Biotechnology, 2007, 18(6):1039-1042.
[5] TSARUK A, FILIP K, SIBIRNY A, et al.Native and recombinant yeast producers of lactic acid:Characteristics and perspectives[J].International Journal of Molecular Sciences, 2025, 26(5):2007.
[6] 曾晓玲, 赵昶灵, 文国松, 等.启动子结构、功能预测和验证方法的研究进展[J].分子植物育种, 2018, 16(12):3915-3925.
ZENG X L, ZHAO C L, WEN G S, et al.Research advances in prediction and validation methods for structures and functions of promoters[J].Molecular Plant Breeding, 2018, 16(12):3915-3925.
[7] WU Y J, FENG S, SUN Z A, et al.An outlook to sophisticated technologies and novel developments for metabolic regulation in the Saccharomyces cerevisiae expression system[J].Frontiers in Bioengineering and Biotechnology, 2023, 11:1249841.
[8] MADHAVAN A, ARUN K B, SINDHU R, et al.Customized yeast cell factories for biopharmaceuticals:From cell engineering to process scale up[J].Microbial Cell Factories, 2021, 20(1):124.
[9] 孙海烨, 张梁, 李由然, 等.利用增强型绿色荧光蛋白研究不同启动子在乳酸克鲁维酵母中的功能[J].生物技术通报, 2017, 33(6):197-206.
SUN H Y, ZHANG L, LI Y R, et al.Study on the function of different promoters in Kluyveromyces lactis by enhanced green fluorescent protein[J].Biotechnology Bulletin, 2017, 33(6):197-206.
[10] QIU Y B, LEI P, WANG R, et al.Kluyveromyces as promising yeast cell factories for industrial bioproduction:From bio-functional design to applications[J].Biotechnology Advances, 2023, 64:108125.
[11] WANG Z, GERSTEIN M, SNYDER M.RNA-Seq:A revolutionary tool for transcriptomics[J].Nature Reviews Genetics, 2009, 10(1):57-63.
[12] 喻林兵, 郑丽圆, 李宛莹, 等.原核启动子文库构建的研究进展[J].工业微生物, 2023, 53(3):97-103.
YU L B, ZHENG L Y, LI W Y, et al.On the research progress of the construction of prokaryotic promoter libraries[J].Industrial Microbiology, 2023, 53(3):97-103.
[13] GAO S, ZHOU H R, ZHOU J W, et al.Promoter-library-based pathway optimization for efficient (2S)-naringenin production from p-coumaric acid in Saccharomyces cerevisiae[J].Journal of Agricultural and Food Chemistry, 2020, 68(25):6884-6891.
[14] SUN M L, SHI T Q, LIN L, et al.Advancing Yarrowia lipolytica as a superior biomanufacturing platform by tuning gene expression using promoter engineering[J].Bioresource Technology, 2022, 347:126717.
[15] ALPER H, FISCHER C, NEVOIGT E, et al.Tuning genetic control through promoter engineering[J].Proceedings of the National Academy of Sciences of the United States of America, 2005, 102(36):12678-12683.
[16] BLAZECK J, LIU L Q, REDDEN H, et al.Tuning gene expression in Yarrowia lipolytica by a hybrid promoter approach[J].Applied and Environmental Microbiology, 2011, 77(22):7905-7914.
[17] NGUYEN L, SCHMELZER B, WILKINSON S, et al.From natural to synthetic:Promoter engineering in yeast expression systems[J].Biotechnology Advances, 2024, 77:108446.
[18] BASSETT S, DA SILVA N A.Engineering a carbon source-responsive promoter for improved biosynthesis in the non-conventional yeast Kluyveromyces marxianus[J].Metabolic Engineering Communications, 2024, 18:e00238.
[19] LAI J, SONG L G, ZHOU Y Y, et al.Fine-tuned gene expression elements from hybrid promoter libraries in Pichia pastoris[J].ACS Synthetic Biology, 2024, 13(1):310-318.
[20] PRESNELL K V, MELHEM O, COLEMAN S M, et al.Design and synthesis of synthetic promoters for consistency of gene expression across growth phases and scale in S.cerevisiae[J].Synthetic and Systems Biotechnology, 2024, 9(2):330-339.
[21] ZHAO S R, YE Z, STANTON R.Misuse of RPKM or TPM normalization when comparing across samples and sequencing protocols[J].RNA, 2020, 26(8):903-909.
[22] PREISSL S, GAULTON K J, REN B.Characterizing cis-regulatory elements using single-cell epigenomics[J].Nature Reviews Genetics, 2023, 24(1):21-43.
[23] 蒋慧慧, 王强, 饶志明, 等.酿酒酵母启动子工程研究进展[J].中国生物工程杂志, 2023, 43(11):78-91.
JIANG H H, WANG Q, RAO Z M, et al.Research progress of the promoter engineering in Saccharomyces cerevisiae[J].China Biotechnology, 2023, 43(11):78-91.