酱香型白酒香气突出、幽雅细腻、酒体醇厚、回味悠长,广受消费者欢迎[1]。独特的香气和口感源于复杂的酿造工艺,在酿造过程中,微生物群落主导着各种原料成分的代谢,是白酒大部分风味物质的主要来源。白酒酿造微生物来源与其开放式的发酵方式密切相关,除了在发酵开始前接种大曲[2]作为发酵剂,生产原料、操作环境[3]、空气等也是酒醅中酿造微生物的重要来源。已有研究表明,环境微生物是发酵过程演替的驱动力[4-5]。堆积发酵是酱香型白酒生产的一个特殊工序环节,通过敞开式的堆积发酵实现网罗和富集各类微生物以及酶类的目的,为入窖发酵创造条件,因此又被称为“二次制曲”[6]。堆积发酵由不受控制的多种微生物群落自然接种,并且在很大程度上受复杂因素的影响,如周围环境微生物群、非生物条件(如温度、湿度和pH值)及发酵基质(原材料,如高粱、小麦)等。堆积发酵温度可以达到50 ℃左右,整个发酵过程会持续4~5 d,在此过程中,酒醅中的微生物在高温压力下被筛选,最终在入窖前形成独特的微生物群落[7]。
白酒生产主要基于人工经验,由于缺乏对酿造机制的深入解析,导致白酒品质容易出现不稳定现象。为了稳定和提高白酒品质,有必要深入研究酿造微生物的来源,以及它们之间的相互作用,进而为生产工艺调控提供理论依据。目前已有部分研究报道结合高通量测序技术、溯源追踪及偏最小二乘法等多元统计方法尝试解决此问题。CHENG等[8]聚焦于复合香型白酒酿造过程,对发酵过程中酒曲、粮醅、发酵酒醅和窖泥等样品的微生物群落结构进行解析,发现不同样品微生物群落组成和多样性存在差异,并结合溯源分析发现,大部分发酵酒醅中微生物来自除高温大曲、中温大曲、麸曲、粮醅、窖泥等外的其他来源。CHEN等[9]解析了酱香型白酒第一轮发酵过程中酵母群落的结构和功能,发现在整个发酵过程中,酵母群落的丰富性和多样性增加,且发酵中的绝大多数酵母来自酿造环境。GE等[10]研究发现,高温放线菌属、毕赤酵母属、酿酒酵母属是酱香型白酒第四轮次堆积过程中的主要微生物群落。本课题组进行酱香型白酒一轮次酒醅微生物群落结构及溯源分析,堆积发酵6 d后,未被分类的乳杆菌科细菌和毕赤酵母属为绝对的优势细菌和真菌属[11]。在酱香型白酒生产过程中,为使出甑的酒醅均匀降温至下曲要求温度并富集酿酒微生物的操作称为摊晾,摊晾过程分为破埂、撒曲、拌曲、上堆等,摊晾是控制酒醅中水分和温度的重要操作步骤,也是发酵过程的开始。本课题组前期研究了不同摊晾方式对酱香型白酒发酵过程的影响,机械化摊晾方式影响了次要细菌的微生物组成,并改变了青霉菌和圆孢菌的相对丰度[12]。但目前对摊晾至堆积发酵过程发酵微生物群落分布规律有待进一步解析,对其来源认识也缺乏系统研究,不利于酱香型白酒堆积发酵管理和控制。
基于此,本研究以酱香型白酒四轮次发酵的堆积酒醅、大曲和环境样品为对象,采用高通量测序技术解析其微生物群落结构和演替规律,并解析酱香型白酒功能微生物的环境分布规律,进一步通过比较不同类型样品的差异解析功能微生物的来源,为逐步实现可控、标准化的生态白酒酿造提供理论数据。
1 材料与方法
1.1 材料与试剂
样品均取自2024年度贵州省遵义市某酱香型酒厂四轮次生产车间。DNA提取试剂盒,美国OMEGA BioTek公司;PCR引物,上海翌圣生物科技股份有限公司;无水乙醇(色谱纯),美国Sigma-Aldrich公司;乙酸正戊酯、2-乙基丁酸、叔戊醇作为内标化合物(色谱纯),上海阿拉丁生化科技股份有限公司。
1.2 仪器与设备
SB25-12DT超声波清洗机,宁波新芝生物科技股份有限公司;KG-AP32L自动蒸汽灭菌器,日本ALP公司;ETC811型PCR仪,北京东胜创新生物科技有限公司;GC8890气相色谱仪,美国Agilent公司;Aquaplore3S超纯水系统,美国艾科浦公司。
1.3 实验方法
1.3.1 酒醅及环境样品采集
分别在同一窖池的出窖上层、中层、下层酒醅的对应操作节点进行摊晾过程样品取样,根据摊晾至收堆过程中不同的操作环节,包括出甑、破埂、工人脚破埂、下曲、拌曲、收堆。在每个操作完成后进行取样,每次分别于操作场地的四周及中心取样后混合,并将出窖上层、中层、下层酒醅的对应操作节点所取样品混合后共得到综合样品6份。分别标记为出甑酒醅(ZP1)、破埂后酒醅(ZP2)、工人脚破埂后酒醅(ZP3)、下曲后酒醅(ZP4)、拌曲后酒醅(ZP5)、收堆酒醅(ZP6)。收堆完成后每隔24 h进行堆积过程酒醅取样,取样方式如图1所示,于堆积酒醅的上层、中层、下层对应的表层及中心位置对应的A~F 6个位点取样,并混合后得到综合样品。根据堆积时间(d)共得到综合样品5个,分别命名为DJ-1~DJ-5。当堆积酒醅温度升高至50 ℃左右,达到入窖条件时同样于A~F 6个位点分别取样后混合成综合样品,命名为XJ。所有酒醅样品采集后迅速装入无菌自封袋中,于-4 ℃带回实验室分析。
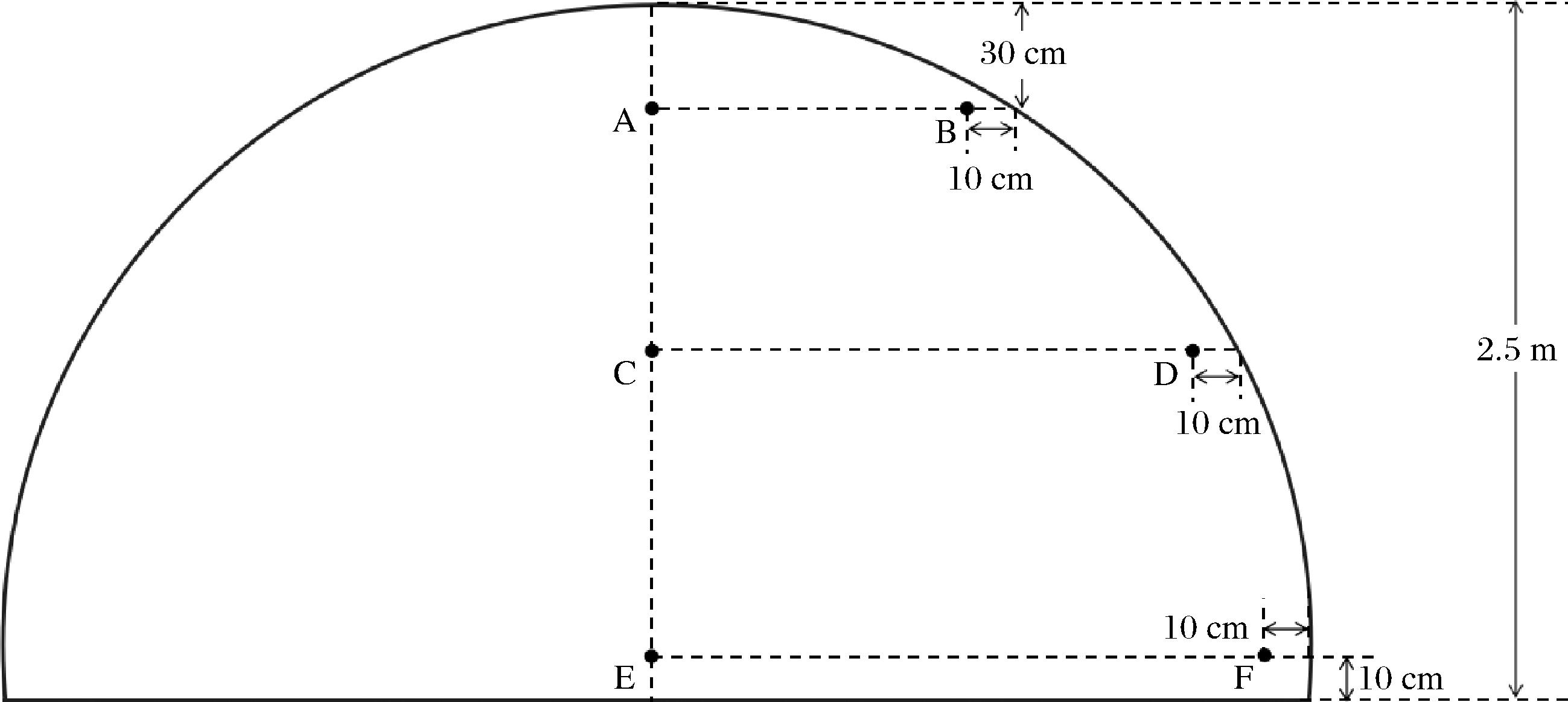
图1 堆积过程样品取样位置示意图
Fig.1 Schematic diagram for the sampling of grains during stacking fermentation
在本轮次开始前进行环境样品取样,分别采集了摊晾操作过程中使用的操作工具、其他物品、原辅料、地面等。其中操作工具、其他物品、地面均用100 mL的0.1 mol/L PBS浸湿的无菌脱脂棉擦拭得到,每次擦拭面积为10 cm×10 cm,随机选取3个取样点擦拭后混合为一个样品,样品放入无菌离心管中。其中操作工具样品有木锨(MC)、铁刀(TC)、钉耙(DP)、铁板(TB)、扫帚(SZ)、铁铲(YC)、抱斗(BD)、工人(GR);其他物品样品有酒罐(JG)、窗台(CT)、消防栓(XFS)、墙壁(QB);地面样品有未堆积地面(WDJ)、摊晾前地面(TLQ)、堆积前地面(DJQ)、厂房外地面(CFW)。同时原辅料样品中大曲(DQ)为生产用曲,糠壳(KK)为上甑前拌入的生产用糠壳,窖泥(JN)为下窖后封窖窖泥,均随机从使用现场各取200 g作为一个样品,放入无菌自封袋中,于-4 ℃带回实验室分析。
1.3.2 高通量测序
高通量测序采用Illumina MiSeq测序平台,分别对细菌16S rRNA基因V3~V4区、真菌ITS3~ITS4区进行高通量测序分析。参考本课题组方法[13],细菌扩增测序采用通用引物341F(CCTACGGGNGGCWGCAG)和805R(GACTACHVGGGTATCTAATCC);真菌扩增测序采用通用引物ITS3(GCATCGATGAAGAACGCAGC)和引物ITS4(TCCTCCGCTTATTGATATGC)。PCR扩增条件为:95 ℃预变性3 min;94 ℃变性20 s,55 ℃退火20 s,72 ℃延伸30 s,25次循环;72 ℃终延伸5 min降至4 ℃。PCR体系为:2×Hieff®Robust PCR Master Mix 15 μL、正向及反向引物各1 μL、DNA模板20~30 ng,使用ddH2O补齐体系至30 μL。高通量测序分析由生工生物工程(上海)股份有限公司完成。
1.3.3 酒醅风味成分检测
气相色谱检测条件参照本课题组方法[13]。称取10 g酒醅于50 mL离心管中,加入20 mL体积分数为53%的乙醇溶液并超声波浸提30 min,浸提液于5 000 r/min离心5 min后,取上清液使用0.22 μm有机系无菌膜过滤,获得检测液。
1.4 数据处理
利用Excel进行数据处理及作样品稀释曲线图,相对丰度气泡图、风味物质组成热图使用联川生物云平台绘制,相关性网络图使用R语言(v.4.4.3)软件进行绘制,组间差异物种判别图利用LEfSe软件绘制,组间功能丰度的差异图利用STAMP绘制,并利用R语言的Source Tracker工具对微生物群落数据进行分析,以探究微生物的来源。
2 结果与分析
2.1 样品微生物群落多样性
对酱香型白酒摊晾至堆积发酵过程酒醅及环境样品中的微生物群落结构进行分析,共对31个样品进行高通量测序。由图2的稀释曲线可知,所有样品不论是细菌还是真菌,基因测序均达到或接近平台期,各样本测序覆盖率均在0.99以上,说明本次测序深度适合,样本中微生物群落信息已被检测完全。
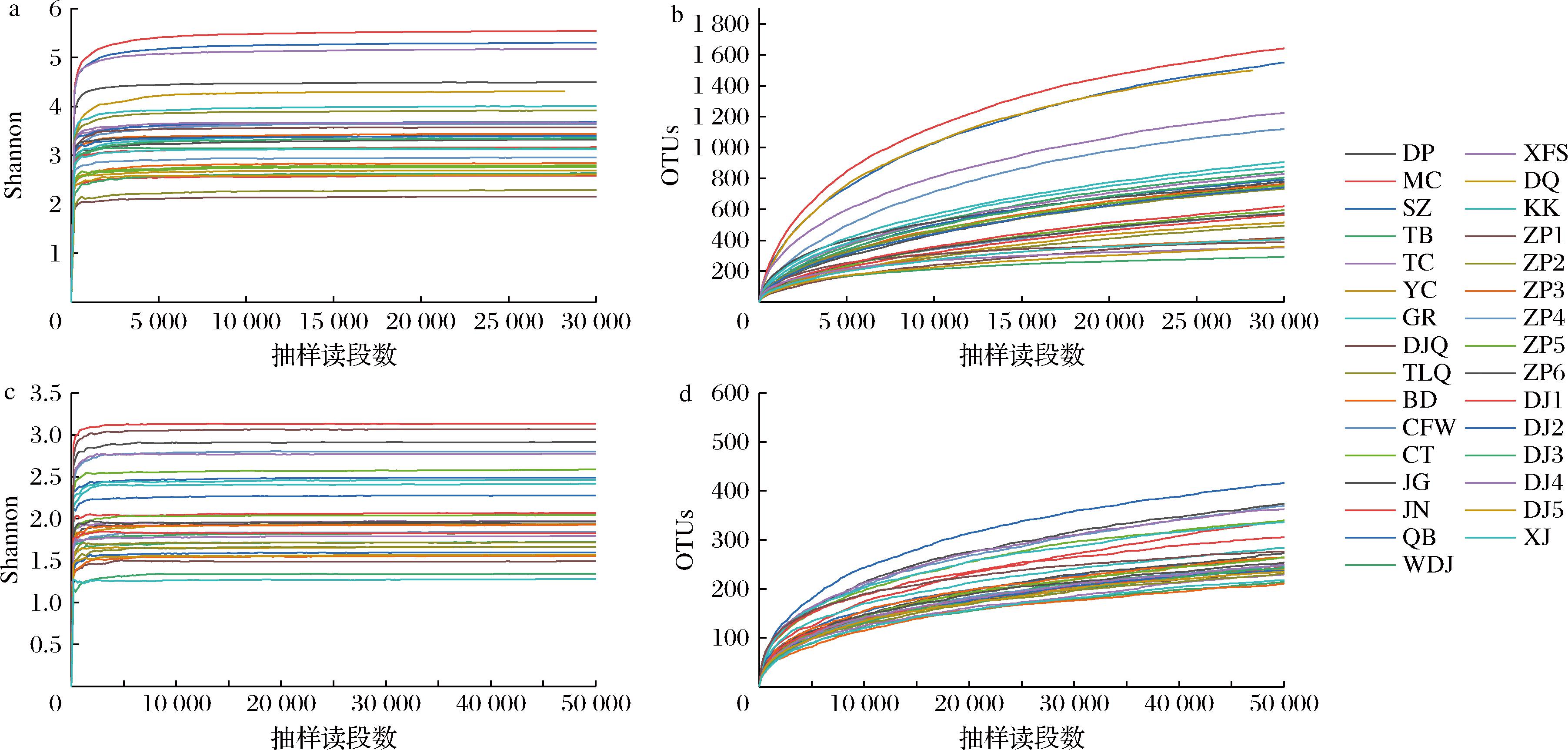
a-细菌稀释性曲线;b-细菌Shannon-Wiener曲线;c-真菌稀释性曲线;d-真菌Shannon-Wiener曲线
图2 不同样品稀释曲线
Fig.2 Rarefaction curve of different samples
由表1可知,从细菌来看,在摊晾过程中,酒醅从出甑(ZP1)到破埂后(ZP2)的Shannon指数和Chao 1指数明显上升,说明细菌的丰富度和物种总数明显增加,环境中的微生物被迅速网罗至酒醅中。但此时酒醅依旧处于蒸馏后的高温状态,部分细菌未能存活,故酒醅温度降低至工人可以用脚破埂后(ZP3)Shannon指数和Chao 1指数均下降,之后随着大曲的加入,Chao 1指数上升。而在堆积发酵过程中,Shannon指数及Chao 1指数先升高后下降,即细菌多样性在堆积发酵的中后期更为丰富。真菌的Chao 1指数及Shannon指数从摊晾至堆积结束整体呈现波动下降趋势,在堆积发酵初期真菌的多样性更为丰富。整体来看在堆积发酵末期微生物多样性降低,这可能与堆积发酵过程中酒醅内微生物所产的热及各类代谢物的积累有关[14],摊晾及堆积发酵过程环境微生态的选择作用对于酒醅微生物群落构建及发酵群落稳定性具有重要作用。
表1 酒醅微生物群落α-多样性指数变化
Table 1 Changes in α-diversity indexes of microbial community in fermented grains
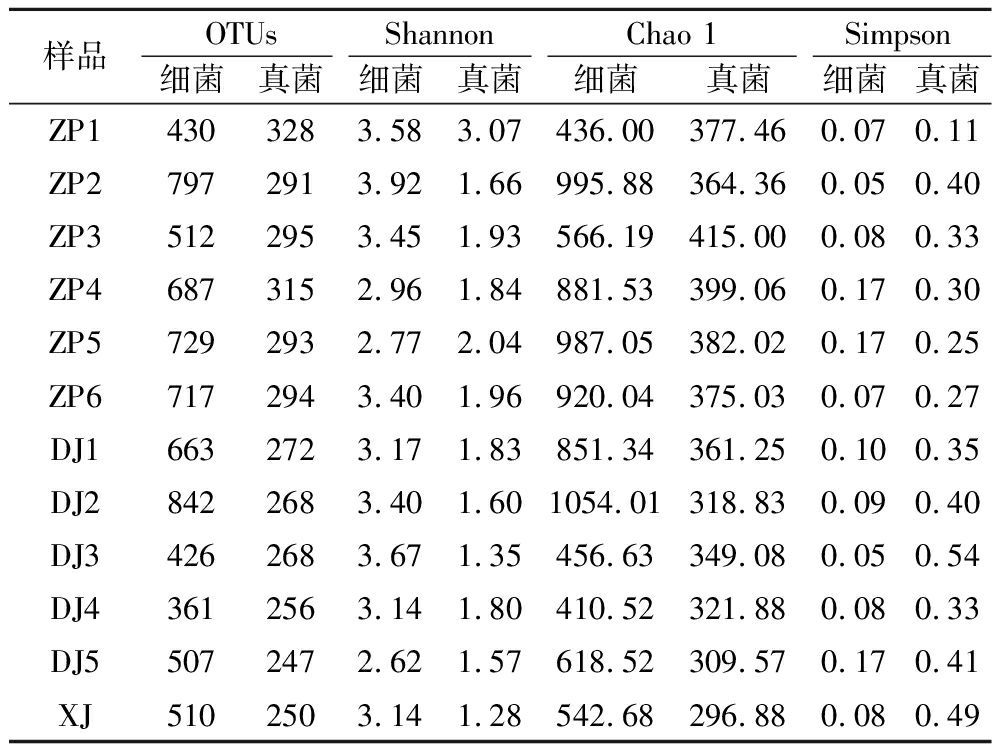
样品OTUsShannonChao 1Simpson细菌真菌细菌真菌细菌真菌细菌真菌ZP14303283.58 3.07436.00 377.460.07 0.11ZP27972913.92 1.66995.88 364.360.05 0.40ZP35122953.45 1.93566.19 415.000.08 0.33ZP46873152.96 1.84881.53 399.060.17 0.30ZP57292932.77 2.04987.05 382.020.17 0.25ZP67172943.40 1.96920.04 375.030.07 0.27DJ16632723.17 1.83851.34 361.250.10 0.35DJ28422683.40 1.601054.01 318.830.09 0.40DJ34262683.67 1.35456.63349.080.05 0.54DJ43612563.14 1.80410.52 321.880.08 0.33DJ55072472.62 1.57618.52 309.570.17 0.41XJ5102503.14 1.28542.68 296.880.08 0.49
2.2 摊晾至堆积发酵过程微生物组成及演替规律解析
为探究随时间序列变化导致微生物群落多样性变化的原因,进一步分析了摊晾至堆积过程中微生物结构的组成及演替规律,摊晾至堆积发酵过程在属水平上相对丰度>1%的优势细菌如图3-a所示。对于细菌多样性而言,出甑时酒醅中细菌组成结构明显区别于其余阶段,其中未分类的叶绿体(norank Chloroplast)及未分类柄杆菌科(norank Caulobacteraceae)丰度分别为27.12%、11.33%,明显高于其他酒醅。随着摊晾过程进行,芽孢杆菌属(Bacillus)、克罗彭施泰特氏菌属(Kroppenstedtia)、高温放线菌属(Thermoactinomyces)、枝芽孢杆菌属(Virgibacillus)的丰度分别从出甑时的0.17%、0.34%、0.13%、0.08%增加到收堆时的13.96%、22.59%、4.73%、12.33%,且进入堆积发酵阶段后依旧作为优势细菌存在,堆积发酵阶段的优势细菌在摊晾过程中得到富集。已有研究表明,芽孢杆菌属(Bacillus)、枝芽孢杆菌属(Virgibacillus)、克罗彭施泰特氏菌属(Kroppenstedtia)等细菌主要由大曲提供[15]。芽孢杆菌属(Bacillus)是酿造大曲发酵过程中的主要优势细菌,影响大曲中的微生物群落结构及代谢图谱[16],克罗彭施泰特氏菌属(Kroppenstedtia)是酱香型白酒酿造过程脂肪酸生物合成的功能微生物[17],高温放线菌属(Thermoactinomyces)可以通过产生多种功能酶调节酿造微生态,而且能产生吡嗪等多种风味化合物[18],高丰度的枝芽孢杆菌属(Virgibacillus)有利于四甲基吡嗪和2,3-丁二醇的生成[19]。同时在堆积发酵阶段乳杆菌属(Lactobacillus)丰度明显增大,其主要代谢产物乳酸是形成乳酸乙酯及其他香味成分的重要基础物质。
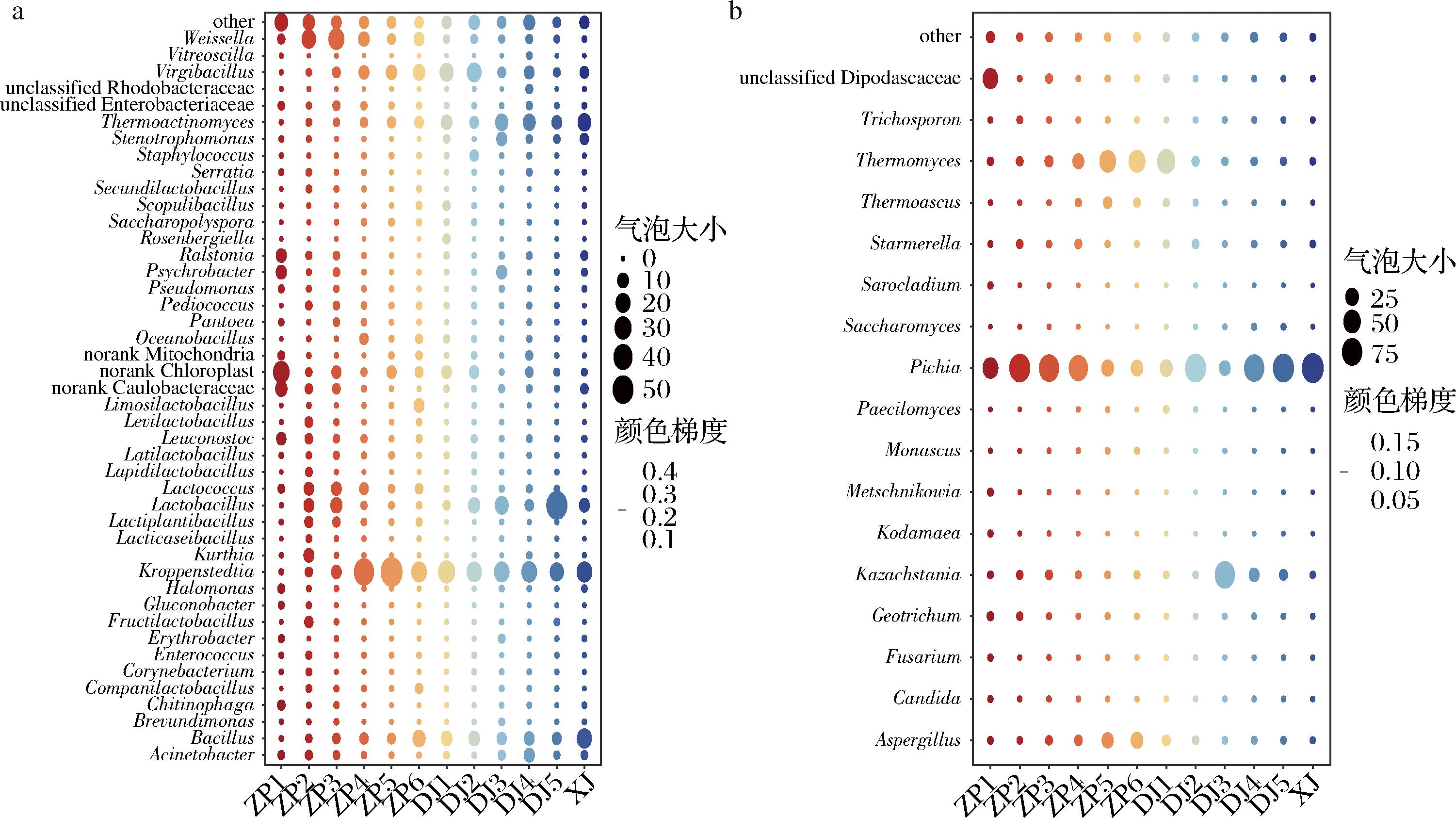
a-细菌丰度;b-真菌丰度
图3 酒醅属水平微生物群落结构
Fig.3 Community structure at the genus level of fermented grains
摊晾至堆积发酵过程在属水平上相对丰度>1%的优势真菌如图3-b所示。对于真菌多样性而言,出甑时酒醅真菌结构同样与其余酒醅存在区别,其中未分类的双足囊菌科(unclassified Dipodascaceae,36.63%)丰度明显高于其他酒醅。随着摊晾过程进行,曲霉属(Aspergillus)、嗜热真菌属(Thermomyces)丰度逐渐增大,由出甑时的1.62%、2.58%分别增大至收堆时的20.23%、46.08%,同时毕赤酵母属(Pichia)丰度在由出甑到破埂显著增加后,随着后续操作环节在摊晾过程逐步降低。堆积前期真菌结构与收堆时较为相似,但随着堆积发酵进行嗜热真菌属(Thermomyces)丰度明显减少,毕赤酵母属(Pichia)丰度逐步增大,至堆积结束时成为绝对的优势真菌,丰度高达90.08%,此外哈萨克斯坦酵母属(Kazachstania)在堆积3 d时丰度突然增大又迅速减小。整体来看,霉菌丰度在摊晾过程中逐渐增大,堆积过程中逐渐减小,堆积过程是霉菌逐步演替为酵母菌的过程。霉菌产生蛋白酶、淀粉酶等酶类,在生产前期降解原料中的大分子物质,为酵母菌的生长和发酵提供底物[15],而酵母菌与白酒的风味、产量有着重要关联,可以产生多种酯类。
2.3 摊晾至堆积发酵过程酒醅中风味物质动态变化
2.3.1 酒醅风味物质的组成变化
为探究酒醅在摊晾至堆积发酵过程中风味物质的变化情况,采用气相色谱法共检出33种风味化合物,其中包含5种醛类物质、8种酸类物质、8种酯类物质、10种醇类物质和2种其他类物质,如图4所示。风味物质总含量及各类物质总含量在摊晾过程中均在逐步上升,风味物质总含量由出甑时的1 872.10 mg/L增加至收堆时的2 547.28 mg/L,且其中酸类风味物质增加了386.20 mg/L,占了总增加含量的57.20%。酸类物质中乙酸、异戊酸、庚酸、异丁酸及己酸增加了1.5~2.7倍,收堆时酒醅中含量最高的风味物质为乙酸,含量达1 002.65 mg/L。在堆积发酵过程中,醛类和酸类风味物质含量明显下降,酯类风味物质含量基本维持不变,但醇类风味物质总含量上升,酸类及醇类风味物质是堆积发酵过程中主要的风味物质,这与本课题组前期的研究报道一致[13]。其中1,2-丙二醇及meso-2,3-丁二醇含量增加明显,乳酸乙酯及苯乙酸乙酯含量略有增加,下窖时酒醅中含量最高的风味物质为1,2-丙二醇,含量达1 207.72 mg/L。值得注意的是,在出甑时未有庚酸、庚酸乙酯及二乙氧基甲烷检出,而后庚酸随着摊晾过程进行含量明显增加,庚酸乙酯及二乙氧基甲烷则在堆积过程才出现,且随着堆积进行庚酸乙酯含量逐渐减少,这可能与酒醅中微生物的相互作用导致风味物质的转化密切相关[20]。
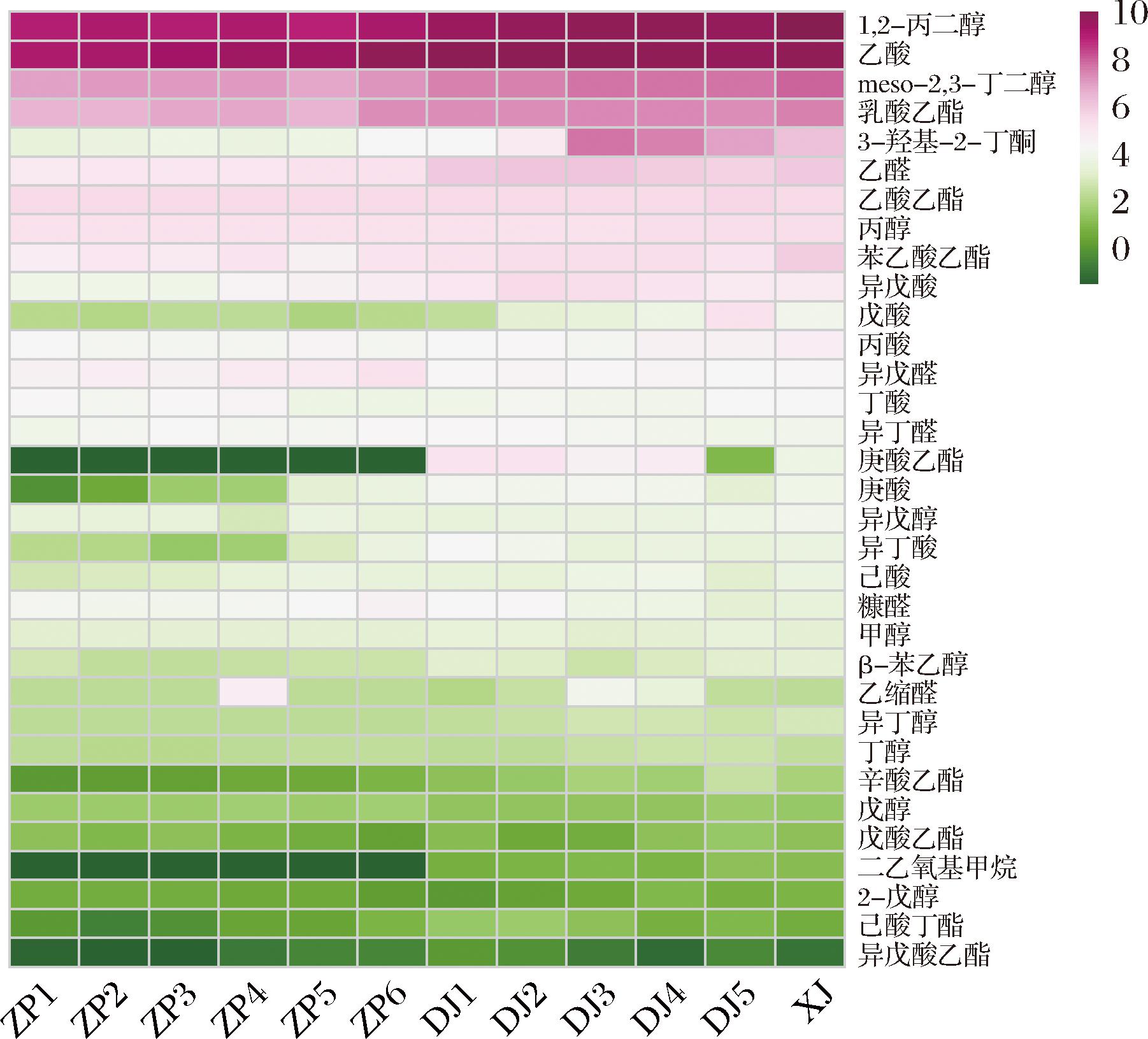
图4 酒醅相对风味成分丰度热图
Fig.4 Heatmap of flavor compounds from fermented grains
2.3.2 微生物群落与风味物质相关性
分别选取细菌和真菌中相对丰度排名前10的物种,以及含量排名前20的风味物质,计算Spearman相关性系数后筛选显著性P<0.01的微生物与风味物质并绘制相关性网络分析图。由图5可以看出,风味物质含量较高的乙酸、1,2-丙二醇及meso-2,3-丁二醇与微生物呈现显著相关性,其中乙酸与15种微生物存在相关性,其中不动杆菌属(Acinetobacter)、未分类柄杆菌科(norank Caulobacteraceae)、罗尔斯通氏菌属(Ralstonia)、高温放线菌属(Thermoactinomyces)、曲霉属(Aspergillus)、哈萨克斯坦酵母菌属(Kazachstania)、拟青霉属(Paecilomyces)、酿酒酵母属(Saccharomyces)与其显著正相关,而芽孢杆菌属(Bacillus)、枝芽孢杆菌属(Virgibacillus)、魏斯氏菌属(Weissella)、毕赤酵母属(Pichia)、嗜热子囊菌属(Thermoascus)、嗜热真菌属(Thermomyces)、未分类双足囊菌科(unclassified Dipodascaceae)与其显著负相关。已有研究表明,库德里阿兹威氏毕赤酵母(Pichia kudriavzevii)、粟酒裂殖酵母(Schizosaccharomyces pombe)、酿酒酵母(Saccharomyces cerevisiae)、拜耳接合酵母(Zygosaccharomyces bailii)以及乳杆菌属(Lactobacillus)在酱香型白酒入池发酵阶段高效地表达了丙酮酸代谢中关于产乙醇、乙酸以及产乳酸的相关酶[21-22]。1,2-丙二醇及meso-2,3-丁二醇则主要与枝芽孢杆菌属(Virgibacillus)呈现显著正相关关系。微生物中毕赤酵母属(Pichia)、嗜热真菌属(Thermomyces)、高温放线菌属(Thermoactinomyces)与风味物质的相关性较强,毕赤酵母属(Pichia)与丙醇、异戊醛、异戊酸、丁酸、异戊酸乙酯呈显著正相关,在发酵过程中,毕赤酵母属(Pichia)可以产生多元醇[23],也可通过抑制其他丝状真菌而引发微生物群落的快速演替,从而使酸类、酯类等风味物质含量增加[15]。嗜热真菌属(Thermomyces)同样也与异戊醛、异戊酸、异戊酸乙酯呈正相关,高温放线菌属(Thermoactinomyces)则在与乙酸显著正相关的同时,与和毕赤酵母属(Pichia)正相关的几个物质负相关,该属微生物在代谢过程中能够产生一些具有特殊风味的物质,如某些酚类化合物[24]、吡嗪类化合物等[25]。
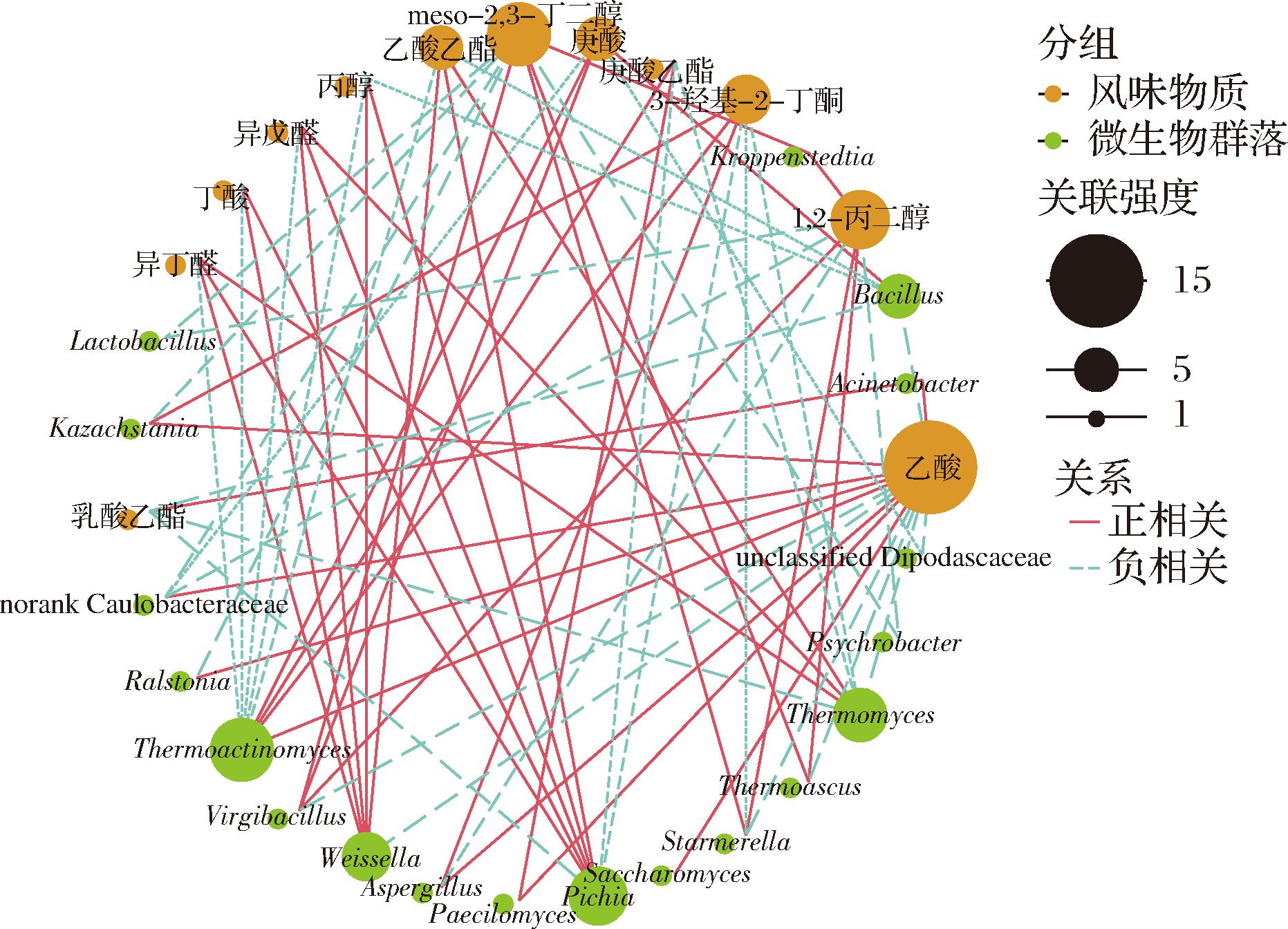
图5 风味成分与微生物群落相关性网络图
Fig.5 Correlation network diagram of flavor compounds and microbial community
2.4 环境微生物群落组成结构
将采集的环境样品划分为操作工具(A组)、其他物品(B组)、原辅料(C组)、地面(D组)。环境细菌在属水平上相对丰度>1%的微生物如图6所示,环境样品中细菌组成更为丰富且较酒醅中存在区别,其中魏斯氏菌属(Weissella)在各样品中均丰度较高,在操作工具(A组)、其他物品(B组)、原辅料(C组)、地面(D组)中丰度分别为1.14%~54.38%、2.57%~11.39%、0.16%~5.24%、17.95%~57.63%,魏斯氏菌属(Weissella)能够进行乳酸发酵,将糖类转化为乳酸,并且在代谢过程中会产生短链脂肪酸等风味前体物质[26]。除魏斯氏菌属(Weissella)外,操作工具(A组)中丰度较高的乳杆菌属(Lactobacillus)、乳球菌属(Lactococcus)、片球菌属(Pediococcus)、植物乳植杆菌属(Lactiplantibacillus)、明串珠菌属(Leuconostoc)也均属于乳酸菌,操作工具表面乳酸菌丰度极高(15.93%~85.93%)。其他物品(B组)中芽孢杆菌属(Bacillus)和不动杆菌属(Acinetobacter)丰度较高,原辅料(C组)中各样品丰度差异较大,其中大曲中克罗彭施泰特氏菌属(Kroppenstedtia)、芽孢杆菌属(Bacillus)、枝芽孢杆菌属(Virgibacillus)丰度较高,糠壳中未分类的叶绿体(norank Chloroplast)及泛菌属(Pantoea)丰度较高,窖泥中不存在显著优势细菌。地面(D组)中会与酒醅直接接触的摊晾前地面(TLQ)与堆积前地面(DJQ)细菌结构较为相似,其中片球菌属(Pediococcus)丰度较高(31.62%~42.32%)。

a-操作工具(A组);b-其他物品(B组);c-原辅料(C组);d-地面(D组)
图6 环境细菌属水平微生物群落结构
Fig.6 Relative abundance of environmental bacteria at the genus level
环境样品真菌优势菌属如图7所示,相较于细菌,环境样品中真菌结构组成与酒醅中更为相似,其中毕赤酵母属(Pichia)在各样品中均丰度较高,在操作工具(A组)、其他物品(B组)、原辅料(C组)、地面(D组)中丰度分别为50.87%~80.82%、23.96%~55.10%、1.71%~57.43%、20.12%~78.86%。除毕赤酵母属(Pichia)外,操作工具(A组)中丰度较高的哈萨克斯坦酵母属(Kazachstania,2.31%~15.87%)、斯塔莫酵母属(Starmerella,1.16%~9.88%),其他物品(B组)中丰度较高的节担菌属(Wallemia,0.97%~38.80%)、嗜热真菌属(Thermomyces,3.73%~13.21%)、曲霉属(Aspergillus,3.08%~18.02%),地面(D组)中也同样是哈萨克斯坦酵母属(Kazachstania)及嗜热真菌属(Thermomyces)丰度较高。原辅料(C组)中各样品真菌丰度同样差异较大,大曲中嗜热真菌属(Thermomyces,57.43%)是绝对的优势真菌,糠壳中镰刀菌属(Fusarium,36.93%)、小树状霉属(Dendryphiella,25.76%)丰度较高,而窖泥中则为地霉属(Geotrichum,30.95%)、假丝酵母属(Candida,21.20%)。
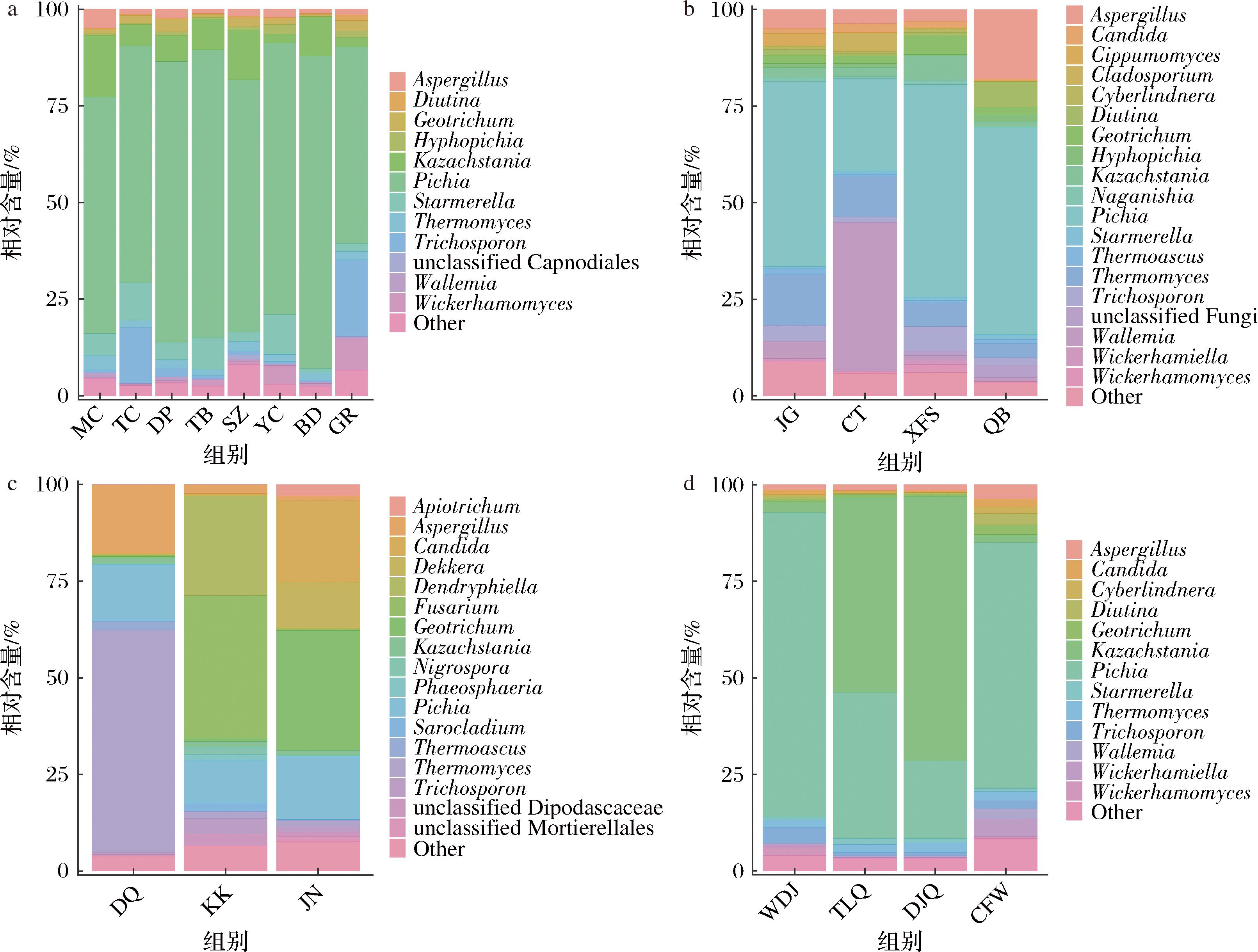
a-操作工具(A组);b-其他物品(B组);c-原辅料(C组);d-地面(D组)
图7 环境真菌属水平微生物群落结构
Fig.7 Relative abundance of environmental fungi at the genus level
2.5 组间微生物及功能差异
2.5.1 不同组间微生物差异物种判别分析
通过LEfSe分析辨别各组间在丰度上存在显著差异的标志物种,把摊晾过程酒醅命名为E组,堆积过程酒醅命名为F组,结果如图8所示。不论是细菌还是真菌,仅有其他物品(B组)、原辅料(C组)有独立的分枝。细菌中,原辅料(C组)的标志物种在进化分支的目水平上表现出5处聚集[19],分别在r(蓝菌门中与叶绿体相关的目,Chloroplast)、o(厌氧绳菌目,Anaerolineales)、h(拟杆菌目,Bacteroidales)、e(假诺卡氏菌目,Pseudonocardiales)、c6(立克次氏体目,Rickettsiales)。而地面(D组)中的标志物种主要集中在b4(乳杆菌目,Lactobacillales)下的b3(链球菌科,Streptococcaceae)、b1(乳杆菌科,Lactobacillaceae)。真菌方面则除了其他物品(B组)在b7(节担菌纲,Wallemiomycetes)有一个单独分枝外,其余各部分均囊括在堆积过程酒醅(F组)的a8(子囊菌门,Ascomycota)中,表明各个分组中真菌标志物种均参与了发酵过程。
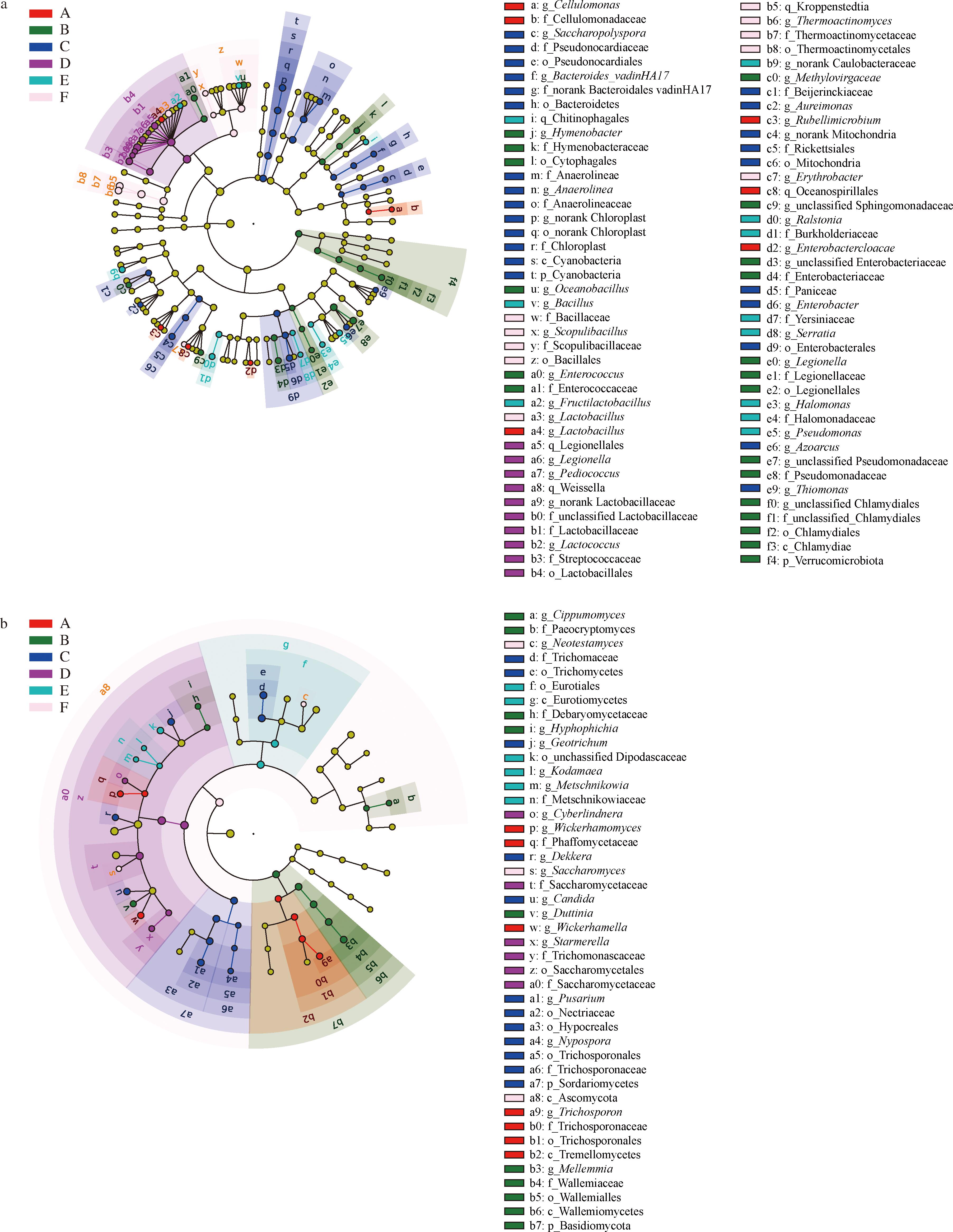
a-细菌LEfSe分析;b-真菌LEfSe分析
图8 不同组别间微生物群落的LEfSe分析图
Fig.8 LEfSe results of microbial communities among different groups
2.5.2 不同组间功能差异分析
为阐明各分组微生物群落的功能差异,进一步分析了微生物群落内代谢途径的差异和功能基因的波动,并分析了不同组与堆积过程酒醅(F组)在KEGG代谢途径的差异,研究结果如图9所示。堆积过程酒醅(F组)在外源性物质生物降解与代谢、脂质代谢、细胞运动、信号转导、萜类和聚酮类化合物的代谢途径上丰度显著高于操作工具(A组),在细胞群体-原核生物、氨基酸代谢、外源性物质生物降解与代谢、细胞运动、萜类和聚酮类化合物的代谢、脂质代谢、信号转导途径上丰度显著高于地面(D组),在能量代谢等途径上丰度显著高于摊晾过程酒醅(E组)。堆积过程酒醅(F组)在多个重要的生物代谢和生理途径上表现出显著高于其他组别的活性或水平,表明以上功能更加倾向于堆积过程酒醅(F组)样本。此外,地面(D组)的碳水化合物代谢丰度超过堆积过程酒醅(F组),碳水化合物代谢包括糖酵解等途径,糖酵解的最终产物是乙酸、乳酸等[27],与地面(D组)中乳酸菌丰度较高密切相关。
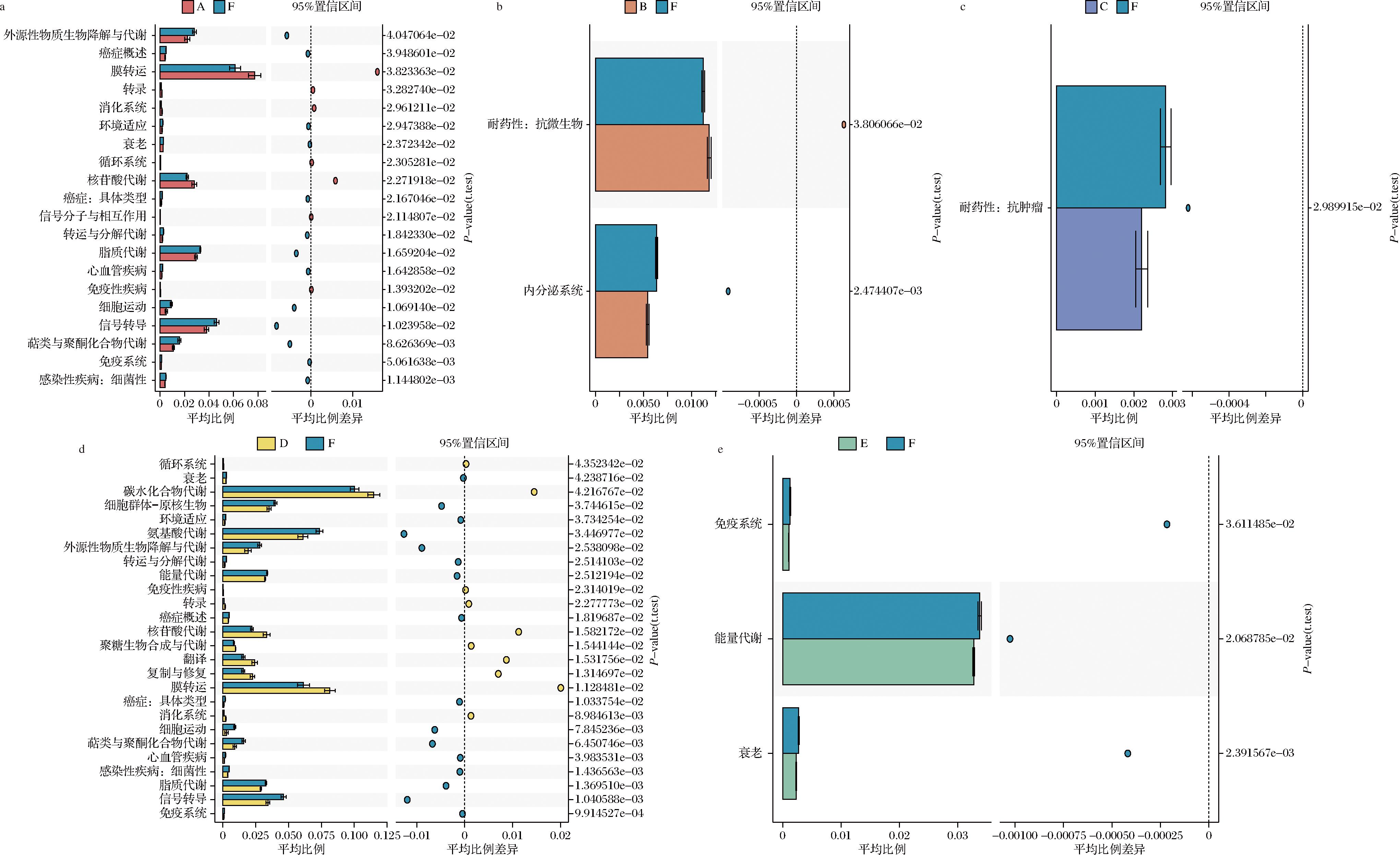
a-A组与F组功能差异分析;b-B组与F组功能差异分析;c-C组与F组功能差异分析;d-D组与F组功能差异分析;e-E组与F组功能差异分析
图9 不同组别间功能差异分析STAMP分析图
Fig.9 STAMP results of functional differences among different groups
2.6 摊晾及堆积发酵过程酒醅微生物溯源
基于R语言使用贝叶斯概率工具Source Tracker进一步分析堆积和窖池发酵酒醅中优势细菌和真菌菌群的来源及比例。细菌菌群溯源结果如图10-a所示,出甑酒醅(ZP1)中细菌来源明显区别于其余酒醅,大量来源于未知及原辅料,其中有25%的细菌来源于糠壳。之后随着摊晾操作的进行,操作工具开始与酒醅接触,未知来源微生物占比迅速下降,在破埂后酒醅(ZP2)、工人脚破埂后酒醅(ZP3)中细菌主要来源于操作工具,分别占比77%、58%。在下曲后酒醅(ZP4)中开始撒入大曲,此时大曲来源微生物占比上升至68%,且在之后的操作过程酒醅及堆积发酵酒醅中大曲来源细菌始终占比较大,达34%~80%。同时堆积过程中其他物品对酒醅细菌菌群有较大贡献,占比为11%~41%。图10-b中展现了真菌菌群溯源结果,摊晾过程真菌微生物来源结构与细菌相似,同样是出甑酒醅(ZP1)中真菌主要来源于未知的环境,且操作工具在摊晾前期对酒醅真菌群落有重大贡献,占比为66%~88%,而在撒入大曲后,大曲成为贡献度最高的来源,达到73%。堆积发酵过程中真菌微生物则主要来源于操作工具和地面,分别占比9%~84%,3%~23%。此外,工人来源对酒醅的细菌及真菌均贡献度不大,此结论与张红霞等[28]研究相符,表明在酱香型白酒生产中使用机械化摊晾设备降低人工操作强度具有可行性。
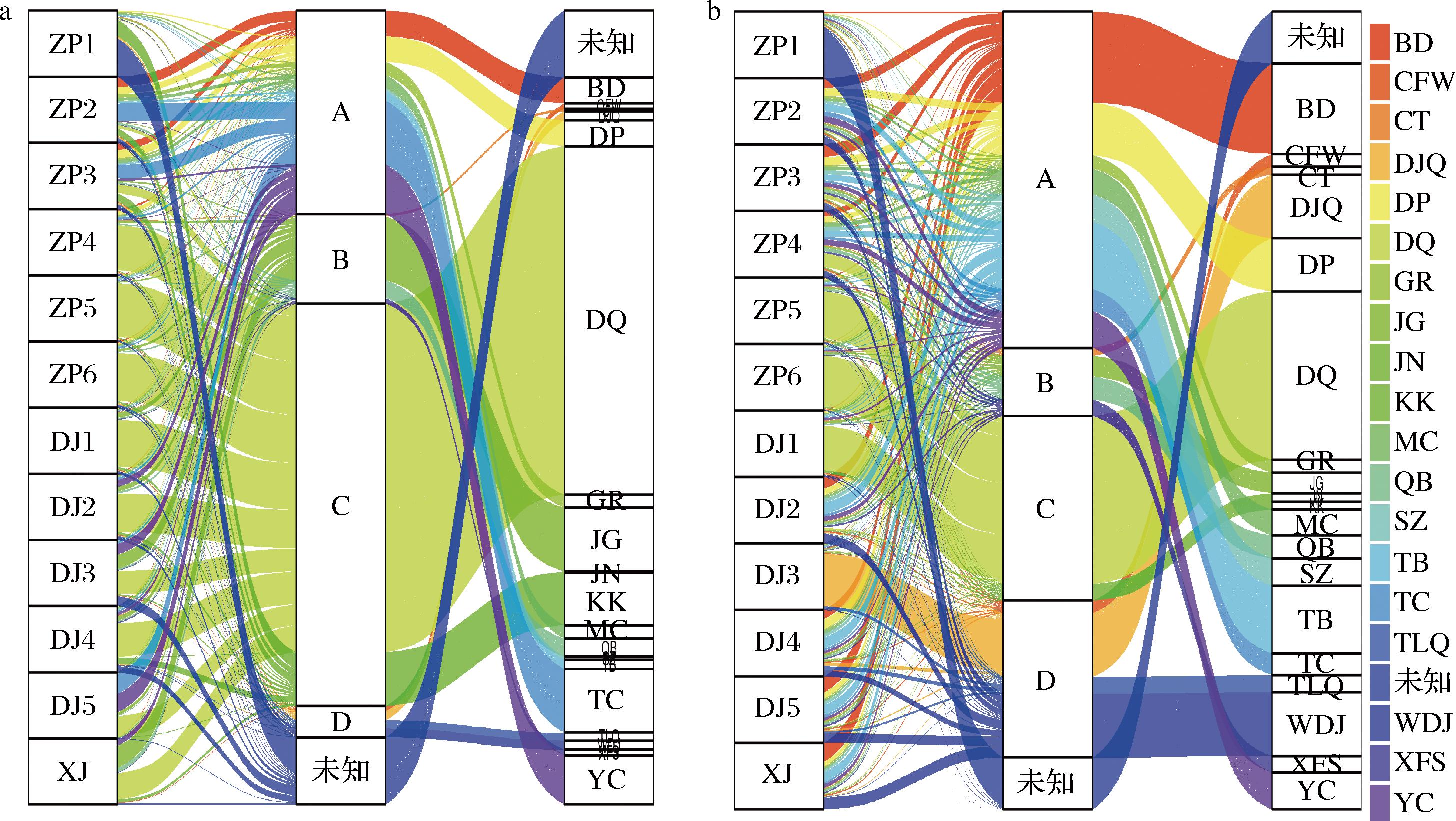
a-细菌;b-真菌
图10 酒醅微生物溯源分析
Fig.10 Microbial traceability of fermented grains
3 结论与讨论
采用高通量测序技术结合气相色谱及多元统计分析法,对酱香型白酒四轮次摊晾至堆积发酵过程微生物群落及风味物质间的相互作用关系进行了解析。结果表明酱香型白酒四轮次摊晾至堆积发酵过程主要的优势细菌和真菌分别为克罗彭施泰特氏菌属(Kroppenstedtia)和毕赤酵母属(Pichia),风味物质变化上,摊晾时总量上升、酸类增加显著,堆积时醛类、酸类下降、醇类上升,且微生物与风味物质相关性显著。不同环境样品分组间微生物组成结构明显不同,组间差异分析显示,堆积过程酒醅在多个代谢途径活性较高。微生物溯源表明,摊晾前期操作工具对酒醅微生物影响大,拌入大曲后大曲成为主要来源,堆积时真菌主要来自操作工具和地面。本研究为优化生态白酒酿造工艺、实现标准化生产提供了理论支撑。
[1] 李小东, 高大禹, 田庆贞, 等.芝麻香型白酒堆积发酵对入窖发酵过程及原酒品质的影响[J].食品与发酵工业, 2018, 44(5):63-69.
LI X D, GAO D Y, TIAN Q Z, et al.Effects of sesame-flavor liquor accumulation on cellar fermentation process and liquor quality[J].Food and Fermentation Industries, 2018, 44(5):63-69.
[2] WU S L, DU H, XU Y.Daqu microbiota adaptability to altered temperature determines the formation of characteristic compounds[J].International Journal of Food Microbiology, 2023, 385:109995.
[3] WANG X S, DU H, ZHANG Y, et al.Environmental microbiota drives microbial succession and metabolic profiles during Chinese liquor fermentation[J].Applied and Environmental Microbiology, 2018, 84(4):e02369-17.
[4] BOKULICH N A, LEWIS Z T, BOUNDY-MILLS K, et al.A new perspective on microbial landscapes within food production[J].Current Opinion in Biotechnology, 2016, 37:182-189.
[5] TAN Y W, DU H, ZHANG H X, et al.Geographically associated fungus-bacterium interactions contribute to the formation of geography-dependent flavor during high-complexity spontaneous fermentation[J].Microbiology Spectrum, 2022, 10(5):e0184422.
[6] 戴奕杰, 李宗军, 田志强, 等.酱香型白酒的轮次酒以及“二次制曲”过程中的风味物质分析[J].食品研究与开发, 2019, 40(19):24-32.
DAI Y J, LI Z J, TIAN Z Q, et al.Flavor components analysis of rounds wine and during the process of secondary starter-making of Maotai-flavor Baijiu[J].Food Research and Development, 2019, 40(19):24-32.
[7] YANG L, HUANG X D, HU J F, et al.The spatiotemporal heterogeneity of microbial community assembly during pit fermentation of soy sauce flavor Baijiu[J].Food Bioscience, 2024, 61:104438.
[8] CHENG W, LAN W, CHEN X F, et al.Source and succession of microbial communities and tetramethylpyrazine during the brewing process of compound-flavor Baijiu[J].Frontiers in Microbiology, 2024, 15:1450997.
[9] CHEN Z P, CAO Q, MENG T T, et al.Yeast community in the first-round fermentation of sauce-flavor Baijiu:Source, succession and metabolic function[J].Food Research International, 2025, 200:115466.
[10] GE D Y, WANG Y R, CAI W C, et al.Correlation analysis of microbial groups and sensory quality in the fourth round of the stacked fermentation of sauce-flavor liquor[J].Food Bioscience, 2024, 59:103958.
[11] 朱安然, 汪地强, 胡建锋, 等.酱香型白酒一轮次糟醅微生物群落结构及溯源分析[J].食品科学, 2025, 46(4):117-125.
ZHU A R, WANG D Q, HU J F, et al.Microbial community structure and traceability in fermented grains for Jiang-Flavor Baijiu during the first round of fermentation[J].Food Science, 2025, 46(4):117-125.
[12] WANG D Q, WU C, HU J F, et al.Exploring the impact mechanisms on different mechanized airing approaches during second round heap fermentation of sauce-flavor Baijiu:From physicochemical parameters, microbial diversity to volatile flavor compounds[J].Food Research International, 2025, 199:115359.
[13] 吴成, 程平言, 谢丹, 等.酱香型白酒4轮次堆积发酵理化因子、风味物质与微生物群落相关性分析[J].食品科学, 2023, 44(2):240-247.
WU C, CHEN P Y, XIE D, et al.Correlation analysis among physicochemical parameters, flavor compounds and microbial community during fourth round of heap fermentation of Jiang-Flavor Baijiu[J].Food Science, 2023, 44(2):240-247.
[14] WU Q, CHEN L Q, XU Y.Yeast community associated with the solid state fermentation of traditional Chinese Maotai-flavor liquor[J].International Journal of Food Microbiology, 2013, 166(2):323-330.
[15] ZHANG H X, WANG L, TAN Y W, et al.Effect of Pichia on shaping the fermentation microbial community of sauce-flavor Baijiu[J].International Journal of Food Microbiology, 2021, 336:108898.
[16] WANG P, WU Q, JIANG X J, et al.Bacillus licheniformis affects the microbial community and metabolic profile in the spontaneous fermentation of Daqu starter for Chinese liquor making[J].International Journal of Food Microbiology, 2017, 250:59-67.
[17] ZHANG J, DU R B, NIU J, et al.Daqu and environmental microbiota regulate fatty acid biosynthesis via driving the core microbiota in soy sauce aroma type liquor fermentation[J].International Journal of Food Microbiology, 2024, 408:110423.
[18] ZHU Q, CHEN L Q, PENG Z, et al.Analysis of environmental driving factors on core functional community during Daqu fermentation[J].Food Research International, 2022, 157:111286.
[19] 杨阳, 禄凌飞, 刘光钱, 等.不同发酵顶温大曲中细菌群落结构的差异性分析[J].食品与发酵工业, 2023, 49(13):70-77.
YANG Y, LU L F, LIU G Q, et al.Difference analysis of bacterial community structure in Daqu with different peak temperatures achieved during fermentation[J].Food and Fermentation Industries, 2023, 49(13):70-77.
[20] ZHU H, LI Q, EL-SAPPAH A H, et al.Influence of two sorghum varieties on metabolic factors, microbial community, and flavor component precursors of strong-flavor Baijiu Zaopei[J].Food Chemistry, 2025, 474:143079.
[21] 宋哲玮. 酱香型白酒核心酿造菌群及群体代谢机制的研究[D].无锡:江南大学, 2020.
SONG Z W.Revealing the core brewing microbes and their metabolic mechanisms in Chinese Maotai-flavor Baijiu[D].Wuxi:Jiangnan University, 2020.
[22] 万旗钰, 程玉鑫, 黄永光, 等.酱酒1、2轮次窖池不同醅层微生态结构与酸性化合物组成解析及其相关性预测[J].食品科学, 2024, 45(4):88-95.
WAN Q Y, CHEN Y X, HUANG Y G, et al.Fermented grains from different layers of cellar in the first and second rounds of fermentation of Maotai-Flavor Baijiu:analysis of microbial community structure and acid composition as well as correlation between them[J].Food Science, 2024, 45(4):88-95.
[23] 白小燕, 邱树毅, 雷安亮, 等.酱香白酒酿造过程中产多元醇功能酵母的筛选[J].中国酿造, 2017, 36(5):58-62.
BAI X Y, QIU S Y, LEI A L, et al.Screening of polyhydric alcohol-producing yeasts from Maotai-flavor Baijiu during brewing[J].China Brewing, 2017, 36(5):58-62.
[24] 翟威涛, 吴双全, 柴丽娟, 等.酱酒酒醅中普通高温放线菌的筛选及其挥发性物质代谢分析[J].食品科学, 2025, 46(12):118-126.
ZHAI W T, WU S Q, CHAI L J, et al.Screening of Thermoactinomyces vulgarisin the fermented grains of sauce-flavor Baijiu and metabolic analysis of volatile compounds[J].Food Science, 2025, 46(12):118-126.
[25] 李豆南, 黄魏, 王晓丹, 等.酱香型大曲中高温放线菌的筛选及风味成分分析[J].食品科学, 2018, 39(6):171-176.
LI D N, HUANG W, WANG X D, et al.Identification and flavor profile of a Thermoactinomycetaceae strain separated from Moutai-flavor Daqu[J].Food Science, 2018, 39(6):171-176.
[26] 李巧玉, 方芳, 堵国成, 等.魏斯氏菌在发酵食品中的应用[J].食品与发酵工业, 2017, 43(10):241-247.
LI Q Y, FANG F, DU G C, et al.The application of Weissella strains in fermented foods[J].Food and Fermentation Industries, 2017, 43(10):241-247.
[27] ZHANG X J, XIAO Q Q, WANG X, et al.Seasonal variations in physicochemical properties, volatile compounds, and microbial community structure of Dajiang fermented using a semi-controlled method[J].Food Bioscience, 2025, 63:105791.
[28] 张红霞, 徐岩, 杜海.酱香型白酒堆积发酵过程中真菌的结构及其来源分析[J].食品与发酵工业, 2024, 50(20):42-49.
ZHANG H X, XU Y, DU H.Fungal community and sources of heap fermentation during Jiangxiangxing Baijiu production[J].Food and Fermentation Industries, 2024, 50(20):42-49.