我国拥有悠久的酿酒历史,与西方国家酒类生产通常采用复杂度较低的混合菌种发酵不同,我国白酒生产主要依赖含有更为复杂微生物群系的大曲、小曲等作为糖化发酵剂。根据最高生产温度不同,大曲可分为高温大曲(60 ℃以上)、中温大曲(50~59 ℃)和低温大曲(40~50 ℃)等几种类型,这些大曲分别用于生产酱香型、浓香型和清香型白酒[1]。由于制曲原料中含有丰富的微生物,加之大曲后续发酵是在开放的环境中进行,在此过程中可以网罗大量周围环境中的各种微生物[2],这使得大曲中的微生物群落结构十分复杂。已有的研究发现,不同质量的大曲在微生物群落结构及一些理化品质方面均存在较大的差异[3]。这些差异化的微生物可以在酒曲发酵过程中及后续白酒酿造过程中产生不同种类和丰度的淀粉酶、纤维素酶、蛋白酶、酯酶等酶类,以及醇类、酯类、醛类等各类代谢产物,因此大曲质量直接影响最终白酒产品的品质,并促进不同白酒酒体风格的形成[4]。
越来越多的研究表明,中温大曲微生物群落结构不仅具有显著的品质依赖性特征,同时不同地区或企业制作的中温大曲在核心微生物群落结构方面也存在巨大差异[5]。KANG等[6]研究发现,糖多孢菌属(Saccharopolyspora)和葡萄球菌属(Staphylococcus)为中温大曲中的优势菌属。此外,吴树坤等[7]研究发现,宜宾和泸州浓香型中温大曲的优势菌属为魏斯氏菌属(Weissella)和高温放线菌属(Thermoactinomyces),遂宁地区浓香型浓香型中温大曲的优势菌属为Staphylococcus、克罗彭施泰特氏菌属(Kroppenstedtia)、芽孢杆菌属(Bacillus)和Saccharopolyspora。这些结果表明,不同地区制作的中温大曲在细菌群落结构方面存在明显的差别。与此同时,SHI等[8]进一步研究发现,与真菌相比,大曲中的细菌更容易受到非生物因素及物种相互作用的影响。因此,充分挖掘大曲的细菌群落结构及其与酒曲品质的关系对于进一步更好的优化大曲制作工艺及改进酒曲品质具有重要意义。此外,在众多白酒酿造微生物中,乳酸菌经常在大曲、酒糟和窖泥细菌群落中占据主导地位[9]。其可以利用真菌分解淀粉而产生的小分子糖类产生乳酸、醋酸等代谢产物,同时对于调节多糖代谢和氨基酸合成有重要作用[10]。因此,酒曲中乳酸菌的种群构成受到众多研究人员的关注。
湖北省襄阳市位于长江中流流域,具有亚热带季风气候特征。截至目前,关于该地区生产并用于浓香型白酒酿造的中温大曲细菌群落结构及其与酒曲滋味品质相关关系的研究尚存在空白,这使得相关企业在后续产品品质改良和升级中缺乏理论依据和方向。本研究通过高通量测序技术与传统可培养方法相结合,系统地研究了湖北襄阳地区中温大曲的细菌群落结构及主要乳酸菌类群,并结合电子舌技术对其滋味品质进行评估。研究不仅有助于深化对该地区中温大曲微生物特征和品质属性的认识,同时也丰富了酒曲细菌菌群与产品品质关系的理论基础。研究成果对本地区及国内相关酿酒企业开发利用酿酒微生物资源和改良制曲工艺具有重要的理论指导意义。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
中温大曲:10份大曲样品均采集自湖北省襄阳市某酿酒企业制曲车间,编号为LZZW1~10,所有样品均以小麦为原料,辅以大麦、豌豆等谷物,经过润麦、粉碎、加水和曲母搅拌、人工踩踏成砖状等工序后,放入曲房堆积发酵30 d,入库贮存3个月后得到成熟曲块。采样时在公司经验丰富的生产工人协助下从储曲车间不同位置采集完整的成熟曲块。具体而言,本研究将公司储曲车间从门口到房间最内部均分为5个区域,每个区域从曲堆表面和内部各采集一块大曲,以确保样本具有足够的空间代表性。样品采集后,将其放入无菌袋中密封,随后迅速运回至实验室粉碎成曲粉,并分别用于高通量测序、酒曲中乳酸菌分离鉴定和酒曲理化指标及滋味品质的测定。
1.1.2 试剂
MRS培养基(牛肉膏、蛋白胨、酵母膏、柠檬酸二胺、KH2PO4、MnSO4·H2O、MgSO4·7H2O、乙酸钠、葡萄糖和吐温-80,均为分析纯),北京奥博星生物技术有限公司;E.Z.N.ATM Mag-Bind DNA提取试剂盒,德国QIAGEN公司;FastPfu Fly DNA Polymerase、dNTPs Mix、5×TransStartTM FastPfu Buffer,上海桑尼生物科技有限公司;电子舌参比溶液、内部溶液和外部溶液,日本INSENT公司。
1.2 仪器与设备
MiSeq PE300高通量测序平台,美国Illumina公司;JFSD-100Ⅱ粉碎机,上海隆拓仪器设备有限公司;AW-1水分活度仪,无锡碧波电子设备厂;K1100全自动凯式定氮仪,山东海能科学仪器有限公司;TG16MW微量高速冷冻离心机,湖南赫西仪器装备有限公司;R40-ⅡB2生物安全柜,成都壹科医疗器械有限公司;S1000梯度PCR仪,美国Bio-Rad公司;DG250厌氧工作站,英国DonWhitley公司;LRH-70生化恒温培养箱,上海一恒科学仪器有限公司;SA402B电子舌系统,日本INSENT公司。
1.3 实验方法
1.3.1 中温大曲中总DNA提取、PCR扩增及高通量测序
按照E.Z.N.ATM Mag-Bind DNA试剂盒的说明书对中温大曲样品进行总DNA提取,参照YANG等[11]的方法,使用引物338F(5′-ACTCCTACGGGAGGCAGCAG-3′)和806R(5′-GGACTACHVGGGTWTC-TAAT-3′)对细菌V3~V4区进行16S rRNA PCR扩增,扩增产物通过1.5%的琼脂糖凝胶回收并将浓度稀释至100 nmol/L后,寄往测序公司进行基于Illumina MiSeq PE300平台的高通量测序。
1.3.2 生物信息学分析
参照薛蓓等[12]的方法在QIIME(V1.9.1)分析平台对下机数据进行质控和生物信息学分析。其中,在97%的相似度阈值下进行分类操作单元(operational taxonomic units,OTU)聚类[13],使用UCHIME软件剔除含有嵌合体的OTU序列[14],选取代表性序列与RDP数据库(Version 11.5)[15]进行同源性比对,在置信度80%阈值条件下确定中温大曲各OTU的分类学地位。
1.3.3 中温大曲中乳酸菌的分离鉴定
采用10倍梯度稀释法对10份中温大曲进行梯度稀释,吸取200 μL合适梯度(10-4、10-5、10-6)的稀释液涂布于至含有质量分数为1.5% CaCO3的MRS培养基上,待培养基半干后倒置于30 ℃的厌氧工作站中培养48 h。挑选菌落形态不同的单菌落进行2~3次的平板划线纯化,把镜检结果为革兰氏阳性、过氧化氢阴性的疑似乳酸菌菌株通过甘油管藏法保藏于-80 ℃备用[16]。参照李娜等[17]的方法对疑似乳酸菌菌株进行富集并提取DNA基因组、PCR扩增16S rRNA基因全长序列(正、反向引物分别为27F 5′-AGAGTTTGATCCTGGCTCAG-3′和1495R 5′-CTAC-GGCTACCTTG-3′),最后对清洁纯化后的扩增产物进行连接和转化,将合格的阳性克隆子送至上海桑尼生物科技有限公司进行测序,返回的拼接序列在NCBI网站进行BLAST同源性比对,并采用邻接法构建系统发育树[18]。
1.3.4 中温大曲理化品质和滋味品质评价
根据行业标准QB/T 4257—2011《酿酒大曲通用分析方法》所规定的检测手段,对中温大曲水分含量、淀粉含量和酸度等理化指标进行了检测分析。此外,使用水分活度仪检测了大曲的水分活度;使用全自动凯式定氮仪测定了大曲中蛋白质的含量。参照王玉荣等[19]的方法,基于电子舌技术对中温大曲的滋味品质进行评价。具体而言,将50 g中温大曲样品用150 mL蒸馏水混匀,静置30 min后,10 000 r/min离心6 min取100 mL上清液,置于-20 ℃备用。本试验采用SA402B电子舌系统,该设备配有5个传感器和2个参比电极,其中CAO、COO、AE1、CTO和AAE传感器分别测定酸味、苦味、涩味、咸味和鲜味的相对强度。电子舌系统在测定之前对传感器进行活化、校正和自检,每个样品平行测定4次,取后3次测定数据用于后续分析。
1.3.5 数据处理
使用R(v4.0.5)软件的“reshape2”包(v1.4.4)和“ggplot2”包(v3.5.1)绘制优势菌门气泡图;使用“pheatmap”包(v1.0.12)绘制微生物基因功能热图;使用软件GraphPad Prism 9绘制滋味品质评价的小提琴图;使用MEGA5.0和R(v4.0.5)软件共同绘制乳酸菌系统发育树;使用Cytoscape(v3.7.2)软件绘制优势细菌属与滋味指标间的相关性网络图。
2 结果与分析
2.1 中温大曲细菌类群α多样性分析
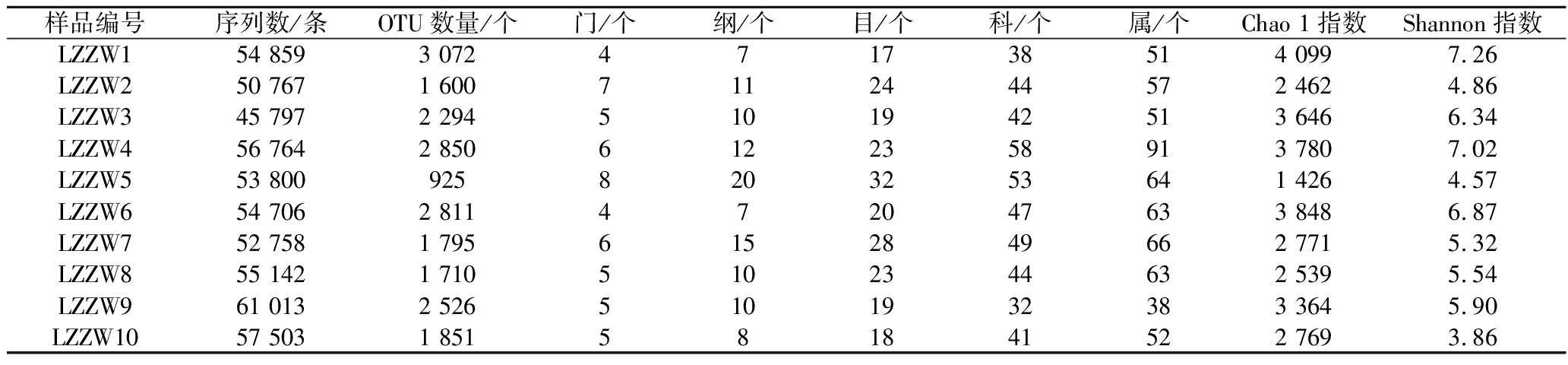
通过高通量测序,本研究中每份中温大曲样品平均得到54 311条(45 797~61 013)高质量16S rRNA基因序列(表1)。在97%的分类阈值下,这些序列被划分为5 488个OTU,平均每个样品中OTU的数量为2 143(925~3 072)个。经数据库对比后,所有测序序列被划分为8个门、26个纲、42个目、85个科和147个属(表1),其中仅有0.16%和1.84%的序列无法鉴定到门和属水平。在α多样性指标方面,本研究采用测序深度统一后的Chao 1指数和Shannon指数评估了样品中微生物群落的物种丰富度及多样性特征,结果发现中温大曲不同样品间Chao1指数和香农指数存在较大差异,2个指标的变异系数分别为0.27和0.20。这表明中温大曲不同曲块间微生物群落构成存在较大差异。
表1 中温大曲细菌类群α多样性指数及各分类学地位
Table 1 α diversity indices and taxonomic status of bacterial communities in medium-temperature Daqu
样品编号序列数/条OTU数量/个门/个纲/个目/个科/个属/个Chao 1指数Shannon指数LZZW154 8593 072471738514 0997.26LZZW250 7671 6007112444572 4624.86LZZW345 7972 2945101942513 6466.34LZZW456 7642 8506122358913 7807.02LZZW553 8009258203253641 4264.57LZZW654 7062 811472047633 8486.87LZZW752 7581 7956152849662 7715.32LZZW855 1421 7105102344632 5395.54LZZW961 0132 5265101932383 3645.90LZZW1057 5031 851581841522 7693.86
2.2 中温大曲细菌群落结构分析
本研究将中温大曲细菌类群中相对含量大于1.0%的门和属分别定义为优势细菌门和优势细菌属。其中优势细菌门的结果见图1。
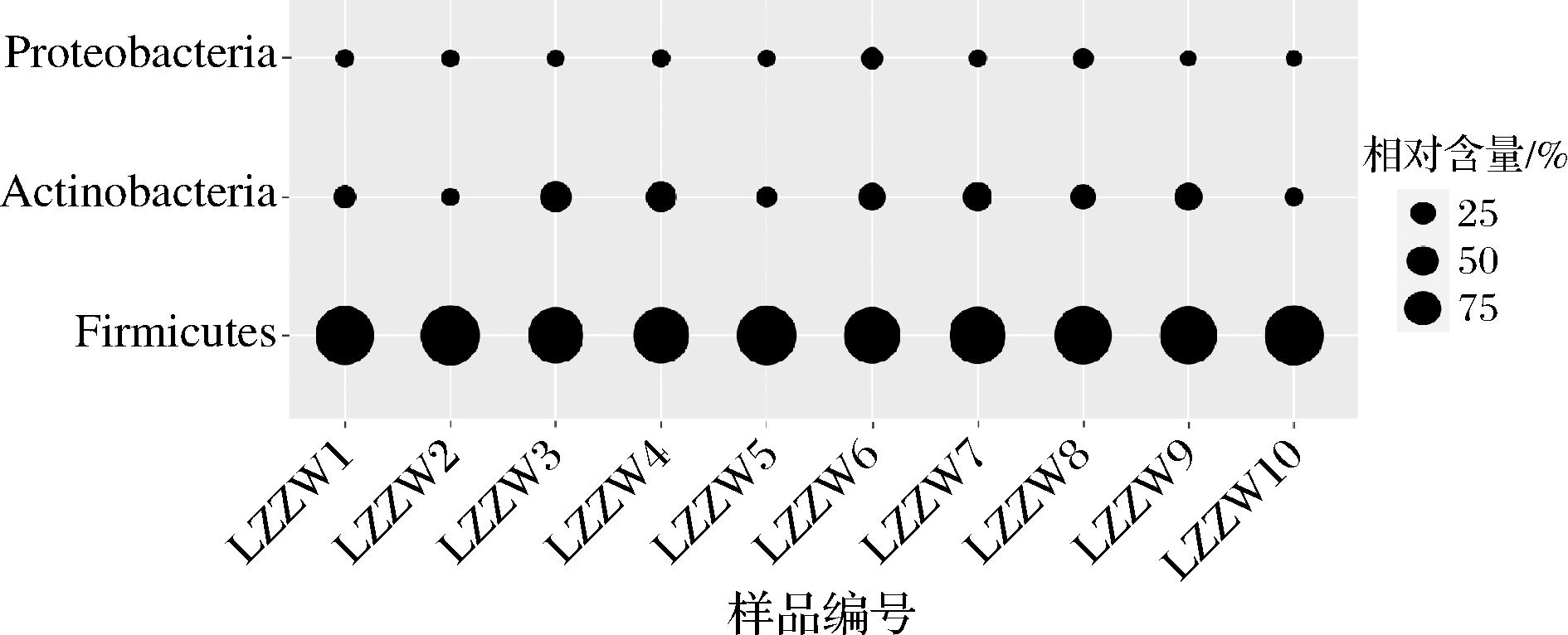
图1 中温大曲优势细菌门气泡图
Fig.1 Bubble chart of dominant bacterial phyla in medium-temperature Daqu
由图1可知,在门水平上,襄阳地区中温大曲细菌类群主要由厚壁菌门(Firmicutes,89.69%)、放线菌门(Actinobacteria,8.20%)和变形菌门(Proteobacteria,1.78%)构成,其中Firmicutes是该地区中温大曲细菌类群中的绝对优势菌门。据报道这些菌门也是其他地区中温大曲中的优势微生物[20],此外,在低温和高温大曲中也有类似的发现[21],表明上述3个菌门细菌是大曲中的常见菌和优势菌。在属水平上,中温大曲中平均相对含量在1%以上的优势细菌属共有10个,其在各个样品中的相对含量结果如图2所示。
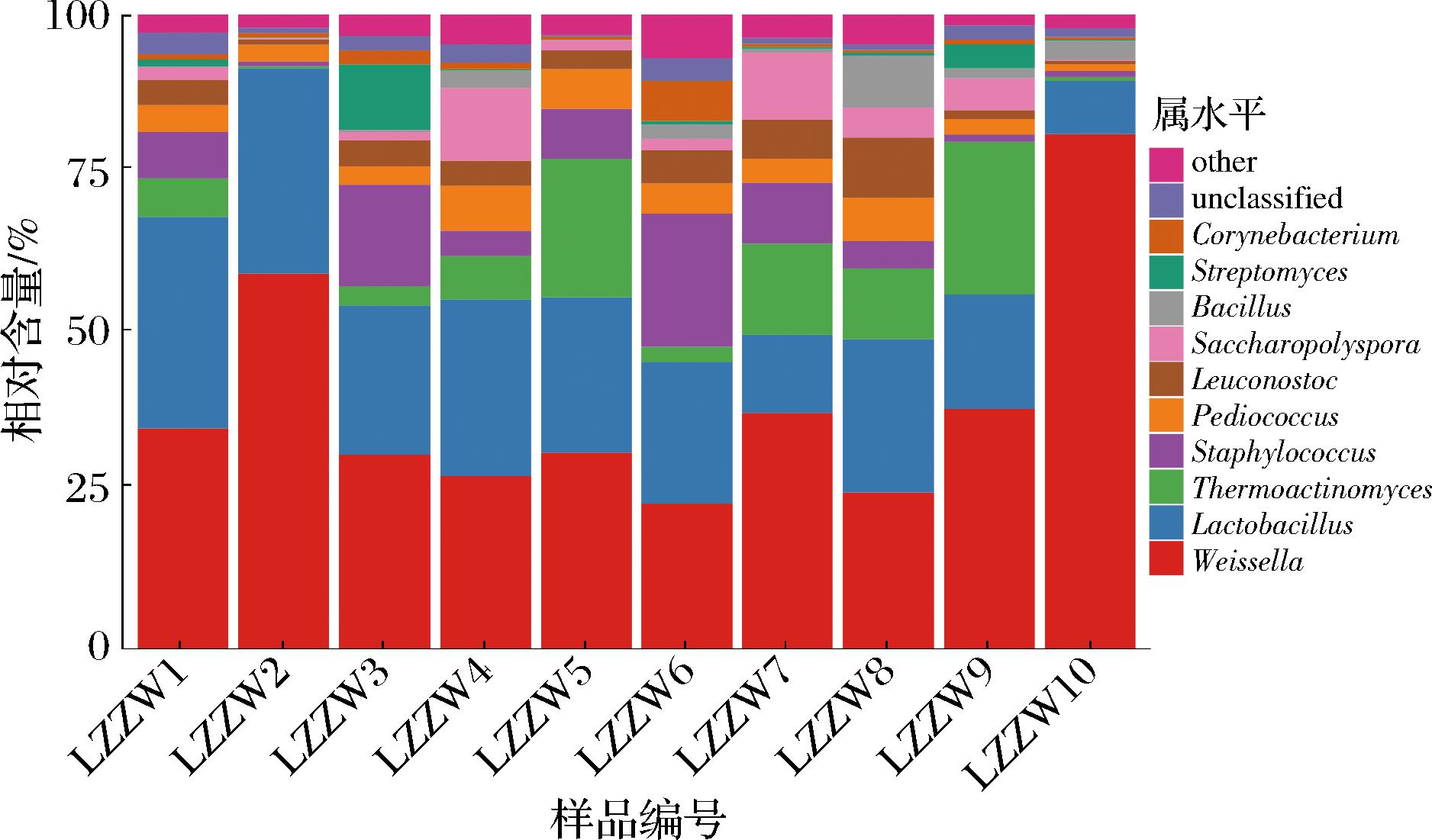
图2 中温大曲优势细菌属柱形图
Fig.2 Bar chart of dominant bacterial genera in medium-temperature Daqu
由图2可知,10个优势细菌属分别为隶属于Firmicutes的魏斯氏菌属(Weissella,38.65%)、乳杆菌属(Lactobacillus,22.67%)、葡萄球菌属(Staphylococcus,7.28%)、片球菌属(Pediococcus,4.19%)、明串珠菌属(Leuconostoc,3.88%)和芽孢杆菌属(Bacillus,1.89%),以及隶属于Actinobacteria的嗜热放线菌属(Thermoactinomyces,9.10%)、糖多孢菌属(Saccharopolyspora,3.87%)、链霉菌属(Streptomyces,1.69%)和棒状杆菌属(Corynebacterium,1.41%)。其中Weissella、Lactobacillus、Leuconostoc和Pediococcus均属于乳酸菌,这些菌合计占各样品的平均相对含量高达69.39%,中温大曲中主要乳酸菌的分布情况与YANG等[22]的研究结果一致。已有的研究发现,乳酸菌代谢产生的大量乳酸不仅可以通过掩盖酒精的辛辣味并延长回味,而且可以提高白酒的醇厚感和甜度[23]。此外,乳酸与酵母菌产生的酒精在酯化酶催化下可以生成白酒骨架风味物质之一的乳酸乙酯[24],同时乳酸也可以作为梭菌合成丁酸、戊酸等风味物质的底物,对于白酒中特定风味物质的形成发挥重要作用[25]。值得注意的是,白酒酿造中并非乳酸菌的数量越多越好,过多的乳酸菌会导致发酵体系中乳酸乙酯的过量积累,导致酒体风味不协调,适当控制乳酸菌数量则有利于酵母菌的酒精发酵,提高出酒率[26]。此外,该地区中温酒曲中Bacillus的相对含量仅为1.89%,这可能是由于乳酸菌产生的细菌素、过氧化物等代谢产物对Bacillus菌属具有一定的抑制作用有关[27]。此外,有研究发现Thermoactinomyces和Saccharopolyspora可产生纤维素酶、酯酶和耐热的α-淀粉酶等酶类,在发酵过程中水解纤维素、淀粉等大分子多糖产生葡萄糖和麦芽糖,从而促进白酒风味前体物质的形成[28]。KANG等[29]的研究则指出,Streptomyces在白酒酿造中可以产生土臭素,这是导致最终产品产生土腥味的主要原因,对白酒的风味具有负面影响。而Corynebacterium菌属在样品中的丰度虽然相对较低,但是该菌是酒曲中的关键菌种之一,其在推动大曲生态系统动态演替过程中发挥着关键作用[30]。上述结果表明,中温大曲中的大部分优势菌属对于白酒酿造具有积极的作用,但是也存在一定数量产生白酒不良风味的微生物,因此该地区酒曲品质仍具备进一步优化的空间。
不同企业之间同类型酒曲在微生物群落方面的差异也是研究者们关注的内容之一。ZHANG等[31]对五粮液集团包包曲中的微生物群落结构进行了解析,结果发现包包曲中的优势菌种主要来自于Lactobacillus、Leuconostoc和Weissella等菌属。该结果与本研究襄阳地区中温酒曲中的主要优势菌相似,但是具体到不同菌属在样品中所占的比例,2个企业存在明显差别。该结果在MA等[32]对山东潍坊、江苏宿迁、四川宜宾、四川绵阳、四川德阳5个地区企业生产的浓香型大曲微生物群落结构特征的研究中也得到了证实,其研究也发现,虽然很多微生物在不同地区浓香型大曲中均存在,但是其在不同企业样品中的比例存在巨大差异,而这种差异可能正是塑造不同酿酒企业产品风味特色的因素之一。
2.3 中温大曲细菌类群基因功能预测
本研究通过PICRUSt软件对中温大曲细菌类群进行了基因功能预测,所有细菌类群共注释到4 104个同源基团簇(clusters of orthologous group,COG),隶属于23个功能大类,各样品细菌类群基因功能预测结果如图3所示。
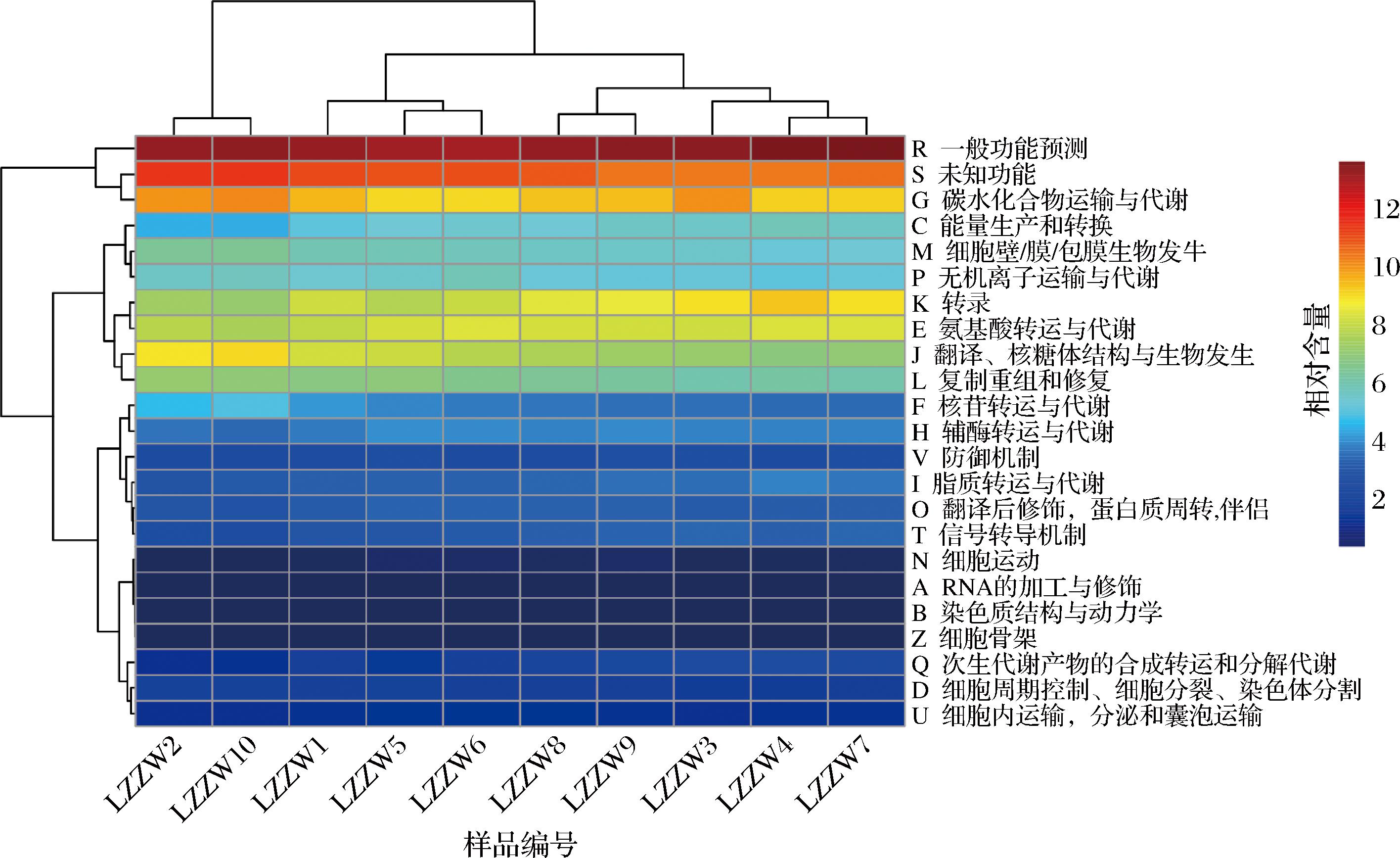
图3 中温大曲细菌类群基因功能预测热图
Fig.3 Heatmap of predicted gene functions of bacterial communities in medium-temperature Daqu
由图3可知,襄阳地区中温大曲细菌类群除维持细胞正常生命活动的功能外,在“G 碳水化合物运输与代谢”、“E 氨基酸转运与代谢”、“J 翻译、核糖体结构与生物发生”和“K 转录”方面的功能较强,而在“A RNA的加工与修饰”、“B 染色体结构与动力学”、“Z 细胞骨架”和“N 细胞运动”方面的功能较弱。“碳水化合物运输与代谢”及“氨基酸转运与代谢”功能较强说明,中温大曲中的细菌在碳水化合物和蛋白质利用方面发挥着重要作用[33]。这些细菌可能通过分泌各类水解酶来降解原料中的淀粉、蛋白质等大分子物质,为后续的酒精发酵提供必要的营养物质底物[34]。同时,这种活跃的代谢活动也可以促进风味前体物质的产生,例如,微生物通过氨基酸代谢一方面可以合成蛋白质、多肽等含氮物质;另一方面,氨基酸可以通过脱氨基、转氨基或脱羧基等反应生成为α-酮酸、胺和CO2等产物,有助于风味物的形成[35]。“翻译、核糖体结构与生物发生”和“转录”功能较强,表明这些细菌群体处于活跃的生长繁殖状态,这也意味着这些细菌能够持续分泌丰富的功能性酶类,参与到发酵过程中[23]。
2.4 乳酸菌的分离与鉴定
通过上述高通量测序的结果本研究揭示了中温大曲中的优势细菌类群为乳酸菌。为了进一步揭示这些乳酸菌在种水平的构成情况,本研究采用传统可培养方法从中温大曲中共分离得到19株乳酸菌菌株,经过对这些菌DNA基因组进行提取、16S rRNA基因全长序列PCR扩增和测序,得到了这些菌株16S rRNA基因序列信息。通过将上述16S全长序列进行测序和NCBI网站同源性比对鉴定,构建了包括模式菌株在内的乳酸菌分离株系统发育树,结果见图4。
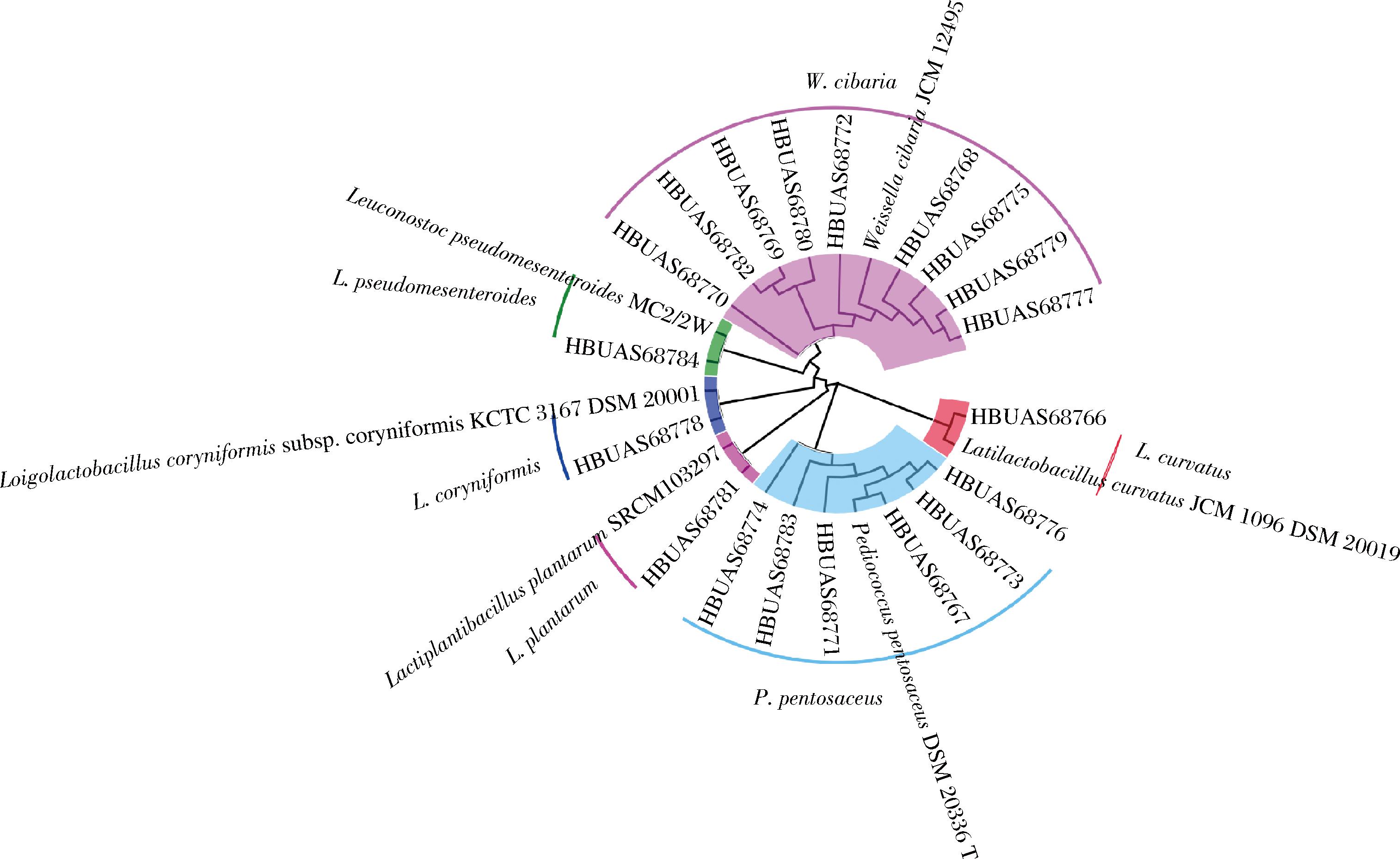
图4 中温大曲中乳酸菌分离株系统发育树
Fig.4 Phylogenetic tree of lactic acid bacteria isolated from medium temperature Daqu
由图4可知,19株乳酸菌分离株被鉴定为6个种,其中9株被鉴定为食窦魏斯氏菌(Weissella cibaria,47.37%),6株被鉴定为戊糖片球菌(Pediococcus pentosaceus,31.58%),余下4株分别被鉴定为棒状腐败乳杆菌(Loigolactobacillus coryniformis,5.26%)、植物乳植杆菌(Lactiplantibacillus plantarum, 5.26%)、假肠膜明串珠菌(Leuconostoc pseudomesenteroides,5.26%)和弯曲广泛乳杆菌(Latilactobacillus curvatus,5.26%)。由此可知,襄阳地区中温大曲的优势乳酸菌为Weissella cibaria,这与高通量测序结果一致。
2.5 中温大曲理化指标和滋味品质评价
对中温大曲基本的理化指标进行了测定,结果如表2所示。
表2 中温大曲理化指标的测定结果
Table 2 Determination of physicochemical parameters in medium-temperature Daqu
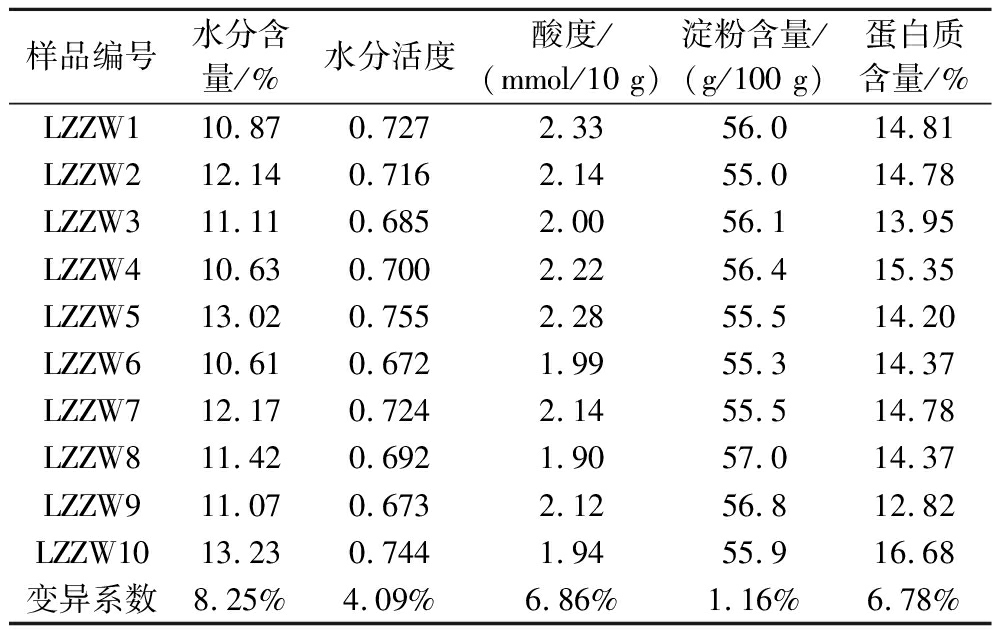
样品编号水分含量/%水分活度酸度/(mmol/10 g)淀粉含量/(g/100 g)蛋白质含量/%LZZW110.870.7272.3356.014.81LZZW212.140.7162.1455.014.78LZZW311.110.6852.0056.113.95LZZW410.630.7002.2256.415.35LZZW513.020.7552.2855.514.20LZZW610.610.6721.9955.314.37LZZW712.170.7242.1455.514.78LZZW811.420.6921.9057.014.37LZZW911.070.6732.1256.812.82LZZW1013.230.7441.9455.916.68变异系数8.25%4.09%6.86%1.16%6.78%
襄阳地区中温大曲水分含量平均为11.63%(10.61%~13.23%),变异系数为8.25%,水分活度平均为0.71(0.67~0.76),变异系数为4.09%;酸度平均为2.11(1.90~2.33) mmol/10 g,变异系数为6.86%;淀粉含量平均为55.95(55~57) g/100 g,变异系数平均为1.16%;蛋白质含量平均为14.71(12.82~16.68) g/100 g,变异系数为6.78%。上述结果表明,水分含量在不同曲块间的波动最大,这可能与不同曲块在车间储存时所处的位置差异导致水分蒸发速度不同有关。此外,与HOU等[20]基于宋河酒业中温大曲的研究结果相比,襄阳地区中温大曲的酸度相对较高。这表明襄阳中温大曲中有机酸积累较多,而这可能与本地区大曲中所富集的大量乳酸菌的代谢活动存在一定关系。本研究进一步利用电子舌对中温大曲的滋味品质进行了评价,电子舌各传感器对中温大曲滋味品质响应的相对强度见图5。
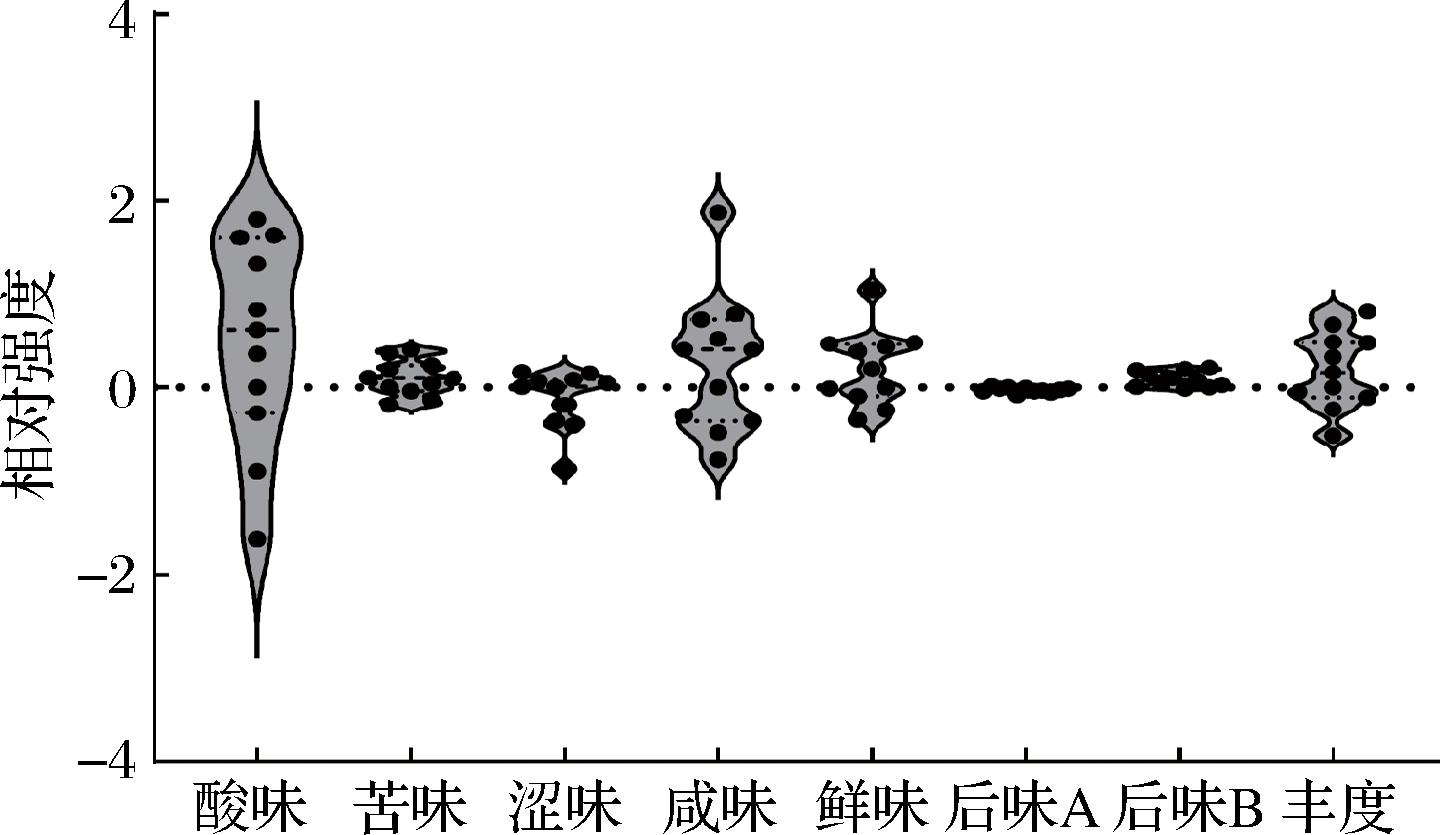
图5 电子舌各传感器对中温大曲滋味品质响应的相对强度
Fig.5 Relative intensity of electronic tongue sensor responses to taste quality of medium-temperature Daqu
由图5可知,酸味、咸味、鲜味和丰度是中温大曲中响应值最高的滋味指标,表明这些核心滋味指标具有较高的风味贡献度。与此同时,上述滋味指标以及涩味在样品间响应值的极差均大于1,尤其是酸味的差异最为明显,表明中温大曲在发酵过程中存在明显的曲块间滋味异质性。这种差异可能源于发酵微环境条件的局部差异以及乳酸菌等优势菌群的代谢活性差异,这导致关键呈味物质的生成与调控呈现非均匀性分布,最终影响大曲品质的批次一致性。具体而言,尽管乳酸菌在所有样品中均占据优势地位,但不同样品中乳酸菌的群落结构并不完全一致,从而导致各曲块各类酸性物质的产量也出现了较大差异[10]。此外,这些乳酸菌代谢过程中释放的乳酸可以通过螯合金属离子或调控酶活性影响涩味(如多酚类物质溶解性)和鲜味(如谷氨酸积累)的呈现[36],从而对酒曲的涩味和鲜味指标带来较大差异。这一结果表明,同一类型大曲,不同曲块间的品质也存在较大的差异,而这种差异可能与微生物的代谢活动存在密切的联系。
2.6 中温大曲滋味品质与细菌属的相关性分析
为进一步探究中温大曲滋味品质与细菌类群之间的关系,使用相关性网络图对中温大曲的8个滋味指标和10个优势细菌属进行了分析,结果见图6。
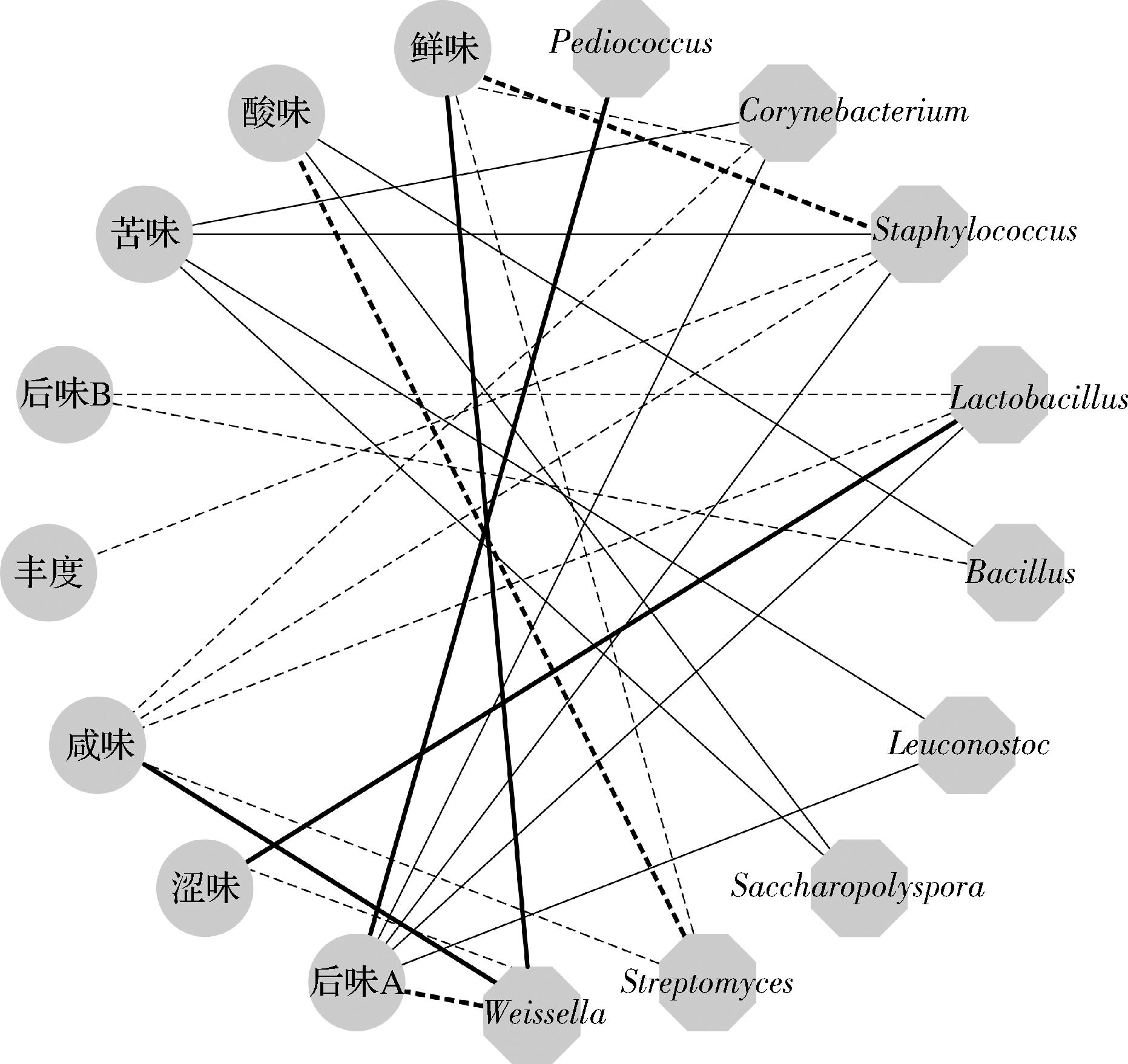
图6 中温大曲滋味品质与优势细菌菌属间的相关性网络图
Fig.6 Correlation network between taste quality and dominant bacterial genera in medium-temperature Daqu
注:实线表示两者呈正相关,虚线表示两者呈负相关,加粗线段代表P<0.05。
中温大曲中滋味指标与优势细菌属存在14个正相关关系和13个负相关关系,但仅有4个正相关关系和3个负相关关系具有统计学意义。其中Weissella与咸味和鲜味呈显著正相关(P<0.05),与后味A(涩味的回味)呈极显著负相关(P<0.01),Lactobacillus与涩味存在极显著正相关关系(P<0.01),Pediococcus与后味A呈显著正相关性(P<0.05),Staphylococcus与鲜味存在显著负相关关系(P<0.05),Streptomyces与酸味存在极显著负相关性(P<0.01)。尽管有一些研究也报道了与本研究类型的结果,如XIANG等[37]的研究指出Pediococcus作为乳酸菌的一种,该菌可以产生乳酸,对白酒的后味有重要影响,与本研究结果一致,但目前对于菌群与滋味指标相关性的作用机制仍缺乏系统阐释。尽管如此,本研究通过构建关键菌属与滋味特征的关联网络,初步揭示了中温大曲风味形成的微生物代谢基础,为基于菌群定向调控的大曲品质优化提供了理论依据。
3 结论
本研究利用高通量测序技术和传统可培养方法对襄阳地区中温大曲细菌类群进行解析,并使用电子舌进行了滋味品质评价。结果发现,襄阳地区中温大曲的细菌群落以Weissella、Lactobacillus、Staphylococcus、Pediococcus和Leuconostoc为核心优势菌群,乳酸菌类群在各样本中占据绝对主导地位,而其中占比最高的乳酸菌是Weissella cibaria。菌群功能分析发现,中温大曲中的细菌在碳水化合物和蛋白质利用方面发挥着重要作用。除常规酿造功能菌外,中温大曲中还存在一定比例的Streptomyces等对白酒风味具有不良影响的微生物,需要进一步加强制曲过程中相关微生物的管控。不同曲块在酸味、涩味、咸味、鲜味及丰度等指标方面存在较大差异,其中酸味差异最为突出,这可能与菌群代谢活动的异质性密切相关。此外,中温大曲的滋味指标与优势细菌属之间存在着大量复杂而显著的关联网络。本研究深化了人们对襄阳地区中温大曲细菌群落结构及其与滋味品质相关关系的认知,同时为区域酿酒企业改进制曲工艺提供了重要的理论依据,对推动传统酿造技术的现代化发展具有一定指导意义。
[1] 田瑞杰. 中温大曲原核微生物群落解析及高产淀粉酶菌株的筛选与应用探究[D].郑州:郑州轻工业大学, 2022.
TIAN R J.Analysis of prokaryotic microbial community in medium temperature Daqu and exploration of screening and application of high amylase producing strains[D].Zhengzhou:Zhengzhou University of Light Industry, 2022.
[2] GOU M, WANG H Z, YUAN H W, et al.Characterization of the microbial community in three types of fermentation starters used for Chinese liquor production[J].Journal of the Institute of Brewing, 2015, 121(4):620-627.
[3] ZHANG Y D, DING F, SHEN Y, et al.Characteristics of the microbiota and metabolic profile of high-temperature Daqu with different grades[J].World Journal of Microbiology and Biotechnology, 2022, 38(8):137.
[4] TIAN N, GUO X, WANG M Z, et al.Bacterial community diversity of shilixiang Baijiu Daqu based on metagenomics[J].Journal of Food Biochemistry, 2020, 44(10):e13410.
[5] 侯强川, 王玉荣, 王文平, 等.茅台和尧治河高温大曲细菌群落结构差异及功能预测[J].食品与发酵工业, 2022, 48(1):36-44.
HOU Q C, WANG Y R, WANG W P, et al.Difference of bacterial community structure and functional prediction in high-temperature Daqu of Maotai and Yaozhihe[J].Food and Fermentation Industries, 2022, 48(1):36-44.
[6] KANG J M, CHEN X X, HAN B Z, et al.Insights into the bacterial, fungal, and phage communities and volatile profiles in different types of Daqu[J].Food Research International, 2022, 158:111488.
[7] 吴树坤, 谢军, 程铁辕, 等.不同地区浓香型大曲质量指标与细菌群落相关性研究[J].食品研究与开发, 2019, 40(4):158-164.
WU S K, XIE J, CHENG T Y, et al.Correlation between quality index and bacterial community of Luzhou flavor Daqu[J].Food Research and Development, 2019, 40(4):158-164.
[8] SHI W, CHAI L J, FANG G Y, et al.Spatial heterogeneity of the microbiome and metabolome profiles of high-temperature Daqu in the same workshop[J].Food Research International, 2022, 156:111298.
[9] ZHANG Z D, MENG Y L, ZHAN J, et al.Comparative analysis of microbial diversity and functional characteristics of low-temperature Daqu from different regions in China[J].Food and Bioproducts Processing, 2024, 147:483-494.
[10] YANG L, CHEN J, LI Z J, et al.Effect of lactic acid bacteria on the structure and potential function of the microbial community of Nongxiangxing Daqu[J].Biotechnology Letters, 2023, 45(9):1183-1197.
[11] YANG J G, DOU X, MA Y Y.Diversity and dynamic succession of microorganisms during Daqu preparation for Luzhou-flavour liquor using second-generation sequencing technology[J].Journal of the Institute of Brewing, 2018, 124(4):498-507.
[12] 薛蓓, 卢灏泽, 杨帆, 等.高通量测序技术分析西藏不同海拔地区曲拉微生物多样性[J].食品科学, 2022, 43(14):176-182.
XUE B, LU H Z, YANG F, et al.High-throughput sequencing technology to analyze microbial community diversity in Qula at different altitudes in Tibet[J].Food Science, 2022, 43(14):176-182.
[13] HOU Q C, WANG Y R, NI H, et al.Deep sequencing reveals changes in prokaryotic taxonomy and functional diversity of pit muds in different distilleries of China[J].Annals of Microbiology, 2022, 72(1):12.
[14] EDGAR R C, HAAS B J, CLEMENTE J C, et al.UCHIME improves sensitivity and speed of Chimera detection[J].Bioinformatics, 2011, 27(16):2194-2200.
[15] COLE J R, WANG Q, FISH J A, et al.Ribosomal Database Project:Data and tools for high throughput rRNA analysis[J].Nucleic Acids Research, 2014, 42(D1):D633-D642.
[16] GUO Z, WANG Y R, XIANG F S, et al.Bacterial diversity in pickled cowpea (Vigna unguiculata[Linn.] walp) as determined by illumina MiSeq sequencing and culture-dependent methods[J].Current Microbiology, 2021, 78(4):1286-1297.
[17] 李娜, 王玉荣, 葛东颖, 等.当阳地区鲊广椒中乳酸菌的分离鉴定及其应用[J].中国酿造, 2019, 38(2):37-41.
LI N, WANG Y R, GE D Y, et al.Isolation, identification and application of lactic acid bacteria from Zhaguangjiao in Dangyang[J].Chinese Brewing, 2019, 38(2):37-41.
[18] KUMAR S, STECHER G, LI M, et al.MEGA X:Molecular evolutionary genetics analysis across computing platforms[J].Molecular Biology and Evolution, 2018, 35(6):1547-1549.
[19] 王玉荣, 张俊英, 胡欣洁, 等.湖北孝感和四川成都地区来源的酒曲对米酒滋味品质影响的评价[J].食品科学, 2015, 36(16):207-210.
WANG Y R, ZHANG J Y, HU X J, et al.Effect of rice wine koji collected from different regions on the taste of rice wine[J].Food Science, 2015, 36(16):207-210.
[20] HOU X G, HUI M, SUN Z K, et al.Comparative analysis of the microbiotas and physicochemical properties inside and outside medium-temperature Daqu during the fermentation and storage[J].Frontiers in Microbiology, 2022, 13:934696.
[21] ZHENG X W, YAN Z, HAN B Z, et al.Complex microbiota of a Chinese “Fen” liquor fermentation starter (Fen-Daqu), revealed by culture-dependent and culture-independent methods[J].Food Microbiology, 2012, 31(2):293-300.
[22] YANG Y, WANG S T, LU Z M, et al.Metagenomics unveils microbial roles involved in metabolic network of flavor development in medium-temperature Daqu starter[J].Food Research International, 2021, 140:110037.
[23] CAI W C, WANG Y R, LIU Z J, et al.Depth-depended quality comparison of light-flavor fermented grains from two fermentation rounds[J].Food Research International, 2022, 159:111587.
[24] PANG X N, CHEN C, HUANG X N, et al.Influence of indigenous lactic acid bacteria on the volatile flavor profile of light-flavor Baijiu[J].LWT, 2021, 147:111540.
[25] CHWIALKOWSKA J, DUBER A, ZAGRODNIK R, et al.Caproic acid production from acid whey via open culture fermentation—Evaluation of the role of electron donors and downstream processing[J].Bioresource Technology, 2019, 279:74-83.
[26] 何培新, 胡晓龙, 郑燕, 等.中国浓香型白酒“增己降乳”研究与应用进展[J].轻工学报, 2018, 33(4):1-12.
HE P X, HU X L, ZHENG Y, et al.Research and application progress of “ethyl caproate-increasing and ethyl lactate-decreasing” in brewing of Chinese Luzhou-flavor liquor[J].Journal of Light Industry, 2018, 33(4):1-12.
[27] WANG P, WU Q, JIANG X J, et al.Bacillus licheniformis affects the microbial community and metabolic profile in the spontaneous fermentation of Daqu starter for Chinese liquor making[J].International Journal of Food Microbiology, 2017, 250:59-67.
[28] GUAN Z B, ZHANG Z H, CAO Y, et al.Analysis and comparison of bacterial communities in two types of ‘wheatQu’, the starter culture of Shaoxing rice wine, using nested PCR-DGGE[J].Journal of the Institute of Brewing, 2012, 118(1):127-132.
[29] KANG J M, HUANG X N, LI R S, et al.Deciphering the core microbes and their interactions in spontaneous Baijiu fermentation:A comprehensive review[J].Food Research International, 2024, 188:114497.
[30] YANG L, FAN W L, XU Y.Qu-omics elucidates the formation and spatio-temporal differentiation mechanism underlying the microecology of high temperature Daqu[J].Food Chemistry, 2024, 438:137988.
[31] ZHANG Q M, DU G C, CHEN J, et al.Systematic analysis of Baobaoqu fermentation starter for Wuliangye Baijiu by the combination of metagenomics and metabolomics[J].Frontiers in Microbiology, 2022, 13:1062547.
[32] MA S Y, SHANG Z C, CHEN J, et al.Differences in structure, volatile metabolites, and functions of microbial communities in Nongxiangxing Daqu from different production areas[J].LWT, 2022, 166:113784.
[33] ZHAO X X, XIANG F S, TANG F X, et al.Bacterial communities and prediction of microbial metabolic pathway in rice wine koji from different regions in China[J].Frontiers in Microbiology, 2022, 12:748779..
[34] FU J X, CHEN L, YANG S Z, et al.Metagenome and analysis of metabolic potential of the microbial community in pit mud used for Chinese strong-flavor liquor production[J].Food Research International, 2021, 143:110294.
[35] XU Y, ZHI Y, WU Q, et al.Zygosaccharomyces bailii is a potential producer of various flavor compounds in Chinese Maotai-flavor liquor fermentation[J].Frontiers in Microbiology, 2017, 8:2609.
[36] FAN Y, HUANG X N, CHEN J Y, et al.Formation of a mixed-species biofilm is a survival strategy for unculturable lactic acid bacteria and Saccharomyces cerevisiae in Daqu, a Chinese traditional fermentation starter[J].Frontiers in Microbiology, 2020, 11:138.
[37] XIANG F S, CAI W C, GUO Z, et al.Comparative analysis of sensory features, microbial diversity, and their correlations in light-flavor Daqu from different regions[J].Food Science &Nutrition, 2024, 12(5):3391-3404.