酱油是深受全球消费者喜爱的一种传统调味品。盐是影响发酵进程和酱油品质的关键因素之一,在酱油发酵过程中起到抑制杂菌生长、调节发酵环境渗透压、影响菌群代谢活动等方面的作用。然而,过量摄入钠或者食盐,会极大地增加人体罹患高血压、心脑血管病等慢性疾病的风险[1]。随着《中国食品工业减盐指南》、《健康中国行动(2019—2030年)》等文件的公布[2],减盐酱油的开发受到广泛关注。减盐发酵体系较难控制腐败菌或发酵有害菌的生长,进而影响酱油的品质与安全。目前,减盐发酵体系中微生物群落组成及变化及其对酱油发酵的影响尚不完全清楚。因此,揭示减盐发酵过程微生物的组成与变化,对于调控和优化酱油减盐发酵具有重要意义。
酱油发酵是一个多菌种混合代谢过程,主要功能微生物包括霉菌、酵母菌、乳酸菌以及其他细菌。近年研究发现,减盐会导致原有微生物群落失衡,腐败微生物数量会显著增长。例如,在高盐稀态酱油的梯度减盐发酵中,功能微生物如魏斯氏菌(Weissella)、接合酵母属(Zygosaccharomyces)和假丝酵母属(Candida)的数量减少,而腐败微生物如芽胞杆菌属(Bacillus)、葡萄球菌属(Staphylococcus)、乳植杆菌属(Lactiplantibacillus)和库特氏菌属(Kurthia)的数量则显著增加[3]。在低盐固态酱油发酵过程细菌组成的研究中发现,肠杆菌属(Enterobacter)是影响酱油品质与风味的优势腐败菌[4]。筛选出能有效抑制腐败菌生长的有益微生物是恢复减盐酱油品质与风味的重要前提。乳酸菌作为一类在食品发酵领域具有重要作用的微生物[5],它不仅能够产生多种有机酸及细菌素等物质,抑制有害微生物的生长,维持发酵过程的稳定性和产品的安全性[6],还能通过自身代谢为食品贡献独特风味[7]。已有研究证实,添加乳酸菌协同发酵能减少腐败微生物数量,进而恢复发酵食品品质。例如,有研究利用功能细菌副肠膜状魏斯氏菌(Weissella paramesenteroides)JL-5和解淀粉芽孢杆菌(Bacillus amyloliquefaciens)JDF-1协同发酵,抑制减盐酱油中的腐败细菌,成功实现了酱油的减盐发酵并提高减盐酱油的品质和风味[8]。利用对腐败肠杆菌有抑制作用的乳酸片球菌(Pediococcus acidilactici)WT1协同发酵,鲜味、甜味氨基酸含量分别提高35.16%、13.44%,挥发性风味物质总量提高19.95%[9]。还有研究筛选得到一株能抑制腐败微生物的植物乳植杆菌(Lactiplantibacillus plantarum)SCP53,将其与腐败菌共接种发酵萝卜,证实该菌株可抑制泡菜生花、改善泡菜品质[10]。由此可见,乳酸菌在传统酿造食品的发酵过程中,凭借其对腐败菌的抑制作用,展现出了巨大的应用潜力。
本研究旨在剖析酱油减盐发酵体系细菌群落结构的动态变化,筛选出既具备抑制优势腐败菌能力,又符合酱油减盐发酵需求的乳酸菌。以期为乳酸菌协同发酵恢复减盐酱油品质提供参考依据,也为发酵食品领域中腐败细菌的有效控制开拓新思路。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株
本研究所用菌株均分离自酱油,其中L.plantarum、P.acidilactici及戊糖片球菌(Pediococcus pentosaceus)等10株菌为本研究室保藏,如表1所示。
表1 本研究所用菌株
Table 1 Strains used in this study

菌株来源L.plantarum JL-20本研究室保藏,来源于酱油酱醪P.acidilactici WT1本研究室保藏,来源于酱油酱醅P.acidilactici WT4本研究室保藏,来源于酱油酱醅P.acidilactici ZQ3本研究室保藏,来源于酱油酱醅P.acidilactici ZQ6本研究室保藏,来源于酱油酱醅P.acidilactici ZQ7本研究室保藏,来源于酱油酱醅P.acidilactici ZQ8本研究室保藏,来源于酱油酱醅P.pentosaceus WT6本研究室保藏,来源于酱油酱醅P.pentosaceus WT7本研究室保藏,来源于酱油酱醅P.pentosaceus WT8本研究室保藏,来源于酱油酱醅地衣芽孢杆菌(Bacillus licheniformis) DYY本研究贝莱斯芽孢杆菌(Bacillus velezensis)BLY1本研究B.velezensis BLY2本研究B.amyloliquefaciens JDY本研究枯草芽孢杆菌(Bacillus subtilis) KCY本研究蜡样芽胞杆菌(Bacillus cereus) LYY本研究沙福芽孢杆菌(Bacillus safensis) SFY本研究短小芽孢杆菌(Bacillus pumilus) DXY本研究屎肠球菌(Enterococcus faecium) SCY1本研究E.faecium SCY2本研究E.faecium SCY3本研究阪崎氏肠杆菌(Enterobacter sakazakii) BQY本研究霍氏肠杆菌(Enterobacter hormaeche ) HSY1本研究E.hormaechei HSY2本研究阴沟肠肝菌(Enterobacter cloacae) YGY1本研究
续表1

菌株来源E.cloacae YGY2本研究腐生葡萄球菌(Staphylococcus saprophyticus) FSY本研究鸡葡萄球菌(Staphylococcus gallinarum) JPY本研究尼泊尔葡萄球菌(Staphylococcus nepalensis) NPY1本研究S.nepalensis NPY2本研究
1.1.2 培养基
MRS培养基(g/L):蛋白胨10.00、牛肉粉5.00、酵母粉4.00、葡萄糖20.00、K2HPO4 2.00、乙酸钠5.00、柠檬酸三铵2.00、MgSO4·7H2O 0.20、MnSO4·4 H2O 0.10、吐温-80 1.00、琼脂20.00、山梨酸1.00,121 ℃灭菌15 min。
LB培养基(g/L):胰蛋白胨10.00、酵母提取物5.00、NaCl 10.00、琼脂15.00,121 ℃灭菌15 min。
酱油模拟培养基[11]:黄豆粉∶小麦粉=1∶1(质量比),加入5倍水(g∶mL)混匀,再加入100 U/g高温淀粉酶97 ℃酶解1 h,冷却至60 ℃后加入1 000 U/g蛋白酶和150 U/g糖化酶60 ℃酶解0.5 h,121 ℃灭菌15 min。
1.1.3 试剂
有机酸标样,美国Sigma公司;酵母提取物、胰蛋白胨,Oxoid公司;PCR引物,上海天霖生物科技有限公司;细菌基因组提取试剂盒,天根生化科技(北京)有限公司。
1.2 仪器与设备
ProFlexTM PCR仪,美国Thermo Fisher公司;HPLC-1260高效液相色谱仪,美国Agilent公司;Nano Drop 2000c超微量分光光度计,美国Thermo Fisher公司;高压灭菌锅,上海医用核子仪器厂;5424R型离心机,德国Eppendorf公司;UV-1240紫外可见分光光度计,日本岛津公司;HHWS-Ⅲ-300恒温恒湿培养箱,上海跃进医疗器械厂。
1.3 实验方法
1.3.1 酱油减盐发酵工艺
制曲工艺:将黄豆加3倍(质量比)水,润料10 h,在121 ℃下灭菌20 min,冷却至室温。以m(黄豆)∶m(小麦粉)=6∶4混合(小麦粉不需杀菌),再加入混合原料0.15%(质量分数)的酱油曲精。在温度30 ℃,湿度95%的制曲仓培养,适时翻曲,待曲料表面长满黄绿色菌丝即为成曲。
发酵工艺:将200 g成曲,按成曲∶盐水=1∶1的比例,与不同盐浓度的盐水混合,体系终浓度盐含量为140、120 g/L和100 g/L。在发酵第14天加入成曲质量1倍的盐水,盐水浓度分别为140、120 g/L和100 g/L。发酵容器采用1 L烧杯,用封口膜与铝箔纸封口,在恒温30 ℃发酵仓中进行发酵。前一周每天搅拌,后面每5 d搅拌1次,分别在第0、5、10、14、20、25、30、40天取混合均匀的固液混合物,每次取样10 g,于-80 ℃保存。
1.3.2 微生物多样性分析
样品DNA提取采用液氮研磨与E.Z.N.ATM Mag-Bind Soil DNA Kit提取试剂盒抽提相结合的方法。Nano Drop 2000c超微量分光光度计测定提取的样品DNA浓度,利用琼脂糖凝胶电泳检测提取的DNA完整度。细菌测序区域为16S rRNA的V3~V4可变区,真菌测序区域为18S rRNA的ITS1-ITS2可变区,获得的扩增子由上海生物工程股份有限公司进行测序信息分析。
1.3.3 菌株分离与纯化
称取1.00 g酱醪与9.00 mL生理盐水混匀,梯度稀释后于MRS培养基和LB培养基涂布,在37 ℃培养12~48 h。挑取单菌落划线纯化3次,然后接种单菌落进行培养和保存。
1.3.4 菌种鉴定
利用细菌基因组DNA提取试剂盒提取菌株的基因组DNA,用16S rRNA通用引物27 F和1492 R进行PCR分析,产物送天霖生物科技有限公司测序。测序结果在NCBI上进行BLAST比对并进行菌种的鉴定。
1.3.5 抑菌能力分析
采用牛津杯法,腐败细菌等指示菌接种至LB液体培养基中,37 ℃,220 r/min培养12 h。乳酸菌接种至MRS肉汤培养基,37 ℃静置培养24 h,8 000 r/min离心10 min,得到发酵上清液。将10 mL 2%琼脂倒入平板,待其凝固。先将无菌牛津杯放置其上,再倒入15 mL含指示菌的LB培养基(指示菌浓度为106 CFU/mL),待其凝固将牛津杯取出。加入100 μL发酵上清于孔内,4 ℃静置2 h后,37 ℃培养箱中静置培养8 h,通过测定抑菌圈大小比较抑菌能力。
采用共培养法,将乳酸菌分别与腐败菌以2%的接种量,两两接种至模拟培养基中,37 ℃静置培养72 h后,进行活菌计数。
1.3.6 温度和盐对乳酸菌的影响
取对数期乳酸菌、腐败细菌菌液以2%的接种量分别接种至MRS培养基、LB培养基中,20 ℃静置/220 r/min培养24 h,测定OD600。
取对数期乳酸菌、腐败细菌菌液离心(8 000 r/min、离心5 min)取菌体,用生理盐水洗涤2次,以1×109 CFU/mL分别接入含有140 g/L NaCl的MRS培养基、LB培养基中,37 ℃培养箱中静置/220 r/min培养48 h后,进行活菌计数计算存活率。
1.3.7 有机酸的测定
取对数期乳酸菌菌液以2%的接种量接种至MRS液体培养基中,37 ℃静置培养24 h。取适量发酵液8 000 r/min、离心10 min,将发酵上清液用0.22 μm无菌水系滤膜过滤备用。
采用高效液相色谱法测定[12],液相系统:岛津20A,色谱柱:Aminex-HPX-87H(300 mm×7.8 mm,9 μm);流动相:5 mmoL/L稀硫酸,进样体积10 μL,洗脱速度0.5 mL/min,洗脱时间30 min,柱温40 ℃,检测器UV 210 nm。
1.3.8 统计及数据分析
采用SPSS 19.0、Excel、Origin 8.0软件进行数据分析及可视化,以P<0.05表示数据之间的显著性差异,所有实验均重复3次。
2 结果与分析
2.1 酱油减盐发酵体系细菌组成与变化
前期研究发现,体系中盐含量降至14%时酱醪中微生物组成与高盐对照存在较大差异,尤其是细菌组成中腐败菌组成和数量显著增加,影响了高盐稀态酱油正常发酵进程[3]。因此,本研究采用先固后稀的发酵工艺,分析体系中的腐败细菌组成与变化,为利用功能菌株调控酱油发酵提供参考。本研究通过对140、120 g/L和100 g/L发酵酱醪不同阶段样品进行细菌菌群16S基因序列高通量测序,分析减盐后酱醪中细菌菌群的结构性变化。其中,D0、E0、F0分别代表发酵第0天浓度分别为140 g/L、120 g/L、100 g/L的发酵样品组别。共获得3 399 074条Reads,每个样品至少产生108 620条Clean Reads。各样品平均获得134 960条有效序列,序列的总碱基长度平均为57 549 308 bp,最长的序列长度为476 bp,最短的序列长度为350 bp,各样品Goods Coverage均在0.999以上,说明数据采集具有足够的完整性及代表性。
如图1、图2所示,经分类学注释分析发现,减盐酱醪中的细菌涵盖了5个细菌门,包括假单胞菌门(Pseudomonadota)(21.28%~96.07%)、芽孢杆菌门(Bacillota)(3.75%~50.40%)、酸杆菌门(Acidobacteriota)(0%~2.74%)、放线菌门(Actinomycetota)(0.06%~2.25%)、疣微菌门(Verrucomicrobiota)(0%~1.14%)。这些细菌源自16个属,不同盐浓度样品中丰度占比前五的属依次是肠杆菌属(Enterobacter)(16.38%~79.13%)、葡萄球菌属(Staphylococcus)(0.05%~71.76%)、芽孢杆菌属(Bacillus)(0.79%~34.46%)、盐单胞菌属(Halomonas)(0.06%~3.98%)以及肠球菌属(Enterococcus)(0.37%~3.73%)。
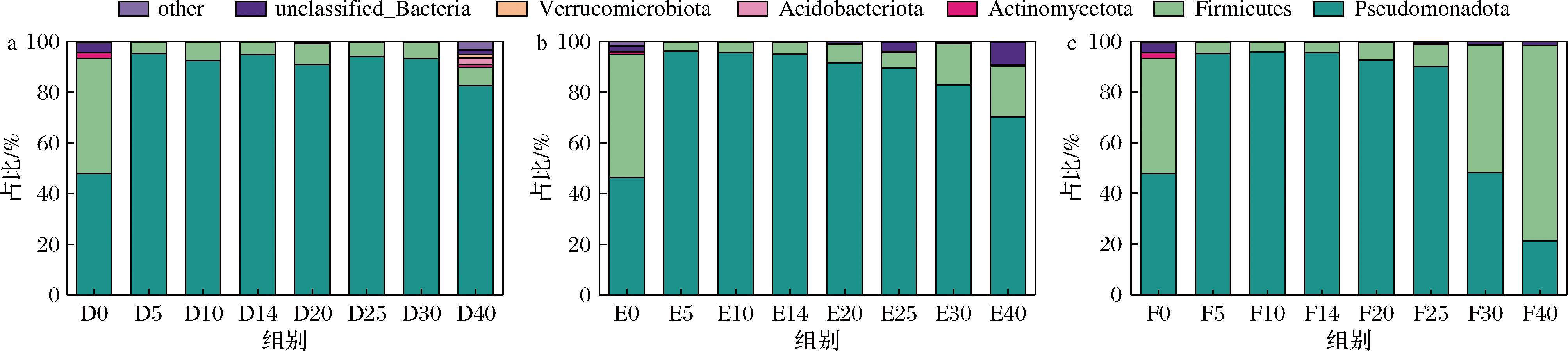
a-140 g/L发酵组;b-120 g/L发酵组;c-100 g/L发酵组
图1 不同盐浓度酱醪发酵过程细菌菌群结构变化-门水平
Fig.1 Bacterial community structure during the fermentation process of soy sauce mash with different salt concentrations at the phylum level
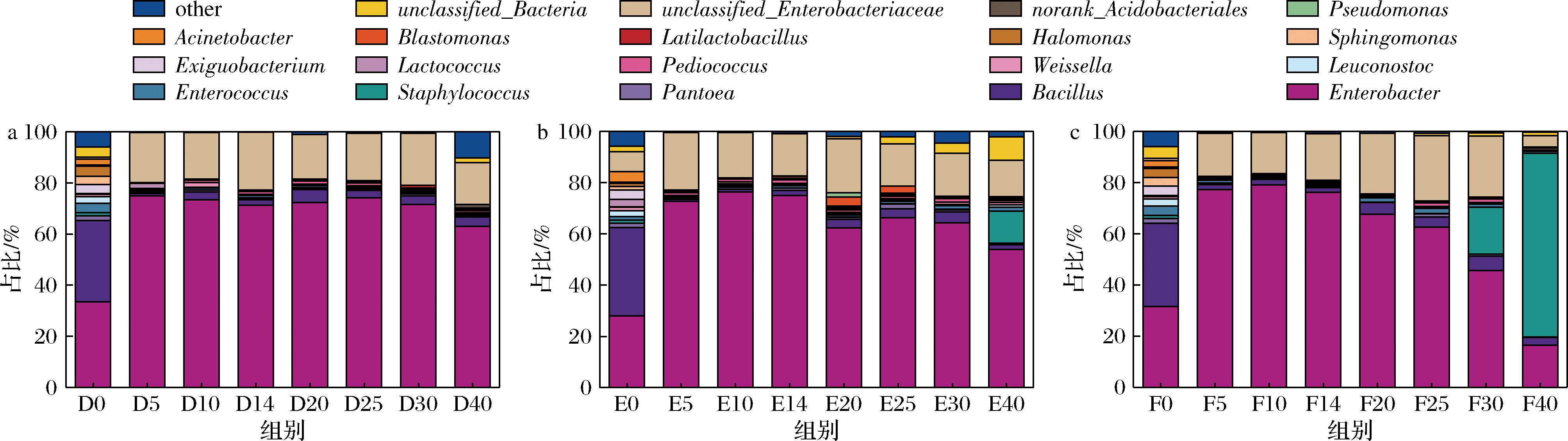
a-140 g/L发酵组;b-120 g/L发酵组;c-100 g/L发酵组
图2 不同盐浓度酱醪发酵过程细菌菌群结构变化-属水平
Fig.2 Bacterial community structure during the fermentation process of soy sauce mash with different salt concentrations at the genus level
不同盐浓度样品中,各细菌属的相对丰度存在显著差异。在固态发酵阶段(0~14 d),肠杆菌属的相对丰度显著上升,F14与F0相比,肠杆菌属的相对丰度上升141.12%,并且盐浓度越低,相对丰度越高。这与王涛[4]的研究结果一致,肠杆菌是低盐固态酱油发酵过程中的优势腐败菌。此外,还有研究发现肠杆菌是发酵食品中常见的产尸胺和腐胺的菌种[13]。在第5天时,芽孢杆菌属的相对丰度显著下降,这可能与体系中盐的存在有关。在稀态发酵阶段(15~20 d),葡萄球菌属在减盐条件下增生较早且相对丰度较高,D40、E40及F40中葡萄球菌属的相对丰度分别为0.10%、12.53%、71.76%,减盐稀态发酵阶段它成为了主要的腐败菌。有研究表明,葡萄球菌属与减盐酱油中主要不可接受挥发性物质4-甲基-2(H)-呋喃酮呈正相关,与主要挥发性风味物质呈负相关[11]。此外,它还与多种传统发酵食品中可导致食物中毒及相关过敏反应的生物胺呈显著正相关[14-16]。同时,整个发酵过程中,酱油发酵功能细菌如魏斯氏菌属、片球菌属、乳杆菌属等[17]的相对丰度均低于肠杆菌属和葡萄球菌属。由此可见,肠杆菌属和葡萄球菌属是先固后稀减盐酱油发酵体系中的优势腐败细菌,后续实验将针对它们的分离与抑制开展研究工作。
2.2 酱油减盐发酵体系中腐败菌与乳酸菌的分离鉴定
酱油发酵是一个涉及多种微生物参与的复杂过程,如表2所示,从发酵酱醪/酱醅中,分离得到Enterobacter、Staphylococcus、Bacillus等菌属的17株细菌。其中包括3种肠杆菌E.cloacae、E.hormaechei、E.sakazakii,3种葡萄球菌S.saprophyticus、S.gallinarum、S.nepalensis,7种芽孢杆菌B.subtilis、B.cereus、B.safensis、B.pumilus、B.licheniformis、B.velezensis、B.amyloliquefaciens。B.cereus是食源性疾病的常见致病菌,S.gallinarum和S.saprophyticus已经被证明携带多种葡萄球菌肠毒素基因[18],后者还会使水产、肉制品产生异味并导致食品变质[18]。Enterobacter是发酵豆制品、发酵水产品及干酪中致敏物生物胺的主要产生菌[19]。后续研究将针对酱油腐败菌以及食品致病菌,包括B.cereus、S.gallinarum、S.saprophyticus、E.cloacae、E.hormaechei、E.sakazakii的抑制展开。此外,从酱醅中分离得属于乳酸菌的3株肠球菌Enterococcus faecium。
表2 本研究所分离的菌株
Table 2 Bacterial strains isolated in this study
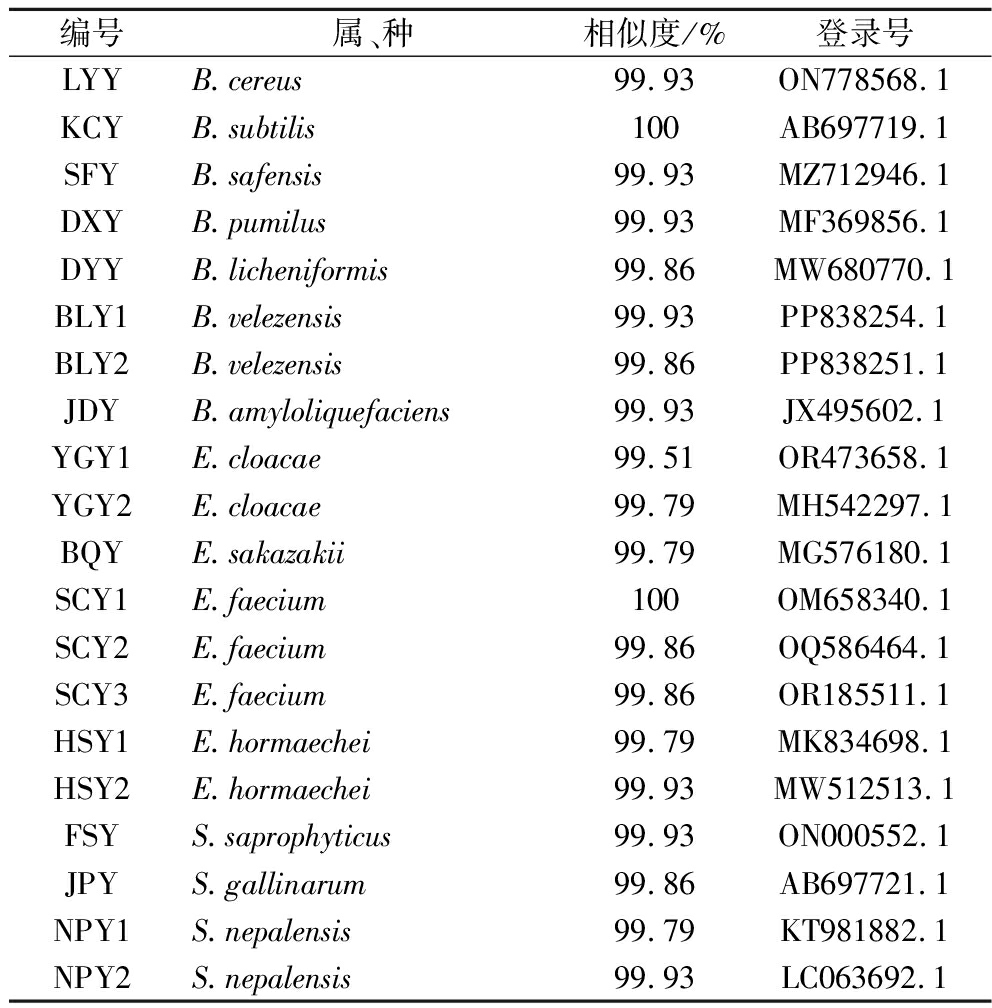
编号属、种相似度/%登录号LYYB.cereus99.93ON778568.1KCYB.subtilis100AB697719.1SFYB.safensis99.93MZ712946.1DXYB.pumilus99.93MF369856.1DYYB.licheniformis99.86MW680770.1BLY1B.velezensis99.93PP838254.1BLY2B.velezensis99.86PP838251.1JDYB.amyloliquefaciens99.93JX495602.1YGY1E.cloacae99.51OR473658.1YGY2E.cloacae99.79MH542297.1BQYE.sakazakii99.79MG576180.1SCY1E.faecium100OM658340.1SCY2E.faecium99.86OQ586464.1SCY3E.faecium99.86OR185511.1HSY1E.hormaechei99.79MK834698.1HSY2E.hormaechei99.93MW512513.1FSYS.saprophyticus99.93ON000552.1JPYS.gallinarum99.86AB697721.1NPY1S.nepalensis99.79KT981882.1NPY2S.nepalensis99.93LC063692.1
2.3 抑制酱油腐败细菌的功能乳酸菌筛选
乳酸菌在食品发酵中发挥关键作用,其产生的细菌素、有机酸和H2O2等物质能有效抑制腐败菌和有害菌,提升食品品质和风味[20-21]。其中,乳酸链球菌素(nisin)能有效地杀死或抑制引起食品腐败的革兰氏阳性菌,是世界上唯一被允许用作食品添加剂的细菌素。本研究分析了从酱油减盐发酵体系中分离的13株乳酸菌(包括Pediococcus、Enterococcus、Lactiplantibacillus)及nisin对6种腐败菌和食品致病菌的抑制能力。如表3所示,13株乳酸菌对6株腐败菌均有抑制效果。Enterococcus对腐败菌的抑制效果不如Lactiplantibacillus和Pediococcus。在0.2~10.0 g/kg的浓度范围内,nisin对3株肠杆菌无抑制作用,而L.plantarum JL-20、P.acidilactici WT1、P.pentosaceus WT6、P.pentosaceus WT8以及P.acidilactici ZQ8对3株肠杆菌有较强抑制作用。但在抑制芽孢杆菌方面,P.acidilactici ZQ8与P.acidilactici WT1相对偏弱。对2株葡萄球菌的抑制中,L.plantarum JL-20与P.pentosaceus WT6的表现优于其他菌株。
表3 乳酸菌的抑菌能力
Table 3 Antimicrobial ability of lactic acid bacteria
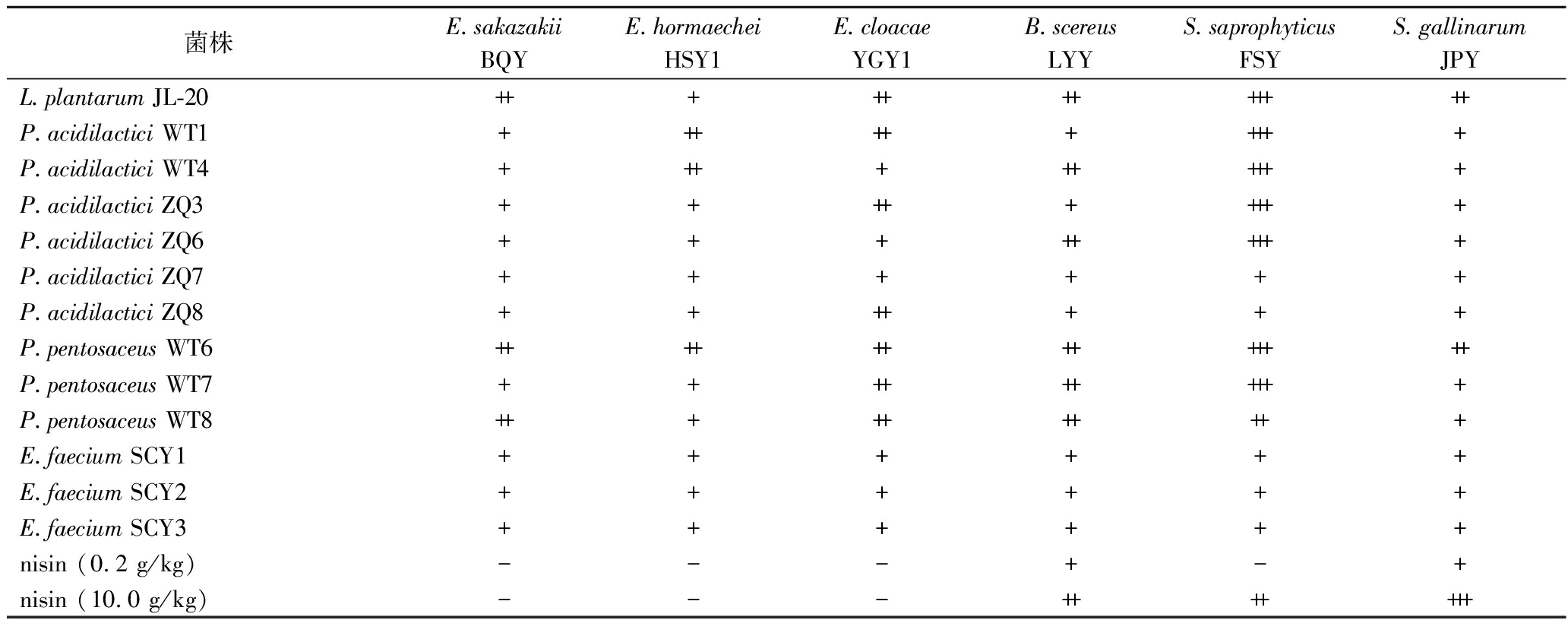
菌株E.sakazakiiBQYE.hormaecheiHSY1E.cloacae YGY1B.scereusLYYS.saprophyticusFSYS.gallinarum JPYL.plantarum JL-20++++++++++++P.acidilactici WT1++++++++++P.acidilactici WT4++++++++++P.acidilactici ZQ3+++++++++P.acidilactici ZQ6+++++++++P.acidilactici ZQ7++++++P.acidilactici ZQ8+++++++P.pentosaceus WT6+++++++++++++P.pentosaceus WT7++++++++++P.pentosaceus WT8++++++++++E.faecium SCY1++++++E.faecium SCY2++++++E.faecium SCY3++++++nisin (0.2 g/kg)---+-+nisin (10.0 g/kg)---+++++++
注:-,无抑菌圈;+,抑菌圈直径10.0~14.9 mm;++,抑菌圈直径15.0~19.9 mm;+++,抑菌圈直径20.0~24.9 mm。
本研究进一步在酱油模拟培养基中通过将乳酸菌与酱油腐败菌共培养,考察乳酸菌对酱油腐败菌生长的影响。如图3所示,在共培养中Pediococcus对肠杆菌的抑制效果优于Lactiplantibacillus和Enterococcus。与纯培养腐败菌数量相比,共培养中P.pentosaceus WT6、P.acidilactici WT4、P.acidilactici WT1可分别使肠杆菌数量下降0.97%~1.92%、0.31%~1.74%、0.83%~1.66%。在与B.scereus LYY、S.saprophyticus FSY、S.gallinarum JPY的共培养中,乳酸菌的活菌数要高于腐败菌数。共培养中P.pentosaceus WT6、P.acidilactici WT4、P.acidilactici WT1的乳酸菌数比腐败菌数分别高3.13%~4.00%、0.49%~1.87%、0.53%~2.36%。

a-L.plantarum JL-20组;b-P.acidilactici WT1组;c-P.acidilactici WT4组;d-P.acidilactici ZQ3组;e-P.acidilactici ZQ6组;f-P.acidilactici ZQ7组;g-P.acidilactici ZQ8组;h-P.pentosaceus WT6组;i-P.pentosaceus WT7组;j-P.pentosaceus WT8组;k-E.faecium SCY1组;l-E.faecium SCY2组;m-E.faecium SCY3组
图3 功能乳酸菌对腐败菌生长的影响
Fig.3 Effect of functional lactic acid bacteria on the growth of spoilage bacteria
2.4 乳酸菌用于酱油减盐发酵的特性研究
已有研究发现,前期低温酿造不仅有利于保证酱油的品质和风味物质的形成,也可在一定程度上抑制腐败菌的生长[22-24]。本研究确定的酱油减盐发酵工艺条件为:乳酸菌在前期固态发酵20 ℃和140 g/L NaCl条件下协同发酵酿造减盐酱油。因此,考察了筛选得到的功能乳酸菌在此条件下的生长和发酵特性以及此条件对酱油腐败菌和有害菌生长的影响,有助于了解功能乳酸菌协同酱油减盐发酵的潜力。
如图4所示,在20 ℃下Lactiplantibacillus的生长优于Pediococcus和Enterococcus,其中L.plantarum JL-20生长得最好,OD600达到3.30,P.pentosaceus WT6的OD600为2.53。Enterococcus的生长情况最差。Enterobacter、Staphylococcus、Bacillu的OD600在0.24~0.52之间,生长情况不如乳酸菌。在含有140 g/L NaCl的MRS/LB液体培养基中,Pediococcus的存活率高于Enterococcus、Lactiplantibacillus,P.pentosaceus WT6的存活率为104.70%,L.plantarum JL-20的存活率较低,为21.17%。Enterobacter、Staphylococcus、Bacillus的存活率低于Pediococcus,在2.32%~53.16%之间。结果说明在20 ℃和140 g/L NaCl条件下乳酸菌的生长情况明显优于酱油腐败菌和食品致病菌,其中P.pentosaceus WT6表现最佳。
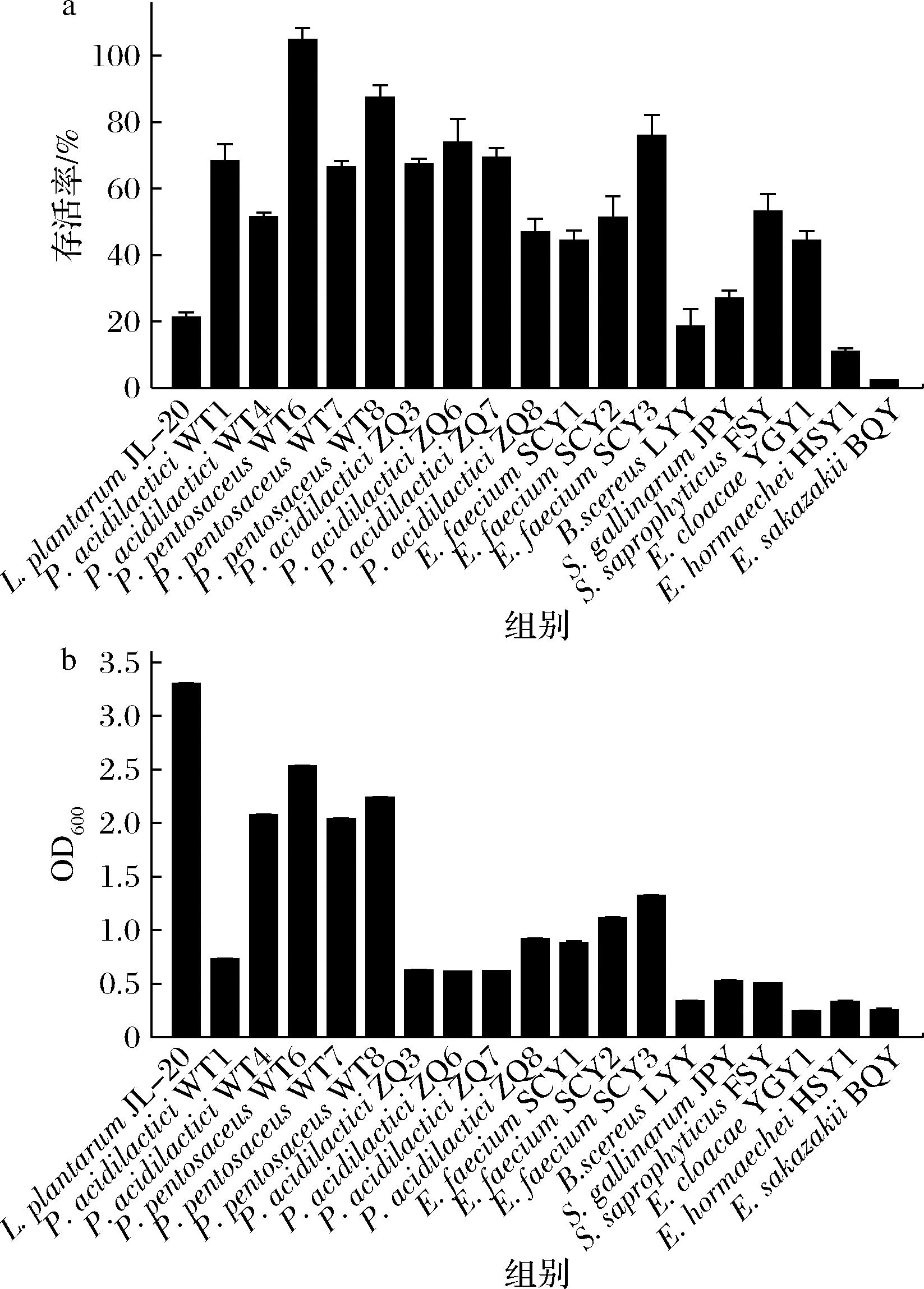
a-存活率;b-生长情况
图4 乳酸菌、腐败菌在140 g/L盐体系中的存活率及在20 ℃下的生长情况
Fig.4 Survival rate of lactic acid bacteria and spoilage bacteria in salt system(140 g/L) and their growth at 20 ℃
已有研究表明,乳酸菌所产生的多种有机酸能抑制杂菌,调控发酵体系微生物组成,并赋予酱油浓郁香味,增加香气复杂性。添加耐盐植物乳植杆菌于酱油中,可抑制非乳酸菌生长,使酯类和醇类物质含量分别提升36.60%、23.24%[25]。在低盐固态酱油中添加嗜酸足球菌,酱油中鲜味和甜味氨基酸含量分别提高了35.16%和13.44%,主要挥发性风味物质愈创木酚和苯酚含量分别提高了35.49%和50.64%[9]。如图5所示,Pediococcus、Enterococcus、Lactiplantibacillus可以产生酒石酸、乙酸、乳酸、琥珀酸、苹果酸、柠檬酸等6种有机酸。L.plantarum JL-20产有机酸能力最强,总产量可达35.70 g/L,但产苹果酸能力较弱。P.pentosaceus WT6和P.pentosaceus WT8的有机酸总产量分别可达33.58、33.08 g/L。
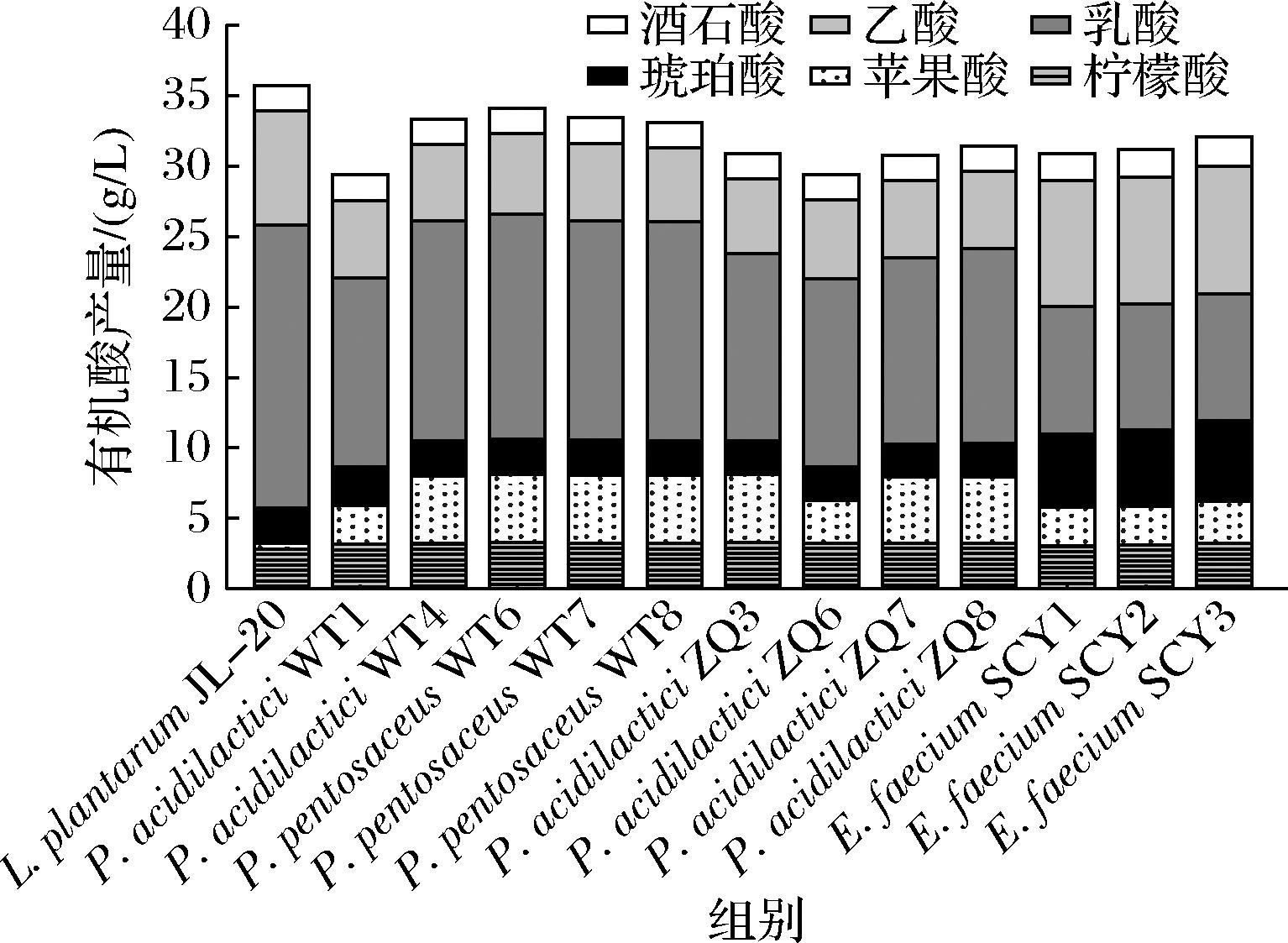
图5 乳酸菌合成有机酸情况
Fig.5 Organic acid synthesis by lactic acid bacteria
综上,在20 ℃和140 g/L NaCl条件下,乳酸菌(Pediococcus、Lactiplantibacillus、Enterococcus)的生长和存活率优于酱油腐败菌、食品致病菌(B.cereus、S.gallinarum、S.saprophyticus、E.cloacae、E.hormaechei、E.sakazakii)。P.pentosaceus WT6在20 ℃培养24 h时OD600可以达到2.53、在含140 g/L NaCl条件下培养48 h的存活率为104.70%、生成有机酸的产量能达33.58 g/L,将其添加至减盐酱油协同发酵中,对于酱油品质与风味的提升有着巨大潜力。
3 结论
本研究利用高通量测序技术,分析了在不同减盐浓度(140、120 g/L和100 g/L)的先固后稀酱油发酵体系中细菌群落结构的动态变化。研究发现,肠杆菌属(Enterobacter)和葡萄球菌属(Staphylococcus)在减盐发酵过程中占据优势地位,是主要的腐败菌。在腐败菌和食品致病菌的抑制实验中,酱醅来源的乳酸菌,包括Pediococcus、L.plantarum和E.faecium,均可有效抑制E.cloacae、E.hormaechei、E.sakazakii、S.saprophyticus、S.gallinarum、B.cereus等腐败菌或有害菌。其中P.pentosaceus、L.plantarum的抑菌能力高于E.faecium、P.acidilactici。在乳酸菌用于酱油减盐发酵的特性研究中,P.pentosaceus WT6表现优异,它在20 ℃下培养24 h时OD600可达2.53、在140 g/L NaCl中耐受性好(存活率为104.7%)、产有机酸的量为33.58 g/L。本研究结果为先固后稀酱油减盐发酵过程腐败菌与食品致病菌的识别、抑制提供参考依据,得到了一株适用于低温减盐发酵条件的乳酸菌,为乳酸菌协同发酵恢复减盐酱油品质提供重要参考意义。
[1] PATEL Y, JOSEPH J.Sodium intake and heart failure[J].International Journal of Molecular Sciences, 2020, 21(24):9474.
[2] 李婷婷, 王蓉, 刘盼, 等.食品减盐措施和氯化钠检测技术研究进展[J].食品安全质量检测学报, 2024, 15(10):144-154.
LI T T, WANG R, LIU P, et al.Research progress of salt reduction measures and detection technology of sodium chloride in food[J].Journal of Food Safety &Quality, 2024, 15(10):144-154.
[3] HU G Y, CHEN J, DU G C, et al.Moromi mash dysbiosis trigged by salt reduction is relevant to quality and aroma changes of soy sauce[J].Food Chemistry, 2023, 406:135064.
[4] 王涛. 功能乳酸菌的筛选及其在低盐固态酱油发酵中的应用[D].无锡:江南大学, 2023.
WANG T.Selection of functional lactic acid bacteria and their applications in low-salt solid-state soy sauce fermentation[D].Wuxi:Jiangnan University, 2023.
[5] WANG Y Y, ZHANG C H, LIU F S, et al.Ecological succession and functional characteristics of lactic acid bacteria in traditional fermented foods[J].Critical Reviews in Food Science and Nutrition, 2023, 63(22):5841-5855.
[6] 吴浪涛, 房峻, 吴新, 等.酱油变质微生物因素及乳酸菌在防腐中的应用[J].中国酿造, 2021, 40(7):22-27.
WU L T, FANG J, WU X, et al.Microbiological factors of spoilage in soy sauce and application of lactic acid bacteria in preventing spoilage[J].China Brewing, 2021, 40(7):22-27.
[7] HU Y Y, ZHANG L, WEN R X, et al.Role of lactic acid bacteria in flavor development in traditional Chinese fermented foods:A review[J].Critical Reviews in Food Science and Nutrition, 2022, 62(10):2741-2755.
[8] HU G Y, WANG Y J, CHEN J, et al.Synergistic fermentation with functional bacteria for production of salt-reduced soy sauce with enhanced aroma and saltiness[J].Food Bioscience, 2024, 57:103459.
[9] 王涛, 胡光耀, 方芳.足球菌协同发酵对低盐固态酱油风味与品质的影响[J].食品与发酵工业, 2023, 49(15):77-84.
WANG T, HU G Y, FANG F.Effect of synergetic fermentation with Pediococcus on the aroma and quality of low-salt solid-state soy sauce[J].Food and Fermentation Industries, 2023, 49(15):77-84.
[10] 敖晓琳, 蒲彪, 蔡义民, 等.能抑制引起泡菜“生花”腐败菌的乳酸菌的筛选[J].食品工业科技, 2014, 35(14):234-236;249.
AO X L, PU B, CAI Y M, et al.Screening Lactobacillus to inhibit spoilage microorganism isolated from film-forming pickle[J].Science and Technology of Food Industry, 2014, 35(14):234-236;249.
[11] 胡光耀. 类肠膜魏斯氏菌协同发酵酱油的机制解析[D].无锡:江南大学, 2023.
HU G Y.Analysis of the mechanism of synergistic fermentation of soy sauce with Weissella paramesenteroides[D].Wuxi:Jiangnan University, 2023.
[12] 房峻, 刘佳乐, 彭玉慧, 等.强化嗜盐四联球菌对模拟低盐酱油发酵的影响[J].中国酿造, 2020, 39(12):146-152.
FANG J, LIU J L, PENG Y H, et al.Effect of enrichment of Tetragenococcus halophilus on simulated fermentation of low-salt soy sauce[J].China Brewing, 2020, 39(12):146-152.
[13] 白妞妞, 白锴凯, 何建林, 等.鱼露生物胺研究进展[J].食品与发酵工业, 2020, 46(24):271-277.
BAI N N, BAI K K, HE J L, et al.Research progress of biogenic amines in fish sauce[J].Food and Fermentation Industries, 2020, 46(24):271-277.
[14] 李晓阳, 汪溢恒, 钮成拓, 等.温度对豆瓣酱发酵过程理化指标、风味物质和微生物群落的影响[J].食品与发酵工业, 2024, 50(2):112-118.
LI X Y, WANG Y H, NIU C T, et al.Effect of temperature on physicochemical parameters, flavor compounds, and microbial community during broad bean paste fermentation[J].Food and Fermentation Industries, 2024, 50(2):112-118.
[15] 杨梓璐. 发酵鱼露中优势菌群与质量的相关性及生物胺的控制[D].上海:上海海洋大学, 2023.
YANG Z L.Correlation between microbiota and quality in fermented fish sauce and control of biogenic amines[D].Shanghai:Shanghai Ocean University, 2023.
[16] 吴双慧, 牛茵, 何济坤, 等.基于宏基因组技术分析自然发酵羊肉香肠中微生物多样性及生物胺的代谢[J].食品科学, 2023, 44(18):133-140.
WU S H, NIU Y, HE J K, et al.Metagenomic analysis of microbial diversity and biogenic amine metabolism in naturally fermented mutton sausage[J].Food Science, 2023, 44(18):133-140.
[17] 彭勃, 侯莎, 周其洋, 等.酱油发酵中乳酸菌的功能及其研究进展[J].中国调味品, 2022, 47(11):216-220.
PENG B, HOU S, ZHOU Q Y, et al.The function and research progress of lactic acid bacteria in soy sauce fermentation[J].China Condiment, 2022, 47(11):216-220.
[18] 李琳. 葡萄球菌分离株肠毒素基因型分析及两种毒素的表达纯化[D].天津:天津大学, 2009.
LI L.Entertoxin genotype analysis of Staphylococcus isolates and expression, purification of two entertoxins[D].Tianjin:Tianjin University,2009.
[19] 隋雨萌, 王慧平, 刘嘉琪, 等.传统发酵食品中基于微生物多样性的生物胺形成研究进展[J].食品工业科技, 2024, 45(2):356-363.
SUI Y M, WANG H P, LIU J Q, et al.Biogenic amine formation based on microbial diversity in fermented foods:A review[J].Science and Technology of Food Industry, 2024, 45(2):356-363.
[20] PRABHURAJESHWAR C, CHANDRAKANTH K.Evaluation of antimicrobial properties and their substances against pathogenic bacteria in-vitro by probiotic Lactobacilli strains isolated from commercial yoghurt[J].Clinical Nutrition Experimental, 2019, 23:97-115.
[21] 胡美丽, 王俊钢, 李宇辉.产细菌素乳酸菌在食品中的应用[J].食品安全质量检测学报, 2022, 13(14):4657-4664.
HU M L, WANG J G, LI Y H.Application of bacteriocin produced by Lactobacillus in food[J].Journal of Food Safety &Quality, 2022, 13(14):4657-4664.
[22] 倪海晴. 提高酱油大曲酶活和改善酱油发酵效果的研究[D].无锡:江南大学, 2010.
NI H Q.Stndy on the improvement of the enzyme activity of Aspergillus oryzae koji and the promotion of fermentation process[D].Wuxi:Jiangnan University, 2010.
[23] 施思, 蒋予箭, 张海珍.温度对高盐稀态酱油风味物质的影响[J].中国调味品, 2015, 40(8):69-73;79.
SHI S, JIANG Y J, ZHANG H Z.Effect of temperature on flavor substances of high-salt liquid-state soy sauce[J].China Condiment, 2015, 40(8):69-73;79.
[24] 牛丽丽, 崔艳, 闫志华, 等.不同酿造工艺对黑豆酱油理化特性和感官品质的影响[J].食品研究与开发, 2023, 44(18):88-93.
NIU L L, CUI Y, YAN Z H, et al.Effects of different brewing techniques on physicochemical properties and sensory quality of black bean soy sauce[J].Food Research and Development, 2023, 44(18):88-93.
[25] 张伟, 杨俊文, 余冰艳, 等.耐盐植物乳杆菌的选育及其对高盐稀态发酵酱油品质的影响[J].食品与发酵工业, 2023, 49(1):86-94.
ZHANG W, YANG J W, YU B Y, et al.Breeding of salt-tolerant Lactobacillus plantarum and their effects on the quality of high-salt liquid-state fermented soy sauce[J].Food and Fermentation Industries, 2023, 49(1):86-94.