我国各地传统发酵乳制品历史悠久,尤以新疆、西藏、内蒙古等地区的发酵乳制品最具特色。这些地区的传统发酵乳不仅风味独特、口感醇厚,更因其丰富的营养价值和优良的品质而备受青睐,形成了多样化的传统乳制品体系。不同地域的发酵乳制品在核心微生物群落构成和风味物质组成方面存在显著差异,这种差异主要源于乳源特性、地域气候条件以及传统发酵工艺等多重因素的共同作用[1-2]。长期生活在新疆草原上的游牧民族一直保留着手工制作传统发酵乳制品的习惯,如酸奶、开菲尔粒、酸奶疙瘩等[3]。奶疙瘩是一种新疆人民非常喜爱的乳制品,手工奶疙瘩以新鲜全脂乳为原料,经自然发酵后倒入锅中熬煮,待乳清与凝乳分离后装入布袋吊挂沥干水分,再手工捏制颗粒状并平铺于木席,借日光与空气完成最终干燥定型。风干后的奶疙瘩不仅营养丰富、口感细腻,还易于储存,因此成为哈萨克族牧人的营养储备佳品[4-6]。
奶疙瘩不仅风味独特还具有丰富营养价值,其营养密度是原料乳的10倍,形成独特的“浓缩效应”,不仅能够增强免疫力、加速人体代谢,长期食用还能有效预防心血管疾病。奶疙瘩成品胆固醇含量仅为原料的1/10,而且有丰富的维生素和钙磷钾等微量元素,不仅如此,奶疙瘩的发酵过程可以转化70%以上乳糖,有效解决了乳糖酶缺乏人群的饮食难题[7]。
宏基因组学突破了传统培养方法的限制,通过直接分析微生物基因序列,能够快速鉴定样品中微生物的种类、丰度和功能,准确揭示微生物群落多样性及其与环境互作关系[8]。目前该技术已应用于酸牛奶、酸马奶等传统发酵乳制品的细菌多样性研究。研究表明,发酵乳制品的微生物群落结构具有地域性和类型特异性,主要受原料乳种类、发酵工艺及环境条件等因素影响[9]。细菌群落以厚壁菌门(Firmicutes)为优势菌群,其中乳杆菌属(Lactobacillus)和链球菌属(Streptococcus)等乳酸菌为主要代表性类群;真菌群落则以子囊菌门(Ascomycota)占优,其代谢产生的风味物质可显著改善产品品质[10],这些发现为传统发酵乳制品的标准化生产提供了重要理论依据。本研究旨在全面解析该特色发酵乳制品中的微生物多样性及群落结构,系统挖掘与脂质代谢调控相关的核心功能基因及代谢通路网络,筛选出具有显著降胆固醇活性的优势菌株,为新疆手工奶疙瘩的降脂功能提供分子层面的科学证据,同时获得优良的降胆固醇功能微生物,为后续益生菌制剂开发及功能性食品研发奠定基础。
1 材料与方法
1.1 样品采集
本研究从新疆伊犁州新源县各乡镇获取手工奶疙瘩制作家庭的名单,采用分层随机抽样方法选取样本。具体抽样方案如下:首先将家庭按生产方式分为游牧和定居2类,随机抽取5户;随后从每户采集5~10块独立制作的奶疙瘩样品[单块质量约(30±5) g],共计获得50~100个样品用于后续实验分析。所有样品采集后立即置于-20 ℃保存,直至实验处理。该抽样方案充分考虑了生产方式的差异性和样品的空间分布特征,为研究结果的可靠性提供了保障。奶疙瘩采用鲜奶为原料,经纱布过滤、煮沸杀菌后冷却至40~45 ℃,添加适量已发酵成熟的酸奶作为引子并搅拌均匀,密封后于适宜温度下发酵至凝乳成型[11]。
1.2 培养基与试剂
牛胆盐、胆固醇,上海麦克林生化科技股份有限公司;大豆蛋白胨、MC培养基、M17琼脂培养基,青岛海博生物科技有限公司;牛肉膏、蛋白胨,北京奥博星生物技术有限责任公司;无水乙醇,天津市致远化学试剂有限公司。试剂均为分析纯。
YGC培养基(g/L):葡萄糖20,酵母粉5,氯霉素0.1,琼脂15。MRS培养基(g/L):蛋白胨 10,酵母粉 5,葡萄糖 20,牛肉膏 8,K2HPO4 2,柠檬酸二胺 2,乙酸钠 5,MgSO4 0.28,MnSO4 0.05,吐温-80 1.0。MRS-CHOL培养基:参考于江傲等[12]的方法并稍作修改,在MRS液体培养基中加入0.3 g/100 mL的牛胆盐,加入1.0%(体积分数)的无菌胆固醇溶液使其终质量浓度为0.1 mg/mL。10 mg/mL胆固醇溶液:称取胆固醇粉末0.1 g溶于无水乙醇中,超声波处理使其完全溶解,并定容至10 mL,获得10 mg/mL的胆固醇溶液,用0.22 μm微孔滤膜过滤除菌;硫酸铁铵储存液:称取硫酸铁铵4.46 g溶于体积分数85%磷酸中,并定容至100 mL,室温放置备用。硫酸铁铵工作液:取10 mL硫酸铁铵储存液10 mL,加浓硫酸定容至100 mL。
1.3 仪器与设备
LDZX-30KBS高压蒸汽灭菌锅,上海申安有限公司;ELx800酶标仪,美国伯腾BioTek仪器有限公司;MIKRO 200R高速冷冻离心机,德国Hettich科学仪器公司;SW-CJ-2FD超净工作台,上海博讯实业有限公司;TS-111B摇床,上海天呈实验仪器制造有限公司;XS205电子天平,Mettler-Toledo仪器有限公司。
1.4 实验方法
1.4.1 具胆盐水解酶(bile salt hydrolase,BSH)活性的样品筛选
将手工奶疙瘩样品进行精细化粉碎与均质化研磨处理,随后精确称取样品粉末,以3%的接种量分别接种至MRS液体培养基(37 ℃)和YGC液体培养基(28 ℃),在150 r/min振荡条件下富集培养24 h。吸取富集培养得到的菌液于BSH固体培养基平板的滤纸片上,根据溶钙圈的情况筛选出BSH活性较强的样品。
1.4.2 BSH活性样品的宏基因组测序及分析
将高BSH活性样品研磨为粉末,2个样品(每个样品3个重复),于-80 ℃低温条件下保存,送至上海美吉生物医药科技有限公司进行宏基因组测序。提取样品DNA,DNA质检合格后,构建测序文库并对文库进行质量检测,库检合格后使用 Illumina测序。运用Kraken2软件实现测序reads的快速物种分类,并采用Bracken算法计算宏基因组数据的物种丰度。Bracken算法通过整合Kraken2分配的分类标签,对样本中各物种对应的reads数量进行估算,进而获取各样本在不同分类学层级上的物种丰度信息。采用Diamond比对工具将非冗余基因集映射至KEGG(Kyoto Encyclopedia of Genes and Genomes)、eggNOG(evolutionary genealogy of genes:Non-supervised Orthologous)、CAZy(Carbohydrate-Active enZYmes Database)等多维功能数据库,建立基因-功能关联网络,同时集合基因丰度表格计算不同数据库比对结果的丰度信息并对注释结果进行对注释结果进行GO/KEGG通路富集分析,揭示基因集在代谢调控、环境适应、催化反应等生物过程中的功能特征。
1.4.3 降胆固醇菌株的分离鉴定
对BSH活性较强的样品进行活化和富集培养,样品进行梯度稀释,取100 μL 10-4~10-6的稀释液于胆固醇固体平板上涂布,倒置厌氧培养48~72 h,挑取单菌落划线6~8次,倒置厌氧培养48~72 h,革兰氏染色并于显微镜下观察并记录形态。将纯化得到的菌株接种于MRS和YGC液体培养基中,12 000 r/min离心3 min,PBS洗涤后收集菌液,用HiPure Bacterial DNA Kit试剂盒提DNA,利用引物27F(5′-AGAGTTTGATCCTGGCTCAG-3′)和1492R(5′-GGTTACCTTGTTACGAC-TT-3′)扩增细菌V3~V4区序列,利用引物NL1(5′-GCATATCAATAAGCGGAGGAAAAG-3′)和NL4(5′-GGTCCGTGTTTCAAGACGG-3′)扩增真菌D1/D2隔间区序列,PCR产物以1%琼脂糖凝胶电泳进行检测后送至新疆有康生物科技有限公司测序,将测序结果与NCBI数据库进行比对,初步确定菌株分类。
1.4.4 菌株体外胆固醇降解能力的测定
采用硫酸铁铵法测定菌株的胆固醇降解能力。将菌株活化后分别以3%的接种量接种至MRS-CHOL培养基,培养24 h后,取接菌和未接菌的MRS-CHOL培养基各0.2 mL加入装有4.8 mL无水乙醇的离心管中,混匀,9 500 r/min离心5 min,离心后取2 mL上清液于新的离心管中,沿管壁缓慢加入2 mL硫酸铁铵工作液,混匀后室温静置30 min,于波长560 nm处测定吸光度。根据胆固醇标准曲线的回归方程计算胆固醇浓度,计算如公式(1)所示。
胆固醇降解率![]()
(1)
式中:A,培养基胆固醇浓度;B,上清液胆固醇浓度。
1.5 统计学分析
对原始测序数据进行质控和去污染处理,获得高质量Clean Reads。随后使用Kraken2结合Bracken算法进行高精度物种分类分析。在功能注释方面,通过Diamond将优化序列比对至UniRef90数据库,获取基因家族ID及其丰度信息。基于该结果,一方面通过KEGG数据库的映射关系,从基因家族ID推导出KO和EC编号,进而获得KEGG Pathway各层级的丰度分布;另一方面通过eggNOG数据库的对应关系,从基因家族ID推导出NOG分类,获得eggNOG功能、类别的丰度信息。该分析流程全面解析了微生物群落的物种组成和功能特征。
2 结果与分析
2.1 BSH活性样品的筛选
由表1可以看出,X1、X2两个样品溶钙圈半径大于其他样品,说明这2个样品的BSH活性显著高于其他样品,因此选取X1、X2样品进行宏基因组分析、菌种的分离纯化和菌株胆固醇降解率的测定。
表1 样品BSH活性分析
Table 1 Analysis of BSH activity in samples
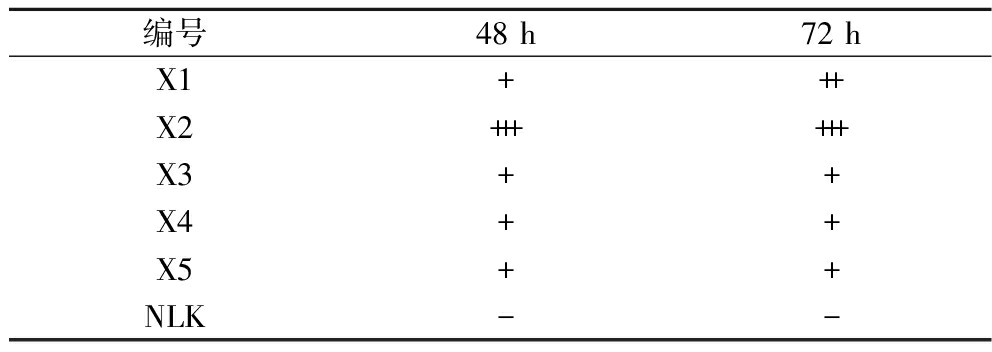
编号48 h72 hX1+++X2++++++X3++X4++X5++NLK--
注:-:无沉淀圈;+;沉淀圈半透明;++:沉淀圈半透明且直径>9 mm;+++:沉淀圈不透明且直径>9 mm。
2.2 BSH活性样品的宏基因组分析
2.2.1 BSH活性样品微生物群落α多样性
α多样性是指在一个特定区域或生态系统内的多样性,它主要用于衡量群落内的生物多样性,是反映生境内部物种数量及相对多度的综合指标。主要包括ACE指数、Chao1指数、Shannon指数和Simpson指数。奶疙瘩样品X1与X2的α多样性分析显示显著差异(P<0.05),由表2可知,X2的Chao1指数和ACE指数显著高于X1,表明X2的潜在微生物物种丰富度更高。同时,X2的Shannon指数高于X1,而Simpson指数呈现相反趋势。这一结果表明,X2微生物群落不仅物种更丰富,且分布更均匀;而X1虽整体多样性较高,但存在显著优势菌属(如Lactobacillus)。这种差异可能源于样品X2采集自游牧家庭,发酵温度受自然温度波动的影响(昼夜温差10~15 ℃),有利于多种微生物共存;而样品X1采集自定居家庭,在相对恒定的温度条件下发酵,更易形成优势菌群。这些发现也为理解发酵环境对微生物群落构建的影响提供了重要依据。
表2 样品间微生物α多样性指数差异
Table 2 Differences in microbial α-diversity indices between samples
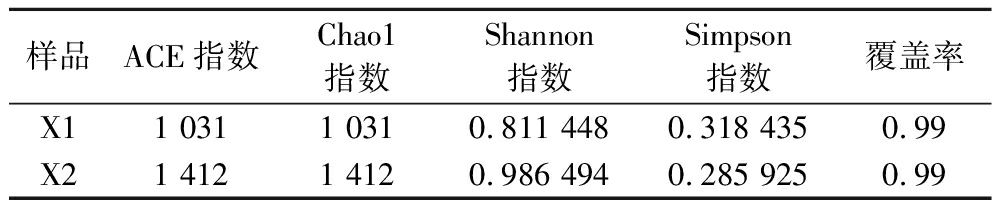
样品ACE指数Chao1指数Shannon指数Simpson指数覆盖率X11 0311 0310.811 4480.318 4350.99X21 4121 4120.986 4940.285 9250.99
2.2.2 BSH活性样品的微生物群落结构
宏基因组测序结果显示,送检样品共检测到5界、31门、62纲、115目、230科、647属和2 274种微生物。
由图1-a可知,在门水平上样品X1中丰度较高的门为厚壁菌门(Firmicutes,92.97%)、子囊菌门(Ascomycota,4.68%)和变形菌门(Proteobacteria,2.06%);样品X2中丰度较高的门为厚壁菌门(Firmicutes,90.80%)、变形菌门(Proteobacteria,6.46%)和子囊菌门(Ascomycota,2.48%)。
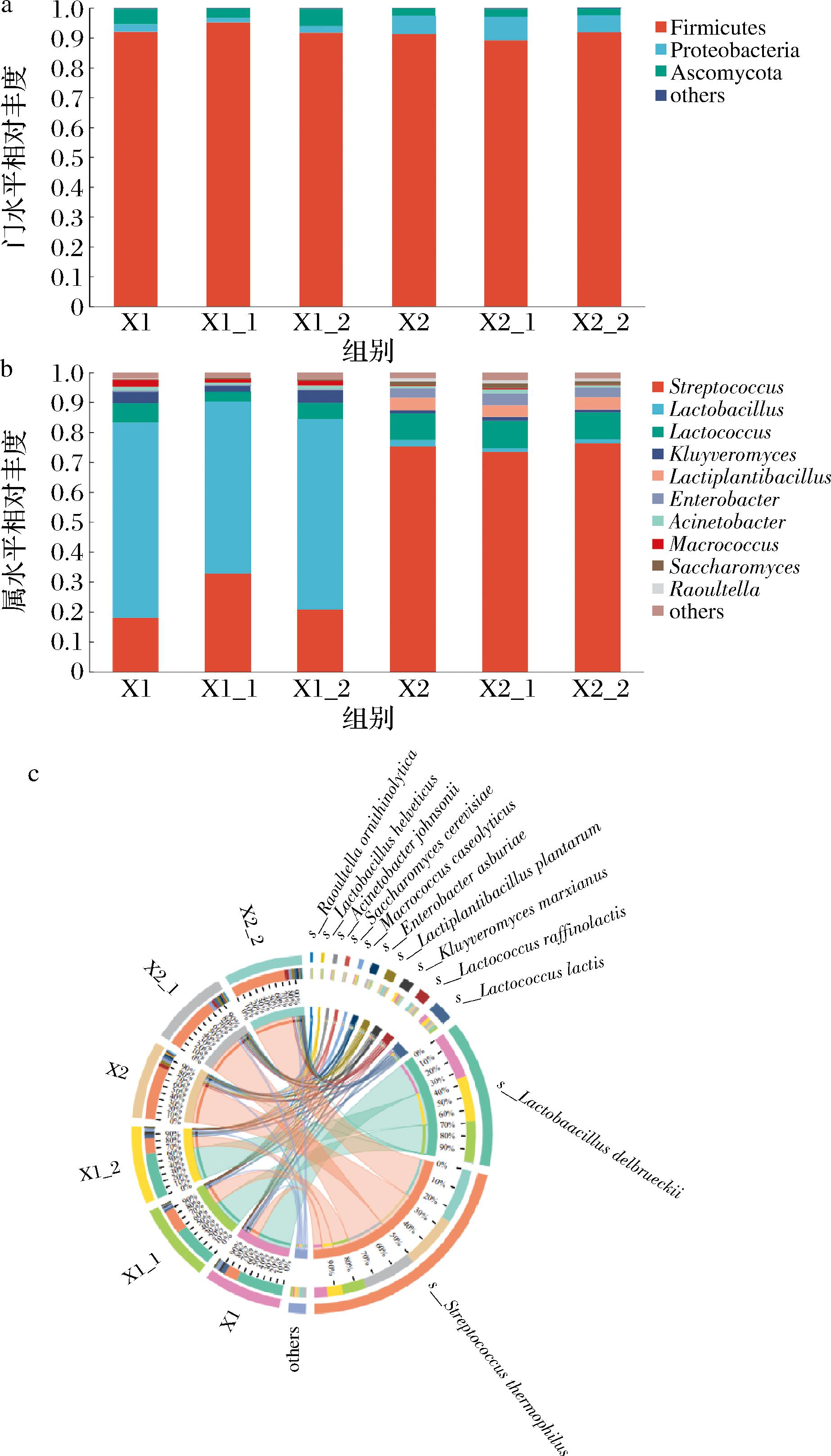
a-门水平;b-属水平;c-种水平
图1 BSH活性样品微生物群落特征
Fig.1 Microbial community characteristics of BSH-active samples
由图1-b可知,在属水平上样品X1中丰度较高的属为乳杆菌属(Lactobacillus,62.02%)、链球菌属(Streptococcus,23.89%)、乳球菌属(Lactococcus,5.06%)、克鲁维酵母属(Kluyveromyces,3.39%)和不动杆菌属(Acinetobacter,1.10%);样品X2中丰度较高的属为链球菌属(Streptococcus,74.97%)、乳球菌属(Lactococcus,9.12%)、乳杆菌属(Lactobacillus,4.05%)、肠杆菌属(Enterobacter,3.51%)和酵母属(Saccharomyces,1.40%)。由图1-c可知,在种水平上样品X1中丰度较高的种为德氏乳杆菌(Lactobacillus delbrueckii,61.97%)、嗜热链球菌(Streptococcus thermophilus,23.86%)、乳酸乳球菌(Lactococcus lactis,4.80%)和马克斯克鲁维酵母(Kluyveromyces marxianus,3.38%);样品X2中丰度较高的种为嗜热链球菌(74.55%)、植物乳杆菌(Lactiplantibacillus plantarum,4.04%)、乳酸乳球菌(3.59%)、酿酒酵母(Saccharomyces cerevisiae,1.40%)和马克斯克鲁维酵母(Kluyveromyces marxianus,1.03%)。微生物群落组成情况结果表明,尽管所处地理环境一致,微生物群落结构在属和种水平上依然存在差异,可能因家庭制作工艺、操作习惯、原料选取等因素的不同,使得奶疙瘩中微生物的种类分布和相对丰度各不相同,这种差异反映了手工制作过程中多种因素塑造了奶疙瘩独特的微生物群落结构。
2.2.3 KEGG功能分析
KEGG功能注释分析显示,2个奶疙瘩样品中共检测到7 377个功能基因。这些基因在KEGG数据库中主要分布于6个一级功能类别和46个二级代谢通路中。6个一级功能类别依次为:代谢,主要参与各类物质代谢过程;遗传信息处理,涉及DNA复制、转录翻译等过程;环境信息处理,包含信号转导等通路;细胞功能,涵盖细胞运动、分裂等功能;生物体系统,包含免疫、内分泌等系统;人类疾病,与多种疾病相关通路。该分析结果系统揭示了奶疙瘩微生物群落的功能多样性特征。如图2所示,在KEGG一级功能类别层面,奶疙瘩中的微生物以新陈代谢为绝对优势功能类别,这表明奶疙瘩中微生物的代谢活动较为活跃,为奶疙瘩独特风味品质的形成奠定了物质基础。在KEGG二级通路分析中,甘油三酯、磷脂、胆固醇和血浆脂蛋白等4种脂质代谢相关途径均得到注释。如表3所示,与胆固醇合成相关的角鲨烯单加氧酶,与胆固醇分解相关的胆固醇酯水解酶、胆酰甘氨酸水解酶以及胆固醇氧化酶等关键酶以及与胆固醇转运相关的NPC1蛋白都得到了注释。推测奶疙瘩中的微生物可能通过choD介导的胆固醇氧化途径降低生物可利用性,NPC1与LIPA的协同作用可能促进胆固醇的细胞内转运。基于脂质代谢途径与胆固醇调节的潜在关联,初步表明本研究选取的奶疙瘩样品可能具备降胆固醇的功能。
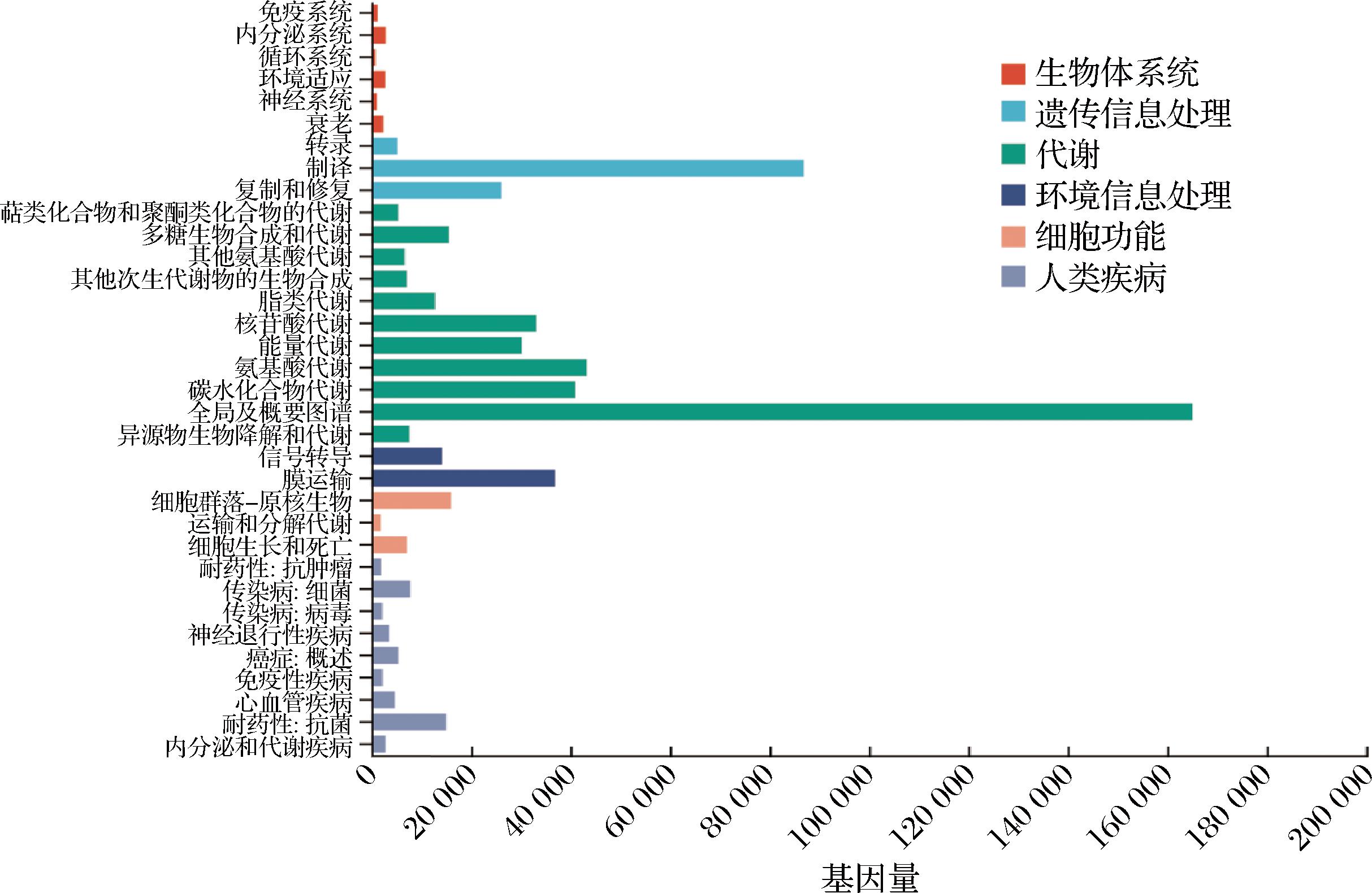
图2 BSH活性样品微生物基因的KEGG代谢通路富集分析
Fig.2 KEGG pathway enrichment analysis of microbial genes from BSH-active samples
表3 胆固醇代谢通路关键酶及蛋白表达丰度
Table 3 Key enzymes and protein abundance in cholesterol metabolic pathways

KOKO 名称KO 功能注释相对丰度/%X1X2K05898kstD3-oxosteroid 1-dehydrogenase(3-氧代类固醇 1-脱氢酶)79.25659.442K12385NPC1Niemann-Pick C1 protein(Niemann-Pick C1蛋白)24.6788.226K01052LIPAlysosomal acid lipase/cholesteryl ester hydrolase(溶酶体酸脂肪酶/胆固醇酯水解酶)24.67816.452K00511SQLEsqualene monooxygenase(角鲨烯单加氧酶)43.00821.504K01442cbhcholoylglycine hydrolase(胆汁酰甘氨酸水解酶)72.10454.078K03333choDcholesterol oxidase(胆固醇氧化酶)19.81439.628
2.2.4 eggNOG功能分析
由图3可知,通过eggNOG数据库对2个奶疙瘩样品中的基因进行注释,样品中功能已知的基因被注释最多的5个功能单元分别为:翻译、核糖体结构与生物合成(15.17%),氨基酸转运和代谢(10.24%),复制、重组和修复(8.44%),碳水化合物转运和代谢(7.59%),以及核苷酸转运和代谢(5.7%)。在这些功能单元中,翻译、核糖体结构与生物合成相关基因,主要通过对胆固醇代谢和合成过程中相关酶的表达调控,间接影响胆固醇的代谢与合成。例如,胆固醇代谢分解的关键酶,如细胞色素P450酶系等,本质上都是蛋白质,它们的合成需要充足的氨基酸作为原料。而氨基酸的合成,离不开核苷酸转运与代谢提供的能量支撑以及物质基础。不仅如此,一些参与胆固醇转运的蛋白质,其合成过程同样依赖核苷酸转运与代谢。值得注意的是,胆固醇的分解代谢受多种信号通路的精确调控。核苷酸代谢过程中产生的信号分子,能够与胆固醇代谢分解相关的信号通路发生相互作用,协同调节胆固醇的分解代谢过程。另外,碳水化合物转运和代谢在奶疙瘩独特风味的形成中发挥着关键的调控作用,可能通过影响微生物代谢、产物生成等途径,塑造了奶疙瘩别具一格的风味特征。
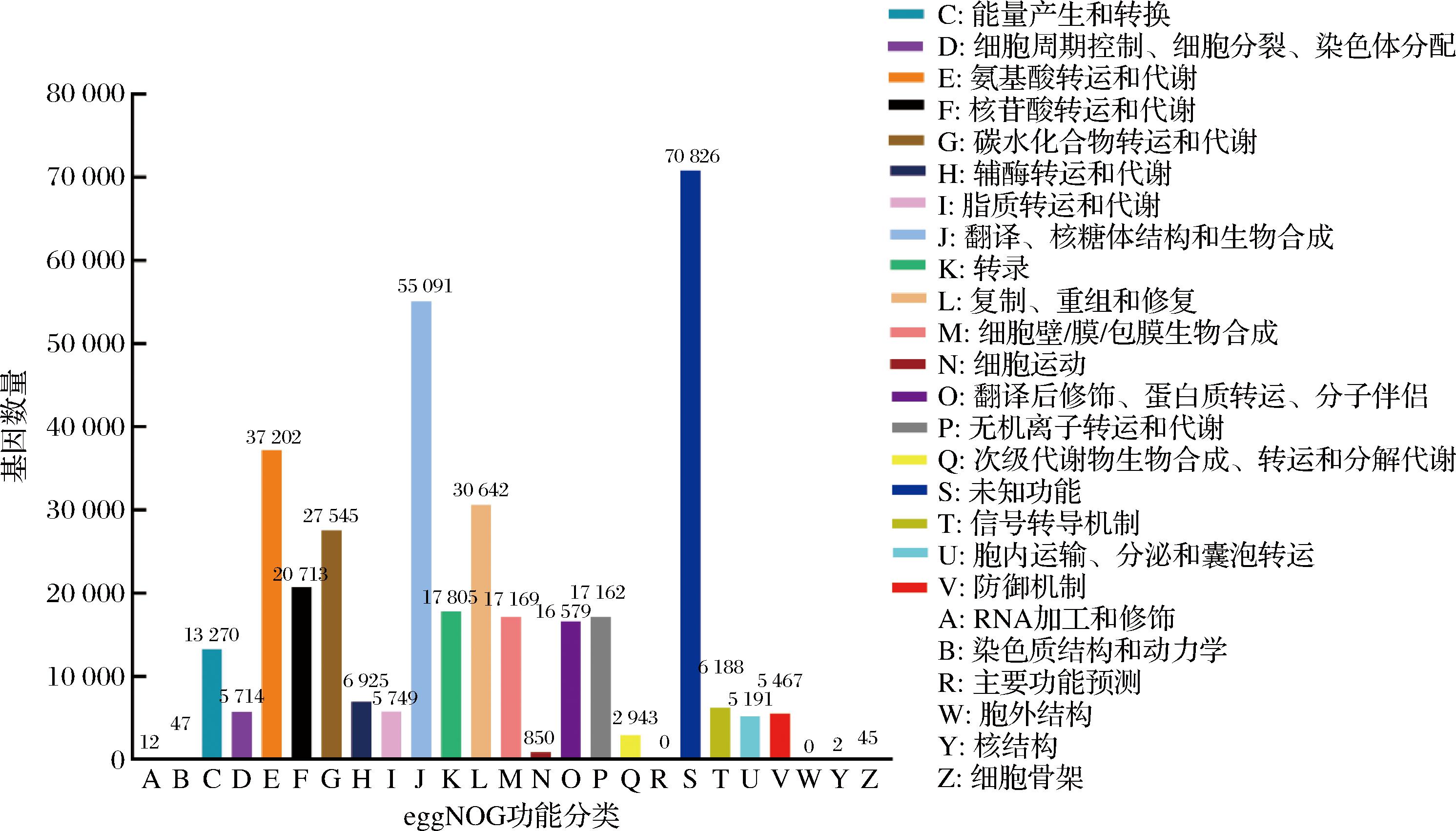
图3 基于eggNOG数据库的降胆固醇相关微生物基因功能分类
Fig.3 Functional categorization of cholesterol-reducing microbial genes using eggNOG database
2.3 降胆固醇菌株的分离鉴定
在胆固醇为1%的培养基上进行菌株分离,对分离菌株进行16S rRNA基因同源性分析,并与NCBI数据库中的序列对比,应用MEGA 11 软件构建系统发育树,结果如图4所示,共分离得到10株细菌和5株酵母菌。其中,1株菌与耐久肠球菌序列同源性较高,命名为Enterococcus durans sp.XY2-6;1株菌与肠膜明串珠菌序列同源性较高,将其命名为Leuconostoc pseudomesenteroides sp.XY2-7;5株菌与屎肠球菌序列同源性较高,命名为E.faecium sp.XY2-1、E.faecium sp.XY2-2、E.faecium sp.XY2-8、E.faecium sp.XY2-9、E.faecium sp.XY2-10;3株与乳酸肠球菌序列同源性较高,命名为E.lactis sp.XY2-3、E.lactis sp.XY2-4和E.lactis sp.XY2-5。酵母菌中1株菌与酿酒酵母的序列同源性较高,命名为S.cerevisiae sp.XX1-2;4株菌与马克斯克鲁维酵母的序列同源性较高,将其命名为K.marxianus sp.XX2-1、K.marxianus sp.XX2-4、K.marxianus sp.DX2-1和K.marxianus sp.DX2-3。
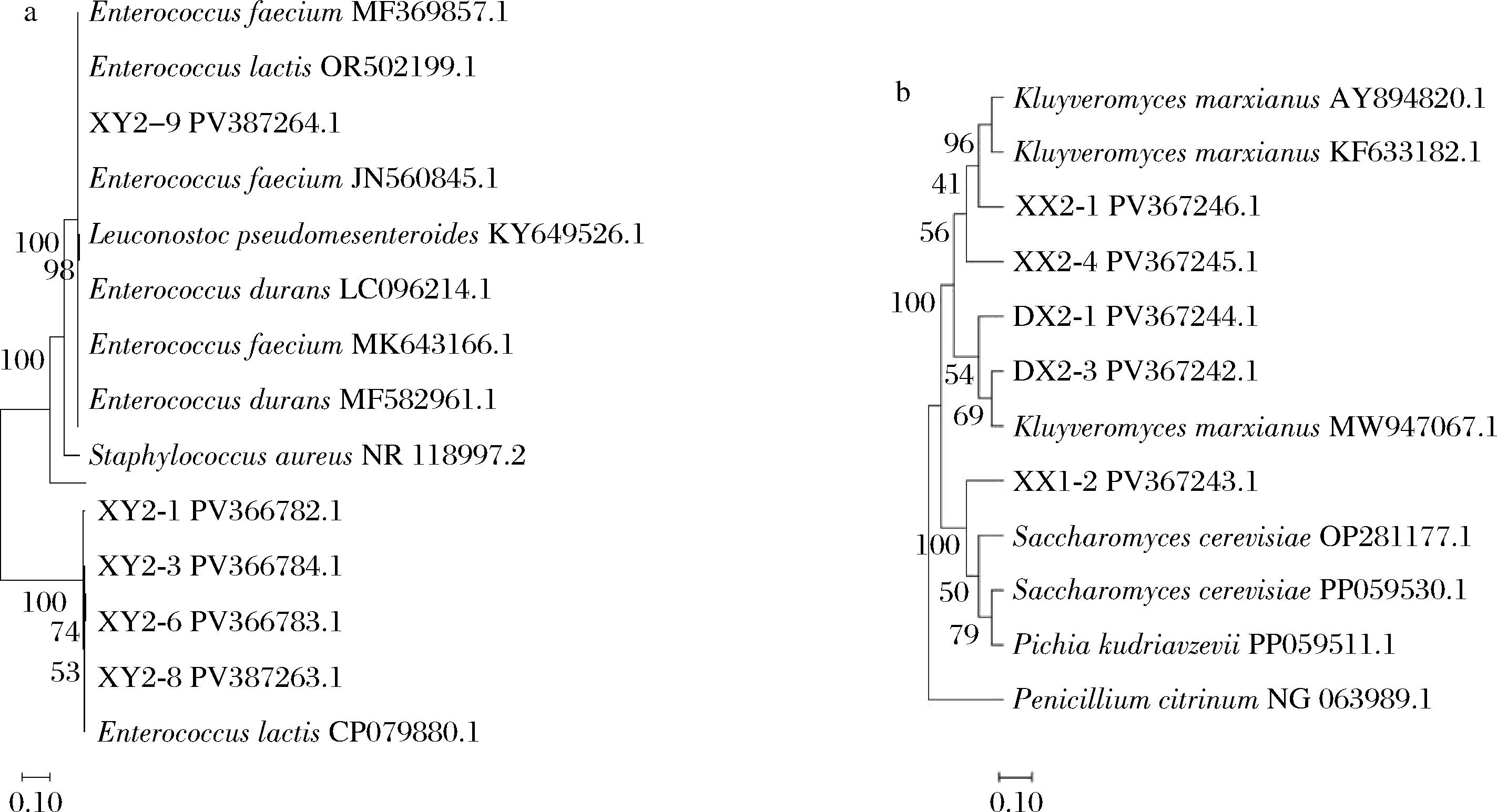
a-细菌;b-真菌
图4 降胆固醇菌株系统发育树分析
Fig.4 Phylogenetic analysis of cholesterol-lowering microbial strains
2.4 菌株体外降胆固醇能力测定
对获得的10株细菌和5株酵母菌进行体外胆固醇降解率的测定,结果如图5所示,细菌中乳酸肠球菌XY2-4胆固醇降解率最高,降解率为66.63%,其次是XY2-3,降解率为43.97%,除此之外,屎肠球菌XY2-1、乳酸肠球菌XY2-5和耐久肠球菌XY2-6的胆固醇降解率均大于30%。酵母菌中酿酒酵母XX1-2的胆固醇降解率最高,达到44.83%,4株马克斯克鲁维酵母中有2株降解率>20%。
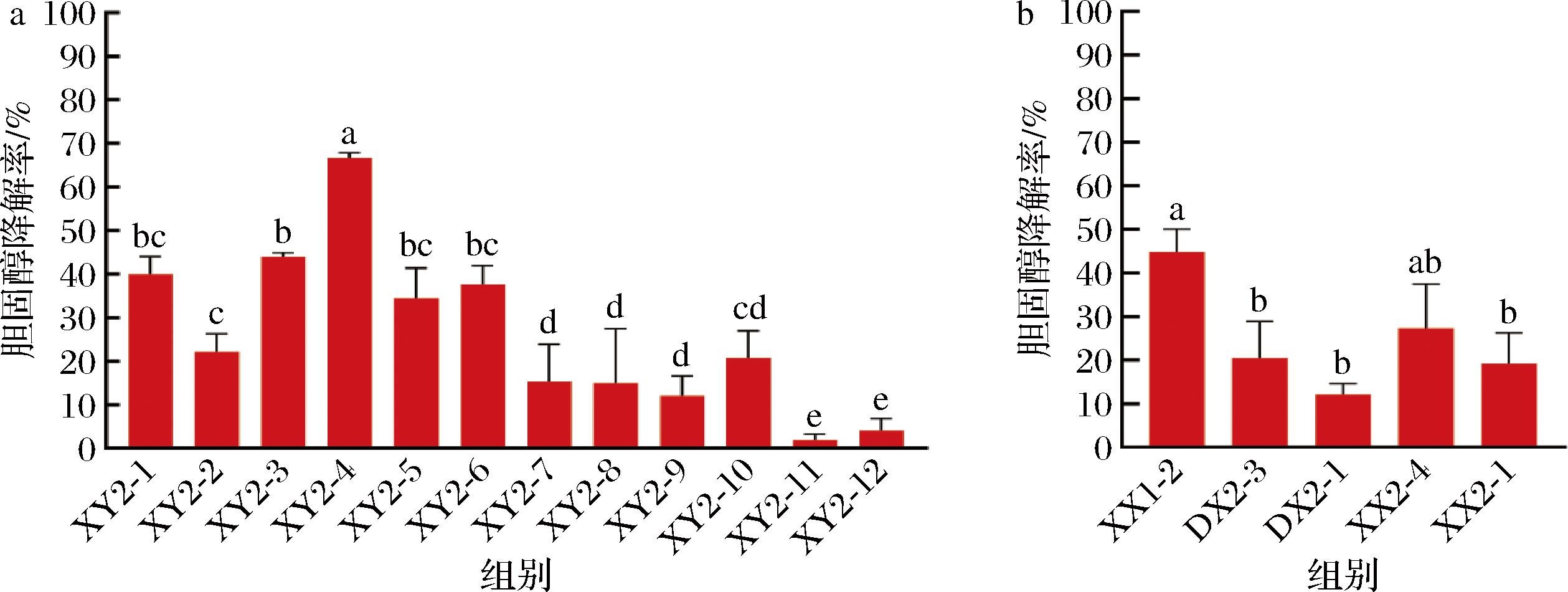
a-细菌菌株;b-真菌菌株
图5 微生物体外降胆固醇效率
Fig.5 In vitro cholesterol-lowering efficiency of microorganisms
注:图中不同字母表示差异显著(P<0.05),相同字母表示差异不显著(P>0.05)。
3 讨论与结论
本研究运用宏基因组测序技术,实现了新疆伊犁州手工奶疙瘩样品中微生物群落的种水平鉴定,为深入探究奶疙瘩微生物群落参与胆固醇降解的分子机制奠定了关键基础。新疆手工奶疙瘩微生物多样性分析结果表明,乳杆菌属、链球菌属和乳球菌属为样品细菌群落中的优势菌属,真菌群落中的优势菌属为酵母属和克鲁维酵母属,与张敏等[13]研究结果一致,其对不同发酵乳制品微生物群落分析发现乳杆菌属(Lactobacillus)为主要菌属,其中牛奶以乳杆菌属和链球菌属(Streptococcus)等细菌种属为主;酸驼奶以乳杆菌属和乳球菌属为主要菌群;酸马奶中除乳杆菌属、乳球菌属外,醋杆菌属(Acetobacter)丰度也较高。同时通过对新疆手工奶疙瘩微生物多样性的分析发现了一个值得关注的现象:即便在同一地区,不同家庭制作的奶疙瘩在微生物组成方面存在差异,这与董晓婉[14]关于新疆不同地区酸马奶微生物群落组成的研究结果相似。产生差异性的原因可能是:虽然生活在同一地区,但不同的家庭饮食偏好存在差异,制造奶疙瘩的发酵时间和温度控制等方面也有差异。正是这种差异性丰富了我国乳酸菌菌质资源,也为新疆传统乳制品中微生物的多样性研究提供了理论依据。
通过KEGG、eggNOG功能注释分析,挖掘新疆手工奶疙瘩微生物代谢过程中的关键酶与功能基因,发现甘油三酯、磷脂、胆固醇和血浆脂蛋白4种脂质代谢相关途径均得到注释,与胆固醇合成和代谢相关的角鲨烯单加氧酶、胆酰甘氨酸水解酶以及胆固醇氧化酶等关键酶也得到了注释,可以初步判断2个奶疙瘩样品中含有胆固醇降解能力的微生物。在奶疙瘩的发酵过程中,乳杆菌属极有可能通过其独特的代谢活动,在降胆固醇功能方面具有巨大的潜力,部分乳杆菌能够巧妙地利用自身产生的代谢产物,如短链脂肪酸、BSH[15]等有效地降低胆固醇在肠道内的吸收效率,促进胆固醇的分解代谢[16]。虽然在样品的基因功能中没有BSH的注释,但是同属于胆酰甘氨酸水解酶家族的基因cbh得到了注释,它是一个对胆固醇降低至关重要的胆汁耐受基因[17]。此外,赵奎[18]研究发现上调小肠Abcg5/8基因并下调小肠Npc1l1基因的表达来增加肝脏胆固醇代谢和转运、增加小肠转运及减少小肠胆固醇吸收,以此改善动脉粥样硬化。链球菌属在发酵过程中同样具有重要作用,其代谢活动可能影响奶疙瘩的风味、质地以及营养特性。关于链球菌属与降胆固醇功能的关系,链球菌在代谢过程中可能产生一些具有潜在降胆固醇活性的物质[19],或者通过调节肠道微生物群落间接影响胆固醇代谢。目前已经报道的乳酸菌降胆固醇的机制主要包括菌体细胞膜的吸附作用、BSH的作用以及产生的代谢产物对胆固醇的分解作用[20]。
我国新疆等地区分布着众多传统发酵乳制品,像酸奶、开菲尔粒、酸奶疙瘩等,这些传统发酵乳制品堪称益生菌资源的“富矿”,蕴含着极为丰富的益生菌[21]。本研究从2个BSH活性较强的新疆伊犁的手工奶疙瘩样品中分离出40株菌,通过耐酸耐胆盐以及体外胆固醇降解率测定等实验,筛选出10株胆固醇降解能力较强的菌株,其中3株为屎肠球菌、2株为乳酸肠球菌、1株为耐久肠球菌、1株为肠膜明串珠菌、2株为马克斯克鲁维酵母、1株为酿酒酵母。虽然已有许多研究报道了传统发酵乳制品中微生物的降胆固醇情况,例如丁小萌等[22]从四川泡菜中筛选到1株具有较高安全性的干酪乳酪杆菌S1,胆盐共沉淀和菌体同化形式的胆固醇去除量分别为47.86%和34.66%;江一帆等[23]从广西传统发酵食品中分离出具有高胆固醇降解能力的植物乳植杆菌HGP42,其静息状态、热死亡状态、裂解状态下的降胆固醇能力分别为34.52%、15.88%、9.46%。然而,这些研究报道中筛选的具有降胆固醇能力的菌株大多是乳酸菌,本研究除了筛选出胆固醇降解率理想的乳酸菌外,还筛选出了3株胆固醇降解率较高的酵母菌,尤其是酿酒酵母XX1-2,胆固醇降解率达到了44.83%。目前对于酵母菌降胆固醇的相关报道较少,其胆固醇降解机制尚不明确,但有部分研究表明酵母菌与乳酸菌在降胆固醇方面展现出显著的协同效应。酵母菌能够通过提高乳酸菌在酸性环境中的存活率[24],从而增强益生菌在胃肠道的定殖能力。在发酵食品中,酵母菌与乳酸菌的混合发酵不仅具备改善食品的风味特性的作用,还能通过调节微生物代谢影响胆固醇水平[25]。此外,酵母菌细胞膜中麦角固醇向胆固醇的转化机制[26],为深入理解其在胆固醇代谢调控中的分子作用提供了重要线索。
在本研究中,通过宏基因组测序技术分析发现新疆手工奶疙瘩中具有丰富的细菌多样性,其中厚壁菌门为优势菌门,乳杆菌属为样品X1的优势菌属,链球菌属为样品X2的优势菌属,X1的优势菌种为德氏乳杆菌,X2的优势菌种为嗜热链球菌。然而,在后续的分离实验中未能成功分离出这些优势菌种,而是分离出了屎肠球菌、乳酸肠球菌和部分酵母。推测出现这种结果的原因可能是:当前采用的培养方法可能更倾向于促进好氧菌或兼性厌氧菌的生长,而优势乳酸菌可能处于活的非可培养状态,难以通过常规培养手段获得。这一结果不仅反映出新疆手工奶疙瘩中微生物群落的复杂性和多样性,还反映出同一地区不同家庭制作的发酵乳制品在微生物群落结构上存在显著差异,分离实验的局限性也提示在研究微生物群落时,需要进一步优化培养条件和分离技术,以更好地揭示微生物群落的真实组成和功能特性。通过KEGG、eggNOG等基因功能预测和分析,发现手工奶疙瘩样品中的大部分微生物与转运代谢功能有关,脂代谢等胆固醇相关代谢途径也得到了注释,它们除了塑造出新疆手工奶疙瘩独特的风味外,还说明了其中具有胆固醇降解能力的微生物。此外,本研究还分离出了10株胆固醇降解能力>20%的菌株,其中乳酸肠球菌XY2-4的胆固醇降解率达到66.63%,酿酒酵母XX1-2胆固醇降解率达到了44.83%。当前研究表明,虽然酵母菌在体外和动物实验中显示出降胆固醇潜力,但其作用机制仍待深入阐明,可能涉及与乳酸菌的协同效应及发酵代谢调控;相比之下,乳酸菌的降胆固醇机制更为明确,主要通过胆盐代谢、胆固醇结合及肠道菌群调节发挥作用;而酵母菌的作用机制研究较少,可能涉及与乳酸菌的协同效应及发酵代谢调控,混合菌株(乳酸菌+酵母)发酵可能通过协同代谢途径更高效地降低胆固醇。未来研究应重点关注酵母菌在胆固醇代谢中的具体分子机制以及乳酸菌与酵母菌联合使用的协同作用机理。二者作用途径虽不同,但均展现出一定的降胆固醇潜力。深入探索这些微生物的互作关系,将有助于开发更高效的多菌种复合益生菌制剂,为胆固醇代谢异常提供精准、创新的解决方案。
[1] 麦日艳古·亚生, 李明源, 王继莲, 等.塔什库尔干地区传统手工乳制品中乳酸菌多样性及其功能分析[J].微生物学通报, 2024, 51(3):950-969.
MAIRIYANGU Y S, LI M Y, WANG J L, et al.Diversity and functions of lactic acid bacteria in traditional handmade dairy products in Tashkurgan region[J].Microbiology China, 2024, 51(3):950-969.
[2] 王进.新疆奶疙瘩细菌多样性与风味解析及菌株的应用[D].上海:上海海洋大学,2021.
WANG J.Analysis of bacterial diversity and flavor in Xinjiang milk curd and application of strains[D].Shanghai:Shanghai Ocean University, 2021.
[3] 陈欢.新疆哈萨克族传统奶酪中乳酸菌发酵剂的筛选及对奶酪风味影响的研究[D].石河子:石河子大学,2019.
CHEN H.Screening of lactic acid bacteria starters from Xinjiang Kazak traditional cheese and study on their influence on cheese flavor[D].Shihezi:Shihezi University, 2019.
[4] 王雪, 谈亚丽, 孙罗曦, 等.西藏传统发酵牦牛乳制品中乳酸菌的分离与鉴定[J].中国乳品工业, 2025, 53(6):27-32.
WANG X, TAN Y L, SUN L X, et al.Isolation and identification of lactic acid bacteria in traditional fermented yak dairy products collected from Tibet[J].China Dairy Industry, 2025, 53(6):27-32.
[5] ZHENG X J, LIU F, LI K X, et al.Evaluating the microbial ecology and metabolite profile in Kazak artisanal cheeses from Xinjiang, China[J].Food Research International, 2018, 111:130-136.
[6] 张苗苗, 蔡文超, 旦巴达贡, 等.哈密地区奶疙瘩微生物多样性研究[J].食品研究与开发, 2021, 42(17):176-182.
ZHANG M M, CAI W C, DANBA D G, et al.Study on microbial diversity of cheese in Hami Region based on high-throughput sequencing technology[J].Food Research and Development, 2021, 42(17):176-182.
[7] 热米拉·阿扎提.新疆传统乳制品奶疙瘩中乳酸菌的筛选及其抗衰老活性的研究[D].杭州:浙江大学,2016.
REMILA A.Screening of lactic acid bacteria from Xinjiang traditional dairy product milk curd and study on their anti-aging activity[D].Hangzhou:Zhejiang University, 2016.
[8] 范蕊, 王文文, 魏琳娜, 等.基于宏基因组学分析不同发酵时期新疆沙棘酵素微生物群落结构及功能[J].食品工业科技, 2025, 46(8):173-181.
FAN R, WANG W W, WEI L N, et al.Metagenomic analysis of microbial community structure and functional profiling during different fermentation stages of Xinjiang sea buckthorn Jiaosu[J].Science and Technology of Food Industry, 2025, 46(8):173-181.
[9] TIAN H X, XIONG J J, YU H Y, et al.Flavor optimization in dairy fermentation:From strain screening and metabolic diversity to aroma regulation[J].Trends in Food Science &Technology, 2023, 141:104194.
[10] BAO W, HE Y X, YU J H, et al.Diversity analysis and gene function prediction of bacteria and fungi of Bactrian camel milk and naturally fermented camel milk from Alxa in Inner Mongolia[J].LWT, 2022, 169:114001.
[11] 蔡扩军, 妥彦峰, 徐敏, 等.新疆传统发酵乳制品调研及其发酵微生物种质资源分析[J].中国乳品工业, 2024, 52(2):12-19.
CAI K J, TUO Y F, XU M, et al.Investigation of traditional fermented dairy products and analysis of fermentation microbial resources in Xinjiang[J].China Dairy Industry, 2024, 52(2):12-19.
[12] 于江傲, 陈晓静, 刘剑桥, 等.乳酸菌代谢产物降解胆固醇作用研究[J].粮食与油脂, 2023, 36(9):116-122.
YU J A, CHEN X J, LIU J Q, et al.Study on cholesterol degradation by metabolites of Lactobacillus[J].Cereals &Oils, 2023, 36(9):116-122.
[13] 张敏, 张艳, 黄丽丽, 等.基于16S rDNA高通量测序方法比较新疆西北部地区乳品中微生物的多样性[J].食品科学, 2017, 38(20):27-33.
ZHANG M, ZHANG Y, HUANG L L, et al.Application of 16S rDNA high-throughput sequencing for comparative study of the microbial diversity of dairy products from western and northern Xinjiang, China[J].Food Science, 2017, 38(20):27-33.
[14] 董晓婉.新疆和布克赛尔县哈萨克族和蒙古族传统乳制品中乳酸菌菌群多样性的研究[D].石河子:石河子大学,2014.
DONG X W.Study on the diversity of lactic acid bacteria flora in traditional dairy products of Kazak and Mongolian in Hoboksar County, Xinjiang[D].Shihezi:Shihezi University, 2014.
[15] JIA B L, ZOU Y Q, HAN X, et al.Gut microbiome-mediated mechanisms for reducing cholesterol levels:Implications for ameliorating cardiovascular disease[J].Trends in Microbiology, 2023, 31(1):76-91.
[16] FAN X K, LING N, LIU C L, et al.Screening of an efficient cholesterol-lowering strain of Lactiplantibacillus plantarum 54-1 and investigation of its degradation molecular mechanism[J].Ultrasonics Sonochemistry, 2023, 101:106698.
[17] CHINTAKOVID N, SINGKHAMANAN K, YAIKHAN T, et al.Probiogenomic analysis of Lactiplantibacillus plantarum SPS109:A potential GABA-producing and cholesterol-lowering probiotic strain[J].Heliyon, 2024, 10(13):e33823.
[18] 赵奎.传统发酵食品源植物乳杆菌WLPL21缓解高胆固醇血症和改善动脉粥样硬化的机制研究[D].南昌:南昌大学,2024.
ZHAO K.Mechanism of Lactobacillus plantarum WLPL21 from traditional fermented foods in alleviating hypercholesterolemia and improving atherosclerosis[D].Nanchang:Nanchang University, 2024.
[19] SINGH J, METRANI R, SHIVANAGOUDRA S R, et al.Review on bile acids:Effects of the gut microbiome, interactions with dietary fiber, and alterations in the bioaccessibility of bioactive compounds[J].Journal of Agricultural and Food Chemistry, 2019, 67(33):9124-9138.
[20] 黄芳, 刘欣桐, 黄佳蓉, 等.酸茶中降胆固醇筛选及安全性与益生特性研究[J/OL].中国食品学报, 2025:1-13.(2025-03-20).https://kns.cnki.net/kcms/detail/11.4528.TS.20250319.1939.010.html.
HUANG F, LIU X T, HUANG J R, et al.Screening for cholesterol-lowering properties in sour tea and assessment of safety and probiotic characteristics[J/OL].Journal of Chinese Institute of Food Science and Technology, 2025:1-13.(2025-03-20).https://kns.cnki.net/kcms/detail/11.4528.TS.20250319.1939.010.html.
[21] 周闯, 宋俊雅, 张华, 等.克州地区传统发酵乳制品中抗氧化益生菌的筛选[J].畜牧与兽医, 2025, 57(2):54-61.
ZHOU C, SONG J Y, ZHANG H, et al.Screening of probiotics with antioxidant activity in traditional fermented dairy products in the Kezhou area[J].Animal Husbandry &Veterinary Medicine, 2025, 57(2):54-61.
[22] 丁小萌, 李明星, 赵芃, 等.一株高效降胆固醇乳酸菌的筛选与特性研究[J].中国微生态学杂志, 2024, 36(4):401-407;413.
DING X M, LI M X, ZHAO P, et al.Screening and characterization of a strain of highly efficient cholesterol-reducing lactic acid bacteria[J].Chinese Journal of Microecology, 2024, 36(4):401-407;413.
[23] 江一帆, 滕建文, 黄丽, 等.具有降解胆固醇益生活性和后生元特性的乳酸菌菌株筛选[J].食品科技, 2023, 48(9):9-16.
JIANG Y F, TENG J W, HUANG L, et al.Screening of lactic acid bacteria strains with cholesterol-degrading probiotic and postbiotic properties[J].Food Science and Technology, 2023, 48(9):9-16.
[24] HIRAI S, KAWASUMI T.Enhanced lactic acid bacteria viability with yeast coincubation under acidic conditions[J].Bioscience, Biotechnology, and Biochemistry, 2020, 84(8):1706-1713.
[25] FANG L P, WANG W J, DOU Z X, et al.Effects of mixed fermentation of different lactic acid bacteria and yeast on phytic acid degradation and flavor compounds in sourdough[J].LWT, 2023, 174:114438.
[26] KURODA K, MORIOKA S, SHIGEMORI T, et al.Modification of sterol composition in yeast cell membrane from ergosterol to cholesterol and its effect on Ste2 signaling[J].The FASEB Journal, 2013, 27(S1):1096.8.