乳制品是人们获取蛋白质和钙的重要来源,它们富含蛋白质、脂肪、必需氨基酸以及多种维生素和矿物质,如钙、钠、磷、镁和铁。其中,钙、维生素D和支链氨基酸含量尤为丰富,这些营养素在传统饮食中一直是促进骨骼和肌肉健康的关键成分[1]。乳制品中的钙质不仅含量高,而且易于吸收,是维持骨骼强度和预防骨质疏松的重要保障。同时,丰富的蛋白质和氨基酸有助于肌肉修复和生长,使乳制品成为缓解肌肉减少症、增加肌肉质量和力量的理想食品选择[2-4]。
在众多乳制品中,奶酪对骨骼与肌肉健康的促进作用也引起了人们的关注。MORA-GUTIERREZ等[5]的研究发现,山羊奶酪的摄入对大鼠的钙吸收和骨矿化有显著影响。DE LUCA等[6]通过细胞实验证明,奶酪的体外消化产物能够显著促进钙的吸收和骨基质的形成,其中酪蛋白磷酸肽起到了重要作用。DE HART等[7]发现切达奶酪的摄入能够提供持久的氨基酸循环,从而促进肌肉蛋白质合成。但是有关奶酪中调节骨骼健康和肌肉健康生物活性物质的相关报道较少。
研究表明,奶酪成熟过程中蛋白质、脂肪、碳水化合物等大分子物质,在微生物和酶的协同作用下发生一系列的生化反应[8],包括乳蛋白的降解与多肽的生成。奶酪的成熟过程主要包括三方面的生化反应,糖类的酵解、脂肪的分解和蛋白质的水解。蛋白质的水解在奶酪成熟过程中对奶酪的风味和组织结构会产生至关重要的影响[9],是奶酪成熟过程中最重要的反应。蛋白质的水解由凝乳酶、牛乳自身的蛋白酶和发酵剂以及附属发酵剂的蛋白酶协同作用。乳蛋白水解不仅赋予奶酪独特的风味,而且会产生丰富的乳源多肽。
如表1所示,目前已报道的乳源生物活性肽多来自于酪蛋白,具有易被人体吸收、特异性高的特点,其功能包括抗高血压、抗菌、调节免疫、预防骨质疏松等多种功能[10]。在乳源生物活性肽中,肽段IPP和VPP的功能被广泛关注,已被证明具有血管紧张素转换酶(angiotensin converting enzyme,ACE)抑制活性、抗炎抗氧化、促进骨骼健康等功能[11-13]。肽段NIPPLTQTPVVVPPFLQPE(NE-19)则被证实具有调节认知的功能[14]。来源于瑞士乳杆菌发酵乳的肽段FPP、NE-19和RHPHPHLSF(RF-9),在细胞实验中分别表现出了促进成骨细胞增殖[15]、促进成肌细胞增殖分化并加速细胞周期[16]的功效。但是,目前尚无研究解析以上生物活性肽在奶酪成熟过程中的生成情况,以及奶酪附属发酵剂对其生成的影响。
表1 相关乳源生物活性肽信息
Table 1 Information of dairy-derived bioactive peptides
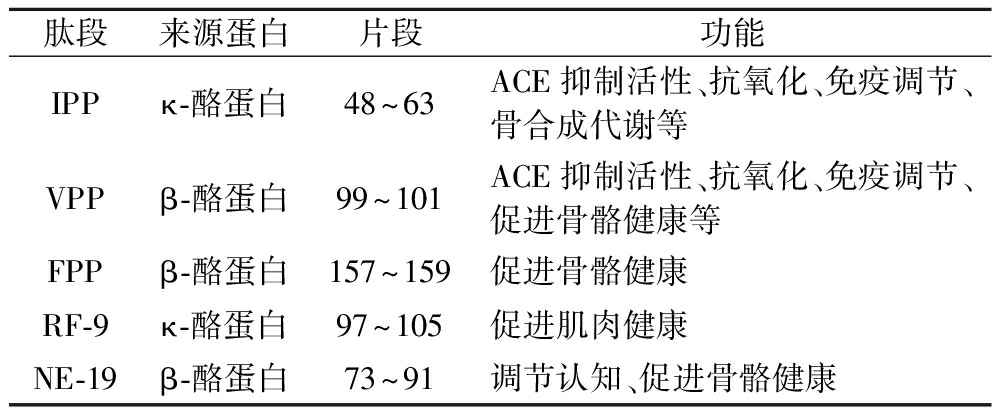
肽段来源蛋白片段功能IPPκ-酪蛋白48~63ACE抑制活性、抗氧化、免疫调节、骨合成代谢等VPPβ-酪蛋白99~101ACE抑制活性、抗氧化、免疫调节、促进骨骼健康等FPPβ-酪蛋白157~159促进骨骼健康RF-9κ-酪蛋白97~105促进肌肉健康NE-19β-酪蛋白73~91调节认知、促进骨骼健康
作为奶酪加工中常用的乳酸菌之一,瑞士乳杆菌的蛋白水解系统如图1所示,主要包括胞壁蛋白酶、肽转运系统、氨肽酶、内肽酶等。奶酪中的酪蛋白在细胞外被胞壁蛋白酶分解成长短不一的多肽,经肽转运系统运输到细胞内部,由胞内酶进一步分解成小肽和氨基酸,同时奶酪成熟过程中,菌体会发生自溶,内部一系列的酶释放出来进入奶酪中直接与底物反应,加速奶酪成熟形成特定风味[17]与生物活性肽。
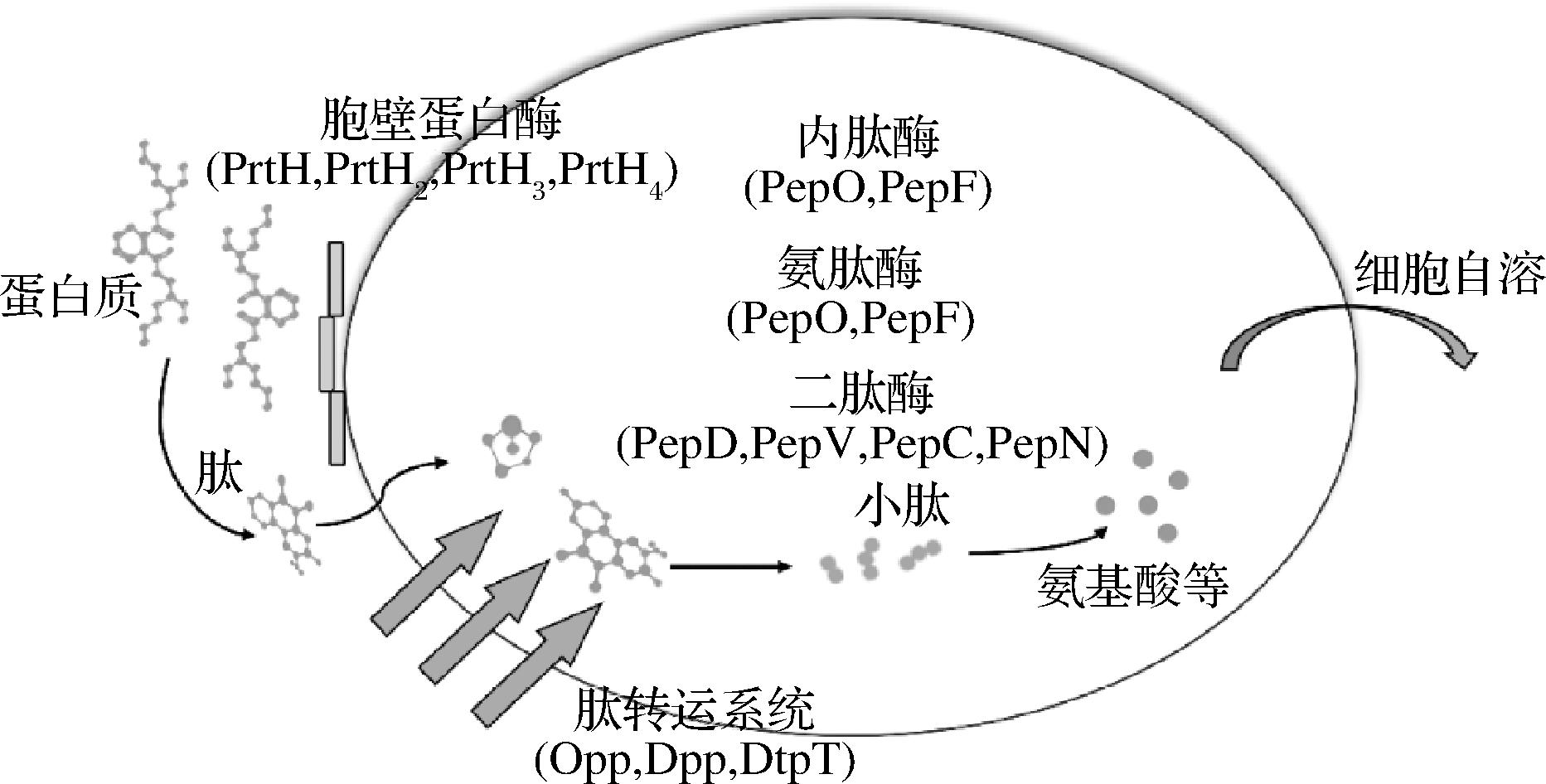
图1 瑞士乳杆菌蛋白水解系统
Fig.1 Proteolytic system of Lactobacillus helveticus
瑞士乳杆菌在长期进化过程中形成了独特的蛋白水解系统以适应乳基质环境。不同基因型的蛋白酶通过差异化的底物识别位点和切割模式赋予菌株异质性的蛋白水解特性。在针对瑞士乳杆菌基因组特征与发酵特性的前期研究中筛选获得了1株拥有3种胞壁蛋白酶(PrtH2-3-4)基因型的菌株,即瑞士乳杆菌CCFM1263[18]。在和其他瑞士乳杆菌对比中,CCFM1263在发酵过程中对αS1-酪蛋白和β-酪蛋白具有更多的水解位点;CCFM1263发酵乳中的多肽种类最多,功能分布最广,峰强度最高[19],具有促进骨骼和肌肉健康的功能[20]。采用奶酪附属发酵剂的评价体系,系统性评估了CCFM1263作为奶酪附属发酵剂的潜力,发现其在模拟奶酪加工与成熟环境下具有良好的生长产酸特性,具有适宜的自溶度、较强的胞壁蛋白酶和肽酶活力等特性,具有作为奶酪附属发酵剂的潜力。因此本研究拟探讨CCFM1263的添加对切达奶酪成熟过程中生物活性肽的产生及其对切达奶酪促进成骨细胞和成肌细胞增殖效果的影响。
1 材料与方法
1.1 材料与试剂
1.1.1 实验试剂
生牛乳,无锡天资乳业。
凝乳酶:MARZYME XT 220 PF Liquid,丹尼斯克公司。
硼酸、NaOH、浓硫酸、CuSO4、K2SO4、石油醚、乙醚、氨水、冰乙酸、乙醇、三氯乙酸(trichloroacetic acid,TCA)、磷钨酸(phosphotungstic acid,PTA)(均为分析纯),国药集团化学试剂有限公司;达尔伯克改良伊格尔培养基(Dulbecco’s modified Eagle’s medium,DMEM)、阿尔法改良极限必需培养基(alpha minimal essential medium,α-MEM),赛默飞世尔科技有限公司;CCK-8试剂盒,上海碧云天生物技术有限公司。
1.1.2 培养基
MRS液体培养基:用于菌株的增殖培养;LBS琼脂培养基:用于乳杆菌的平板计数;GM17琼脂培养基:用于乳球菌的平板计数。
1.1.3 实验菌株
本文所使用的瑞士乳杆菌CCFM1263由江南大学食品学院生物技术中心提供。奶酪发酵剂菌株:CHOOZIT RA 14 LYO 50 DCU(组成为乳酸乳球菌乳亚种R8、乳脂乳球菌R9、唾液链球菌嗜热亚种ST),丹尼斯克公司。
1.2 仪器与设备
GR60DA高压蒸汽灭菌器,美国ZEALWAY公司;MCB-900VA9N超净工作台,中科美菱低温科技股份有限公司;HWS-150恒温恒湿培养箱、DK-S12恒温水浴锅、DGG-9123A电热恒温鼓风干燥箱,上海森信实验仪器有限公司;AW500SG-7101厌氧工作站,英国依莱科泰有限公司;25L奶酪槽,天津隆业轻工机械有限公司;TGL-16M台式高速离心机,上海卢湘仪仪器有限公司;FE28-Standard pH计,梅特勒-托利多仪器有限公司;K1100自动凯氏定氮仪,山东海能仪器有限公司;QTRAP5500三重四极杆复合线性离子阱液质联用仪,美国应用生物系统公司。
1.3 实验方法
1.3.1 切达奶酪制作
参考江丽红[21]的方法并根据实际操作修改,其制作流程如下:
生牛乳巴氏杀菌后,冷却至32 ℃,加入发酵剂,其中CC组奶酪只添加106 CFU/mL牛奶的奶酪发酵剂,AC组奶酪在添加奶酪发酵剂的基础上添加106 CFU/mL牛奶的CCFM1263。发酵30 min,凝乳酶以质量分数0.025%添加至牛乳中凝乳,用线刀进行切割并愈合,升温后进行排乳清和堆酿,至乳清酸度降至45~55 °T再切块加盐,压榨机压榨过夜,真空包装并放置在成熟箱中进行成熟。成熟温度为6~8 ℃,成熟周期为6个月。
1.3.2 奶酪基本组分测定
参照GB 5009.3—2016《食品安全标准 食品中水分的测定》烘箱常压干燥法测定切达奶酪中的水分含量;脂肪含量的测定参照GB 5009.6—2016《食品安全标准 食品中脂肪的测定》;蛋白质含量测定采用凯氏定氮法,换算系数为6.38;使用pH计对奶酪样品pH值测定。每组实验平行3次。
1.3.3 奶酪中微生物的测定
奶酪样品前处理参考FRANCIOSI等[22]的方法略作修改:将奶酪用无菌生理盐水10倍梯度稀释。取稀释液1 mL进行倾注实验,一式三份。LBS、GM17培养基分别用于乳杆菌、乳球菌的计数。
1.3.4 蛋白水解的测定
1.3.4.1 水溶性氮(water-soluble nitrogen,WSN)测定
参考殷俊玲[23]的方法,将奶酪加入pH 4.6的醋酸盐缓冲液充分打碎,离心取上清液定量进行凯氏定氮,并以奶酪总氮量的比例(%)表示。
1.3.4.2 0.12 g/mL三氯乙酸可溶性氮(nitrogen soluble in 0.12 g/mL trichloroacetic acid,TCA-SN)测定
取1.3.4.1节中WSN和0.48 g/mL的TCA溶液按照体积比1∶3混合,充分振荡混匀静置30 min后,离心取上清液定量进行凯氏定氮,并以占奶酪总氮量的质量分数(%)表示。
1.3.4.3 0.05 g/mL磷钨酸可溶性氮(nitrogen soluble in 0.05 g/mL phosphotungstic acid,PTA-SN)测定
取1.3.4.1节中制备的WSN与0.10 g/mL的PTA溶液按照体积比1∶1混合,充分振荡混匀4 ℃静置24 h,离心取上清液进行凯氏定氮,并以占奶酪总氮量的质量分数(%)表示。
1.3.5 切达奶酪生物活性肽的定量
样品预处理:准确量取1.00 g奶酪,加9 mL的超纯水,将奶酪充分打碎,静置30 min,4 ℃、12 000 r/min离心20 min,取上清液过0.22 μm有机相滤膜装于进样瓶待测。生物活性肽标品稀释至1 mg/L。
检测条件:色谱柱选用HSS T3柱(1.8 μm,2.1 mm×100 mm),流动相A为含0.1%(体积分数)甲酸的水溶液,流动相B为乙腈,洗脱梯度为:2% B,0~1 min;2%~20% B,2~5 min;20%~98% B,5~9 min;98%~2% B,9~12 min。流速设置为0.3 mL/min,柱温40 ℃。每个样品3组平行。
1.3.6 切达奶酪对MC3T3-E1细胞增殖能力的影响
奶酪提取物的处理:精确称取奶酪3.00 g和27 mL纯净水混匀打碎,静置1 h,4 ℃、4 000 r/min离心20 min,取上清液过0.22 μm有机相滤膜除菌后于培养基中稀释。
将MC3T3-E1以1×104个细胞/孔的密度接种于96孔板中,在37 ℃、5% CO2的完全培养基(α-MEM,体积分数10%胎牛血清和体积分数1%青霉素-链霉素)中培养24 h后取出,洗去旧培养基后,用含400 mg/L奶酪水溶物的培养基培养24 h,随后加入CCK-8溶液测定吸光度。
1.3.7 切达奶酪对C2C12细胞增殖能力的影响
将C2C12以1×104个细胞/孔的密度接种于96孔板中,在37 ℃、5% CO2的完全培养基(DMEM,体积分数10%胎牛血清和体积分数1%青霉素-链霉素)中培养24 h后取出,洗去旧培养基后,用含400 mg/L奶酪水溶物的培养基培养24 h,随后加入CCK-8溶液测定吸光度。
1.4 统计分析及数据处理
采用Origin Pro 2025和Graphpad prism 9.0对实验数据进行绘图;利用SPSS 24.0对实验结果进行显著性分析,其中所有检测结果图、表中,同列/行数据的上标字母不同表示差异显著(P<0.05)。
2 结果与讨论
2.1 切达奶酪的基本成分
如表2所示,CC组和AC组奶酪在基本成分上无显著性差异。2组奶酪的水分占奶酪非脂乳固体比例分别为(61.76±0.49)%和(61.89±0.15)%,其干物质中脂肪含量为(52.41±0.76)%和(53.28±0.25)%,属于全脂半硬质奶酪。
表2 切达奶酪成熟0 d的基本组成
Table 2 Composition of fresh (0 d) Cheddar cheeses in control and experiment cheese

组别脂肪/%蛋白质/%水分/%pHCC组29.63±0.42a20.51±0.26a43.46±0.25a5.35±0.01aAC组30.30±0.16a20.44±0.37a43.14±0.10a5.37±0.02a
注:同列不同字母表示存在显著性差异(P<0.05)。
2.2 切达奶酪在成熟过程中的微生物变化
在2组奶酪成熟6个月的过程中,采用GM17和LBS培养基分别对发酵剂(乳酸乳球菌乳亚种R8、乳脂乳球菌R9、唾液链球菌嗜热亚种ST)和附属发酵剂(瑞士乳杆菌CCFM1263)进行平板计数,观察奶酪体系中微生物的变化情况,结果如图2所示。奶酪整体的活菌数在整个成熟过程中保持较高的活菌数,发酵剂和附属发酵剂的活菌数都在7.00 lg CFU/g以上,同时在成熟期间奶酪中发酵剂的活菌数一直处于下降趋势。以CC组为例,发酵剂活菌数从最初的8.20 lg CFU/g减少到7.21 lg CFU/g,相较于发酵剂,CCFM1263在成熟过程中活菌数下降趋势更快,从最初的8.07 lg CFU/g减少到6.81 lg CFU/g。但是,添加附属发酵剂后,AC组奶酪的发酵剂活菌数下降速度减缓,在6个月依旧能保持7.88 lg CFU/g。奶酪成熟过程中的低酸与高盐环境使奶酪中的活菌数不断减少,最终达到稳定水平,而添加了CCFM1263的奶酪中发酵剂的活菌数显著高于CC组,说明CCFM1263的加入有助于奶酪发酵剂在成熟过程中保持较高的活菌数,同时CCFM1263在AC组中能够保证较高的活菌数,AC组奶酪的高微生物存活率为奶酪成熟中的蛋白水解和生物活性肽的产生提供了良好的基础。
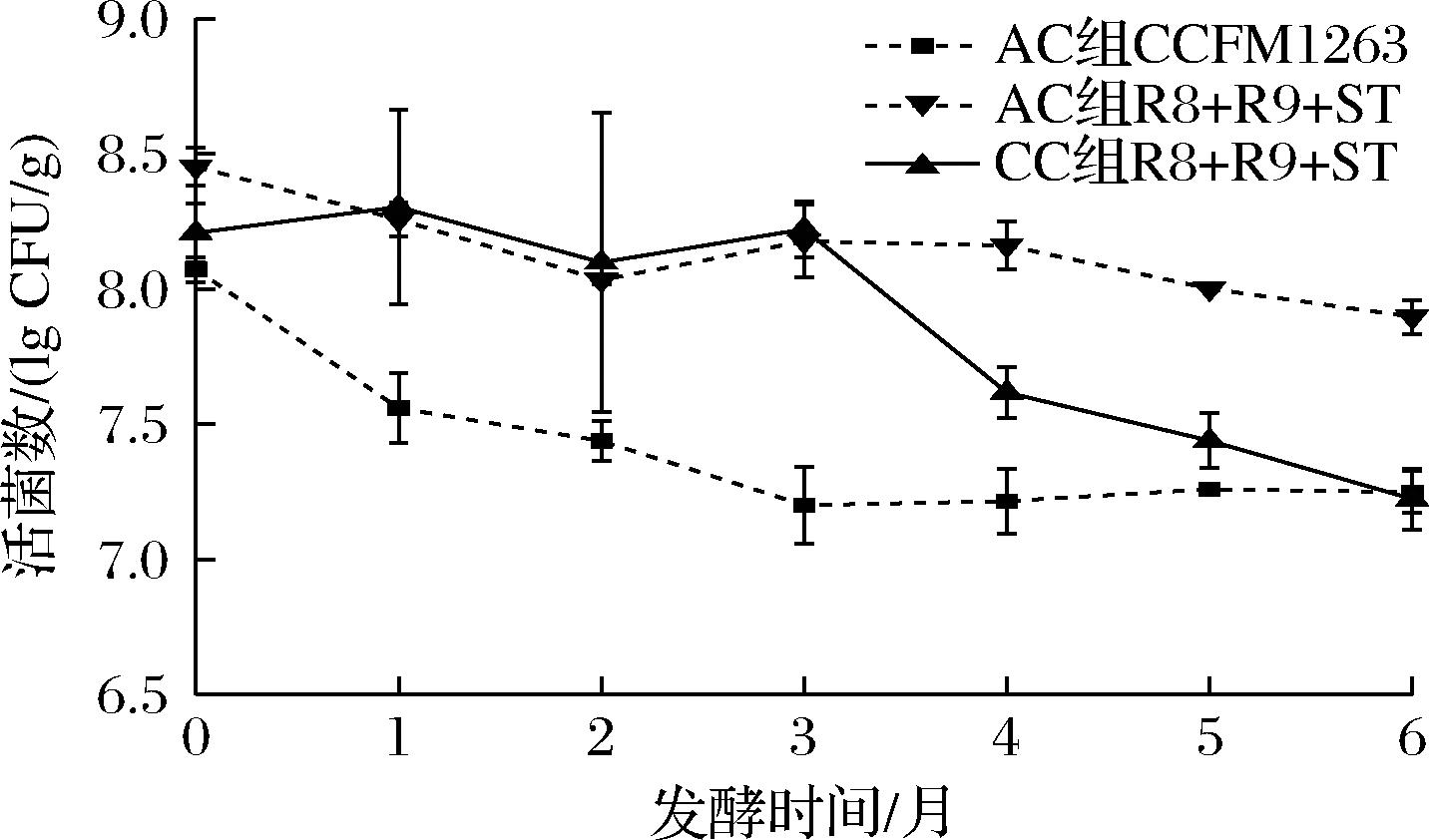
图2 切达奶酪成熟过程中微生物变化情况
Fig.2 Microbial changes during ripening process of Cheddar cheese
注:CC组R8、R9、ST总活菌数 (▲),AC组R8、R9、ST总活菌数 (▼),AC组CCFM1263活菌数 (■)。
2.3 切达奶酪在成熟过程中的蛋白质水解和生物活性肽产生规律
奶酪的成熟与蛋白水解密切相关,酪蛋白在凝乳酶、发酵剂与附属发酵剂提供的多种酶(如胞壁蛋白酶、肽转运系统、氨肽酶、内肽酶等)作用下水解蛋白[24]。具体而言,凝乳酶主要负责将完整蛋白质裂解为长链多肽,胞壁蛋白酶则进一步将其降解为较短肽链,而氨基酸和风味物质的形成主要依赖于胞内肽酶释放[8]。瑞士乳杆菌CCFM1263体现出其独特的蛋白水解特性,不仅体现在其胞壁蛋白酶的高活性[25],同时其对酪蛋白的水解能力具有显著的菌株特异性[26]。
如表3所示,奶酪的WSN、12% TCA-SN和5% PTA-SN含量随着成熟时间的延长而不断上升。在奶酪成熟初期,WSN的形成主要是由凝乳酶及发酵剂中的蛋白酶产生作用[27]。所以前期2组奶酪之间WSN并无显著性差异,而到了后期,AC组奶酪的WSN为(31.74±0.01)%,显著高于CC组的(25.28±0.02)%。12% TCA-SN主要是受切达奶酪中菌株的胞壁蛋白酶和肽酶影响,AC组切达奶酪在第3个月时其的12% TCA-SN含量就达到(14.40±0.21)%,显著高于CC组,这表明附属发酵剂CCFM1263可为奶酪成熟过程提供更高的肽酶水解产物。分子质量<500 kDa的小肽和氨基酸类物质能够溶于5% PTA溶液。由2组切达奶酪的5% PTA-SN的变化可以看出,在成熟初期AC组的奶酪就有较高的5% PTA-SN,其含量为(3.54±0.09)%,显著高于CC组的(1.99±0.01)%。这说明在奶酪发酵时期CCFM1263中的肽酶就具有快速分解蛋白生成小肽的能力,在奶酪成熟全过程中,AC组奶酪的5% PTA-SN都显著大于CC组。
表3 两组切达奶酪成熟过程中蛋白质水解情况
Table 3 Analysis of protein hydrolysis during ripening in two sets of Cheddar cheese
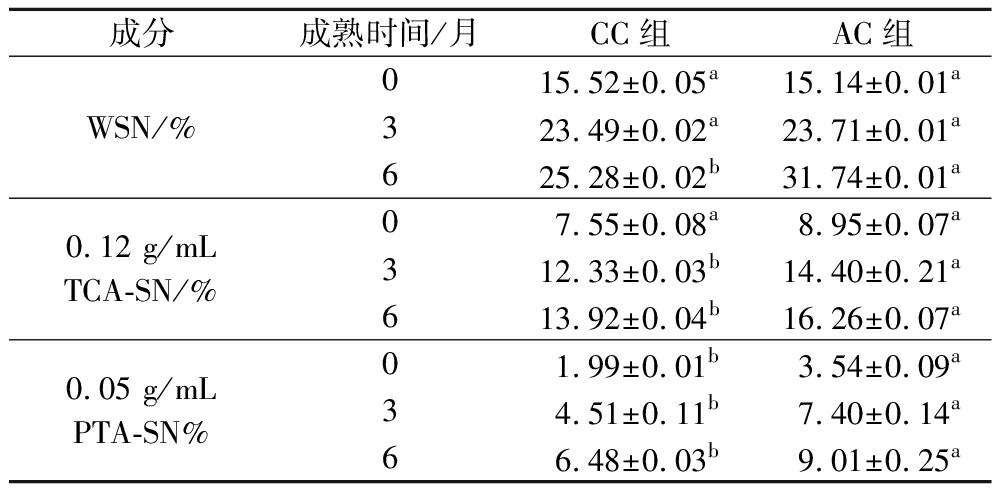
成分成熟时间/月CC组AC组WSN/%0 15.52±0.05a15.14±0.01a3 23.49±0.02a23.71±0.01a6 25.28±0.02b31.74±0.01a0.12 g/mL TCA-SN/%0 7.55±0.08a8.95±0.07a3 12.33±0.03b14.40±0.21a6 13.92±0.04b16.26±0.07a0.05 g/mLPTA-SN%0 1.99±0.01b3.54±0.09a3 4.51±0.11b7.40±0.14a6 6.48±0.03b9.01±0.25a
注:同行不同字母表示存在显著性差异(P<0.05)。
CCFM1263不仅能够显著促进切达奶酪中的多肽、小肽和氨基酸的产生速率,加速奶酪的成熟,更能产生具有独特氨基酸序列的特征性肽段。瑞士乳杆菌CCFM126对酪蛋白的蛋白序列有广泛的水解能力,其中对β-酪蛋白具有更强的水解作用,同时反映在其产肽的数量上,对β-酪蛋白有其偏好的水解位点[28]。研究表明,瑞士乳杆菌CCFM1263在酪蛋白上有特异性切割位点,能够产生特异性的生物活性肽[19],其中FPP和NE19已经被证明具有促进骨骼健康的功能[16],RF-9能够促进肌肉健康[15]。已经有大量文献报道IPP和VPP具有ACE抑制活性、抗氧化、免疫调节、参与骨合成代谢等功能[11-13]。如图3所示,这5种生物活性肽在2组奶酪中的含量都随着成熟时间的延长而上升,其中AC组生物活性肽FPP、RF-9和NE-19在成熟3个月时,含量显著高于CC组,分别达到(27.47±1.89)、(427.477±92.21)、(296.30±37.85) μg/kg。AC组奶酪的IPP和VPP的含量在前3个月和CC组相当,在成熟6个月时AC组的IPP和VPP大量积累,含量为(105.97±3.82)、(103.93±4.15) μg/kg,显著高于CC的(66.80±5.41)、(76.37±3.76) μg/kg。AC组奶酪在添加CCFM1263后加速了FPP、RF-9和NE-19的产生,提高了IPP和VPP的含量,具有更高的生物活性肽含量。
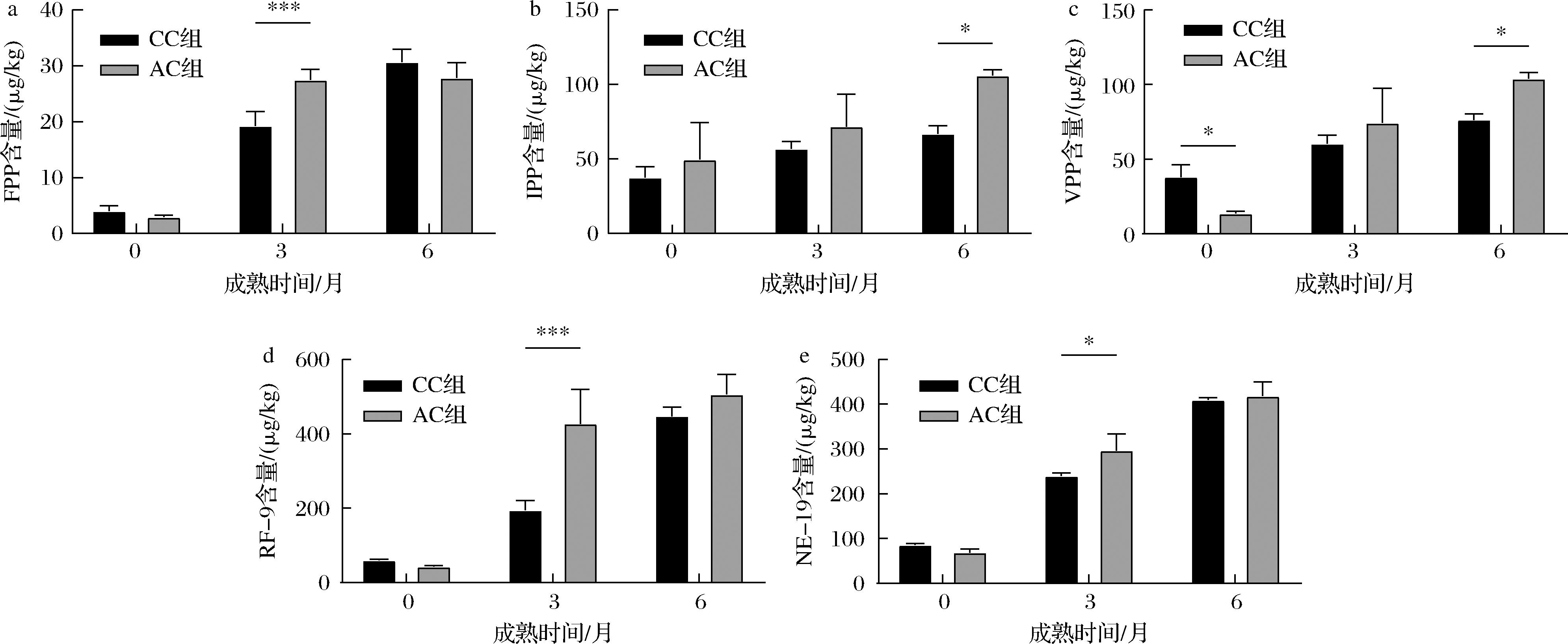
a-FPP;b-IPP;c-VPP;d-RF-9;e-NE-19
图3 切达奶酪中生物活性肽的浓度
Fig.3 Concentrations of bioactive peptides in Cheddar cheese
注:*差异显著(P<0.05);***差异高度显著(P<0.001)。
2.4 切达奶酪对成骨细胞和成肌细胞增殖的作用
切达奶酪提取物添加在细胞培养基后对成骨细胞和成肌细胞的增殖具有显著影响,且其效果与奶酪的成熟时间和是否添加附属发酵剂CCFM1263密切相关。如图4所示,在400 μg/mL的最佳质量浓度下,添加奶酪提取物培养24 h后,所有实验组较对照组均呈现显著促增殖效果。
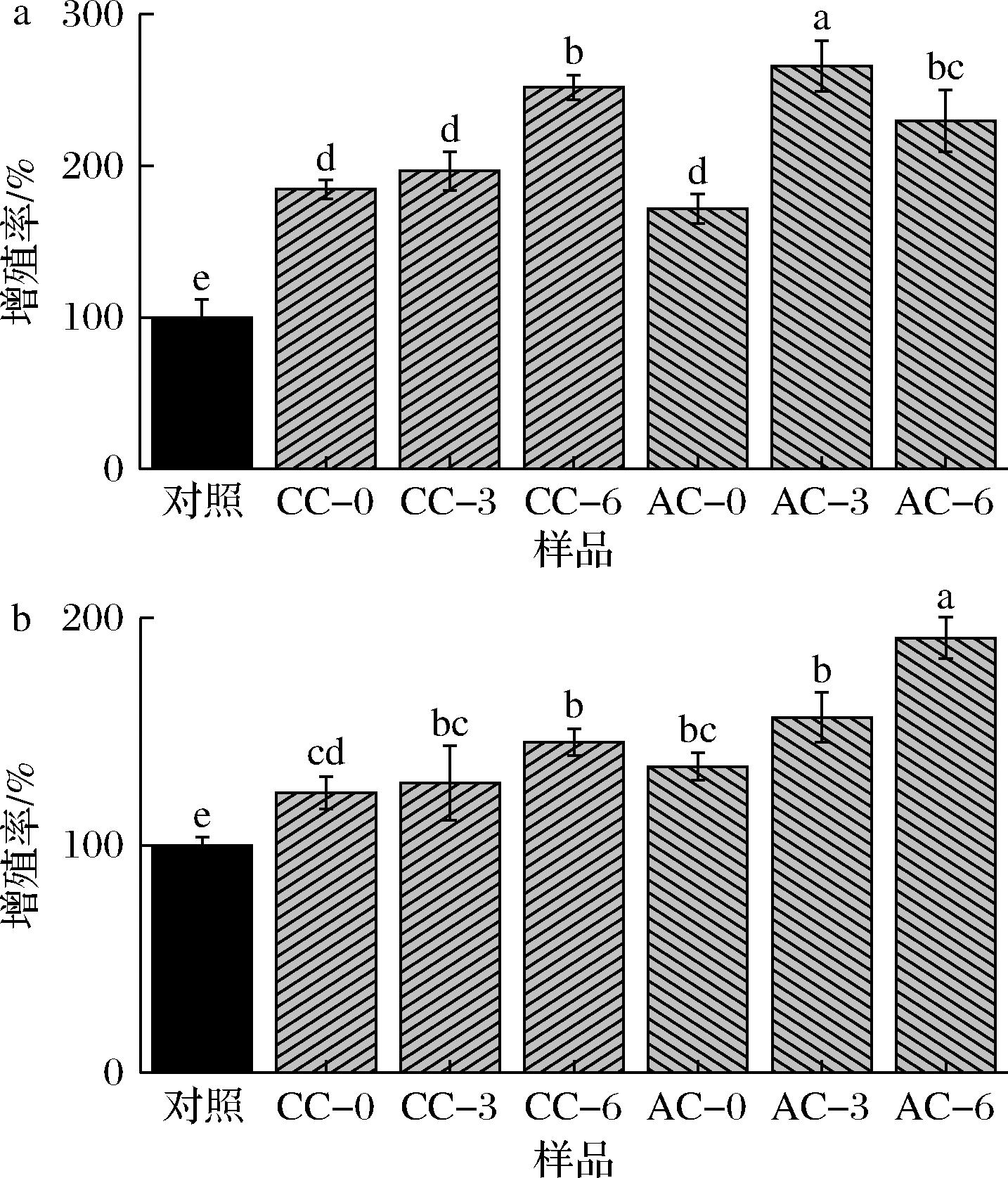
a-MC3T3-E1成骨细胞;b-C2C12成肌细胞
图4 不同成熟时间奶酪样品对成骨细胞MC3T3-E1和成肌细胞C2C12增殖率的影响
Fig.4 Impact of cheese samples with different maturation times on the proliferation rate of pre-osteoblast MC3T3-E1 and myoblast C2C12
注:不同的字母表示一组数据之间存在显著性差异(P<0.05)。
成骨细胞MC3T3-E1在骨形成过程中起着非常重要的作用。如图4-a所示,AC组奶酪成熟3个月的提取物对成骨细胞增殖效果最佳,其增殖率达到了(265.64±16.72)%。同时,未成熟的AC组奶酪提取物对MC3T3-E1细胞的增殖作用和成熟3个月的CC组奶酪提取物相当,但是AC组奶酪成熟6个月后对MC3T3-E1的增殖率较3个月样品有所下降。在对奶酪的生物活性肽定量时,发现其AC组奶酪成熟3个月时的FPP含量和NE-19含量都显著高于CC组,FPP和NE-19通过分子对接筛选,在细胞实验中被验证能够促进成骨细胞形成并抑制破骨细胞生成[15]。其肽含量在成熟3个月时具有显著优势,因此可以推测在添加CCFM1263后与促骨骼健康相关物质产量更高且可能在成熟3个月时达到最高。
切达奶酪提取物对成肌细胞C2C12细胞增殖影响如图4-b所示,效果最好的是成熟时间为6个月的AC奶酪提取物,其增殖率能够达到(191.25±9.04)%,值得一提的是,未成熟的AC组奶酪提取物对C2C12细胞的增殖作用和成熟3个月的CC组奶酪提取物相当,同时成熟3个月的AC组奶酪提取物对C2C12细胞增殖作用和成熟6个月的CC组奶酪相当。说明CCFM1263加入帮助切达奶酪产出更多利于肌肉健康的物质。其中RF-9在细胞实验中能够调节肌肉细胞中蛋白质合成和细胞周期相关基因表达,从而显著增强C2C12细胞的增殖并加速细胞周期[16]。在对奶酪肽浓度定量时,AC组成熟6个月时肌肉生成调节肽RF-9的含量最高,且AC组奶酪成熟3个月时RF-9含量显著高于CC组,因此可以推断出,CCFM1263可促进促肌肉健康物质的合成与积累。综上,切达奶酪提取物对骨骼和肌肉健康的促进作用和CCFM1263和成熟时间有关,具体机制仍需进一步研究。
3 结论
本研究旨在探究CCFM1263作为奶酪附属发酵剂能否缩短切达奶酪的成熟时间,提高生物活性肽含量与奶酪功能性。结果表明添加CCFM1263作为附属发酵剂可显著缩短切达奶酪成熟时间,同时促进生物活性肽的高效积累。2组切达奶酪对骨骼细胞与肌肉细胞的增殖都有作用,但是,添加了CCFM1263的切达奶酪对成骨细胞和成肌细胞的增殖效果更为显著,且可在更短的成熟时间内发挥促进骨骼细胞与肌肉细胞的增殖作用。接下来,尚需进一步评价CCFM1263对奶酪风味、感官等方面的影响,并探讨其促进骨骼肌肉功能的机制。
[1] TUNICK M H, VAN HEKKEN D L.Dairy products and health:Recent insights[J].Journal of Agricultural and Food Chemistry, 2015, 63(43):9381-9388.
[2] HANACH N I, MCCULLOUGH F, AVERY A.The impact of dairy protein intake on muscle mass, muscle strength, and physical performance in middle-aged to older adults with or without existing sarcopenia:A systematic review and meta-analysis[J].Advances in Nutrition, 2019, 10(1):59-69.
[3] DU Y, OH C, NO J.Advantage of dairy for improving aging muscle[J].Journal of Obesity &Metabolic Syndrome, 2019, 28(3):167-174.
[4] MASTER P B Z, MACEDO R C O.Effects of dietary supplementation in sport and exercise:A review of evidence on milk proteins and amino acids[J].Critical Reviews in Food Science and Nutrition, 2021, 61(7):1225-1239.
[5] MORA-GUTIERREZ A, FARRELL H M, ATTAIE R, et al.Effects of bovine and caprine Monterey Jack cheeses fortified with milk calcium on bone mineralization in rats[J].International Dairy Journal, 2007, 17(3):255-267.
[6] DE LUCA P, BRUSCHI S, MAGGIONI M, et al.Gastrointestinal digestates of Grana Padano and Trentingrana cheeses promote intestinal calcium uptake and extracellular bone matrix formation in vitro[J].Food Research International, 2016, 89:820-827.
[7] DE HART N M M P, MAHMASSANI Z S, REIDY P T, et al.Acute effects of cheddar cheese consumption on circulating amino acids and human skeletal muscle[J].Nutrients, 2021, 13(2):614.
[8] AZARNIA S, ROBERT N, LEE B.Biotechnological methods to accelerate cheddar cheese ripening[J].Critical Reviews in Biotechnology, 2006, 26(3):121-143.
[9] LAMICHHANE P, SHARMA P, KENNEDY D, et al.Microstructure and fracture properties of semi-hard cheese:Differentiating the effects of primary proteolysis and calcium solubilization[J].Food Research International, 2019, 125:108525.
[10] LI-CHAN E C.Bioactive peptides and protein hydrolysates:Research trends and challenges for application as nutraceuticals and functional food ingredients[J].Current Opinion in Food Science, 2015, 1:28-37.
[11] BÜTIKOFER U, MEYER J, SIEBER R, et al.Occurrence of the angiotensin-converting enzyme-inhibiting tripeptides val-pro-pro and ile-pro-pro in different cheese varieties of Swiss origin[J].Journal of Dairy Science, 2008, 91(1):29-38.
[12] CHAKRABARTI S, LIAO W, DAVIDGE S T, et al.Milk-derived tripeptides IPP (Ile-Pro-Pro) and VPP (Val-Pro-Pro) differentially modulate angiotensin Ⅱ effects on vascular smooth muscle cells[J].Journal of Functional Foods, 2017, 30:151-158.
[13] HUTTUNEN M M, PEKKINEN M, AHLSTRÖM M E B, et al.Effects of bioactive peptides isoleucine-proline-proline (IPP), valine-proline-proline (VPP) and leucine-lysine-proline (LKP) on gene expression of osteoblasts differentiated from human mesenchymal stem cells[J].British Journal of Nutrition, 2007, 98(4):780-788.
[14] OHSAWA K, NAKAMURA F, UCHIDA N, et al.Lactobacillus helveticus- fermented milk containing lactononadecapeptide (NIPPLTQTPVVVPPFLQPE) improves cognitive function in healthy middle-aged adults:A randomised, double-blind, placebo-controlled trial[J].International Journal of Food Sciences and Nutrition, 2018, 69(3):369-376.
[15] XIA A N, JIANG Y, LEE Y K, et al.Identification and validation of fermented milk-derived osteogenic peptides via molecular docking and osteoblastic cell model[J].Food Bioscience, 2024, 58:103698.
[16] LU Y H, XIA A N, ZHAO J X, et al.Identification and characterization of myogenic regulatory peptides from fermented milk[J].International Dairy Journal, 2025, 166:106248.
[17] HANNON J A, KILCAWLEY K N, WILKINSON M G, et al.Flavour precursor development in Cheddar cheese due to lactococcal starters and the presence and lysis of Lactobacillus helveticus[J].International Dairy Journal, 2007, 17(4):316-327.
[18] QI Y R, JIANG Y, ZHANG X Y, et al.Diversity in genetic and peptidase activity of Lactobacillus helveticus strains biodiversity of Lactobacillus helveticus[J].Food Bioscience, 2021, 40:100915.
[19] 高舒曼. 瑞士乳杆菌发酵乳乳清认知调节功能评价及功能肽解析[D].无锡:江南大学, 2023.
GAO S M.Cognitive regulation function evaluation and bioactive peptide analysis of Lactobacillus helveticus fermented milk whey.[D].Wuxi:Jiangnan University, 2023.
[20] HU W, PEI Z W, XIA A N, et al.Lactobacillus helveticus-derived whey-calcium chelate promotes calcium absorption and bone health of rats fed a low-calcium diet[J].Nutrients, 2024, 16(8):1127.
[21] 江丽红. 切达奶酪附属发酵剂的筛选及其在促熟中的应用[D].无锡:江南大学, 2014.
JIANG L H.Research on the screening of adjunct culture of Cheddar cheese and application in accelerating of aging.[D].Wuxi:Jiangnan University, 2014.
[22] FRANCIOSI E, SETTANNI L, CARLIN S, et al.A factory-scale application of secondary adjunct cultures selected from lactic acid bacteria during puzzone di moena cheese ripening[J].Journal of Dairy Science, 2008, 91(8):2981-2991.
[23] 殷俊玲. 基于双乙酰的切达奶酪奶香味的改善研究[D].无锡:江南大学, 2016.
YIN J L.Study on enhancement of buttery flavor of Cheddar cheese based on diacetyl.[D] Wuxi:Jiangnan University, 2016.
[24] MANE A, MCSWEENEY P L H.Proteolysis in Irish farmhouse Camembert cheese during ripening[J].Journal of Food Biochemistry, 2020, 44(1):e13101.
[25] 张心怡. 瑞士乳杆菌及其胞壁蛋白酶的乳蛋白水解特性研究[D].无锡:江南大学, 2021.
ZHANG, X Y.Hydrolytic properties of milk proteins by Lactobacillus helveticus and its cell envelope proteinases[D].Wuxi:Jiangnan University, 2021.
[26] 张心怡, 姜杨, 刘小鸣, 等.基于肽组学的瑞士乳杆菌酪蛋白水解差异分析[J].中国食品学报, 2022, 22(6):53-61.
ZHANG, X Y, JIANG, Y, LIU, X M, et al.Comparative analysis of casein hydrolysis in Lactobacillus helveticus based on peptidomics[J].Journal of Chinese Institute of Food Science and Technology, 2022, 22(6):53-61.
[27] ONG L, SHAH N P.Influence of probiotic Lactobacillus acidophilus and L.helveticus on proteolysis, organic acid profiles, and ACE-inhibitory activity of cheddar cheeses ripened at 4, 8, and 12 degrees C[J].Journal of Food Science, 2008, 73(3):M111-M120.
[28] GAO S M, JIANG Y, ZHANG X Y, et al.Comparative peptidomics analysis of milk fermented by Lactobacillus helveticus[J].Foods, 2022, 11(23):3885.