马铃薯(Solanum tuberosum L.)是茄科茄属一年生草本双子叶植物,是继水稻、小麦和玉米之后的第四大粮食作物。据联合国粮食与农业组织(Food and Agriculture Organization of the United Nations,FAO)统计,2022年中国马铃薯年产量为9 563万t,居世界首位。马铃薯富含淀粉、蛋白质、膳食纤维、多酚、维生素、矿物质等营养物质和功能成分,具有潜在的抗氧化、抗炎、抗肥胖、抗糖尿病等生理活性[1-2]。在中国,马铃薯除鲜食外,主要用于加工淀粉及其制品(如粉条等)、全粉、薯片等,存在产品形式单一、营养价值较低、副产物资源浪费严重等问题。此外,鲜食马铃薯在收获、运输、贮存中由于机械碰撞、萌芽、失水等原因,腐烂率较高,每年可达15%~25%[1]。因此,开发有效的马铃薯加工方式对马铃薯产业的可持续发展具有重要意义。
乳酸菌被认为是可以在食品工业中安全使用的革兰氏阳性菌,具有维持肠道菌群平衡、降低肠道炎症反应、减少氧化应激和保持肠道黏膜屏障完整性等潜在的益生活性[3]。乳酸菌发酵作为一种传统且有价值的食品加工技术手段,在谷物、水果和蔬菜等植物性原料中得到广泛应用,可以提高植物性原料的营养与功能成分,增强抗氧化活性,改善食品感官品质,延长保质期等[3]。目前,也有一些学者对乳酸菌发酵马铃薯制备马铃薯酵素、马铃薯发酵饮料等进行了探讨。例如,石雪等[4]采用植物乳植杆菌和酵母菌复合发酵黄玫瑰、红玫瑰和紫玫瑰生产3种彩色马铃薯酵素,结果显示紫玫瑰马铃薯酵素的抗氧化活性及感官评价最高。刘新雨等[5]采用乳酸菌、酵母菌复合发酵马铃薯制备格瓦斯饮料,最佳工艺参数为菌种质量比(乳酸菌∶酵母菌)=2∶1、接种量为马铃薯浆液质量的2.5%、发酵时间19 h、发酵温度28 ℃,所得饮料的酸度和乙醇体积分数分别为0.45%(以乙酸计)和0.48%。前期研究表明,与单一菌种相比,鼠李糖乳酪杆菌与戊糖片球菌复合发酵可以显著提高甘薯渣中可溶性膳食纤维、短链脂肪酸、多酚含量及抗氧化活性[3]。ZHU等[6]探究了中试规模下不同发酵时间对马铃薯发酵饮料及高纤粉营养功能成分、抗氧化活性及感官特性的影响规律,结果显示,当发酵时间为48 h时,马铃薯发酵饮料具有最高的有机酸、总多酚含量和抗氧化活性,马铃薯高纤粉具有最高的可溶性膳食纤维、总氨基酸、半乳糖醛酸和挥发性酸含量。然而,缺乏乳酸菌发酵前后马铃薯饮料和高纤粉代谢物及其代谢通路的分析。采用非靶向代谢组学技术能够更全面、深入地了解马铃薯发酵饮料和高纤粉中代谢物的变化情况,从而为后续深度开发马铃薯发酵产品提供一定的参考。
因此,本研究以马铃薯为原料,采用鼠李糖乳酪杆菌和戊糖片球菌复合发酵制备马铃薯发酵饮料和高纤粉,探究马铃薯发酵饮料和高纤粉的主要差异代谢物,并分析其富集代谢通路,以期为基于乳酸菌发酵技术开发马铃薯饮料和高纤粉产品提供理论依据和数据支持。
1 材料与方法
1.1 材料与试剂
马铃薯(青薯9号),新疆农业科学院综合试验站;鼠李糖乳酪杆菌CICC 23119和戊糖片球菌CICC 21862,中国工业微生物菌种保藏中心;甲醇、乙腈、乙酸铵和氢氧化铵,Sigma-Aldrich试剂公司;α-淀粉酶(酶活性≥3 000 U/mL)、中性蛋白酶(酶活性≥3 000 U/mg)和其他化学试剂均为分析纯,索莱宝生物科技有限公司。
1.2 仪器与设备
PHS-25 pH计,上海精密科学仪器公司;SHA-300恒温水浴摇床,江苏太仓培英实验设备有限公司;LDZM-40KCS立式压力蒸汽灭菌锅,上海申安医疗器械厂;HZCO2-1311K立式恒温摇床,太仓市华利达实验设备有限公司;GL-21M低温冷冻离心机,北京天林恒泰科技有限公司;D-3L高压均质机,美国PhD科技有限公司;1290 Infinity LC超高效液相色谱,安捷伦公司;Triple TOF 6600质谱仪,美迪希实验仪器公司。
1.3 实验方法
1.3.1 马铃薯发酵饮料和高纤粉的制备
将新鲜马铃薯清洗、去皮、切片、蒸煮、捣泥后,与蒸馏水以料液比1∶2(g∶mL)混匀。按马铃薯泥质量的0.1%加入耐高温α-淀粉酶,95 ℃水解30 min,冷却至60 ℃后,用6 mol/L的NaOH将pH值调至7.0±0.2。然后按马铃薯泥质量的0.05%加入中性蛋白酶,60 ℃水解30 min,后121 ℃灭菌15 min,冷却至37 ℃,按马铃薯泥质量的0.05%加入复合菌(鼠李糖乳酪杆菌∶戊糖片球菌=1∶1,质量比),37 ℃发酵48 h,7 000×g离心10 min,上清液60 MPa高压均质2次得马铃薯发酵饮料,沉淀在50 ℃烘箱中干燥48 h得马铃薯高纤粉,以经过酶解、灭菌、发酵0 h的马铃薯上清液和干燥后的马铃薯粉作为对照。
1.3.2 马铃薯发酵饮料和高纤粉的代谢物提取
参照GU等[7]的方法并做一定修改。马铃薯发酵饮料和高纤粉在-20 ℃、100 W的低温超声波下用V(甲醇)∶V(乙腈)∶V(H2O)=2∶2∶1提取30 min后,-20 ℃孵育10 min,4 ℃、14 000×g离心20 min。所得上清液冷冻干燥后用100 μL乙腈水溶液(乙腈∶水=1∶1,体积比)复溶,4 ℃、14 000×g离心20 min,所得上清液用于非靶向代谢组学分析。
1.3.3 非靶向代谢组学分析
采用配备ACQUIY BEH 1.7 μm×2.1 mm×100.0 mm液相色谱柱的超高效液相色谱-四极杆飞行时间质谱(ultra-performance liquid chromatography-quadrupole-time-of-flight-mass spectrometry, UPLC-Q-TOF-MS)对马铃薯发酵饮料和高纤粉中代谢物进行分析。柱温25 ℃,流动相为25.0 mmol/L乙酸铵/氢氧化铵水溶液(A)和乙腈溶液(B),进样量2 μL,流速0.4 mL/min。线性梯度洗脱程序:0~1.5 min,98% B;1.5~12 min,B从98%下降到2%;12~14 min,2% B;14~14.1 min,从2%增加到98%;14.1~17 min,98% B。在自动MS/MS采集中,一级质荷比检测范围:60~1 000 Da,二级子离子质荷比检测范围:25~1 000 Da,一级质谱扫描累积时间:0.20 s/spectra,二级质谱扫描累积时间0.05 s/spectra。数据依赖型采集模式用于获得质谱,并采用峰强度值筛选模式采集产物离子扫描,参数设置为碰撞能量35 V±15 eV,去簇电位±60 V,动态排除同位素离子为4 Da。
1.4 数据分析
原始数据经ProteoWizard转换成.mzXML格式,采用XCMS软件进行峰对齐、保留时间校正和提取峰面积。对XCMS提取得到的数据进行代谢物结构鉴定、数据预处理、实验数据质量评价及数据分析。使用MetaboAnalyst 5.0软件对代谢物的结果进行处理、分析和可视化(http://www.metaboanalyst.ca)。通过KEGG(Kyoto Encyclopedia of Genes and Genomes,www.genome.jp/kegg)数据库阐明与代谢物相关的代谢途径。所有实验重复6次。
2 结果与分析
2.1 马铃薯乳酸菌发酵饮料及高纤粉代谢物鉴定
非靶向代谢组学可以通过匹配数据库中代谢物的基本信息(如分子质量、保留时间、质谱碎片等),对样品中的代谢物进行分析鉴定[8]。基于二级质谱,通过搜索代谢组学数据库对马铃薯乳酸菌发酵饮料和高纤粉中的代谢物分类及数量进行分析,结果见表1。
表1 马铃薯乳酸菌发酵饮料及高纤粉中的代谢物分类
Table 1 Classification of metabolites in potato juice and high-fiber powder fermented by lactic acid bacteria
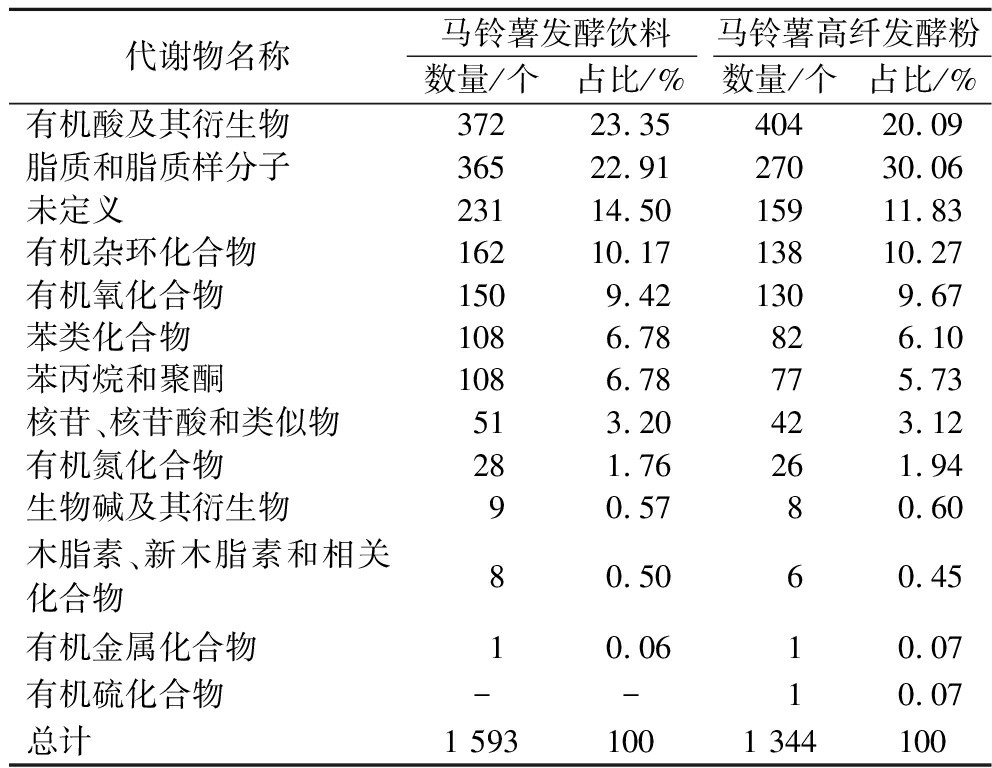
代谢物名称马铃薯发酵饮料马铃薯高纤发酵粉数量/个占比/%数量/个占比/%有机酸及其衍生物37223.3540420.09脂质和脂质样分子36522.9127030.06未定义23114.5015911.83有机杂环化合物16210.1713810.27有机氧化合物1509.421309.67苯类化合物1086.78826.10苯丙烷和聚酮1086.78775.73核苷、核苷酸和类似物513.20423.12有机氮化合物281.76261.94生物碱及其衍生物90.5780.60木脂素、新木脂素和相关化合物80.5060.45有机金属化合物10.0610.07有机硫化合物--10.07总计1 5931001 344100
马铃薯乳酸菌发酵饮料中共鉴定出1 593种代谢物,其中有机酸及其衍生物、脂质和脂质样分子及有机杂环化合物占比较高,分别为23.35%、22.91%和10.17%。马铃薯高纤粉中也有类似的结果,其中有机酸及其衍生物代谢物数目为404个,脂质和脂质样分子代谢物有270个,有机杂环化合物代谢物有138个,为占比最高的前3类。结果表明,经乳酸菌发酵后,马铃薯发酵饮料和高纤粉中的差异代谢物主要集中在有机酸、脂质及有机杂环化合物等方面,其中有机酸及其衍生物在发酵饮料中的含量及种类变化差异最大,而脂质和脂质样分子代谢物在高纤粉中的含量及种类变化差异最大,这些化合物对马铃薯发酵饮料和高纤粉的品质影响至关重要[9]。XU等[10]也发现了相似的结果,西兰花汁经戊糖片球菌发酵后,脂质和脂质样分子、有机酸及其衍生物的代谢物占比最高。
2.2 基于OPLS-DA的差异代谢物分析
正交偏最小二乘法判别分析(orthogonal partial least squares discrimination analysis,OPLS-DA)可以更好地去除与分类信息无关的噪声,提高模型的有效性,最大化模型内各组之间的差异,横坐标方向表示组间的差异,纵坐标方向表示组内的差异,纵向距离越近,表明组内重复性越好[11]。图1-a和图1-b分别表示在乳酸菌发酵过程中马铃薯发酵饮料和高纤粉的OPLS-DA模型得分图,结果显示,发酵饮料和高纤粉的横坐标距离较大,表明未发酵马铃薯与经乳酸菌发酵48 h后制备的样品相比有显著差异。图1-c和图1-d分别为马铃薯发酵饮料和高纤粉的OPLS-DA模型置换验证图,R2X、R2Y和Q2是OPLS-DA模型的预测参数,其中R2Y和Q2值越大,模型越成功,Q2越接近1,模型越稳定可靠[12]。马铃薯发酵饮料和高纤粉的R2Y均为1,Q2分别为0.996和0.993,表明该模型拟合度好,具有预测性和稳定性,可用于后续代谢物差异分析。
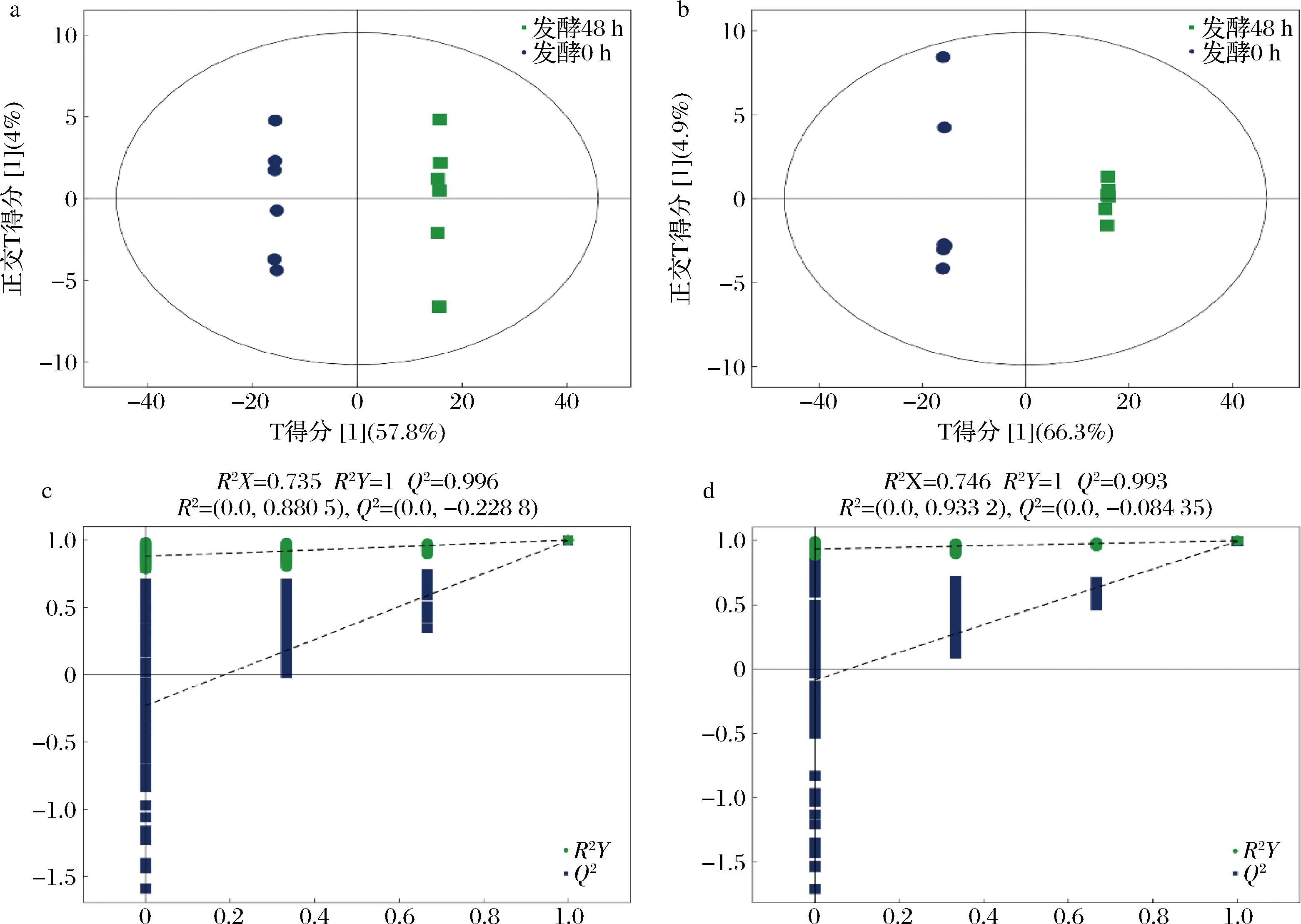
a、c-马铃薯乳酸菌发酵饮料的模型得分和置换验证图;b、d-马铃薯乳酸菌发酵高纤粉的模型得分和置换验证图
图1 乳酸菌发酵饮料及高纤发酵粉的OPLS-DA模型得分和置换验证图
Fig.1 OPLS-DA model scores and replacement verification diagram for potato juice and high-fiber powder fermented by lactic acid bacteria
2.3 马铃薯发酵饮料和高纤粉差异代谢物火山图分析
单变量结合多维统计分析是代谢组学中广泛应用的一种筛选差异代谢物的方法,差异火山图以一种直观的方式来展示代谢物的变化差异,以便于后续分析中继续挖掘和筛选出关键的差异代谢物[8]。对马铃薯发酵饮料和高纤粉样品中基于单变量统计分析方法检测到的所有代谢产物进行差异性分析,差异改变倍数(fold change,FC)取log2,火山图按照|log2 FC|>1、P<0.05的标准筛选差异代谢物,结果如图2-a和图2-b所示,红色代表代谢物被上调,蓝色代表代谢物被下调,|log2 FC|<1及P≥0.05的部分代表无显著性变化。马铃薯发酵饮料中显著上调的代谢物有382种,显著下调的代谢物有125种,无显著变化的代谢物有577种;马铃薯高纤粉中显著上调的代谢物有236种,显著下调的代谢物有160种,无显著变化的代谢物有395种。
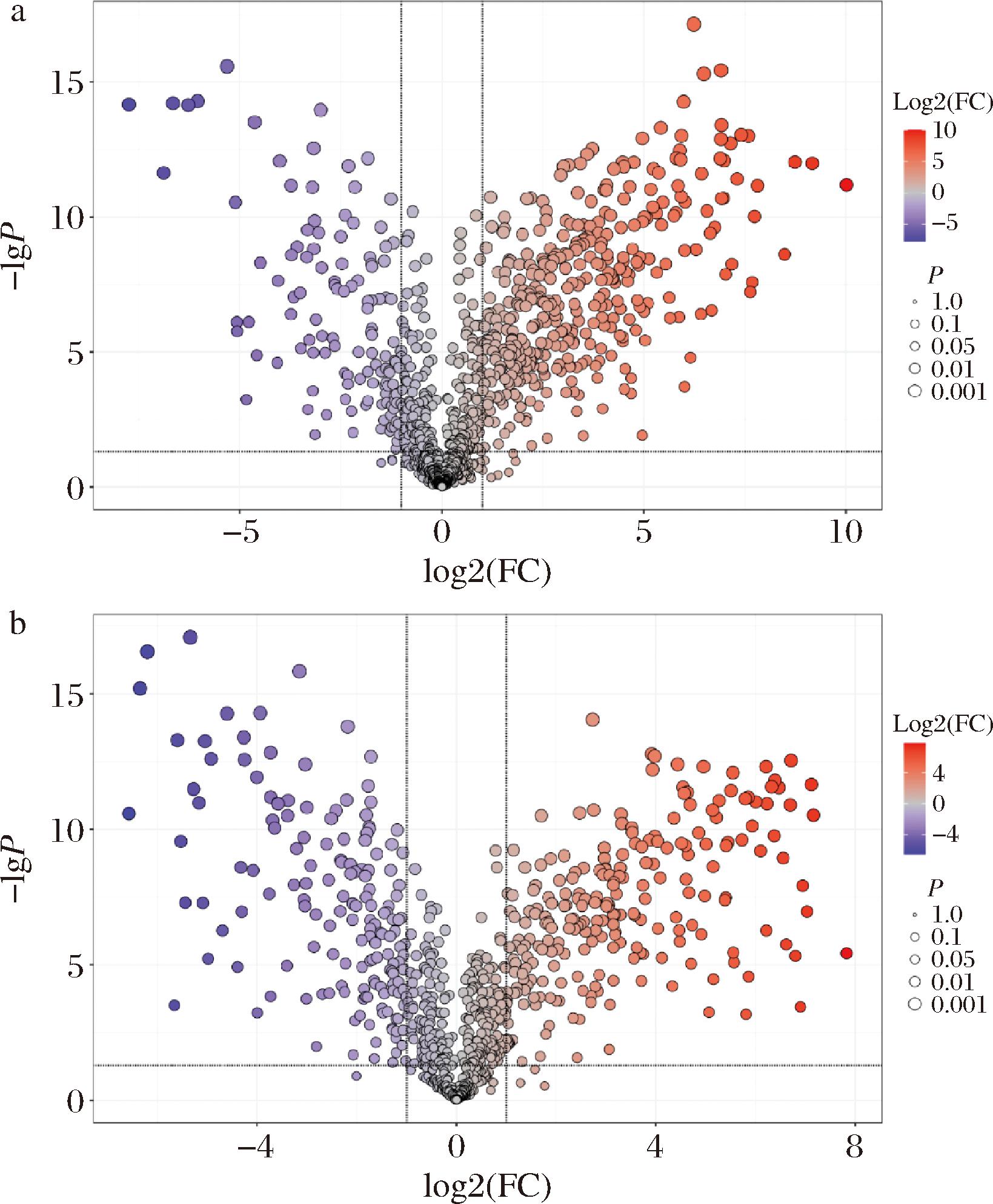
a-马铃薯发酵饮料;b-马铃薯发酵高纤粉
图2 马铃薯发酵饮料和高纤粉的差异代谢物火山图
Fig.2 Volcano diagram of differential metabolite of potato juice and high-fiber powder fermented by lactic acid bacteria
2.4 马铃薯发酵饮料和高纤粉关键差异代谢物及其通路分析
为了进一步了解发酵过程中马铃薯发酵饮料和高纤粉关键差异代谢产物的变化规律,根据P<0.05和变量投影重要度(variable importance in projection,VIP)≥1进一步筛选关键差异代谢物,结果见图3-a~图3-d。马铃薯发酵饮料中筛选出18种关键差异代谢物,其中乙酰胆碱、甘油磷酸、胡芦巴碱、乳糖等被上调,而腺嘌呤、烟酰胺、异亮氨酸-精氨酸、腺苷、L-肌肽等被下调。马铃薯高纤粉中筛选出19种关键差异代谢物,其中,乳糖、松三糖、腺苷、麦芽糖等被下调,而乙酰胆碱、甘油磷酸、硫醚酰胺-磷脂酰胆碱、1,2-二油酸基-sn-甘油-3-磷脂酰胆碱、二棕榈酰磷脂酰胆碱/PC(16∶0/16∶0)、L-精氨酸等被上调。
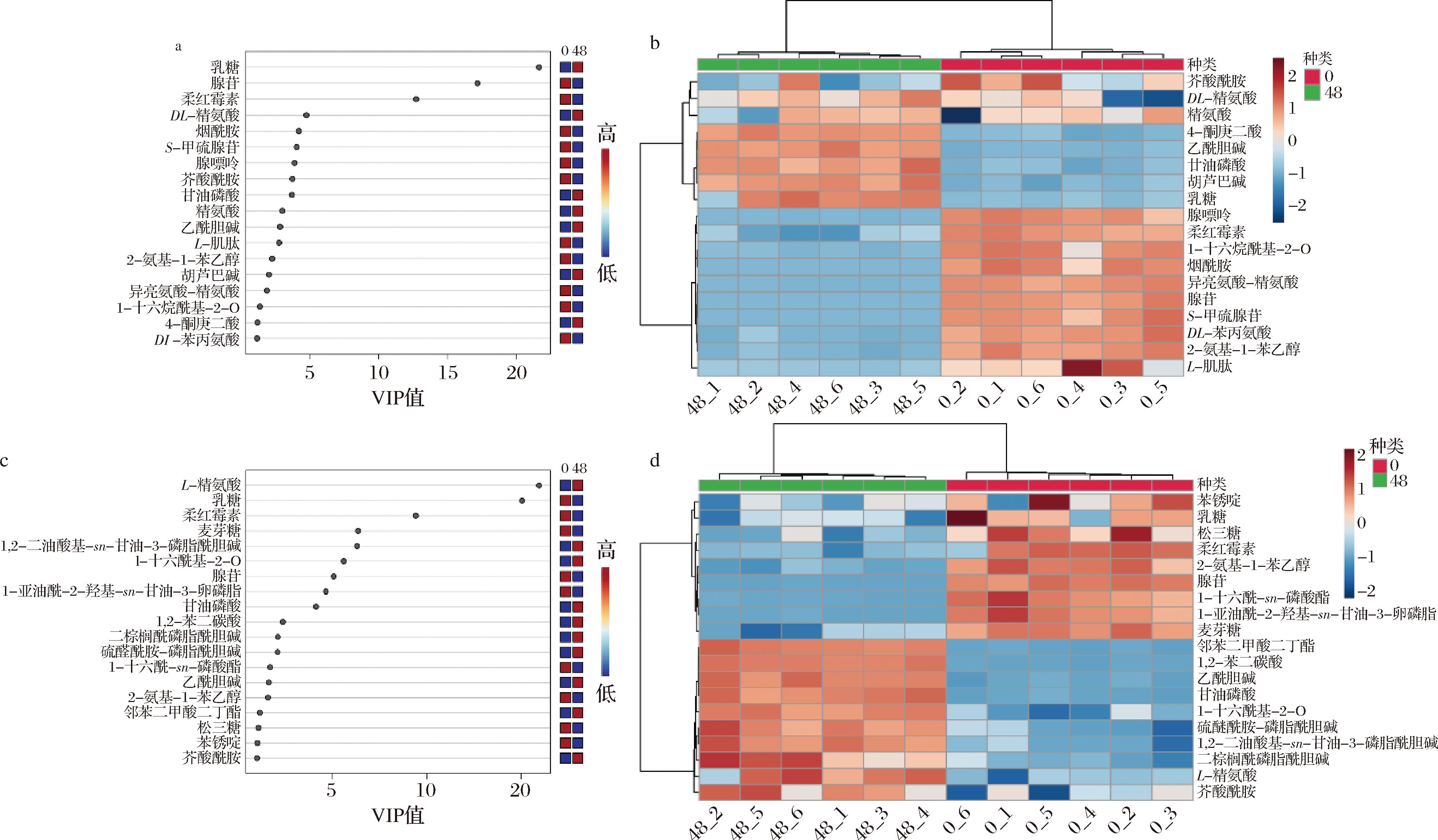
a-马铃薯发酵饮料关键差异代谢物VIP值;b-马铃薯发酵饮料关键差异代谢物丰度热图;c-马铃薯发酵高纤粉关键差异代谢物VIP值;d-马铃薯发酵高纤粉关键差异代谢物丰度热图
图3 马铃薯发酵饮料和高纤粉关键差异代谢物VIP值及丰度热图
Fig.3 VIP values and abundance heatmap of key differential metabolites in potato juice and high-fiber powder fermented by lactic acid bacteria
进一步采用代谢通路富集分析来揭示乳酸菌发酵对马铃薯发酵饮料和高纤粉中相关代谢通路的影响。图4-a和图4-b显示了马铃薯发酵饮料中关键差异代谢物的KEGG通路富集分析,包括甘油磷脂代谢、嘌呤代谢、精氨酸生物合成、烟酸和烟酰胺代谢、组氨酸代谢、醚脂代谢、β-丙氨酸代谢、半乳糖代谢、半胱氨酸和蛋氨酸代谢、精氨酸和脯氨酸代谢10种途径。其中,富集比排名前3的有精氨酸生物合成、烟酸/烟酰胺代谢、甘油磷脂代谢,分别为12.22、11.42和8.71。图4-c和图4-d显示了马铃薯高纤粉中关键差异代谢物的KEGG通路富集分析,包括甘油磷脂代谢、精氨酸生物合成、淀粉/蔗糖代谢、醚脂代谢、半乳糖代谢、精氨酸和脯氨酸代谢、嘌呤代谢7种途径。其中,精氨酸生物合成、淀粉/蔗糖代谢途径、甘油磷脂代谢富集比最高,分别为17.67、13.59和13.59。
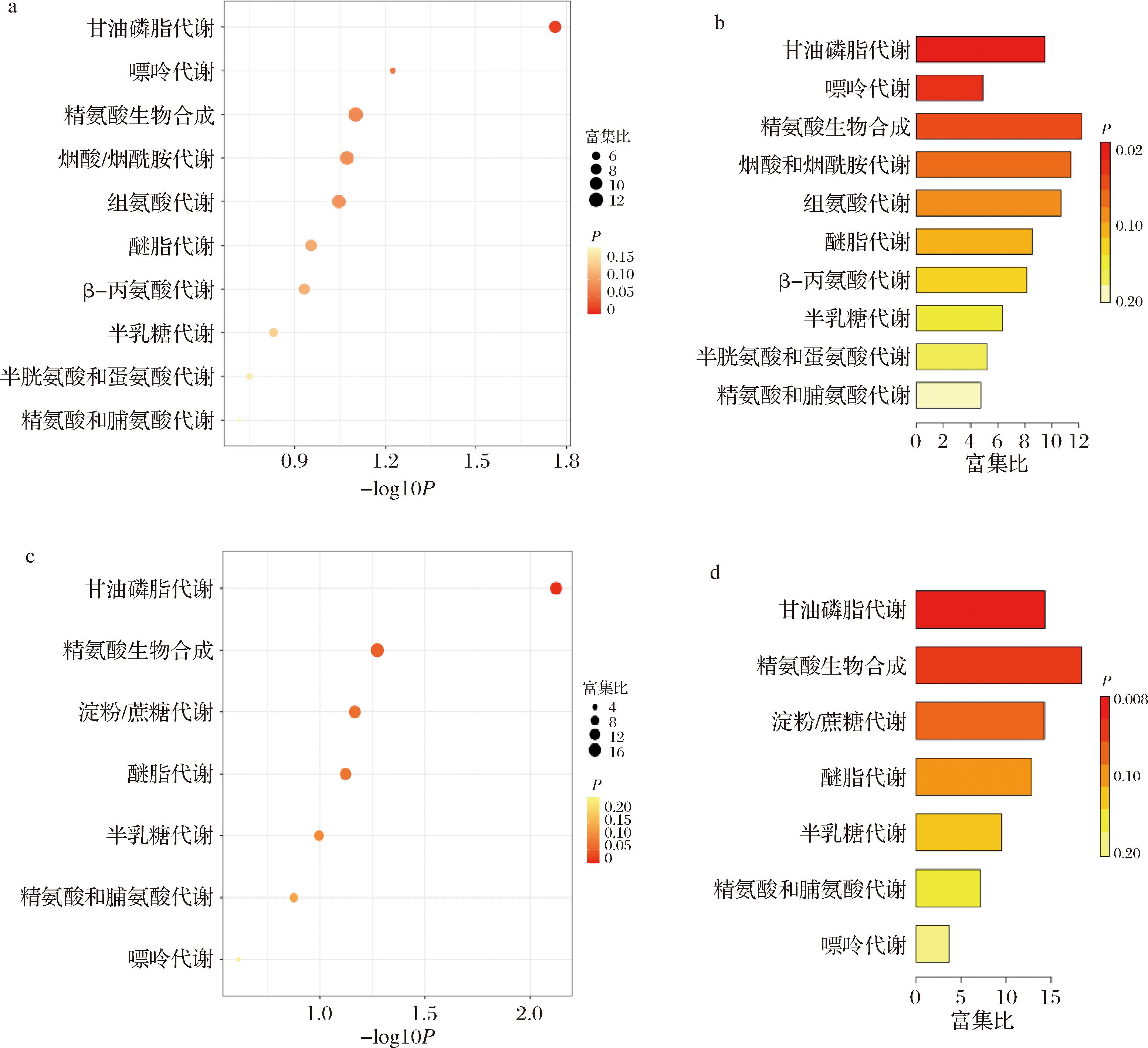
a、b-马铃薯发酵饮料;c、d-马铃薯发酵高纤粉
图4 马铃薯发酵饮料和高纤粉前25位代谢物KEGG通路富集途径图
Fig.4 KEGG pathway enrichment map of the top 25 metabolites in potato juice and high-fiber powder fermented by lactic acid bacteria
注:圆圈大小表示通路富集代谢物数目多少。
甘油磷脂代谢途径在马铃薯发酵饮料和高纤粉中的富集比均最高,其中参与的关键差异代谢物包括在马铃薯发酵饮料和高纤粉中均显著上调的乙酰胆碱和甘油磷酸,以及在马铃薯高纤粉中显著上调的硫醚酰胺-磷脂酰胆碱、1,2-二油酸基-sn-甘油-3-磷胆碱和二棕榈酰磷脂酰胆碱/PC(16∶0/16∶0),这是由于乳酸菌发酵影响了甘油磷脂代谢[13]。三月等[13]也报道了类似的结果,麦麸经鼠李糖乳酪杆菌和植物乳植杆菌发酵后,分别鉴定出84和66种差异脂质代谢物,其中甘油磷脂代谢途径具有代谢物富集现象。1,2-二油酸基-sn-甘油-3-磷胆碱是细胞膜的主要成分之一,也是一种神经递质,可以通过激活p38信号通路诱导白色脂肪组织棕色化,进而抵抗高脂膳食诱导的肥胖[14]。PC(16∶0/16∶0)是一种磷脂酸胆碱,是细胞膜和细胞器膜的基本结构,也参与细胞中信号转导,是脂蛋白组装和分泌的必需物质,在调节细胞脂质代谢和脂质稳态中发挥重要作用[15]。胡亚欣[16]报道PC(16∶0/16∶0)可以提高认知功能障碍小鼠脑组织中谷光甘肽的含量,还可以通过减轻氧化应激和脂质过氧化,改善小鼠卒中后的认知功能,此外,硫醚酰胺-磷脂酰胆碱和PC(16∶0/16∶0)可能是沟通肠-脑的物质桥梁,且PC(16∶0,16∶0)与硫醚酰胺-磷脂酰胆碱的比例与认知功能呈正相关。马铃薯发酵饮料和高纤粉中精氨酸均被上调,其参与的代谢途径为精氨酸生物合成,精氨酸在生物体内不仅与蛋白质合成相关,还是多种生物活性物质(如多胺和NO等)的合成前体[17]。马铃薯发酵饮料中被下调的L-肌肽参与了组氨酸代谢和β-丙氨酸代谢途径,其与氨基酸的生物合成与转化相关[18]。嘌呤代谢是核苷酸代谢的最后阶段,被认为是核酸合成和代谢途径的基础,腺嘌呤和腺苷可以参与多种生理调节,如为代谢提供能量、为蛋白质合成提供“指导”、维生素合成的中间体等[19]。经乳酸菌发酵后,马铃薯发酵饮料和高纤粉中腺嘌呤和腺苷等关键嘌呤代谢物被显著下调,腺嘌呤和腺苷的下调可能是由于乳酸菌消耗嘌呤代谢物以促进自身的生长和代谢[20]。WANG等[21]也报道了相似的结果,研究显示乳酸菌发酵仙人掌果汁后,鸟嘌呤、腺嘌呤和腺苷的丰度降低。马铃薯高纤粉中乳糖、松三糖和麦芽糖被显著下调,说明其参与淀粉和蔗糖代谢途径,乳糖、松三糖和麦芽糖可以被降解转化为单糖,然后进一步转化为丙酮酸和乙酰辅酶A进入三羧酸循环[6]。其中,松三糖是一种非还原性三糖,可以通过下调MHCⅡ(major histocompatibility complex class Ⅱ)蛋白和上调CD4(cluster of differentiation 4)蛋白表达来激活T细胞信号通路,从而抑制溃疡性结肠炎小鼠的炎症反应[22]。马铃薯发酵饮料中的关键差异代谢物烟酰胺和胡芦巴碱参与了烟酸和烟酰胺代谢途径,乳酸菌发酵可以上调马铃薯发酵饮料中的胡芦巴碱,胡芦巴碱具有降低胆固醇和血糖的功能特性[23]。烟酰胺可以参与蛋白质的新陈代谢,乳酸菌发酵下调了马铃薯饮料中的烟酰胺,李曦明等[24]也发现,经植物乳植杆菌发酵后辣木叶中的烟酰胺显著下调,这可能是由于烟酰胺具有不稳定性,在乳酸菌发酵过程中发生了降解。辛易燃[25]也报道了相似的结果,乳酸菌发酵金花葵后烟酸和烟酰胺代谢通路关键差异代谢物的富集数较多。
3 结论
本文以马铃薯为研究对象,探讨了鼠李糖乳酪杆菌和戊糖片球菌复合发酵过程中马铃薯饮料和高纤粉中的代谢物变化。通过UHPLC-Q-TOF MS在马铃薯乳酸菌发酵饮料和高纤粉中分别鉴定出1 593种和1 344种代谢物。根据VIP≥1和P<0.05进一步筛选出马铃薯发酵饮料和高纤粉中分别有18种和19种关键差异代谢物,马铃薯发酵饮料中乙酰胆碱、甘油磷酸、胡芦巴碱、乳糖等被上调,腺嘌呤、烟酰胺、异亮氨酸-精氨酸、腺苷、L-肌肽等被下调;马铃薯发酵高纤粉中乳糖、松三糖、腺苷、麦芽糖等被下调,而乙酰胆碱、甘油磷酸、硫醚酰胺-磷脂酰胆碱、1,2-二油酸基-sn-甘油-3-磷胆碱、二棕榈酰磷脂酰胆碱、L-精氨酸等被上调。KEGG通路富集分析结果显示,甘油磷脂代谢、精氨酸生物合成、烟酸/烟酰胺代谢途径是马铃薯发酵饮料中代谢物富集比最高的代谢通路,而马铃薯发酵高纤粉中代谢物富集比最高的代谢通路有甘油磷脂代谢、精氨酸生物合成、淀粉/蔗糖代谢途径。这些代谢途径与马铃薯氨基酸、磷脂胆碱生物合成、糖类分解代谢以及烟酰胺合成与代谢有关,表明乳酸菌发酵对马铃薯发酵饮料和高纤粉代谢物生物活性的提高有一定促进作用。
[1] 伍玉菡, 尤逢惠, 万娅琼.马铃薯贮藏·加工·主食化研究进展[J].安徽农业科学, 2016, 44(29):71-72.
WU Y H, YOU F H, WAN Y Q.Research advances of potato storage, process and staple food industrialization[J].Journal of Anhui Agricultural Sciences, 2016, 44(29):71-72.
[2] RAIGOND P, JAYANTY S S, PARMAR V, et al.Health-promoting compounds in potatoes:Tuber exhibiting great potential for human health[J].Food Chemistry, 2023, 424:136368.
[3] ZHU L L, SUN H N, MA M M, et al.The sustainability of sweet potato residues from starch processing by-products:Preparation with Lacticaseibacillus rhamnosus and Pediococcus pentosaceus, characterization, and application[J].Foods, 2022, 12(1):128.
[4] 石雪, 李敏, 陈勤, 等.彩色马铃薯品种与发酵方式对其酵素品质及抗氧化特性的影响[J].食品与发酵工业, 2023, 49(9):120-127.
SHI X, LI M, CHEN Q, et al.Effects of colored potato varieties and fermentation methods on ferment quality and antioxidant properties[J].Food and Fermentation Industries, 2023, 49(9):120-127.
[5] 刘新雨, 张岚, 王红梅, 等.乳酸菌、酵母菌复合发酵马铃薯格瓦斯生产工艺及其稳定性优化[J].粮食与油脂, 2023, 36(7):124-129.
LIU X Y, ZHANG L, WANG H M, et al.Optimization of the production process and stability of potato Kvass by compound fermentation of lactic acid bacteria and yeast[J].Cereals &Oils, 2023, 36(7):124-129.
[6] ZHU L L, SUN H N, MA M M, et al.Utilization of Lacticaseibacillus rhamnosus and Pediococcus pentosaceus cofermentation on potato for juice and high-fiber powder production:An innovative approach for pilot scale manufacturing[J].ACS Food Science &Technology, 2024, 4(11):2724-2738.
[7] GU M H, LI C, CHEN L, et al.Insight from untargeted metabolomics:Revealing the potential marker compounds changes in refrigerated pork based on random forests machine learning algorithm[J].Food Chemistry, 2023, 424:136341.
[8] 侯菲翔, 蔡燕雪, 肖珊, 等.乳酸菌发酵西兰花的代谢组学分析及其对萝卜硫素含量的影响[J].食品与发酵工业, 2024, 50(5):88-93.
HOU F X, CAI Y X, XIAO S, et al.Metabolomic analysis of broccoli fermented by lactic acid bacteria and its effect on the content of sulforaphane[J].Food and Fermentation Industries, 2024, 50(5):88-93.
[9] 阎佳慧,王玉婷,刘书亮,等.不同乳酸菌发酵枇杷汁的特性分析[J].食品与发酵工业,2024,50(24):282-288.
YAN J H, WANG Y T, LIU S L, et al.Characterization of loquat juice fermented by different lactic acid bacteria[J].Food and Fermentation Industries, 2024,50(24):282-288.
[10] XU X X, BI S, LAO F, et al.Comprehensive investigation on volatile and non-volatile metabolites in broccoli juices fermented by animal- and plant-derived Pediococcus pentosaceus[J].Food Chemistry, 2021, 341:128118.
[11] 廖茂雯, 韩琛, 刘玮, 等.植物乳杆菌发酵蓝莓汁发酵和贮藏过程中理化指标及挥发性风味物质的变化[J].食品工业科技, 2025, 46(1):259-273.
LIAO M W, HAN C, LIU W, et al.Effects of Lactobacillus plantarum on physicochemical properties and volatile flavor substances of blueberry juice during fermentation and storage[J].Science and Technology of Food Industry, 2025, 46(1):259-273.
[12] LI X Y, YAO Y Q, CHEN M L, et al.Comprehensive evaluation integrating omics strategy and machine learning algorithms for consistency of Calculus bovis from different sources[J].Talanta, 2022, 237:122873.
[13] 三月, 武国栋, 艳茹, 等.不同型乳酸菌发酵麦麸中脂质代谢的差异性分析[J].食品与发酵工业, 2025, 51(14):327-335.
SAN Y, WU G D, YAN R, et al.Difference analysis of lipid metabolism in wheat bran fermented by different types of lactic acid bacteria[J].Food and Fermentation Industries,2025, 51(14):327-335.
[14] HU X D, SUN M W, CHEN Q, et al.Skeletal muscle-secreted DLPC orchestrates systemic energy homeostasis by enhancing adipose browning[J].Nature Communications, 2023, 14:7916.
[15] 姜月华, 陈健乔, 李晓, 等.磷脂酰胆碱的生物学功能及其在心血管疾病中的作用[J].生命的化学, 2022, 42(3):412-423.
JIANG Y H, CHEN J Q, LI X, et al.Biological function of phosphatidylcholine and its role in cardiovascular diseases[J].Chemistry of Life, 2022, 42(3):412-423.
[16] 胡亚欣. 从代谢组学角度探索脑缺血卒中后的肠-脑对话及其对卒中后认知功能的影响[D].贵阳:贵州医科大学, 2021.
HU Y X.Gut-brain crosstalk after ischemic stroke and its effecton post-stroke cognitive function from the perspectiveof metabolomics[D].Guiyang:Guizhou Medical University, 2021.
[17] 叶峥, 张江宁.基于非靶向代谢组学探究不同菌种发酵骏枣汁的代谢差异分析[J].食品与发酵工业, 2025, 51 (11):81-89.
YE Z, ZHANG J N.Non-targeted metabolomics analysis on metabolic differences among Ziziphus jujuba Mill.juices fermented by different strains[J].Food and Fermentation Industries, 2025, 51 (11):81-89.
[18] 王长斌, 刘文涛, 任文杰, 等.L-肌肽的合成方法改进[J].食品与药品, 2015, 17(3):190-192.
WANG C B, LIU W T, REN W J, et al.Improvement of synthetic method of L-carnosine[J].Food and Drug, 2015, 17(3):190-192.
[19] 孙鹏杰.腺嘌呤工程菌的构建及代谢控制发酵研究[D].天津:天津科技大学, 2023.
SUN P J.Construction of adenine engineering bacteria and study on metabolism control fermentation[D].Tianjin:Tianjin University of Science and Technology, 2023.
[20] YUE M Z, FENG Z, ZHOU J P, et al.Improving functionality and metabolite profiles of black sapote juice through lactic acid bacteria fermentation[J].LWT, 2024, 213:117048.
[21] WANG H X, HE X Q, LI J N, et al.Lactic acid bacteria fermentation improves physicochemical properties, bioactivity, and metabolic profiles of Opuntia ficus-indica fruit juice[J].Food Chemistry, 2024, 453:139646.
[22] 陈章浩,高霜,李进发,等.松三糖对溃疡性结肠炎的作用[J].中国临床药理学杂志, 2024, 40(14):2083-2087.
CHEN Z H, GAO S, LI J F, et al.Effects of melezitose on ulcerative colitis mice[J].The Chinese Journal of Clinical Pharmacology, 2024, 40(14):2083-2087.
[23] 姜海斌, 蒋锐, 杨丽洁.葫芦巴碱结合有氧运动对高脂血症大鼠降脂作用及PCSK9/LDLR通路的影响[J].中国临床药理学杂志, 2024, 40(12):1794-1798.
JIANG H B, JIANG R, YANG L J.Effects of trigonelline combined with aerobic exercise on lipid lowering and PCSK9/LDLR pathway in hyperlipidemia rats[J].The Chinese Journal of Clinical Pharmacology, 2024, 40(12):1794-1798.
[24] 李曦明, 温燕龙, 杨雪莹, 等.基于非靶向代谢组学分析辣木叶发酵前后营养物质及代谢物变化[J].食品与发酵工业, 2023, 49(23):105-110.
LI X M, WEN Y L, YANG X Y, et al.Nutrient and metabolite changes before and after fermentation of Moringa oleifera leaves based on non-targeted metabolomics[J].Food and Fermentation Industries, 2023, 49(23):105-110.
[25] 辛易燃. 益生菌发酵金花葵及其工艺优化和功能预测[D].沈阳:沈阳农业大学, 2023.
XIN Y R.Probiotic fermentation of Hibiscus manihot L.flower andits process optimization and functional prediction[D].Shenyang:Shenyang Agricultural University, 2023.