浆果类水果有更丰富的营养成分,富含多酚类物质尤其是花色苷类,有着“花青素之王”的蓝莓,花青素含量高达387~487 mg/100 g,具有强抗氧化作用,可预防多种慢性疾病[1]。但浆果由于其高水分和高糖分的特点,易腐败变质,深加工和发酵成为保留并提高其营养品质的有效途径[2]。同时从市场需求的角度来看,浆果发酵酒在市场上较为常见,如发酵沙棘葡萄酒、发酵蓝莓酒,而低酒精或者无酒精的发酵浆果汁相对较少。随着消费者对健康饮品的需求不断增加,低酒精或无酒精的发酵浆果汁具有广阔的市场前景。
蓝莓被誉为“浆果之王”,营养价值极高,富含维生素、矿物质和抗氧化物质[1]。蓝莓汁本身具有一定的酸涩感,这可能会影响其口感和消费者的接受度。然而在发酵过程中,益生菌能够分解蓝莓中的复杂成分,使其口感更加醇厚、柔和,还能提高蓝莓汁的营养品质,使其中的营养成分更易于被人体吸收,进一步提升了蓝莓汁的营养价值[3]。益生菌除了改善果汁本身的营养和风味外,其本身也有诸多益处,它们可以有效改善肠道菌群平衡,从而降低肠道疾病的发生风险,增强肠道屏障功能,刺激肠道上皮细胞产生黏液形成保护膜,阻止有害菌和毒素与肠道上皮接触,还能促进肠道上皮细胞分泌抗菌肽,抑制有害菌黏附和入侵,降低炎症反应,减少炎症因子产生,预防和改善炎症性疾病[4],同时蓝莓中的多酚类物质还可作为益生元选择性促进乳杆菌等有益菌增殖[5]。这种“底物-菌群”互作模式为开发兼具营养与微生态调节功能的发酵产品提供了独特优势。
本研究采用系统性研究策略分阶段揭示益生菌发酵蓝莓汁的工艺特性与健康功效:首先通过多维度评价体系(涵盖感官品质、理化指标、抗氧化活性及挥发性风味物质)对5株益生菌发酵产物进行综合比较,筛选出发酵特性最优菌株;进而基于肠道菌群失调小鼠模型,采用病理组织学观察、血清生化分析及16S rRNA测序技术,系统探究优势菌株发酵产物对肠道屏障功能、器官病理损伤及微生物群落结构的调节效应。本研究旨在构建益生菌发酵蓝莓汁的品质评价体系,并阐明益生菌发酵蓝莓汁对肠道健康调控机制,为开发功能型浆果发酵产品提供理论依据和技术支撑。
1 材料与方法
1.1 试验材料
1.1.1 试验菌株及实验动物
试验菌株:植物乳植杆菌(Lactiplantibacillus plantarum)LP、干酪乳酪杆菌(Lacticaseibacillus casei)LC、嗜酸乳杆菌(Lactobacillus acidophilus)LA、德氏乳杆菌保加利亚亚种(Lactobacillus delbrueckii subsp.bulgaricus)LB和唾液链球菌嗜热亚种(Streptococcus salivarius subsp.thermophilus)ST,冻干粉(规格100亿),陕西瑞茂生物科技有限公司。
实验动物:SPF级美国癌症研究所(institute of cancer research,ICR)雄性小鼠30只(体质量30~35 g),杭州启真有限公司。
1.1.2 原料与试剂
蓝莓鲜果采自浙江绍兴,用于蓝莓汁的制备;葡萄糖、果胶酶(食品级),河南中辰生物科技有限公司;苯酚、硫酸、葡萄糖、福林酚试剂、NaOH、HCl、KCl、无水醋酸钠、甲醇、无水乙醇和4%多聚甲醛(分析纯),上海阿拉丁试剂有限公司;没食子酸分析标准品(98%)、氨苄青霉素三水物(98%),中国源叶生物科技有限公司;总胆固醇、甘油三酯、高密度脂蛋白胆固醇、谷草转氨酶和谷丙转氨酶试剂盒,南京建成科技有限公司。
1.2 仪器与设备
ME 103E/02电子天平,瑞士梅特勒-托利多仪器有限公司;311 CO2恒温培养箱,美国赛默飞世尔科技公司;MTD-8222水浴锅,上海精宏实验设备有限公司;PHS-3C型pH计,上海雷磁有限公司;Fresco 17高速冷冻离心机,美国Thermo公司;Flavour Spec®GC-IMS气相色谱-离子迁移谱联用仪(gas chromatography-ion migration spectrometer,GC-IMS),德国G.A.S.公司;MJ-WJS2009P榨汁机,中国美的集团股份有限公司;KQ 5200B超声仪,昆山市超声仪器有限公司;SW-CJ-1FD超净工作台,苏州集团安泰空气技术有限公司;WZ手持糖度计,北京阳光亿事达科技有限公司;ReadMax 1900型光吸收全波长酶标仪,上海闪谱生物科技有限公司。
1.3 试验方法
1.3.1 工艺流程与技术路线
原料处理→榨汁[料水比(g∶mL)1∶2]→酶解(添加体积分数0.1%的果胶酶,55 ℃,100 min)→调配(添加葡萄糖使其糖度达到13 °Bx)→过滤→装罐→杀菌(85 ℃,20 min)→接种(体积分数3%)→发酵→成品→产品质量分析评价与筛选
1.3.2 发酵蓝莓汁的制备
将5株菌的冻干菌粉采用直投式[6]分别以体积分数3%接种在灭过菌的蓝莓汁中,接种植物乳植杆菌、干酪乳酪杆菌、嗜酸乳杆菌和德氏乳杆菌保加利亚亚种的蓝莓汁于37 ℃恒温培养箱发酵24 h,接种唾液链球菌嗜热亚种的蓝莓汁置于40 ℃恒温装置中持续培养24 h[7],随后对5种益生菌发酵蓝莓汁分别开展感官评测与质量检测。
1.3.3 感官指标分析与评价
参照廖茂雯等[3]的方法,组建由10名食品专业学生构成的感官评估团队,分别从味觉特性(30分)、口感(20分)、气味表现(20分)、组织形态(15分)及颜色特征(15分)5个维度,对蓝莓发酵饮品进行系统评价,最终采用加权平均法得出综合评分结果。感官评价表如表1所示。
表1 发酵蓝莓汁感官品质评价标准
Table 1 Sensory quality evaluation criteria for fermented blueberry juice
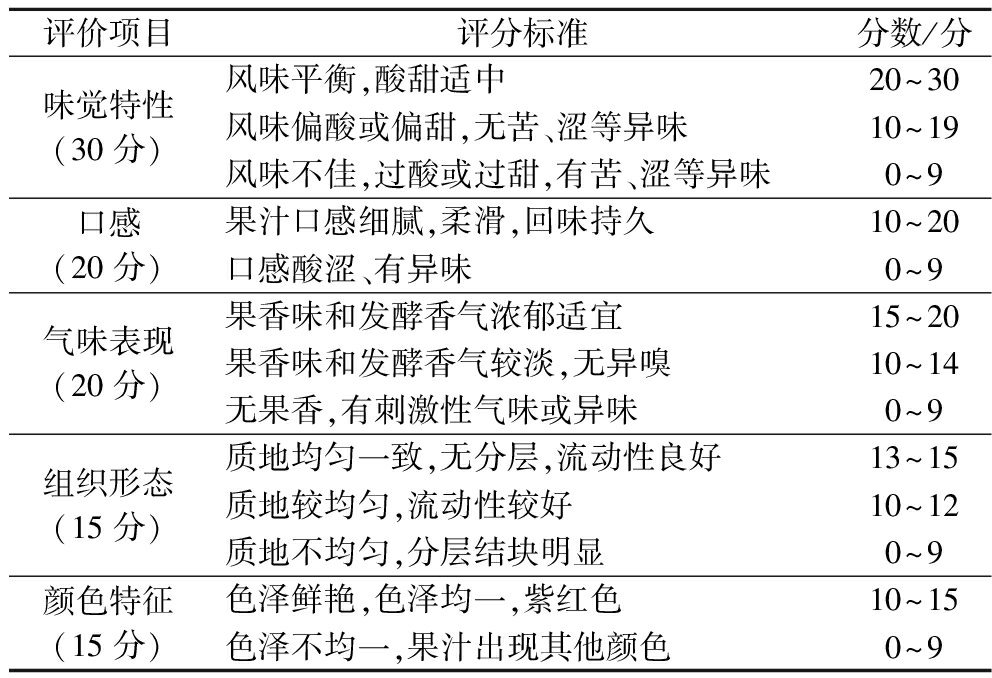
评价项目评分标准分数/分味觉特性(30分)风味平衡,酸甜适中20~30风味偏酸或偏甜,无苦、涩等异味10~19风味不佳,过酸或过甜,有苦、涩等异味0~9口感(20分)果汁口感细腻,柔滑,回味持久10~20口感酸涩、有异味0~9气味表现(20分)果香味和发酵香气浓郁适宜15~20果香味和发酵香气较淡,无异嗅10~14无果香,有刺激性气味或异味0~9组织形态(15分)质地均匀一致,无分层,流动性良好13~15质地较均匀,流动性较好10~12质地不均匀,分层结块明显0~9颜色特征(15分)色泽鲜艳,色泽均一,紫红色10~15色泽不均一,果汁出现其他颜色0~9
1.3.4 发酵蓝莓汁产品的质量分析与评价
蓝莓发酵汁于4 ℃下以3 000 r/min离心10 min后,进行质量分析与评价,进而筛选出最佳菌株。
1.3.4.1 理化性质与营养指标
pH值:采用pH计测定;可溶性固形物:采用糖度计测定;总酸:参照GB 12456—2021《食品安全国家标准 食品中总酸的测定(含第1号修改单)》进行测定。总糖含量:以葡萄糖为标准品,采用苯酚硫酸法测定[8];总酚含量:以没食子酸为标品,采用福林酚法测定[8];总花色苷含量采用pH示差法测定[8]。
1.3.4.2 抗氧化指标分析与评价
参照杨琦等[9]的方法测定DPPH自由基、ABTS阳离子自由基和羟自由基清除率
1.3.4.3 GC-IMS分析
参考LIAO等[10]的研究,将2.0 mL蓝莓汁加入20 mL顶空进样瓶中。在40 ℃和500 r/min下孵育20 min后,通过预先加热至85 ℃的注射器注入200 μL顶空。然后,将顶空输送到GC进行预分离。在60 ℃下使用MXT-WAX毛细管柱(30 m×0.53 mm,1.0 μm),以N2(纯度99.99%)作为初始载气。流速在前2 min内为2 mL/min,在2~10 min为10 mL/min,在10~20 min为100 mL/min,最后在20~25 min增加到150 mL/min。漂移管温度45 ℃,管道迁移区载气流速150 mL/min。
正酮C4~C9从中国国药化学试剂北京有限公司获得,用作外部标准,在Laboratory Analysis View软件中计算蓝莓汁中挥发性化合物的保留指数(retention index,RI)。通过将真实标准化合物的RI和漂移时间与GC-IMS数据库G.A.S进行比较来确认每种挥发性化合物的类型。
1.3.5 发酵蓝莓汁产品对肠道健康的探究
1.3.5.1 动物实验分组和模型建立
在经过1周适应性饲养后,选择30只体质量在30~35 g的ICR雄性小鼠。随机挑选10只作为对照组,其余20只小鼠则接受连续3 d的灌胃处理,使用氨苄青霉素,剂量为22.4 g/kg(以小鼠体质量计算),每次剂量为11.2 g/kg,频率为2次/d。造模成功的标准为小鼠出现稀便及背毛失去光泽[11]。对照组实验动物接受等体积生理盐水灌胃处理。模型验证通过后,将符合建模标准的小鼠随机划分为2个组:模型组和LP发酵蓝莓汁处理组。其中LP发酵蓝莓汁处理组灌胃LP发酵蓝莓汁200 μm/只,模型组和对照组灌胃同体积生理盐水,每天定时且连续灌胃12 d。饲养期间,供给充足的饲料和饮水供小鼠自由摄取。小鼠喂养12 d后,禁食12 h,处死前称重。动物实验伦理审查号:25ZALAS18。
1.3.5.2 血清生化指标分析
连续灌胃12 d相应受试物后,禁食不禁水12 h,采用无水乙醚麻醉后,眼球取血,静置2 h后,离心取血清,对小鼠血清中总胆固醇、甘油三酯、高密度脂蛋白胆固醇、谷丙转氨酶和谷草转氨酶进行测定。
1.3.5.3 小肠、肝脏和肾脏组织病理切片及苏木精-伊红染色观察分析
小鼠脱颈处死并解剖后,摘取肝脏和肾脏组织和剪取1~2 cm小肠都置于4%多聚甲醛中,固定48 h,委托杭州研趣信息技术有限公司旗下的科学指南针进行各组小鼠的组织病理切片及苏木精-伊红染色染色。
1.3.5.4 16S rRNA高通量测序分析肠道菌群
实验前对小鼠实施12 h禁食(自由饮水),随后在无菌条件下采集各组粪便样本。样品经液氮速冻后保存于-80 ℃超低温环境,采用干冰冷链运输至上海美吉生物医药科技有限公司进行Illumina NovaSeq 6000平台测序。基于样本特异性条形码完成序列分选后,经Trimmomatic质控过滤(Q≥30),最终通过QIIME2流程进行微生物群落分析,包括Alpha多样性指数(Shannon/Chao1)、Beta多样性[基于Bray-Curtis距离的主坐标分析(principal coordinates analysis,PCoA)]及门/属水平物种组成解析。
1.4 统计学处理
利用Excel和SPSS 26.0进行统计及方差分析。数据采用单因素方差分析结合Dun-can’s多重比较检验,数据以“平均值±标准差”(P<0.05)表示,采用Origin 2025软件进行数据可视化分析。小鼠肠道微生物数据分析均在美吉生物云平台(https://cloud.majorbio.com),具体如下:采用mothur软件(http://www.mothur.org/wiki/Calculators)计算Alpha多样性指数、Chao 1、Shannon指数等,并采用Wilxocon秩和检验进行Alpha多样性的组间差异分析;使用基于bray-curtis距离算法的PCoA检验样本间微生物群落结构的相似性,并结合PERMANOVA非参数检验分析样本组间微生物群落结构差异是否显著;采用Kruskal-Wallis检验进行多组比较的非参数检验,采用Wilxocon秩和检验进行组间差异检验,确定不同组间在属水平丰度显著差异的的细菌类群。采用R-3.3.1软件进行数据可视化分析。
2 结果与分析
2.1 发酵蓝莓汁感官指标分析与评价
如图1所示,蓝莓原汁初始感官得分69.2分,存在酸涩刺激明显、收敛性强及果香弱化等缺陷。经益生菌发酵后,LP组得分最高79.2分,显著优于CK组及其他菌株(LB 73.8分,LC 74.7分,LA 71.7分,ST 71.4分)(P<0.05)。感官特性分析显示,发酵后香气显著增强(P<0.05),但菌株间差异不显著,发酵前后颜色无显著变化;发酵组均无明显沉淀,与含沉淀的CK组差异显著;发酵后酸甜适口性显著提升(P<0.05)。综合评估表明,LP组在香气、口感与味觉协调性方面表现最优;ST滋味突出但香气欠佳;LC、LA、LB在香气与口感改善方面效果良好。
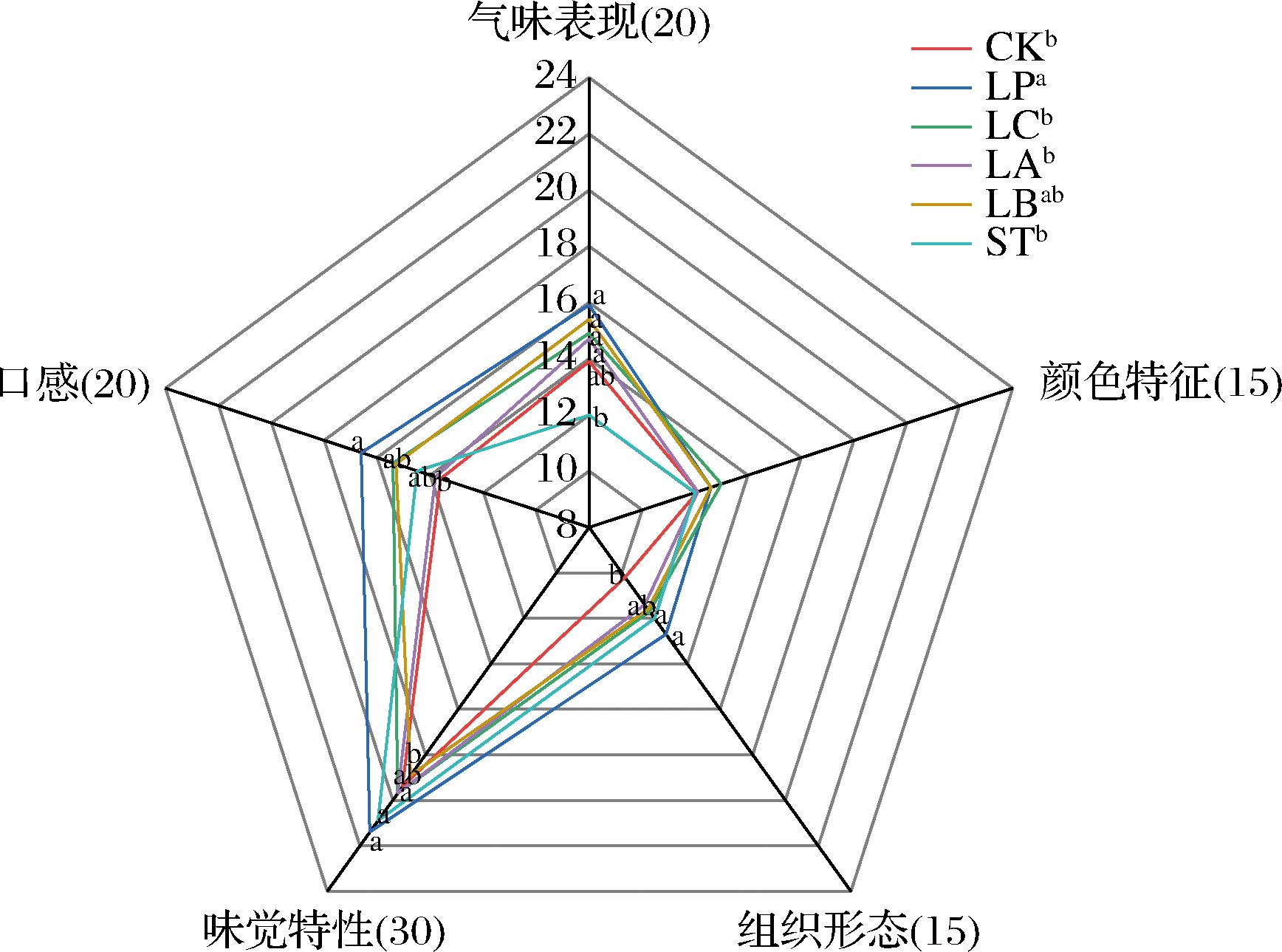
图1 发酵蓝莓汁感官评分雷达图
Fig.1 Radar chart for sensory evaluation of fermented blueberry juice
注:不同小写字母表示不同样品间差异显著(P<0.05)(下同)。
2.2 理化性质与主要营养功能性成分分析
由图2-a可知,CK组可溶性固形物含量的初始值为13.52%,蓝莓原浆经益生菌发酵后LP组(11.43%)、LA组(11.20%)和LC组(12.07%)发生显著性下降,LB组(12.25%)和ST组(12.59%)虽然有所下降但并无显著性。表明LP、LC和LA这3种益生菌对蓝莓中可溶性糖的利用程度较高。
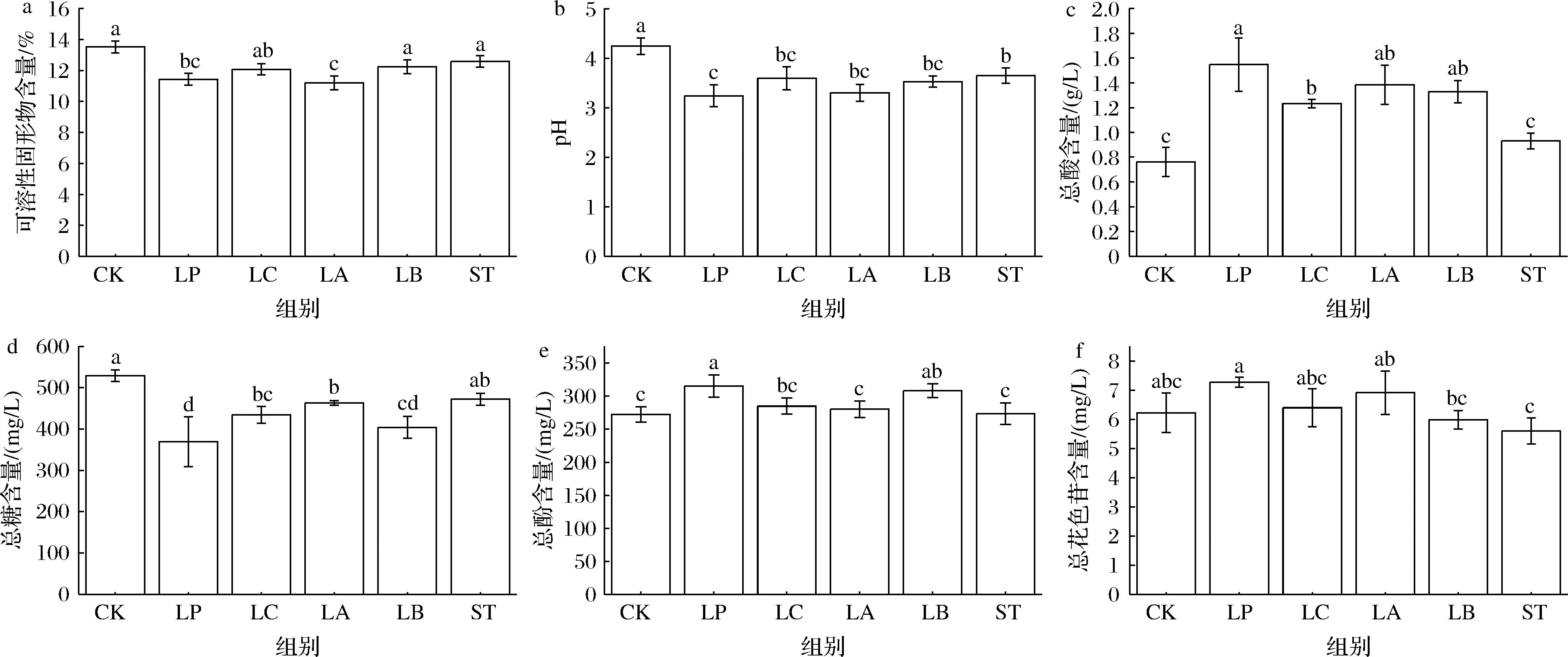
a-可溶性固形物;b-pH;c-总酸;d-总糖;e-总酚;f-总花色苷
图2 发酵蓝莓汁理化性质和主要营养功能性成分的变化
Fig.2 Changes in physicochemical properties and major nutritional and functional components of fermented blueberry juice
由图2-b和2-c可知,经过益生菌发酵处理的蓝莓汁中,pH值与总酸指标相较CK组均产生显著差异性变化(P<0.05)。其中LP和LA组显著下降(P<0.05),与朱丹实等[12]关于苹果汁发酵中pH变化一致。LP组的总酸含量为1.55 g/L,显著高于LC和ST组(P<0.05),其次为LA组(1.39 g/L),ST组最低(0.93 g/L),这与丁明可等[13]的研究结果一致。ST组发酵前后总酸含量虽有所提升,但无显著差异。研究显示,5株益生菌株在蓝莓汁基质内均展现出显著的产酸发酵能力。其中LP、LC、LA和LB组的产酸能力较为突出。
由图2-d可知,5株益生菌发酵处理蓝莓汁总糖含量均显著降低(P<0.05),而CK组维持初始糖质量浓度(529.19 mg/L),LP、LC、LA、LB和ST这5组不同益生菌菌株发酵后的总糖含量分别为369.50、434.39、463.06、404.10、472.10 mg/L,LP组的总糖含量消耗量最大,其次是LB组和LC组。上述结果说明,LP组在蓝莓汁中利用糖类能力高,生长繁殖效果较好。
由图2-e和图2-f可知,LP和LB发酵蓝莓汁中的总酚含量较CK组(272.28 mg/L)均显著升高(P<0.05),其余发酵组也有所提升但与CK组并无显著性差异。总花色苷含量方面,LP、LC和LA组的总花色苷含量高于CK组,说明益生菌延缓了花色苷的降解速度,该发现与刘晓翠等[14]对猕猴汁发酵的研究相吻合。可能是蓝莓汁中的糖类被有机酸或酚酸酰化,这些酰化在增强花色苷的稳定性方面起着至关重要的作用[15],但相较于CK组未呈现统计学差异(P>0.05)。而ST发酵组总花色苷含量却有所降低,其原因可能是40 ℃的发酵温度导致花色苷的降解过快。上述结果表明:5种益生乳酸菌在蓝莓汁中均可以改善蓝莓汁中营养物质品质,其中LP和LB在总酚含量方面提升较大,LB和ST在总花色苷含量方面有所降低。
2.3 抗氧化指标分析与评价
果蔬经益生菌发酵后,其抗氧化能力增强。由表2可知,与未发酵蓝莓汁CK组相比,LP、LA和LB组的蓝莓汁在3项体外抗氧化指标均显著提高(P<0.05),这与杨琦等[9]研究结果一致。其中LP和LB组,在DPPH自由基、ABTS阳离子自由基和羟自由基清除方面无显著性差异。但是LC组在DPPH自由基和ABTS阳离子自由基清除方面,ST组在羟自由基和ABTS阳离子自由基清除方面,虽较CK组有所提升但无显著性差异。其中,抗氧化能力提升最大的是LP组,每毫升果汁的DPPH自由基清除率由CK组的70.60%提高到90.86%,羟自由基清除率由CK组的31.82%提高到58.36%,ABTS阳离子自由基清除率由CK组的74.06%提高到87.83%,表明经益生菌发酵后的蓝莓汁产品具有更好的抗氧化活性。
表2 5种益生菌发酵蓝莓汁抗氧化指标检测结果 单位:%
Table 2 Test results of antioxidant indexes of five probiotic fermented blueberry juice
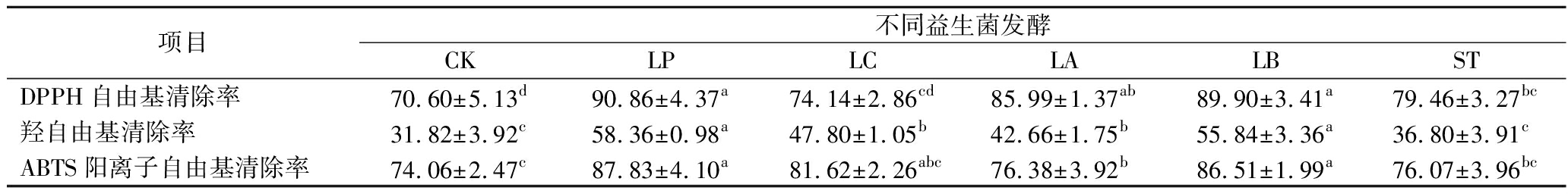
项目不同益生菌发酵CKLPLCLALBSTDPPH自由基清除率70.60±5.13d90.86±4.37a74.14±2.86cd85.99±1.37ab89.90±3.41a79.46±3.27bc羟自由基清除率31.82±3.92c58.36±0.98a47.80±1.05b42.66±1.75b55.84±3.36a36.80±3.91cABTS阳离子自由基清除率74.06±2.47c87.83±4.10a81.62±2.26abc76.38±3.92b86.51±1.99a76.07±3.96bc
注:不同小写字母表示差异显著(P<0.05)(下同)。
2.4 GC-IMS结果分析
2.4.1 发酵前后蓝莓汁挥发性风味物质特征
如图3所示,该图谱采用蓝色基底,坐标系严格对应三维离子迁移谱参数标准,横轴1.0刻度处可见指示反应离子峰的红色垂直标识线。反应离子峰周围的点为样品挥发性成分标记,通过显色点的分布形态及深浅变化,可鉴别不同样品间风味物质种类与含量的差异性[16]。以CK组谱图为基准,扣除相同特征峰后构建二维差异分析图谱,其中蓝色标识对应化合物相对CK组含量减少,红色标识代表含量增加且色度与差异程度正相关[16]。如图3所示,蓝莓汁发酵后在差异图中呈现密集分布的深红色标识,表明其挥发性风味组分相较蓝莓原浆呈现显著富集现象。
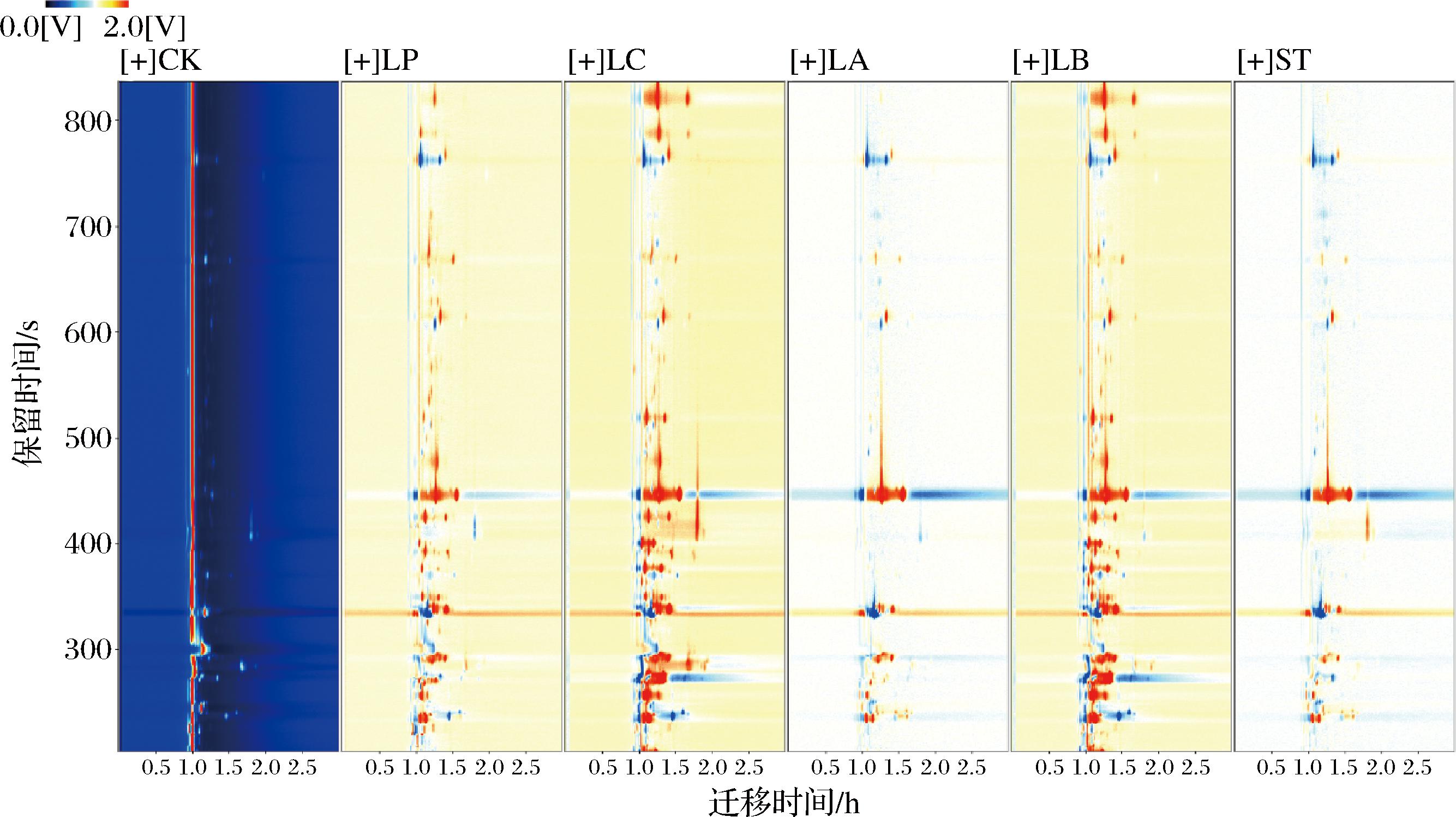
图3 发酵前后蓝莓汁中挥发性化合物成分对比差异谱图
Fig.3 Comparative difference spectra of composition of volatile organic compounds in blueberry juice before and after fermentation
2.4.2 发酵前后蓝莓汁挥发性风味物质定性及指纹图谱分析
如图4所示,指纹谱图通过二维矩阵结构呈现分析结果,其中横向维度对应各检测样本的特征峰信息,纵向维度揭示同一挥发性化合物在不同样品中的峰信号存在状态[17]。

图4 发酵前后蓝莓汁中挥发性化合物的指纹谱图
Fig.4 Fingerprinting of volatile organic compounds in blueberry juice before and after fermentation
由GC-IMS检测结果可知,在发酵处理前后的蓝莓汁样本中,累计鉴定出35种挥发性成分,包括:4种醇类物质、5种醛类物质、6种酯类物质、7种酮类衍生物,以及2种酸类、3种呋喃衍生物和3种吡嗪类化合物。还有其他类5种,包括烯烃类、内酯类、杂环类、吡啶类和噻唑类各1种。采用峰面积归一化法对蓝莓发酵液挥发性组分进行定量分析,获得各化合物相对含量分布,将检测到的挥发性化合物信息绘制成表,如电子版增强出版附表1所示(https://doi.org/10.13995/j.cnki.11-1802/ts.042802)所示。
醇类物质是构成发酵前后蓝莓汁挥发性香气成分种类最丰富,相对含量较高的一类重要的香气物质[17]。益生菌发酵丰富了蓝莓汁中醇类物质含量,从相对含量上来看,非发酵的蓝莓汁中醇类占32.49%,LP、LC、LB、LA和ST发酵后醇类分别占38.68%、34.37%、35.70%、29.67%和30.66%。发酵蓝莓汁中另一种重要的香气物质就是醛类物质。研究结果表明,未发酵蓝莓汁中醛类物质占比21.69%,经LP、LA和ST发酵后分别提升到22.74%、22.32%和22.39%,而LC和LB发酵后分别减少到16.68%和17.59%(附表1)。可能是发酵时间较长导致醛类含量均随着发酵的延长而降低,这与在西瓜汁中进行乳酸菌发酵研究一致[18]。酯类化合物作为蓝莓汁发酵产物的关键呈香组分,其显著特征表现为种类多样性与浓度富集性,主要呈现典型果香属性。从相对含量上看,非发酵的蓝莓汁中酯类占7.11%,而经LP、LC、LB、LA和ST发酵后酯类占比显著提升,分别占11.09%、20.97%、20.20%、17.12%和15.95%,说明益生菌发酵后极大丰富了酯类物质含量。酮类物质主要来源于醇类物质的氧化代谢过程,其在果香特征的形成中具有显著促进作用[17]。未发酵蓝莓汁中酮类物质占比13.53%,经LP和LC发酵后分别提升到17.59%和14.07%,而经LB、LA和ST发酵后其含量反而降低到12.07%、12.20%和12.62%。发酵蓝莓汁中还检测到酸类、呋喃类和吡嗪类含量都有所提升,特别吡嗪类的含量上从未发酵的0.45%提升到LA和ST发酵组的4.11%和3.87%,提升幅度显著超过LP、LC和LB组的0.84%、0.47%和0.49%。还有烯烃类的莰烯、内酯类的γ-己内酯、杂环类的4-甲基-2-苯基-1,3-二氧戊环、吡啶类的3-乙基吡啶都有所提升,因此益生菌发酵可以极大地丰富了蓝莓汁的风味,其中LP发酵组在各类挥发性物质中都有所提升,虽然在酯类物质方面提升不高,但在醇类、醛类、酮类和酸类方面显著提升,而LC组和LB组在醇类、酮类等方面变化不大,且醛类反而有所降低,仅酯类提升较大。LA和ST组在醇类、醛类、酮类和酸类方面有小幅度提升,但在酯类和吡嗪类有较大提升。
2.5 发酵蓝莓汁产品肠道健康功能的研究
综合评价5组益生菌发酵蓝莓汁在感官评价、营养指标、抗氧化能力和风味等方面的特性,以LP表现较为突出,故使用LP发酵的蓝莓汁作为目标产品进行后续肠道健康研究。
2.5.1 植物乳植杆菌发酵蓝莓汁对小鼠体质量和血清生化指标的影响
如图5所示,随着氨苄青霉素的干扰造成了小鼠肠道紊乱,从而影响消化吸收导致体质量较对照组显著减轻,在停止干扰并灌胃LP发酵蓝莓汁后体质量逐渐恢复,LP发酵蓝莓汁处理组体质量较模型组出现回升。
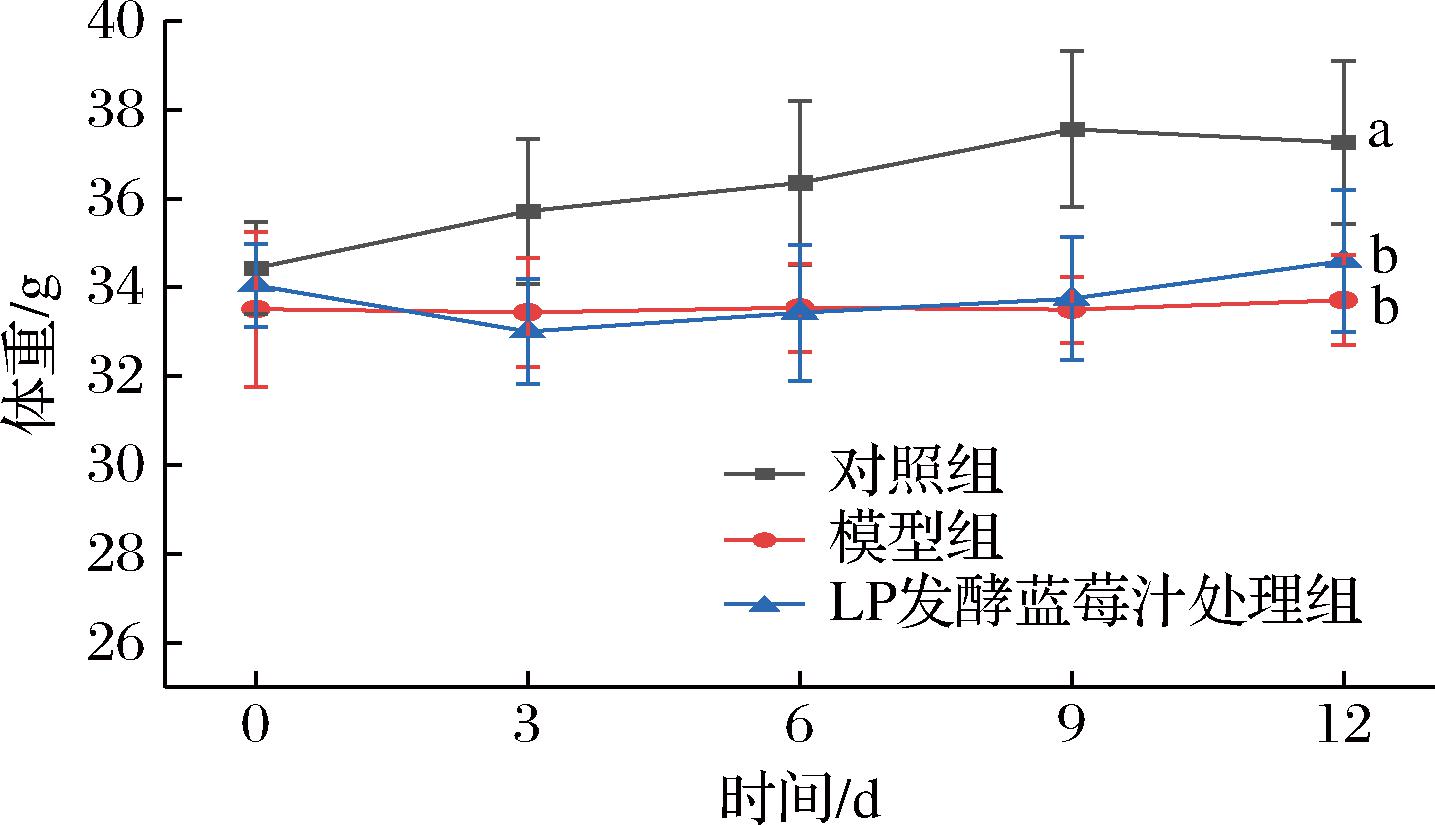
图5 LP发酵蓝莓汁对小鼠体质量的影响
Fig.5 Effect of LP fermented blueberry juice on body weight of mice
如表3所示,相较于对照组,模型组及经LP发酵蓝莓汁处理的小鼠中,血清总胆固醇、甘油三酯及高密度脂蛋白胆固醇水平均维持稳定状态,组间均无统计学差异(P>0.05)。这表明氨苄青霉素诱导的肠道菌群紊乱及后续益生菌补充干预均未引发实验小鼠脂代谢异常。谷丙转氨酶与谷草转氨酶是评估肝组织损伤的关键生物标志物[11]。模型组血清中谷丙转氨酶和谷草转氨酶活性水平较对照组呈现显著上升趋势(P<0.05),表明肠道健康失调可能通过肠-肝轴途径引发继发性肝损伤[19]。然而,LP发酵蓝莓汁处理后2种转氨酶活性相较于模型组表现出显著的回落现象,证实益生菌可能通过调节肠道微生态对肝组织损伤产生修复作用。
表3 LP发酵蓝莓汁对小鼠血清生化指标的影响
Table 3 Effect of LP fermented blueberry juice on serum biochemical indices in mice
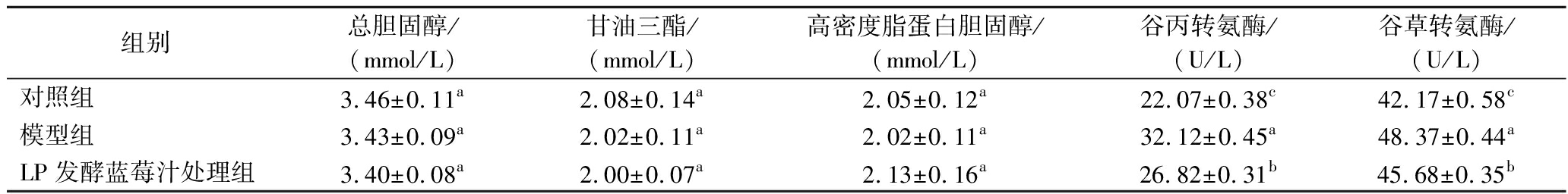
组别总胆固醇/(mmol/L)甘油三酯/(mmol/L)高密度脂蛋白胆固醇/(mmol/L)谷丙转氨酶/(U/L)谷草转氨酶/(U/L)对照组3.46±0.11a2.08±0.14a2.05±0.12a22.07±0.38c42.17±0.58c模型组3.43±0.09a2.02±0.11a2.02±0.11a32.12±0.45a48.37±0.44aLP发酵蓝莓汁处理组3.40±0.08a2.00±0.07a2.13±0.16a26.82±0.31b45.68±0.35b
2.5.2 植物乳植杆菌发酵蓝莓汁对小鼠组织器官的影响
肠黏膜屏障作为宿主抵御共生菌及致病微生物侵袭的首要保护结构[20]。由图6-a、图6-b和图6-c可知,对照组小鼠的小肠绒毛排列整齐呈梳状排列,隐窝结构清晰,杯状细胞完整,黏膜上皮细胞无明显脱落,模型组的小肠绒毛呈现绒毛断裂萎缩,隐窝丢失,杯状细胞数量减少,黏膜上皮细胞皱缩,排列稀疏,经LP发酵蓝莓汁处理后小鼠的小肠绒毛长度有所增加,小肠黏膜上皮细胞损伤有所恢复,细胞间隙明显缩小。表明LP可能黏附于肠道上皮细胞,有效维持黏膜机械屏障功能[20]。
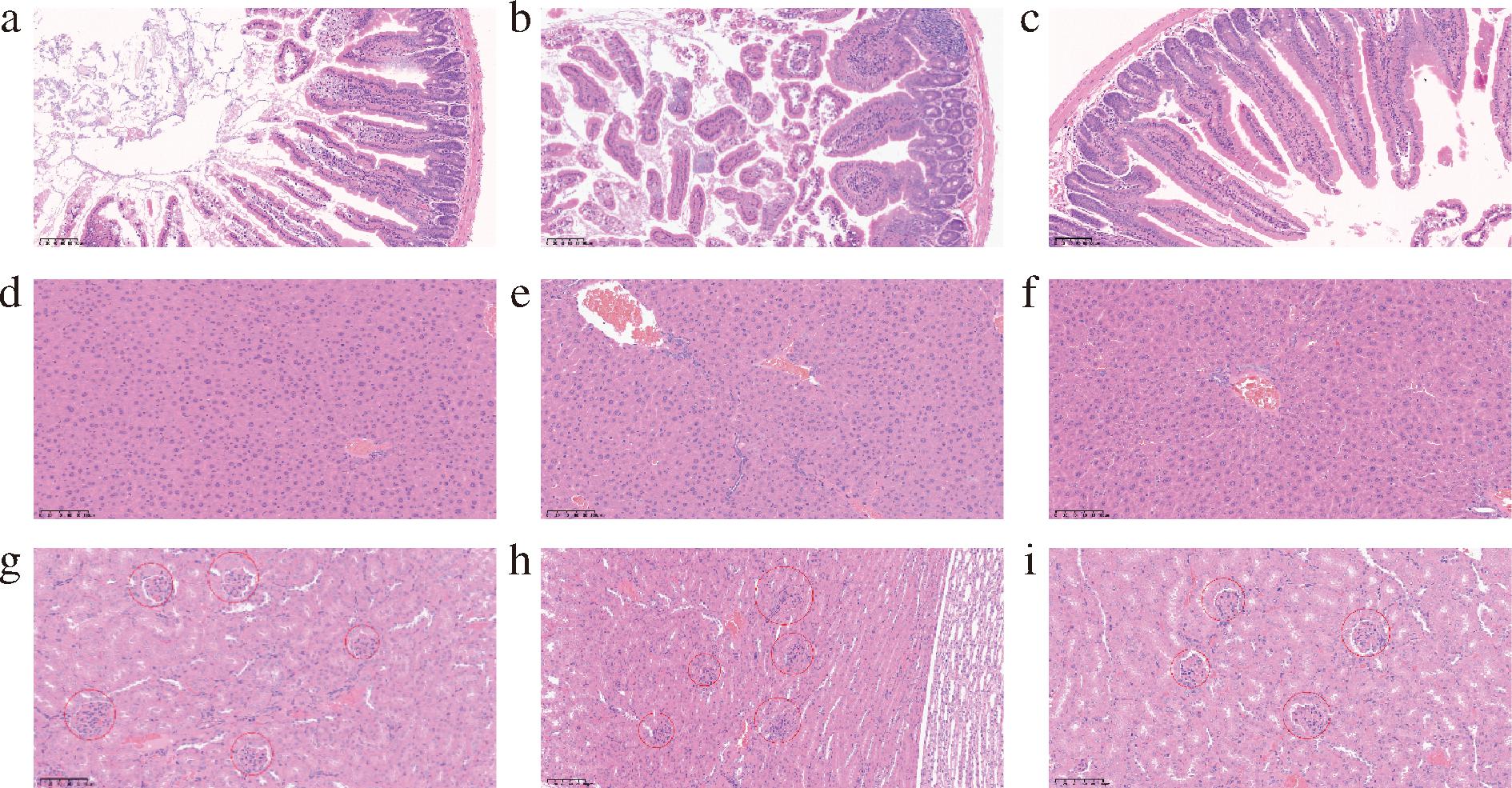
a-对照组小肠绒毛;b-模型组小肠绒毛;c-LP发酵蓝莓汁处理组小肠绒毛;d-对照组肝脏;e-模型组肝脏;f-LP发酵蓝莓汁处理组肝脏;g-对照组肾脏;h-模型组肾脏;i-LP发酵蓝莓汁处理组肾脏
图6 LP发酵蓝莓汁对小鼠组织器官的影响
Fig.6 Effects of LP fermented blueberry juice on the tissues and organs of mice
注:放大倍数×200,图g~图i中红色圆圈表示肾小球。
图6-d、图6-e和图6-f为小鼠肝损伤情况,对照组的小鼠肝小叶结构清晰,但模型组和LP发酵蓝莓汁处理组小鼠的肝脏周围有轻微炎性浸润,这可能是肠黏膜屏障功能障碍可引发肠壁渗透性异常升高,促使微生物的代谢产物脂多糖在门脉循环中进入肝脏的病理性蓄积,同时,肝脏通过胆汁酸分泌及免疫调节物质合成参与肠道稳态维持,当发生肝功能障碍时,将引发继发性肠道屏障损伤[19]。这种肠-肝轴交互作用最终诱发肝组织炎性反应,同时这种变化与肠道菌群失调引发的系统性低度炎症相关,而非器质性病变。
由图6-g、图6-h和图6-i可知,对照组和LP发酵蓝莓汁处理组小鼠的肾组织形态正常,而模型组小鼠的肾小球结构轻度紊乱,可能是源于肠道微生物群的改变,增加了炎症等反应导致,可见富含膳食纤维、多酚的益生菌的LP发酵蓝莓汁处理可以显著缓解肾相关炎症[21]。
2.5.3 植物乳植杆菌发酵蓝莓汁对肠道紊乱小鼠肠道菌群结构影响
2.5.3.1 Alpha多样性指数分析
Alpha多样性指数用于表示微生物多样性和丰富度[11],如图7所示,与对照组和模型组相比,LP发酵蓝莓汁处理组中小鼠肠道菌群的Sobs、Chao1和基于丰度的覆盖度估计量(abundance-based coverage estimator,ACE)指数均显示出更大的丰富性。但是本研究发现3组的Shannon和Simpson指数虽有升降但并无明显差异,说明相关处理无法显著改变群落多样性,只能改变丰富性。
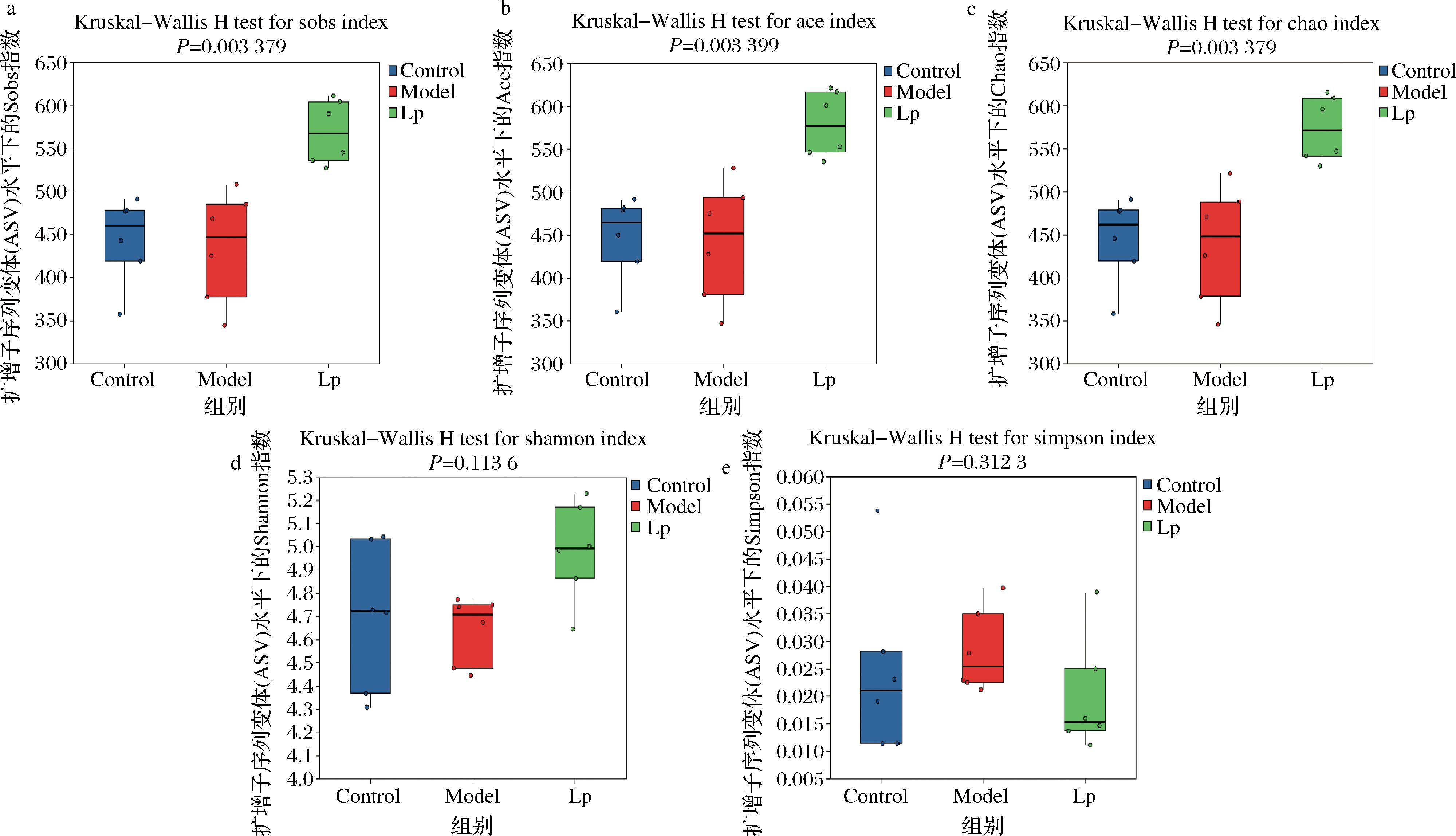
a-Sobs;b-Ace;c-Chao 1;d-Shannon;e-Simpson
图7 各组Alpha多样性指数分析比较箱线图
Fig.7 Comparative box plot of Alpha diversity index analyses by groups
注:Control-对照组,Model-模型组,Lp- LP发酵蓝莓汁处理组;0.01<P<0.05标记为*,0.001<P<0.01标记为**,P<0.001标记为***,下同。
2.5.3.2 Beta多样性指数分析
PCoA结果中,横纵坐标轴分别代表主坐标分量,每个散点对应一个样本,样本间距采用Bray-Curtis距离算法计算:每组质心间距>8个单位,表明其菌群结构存在显著分化[11]。图8中的PCoA显示,对照组样本集中分布于第一象限,模型组菌群结构向第四象限偏移,而LP发酵蓝莓汁干预组呈现向对照组趋近的分布特征,表明氨苄青霉素干预引发肠道微生物Beta多样性改变,该异常可被蓝莓发酵产物部分逆转。同时LP发酵蓝莓汁处理组远离模型组靠近对照组,表明LP发酵蓝莓汁处理组更有利于促进肠道菌群失衡模型小鼠肠道菌群恢复。
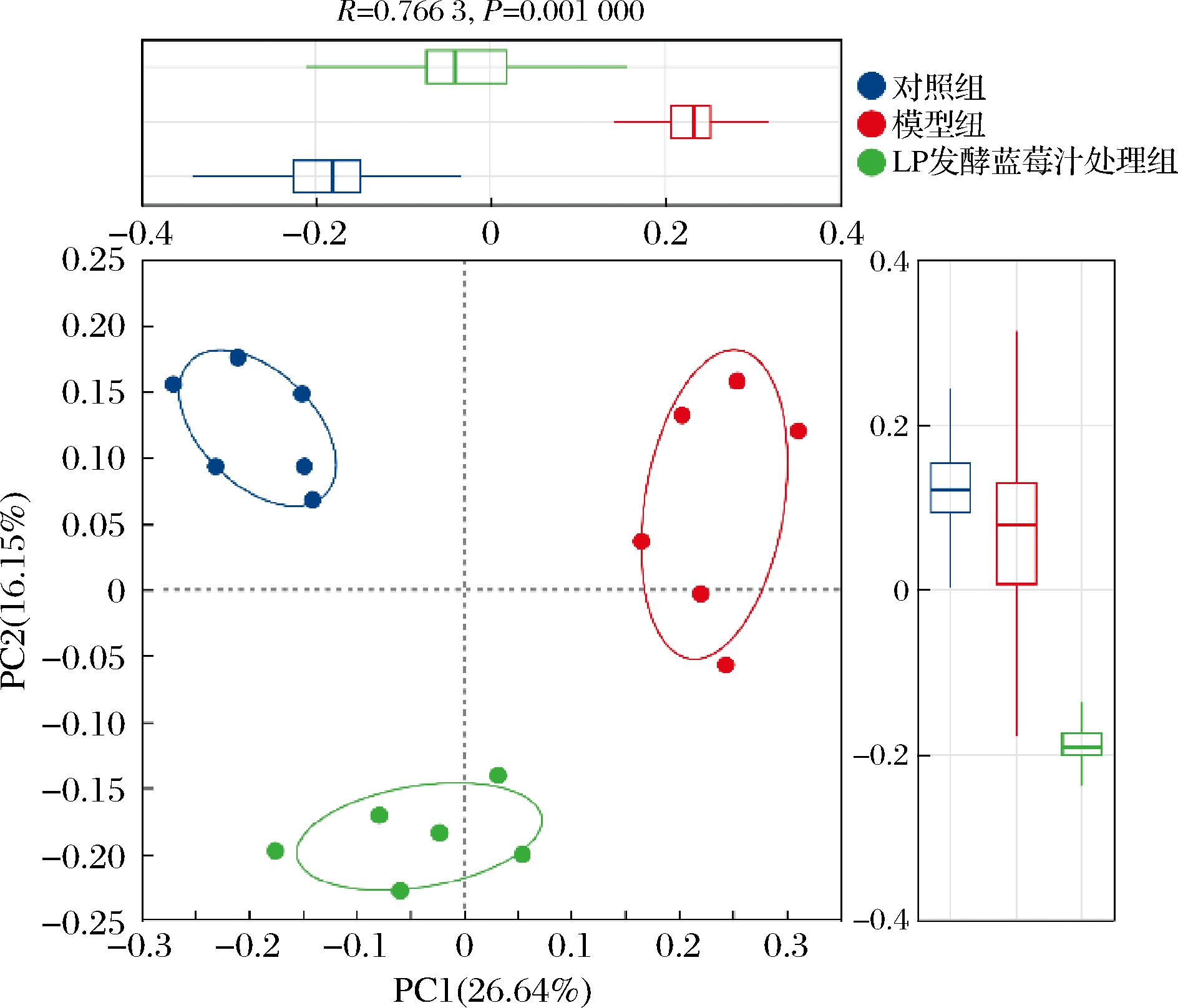
图8 各组PCoA
Fig.8 PCoA by group
2.5.3.3 植物乳植杆菌发酵蓝莓汁对肠道菌群失衡模型小鼠肠道菌群的影响
由图9-a可知,在门水平上,对照组、模型组和LP发酵蓝莓汁处理组的肠道微生物群落主要包括拟杆菌门(Bacteroidota)、厚壁菌门(Bacillota)、弯曲杆菌门(Campylobacterota)、放线菌门(Actinomycetota)、热脱磺杆菌门(Thermodesulfobacteriota)和假单胞菌门(Pseudomonadota),优势菌门为拟杆菌门和厚壁菌门。由图9-b可知,与对照组相比,模型组小鼠的肠道菌群物种丰度在门水平上出现了变化,放线菌门、热脱磺杆菌门和假单胞菌门的相对丰度升高,拟杆菌门、厚壁菌门和弯曲杆菌门的相对丰度降低,这表明肠道菌群结构出现了紊乱[22]。而经过LP发酵蓝莓汁的饲喂后,与模型组相比,LP发酵蓝莓汁处理组的干预能显著升高厚壁菌门、弯曲杆菌门和热脱磺杆菌门的丰度(P<0.05)。其中,相较于模型组,LP组厚壁菌门丰度显著提升13.38%(P<0.05)。总体上,在门水平方面抗生素和LP发酵蓝莓汁通过干预正常小鼠中厚壁菌门、弯曲杆菌门和热脱磺杆菌门的丰度来影响小鼠肠道菌群变化从而影响小鼠肠道菌群健康。另外,肠道菌群稳态的重要标志—厚壁菌门/拟杆菌门比值与其宿主机体功能密切相关,研究表明,比值异常降低可能诱发多种病理状态,包括但不限于抑郁症、阿尔茨海默病及炎症性肠病等系统性功能障碍[23]。如图9-b显示,对照组、模型组和LP发酵蓝莓汁处理组拟杆菌门比例分别为61.72%、60.26%和46.03%,厚壁菌门的比例分别为29.34%、26.63%和40.01%。对照组、模型组和LP发酵蓝莓汁处理组的厚壁菌门和拟杆菌门比值分别为0.48、0.44和0.87,与对照组相比,模型组中厚壁菌门/拟杆菌门比值有所降低,而灌胃LP发酵蓝莓汁后厚壁菌门/拟杆菌门比值显著提高,甚至高于对照组(P<0.05)。
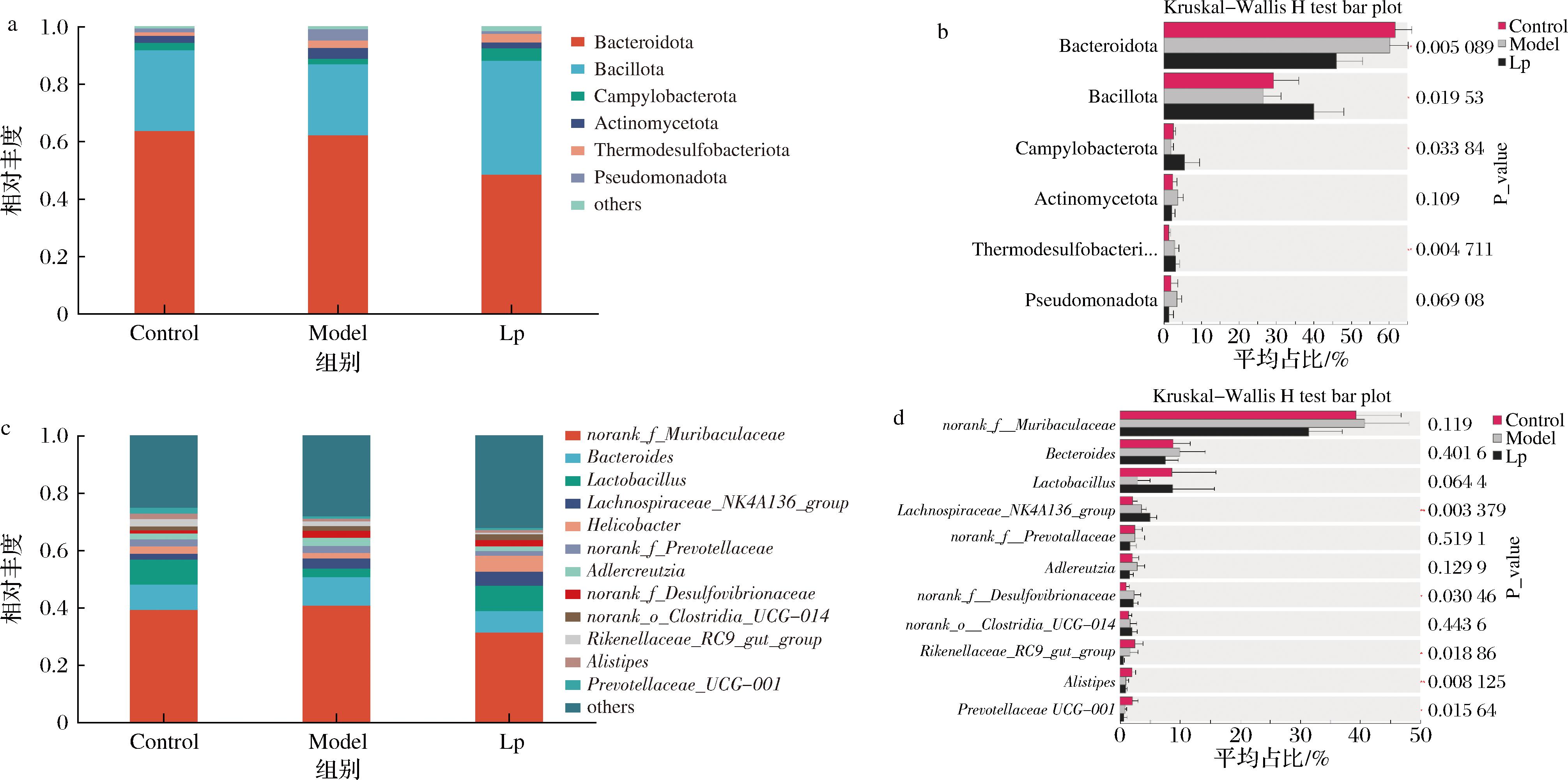
a-门水平菌群相对丰度;b-门水平各组优势菌群;c-属水平菌群相对丰度;d-属水平各组优势菌群
图9 LP发酵蓝莓汁对小鼠肠道菌群相对丰度的影响
Fig.9 Effect of LP fermented blueberry juice on relative abundance of intestinal flora in mice
在属水平上,3组小鼠的优势菌群分布如图9-c所示,主要是鼠杆菌科未定级分支(norank_f__Muribaculaceae)、拟杆菌属(Bacteroides)、乳杆菌属(Lactobacillus)、毛螺菌属(Lachnospiraceae_NK4A136_group)、幽门螺杆菌(Helicobacter)、普雷沃氏菌属(norank_f__Prevotellaceae)、阿德勒克鲁茨菌属(Adlercreutzia)、脱硫弧菌属(norank_f__Desulfovibrionaceae)、无级别分类的梭状芽孢杆菌群UCG-014(norank_o__Clostridia_UCG-014)、瑞肯氏菌科RC9肠道群(Rikenellaceae_RC9_gut_group)、另枝菌属(Alistipes)和普雷沃氏菌科UCG-001(Prevotellaceae_UCG-001)。在3组比较中发现,毛螺菌属NK4A136、脱硫弧菌属、瑞肯氏菌科RC9肠道群、另枝菌属和普雷沃氏菌科UCG-001变化较为显著(P<0.05),同时结果表明乳杆菌属在LP发酵蓝莓汁处理后丰度升高达到对照组水平,但并无显著性差异。以上结果表明,在属水平上抗生素和LP发酵蓝莓汁通过干预正常小鼠中毛螺菌属、脱硫弧菌属、瑞肯氏菌科RC9肠道群、另枝菌属和普雷沃氏菌科UCG-001的丰度来影响小鼠肠道菌群变化从而影响小鼠肠道菌群健康。
根据LDA>3.5,P<0.05共鉴定出44种差异菌株,图10-a描述了从门到属的层次结构关系,其中不同颜色节点表示在对应组别中显著富集,且对组间差异存在显著影响的微生物类群;淡黄色节点表示在不同分组中均无显著差异,或对组间差异无显著影响的微生物类群。结果显示,不同组小鼠的肠道菌群存在显著差异,每组选择前5种LDA得分较高的菌群后发现(图10-b),在对照组中拟杆菌门(p__Bacteroidota)的贡献最大,模型组中脱硫弧菌属(g__norank_f__Desulfovibrionaceae)的贡献最大、LP发酵蓝莓汁组中厚壁菌门(p__Bacillota)的贡献最大。
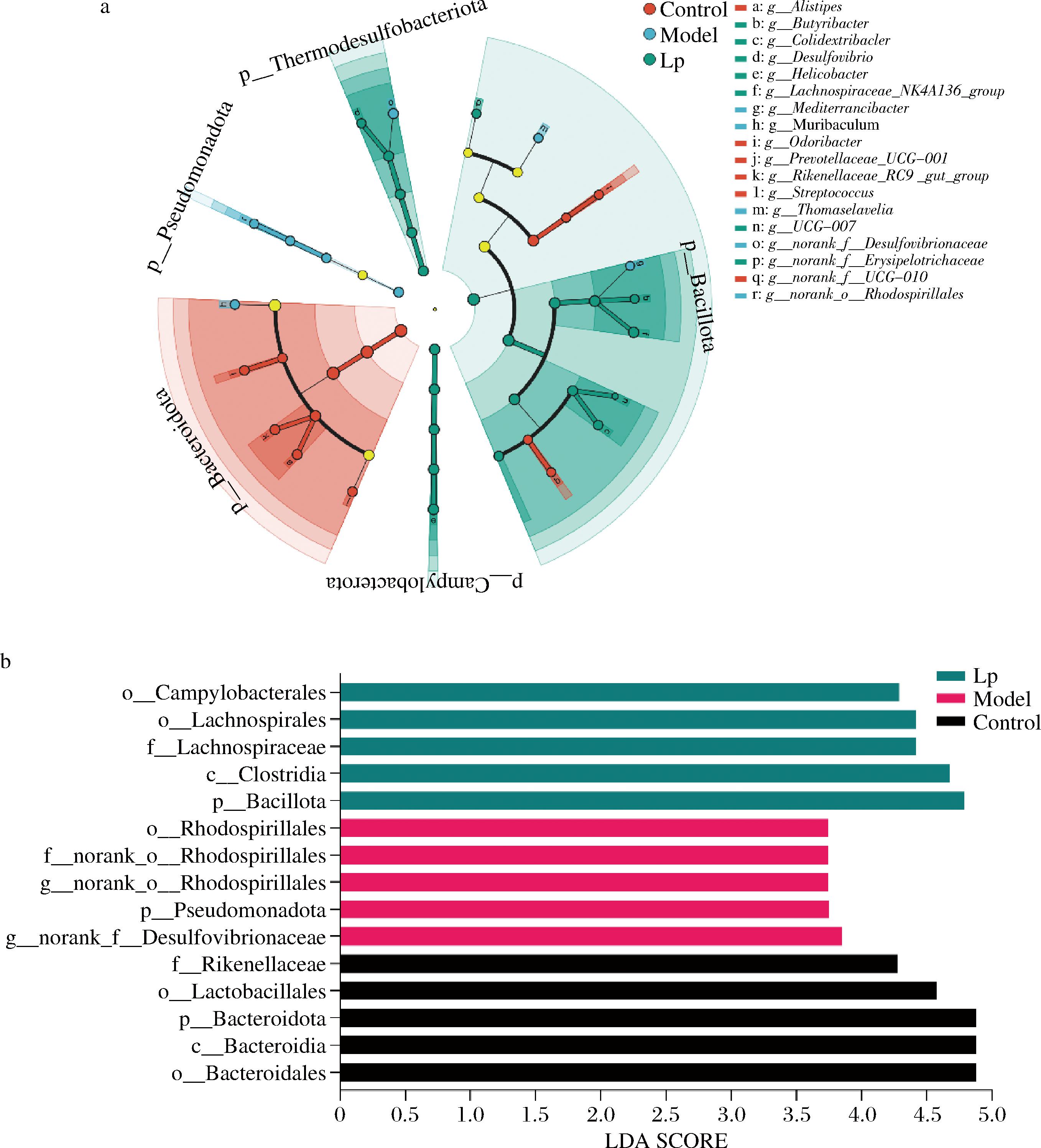
a-小鼠肠道菌群样本生成分支图;b-前5种LDA得分
图10 对照组、模型组和LP发酵蓝莓汁组小鼠肠道菌群的线性判别分析效应大小分析
Fig.10 Linear discriminant analysis effect size analysis of intestinal flora in control, model and LP fermented blueberry juice groups of mice
在属水平上,如图11-a所示,相比于对照组,模型组中未明确分类的丹毒菌科(norank_f__Erysipelotrichaceae)、臭气杆菌属(Odoribacter)、普雷沃氏菌科UCG-001(Prevotellaceae_UCG-001)、另枝菌属(Alistipes)和未明确分类的norank_f__UCG-010显著富集(P<0.05),其中未明确分类的丹毒菌科和臭气杆菌属极显著富集(P<0.01);毛螺菌属(Lachnospiraceae_UCG-006)、丹毒梭菌属(Thomasclavelia)、粪单胞菌属(Faecalimonas)、厌氧杆菌属(Family_XIII_AD3011_group)、未明确分类的脱硫弧菌属(norank_f__Desulfovibrionaceae)、毛螺菌属(Lachnospiraceae_NK4A136_group)、瘤胃球菌属(Ruminococcus)、Colidextribacter和Muribaculum显著减少(P<0.05),其中毛螺菌属(Lachnospiraceae_UCG-006)、丹毒梭菌属(Thomasclavelia)、粪单胞菌属(Faecalimonas)极显著减少(P<0.01)。
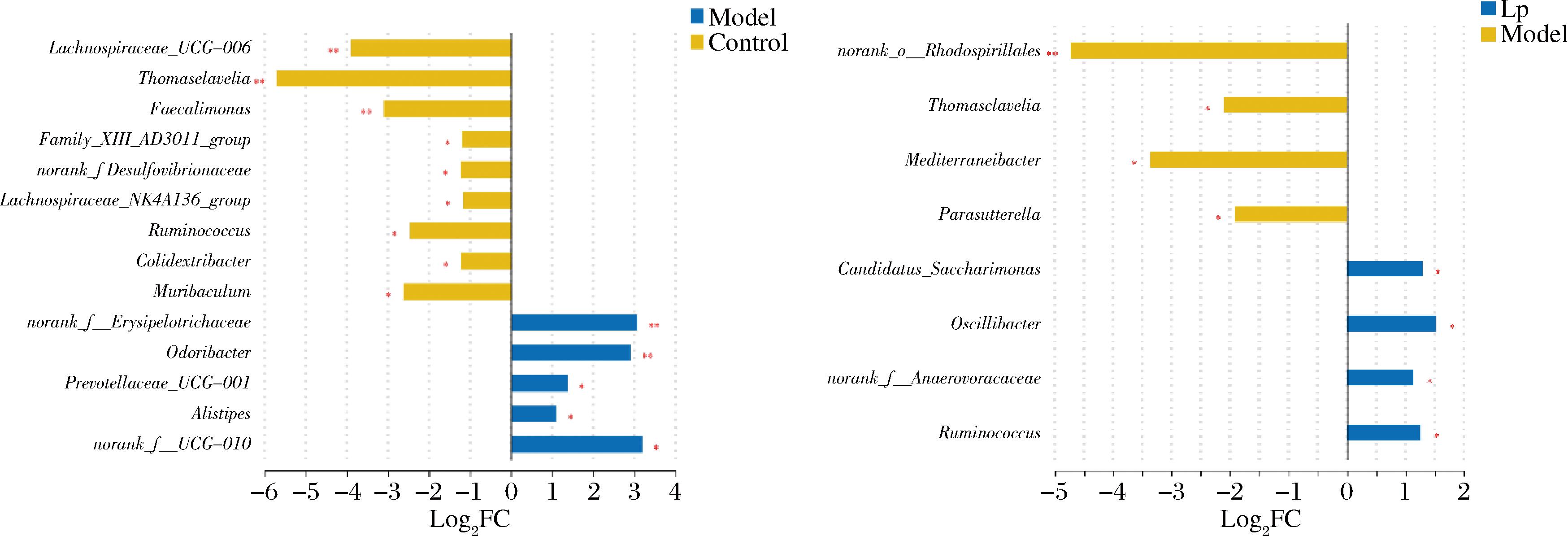
a-模型组 vs 对照组;b-Lp发酵蓝莓汁组 vs 模型组
图11 组间具有显著性差异的物种信息
Fig.11 Information on species with significant differences between groups
注:纵坐标表示不同分类水平下的物种名,横坐标表示组间差异倍数的log2计算结果,黄色为对照组,蓝色为处理组,正值表示物种注释相对于对照组富集,反之减少。
在属水平上,如图11-b所示,相比与模型组,LP发酵蓝莓汁处理组中颤螺菌属(Oscillibacter)、Candidatus_Saccharimonas、未明确分类的厌氧菌科(norank_f__Anaerovoracaceae)和瘤胃球菌属(Ruminococcus)显著富集(P<0.05);未明确分类的红螺菌目(norank_o__Rhodospirillales)、托马斯菌属(Thomasclavelia)、地中海杆菌属(Mediterraneibacter)和副萨特氏菌属(Parasutterella)显著减少(P<0.05),其中未明确分类的红螺菌目(norank_o__Rhodospirillales)极显著减少(P<0.01)。
3 结论与讨论
本研究系统筛选并评价了5种益生菌发酵对蓝莓汁品质的影响,结果显示经5株乳酸菌菌株发酵处理的蓝莓汁中,可溶性固形物含量、总酸值及pH指标均呈现显著性变化。其中LP和LA发酵后可溶性固形物含量和pH较低,产酸量较高。蓝莓中富含花色苷和多酚等抗氧化活性物质[9]。测定蓝莓的营养物质含量发现,各发酵组的总糖含量下降。发酵后蓝莓汁中的总酚和总花色苷的含量有所增加。深入分析蓝莓汁发酵产物的抗氧化特性发现,经5株益生菌菌株处理后,其DPPH自由基清除率、ABTS阳离子自由基清除率及羟自由基抑制率均呈现显著提升趋势。气味分析也是评价蓝莓汁发酵产品的重要指标。GC-IMS结果发现不同发酵组不同类的风味物质占比差异较大。其中LP发酵组在各类挥发性物质中都有所提升,特别是在醇类、醛类、酮类和酸类方面显著提升,气味表现较为突出,故使用LP发酵的蓝莓汁作为目标产品进行后续肠道健康调节研究。
筛选并确定植物乳植杆菌为发酵蓝莓汁最优菌株后,采用氨苄青霉素干扰正常小鼠的健康肠道菌群环境后饲喂LP发酵蓝莓汁干预其恢复过程。研究发现,氨苄青霉素造成的肠道菌群失衡会造成体质量的下降、肝脏和肾脏的轻微炎性浸润和小肠绒毛及其周围组织细胞的损伤,而益生菌LP发酵蓝莓汁的加入可有效缓解以上症状。
在对肠道菌群的研究中发现,在门水平上,LP发酵蓝莓汁的干预可以显著提升厚壁菌门的丰度,LP发酵蓝莓汁通过影响厚壁菌门丰度提高厚壁菌门和拟杆菌门的比值来影响小鼠肠道菌群从而影响小鼠肠道菌群健康。
本研究还在属水平上更深入地研究了小鼠肠道菌群的变化,模型组相较于对照组发现丹毒菌科、臭气杆菌属、普雷沃氏菌科UCG-001和另枝菌属等有害菌富集,而毛螺菌属_UCG-006、粪单胞菌属、厌氧杆菌属群_XIII_AD3011、毛螺菌属群_NK4A136和瘤胃球菌属等有益菌减少。与模型组相比,LP发酵蓝莓汁处理组在颤螺菌属、厌氧菌科和瘤胃球菌属等有益菌的相对丰度方面有了显著提升。其中,颤螺菌属和瘤胃球菌属属于厚壁菌门,是丁酸产生菌类[27]。作为厚壁菌门的一员,它们可以通过纤维素体途径降解纤维素和半纤维素,然后膳食纤维降解产生的一些低聚糖和葡萄糖可以作为微生物生长的碳和能量来源,从而增加微生物的多样性[28]。这些糖被产生短链脂肪酸的细菌如颤螺菌属和瘤胃球菌属,通过不同的途径发酵成短链脂肪酸—主要包括乙酸盐、丙酸盐和丁酸盐,短链脂肪酸可以调节宿主的代谢,包括能量代谢、宿主食欲、肝脏代谢和葡萄糖平衡[28]。厌氧菌科也可以分解食物中的复合碳水化合物,产生有益的短链脂肪酸,为肠道细胞提供能量[29]。虽然乳杆菌属和毛螺菌属,在组间比较中不显著,但在LP发酵蓝莓汁的干预下小鼠肠道内的乳杆菌属和毛螺菌属丰度有所提升。乳杆菌属作为厚壁菌门的一员,是肠道共生体系的核心益生菌群,其通过代谢产生短链脂肪酸实现肠腔微环境酸化(pH 5.3~6.5),这种生理调控作用可显著增强定植抗力,抑制条件致病菌(如大肠杆菌、产气荚膜梭菌)的生物膜形成与过度增殖[23]。同样毛螺菌属也属于厚壁菌门,其作为肠道核心产丁酸菌,通过发酵膳食纤维生成短链脂肪酸丁酸,该物质不仅是结肠上皮细胞的主要能量基质,同时维持宿主黏膜屏障功能[20]。在有害菌方面,与模型组相比,托马斯菌属、地中海杆菌属和副萨特氏菌属相对丰度显著减少。其中,托马斯菌属是一种已经与菌群失调相关的物种[30];地中海杆菌属与多种病理有关,包括肥胖,肠道炎症、儿童过敏和非酒精性脂肪变性[31]和副萨特氏菌属—也是一种常见的致病菌,与肠道黏膜的炎症反应有关、全身代谢异常,人类肥胖和Ⅱ型糖尿病,并在微生态失衡引起的系统性低度代谢炎症的发展中发挥作用[32]。有害菌下降的原因可能是益生菌发酵蓝莓汁产生的乳酸、酚酸等物质可以抑制病原体的生长繁殖[33],同时发酵蓝莓汁中含有丰富的多酚类物质可以有效缓解炎症,抑制普雷沃氏菌属、另枝菌属等促炎菌群的生长繁殖[34]。肠道菌群分析结果表明,LP发酵蓝莓汁饲喂氨苄青霉素诱导的肠道菌群失衡模型小鼠能够升高小鼠肠道中的颤螺菌属、厌氧菌科和瘤胃球菌属等有益菌群的相对丰度,降低托马斯菌属、地中海杆菌属和副萨特氏菌属等有害菌群的相对丰度;富集到颤螺菌属和瘤胃球菌属等厚壁菌门菌群以及厌氧菌科等可能是LP发酵蓝莓汁恢复氨苄青霉素诱导小鼠的肠道菌群紊乱、调节肠道屏障修复功能的菌群。
本研究通过系统评价益生菌发酵对蓝莓汁品质的影响,并揭示了植物乳植杆菌发酵蓝莓汁在改善肠道菌群健康中的关键作用。结果表明,益生菌发酵可显著提升蓝莓汁的感官特性、营养品质及抗氧化活性,其中LP发酵组表现出显著优势:总酸含量提升至1.55 g/L,总酚含量315.34 mg/L,DPPH自由基清除率提高到90.86%,并形成以醇类(38.68%)、醛类(22.74%)为主的果香风味体系。这种综合品质提升为后续肠道菌群健康研究奠定了物质基础。进一步通过肠道菌群失衡模型研究发现,LP发酵蓝莓汁具有显著的肠道调节功效。其作用机制主要体现在两个层面:其一,通过改善肠-肝轴功能缓解器官损伤,使血清谷丙转氨酶/谷草转氨酶水平较模型组降低10.6%(P<0.05),小肠绒毛长度恢复至对照组;其二,重构肠道菌群生态,相较于模型组显著提高厚壁菌门丰度(40.01%),其中产丁酸功能菌属尤为突出—颤螺菌属和瘤胃球菌属相对丰度较模型组显著增加,协同毛螺菌属及乳杆菌属共同促进短链脂肪酸合成。同时有效抑制促炎菌群,使普雷沃氏菌属、托马斯菌属、地中海杆菌属和副萨特氏菌属等有害菌的丰度显著降低。这种菌群结构的优化证实LP发酵产物可通过"代谢产物-菌群互作"机制发挥肠道屏障保护作用。该发现不仅为开发功能性发酵蓝莓制品提供了理论依据,更揭示了益生菌发酵食品通过多方面调控改善肠道菌群健康的新途径,具有重要的应用价值。
[1] 周勤文, 孙力军, 卢蓓蓓, 等.小浆果多酚生物活性功效研究进展[J].中国野生植物资源, 2023, 42(2):94-97, 102.
ZHOU Q W, SUN L J, LU B B, et al.Research Progress on Bioactivity of Polyphenols of Small Berries[J].Chinese Wild Plant Resources, 2023, 42(2):94-97, 102.
[2] BARKAOUI S, MADUREIRA J, BOUDHRIOUA N, et al.Berries:Effects on health, preservation methods, and uses in functional foods:A review[J].European Food Research and Technology, 2023, 249(7):1689-1715.
[3] 廖茂雯, 韩琛, 刘玮, 等.植物乳杆菌发酵蓝莓汁发酵和贮藏过程中理化指标及挥发性风味物质的变化[J].食品工业科技, 2025, 46(1):259-273.
LIAO M W, HAN C, LIU W, et al.Effects of Lactobacillus plantarum on physicochemical properties and volatile and flavor substances of blueberry juice during fermentation and storage[J].Science and Technology of Food Industry, 2025, 46(1):259-273.
[4] GUL S, DURANTE-MANGONI E.Unraveling the puzzle:Health benefits of probiotics-a comprehensive review[J].Journal of Clinical Medicine, 2024, 13(5):1436.
[5] ALVES-SANTOS A M, SUGIZAKI C S A, LIMA G C, et al.Prebiotic effect of dietary polyphenols:A systematic review[J].Journal of Functional Foods, 2020, 74:104169.
[6] 邹伟, 丁翘, 朱思莹, 等.单一及混合益生菌发酵南酸枣果汁理化性质、感官评定和香气成分分析[J].食品与发酵工业, 2025, 51(13):301-310.
ZOU W, DING Q, ZHU S Y, et al.Analysis of physicochemical properties, sensory evalution and aroma components of fermented Choerospondias axillaris juices inoculated with single and mixed probiotics[J].Food and Fermentation Industries, 2025, 51(13):301-310.
[7] 裴志雯, 胡炜, 刘梓璇, 等.唾液链球菌嗜热亚种生长及发酵特性研究[J].食品与发酵工业, 2025, 51(9):59-66.
PEI Z W, HU W, LIU Z X, et al.Study on growth and fermentation characteristics of Streptococcus salivarius subsp.thermophilus[J].Food and Fermentation Industries, 2025, 51(9):59-66.
[8] ZHANG Y Q, WANG H X, CHEN H J, et al.The crucial evaluation indexes and relative measurement methods of edible value for fresh fruits and vegetables:A review[J].Future Postharvest and Food, 2024, 1(2):222-236.
[9] 杨琦, 谢纯良, 周映君, 等.益生菌发酵蓝莓的体外抗氧化活性分析[J].食品与发酵工业, 2022, 48(9):112-116.
YANG Q, XIE C L, ZHOU Y J, et al.Antioxidant activity in vitro of probiotics fermented blueberry drink[J].Food and Fermentation Industries, 2022, 48(9):112-116.
[10] LIAO W H, SHEN J, MANICKAM S, et al.Investigation of blueberry juice fermentation by mixed probiotic strains:Regression modeling, machine learning optimization and comparison with fermentation by single strain in the phenolic and volatile profiles[J].Food Chemistry, 2023, 405:134982.
[11] 凌旺, 乔晓利, 胡海峰.复合益生菌制剂对小鼠肠道菌群的影响研究[J].轻工科技, 2021, 37(8):18-21.
LING W, QIAO X L, HU H F.Effect of compound probiotics on intestinal flora in mice[J].Light Industry Science and Technology, 2021, 37(8):18-21.
[12] 朱丹实, 王芳平, 赵国苍, 等.5种益生菌发酵寒富苹果汁特性的研究[J].中国食品学报, 2024, 24(10):204-214.
ZHU D S, WANG F P, ZHAO G C, et al.Studies on the fermentation properties of Hanfu apple juice by five probiotics[J].Journal of Chinese Institute of Food Science and Technology, 2024, 24(10):204-214.
[13] 丁明可, 陈慧芝, 吴伟杰, 等.不同乳酸菌发酵蓝莓桑葚原浆营养品质及风味变化分析[J].核农学报, 2025, 39(2):297-306.
DING M K, CHEN H Z, WU W J, et al.Analysis of nutritional quality and flavor change of blueberry mulberry juice fermented by different lactic acid bacteria[J].Journal of Nuclear Agricultural Sciences, 2025,39(2):297-306.
[14] 刘晓翠, 李仲巧, 朱慧君, 等.乳酸菌发酵猕猴桃汁的工艺优化[J].西华大学学报(自然科学版), 2023, 42(3):1-9.
LIU X C, LI Z Q, ZHU H J, et al.Optimization of fermentation technology of kiwifruit juice by lactic acid bacteria[J].Journal of Xihua University (Natural Science Edition), 2023, 42(3):1-9.
[15] FAN X K, LIU M Z, SHI Z H, et al.Binary probiotic fermentation promotes signal (cyclic AMP) exchange to increases the number of viable probiotics, anthocyanins and polyphenol content, and the odor scores of wolfberry fermented beverages[J].Food Chemistry, 2024, 448:139085.
[16] 张伯雅, 郑璞帆, 李晓雪, 等.基于电子舌结合GC-IMS分析不同品种梨果实的风味成分差异[J].保鲜与加工, 2024, 24(10):109-118.
ZHANG B Y, ZHENG P F, LI X X, et al.Analysis of flavor components differences in different varieties of pear fruits based on electronic tongue combined with GC-IMS[J].Storage and Process, 2024, 24(10):109-118.
[17] 田芸, 孙海燕, 朱旋, 等.基于气相离子迁移色谱分析不同贮藏时期蓝莓的挥发性化合物变化[J].食品研究与开发, 2024, 45(24):168-175.
TIAN Y, SUN H Y, ZHU X, et al.Analysis of changes in volatile components of blueberries under different storage periods based on GC-IMS[J].Food Research and Development, 2024, 45(24):168-175.
[18] MANDHA J, SHUMOY H, DEVAERE J, et al.Effect of lactic acid fermentation of watermelon juice on its sensory acceptability and volatile compounds[J].Food Chemistry, 2021, 358:129809.
[19] FAN S X, WANG J, LI Q, et al.Mechanism of gut-microbiota-liver axis in the pathogenesis of intestinal failure-associated liver disease[J].Chinese Journal of Gastrointestinal Surgery, 2021, 24(1):94-100.
[20] LIU Y H, LIU G, FANG J.Progress on the mechanisms of Lactobacillus plantarum to improve intestinal barrier function in ulcerative colitis[J].The Journal of Nutritional Biochemistry, 2024, 124:109505.
[21] JIAN S Y, YANG K, ZHANG L N, et al.The modulation effects of plant-derived bioactive ingredients on chronic kidney disease:Focus on the gut-kidney axis[J].Food Frontiers, 2023, 4(1):262-282.
[22] HE M X, SHI J C, LIU A Y, et al.Antibiotic-induced gut microbiota dysbiosis altered host metabolism[J].Molecular Omics, 2023, 19(4):330-339.
[23] 宋晓妍, 肖灵, 刘雅萱, 等.益生菌协同黑茶调节肠道菌群缓解盐酸洛哌丁胺诱导的小鼠便秘[J].食品与发酵工业,2025,51(12):294-302.
SONG X Y, XIAO L, LIU Y X, et al.Probiotics synergize with dark tea to regulate intestinal flora and alleviateloperamide-induced constipation in mice[J].Food and Fermentation Industries, 2025,51(12):294-302.
[24] XIE Y Z, PEI F Y, LIU Y C, et al. Fecal fermentation and high-fat diet-induced obesity mouse model confirmed exopolysaccharide from Weissella cibaria PFY06 can ameliorate obesity by regulating the gut microbiota[J]. Carbohydrate Polymers, 2023, 318: 121122.
[25] HOU L Y, YANG Y N, SUN B S, et al. Dietary fiber, gut microbiota, short-chain fatty acids, and host metabolism[J]. American Journal of Life Sciences, 2021, 9(6): 162.
[26] YANG Y Y, QUAN Y Y, LIU Y T, et al. Exploring the potential mechanism of Xiaojin Pill therapy for benign prostatic hyperplasia through metabolomics and gut microbiota analysis[J]. Frontiers in Microbiology, 2024, 15: 1431954.
[27] MBAYE B, WASFY R M, ALOU M T, et al. Limosilactobacillus fermentum, Lactococcus lactis and Thomasclavelia ramosa are enriched and Methanobrevibacter smithii is depleted in patients with non-alcoholic steatohepatitis[J]. Microbial Pathogenesis, 2023, 180: 106160.
[28] MBAYE B, MAGDY WASFY R, BORENTAIN P, et al. Increased fecal ethanol and enriched ethanol-producing gut bacteria Limosilactobacillus fermentum, Enterocloster bolteae, Mediterraneibacter gnavus and Streptococcus mutans in nonalcoholic steatohepatitis[J]. Frontiers in Cellular and Infection Microbiology, 2023, 13: 1279354.
[29] SUN Y J, WANG R C, SUN Y Y, et al. The attenuating effect of fermented soymilk on DSS-induced colitis in mice by suppressing immune response and modulating gut microbiota[J]. Food Research International, 2024, 176: 113797.
[30] ZUO F L, SOMIAH T, GEBREMARIAM H G, et al. Lactobacilli downregulate transcription factors in Helicobacter pylori that affect motility, acid tolerance and antimicrobial peptide survival[J]. International Journal of Molecular Sciences, 2022, 23(24): 15451.
[31] PARKER B J, WEARSCH P A, VELOO A C M, et al. The genus Alistipes: Gut bacteria with emerging implications to inflammation, cancer, and mental health[J]. Frontiers in Immunology, 2020, 9(11): 906.