橄榄苦苷是具有多种生物活性的天然裂环烯醚萜苷类多酚化合物。研究表明,橄榄苦苷在多种人类癌细胞系中表现出显著的抗肿瘤活性,能够通过多种机制抑制肿瘤细胞增殖并诱导其凋亡[1-3]。橄榄苦苷是一种具有防治糖尿病及其并发症潜力的生物活性成分。研究表明,它可通过调节胰岛素分泌、修复胰岛形态、改善糖耐量和胰岛素抵抗来改善糖尿病;此外,橄榄苦苷还能缓解糖尿病肾病、心血管病变和视网膜病变等并发症[4]。橄榄苦苷已被研究证实具有显著的清除自由基和抗氧化活性,是一种有效的天然抗氧化剂[5]。橄榄苦苷还具有抗菌[6]、抗病毒[7]、保护心脏[8]和抗精神疾病[9]等多种生理活性。由于橄榄苦苷具有广泛的药理活性,该化合物在食品、医药、保健品和化妆品等领域应用日益广泛,其市场需求也随增长。橄榄苦苷作为油橄榄叶中的主要酚类化合物,已在地中海国家作为食品补充剂上市[10]。
油橄榄不同组织中橄榄苦苷的含量差异显著,其叶中橄榄苦苷的含量最高[11]。因此,目前橄榄苦苷主要是从油橄榄的叶片中进行提取。但植物提取法存在一定的局限性:一方面橄榄叶的供应受种植区域、季节和气候影响较大;另一方面提取效率低、耗时长、耗能大、纯化过程复杂,而且提取过程会使用大量的有机溶剂,易造成环境污染。利用微生物异源合成橄榄苦苷,不受自然条件的限制、生产周期短、产物纯度和一致性高,而且环境友好,是极具潜能的替代方案。天然产物的微生物异源合成,依赖于其生物合成途径的解析,然而目前橄榄苦苷的生物合成途径尚未完全解析。已有研究者推测了橄榄苦苷的完整合成途径[12],如图1所示。从牻牛儿基焦磷酸(geranylpyrophosphate,GPP)到木犀榄苷-11-甲酯(oleoside 11-methyl ester)生物合成途径中的酶已被鉴定[13-15],而从木犀榄苷-11-甲酯到橄榄苦苷的转化过程中所涉及的酶仍未被报道。挖掘橄榄苦苷合成途径中的关键酶,进一步解析橄榄苦苷的合成途径对于实现橄榄苦苷的微生物异源合成具有重要意义。
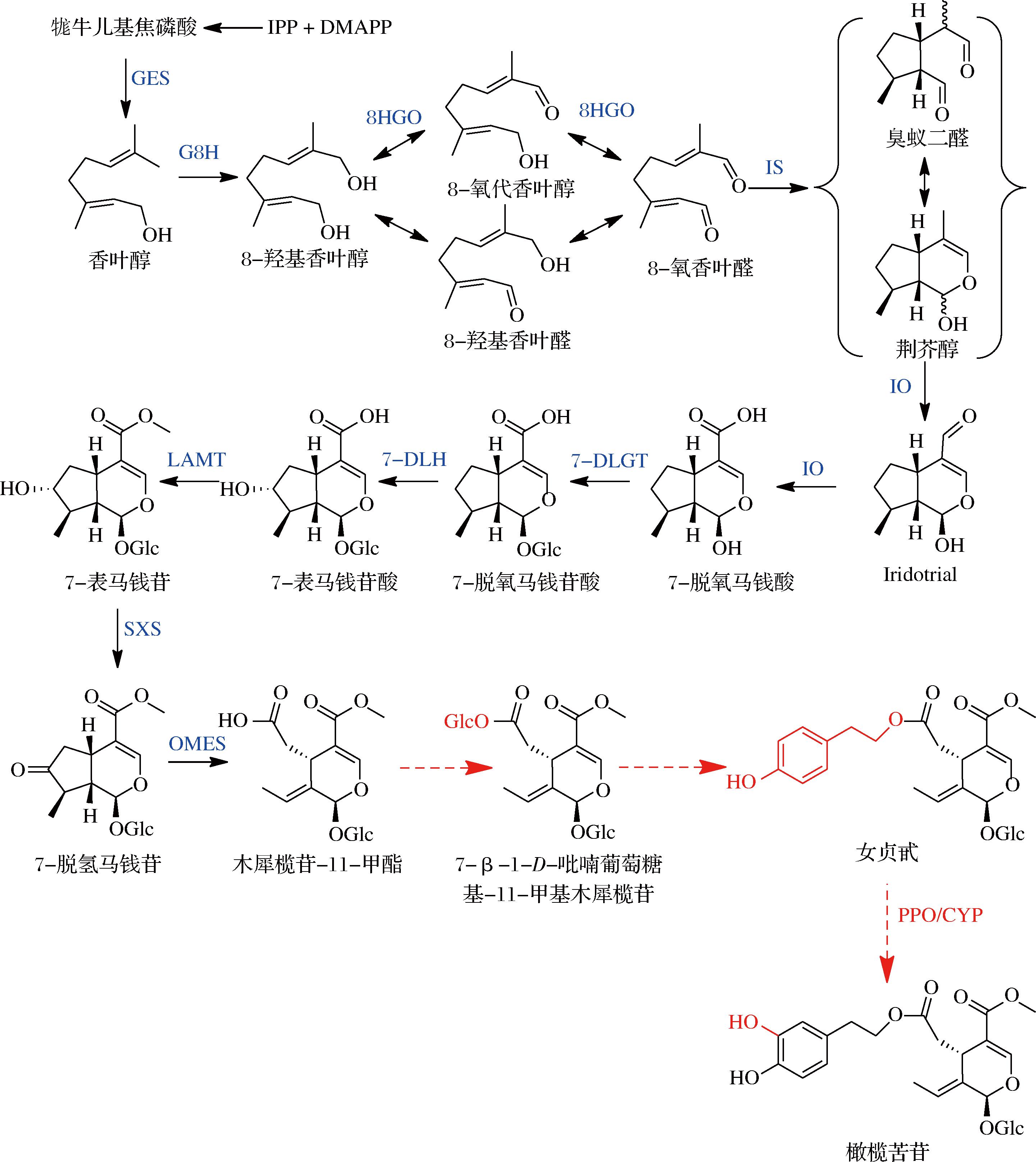
图1 推测的橄榄苦苷的生物合成途径[12]
Fig.1 The proposed biosynthetic pathway of oleuropein[12]
注:IPP,异戊烯基焦磷酸;DMAPP,二甲基烯丙基焦磷酸;GES,香叶醇合成酶;G8H,香叶醇8-羟化酶;8HGO,8羟基香叶醇氧化还原酶;IS,环烯醚萜合酶;IO,环烯醚萜氧化酶;7-DLGT,7-脱氧马钱酸-O-葡萄糖基转移酶;7-DLH,7-脱氧马钱苷酸7-羟化酶;LAMT,马钱苷酸氧甲基转移酶;SXS,断氧马钱苷合成酶;OMES,木犀榄苷甲酯合成酶。
从女贞甙到橄榄苦苷发生了羟基化反应,本研究推测此羟基化反应由多酚氧化酶(polyphenol oxidase,PPO)或细胞色素P450酶(cytochromeP450,CYP)催化完成。通过对油橄榄转录组数据的差异表达分析和共表达分析获得PPO的候选基因,对其进行异源表达,通过体外酶促反应验证候选基因的功能,并对目标PPO纯化后进行酶学性质探究。本研究进一步促进了橄榄苦苷生物合成途径的解析,提供了橄榄苦苷生物合成关键酶元件,为其他PPO的挖掘鉴定提供了参考。
1 材料与方法
1.1 材料
1.1.1 植物材料
油橄榄(Olea europaea L.)植株,甘肃省陇南市,并在实验室条件[(23±1)℃,16 h光照,8 h黑暗]下培养2~3月后进行实验。
1.1.2 菌株和质粒
DH5α和BL21(DE3)感受态细胞购自北京擎科生物科技股份有限公司,质粒pET-28a由本实验室保存。
1.1.3 培养基
Luria-Bertani(LB)液体培养基(g/L):酵母粉5,蛋白胨10,NaCl 10,121 ℃高压蒸汽灭菌20 min。
LB固体培养基(g/L):酵母粉5,蛋白胨10,NaCl 10,琼脂粉15,121 ℃高压蒸汽灭菌20 min。
1.1.4 试剂
高保真DNA聚合酶和One Step Cloning Kit,南京诺唯赞生物科技股份有限公司;限制性内切酶,赛默飞世尔科技有限公司;卡那霉素,北京科创欣达科技有限公司;BCA蛋白浓度测定试剂盒,北京索莱宝科技有限公司;IPTG、水杨酸、橄榄苦苷,上海阿拉丁生化科技股份有限公司;女贞甙、对香豆酸,上海源叶生物科技有限公司;红景天苷、对羟基苯甲酸、阿魏酸、异香兰酸、7-羟基-4-甲基香豆素,上海麦克林生化科技股份有限公司;酪醇,上海吉至生化科技有限公司;桂叶苷B,北京奇松生物科技有限公司;桂叶苷A由本实验室合成[16];琼脂糖凝胶DNA回收试剂盒、质粒小提试剂盒、普通DNA产物纯化试剂盒,天根生化科技有限公司。
1.1.5 仪器与设备
Mastercycler X40 PCR仪,德国Eppendorf公司;Mini-sub cell GT核酸电泳仪、Gel Doc XR+凝胶成像仪,Bio-Rad公司;ZQZY-78A恒温振荡摇床,上海知楚仪器有限公司;JY92-IIN超声波细胞破碎仪,宁波新芝生物科技股份有限公司;SpectraMax Mini酶标仪,Molecular Devices公司;LC-20AD高效液相色谱仪,岛津仪器有限公司;SQ810C立式压力蒸汽灭菌锅,上海申安医疗器械厂;1200高效液相色谱仪,安捷伦科技有限公司;Bruker micrOTOF-Q Ⅱ高分辨质谱仪,布鲁克·道尔顿公司。
1.2 实验方法
1.2.1 油橄榄中橄榄苦苷的提取和检测
从实验室培养3个月的油橄榄树上,剪取茎和叶,用蒸馏水洗净、烘干、研磨成粉,称取0.3 g粉末加入7.5 mL体积分数80%甲醇溶液(料液比1∶25),超声波萃取40 min,12 000 r/min离心5 min,经0.22 μm的有机相滤膜过滤后取1 mL滤液进行HPLC和LC-MS分析。
1.2.2 转录组测序及PPO候选基因的筛选
选取新鲜茎、叶各3份送至北京百迈客生物科技有限公司进行二代转录组测序。参考基因组为油橄榄基因组(GCA_902713445.1_OLEA9)。通过聚类、合并去冗余等生物信息学分析,初步筛选茎、叶组织间差异表达的PPO基因。使用TBtools软件将差异表达的PPO基因与已报道的参与橄榄苦苷生物合成途径的基因进行聚类共表达分析来确定候选基因。
1.2.3 PPO候选基因的克隆
以油橄榄的cDNA为模板,使用表1中的引物进行PCR扩增得到PPO候选基因的片段,使用无缝克隆技术将其与线性化载体pET-28a连接,将重组质粒pET-28a-PPO转化DH5a感受态细胞,菌落PCR方法筛选阳性克隆,提取质粒进行Sanger测序验证。
表1 本研究所使用的引物
Table 1 Primers used in this study

引物序列 (5′-3′)T7-FGCGAAATTAATACGACTCACTATAGT7-RAAAAAACCCCTCAAGACCCGA068152-FCGCGGCAGCCATATGGCTAGCATGCATTGCACAATATCTAACCA068152-RACGGAGCTCGAATTCGGATCCTTAGATAGAAAGATATATAAT-TTTGATACCACCA046766-FATGGGTCGCGGATCCGAATTCATGGCATCCATTGTTCCATTGA046766-RTTGTCGACGGAGCTCGAATTCTCAATCATCAAGTTCAATCTTGA046262-FATGGGTCGCGGATCCGAATTCATGGCTTCTTTTTGTGTAATTGCA046262-RTTGTCGACGGAGCTCGAATTCCTAGGTATCAAACTTAATGTTG
1.2.4 PPO候选基因的异源表达
将测序正确的pET-28a-PPO转化BL21(DE3)的感受态细胞,涂布在含有50 μg/mL卡那霉素的LB平板上,37 ℃过夜培养。挑取单菌落至含有50 μg/mL卡那霉素的5 mL LB液体培养基中,37 ℃、220 r/min过夜培养,获得种子液。随后,将种子液按照体积比1∶100转接至50 mL含相同抗生素的LB液体培养基中,37 ℃、220 r/min培养2~3 h,待培养液OD600值达到0.6~0.8时,加入IPTG至终浓度为0.1 mmol/L,16 ℃、220 r/min继续培养18 h,诱导蛋白的表达。收集菌体后用10 mL的Buffer C(50 mmol/L Tris-HCl,100 mmol/L NaCl,体积分数10%甘油,pH 7.5)重悬,超声波破碎10 min,离心获得上清液,进行粗酶反应。并采用SDS-PAGE方法对蛋白表达情况进行检测分析。
1.2.5 候选PPO的酶活验证
在100 μL的酶促反应体系中,包含87 μL粗酶液,其余各组分的终浓度分别为:0.2 mmol/L女贞甙、2 mmol/L十二烷基硫酸钠(sodium dodecyl sulfate,SDS)、2 μmol/L CuSO4·5H2O和2 mmol/L抗坏血酸。以空质粒pET-28a转化菌粗酶液作为阴性对照。30 ℃反应2 h,加入100 μL的甲醇终止反应。12 000 r/min 离心10 min,用0.22 μm的有机相滤膜过滤后,进行HPLC和LC-MS的分析。
1.2.6 蛋白纯化
培养1 L的菌液,4 000 r/min离心10 min收集菌体,去上清液,用适量的Buffer A(50 mmol/L Tris-HCl,20 mmol/L咪唑,100 mmol/L NaCl,体积分数10%甘油,pH 7.5)洗菌1次。50 mL Buffer A重悬,在冰浴中超声波破碎20 min(功率35%,运行3 s暂停2 s),4 ℃、12 000 r/min,离心30 min,获得上清液。将上清液分批加入平衡好的镍柱中,用60 mL的Buffer A洗涤杂蛋白,然后用10 mL含有不同浓度咪唑的缓冲液(50、100、150、200、300、500 mmol/L)进行梯度洗脱,分别收集洗脱液。不同浓度的咪唑缓冲液由Buffer B(50 mmol/L Tris-HCl,500 mmol/L咪唑,100 mmol/L NaCl,体积分数10%甘油,pH 7.5)和Buffer C配制而成。采用SDS-PAGE分析目的蛋白的洗脱情况,收集含目的蛋白的洗脱液,使用30 kDa截留分子质量的超滤离心管进行缓冲液置换(Buffer C)和样品浓缩。通过重复补加Buffer C和离心操作,最终将目的蛋白浓缩至1 mL,并采用BCA试剂盒测定蛋白浓度。
1.2.7 OePPO3酶学性质的探究
1.2.7.1 pH对OePPO3酶活性的影响
采用100 μL反应体系(含0.2 mmol/L女贞甙、2 mmol/L SDS、2 μmol/L CuSO4·5H2O、2 mmol/L抗坏血酸、10 μg纯酶及50 mmol/L缓冲液),分别以pH 4~5的柠檬酸-柠檬酸钠、pH 6~8的PBS和pH 9的Tris-HCl缓冲液构建pH梯度。30 ℃反应2 h后,加入100 μL甲醇终止反应,12 000 r/min,离心10 min,用0.22 μm的有机相滤膜过滤后,进行HPLC分析。
1.2.7.2 温度对OePPO3酶活性的影响
在50 mmol/L PBS(pH 6)体系中,考察0~40 ℃温度梯度(0、10、20、30、40 ℃)对酶活力的影响,其余反应条件同1.2.7.1节,反应终止后按相同方法处理样品并检测。
为探究OePPO3的热稳定性,参考文献[17]中的方法,将酶液在不同温度(10、30、50、70、80、90 ℃)下分别保温10、30 min,再分别测定不同保温时间下残余的酶活力,将初始酶活力定为100%,分别计算相对酶活力。
1.2.7.3 OePPO3动力学参数的测定
在最适pH和温度条件下,固定体系中的SDS(2 mmol/L)、CuSO4·5H2O(2 μmol/L)、抗坏血酸(2 mmol/L)及纯酶量(5 μg),调节女贞甙浓度(0.02~1.5 mmol/L),反应10 min后终止反应,进行HPLC检测分析。计算不同底物浓度条件下的反应初速度,采用软件GraphPad Prism 8进行非线性回归分析,获得动力学参数Km、kcat和kcat/Km。
1.2.7.4 OePPO3的底物谱
OePPO3能够催化底物女贞甙中酪醇基团的苯环邻位羟化反应,从而生成橄榄苦苷。为研究其底物宽泛性,本研究筛选了对香豆酸、酪醇、红景天苷、桂叶苷A、桂叶苷B、7-羟基-4-甲基香豆素、阿魏酸、异香兰酸、对羟基苯甲酸和水杨酸共10种单酚类底物进行OePPO3的底物谱测试。在酶的最适反应条件下,反应2 h。以未加酶体系为阴性对照,通过HPLC和LC-MS分析催化产物。
1.2.8 系统发育分析
本研究采用MEGA11软件对OePPO3及其他植物来源的PPO进行系统发育分析,分析其进化关系。多序列比对使用ClustalW算法构建,基于比对结果,运用邻接法(neighbor-joining,NJ)构建系统发育树,并通过1 000次重复的Bootstrap检验评估分支节点支持率。
1.2.9 HPLC和LC-MS分析
油橄榄茎和叶提取物的HPLC检测方法:C18反向色谱柱(4.6 mm×250 mm,5 μm);流动相A为体积分数0.1%甲酸溶液;流动相B为乙腈;流速1 mL/min,柱温40 ℃;梯度洗脱条件:0~5 min,5% B;5~45 min,5%~100% B;45~55 min,100% B;55~55.5 min,100%~5% B;55.5~65 min,5% B。
酶促反应液的HPLC检测方法:C18反向色谱柱(4.6 mm×250 mm,5 μm),流动相A为体积分数0.1%甲酸溶液;流动相B为甲醇,流速1 mL/min,柱温40 ℃。梯度洗脱条件是:0~5 min,5% B;5~45 min,5%~100% B;45~55 min,100% B;55~56 min,100%~5% B;56~62 min,5% B。
LC-MS检测方法:HPLC条件与上述相同,质谱检测采用正离子监测模式,在m/z 50~1 000范围内进行全扫描采集。
1.3 数据处理分析
实验重复3次,结果以“平均值±标准差”表示,使用Origin 2024和GraphPad Prism 8软件进行绘图。
2 结果与分析
2.1 油橄榄中橄榄苦苷的提取和检测
对油橄榄新鲜茎和叶中橄榄苦苷进行检测。HPLC的结果如图2-a所示,油橄榄的茎和叶中均存在与橄榄苦苷标准品保留时间一致的化合物,其中叶中含量显著高于茎中,并对其进行LC-MS检测,结果如图2-b所示,该化合物出现特征峰[M+H]+的m/z为541.191 6,[M+Na]+的m/z为563.174 0,与橄榄苦苷的理论分子质量一致。因此购买的油橄榄中含有橄榄苦苷,其叶中含量显著高于茎中,后续对油橄榄的茎和叶进行转录组测序。
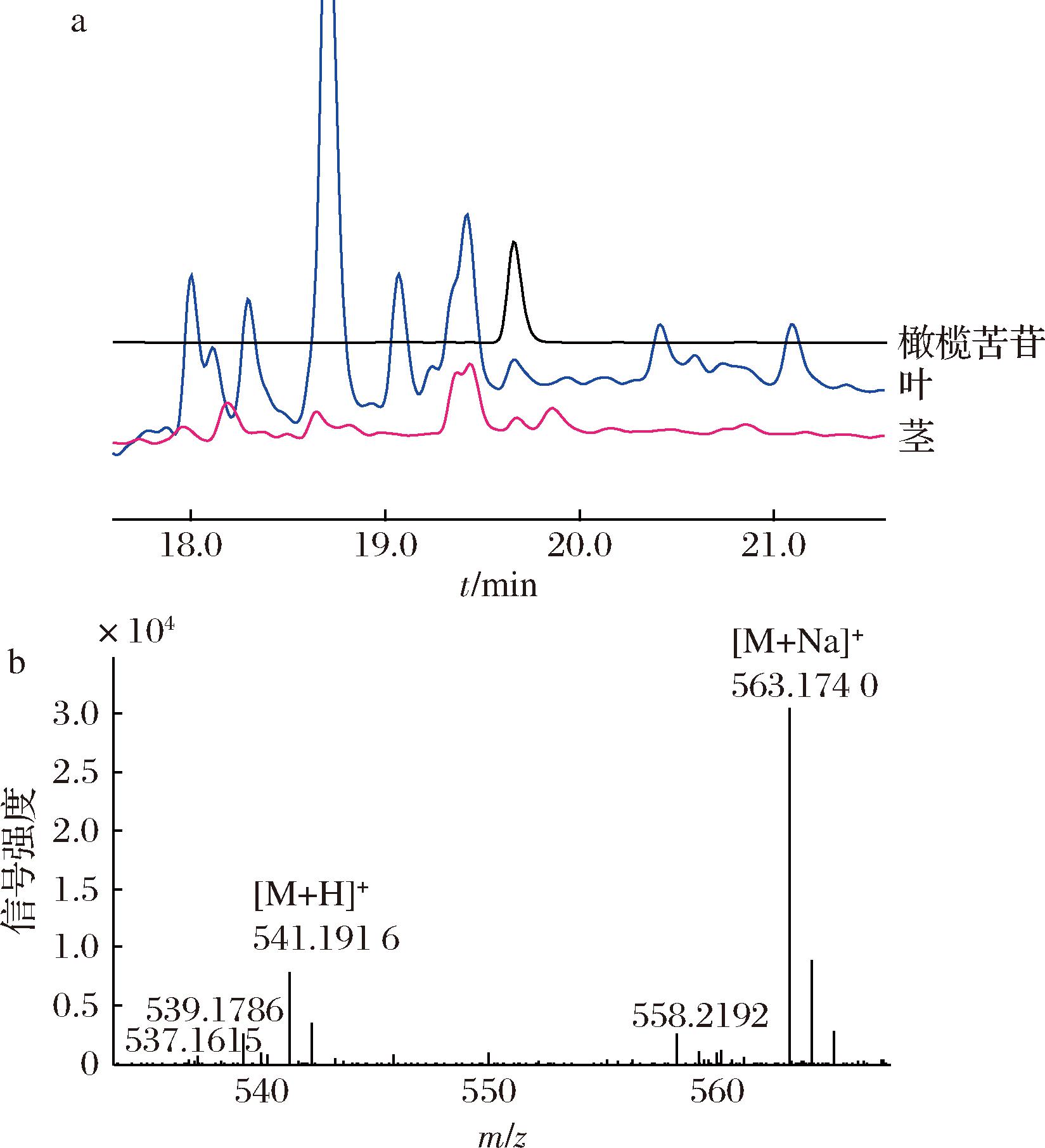
a-HPLC分析;b-LC-MS分析
图2 油橄榄茎和叶萃取物的HPLC和LC-MS分析
Fig.2 HPLC and LC-MS analysis of extracts from O. europaea stems and leaves
2.2 PPO候选基因的筛选
基于差异表达分析筛选出在茎、叶中差异表达的8个PPO,将这8个PPO与已报道的参与橄榄苦苷生物合成途径的其他基因进行聚类共表达分析。如图3所示,发现2个基因A046262、A068152与8个已经报道的参与橄榄苦苷生物合成途径的基因(OeIO[15]、OeSXS[14]、OeISY-1[15]、Oe1,4-R[15]、Oe8HGO[15]、OeISY-2[15]、OeLAMT[15]和Oe7-DLGT[15])具有相似的表达模式;另外发现A046766与3个已经报道的橄榄苦苷生物合成途径中的基因(OeMES[14]、Oe7-DLH-like[15]和Oe7-DLH-like2[15]),具有相似的表达模式,所以推测A046262、A068152和A046766可能参与橄榄苦苷的生物合成途径,将这3个基因作为候选基因,进行后续的研究。
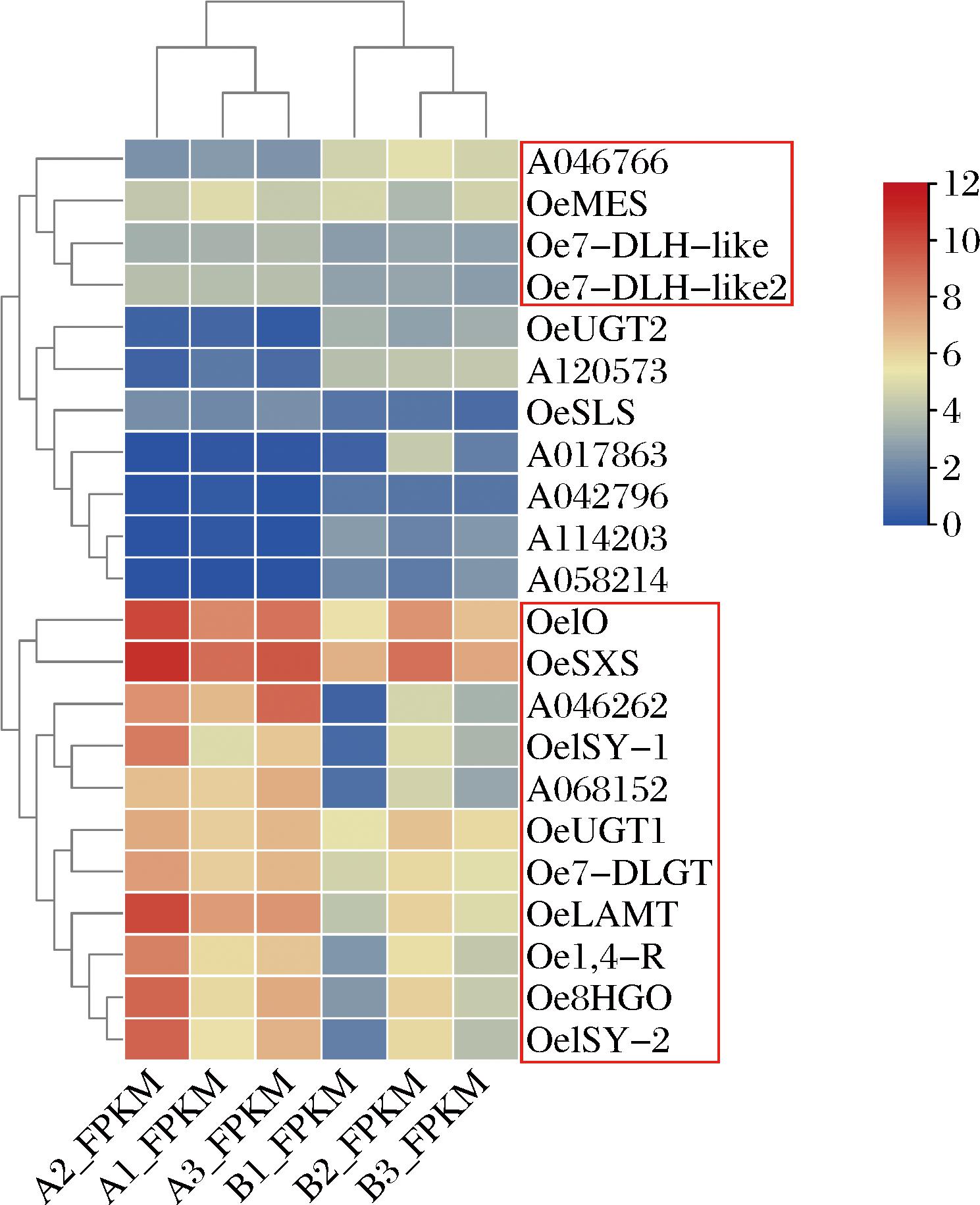
图3 PPO候选基因和报道的橄榄苦苷生物合成途径基因的聚类共表达分析
Fig.3 Cluster co-expression analysis of PPO candidate genes and reported oleuropein biosynthesis pathway genes
2.3 PPO候选基因的异源表达
如图4所示,A068152、A046766和A046262的全细胞裂解液和上清液在约70 kDa的位置都有蛋白条带,且目标条带大小与实验预期相符;A068152和A046262的蛋白条带较浅,表明蛋白的表达量较低,A046766在全细胞裂解液和上清液中的蛋白条带都比较明显,表明A046766的表达量较高且可溶性表达较好。
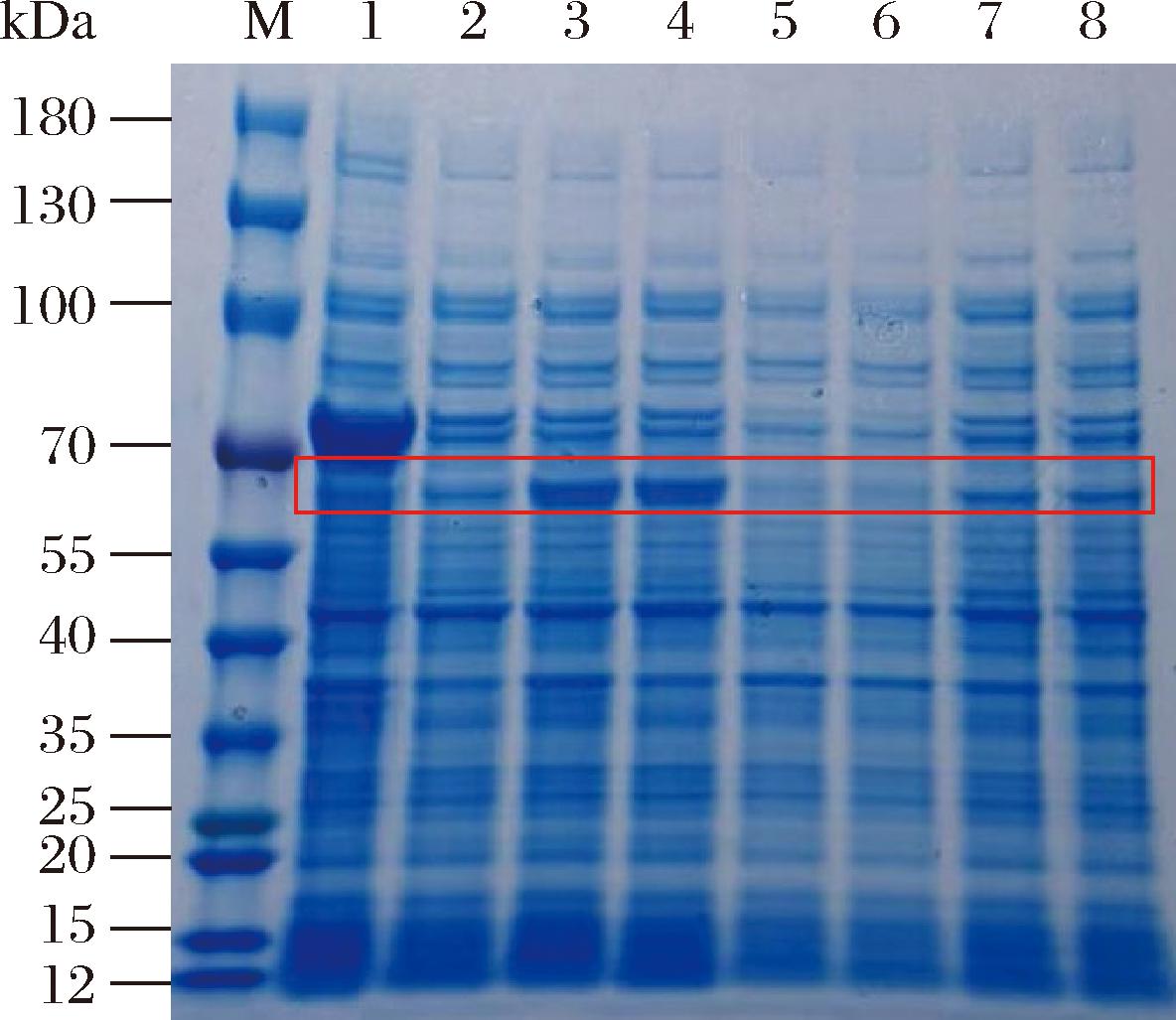
M-Marker;1~2-A068152的全细胞、上清液;3~4-A046766的全细胞、上清液;5~6-pET-28a的全细胞、上清液;7~8-A046262的全细胞、上清液。
图4 候选PPO蛋白表达的SDS-PAGE分析
Fig.4 SDS-PAGE analysis of candidate PPO protein expression
2.4 候选PPO的功能鉴定
将这3个候选PPO按照1.2.5节中的方法进行体外粗酶反应,验证其功能。如图5-a所示,与对照相比,候选多酚氧化酶A046766催化底物女贞甙产生了一个新峰,并且新峰与橄榄苦苷标准品出峰时间一致,推测其为橄榄苦苷,而A068152和A046262并没有新峰出现。为了进一步验证新峰对应的化合物是否为橄榄苦苷,对其进行LC-MS分析,如图5-b所示,该化合物出现特征峰[M+H]+的m/z为541.191 3,[M+Na]+的m/z为563.174 5,与橄榄苦苷的理论分子质量一致,因此可以确定新峰对应的化合物为橄榄苦苷。A046766即为目标多酚氧化酶,由584个氨基酸残基组成,编码基因长度为1 755 bp。S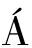 NCHEZ等[18]研究发现油橄榄来源的多酚氧化酶OePPO3,通过氨基酸序列比对发现其与本研究中的A046766仅相差7个氨基酸残基。本研究初步认定A046766与文献中的OePPO3为同一个酶,S
NCHEZ等[18]研究发现油橄榄来源的多酚氧化酶OePPO3,通过氨基酸序列比对发现其与本研究中的A046766仅相差7个氨基酸残基。本研究初步认定A046766与文献中的OePPO3为同一个酶,S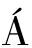 NCHEZ等[18]仅定性其属于酪氨酸酶,并未测定其对女贞甙的催化活性,也未证明其参与橄榄苦苷的生物合成途径。后续对OePPO3(A046766)进行了蛋白纯化,并采用SDS-PAGE分析蛋白的纯化情况,如图5-c所示,经过镍柱纯化后的蛋白条带较为单一,采用BCA试剂盒测定蛋白浓度,用于后续纯酶反应。
NCHEZ等[18]仅定性其属于酪氨酸酶,并未测定其对女贞甙的催化活性,也未证明其参与橄榄苦苷的生物合成途径。后续对OePPO3(A046766)进行了蛋白纯化,并采用SDS-PAGE分析蛋白的纯化情况,如图5-c所示,经过镍柱纯化后的蛋白条带较为单一,采用BCA试剂盒测定蛋白浓度,用于后续纯酶反应。
M-Marker;1~2-OePPO3的全细胞、上清液;3-镍柱纯化的OePPO3蛋白。
a-候选PPO粗酶反应的HPLC分析;b-新峰的LC-MS的分析;c-纯化的OePPO3的SDS-PAGE分析
图5 候选PPO的功能鉴定和OePPO3的蛋白纯化
Fig.5 Functional identification of candidate PPO and protein purification of OePPO3
2.5 OePPO3酶学性质的探究
2.5.1 pH对OePPO3酶活性的影响
以女贞甙为底物,以SDS和Cu2+作为激活剂,以抗坏血酸作为抑制剂,系统探究了OePPO3在不同pH条件下的催化活性。如图6-a所示,pH对OePPO3的催化活性影响较为显著,在pH 6的PBS体系中表现出最高底物转化率,表明该酶的最适反应pH值为6;当pH值偏离6时,酶活性显著降低,当pH值为4和9时,酶催化底物的转化率降低到了5%以下。
a-pH对OePPO3酶活性的影响;b-OePPO3的最适温度;c-OePPO3的热稳定性;d-OePPO3催化女贞甙的动力学曲线
图6 pH、温度对OePPO3酶活性的影响和OePPO3催化女贞甙的动力学曲线
Fig.6 Effects of pH and temperature on the enzyme activity of OePPO3 and the kinetic curve of OePPO3 catalyzing ligstroside
2.5.2 温度对OePPO3酶活性的影响
在最适pH下探究OePPO3的最适温度,结果如图6-b所示。当温度为0~10 ℃的时候底物的转化率较高,其中10 ℃时转化率最高,达到83%;随着反应温度从10 ℃升高至40 ℃,底物转化率逐渐降低,酶的催化活性呈显著下降趋势。这一现象表明低温条件下酶具有较高的催化活性,在较高温度下反而会使酶的催化活性降低,推测这可能是由于高温环境导致多酚氧化酶的构象改变或稳定性降低,从而显著影响酶的催化效率,而低温环境使多酚氧化酶的结构更稳定,活性也更高。
将OePPO3置于不同温度下保温一段时间后,测定其酶活力,分析其热稳定性,如图6-c所示。OePPO3≤70 ℃时比较稳定,70 ℃保温30 min,其残余酶活力约为78%。80 ℃时酶稳定性急剧下降,80 ℃保温10 min,其残余酶活力仅有约12%,90 ℃时酶基本失活,说明OePPO3的热稳定性相对较高。
2.5.3 OePPO3酶促动力学参数分析
在最适pH 6和最适温度10 ℃的条件下,进一步探究了OePPO3催化女贞甙的动力学参数。动力学曲线如图6-d所示,OePPO3对女贞甙的米氏常数(Km)为(0.82±0.15) mmol/L,催化常数(kcat)为(17.18±1.53) min-1,催化效率(kcat/Km)达到(20.95±4.22) L/(mmol·min)。
2.5.4 OePPO3底物谱分析
在最适反应条件下,探究OePPO3的底物特异性,结果如图7和图8所示。OePPO3对红景天苷(1)、对香豆酸(2)、酪醇(3)、桂叶苷A(4)、桂叶苷B(5)和7-羟基-4-甲基香豆素(6)均表现出催化活性,催化其产生了新峰,然后分别对新峰进行LC-MS分析鉴定其分子质量。HPLC和LC-MS分析结果表明,OePPO3能够催化红景天苷(1)、对香豆酸(2)、酪醇(3)和7-羟基-4-甲基香豆素(6)发生邻位羟化,分别生成3,4-二羟基苯乙醇葡萄糖苷(1a)、咖啡酸(2a)、羟基酪醇(3a)和6,7-二羟基-4-甲基香豆素(6a);值得注意的是,在催化桂叶苷A(4)和桂叶苷B(5)的转化过程中,OePPO3表现出逐步羟基化的特性,分别生成木通苯乙醇苷A(4a)和毛蕊花糖苷(5a),同时检测到单侧邻位羟化的中间体(4b、5b和5c)。这些结果表明,OePPO3具有一定的底物宽泛性,对多种酚类化合物均具有催化活性,能够选择性地在苯环邻位引入羟基,从而拓展其潜在应用价值。
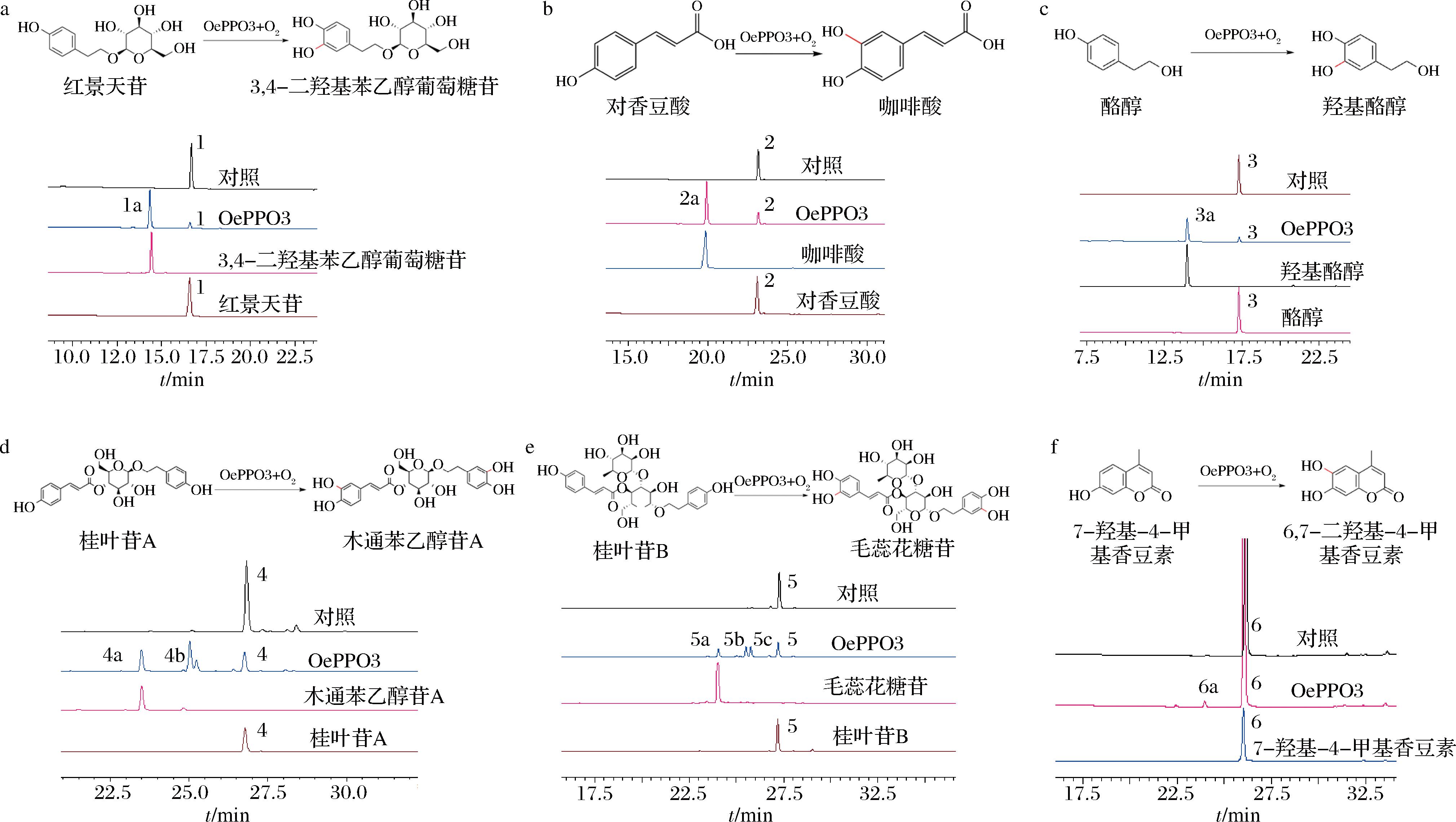
a-红景天苷;b-对香豆酸;c-酪醇;d-桂叶苷A;e-桂叶苷B;f-7-羟基-4-甲基香豆素
图7 OePPO3催化不同底物羟化反应的HPLC分析
Fig.7 HPLC analysis of OePPO3-catalyzed hydroxylation reactions of various substrates
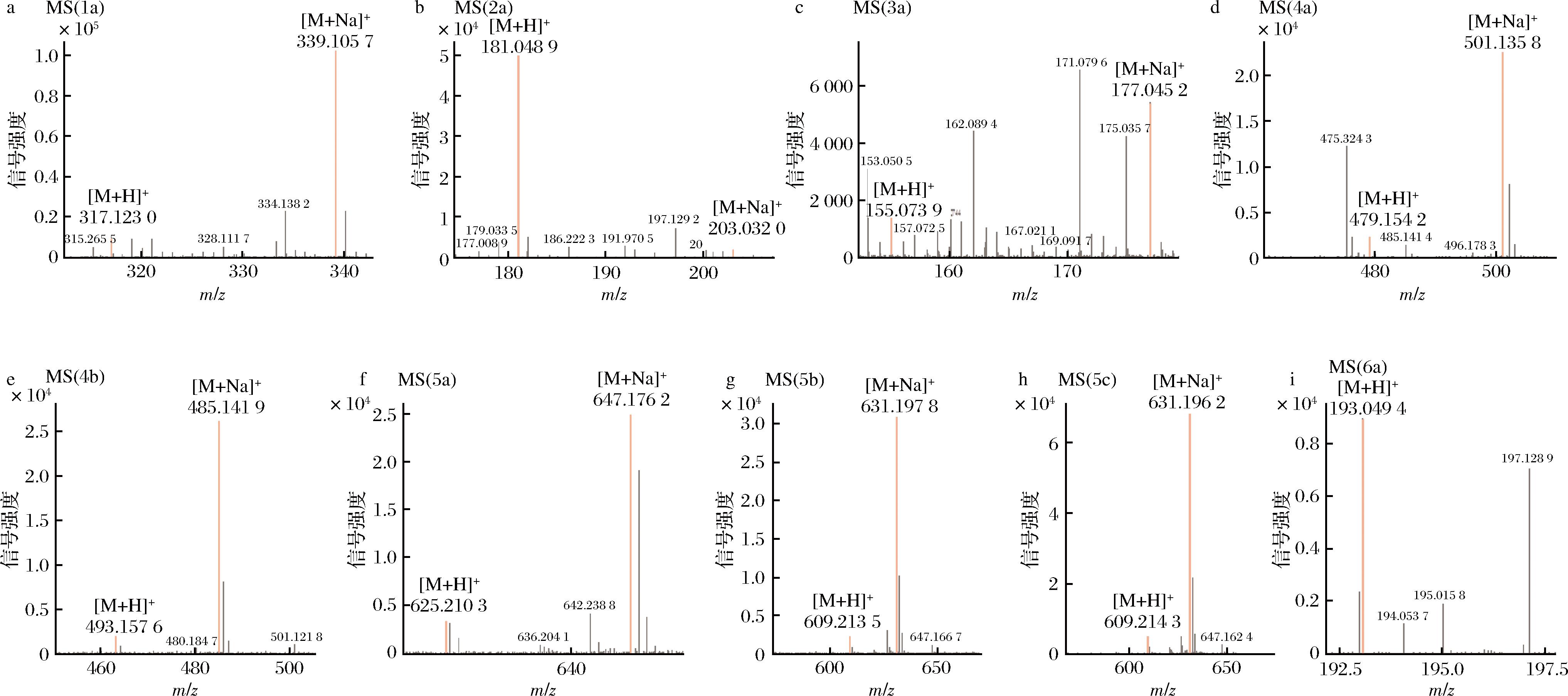
a-1a;b-2a;c-3a;d-4a;e-4b;f-5a;g-5b;h-5c;i-6a
图8 OePPO3催化不同底物形成相应的羟基化产物的LC-MS分析
Fig.8 LC-MS analysis of hydroxylated products formed by OePPO3-catalyzed reactions with different substrates
2.6 系统发育分析
为了深入研究OePPO3的系统进化关系,采用MEGA11软件中的邻接法,将其与其他植物来源的PPO进行系统发育分析,构建系统发育树,结果如图9所示。OePPO3与4个酪氨酸酶(OfPPO2[19]、AmAS1[20]、ToPPO1[21]和ToPPO2[21])聚集在同一个小的分支上,其中OePPO3与桂花(Osmanthus fragrans)来源的OfPPO2具有较近的亲缘关系,它们的功能也极为相似,OfPPO2能够羟基化酪氨酸、酪醇、酪胺、4-羟基苯乙醛、红景天苷和桂叶苷A等多种单酚类底物,生成相应的邻苯二酚类中间体,从而参与毛蕊花糖苷的生物合成。
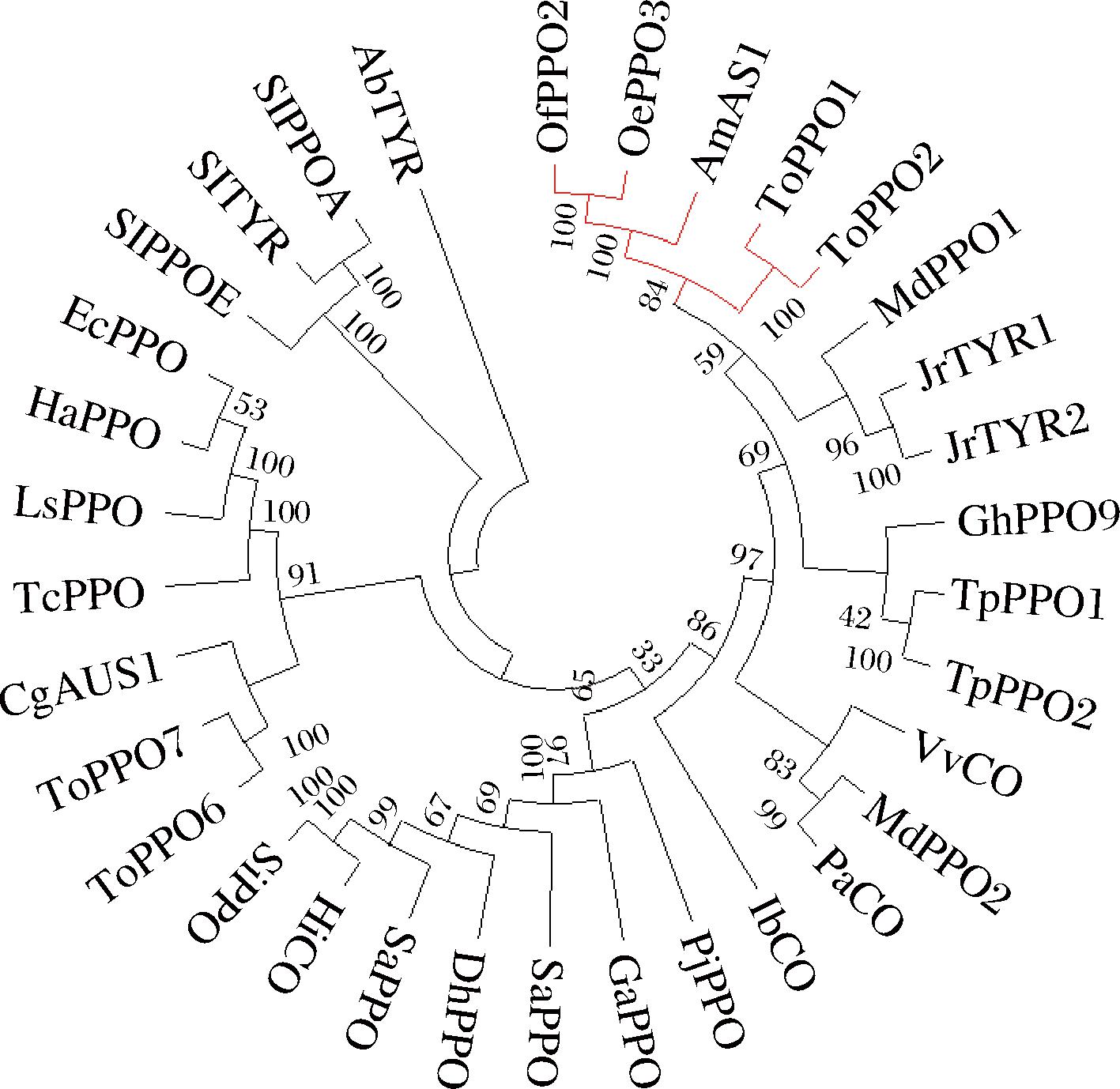
图9 OePPO3和其他植物来源的PPO的系统发育树分析
Fig.9 Phylogenetic tree analysis of OePPO3 and other plant-derived PPO
注:HiCO(PIN03650.1)、SiPPO(NP_001304907.1)、SaPPO(GER45097.1)、DhPPO(KZV45880.1)、SsPPO(XP_042058840.1)、GaPPO(EPS59410.1)、TcPPO(GEV51020.1)、HaPPO(XP_021989494.1)、PjPPO(GFP78722.1)、EcPPO(XP_043626822.1)、LsPPO(XP_023763958.1)、GhPPO9(NP_001314636.1)、SlTYR(Q08303.2)、AbTYR(C7FF05.1)、MdPPO1(NP_001306190.1)、MdPPO2(AAK56323.1)、JrTYR1(ACN86310.1)、JrTYR2(XP_018805282.2)、AmAS1(BAB20048.1)、VvCO(P43311.1)、IbCO(XP_031123625.1)、SIPPOE(Q08307)、SIPPOA(Q08303)、PaCO(O81103.1)、CgAUS1(AHN09736.1)、ToPPO1(ABX09994.1)、ToPPO2(CAQ76694.1)、ToPPO6(CCA94610.1)、ToPPO7(CCD61123.1)、 TpPPO1(AAK13242.1)、TpPPO2(AAK13243.1)。
3 结论与讨论
本研究基于转录组数据分析、基因异源表达和体外酶活性验证,从油橄榄转录组中成功鉴定出一个参与橄榄苦苷生物合成的关键多酚氧化酶OePPO3(A046766),该酶能够催化女贞甙转化为橄榄苦苷,为橄榄苦苷生物合成途径的解析提供了重要线索,更为后续利用微生物细胞工厂实现橄榄苦苷的异源合成提供了重要的酶功能元件。
OePPO3还展现出一定的底物宽泛性,能够催化红景天苷、桂叶苷A、桂叶苷B等多种单酚类化合物生成相应的邻苯二酚类中间体,表明其在植物苯丙烷类代谢途径中具有潜在的多功能催化作用,同时也为其他具有邻二酚羟基结构天然产物的酶法合成提供了新催化工具。
值得注意的是,在以女贞甙为底物时,OePPO3的最适反应温度为10 ℃,低于植物PPO通常报道的最适温度范围(15~50 ℃)[22]。另外,菠萝蜜来源的PPO也是一个例外,在使用邻苯二酚和4-甲基邻苯二酚为底物时,其最适反应温度为8 ℃[23]。OePPO3的低温生物催化特性使其适用于温度敏感型药物中间体的合成及低温环境生物传感器的构建,未来研究可通过解析酶结构与低温适应性的分子机制,结合代谢工程或化学修饰技术提升其工业适用性,从而推动该酶在绿色制造领域的实际应用。
[1] 韦奎丞, 黄晖, 白宇.橄榄苦苷对人骨肉瘤MG-63细胞的增殖抑制和诱导凋亡[J].河北医药, 2024, 46(18):2828-2831.
WEI K C, HUANG H, BAI Y.Inhibitory effect of oleuropein on proliferation and apoptosis of human osteosarcoma MG-63 cells[J].Hebei Medical Journal, 2024, 46(18):2828-2831.
[2] ASGHARZADE S, SHEIKHSHABANI S H, GHASEMPOUR E, et al.The effect of oleuropein on apoptotic pathway regulators in breast cancer cells[J].European Journal of Pharmacology, 2020, 886:173509.
[3] PRZYCHODZEN P, KUBAN-JANKOWSKA A, WYSZKOWSKA R, et al.PTP1B phosphatase as a novel target of oleuropein activity in MCF-7 breast cancer model[J].Toxicology in Vitro, 2019, 61:104624.
[4] ZHENG S J, HUANG K L, TONG T.Efficacy and mechanisms of oleuropein in mitigating diabetes and diabetes complications[J].Journal of Agricultural and Food Chemistry, 2021, 69(22):6145-6155.
[5] BENAVENTE-GARC A O, CASTILLO J, LORENTE J, et al.Antioxidant activity of phenolics extracted from Olea europaea L.leaves[J].Food Chemistry, 2000, 68(4):457-462.
A O, CASTILLO J, LORENTE J, et al.Antioxidant activity of phenolics extracted from Olea europaea L.leaves[J].Food Chemistry, 2000, 68(4):457-462.
[6] SOMERVILLE V, MOORE R, BRAAKHUIS A.The effect of olive leaf extract on upper respiratory illness in high school athletes:A randomised control trial[J].Nutrients, 2019, 11(2):358.
[7] MA S C, HE Z D, DENG X L, et al.In vitro evaluation of secoiridoid glucosides from the fruits of Ligustrum lucidum as antiviral agents[J].Chemical &Pharmaceutical Bulletin, 2001, 49(11):1471-1473.
[8] XING C H, XU L, YAO Y J.Beneficial role of oleuropein in sepsis-induced myocardial injury.Possible involvement of GSK-3β/NF-kB pathway[J].Acta Cirurgica Brasileira, 2021, 36(1):e360107.
[9] MIKAMI T, KIM J, PARK J, et al.Olive leaf extract prevents obesity, cognitive decline, and depression and improves exercise capacity in mice[J].Scientific Reports, 2021, 11:12495.
[10] 吴倩. 橄榄苦苷对皮肤的生物活性研究进展[J].香料香精化妆品, 2023(5):52-58;150.
WU Q.Research progress in bioactivity of oleuropein on skin[J].Flavour Fragrance Cosmetics, 2023(5):52-58;150.
[11] 杨春苗, 刘雨萌, 杨东生.油橄榄叶的化学成分及其在化妆品领域的研究进展[J].广东化工, 2022, 49(22):103-104;87.
YANG C M, LIU Y M, YANG D S.Research progress on chemical constituents of Olea europaea leaves and application in the field of cosmetics[J].Guangdong Chemical Industry, 2022, 49(22):103-104;87.
[12] KOUDOUNAS K, THOMOPOULOU M, RIGAKOU A, et al.Silencing of oleuropein β-glucosidase abolishes the biosynthetic capacity of secoiridoids in olives[J].Frontiers in Plant Science, 2021, 12:671487.
[13] 戴欣怡, 朱锦峰, 韦善屹, 等.药用植物裂环烯醚萜苷类化合物生物合成途径关键酶基因研究进展[J].西北植物学报, 2023, 43(3):527-538.
DAI X Y, ZHU J F, WEI S Y, et al.Research progress of key enzyme genes in biosynthetic pathway of schizoiridoid glycosides in medicinal plants[J].Acta Botanica Boreali-Occidentalia Sinica, 2023, 43(3):527-538.
[14] RODR GUEZ-L
GUEZ-L PEZ C E, HONG B K, PAETZ C, et al.Two bi-functional cytochrome P450 CYP72 enzymes from olive (Olea europaea) catalyze the oxidative C-C bond cleavage in the biosynthesis of secoxy-iridoids-flavor and quality determinants in olive oil[J].New Phytologist, 2021, 229(4):2288-2301.
PEZ C E, HONG B K, PAETZ C, et al.Two bi-functional cytochrome P450 CYP72 enzymes from olive (Olea europaea) catalyze the oxidative C-C bond cleavage in the biosynthesis of secoxy-iridoids-flavor and quality determinants in olive oil[J].New Phytologist, 2021, 229(4):2288-2301.
[15] ALAGNA F, GEU-FLORES F, KRIES H, et al.Identification and characterization of the iridoid synthase involved in oleuropein biosynthesis in olive (Olea europaea) fruits[J].Journal of Biological Chemistry, 2016, 291(11):5542-5554.
[16] YANG Y H, XI D Y, WU Y N, et al.Complete biosynthesis of the phenylethanoid glycoside verbascoside[J].Plant Communications, 2023, 4(4):100592.
[17] 杨昌鹏, 胡艳妮, 陈智理, 等.杨桃多酚氧化酶的部分纯化及其特性研究[J].食品与发酵工业, 2010, 36(1):34-38.
YANG C P, HU Y N, CHEN Z L, et al.Partial purification and characterization of polyphenol oxidase from carambola[J].Food and Fermentation Industries, 2010, 36(1):34-38.
[18] S NCHEZ R, ARROYO L, LUACES P, et al.Olive polyphenol oxidase gene family[J].International Journal of Molecular Sciences, 2023, 24(4):3233.
NCHEZ R, ARROYO L, LUACES P, et al.Olive polyphenol oxidase gene family[J].International Journal of Molecular Sciences, 2023, 24(4):3233.
[19] LIU Y T, HAN X Y, ZHAO M Y, et al.Functional characterization of polyphenol oxidase OfPPO2 supports its involvement in parallel biosynthetic pathways of acteoside[J].The Plant Journal, 2024, 119(2):927-941.
[20] NAKAYAMA T, YONEKURA-SAKAKIBARA K, SATO T, et al.Aureusidin synthase:A polyphenol oxidase homolog responsible for flower coloration[J].Science, 2000, 290(5494):1163-1166.
[21] WAHLER D, GRONOVER C S, RICHTER C, et al.Polyphenoloxidase silencing affects latex coagulation in Taraxacum species[J].Plant Physiology, 2009, 151(1):334-346.
[22] ZHANG S.Recent advances of polyphenol oxidases in plants[J].Molecules, 2023, 28(5):2158.
[23] TAO Y M, YAO L Y, QIN Q Y, et al.Purification and characterization of polyphenol oxidase from jackfruit (Artocarpus heterophyllus) bulbs[J].Journal of Agricultural and Food Chemistry, 2013, 61(51):12662-12669.