随着苹果种植面积及产量的增长,苹果加工产业逐渐兴起,同时也产生了大量的副产物。苹果皮是苹果加工过程中的主要副产物,苹果皮中酚类、黄酮类、矿物质等营养成分含量丰富,总膳食纤维(total dietary fiber, TDF)含量高达70 g/100 g[1],其中包含可溶性膳食纤维(soluble dietary fiber, SDF)和不溶性膳食纤维(insoluble dietary fiber,IDF)。苹果皮的SDF被认为是一种高品质的膳食纤维,具有降低肠道炎症、调节肠道菌群以及提高机体抗氧化能力的功效[2],是一种优质天然膳食纤维的来源,具有极高的加工潜力。目前仅有小部分苹果皮被用来制作动物饲料、生产食用菌培养基等,绝大部分苹果皮被丢弃[3],造成环境污染和资源浪费,因此开发苹果皮产品,深入研究苹果皮精深加工技术十分有必要。
苹果皮可作为膳食纤维补充剂和功能性食品加工辅料,干制后更易贮存和运输。目前,食品加工业中干制方法常选用成本低且操作便捷的热风干燥,但该方法对食品品质有一定不良影响。而真空冷冻干燥通过升华去除食品中的水分,有利于食品中营养成分和基本性状的保持。此外,微生物发酵技术手段能够提高苹果的营养、功能和感官特性。有研究表明,利用益生菌发酵苹果汁,总酚、类黄酮以及挥发性酯类物质种类及含量均有所增加,抗氧化能力显著提高,并极大丰富果汁风味[4]。目前,微生物发酵技术多应用于苹果果汁产品,但苹果皮中的营养成分,除膳食纤维以外,酚类、烷醇类等含量甚至高于苹果果肉[5],所以利用微生物发酵苹果皮来开发功能性食品、天然食品营养补充剂等具有极高的发展前景。
体外模拟消化通过模仿口腔、胃和肠道的消化环境,更易于分析食物分解和变化规律,具有可重复性强、易操作的特点[6]。本研究以苹果皮为研究对象,探究植物乳植杆菌发酵对不同干燥方式的苹果皮的影响,分析干燥后苹果皮粉的色泽、堆积密度、流动性等粉质特性变化,利用体外消化模拟实验分析总酚、膳食纤维和抗氧化能力的变化规律,为苹果资源的充分利用和苹果食品精深加工提供理论依据。
1 材料与方法
1.1 材料与试剂
1.1.1 实验材料
红富士苹果,市售;植物乳植杆菌(Lactiplantibacillus plantarum)LNJ-HQ-01,实验室自主筛选。
1.1.2 实验试剂
植物总酚试剂盒、羟自由基(·OH)测定试剂盒、总抗氧化能力试剂盒、DPPH自由基清除能力试剂盒,上海化邦生物科技有限公司;胃蛋白酶、胰酶、α-淀粉酶、牛胆盐(胆酸含量≥75 g/100 g),上海麦克林生化科技股份有限公司;其余试剂均为实验室常用分析纯试剂。
1.2 仪器与设备
Slxfa-sn全自动酶标仪,美国伯腾仪器有限公司;Freezone2.5真空冷冻干燥机,北京照生行仪器设备有限公司;RT-N12尘式粉碎机,荣聪精密科技有限公司;PN-48A白度颜色测定仪,杭州品享科技有限公司;Sartorius MA150水分测定仪,赛多利斯科学仪器(北京)有限公司;ZQPW-70全温振荡培养箱,天津市莱波特瑞仪器设备有限公司。
1.3 实验方法
1.3.1 菌种活化
缓冻后的菌种按0.02 g/mL接种量接种到MRS液体培养基中,培养温度30 ℃,培养24 h,此步骤重复2次,使菌体浓度达到109 CFU/mL。
1.3.2 苹果皮粉制作流程
苹果清洗干净,削皮,控制苹果皮附着果肉厚度为0.5~1 mm,加入苹果皮质量2~3倍的无菌水,按体积分数2%接种活化后的菌液,室温发酵2周,沥干水分即得到发酵苹果皮,另取1组不接种菌液作为未发酵苹果皮对照组。
热风干燥(热干):将发酵苹果皮均匀铺在干燥托盘中,70 ℃烘干4 h,风速2.5 m/s,得到发酵热干苹果皮,同时设置未发酵热干苹果皮为对照组。
真空冷冻干燥(冻干):将发酵苹果皮于-80 ℃预冻24 h后均匀铺平在冻干托盘中,真空度为0.01 kPa,-58 ℃冷阱温度,冻干48 h得到发酵冻干苹果皮,同时设置未发酵冻干苹果皮为对照组。
利用尘式粉碎机将4组干燥后的苹果皮分别粉碎5 min,过80目筛,得到发酵热干苹果皮粉(F-H)、未发酵热干苹果皮粉(N-H)、发酵冻干苹果皮粉(F-F)、未发酵冻干苹果皮粉(N-F),密封保存备用。
1.3.3 水分含量的测定
准确称取0.1 g样品,利用水分测定仪直接测量水分含量。
1.3.4 堆积密度和振实密度的测定
1.3.4.1 堆积密度
称取2 g样品,缓慢倒入5 mL量筒中,避免振动,记录此时样品的体积,计算见公式(1)。
堆积密度![]()
(1)
式中:m,样品的质量,g;V1,样品振荡前的体积,mL。
1.3.4.2 振实密度
振荡上述称量样品的量筒,以相同幅度上下振荡5 min,直至体积不再变化,记录此时样品体积,计算见公式(2)。
振实密度![]()
(2)
式中:m1,样品的质量,g;V2,样品振荡后的体积,mL。
1.3.5 休止角和滑角的测定
1.3.5.1 休止角(θ)
固定漏斗底端与平面距离垂直距离为3 cm,将相同质量的样品从漏斗中流下,呈圆锥体,静置1 min后测量圆锥体高度和直径,休止角计算见公式(3)。
(3)
式中:d,圆锥体直径,cm;h,漏斗底端与平面的垂直高度,cm。
1.3.5.2 滑角(α)
将相同质量的样品放置于10 cm长的光滑玻璃平板上,缓慢抬高玻璃平板一端,直至90%质量的样品滑落,记录平板的高度,滑角计算见公式(4)。
(4)
式中:H,玻璃平板一段抬高的距离,cm;10,玻璃平板的长度,cm。
1.3.6 色泽的测定
利用颜色测定仪,经过标准黑白板校准调零,测定4组样品的色泽,记录各组的L*、a*、b*值。
1.3.7 总酚含量的测定
利用福林酚比色法,按照植物总酚试剂盒规定方法进行总酚提取和上机测定,绘制标准曲线为:y=0.110 0x-0.000 9,R2=0.999 5。
1.3.8 抗氧化能力的测定
1.3.8.1 ·OH清除能力
按·OH清除能力测定试剂盒要求,使用酶标仪上机测定,计算见公式(5)。
·OH清除率![]()
(5)
式中:A测定、A对照、A空白分别为测定样品、对照样品、空白样品在510 nm波长下读取的吸光值。
1.3.8.2 DPPH清除能力
按DPPH清除能力试剂盒要求,使用酶标仪上机测定,计算见公式(6),绘制标准曲线为:y=2.848 6x-0.708 4,R2=0.999 1。
DPPH清除能力/(μg Trolox/g干重)
(6)
式中:A测定、A对照、A空白分别为测定样品、对照样品、空白样品在517 nm波长下读取的吸光值;m为样品质量,g。
1.3.8.3 总抗氧化能力
利用铁离子还原/抗氧化能力法(ferric ion reducing antioxidant power, FRAP)测量总抗氧化能力。按总抗氧化能力试剂盒要求,使用酶标仪上机测定,计算见公式(7),绘制标准曲线为:y=0.097 2x+0.004 2,R2=0.999 7。
总抗氧化能力/(μmol Trolox/g干重)
=2.06×(A测定-A空白-0.004 2)×D
(7)
式中:A测定、A空白分别为测定样品、空白样品在590 nm波长下读取的吸光值;D为稀释倍数。
1.3.9 膳食纤维含量测定
IDF和SDF均采用GB 5009.88—2023《食品安全国家标准 食品中膳食纤维的测定》测定。TDF为IDF和SDF的总和。
1.3.10 体外消化模拟实验
口腔消化:准确称取5 g样品,加入100 mL蒸馏水和400 U酶活力的α-淀粉酶溶液(溶剂为pH 7.0的1 mmol/L CaCl2)。在37 ℃、300 r/min的恒温振荡箱振荡,10 min后取出,得到口腔消化液。离心后冷藏备用。
胃消化:取上述口腔消化液20 mL,用1 mol/L HCl调节pH值至2.0。加入4 800 U酶活力的胃蛋白酶溶液(溶剂为体积分数0.01%浓盐酸),在37 ℃、150 r/min的恒温振荡箱振荡,2 h后取出,得到胃消化液。离心后冷藏备用。
肠消化:取上述胃消化液20 mL,用2 mol/L NaOH调节pH值至7.0,加入0.2 g牛胆盐和2 600 U酶活力的胰酶溶液(溶剂为0.1 mol/L Na2CO3),在37 ℃、150 r/min的恒温振荡箱振荡,2 h后取出,得到肠消化液。离心后冷藏备用。
1.4 数据处理
实验均进行3次平行,结果以“平均值±标准差”表示。利用Excel作图,SPSS 20.0软件进行单因素(ANOVA)方差分析和邓肯多重检验。差异显著(P<0.05)用不同小写字母表示。
2 结果与分析
2.1 水分含量、堆积密度和振实密度
堆积密度和振实密度反映粉体颗粒自身大小和颗粒间空隙大小的状态,4组样品经过相同的80目过筛处理,粒径大小基本相同,在此情况下水分含量对堆积密度和振实密度影响较大。由图1可知,N-F、F-F水分含量较高,是N-H、F-H的2.3~2.7倍,而N-H、F-H的堆积密度和振实密度较高,是N-F、F-F的1~2倍,水分含量与堆积密度、振实密度呈负相关。这可能是由于冻干过程中,水分结成冰晶升华形成多孔结构,使粉体空隙变大,相同质量下体积变大,同时未升华的水分填充了粉体颗粒间的空隙,进一步增加粉质整体体积[7]。N-F、N-H堆积密度是F-F、F-H的1.4~2.3倍,与堆积密度相比,N-F、N-H振实密度增长15%~22%,而F-F、F-H振实密度增长11%左右。这是由于微生物发酵使苹果皮中碳水化合物被分解利用,细胞壁被破坏,使结构疏松化,颗粒间空隙变大[8],使得堆积密度变小,振实密度较堆积密度的增长幅度较小。
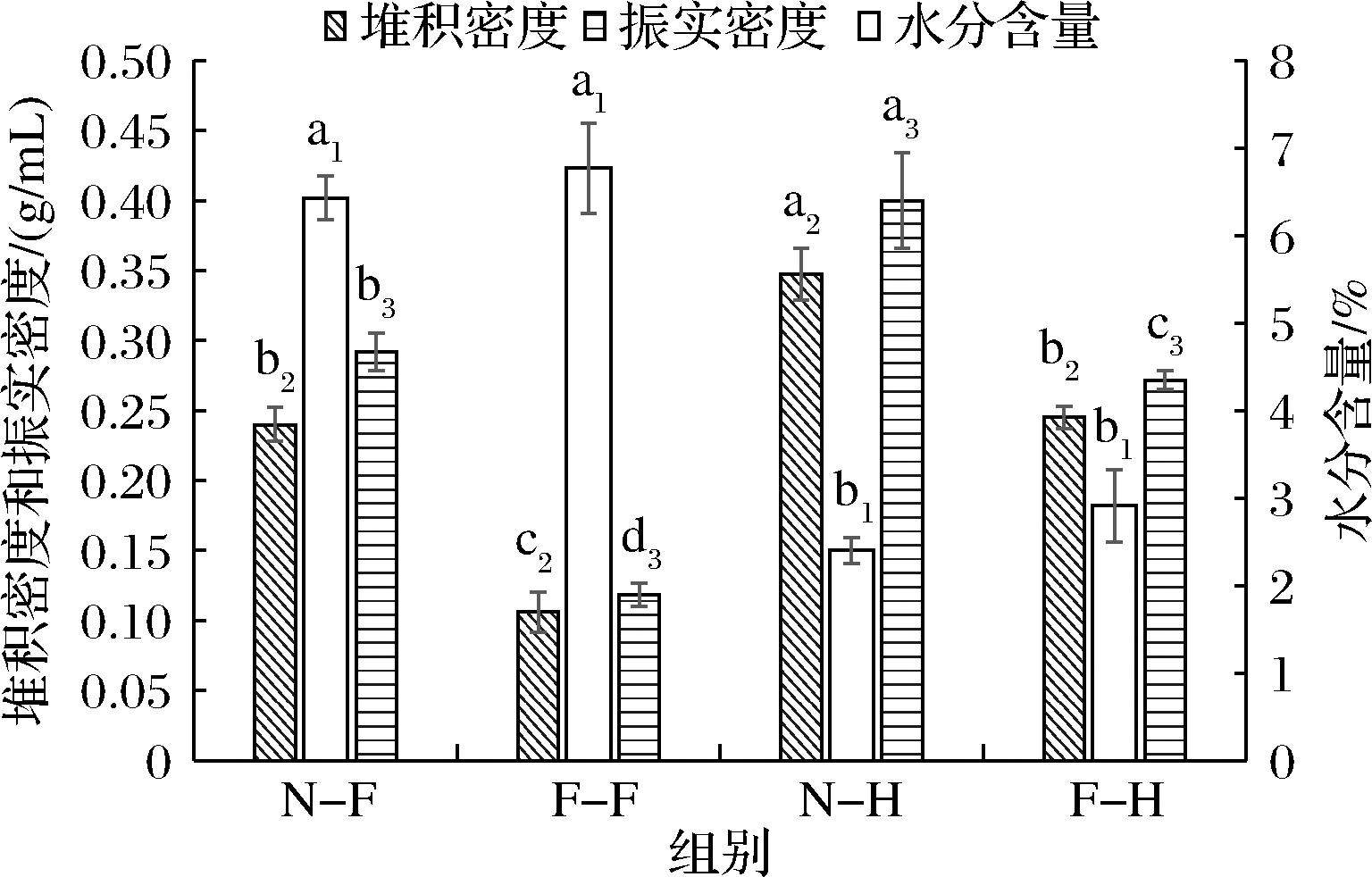
图1 不同组分的水分含量、堆积密度和振实密度
Fig.1 Moisture content, bulk density, and tap density of different groups
注:标注相同下角标的小写字母为同一组差异显著性(下同)。
2.2 休止角和滑角
休止角和滑角是描述颗粒状粉体流动性和摩擦力大小的重要参数,休止角小于35°表示流动性极好,大于45°表示流动性差,滑角越大表明粉体摩擦力越大[9]。由图2可知,N-F、F-F的休止角大于45°,流动性差,N-H、F-H的休止角小于45°流动性较好,N-F、F-F的滑角均大于N-H、F-H,摩擦力大。这是由于冻干能够保持苹果皮粉原有组织,所以粉质细腻,粉体疏松多孔,粉体颗粒表面凹凸不平,导致苹果皮粉表面黏着力强,使得流动性减小,摩擦力增大,这与茹超等[10]关于木瓜果粉的结论相同。F-F、F-H的休止角和滑角均略高于N-F、N-H,这可能是由于微生物发酵破坏细胞壁结构,导致粉质变得松散,粉体表面出现多孔的蜂窝状结构,使得摩擦力增大,流动性差,发酵后的休止角和滑角均增大[11]。
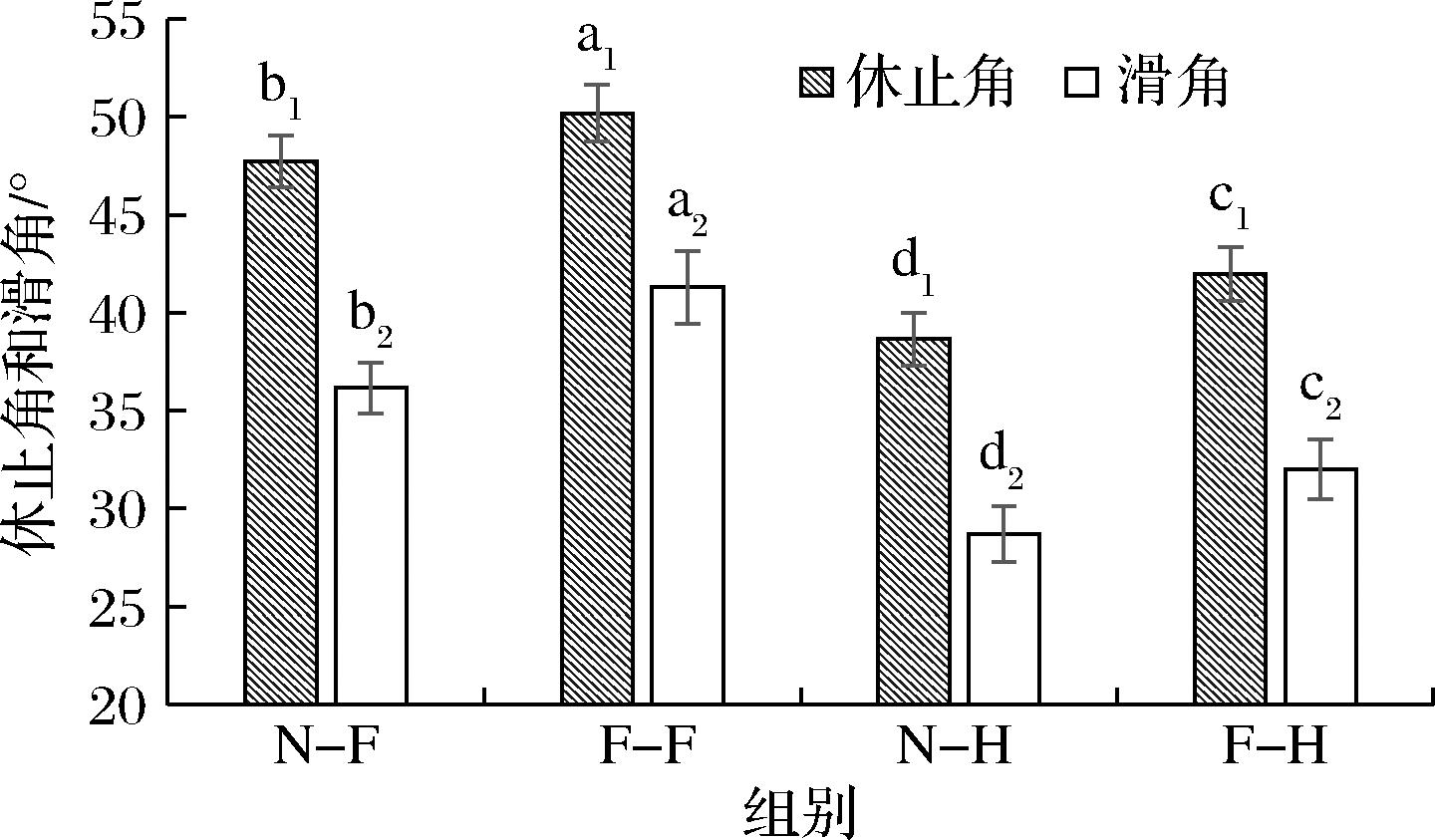
图2 不同组分的休止角和滑角
Fig.2 Angle of repose and slip of different groups
2.3 色泽
色泽是判断果粉品质的最重要、最直观的指标,L*值越大,样品亮度越高;a*值越大,样品颜色越红;b*值越大,样品颜色越黄。由表1及图3可知,N-F、F-F的L*和a*值较N-H、F-H整体偏大,b*值偏小,表示冻干苹果皮粉亮度高、红色深、黄色浅,粉体呈肉粉色;热干苹果皮亮度低、红色浅、黄色深,粉体呈深黄色,这可能是由于冻干将苹果皮粉中的水分冻结成冰晶直接升华,且苹果皮粉在低温中受到保护,所以颜色最接近苹果皮本身的颜色,而高温使热干的苹果皮粉氧化褐变,颜色较暗,对粉体颜色影响较大[12]。F-F、F-H的b*值较N-F、N-H偏小,L*和a*值偏大,表示发酵苹果皮粉亮度高,红色较深,黄色较浅,这可能是由于植物乳植杆菌发酵代谢产生的乳酸使苹果皮粉pH值降低,苹果皮中酚类物质在酸性条件下呈红色,使a*值升高,颜色更红,同时发酵破坏苹果皮的刚性结构,释放出更多的酚类物质,抗氧化活性高,减少了氧化褐变,从而使亮度高,这与林淑敏[13]的研究结果一致。
表1 不同组分的色度值
Table 1 Chromaticity values of different groups

样品组别L∗a∗b∗N-F60.26±0.04b6.46±0.71ab20.03±0.13aF-F62.69±0.36a7.22±0.88a15.66±0.06bN-H52.48±1.81c4.57±0.35c21.29±1.91aF-H54.86±1.52c5.78±0.3bc19.55±0.94a
注:同列不同小写字母表示差异显著(P<0.05)(下同)。

a-N-F组;b-F-F组;c-N-H组;d-F-H组
图3 不同组分的苹果皮粉体图
Fig.3 Image of apple peel powder with different groups
2.4 总酚含量及抗氧化能力
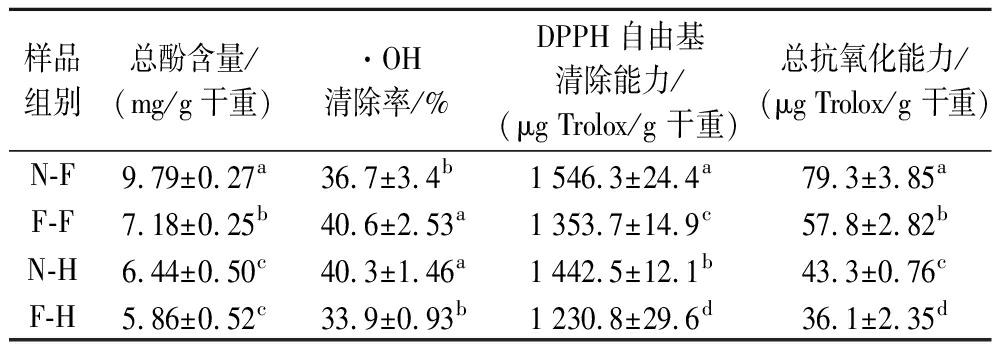
酚类物质是苹果皮中主要营养物质,温度、酶活性以及氧化程度对酚类物质影响较大。由表2可知,N-F、F-F较N-H、F-H组的总酚含量高23%~52%,可能是由于冻干的低温条件和真空环境,能够保护受热易分解、易氧化的酚类物质成分稳定[14]。发酵后苹果皮粉的总酚含量降低,这与BEI等[15]的研究结果不一致,可能是由于本实验采用液态发酵的方式,发酵过程中产生的酶将苹果皮细胞壁破坏,释放出的酚类物质部分溶解在发酵液中,干燥后酚类物质流失,而BEI等[15]采用了固态发酵的方式。
表2 不同组分的总酚含量及抗氧化能力
Table 2 Total phenolic content and antioxidant capacity of different groups
样品组别总酚含量/(mg/g干重)·OH清除率/%DPPH自由基清除能力/(μg Trolox/g 干重)总抗氧化能力/(μg Trolox/g 干重)N-F9.79±0.27a36.7±3.4b1 546.3±24.4a79.3±3.85aF-F7.18±0.25b40.6±2.53a1 353.7±14.9c57.8±2.82bN-H6.44±0.50c40.3±1.46a1 442.5±12.1b43.3±0.76cF-H5.86±0.52c33.9±0.93b1 230.8±29.6d36.1±2.35d
由表2可知,N-F的DPPH自由基清除能力和总抗氧化能力最强,F-F、N-H的·OH清除能力强,比N-F、F-H组高10%~20%,4组样品抗氧化能力有一定差异,一方面由于3种抗氧化能力检测方法和原理不同,另一方面由于不同组分苹果皮粉的酚类含量及种类不同,影响了抗氧化能力[16]。N-F、F-F较N-H、F-H组的总抗氧化能力高,与总酚含量的趋势相同,二者呈正相关。N-F、N-H的DPPH自由基清除能力较高,可能是由于发酵使苹果皮中对DPPH自由基清除能力的贡献率最大的绿原酸含量降低,导致发酵苹果皮粉的总酚与DPPH自由基清除能力均下降[17]。
2.5 膳食纤维
由图4可知,4组样品中的IDF含量均高于SDF,说明苹果皮中的膳食纤维以IDF为主。F-F、F-H组的IDF比N-F、NH高124%~141%,而F-F、F-H组的TDF比N-F、N-H高104%~127%,说明发酵能显著提高苹果皮的膳食纤维含量。其中,F-F、F-H的IDF和SDF含量均大于N-F、N-H,可能是由于发酵破坏苹果皮细胞壁,促进IDF释放,同时发酵产生的酶类代谢物打破苹果皮中纤维素、半纤维素和木质素的酯基和氢键,促进膳食纤维总量增加[18]。
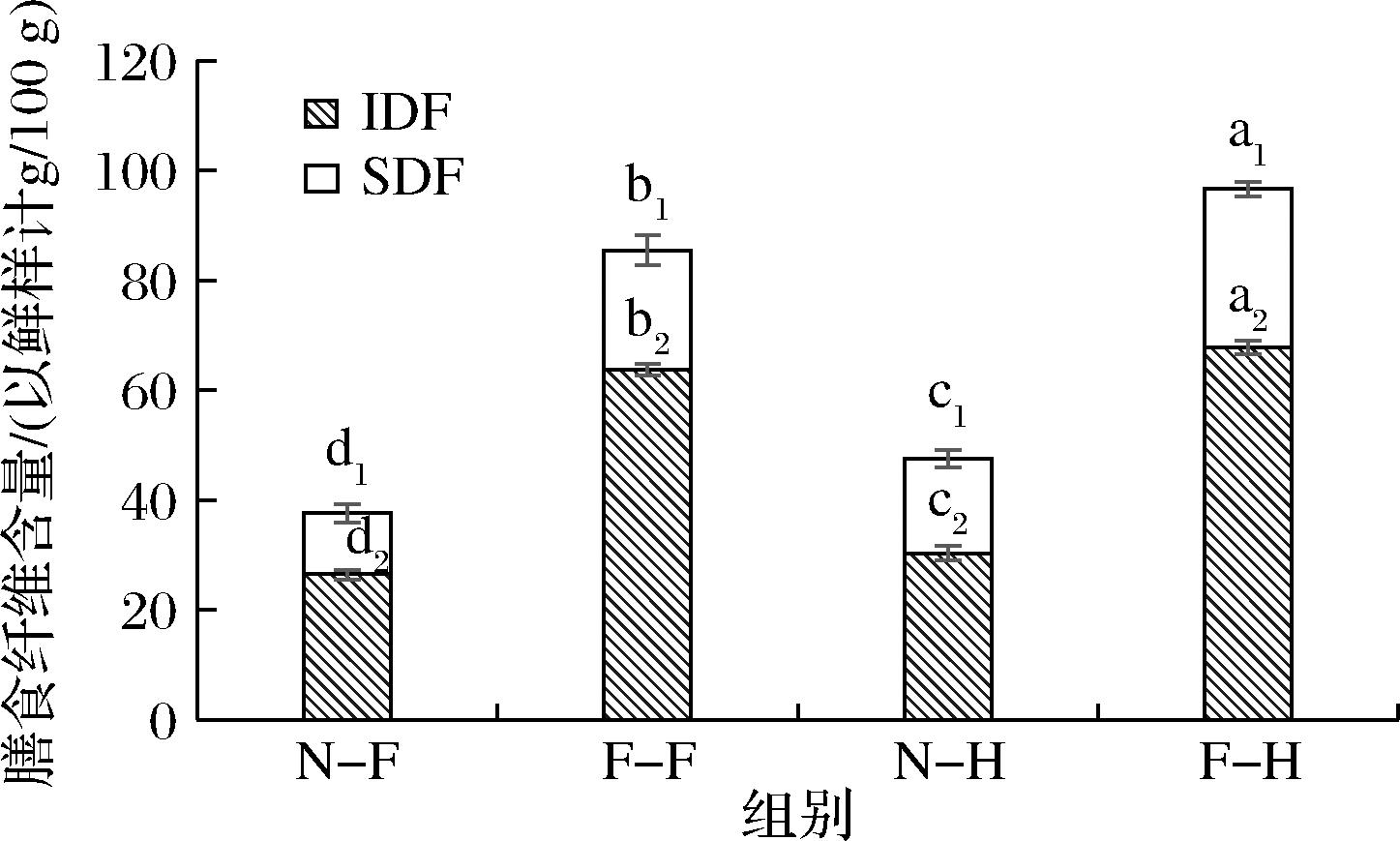
图4 不同组分的膳食纤维含量
Fig.4 Dietary fiber content of different groups
2.6 体外消化特性研究
通过对4组样品粉质特性和营养成分的综合分析,结果显示,冻干苹果皮粉色泽好、粉体轻,总酚含量和抗氧化能力得到很好地保持,而植物乳植杆菌发酵的苹果皮粉膳食纤维含量显著提高,所以将冻干技术与发酵技术结合,针对特殊人群开发膳食纤维补充食品是重要且相关的,更能够体现研究意义和价值。所以后续选取N-F和F-F进行体外消化特性分析。
2.6.1 不同消化阶段的总酚含量及抗氧化能力
由图5-a可知,与未消化样品相比,消化阶段中N-F总酚含量下降20%~28%,而F-F总酚含量提高37%~56%,并且3个消化阶段中F-F比N-F的总酚含量高40%~60%,均有显著提高,表明发酵可以促进消化过程中酚类物质释放。这是由于植物基的酚类物质多以糖苷键、酯键等与多糖等大分子结合形成的凝胶结构,被体外模拟消化实验的酶和酸碱环境破坏,使酚类物质被释放,含量增加[19]。2组样品在体外消化过程中总酚含量变化趋势一致,胃消化阶段降低,肠消化阶段升高,这可能是由于胃消化模拟酸性环境与大分子酚类物质结合形成沉淀,从而使总酚含量下降,而在肠道模拟碱性环境以及胰酶的作用下,多糖和酚类物质之间的共价键发生水解,从而使总酚含量升高,与王旭辉等[20]的研究结果相同。
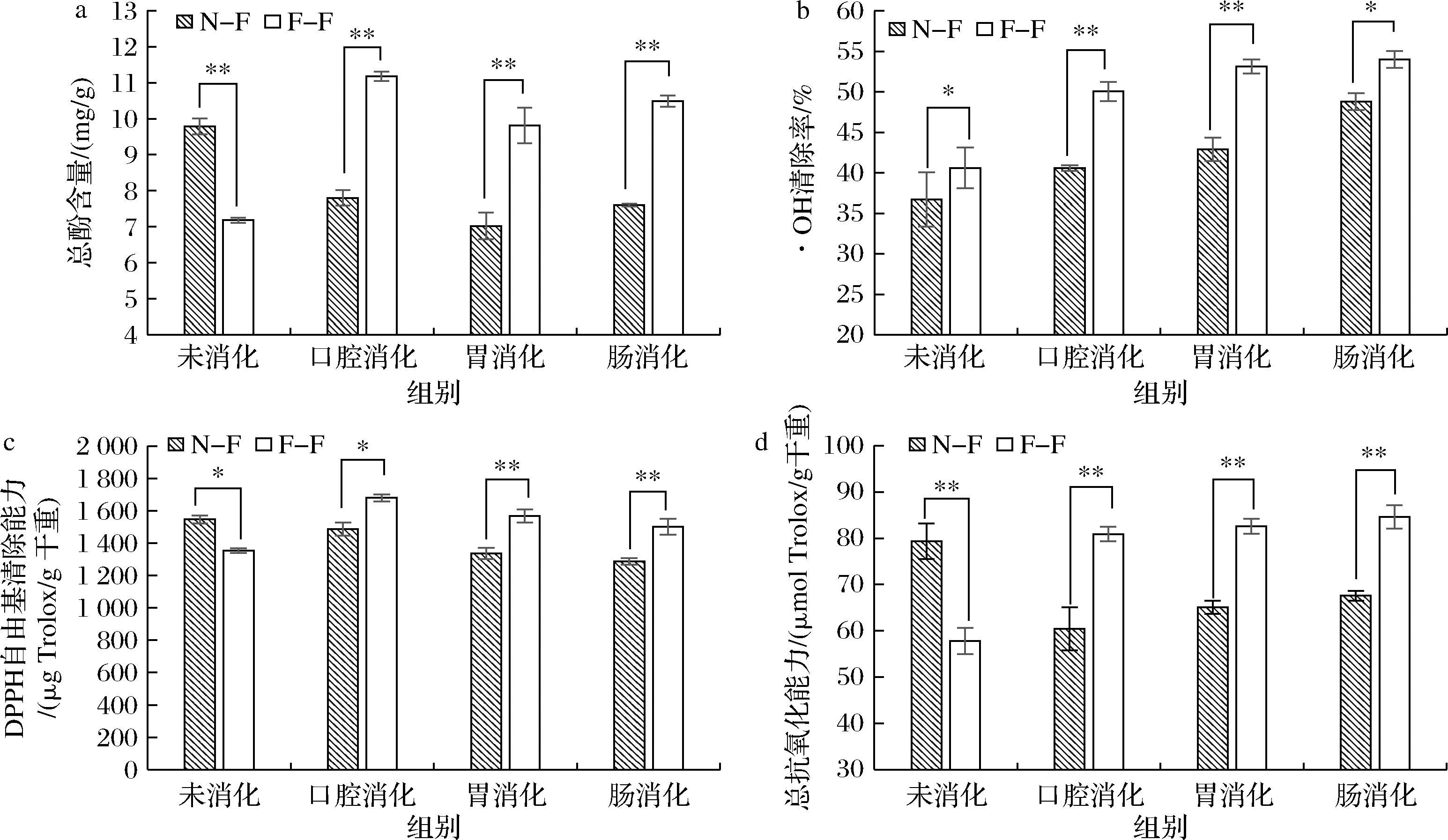
a-总酚含量;b-·OH清除率;c-DPPH自由基清除能力;d-总抗氧化能力
图5 不同消化阶段的总酚含量及抗氧化能力
Fig.5 Total phenolic content and antioxidant capacity at different stages of digestion
注:*代表差异显著(P<0.05),**代表差异极显著(P<0.01)(下同)。
多种抗氧化测定方法综合分析,能够更全面地反映苹果皮的抗氧化特性。如图5-b、图5-d所示,苹果皮的·OH清除能力和总抗氧化能力在3个消化阶段逐渐上升,DPPH自由基清除能力逐渐下降但趋势较缓(图5-c)。F-F的3种抗氧化能力均高于N-F,其中F-F的·OH清除能力比N-F高10%~23%、总抗氧化能力高25%~34%、DPPH自由基清除能力高13%~17%,这可能是由于酚类物质与抗氧化能力之间呈显著正相关性[21],在体外消化过程中,苹果皮的酚类物质被释放,所以抗氧化能力提高。同时发酵和发酵代谢产物能够破坏细胞壁结构,从而使更多的抗氧化活性物质从细胞内释放出来,提高抗氧化能力[22]。
2.6.2 不同消化阶段膳食纤维含量
由图6-a可知,F-F在3种消化环境中的SDF含量均显著高于N-F,分别是N-F组的5.26、3.54、1.78倍,并且2组样品的IDF在消化过程中均呈现下降趋势,F-F下降趋势较缓(图6-b)。可能是由于SDF主要由果胶、葡聚糖等多糖组成,而微生物发酵的代谢活动产生的酶催化糖苷键断裂,促进IDF向SDF转化,对膳食纤维产生改性效果[23]。2组样品的SDF含量在消化过程中呈现先下降后上升的趋势,与总酚含量在消化过程的趋势相同。这可能是模拟胃消化环境使TDF中的多糖大分子产生沉淀,SDF含量减少,而在肠消化阶段由酸性条件过渡到包含胆盐及Na2CO3的温和碱性条件,使多糖大分子被分解为小分子,SDF含量增加[24],所以呈现先下降后上升的趋势。
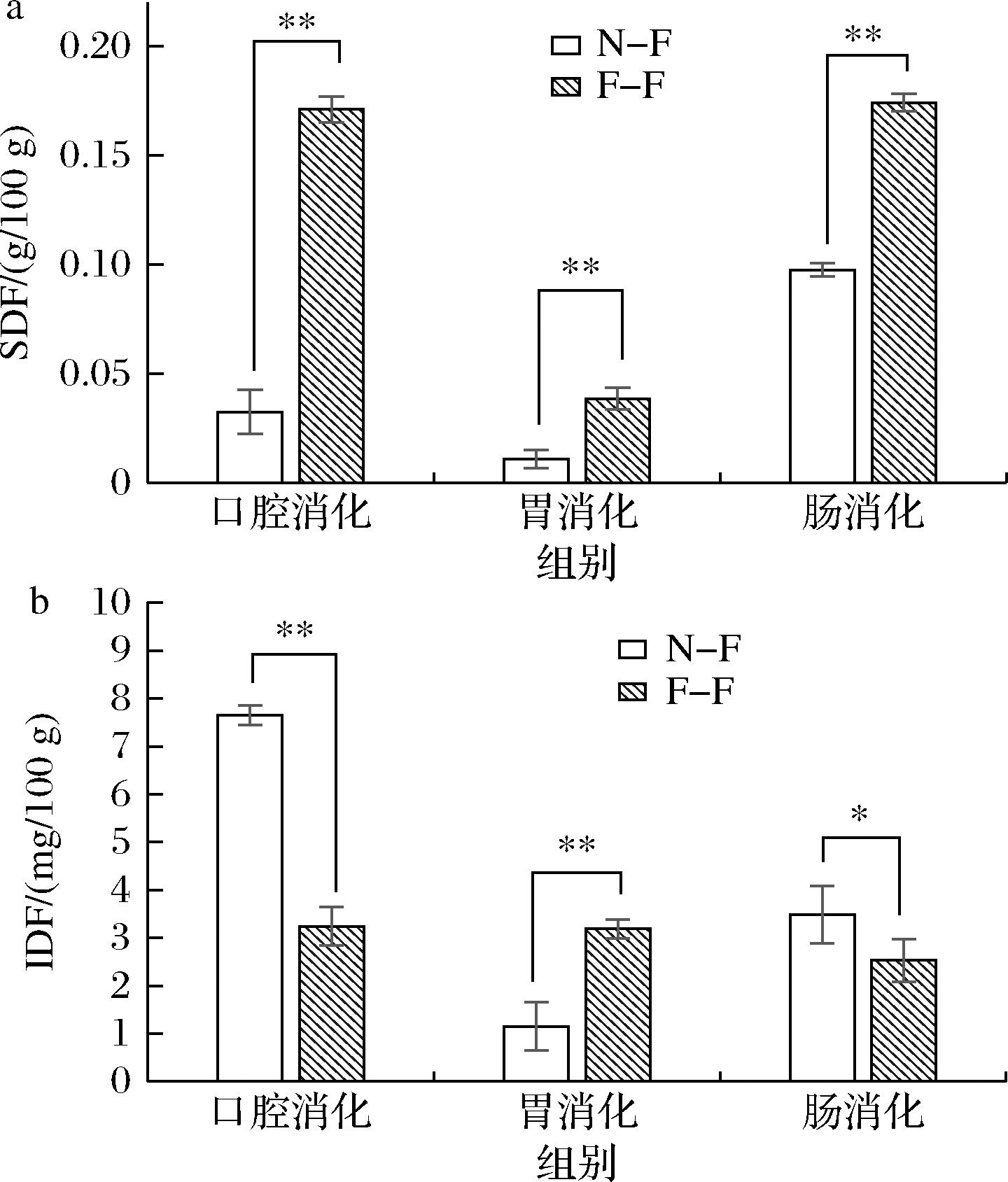
a-SDF含量;b-IDF含量
图6 不同消化阶段膳食纤维含量
Fig.6 Dietary fiber content at different stages of digestion
注:膳食纤维含量均以鲜样计。
3 结论及展望
本研究明确了植物乳植杆菌发酵对不同干燥方式苹果皮的粉质特性、营养成分和抗氧化能力的影响,同时利用体外模拟消化实验探究苹果皮粉在口腔、胃、肠道3种环境中的变化情况。结果表明,冻干苹果皮粉堆积密度和振实密度小,粉体轻盈;粉质亮度高,颜色淡粉,更接近苹果皮本身的颜色,总酚含量以及抗氧化能力高,能够保持苹果皮中的营养成分及生物活性,更适宜于加工。此外,植物乳植杆菌发酵在消化过程中体现良好的特性,与未发酵苹果皮相比,发酵苹果皮在3种消化过程中SDF和总酚的释放量更高,因此发酵后的苹果皮更容易被人体消化,有助于肠道健康。将发酵技术和冻干技术结合开发优质天然苹果皮膳食纤维产品,能满足特殊人群的需求,具有广阔的应用前景。
[1] 焦孝平, 李建林, 吴丽君.苹果皮渣膳食纤维固体酸奶生产技术[J].甘肃科技, 2023, 39(12):99-101;105.
JIAO X P, LI J L, WU L J.Production technology of solid yogurt with dietary fiber from apple peel residue[J].Gansu Science and Technology, 2023, 39(12):99-101;105.
[2] VAZ A A, BELL G, OMS-OLIU G, et al.Exploring the prebiotic potential of unpurified apple dietary fibre concentrate[J].LWT, 2025, 222:117608.
G, OMS-OLIU G, et al.Exploring the prebiotic potential of unpurified apple dietary fibre concentrate[J].LWT, 2025, 222:117608.
[3] 张坤, 李明月, 钟义, 等.苹果皮加工利用研究进展[J].食品安全导刊, 2024(13):165-168.
ZHANG K, LI M Y, ZHONG Y, et al.Research progress in apple peel processing and utilization[J].China Food Safety Magazine, 2024(13):165-168.
[4] 杨胜博, 孟园, 李学震, 等.不同苹果品种的益生菌发酵适应性评价[J].中国果菜, 2025, 45(2):38-44.
YANG S B, MENG Y, LI X Z, et al.Adaptability evaluation of probiotic fermentation in different apple varieties[J].China Fruit &Vegetable, 2025, 45(2):38-44.
[5] 常虹, 王爽, 周家华, 等.体外模拟消化对鲜切苹果皮渣黄酮类物质及其还原力的影响[J].食品工业科技, 2022, 43(20):39-44.
CHANG H, WANG S, ZHOU J H, et al.Effect of in vitro simulated digestion on flavonoid and reducing ability of fresh-cut apple residue[J].Science and Technology of Food Industry, 2022, 43(20):39-44.
[6] WU X L, ZHANG B Q, ZHANG Q, et al.Optimization of the response surface for semi-dry preparation of acetylated chickpea starch and its structural, physicochemical and in vitro digestibility[J].LWT, 2025, 223:117764.
[7] WANG A N, WANG Y, KAN H, et al.Comparison of different drying techniques for Zanthoxylum bungeanum leaves:Changes in color, microstructure, antioxidant capacities, and volatile components[J].LWT, 2023, 188:115469.
[8] 李广志, 关莹, 陈玉芳, 等.蓝靛果酵素粉体制备及加工特性的研究[J].中国调味品, 2024, 49(7):79-85.
LI G Z, GUAN Y, CHEN Y F, et al.Study on preparation and processing characteristics of honeyberry enzyme powder[J].China Condiment, 2024, 49(7):79-85.
[9] KALSI B S, SINGH S, ALAM M S, et al.Comparison of ANN and ANFIS modeling for predicting drying kinetics of Stevia rebaudiana leaves in a hot-air dryer and characterization of dried powder[J].International Journal of Food Properties, 2023, 26(2):3356-3375.
[10] 茹超, 王奕然, 邱荔, 等.干燥方式对木瓜果粉性状品质的影响[J].食品工业科技, 2025, 46(17):203-212.
RU C, WANG Y R, QIU L, et al.Effect of drying methods on the properties and quality of papaya fruit powder[J].Science and Technology of Food Industry, 2025, 46(17):203-212.
[11] 张振民. 复合益生菌发酵枣粉制备及其体外模拟胃肠消化特性的研究[D].银川:宁夏大学, 2021.
ZHANG Z M.Study on preparation of jujube powder fermented by compound probiotics and its in vitro gastric and intestinal digestion simulation[D].Yinchuan:Ningxia University, 2021.
[12] 董婧婧, 宋亚, 范蓓, 等.不同加工方式对石斛品质的影响研究进展[J].现代食品科技, 2025, 41(6):318-326.
DONG J J, SONG Y, FAN B, et al.Research progress on the effects of different processing methods on the quality of Dendrobium products[J].Modern Food Science and Technology, 2025, 41(6):318-326.
[13] 林淑敏. 乳酸菌发酵对不同碾磨组分黑米糠品质特性的影响及应用研究[D].无锡:江南大学, 2024.
LIN S M.The effect of lactic acid bacteria fermentation on the quality characteristics of different milling fractions of black rice bran and its application[D].Wuxi:Jiangnan University, 2024.
[14] WANG L Q, HU Q H, PEI F, et al.Influence of different storage conditions on physical and sensory properties of freeze-dried Agaricus bisporus slices[J].LWT, 2018, 97:164-171.
[15] BEI Q, CHEN G, LU F J, et al.Enzymatic action mechanism of phenolic mobilization in oats (Avena sativa L.) during solid-state fermentation with Monascus anka[J].Food Chemistry, 2018, 245:297-304.
[16] ZHANG X Y, CHEN J, LI X L, et al.Dynamic changes in antioxidant activity and biochemical composition of Tartary buckwheat leaves during Aspergillus niger fermentation[J].Journal of Functional Foods, 2017, 32:375-381.
[17] 李建婷. 米曲霉固态发酵改性苹果皮的研究[D].重庆:西南大学, 2020.
LI J T.Study on modified apple peel by solid state fermentation with Aspergillus oryzae[D].Chongqing:Southwest University, 2020.
[18] 廖望. 混合发酵释放胡萝卜膳食纤维中结合多酚及可溶性膳食纤维在速食面条中的应用[D].南昌:南昌大学, 2022.
LIAO W.Mixed fermentation releases polphenols bound in carrot dietary fiber and application of soluble dietary fiber in instant noodles[D].Nanchang:Nanchang University, 2022.
[19] 江慧斌, 聂攀, 吕玮, 等.藜麦与黑大麦复合谷物发酵富集多酚和黄酮工艺优化及其生物有效性研究[J].食品工业科技, 2024, 45(6):150-160.
JIANG H B, NIE P, LYU W, et al.Study on the processing optimization for the enrichment of polyphenols and flavonoids in co-fermentation of quinoa and black barley and its bioavailability[J].Science and Technology of Food Industry, 2024, 45(6):150-160.
[20] 王旭辉, 钟方丽, 王晓林, 等.体外模拟胃肠消化过程中黑果腺肋花楸果提取物活性成分及其抗氧化作用变化规律[J].食品研究与开发, 2024, 45(4):89-95.
WANG X H, ZHONG F L, WANG X L, et al.Changes of active components and antioxidant activity of Aronia melanocarpa extract during simulated gastrointestinal digestion in vitro[J].Food Research and Development, 2024, 45(4):89-95.
[21] SANTANA ANDRADE J K, CHAGAS BARROS R G, GUALBERTO N C, et al.Influence of in vitro gastrointestinal digestion and probiotic fermentation on the bioaccessibility of Gallic acid and on the antioxidant potential of Brazilian fruit residues[J].LWT, 2022, 153:112436.
[22] 任志龙, 王涵, 杨昊鹏, 等.发芽与发酵协同处理对莜麦总酚生物可及性的影响[J].食品工业科技, 2025, 46(7):70-77.
REN Z L, WANG H, YANG H P, et al.Effects of cooperative treatment of germination and fermentation on bioaccessibility of total phenolics of naked oats[J].Science and Technology of Food Industry, 2025, 46(7):70-77.
[23] 游艳芝, 苏萃扬, 张亮, 等.膳食纤维不同改性技术研究进展[J].食品科学, 2025, 46(13):406-416.
YOU Y Z, SU C Y, ZHANG L, et al.A review of different modification technologies for dietary fiber[J].Food Science, 2025, 46(13):406-416.
[24] LIU X Z, LIAO R Y, LAI M T, et al.In vitro releasing characteristics of bound phenolics from mangosteen (Garcinia mangostana L.) pericarp dietary fiber and its role in gut microbiota regulation[J].Food Bioscience, 2025, 63:105685.