玫瑰酱是我国的一种传统发酵食品,因其营养价值高,具有良好的风味受人喜爱[1]。然而,食用玫瑰花期短,不易贮藏,贮藏过程中营养损失大[2],因此,以可食用玫瑰花瓣为原料制成玫瑰酱,可有效解决营养损失及资源浪费等问题。蔗糖在玫瑰酱发酵过程中作为微生物营养剂有助于产生良好的风味物质,减少发酵时长。在传统玫瑰酱的生产中一般使用大量的蔗糖,以延长产品的保质期,具有一定的防腐作用[3]。高糖形成的高渗透环境抑制了大多数微生物的生长繁殖,其中也包括益生菌,这就大大延长了玫瑰酱的发酵时间;另外,蔗糖摄入过量是糖尿病、龋齿等健康问题的关键所在。代糖木糖醇因其具有消化缓慢,对血糖水平影响不大,对牙齿和免疫有积极作用等优点[4],被用于高糖产品的改良中。如木糖醇加入酸樱桃泥后,在贮藏期间可维持酚类化合物、抗氧化活性和颜色的稳定[5]。然而,由于在发酵过程中低糖玫瑰酱的品质难以得到保障,并且其工业化生产过程也未标准化,关于高品质的低糖玫瑰酱的研究亟待补充。
高糖玫瑰酱的发酵时间一般多于30 d,在发酵过程中,微生物菌群变化引起不同的生命代谢活动,使玫瑰酱的风味物质出现明显变化,另外,主导微生物菌群是保障玫瑰酱食用安全的关键因素。目前,关于玫瑰酱微生物演替规律的研究主要集中于传统玫瑰酱中玫瑰品种与微生物菌群之间的关系,鲜少有研究利用木糖醇改善玫瑰酱高糖特性并研究其发酵过程中微生物的演替规律。其中罗亚楠[6]采用高通量测序技术对云南玫瑰酱中微生物群落进行鉴定,并对其理化性质、植物活性成分、抗氧化活性、风味物质等进行测定,发现细菌对云南玫瑰酱的影响比真菌显著。夏傲喃[7]采用高通量测序研究高糖玫瑰酱中的微生物群落及菌群结构。利用代糖木糖醇改善高糖玫瑰酱的产品品质,并利用微生物多样性在分子水平解析低糖玫瑰酱品质变化规律。
本研究通过测定5种不同蔗糖与木糖醇配比的玫瑰酱在自然发酵过程中理化指标的变化,对发酵结束的5种玫瑰酱进行感官评价;同时采用高通量测序技术对低糖玫瑰酱微生物菌群进行分析,并进一步揭示优势菌属和风味物质之间的联系,可以为减糖发酵生产的调整提供理论依据。
1 材料与方法
1.1 材料与试剂
玫瑰鲜花瓣采自山东平阴玫瑰园,于晴天上午8:00~10:00采集、筛选,4 ℃运输至实验室,在12 h处理完毕;白砂糖,广州华糖食品有限公司;木糖醇,河南豫鑫糖醇有限公司;戊糖片球菌MP13,本实验室(从高糖玫瑰酱中筛出)。
芦丁、没食子酸、DPPH、ABTS,上海源叶生物科技有限公司;抗坏血酸,比克曼生物科技有限公司;花青素试剂盒,北京索莱宝科技有限公司;无水乙醇,烟台远东精细化工有限公司;Al(NO3)3·9H2O、NaNO2、K2CO3、NaOH、K2HPO4、KH2PO4,天津市恒兴化学试剂制造有限公司。
1.2 仪器与设备
500 mL玻璃发酵罐,临沂美居晶品玻璃有限公司;752 N Plus紫外可见分光光度计,上海仪电分析仪器有限公司;PH700酸度计,美国EUTECH公司;台式高速离心机、黏度计,上海力辰邦西仪器科技有限公司;阿贝折射仪,上海力辰仪器科技有限公司;IlluminaMiseq测序平台,上海美吉生物医药科技有限公司;电子鼻,上海保圣实业发展有限公司;气相离子迁移谱(gas chromatography ion mobility spectrometry,GC-IMS),山东海能科学仪器有限公司。
1.3 实验方法
1.3.1 玫瑰酱及其水提物的制备
选取颜色鲜艳、花瓣完整的玫瑰鲜花瓣,将m(玫瑰花瓣)∶m(蔗糖)∶m(木糖醇)分别按照1∶3∶0、1∶2.25∶0.75、1∶1.5∶1.5、1∶0.75∶2.25、1∶0∶3的质量比称量,然后将玫瑰鲜花瓣和糖混合,揉搓均匀,将戊糖片球菌MP13以1×107 CFU接入玫瑰酱中,制作成质量分数100%(A,100%蔗糖+0%木糖醇)、75%(B,75%蔗糖+25%木糖醇)、50%(C,50%蔗糖+50%木糖醇)、25%(D,25%蔗糖+75%木糖醇)、0%(E,0%蔗糖+100%木糖醇)含糖量的玫瑰酱。放入密闭玻璃发酵罐内(每罐400 g),自然发酵,分别在0、11、22、33、44 d取样,样品储存于-80 ℃中备用。
玫瑰酱均质液的制备:准确称取5 g玫瑰酱于研钵中,分次加入45 mL超纯水研磨转移至50 mL离心管中,8 000 r/min离心10 min,低温保存备用。
1.3.2 感官评价
参照陈璟等[8]的方法,经过统一培训的20名感官评定人员对结束发酵的5种不同糖配比的玫瑰酱进行感官评价,感官评定标准见表1。
表1 感官评价标准
Table 1 Sensory evaluation criteria

评分色泽气味质地口感整体接受性16~20鲜艳明亮香气浓郁黏稠适中甜酸适中高7~15玫瑰色,但不均匀香气不纯涂抹不均匀偏甜和酸适中0~6颜色褐变严重异味太黏或流汤难以涂抹太酸太甜甚至苦涩较差
1.3.3 理化指标的测定
1.3.3.1 pH和可滴定酸(titratable acid,TTA)的测定
利用pH计测定玫瑰酱溶液的pH。利用NaOH-酚酞指示法测定玫瑰酱溶液的可滴定酸度[9],结果用g/100 g柠檬酸表示。
1.3.3.2 抗氧化能力的测定
参考HUANG等[9]的方法测定发酵玫瑰酱的DPPH自由基清除能力。取2 g玫瑰酱与10 mL乙醇溶液混合均质,在8 000 r/min离心5 min,取上清液。取2 mL样品溶液与2 mL无水乙醇混合均匀作为本底吸收组;取2 mL样品溶液加入2 mL 0.2 mmol/L 的DPPH溶液作为样品组;取2 mL无水乙醇加入2 mL 0.2 mmol/L的DPPH溶液作为空白组。在37 ℃下避光孵育1 h后,在517 nm下检测吸光值,空白组吸光度为A0,样品组吸光度为A1,本底吸光度为A2,DPPH自由基清除能力的计算如公式(1)所示:
(1)
参照RODR GUEZ-BONILLA等[10]的方法测定发酵玫瑰酱的ABTS阳离子自由基清除能力。取2 g玫瑰酱与10 mL乙醇溶液混合均质,在8 000 r/min离心5 min,取上清液。取0.6 mL样品溶液加入1.6 mL 0.081 mmol/L的ABTS溶液(含过硫化钾)作为样品组;取0.6 mL无水乙醇加入1.6 mL 0.081 mmol/L 的ABTS溶液作为空白组。在室温下避光充分混合后在734 nm下检测吸光值,样品组吸光度为A1,对照组吸光度为A2,以乙醇溶液为空白调零,ABTS阳离子自由基清除能力的计算如公式(2)所示:
GUEZ-BONILLA等[10]的方法测定发酵玫瑰酱的ABTS阳离子自由基清除能力。取2 g玫瑰酱与10 mL乙醇溶液混合均质,在8 000 r/min离心5 min,取上清液。取0.6 mL样品溶液加入1.6 mL 0.081 mmol/L的ABTS溶液(含过硫化钾)作为样品组;取0.6 mL无水乙醇加入1.6 mL 0.081 mmol/L 的ABTS溶液作为空白组。在室温下避光充分混合后在734 nm下检测吸光值,样品组吸光度为A1,对照组吸光度为A2,以乙醇溶液为空白调零,ABTS阳离子自由基清除能力的计算如公式(2)所示:
(2)
1.3.3.3 黏度的测定
参照GB/T 10247—2008《粘度测量方法》,利用落球法测定发酵玫瑰酱的黏度。将10 g均质化的玫瑰酱稀释10倍混匀,高糖玫瑰酱(A和B)选用小转子(3号和4号),转速分别为10、20 r/min,低糖玫瑰酱(C、D和E)黏度较低,选用大转子(1号和2号),转速分别为50、60、100 r/min。转子需完全浸没于被测样品中,转子上的标记与液面相平。按下测量键时开始计数,待30 s读数稳定后,记录当前转子、转速下的黏度值和百分计标度扭矩。(每次测量的百分计标度扭矩在20%~90%之间为正常值,低于或超过正常值需要更换转子或调整转速)。
1.3.3.4 可溶性固形物的测定
参照NY/T 2637—2014《水果和蔬菜可溶性固形物含量的测定 折射仪法》,利用折射仪法测定发酵玫瑰酱的可溶性固形物含量。用蒸馏水校准折射仪读数,将可溶性固形物含量调整至0%。将5 g玫瑰酱和5 mL蒸馏水充分混合,滴加2~3滴待测样液于棱镜中央,闭合上下2块棱镜,对准光源,转动消色调节旋钮,使视野分成明暗两部分,转动棱镜旋钮,使明暗分界线在物镜的十字交叉点上,读取读数P,P为测定液可溶性固形物含量(%),记录测定时的温度。
1.3.3.5 总酚的测定
参考许海棠等[11]的方法,以没食子酸为标准品,取2 g均质玫瑰酱和60%无水乙醇(体积分数)混合,用超声波提取20 min,对超声波提取物进行测定,总酚含量用mg/g表示。
1.3.3.6 总黄酮的测定
参考韩红娟等[12]的方法,以芦丁为标准品,空白用无水乙醇,总黄酮含量用mg/g表示。
1.3.3.7 花青素的测定
参照DB22/T 2529—2016《紫穗玉米花青素测定 分光光度法》,利用分光光度法测定发酵玫瑰酱的花青素含量。取玫瑰酱2 g加入40 mL盐酸-乙醇混合溶液均质后,超声波提取30 min,将提取液转移到容量瓶中。再次加入20 mL盐酸-乙醇混合溶液,超声波提取10 min,将二次提取液转移到容量瓶中。用盐酸-乙醇混合溶液定容,取10 mL提取液,10 000 r/min离心10 min,吸取上清液,待测。使用不同浓度的花青素标准品溶液绘制标准曲线,用盐酸-乙醇混合溶液为空白,在520 nm波长下测定吸光度。玫瑰酱样液的花青素含量(g/kg)的计算如公式(3)所示:
(3)
式中:C,花青素标准曲线计算所得含量,mg/L;V,定容体积,mL;m,试样的质量,g。
1.3.3.8 抗坏血酸的测定
参照GB 5009.86—2016《食品安全国家标准 食品中抗坏血酸的测定》,利用2,6-二氯靛酚滴定法测定发酵玫瑰酱的抗坏血酸含量。取10 g玫瑰酱,加入10 mL偏磷酸溶液,匀浆后,用偏磷酸溶液转移至100 mL容量瓶中,摇匀后过滤。吸取10 mL滤液,用标定过的2,6-二氯靛酚溶液滴定,直至溶液呈粉红色15 s不褪色为止。同时用10 mL偏磷酸溶液做空白试验。玫瑰酱样液的抗坏血酸含量的计算如公式(4)所示:
(4)
式中:X,试样中L(+)-抗坏血酸含量,mg/100 g;V,滴定试样所消耗2,6-二氯靛酚溶液的体积,mL;V0,滴定空白所消耗2,6-二氯靛酚溶液的体积,mL;T,2,6-二氯靛酚溶液的滴定度0.44,mg/mL;A,稀释倍数;m,试样质量,g。
1.3.4 挥发性风味物质的测定
采用顶空-气相色谱-离子迁移谱(headspace-gas chromatography-ion mobility spectrometry,HS-GC-IMS)测定玫瑰酱发酵过程中挥发性有机化合物的变化。取1 g样品置于20 mL顶空瓶中,在60 ℃下孵育15 min。以进样量300 μL注射进样,孵育速度设置为500 r/min,注射针温度为85 ℃。使用毛细管柱为CPC-PAL(15 m×0.53 mm, 1.0 μm),柱温设置为60 ℃,初始流速2.00 mL/min,2~8 min内线性增加至10.00 mL/min,8~10 min内线性增加至100.00 mL/min并保持10 min。迁移管长度53 mm,管温度45 ℃,管内电场强度500 V/cm,流速150 mL/min,以高纯氮气为漂移气体。
1.3.5 微生物多样性的测定
根据E.Z.N.A.@ soil DNA kit进行微生物群落总基因组DNA抽提,使用1%的琼脂糖凝胶电泳检测抽提的基因组DNA的质量,使用Nano Drop2000测定DNA浓度和纯度。使用338F(5′-ACTCCTACG-GGAGGCAGCAG-3′)和806R(5′-GGACTACHVGGGTWTCTAAT-3′)引物扩增细菌16S rRNA基因V3~V4可变区进行PCR扩增。使用ITS1(5′-TCCGTAGGTGAACCTGCGG-3′)和ITS4(5′-TCCTCCGCTTATTGATATGC-3′)引物扩增真菌的内转录间隔区的ITS1和ITS4区域进行PCR扩增。
1.4 数据处理
所有实验均开展3次,用“平均值±标准差”表示,使用SPSS Statistics进行差异显著性分析和相关性分析;使用Origin 2021软件(美国Origin Lab公司)绘制感官评价雷达图和理化指标折线图,处理风味数据绘制柱形图和热图;利用Mothur(version 1.30.2)分析发酵样品的α多样性指数(Shannon、Simpson、ACE、Chao1以及Sobs指数),利用Uparse(version 11)将OTU水平相似度为97%进行聚类,绘制OTU丰度曲线和Venn图。利用Qiime(version 1.9.1)生成分类学丰度表,计算Beta多样性距离。使用Cytoscape软件进行优势菌、风味和理化指标之间的相关性分析。
2 结果与分析
2.1 不同糖含量发酵玫瑰酱的感官品质变化
经过44 d发酵后,不同糖含量玫瑰酱的色泽、气味、质地、口感、整体接受性呈现于图1。C组具有最高的感官评价总分,其次是A组和B组,D组和E组具有较差的质地和口感,实验过程中还出现了明显的霉菌污染现象,可食用性极差。A组、B组和C组具有50%以上的蔗糖含量,可以起到明显的抑制杂菌生长繁殖的作用,其中C组具备明显的酸甜适中,质地均匀,整体接受性优良的特点。
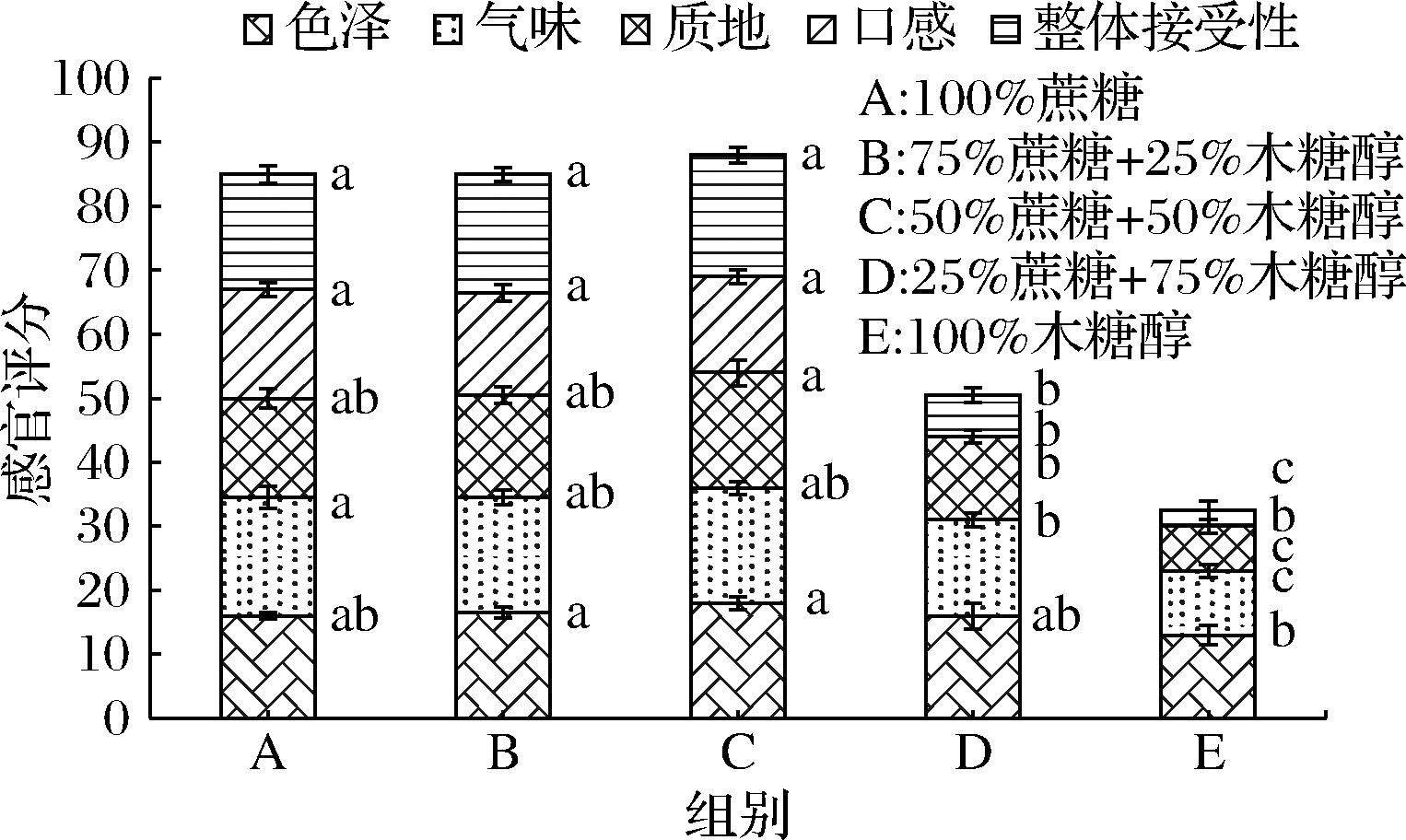
图1 不同蔗糖含量发酵玫瑰酱的感官品质
Fig.1 Sensory evaluation of fermented rose jams with different sucrose content
注:不同小写字母表示差异显著(P<0.05,下同)。
2.2 不同糖含量发酵玫瑰酱的理化特性变化
玫瑰酱的发酵过程伴随着多种理化性质的改变,图2呈现了不同蔗糖添加量的玫瑰酱在发酵过程中pH、可滴定酸、ABTS阳离子自由基清除能力、可溶性固形物含量、黏度、总酚含量、总黄酮含量、花青素含量、抗坏血酸含量和DPPH自由基清除能力的变化。其中pH值对于评估玫瑰酱产品的安全性具有重要意义[13],各发酵组随着发酵时间的延长pH逐渐降低,D组和E组的最终pH更低,可能是由于糖含量降低,抑菌能力下降,从而导致杂菌污染,产酸性微生物代谢活动剧烈。可滴定酸是影响产品品质、口感和风味的重要因素,发酵终点时,B组和C组发酵玫瑰酱的可滴定酸度无明显差异,赋予了它们相似的酸味口感风味特征(图1)。除了酸度,玫瑰酱的突出特征风味就是甜度,可溶性固形物含量可以间接表示玫瑰酱中的糖含量。如图所示,随发酵时间的延长,A组、B组和C组玫瑰酱的黏度增加,可溶性固形物含量逐渐降低。A组作为100%蔗糖组,拥有最高的可溶性固形物含量(>85%),其次是B组(>73%),可以满足抑制微生物生长繁殖的需求。C组的可溶性固形物含量有适当的下降,但是远高于D组和E组。相似的结果也体现于黏度中,前3组发酵玫瑰酱的黏度变化趋势一致,随发酵时间延长显著升高,与后2组形成显著差异(P>0.05),这可能是由于木糖醇具有结晶能力,会对玫瑰酱的黏度有影响。
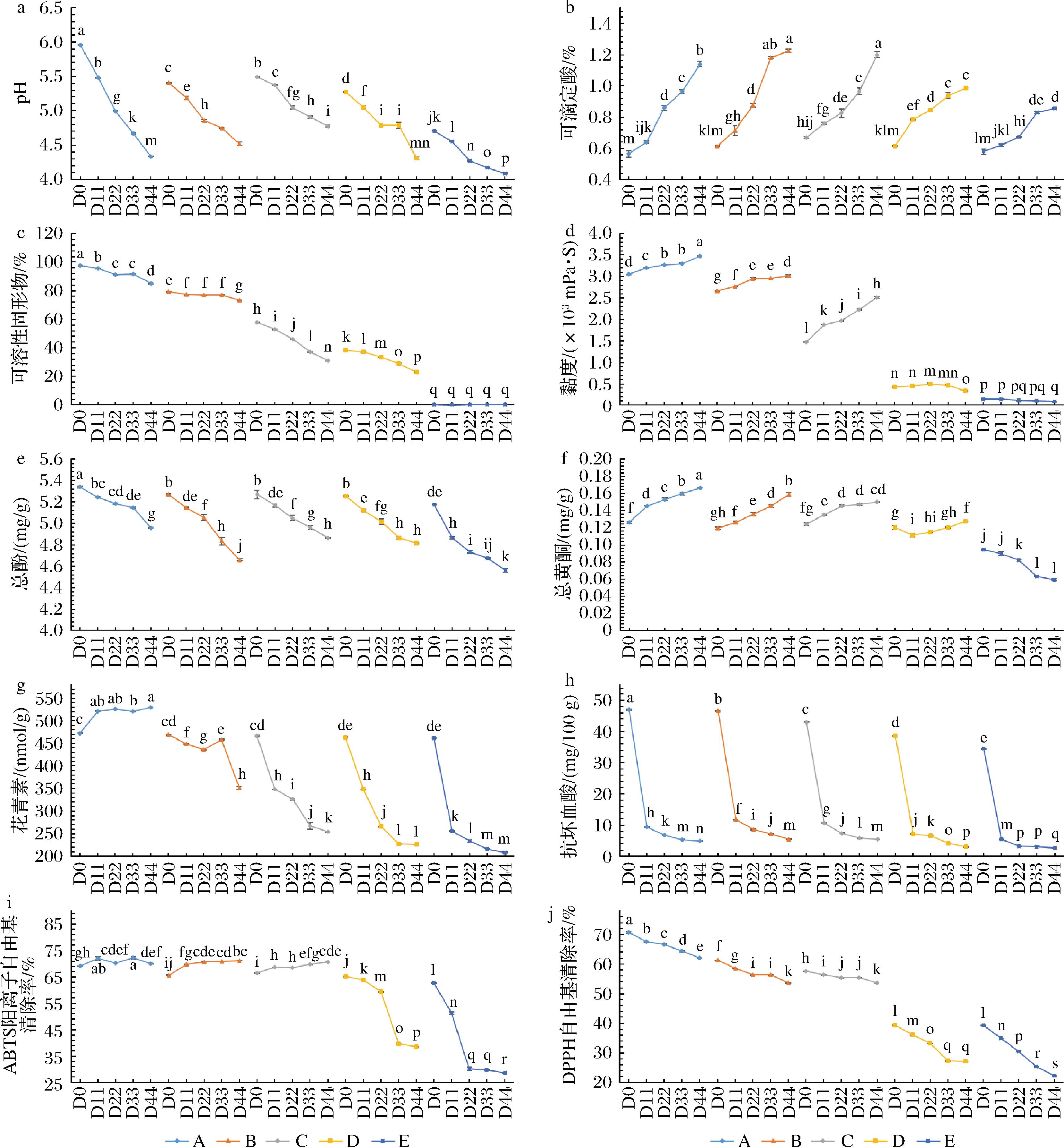
a-pH变化;b-可滴定酸度变化;c-可溶性固形物变化;d-黏度变化;e-总酚含量变化;f-总黄酮含量变化;g-花青素含量变化;h-抗坏血酸含量变化;i-ABTS阳离子自由基清除能力;j-DPPH自由基清除能力
图2 不同蔗糖含量发酵玫瑰酱的理化特性
Fig.2 Physicochemical properties of fermented rose jams with different sucrose
食用玫瑰花瓣中含有丰富的功能活性物质,包括多酚类化合物和黄酮类化合物等。其中多酚类物质具有一定的抗菌活性可以延长食品的保质期[14],黄酮类物质具有抗氧化、抗炎和神经递质调节的药学特性,具有潜在的健康益处[15]。在本研究中发现,发酵过程会导致总酚含量下降,并提高总黄酮含量,这可能是由于随着发酵时间的延长,微生物代谢活动加剧,部分酚类化合物被微生物利用,并充分破坏玫瑰花瓣组织结构,释放出更多黄酮类物质。除此之外,花青素也是一种类黄酮物质,它作为天然色素存在于水果和蔬菜(植物)中,本身具有较强的抗氧化活性[16]。然而由于花青素具有热、光、酸等不稳定性,不同发酵组的花青素损失程度较高。
食用玫瑰具有较高的抗氧化性,抗坏血酸含量也是反映食品营养价值的重要指标[17]。为了更好地表征不同发酵组抗氧化活性差异,抗坏血酸含量、ABTS阳离子自由基清除能力和DPPH自由基清除能力呈现于图2中,5组玫瑰酱的抗坏血酸含量变化趋势相似,在发酵初期抗坏血酸含量较高,经过11 d发酵,抗坏血酸含量急剧下降,这是由于抗坏血酸作为强还原剂,极易被氧化。A、B和C组的ABTS抗氧化能力和DPPH自由基清除能力明显优于D和E组。
综上所述,C组不仅具有较优良的感官特征,其理化特性,包括酸度、糖度、功能活性物质和抗氧化能力也同样优越。因而,本研究以50%木糖醇代替蔗糖制备发酵玫瑰酱,并探讨其在微生物群落调控下的内在风味形成机制。
2.3 低糖发酵玫瑰酱的挥发性风味物质组成
借助HS-GC-IMS分析,在不同发酵阶段,共有58种已知的挥发性风味化合物被发现于低糖(50%蔗糖+50%木糖醇)发酵玫瑰酱中(图3)。在发酵初期,醛类、醇类和酮类化合物是玫瑰酱的主要风味,包括3-羟基-2-丁酮-M、2-庚酮-M、正丁醇-M、异戊醇-M、异丁醇、丙醛、正戊醇、(Z)-2戊醇、芳樟醇、2-己烯醛-M、1-戊烯-3-醇、1-丙醇-D、苯甲醛、2-丁酮、庚醛等。其中,芳樟醇、苯甲醛和糠醛是玫瑰花酱的关键风味物质[18],丙醇、庚醇等直链醇可通过微生物和酶转化短链脂肪酸生成的[19],酮类物质具有油腻的香气,随着碳链的延长,使花香更浓[20]。在发酵中期,酯类化合物增加,比如丙酸乙酯、乙酸异戊酯、醋酸异丁酯、乙酸乙酯和乙酸甲酯等。酯是由醇和短链脂肪酸反应形成的挥发性化合物,使酯类成为发酵中后期主要的挥发性化合物,赋予了食品特有的花香和果香气味[21]。在发酵末期,醛类化合物、醇类化合物、酸类化合物和酯类化合物占比有所增加,酸类化合物主要是乙酸,醇类化合物主要有异戊醇、2-甲基-1丙醇、3-甲基-3-丁烯-1-醇,醛类化合物主要有正丁醛,酯类化合物有乙酸乙酯等。挥发性风味物质的种类减少但含量增加,特征风味物质分布更集中。其中,乙酸的浓度对乳酸菌的代谢和积累有抑制作用[22]。
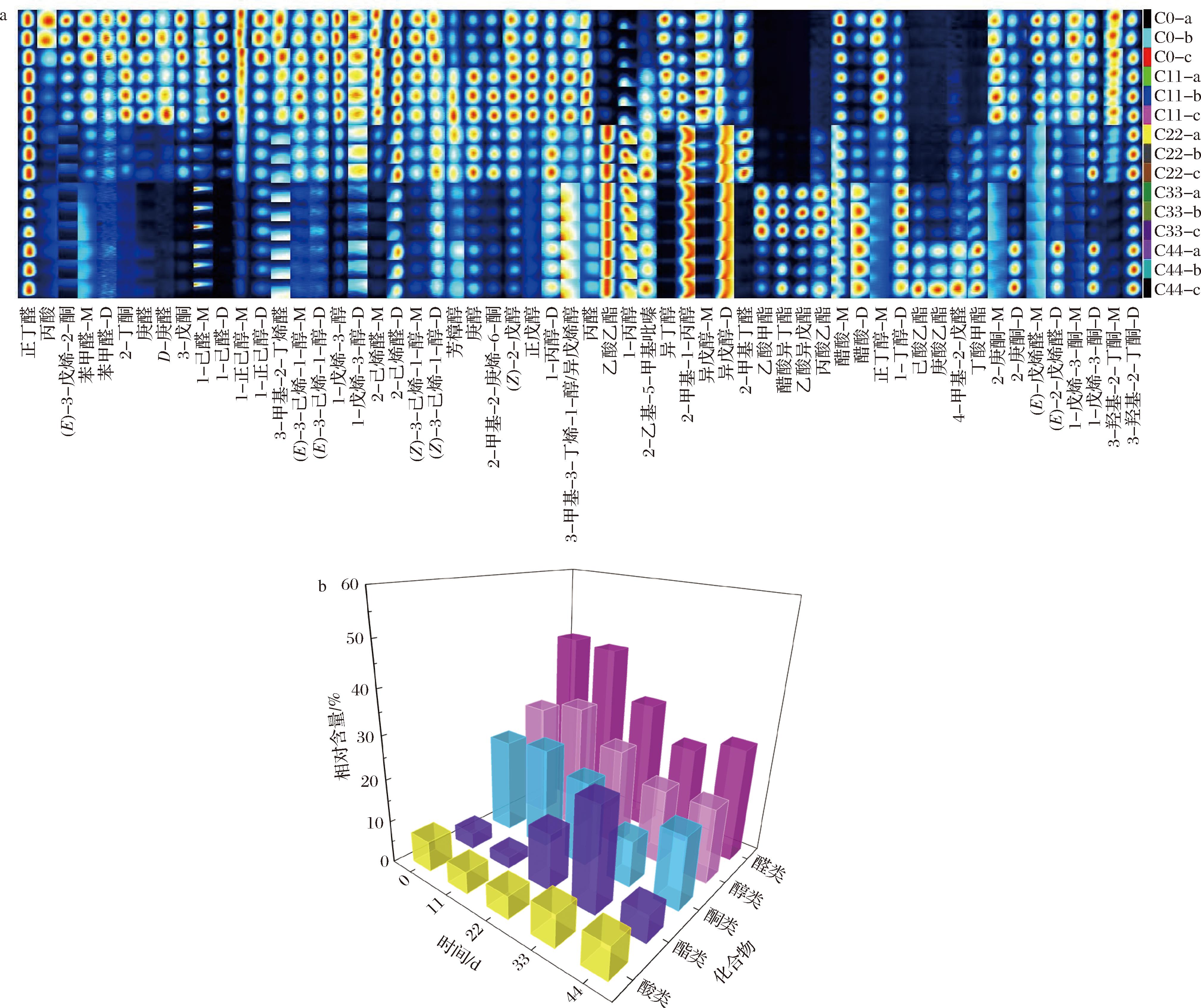
a-离子迁移谱;b-化合物分类及其变化
图3 不同发酵时间下低糖发酵玫瑰酱的挥发性风味物质组成
Fig.3 Composition of volatile flavor substances in low-sugar fermented rose jam with different fermentation time
注:酸类化合物:醋酸-D、醋酸-M、丙酸;酯类化合物:丁酸甲酯、庚酸乙酯、己酸乙酯、丙酸乙酯、乙酸异戊酯、醋酸异丁酯、乙酸甲酯、乙酸乙酯;酮类化合物:3-羟基-2-丁酮-D、3-羟基-2-丁酮-M、1-戊烯-3-酮-D、1-戊烯-3-酮-M、2-庚酮-D、2-庚酮-M、2-甲基-2-庚烯-6-酮、3-戊酮、2-丁酮、(E)-3-戊烯-2-酮;醇类化合物:1-丁醇-D、正丁醇-M、异戊醇-D、异戊醇-M、2-甲基-1-丙醇、异丁醇、1-丙醇、3-甲基-3-丁烯-1-醇/异戊烯醇、1-丙醇-D、正戊醇、(Z)-2-戊醇、庚醇、芳樟醇、(Z)-3-己烯-1-醇-D、(Z)-3-己烯-1-醇-M、1-戊烯-3-醇-D、1-戊烯-3-醇、(E)-3-己烯-1-醇-D、(E)-3-己烯-1-醇-M、1-正己醇-D、1-正己醇-M;醛类化合物:(E)-2-戊烯醛-D、(E)-戊烯醛-M、4-甲基-2-戊醛、2-甲基丁醛、丙醛、2-己烯醛-D、2-己烯醛-M、3-甲基-2-丁 烯醛、1-己醛-D、1-己醛-M、D-庚醛、庚醛、苯甲醛-D、苯甲醛-M、正丁醛;其他:2-乙基-5-甲基吡嗪。
2.4 低糖发酵玫瑰酱的微生物菌群多样性
α多样性指数包括Sobs指数、Shannon指数、Simpson指数、ACE指数、Chao指数和Coverage指数,可以表征和分析发酵玫瑰酱样本中微生物群落的丰富度和多样性[23]。由图4可知,每个低糖发酵玫瑰酱样品的Coverage指数都接近1,说明高通量测序结果覆盖程度高,测定的微生物群落结果准确可靠,序列测定结果具有稳定性。Sobs指数是用数值(OTU)来直接反映样品中微生物丰富度的一个重要指标。结果显示,随着发酵时间的延长,细菌的微生物丰富度远远高于真菌微生物丰富度,C11_B样品中细菌物种数目最高。Shannon指数与Simpson指数是衡量物种群落多样性的常用指标,一般来说,Shannon指数的数值越大,说明样本中群落的多样性较高。而Simpson指数的数值越小表示群落的多样性越高。细菌群落多样性呈现为C11>C22>C33>C44>C0。真菌群落多样性在初期最高,之后呈现出下降的趋势。同时,Simpson指数也呈现与之相反的变化,说明了低糖发酵玫瑰酱在发酵的不同时期群落的多样性变化不同。ACE指数和Chao指数可以表征样品群落丰富度,经过11 d发酵后,发酵玫瑰酱的群落丰富度大大增加,并逐渐降低并趋于稳定。综上所述,在不同盐浓度低糖发酵玫瑰酱样本中,细菌的微生物多样性高于真菌的微生物多样性,在发酵前期阶段细菌的多样性最高,而后出现下降趋势直至后期逐渐趋于一种稳定的状态。
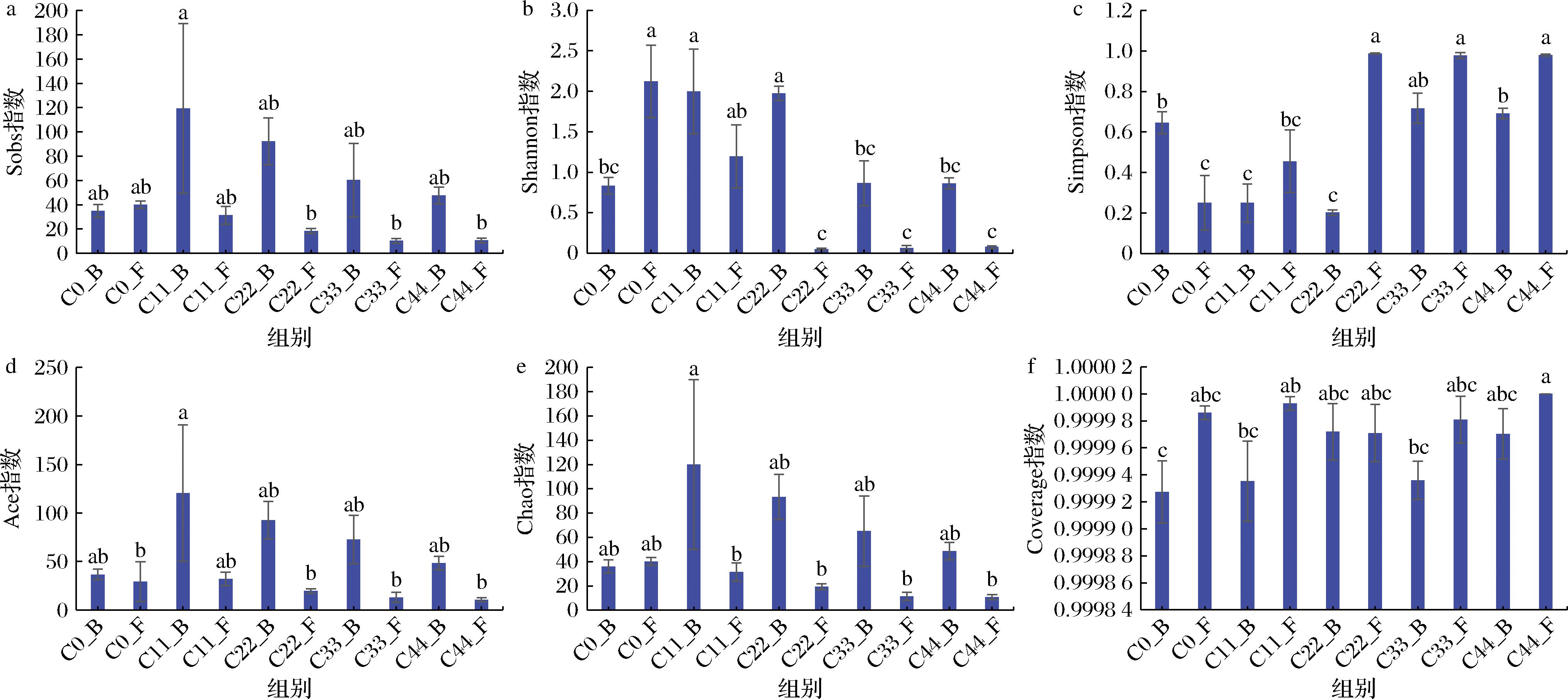
a-Sobs指数;b-Shannon指数;c-Simpson指数;d-Ace指数;e-Chao指数;f-Coverage指数
图4 低糖玫瑰酱的不同发酵时间的细菌α多样性和真菌α多样性
Fig.4 α diversity of bacteria and fungi at different fermentation times in low-sugar rose jam
注:B代表细菌,F代表真菌。

a-细菌稀释曲线;b-真菌稀释曲线
图5 低糖玫瑰酱不同发酵时间的细菌稀释曲线和真菌稀释曲线
Fig.5 Rarefaction curves of bacteria and fungi at different fermentation times in low-sugar rose jam
为了判断确保测序数据量的准确性,本研究以抽取的数据量为横坐标,以α多样性指数值为纵坐标绘制曲线,查看曲线是否达到平缓,以此判断数据量准确。同时,基于OTU水平的Sobs指数、Simpson指数、Shannon指数、Coverage指数等数据是否达到平缓确定此次测序数据是否可应用于细菌和真菌α多样性的比较分析。由图5可知,不同发酵时期不同的减盐低糖发酵玫瑰酱样本随着测序量的不断扩大,稀释曲线趋近于平缓,说明本次测序几乎覆盖样本中全部细菌和真菌,因此测序结果可以反映玫瑰酱样品细菌和真菌微生物的丰富度和多样性。
2.5 低糖发酵玫瑰酱的微生物群落组成
对于细菌而言,低糖发酵玫瑰酱的微生物由6个细菌门组成(图6-a),包括厚壁菌门(Firmicutes)、变形菌门(Proteobacteria)、放线菌门(Actinobacteria)、酸杆菌门(Acidobacteria)、脱铁杆菌门(Deferribacteria)和热脱硫菌门(Thermodesulfobiota)。其中,厚壁菌门和变形菌门是低糖发酵玫瑰酱在不同发酵时期的优势细菌门。共有177个细菌菌属存在于低糖发酵玫瑰酱中(图6-b),其中优势细菌属分别为片球菌属(Pediococcus)、罗森伯格菌属(Rosenbergiella)、假单胞菌属(Pseudomonas)、赖氏菌属(Leifsonia)和不动杆菌属(Acinetobacter)等。其中片球菌属是乳酸菌的一类,可以将碳水化合物转化成酸类物质,戊糖片球菌(Pediococcus pentosaceus)MP13作为低糖玫瑰酱发酵的接种菌株,在本研究中,其丰度随着发酵时间的延长而逐渐降低。罗森伯格菌属可能是存在于花蜜中,适合独特的高糖浓度并且具有一定的抗菌特性[24]。在本研究中,罗森伯格菌属随着发酵时间的延长丰度先增加后降低,假单胞菌属在发酵后期成为优势菌属。夏傲喃[7]研究发现,戊糖片球菌属和罗森伯格菌属在传统高糖玫瑰酱中也是主要优势菌属,具有较好的耐高糖作用,能够优先利用营养物质。在种水平上,发现了19种细菌(相对丰度>0.1%),其中随着发酵时间的进行,西班牙弧菌(Achromobacter spanius)逐渐取代P.pentosaceus成为优势菌种(图6-c)。
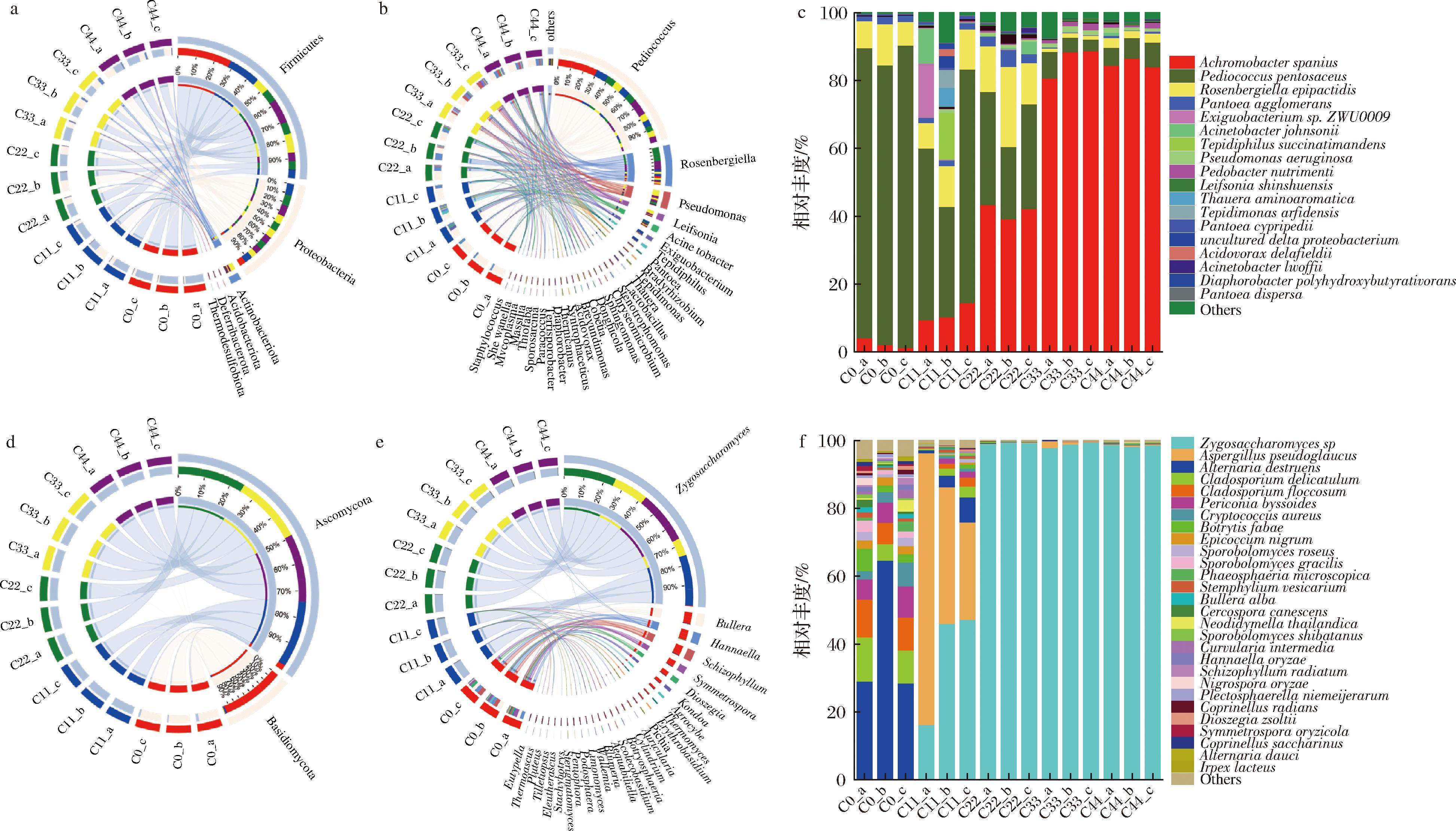
a-门水平细菌丰度变化;b-属水平细菌丰度变化;c-种水平细菌丰度变化;d-门水平真菌丰度变化;e-属水平真菌丰度变化;f-种水平真菌丰度变化
图6 低糖玫瑰酱的不同发酵时间的微生物群落组成
Fig.6 Microorganism community composition of low-sugar rose jam with different fermentation time
对于真菌而言,只有2个真菌门子囊菌门(Ascomycota)和担子菌门(Basidiomycota)被鉴定到(图6-d)。真菌菌属有28个,其中优势真菌属为接合酵母属(Zygosaccharomyces)、布勒酵母属(Bullera)、汉纳酵母属(Hannaella)、裂褶菌属(Schizophyllum)和Symmetrospora等(图6-e)。在发酵初期,布勒酵母属(21.67%)、汉纳酵母属(19.33%)、裂褶菌属(18.67%)和Symmetrospora(12%)是优势菌属;发酵开始后(C11、C22、C33和C44),接合酵母属成为绝对优势菌属。在菌种水平上,接合酵母属菌株(Zygosaccharomyces sp.)逐渐成为低糖发酵玫瑰酱的优势真菌菌种(图6-f)。
2.6 低糖发酵玫瑰酱的风味形成机制
为了探明低糖发酵玫瑰酱的特征风味物质的形成机制,高丰度的细菌菌种Achromobacter spanius、戊糖片球菌(Pediococcus pentosaceus)、Rosenbergiella epipactidis、成团泛菌(Pantoea agglomerans)、微小杆菌属ZWU0009菌株(Exiguobacterium sp. ZWU0009)、约氏不动杆菌(Acinetobacter johnsonii)、Tepidiphilus succinatimandens、铜绿假单胞菌(Pseudomonas aeruginosa)、Pedobacter nutrimenti、Pseudomonas extremorientalis和莱夫森氏菌(Leifsonia shinshuensis)和真菌菌种主要包括接合酵母菌菌种(Zygosaccharomyces sp. )、Aspergillus pseudoglaucus、Alternaria destruens、Cladosporium delicatulum、絮状枝孢霉(Cladosporium floccosum)、Periconia byssoides、金黄隐球菌(Cryptococcus aureus)、蚕豆葡萄(Botrytis fabae)、黑附球菌(Epicoccum nigrum)和Sporobolomyces roseus被用于与特征风味物质的Pearson相关性分析(图7)。发酵是通过细菌和酵母的共生作用进行的,而酵母对发酵食品的香气也具有影响,可以在发酵过程中产生乙醇和有机酸[25]。在本研究中,Zygosaccharomyces sp.、Achromobacter spanius、Pseudomonas aeruginosa、Pedobacter nutrimenti和Leifsonia shinshuensis与醋酸异丁酯、乙酸异戊酯、乙酸甲酯、丙酸乙酯、醋酸-D、乙酸乙酯、2-甲基-1-丙醇和异戊醇-D等化合物具有显著正相关。有趣的是,醋酸-D、乙酸乙酯、2-甲基-1-丙醇和异戊醇-D也是发酵末期低糖玫瑰酱的主要风味化合物。片球菌是对食品风味有重要作用的一种乳酸菌,对于食品风味具有重要作用,可以产生有机酸和H2O2来降低食物的酸碱度,抑制腐败微生物的生长[26],片球菌与玫瑰酱中醇类物质具有正向相关性,LIANG等[27]结合风味发现,片球菌与酸菜中醇类物质的产生也具有相关性。在本研究中,P.pentosaceus对玫瑰酱的风味起到了关键作用,与1-戊烯-3-醇、3-羟基-2-丁酮-M、正戊醇、异戊醇-M、2-己烯醛-M、异丁醇、2-丁酮、庚醛、正丁醇-M、2-庚酮-M、(Z)-2-戊醇、丙醛、正丁醛、苯甲醛-M、苯甲醛-D、醋酸-M和3-甲基-3-丁烯-1-醇等风味化合物有明显的正相关性。
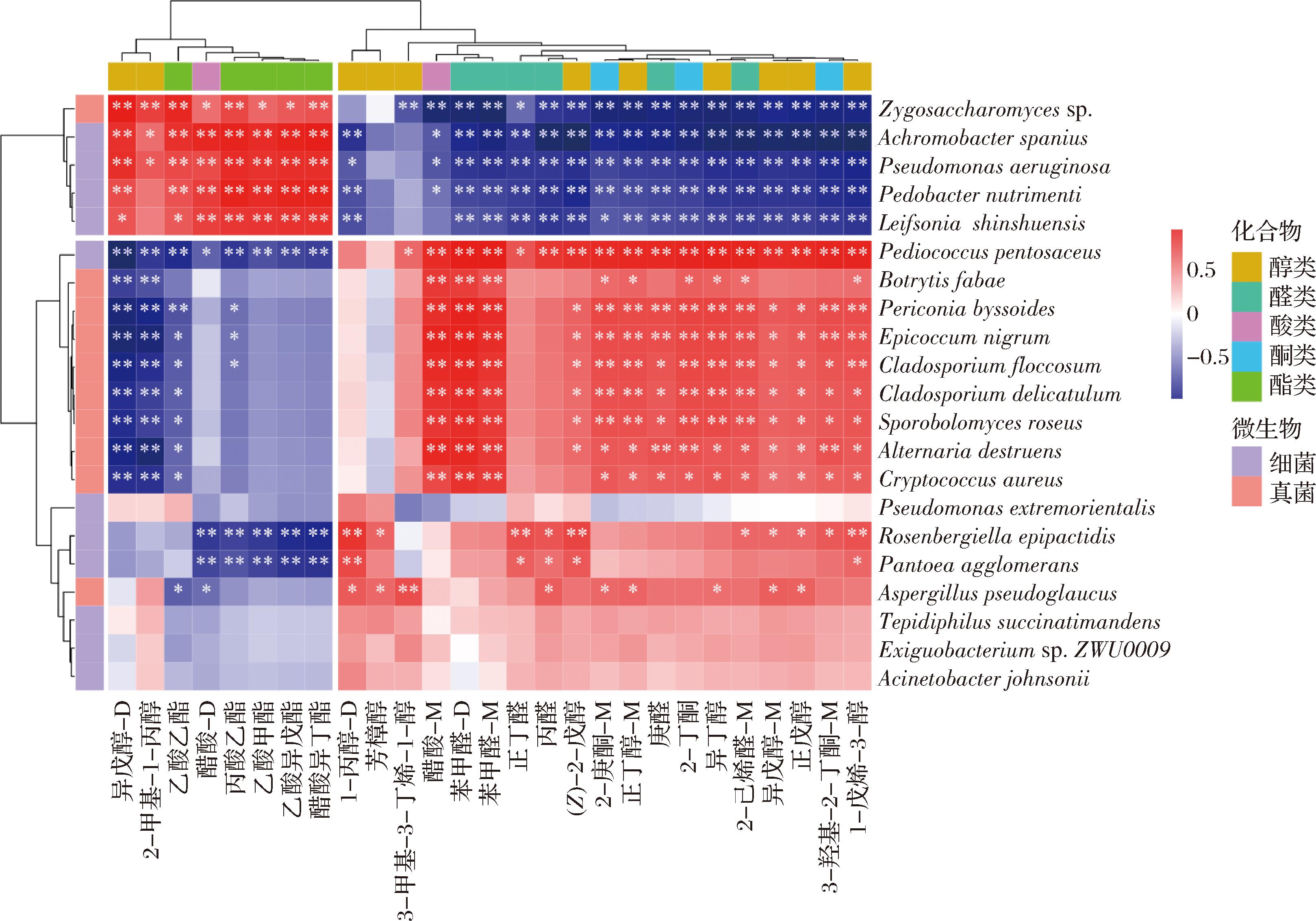
图7 低糖玫瑰酱的风味形成机制
Fig.7 Formation mechanism of flavor in low-sugar rose jam
3 结论
传统发酵玫瑰酱因其高糖环境抑制微生物生长繁殖,造成发酵周期长营养价值偏低等问题。为同时兼顾发酵玫瑰酱的营养及风味,对发酵结束的5种不同蔗糖与木糖醇配比的玫瑰酱进行感官评价;发现适度减糖(50%木糖醇)处理的发酵玫瑰酱具有较高的感官特性(具备明显的酸甜适中,质地均匀,整体接受性优良等特征)及理化特性(酸度、糖度、功能活性物质和抗氧化能力)等。同时对低糖玫瑰酱的风味物质进行分析后,发现低糖发酵后,玫瑰酱的醛类化合物(正丁醛)、醇类化合物(异戊醇、2-甲基-1丙醇、3-甲基-3-丁烯-1-醇)、酸类化合物(乙酸)和酯类化合物(乙酸乙酯)占比有所增加,挥发性风味物质的种类减少但含量增加,特征风味物质分布更集中。Zygosaccharomyces sp.、A.spanius、P.aeruginosa、P.nutrimenti和L.shinshuensis显著促进了醋酸异丁酯、乙酸异戊酯、乙酸甲酯、丙酸乙酯、醋酸-D、乙酸乙酯、2-甲基-1-丙醇和异戊醇-D等化合物的增加。本研究提出了木糖醇处理减糖发酵玫瑰酱的优势,并为减糖发酵生产其他产品提供理论依据。
[1] 杨文清. 玫瑰花酱的功能特性与香气研究[D].天津:天津科技大学, 2022.
YANG W Q.Study on functional properties and aroma of rose paste[D].Tianjin:Tianjin University of Science and Technology, 2022.
[2] 青舒婷, 杨丰, 张海仑, 等.远红外辅助热泵干燥食用玫瑰花瓣及产品品质分析[J].食品工业科技, 2021, 42(22):246-253.
QING S T, YANG F, ZHANG H L, et al.Far-infrared assisted heat pump drying of edible roses petals and the product quality analysis[J].Science and Technology of Food Industry, 2021, 42(22):246-253.
[3] LI M, ZI X J, ZHOU H L, et al.Effects of sucrose, glucose, molasses and cellulase on fermentation quality and in vitro gas production of king grass silage[J].Animal Feed Science and Technology, 2014, 197:206-212.
[4] GASMI BENAHMED A, GASMI A, ARSHAD M, et al.Health benefits of xylitol[J].Applied Microbiology and Biotechnology, 2020, 104(17):7225-7237.
[5] NOWICKA P, WOJDY O A.Stability of phenolic compounds, antioxidant activity and colour through natural sweeteners addition during storage of sour cherry puree[J].Food Chemistry, 2016, 196:925-934.
O A.Stability of phenolic compounds, antioxidant activity and colour through natural sweeteners addition during storage of sour cherry puree[J].Food Chemistry, 2016, 196:925-934.
[6] 罗亚楠. 云南传统玫瑰酱发酵过程中微生物和品质变化研究[D].昆明:云南农业大学, 2023.
LUO Y N.Study on microbial and quality changes during the fermentation process of Yunnan traditional rose jam[D].Kunming:Yunnan Agricultural University, 2023.
[7] 夏傲喃. 玫瑰酱中微生物多样性分析及优势菌群的鉴定[D].乌鲁木齐:新疆大学, 2022.
XIA A N.Analysis of microbial diversity and identification of dominant flora in rose jam[D].Urumqi:Xinjiang University, 2022.
[8] 陈璟, 任田, 赵子龙, 等.郫县豆瓣酱香气成分与感官评价[J].食品与机械, 2024, 40(4):34-39.
CHEN J, REN T, ZHAO Z L, et al.Aroma components and sensory evaluation of Pixian Douban sauce[J].Food and Machinery, 2024, 40(4):34-39.
[9] HUANG H, CEN J W, YANG D Q, et al.Isolation and characterization of antioxidant peptides from oyster (Crassostrea rivularis) protein enzymatic hydrolysates[J].Food Science &Nutrition, 2022, 11(1):261-273.
[10] RODR GUEZ-BONILLA P, GAND
GUEZ-BONILLA P, GAND A-HERRERO F, MATENCIO A, et al.Comparative study of the antioxidant capacity of four stilbenes using ORAC, ABTS+, and FRAP techniques[J].Food Analytical Methods, 2017, 10(9):2994-3000.
A-HERRERO F, MATENCIO A, et al.Comparative study of the antioxidant capacity of four stilbenes using ORAC, ABTS+, and FRAP techniques[J].Food Analytical Methods, 2017, 10(9):2994-3000.
[11] 许海棠, 马少姝, 张金彦.青天葵4种提取物抗氧化活性与其总黄酮和总酚含量的相关性[J].中成药, 2017, 39(1):121-125.
XU H T, MA S S, ZHANG J Y.Correlations between antioxidant activities and contents of total flavonoids and total phenols of four extracts from Nervilia fordii[J].Chinese Traditional Patent Medicine, 2017, 39(1):121-125.
[12] 韩红娟, 杨静, 陈晓, 等.树莓叶片中主要抗氧化物质提取工艺优化研究[J].云南大学学报(自然科学版), 2018, 40(2):321-331.
HAN H J, YANG J, CHEN X, et al.Study on optimization of extraction technology of main antioxidant substances in raspberry leaves[J].Journal of Yunnan University (Natural Science Edition), 2018, 40(2):321-331.
[13] PASQUET P L, JULIEN-DAVID D, ZHAO M, et al.Stability and preservation of phenolic compounds and related antioxidant capacity from agro-food matrix:Effect of pH and atmosphere[J].Food Bioscience, 2024, 57:103586.
[14] CARLSEN M H, HALVORSEN B L, HOLTE K, et al.The total antioxidant content of more than 3100 foods, beverages, spices, herbs and supplements used worldwide[J].Nutrition Journal, 2010, 9:3.
[15] ULLAH A, MUNIR S, BADSHAH S L, et al.Important flavonoids and their role as a therapeutic agent[J].Molecules, 2020, 25(22):5243.
[16] KHOO H E, AZLAN A, TANG S T, et al.Anthocyanidins and anthocyanins:Colored pigments as food, pharmaceutical ingredients, and the potential health benefits[J].Food &Nutrition Research, 2017, 61(1):1361779.
[17] DENG H H, XIA H, GUO Y Q, et al.Dynamic changes in ascorbic acid content during fruit development and ripening of Actinidia latifolia (an ascorbate-rich fruit crop) and the associated molecular mechanisms[J].International Journal of Molecular Sciences, 2022, 23(10):5808.
[18] 杨文清, 李梦茹, 李西西, 等.玫瑰酱的功能特性与香气成分分析[J].中国调味品, 2023, 48(3):156-160;169.
YANG W Q, LI M R, LI X X, et al.Analysis of functional properties and aroma components of rose sauce[J].China Condiment, 2023, 48(3):156-160;169.
[19] QIAO L N, WANG J, WANG R F, et al.A review on flavor of Baijiu and other world-renowned distilled liquors[J].Food Chemistry:X, 2023, 20:100870.
[20] ZHANG J H, CAO J, PEI Z S, et al.Volatile flavour components and the mechanisms underlying their production in golden pompano (Trachinotus blochii) fillets subjected to different drying methods:A comparative study using an electronic nose, an electronic tongue and SDE-GC-MS[J].Food Research International, 2019, 123:217-225.
[21] XU S Z, MA Z W, CHEN Y, et al.Characterization of the flavor and nutritional value of coconut water vinegar based on metabolomics[J].Food Chemistry, 2022, 369:130872.
[22] SUN D Y, QU J J, HUANG Y, et al.Analysis of microbial community diversity of muscadine grape skins[J].Food Research International, 2021, 145:110417.
[23] LENAERTS M, ALVAREZ-PÉREZ S, DE VEGA C, et al.Rosenbergiella australoborealis sp.nov., Rosenbergiella collisarenosi sp.nov.and Rosenbergiella epipactidis sp.nov., three novel bacterial species isolated from floral nectar[J].Systematic and Applied Microbiology, 2014, 37(6):402-411.
[24] XIA A N, LIU L X, TANG X J, et al.Dynamics of microbial communities, physicochemical factors and flavor in rose jam during fermentation[J].LWT, 2022, 155:112920.
[25] DE OLIVEIRA DUARTE F A, RAMOS K K, GINI C, et al.Microbiological characterization of kombucha and biocellulose film produced with black tea and cocoa bean shell infusion[J].Food Research International, 2024, 190:114568.
[26] SEMJONOVS P, ZIKMANIS P.Evaluation of novel lactose-positive and exopolysaccharide-producing strain of Pediococcus pentosaceus for fermented foods[J].European Food Research and Technology, 2008, 227(3):851-856.
[27] LIANG H P, HE Z, WANG X Y, et al.Bacterial profiles and volatile flavor compounds in commercial Suancai with varying salt concentration from Northeastern China[J].Food Research International, 2020, 137:109384.