铁作为人体必需的微量元素,主要存在于肌红蛋白和血红蛋白中,参与细胞能量代谢、免疫功能调节以及大脑发育等多种重要生理过程。此外,大脑中铁含量的失衡会导致多种神经退行性疾病(如肌萎缩侧索硬化症、阿尔茨海默病和帕金森病)的发生[1]。然而,饮食计划不合理、饮食结构不均衡以及环境因素都可能导致缺铁性贫血。因此,针对铁补充剂的功能性食品和保健食品的研究正逐渐增多。其中,铁盐存在生物利用率低、口感差等问题,而肽铁螯合物作为第4代铁补充剂,能够有效防止体内游离金属的拮抗作用以及食物中植酸对金属离子的沉淀作用,因此展现出更强的化学稳定性、更高的吸收率和更好的生物利用度[2-3]。
花生粕(peanut meal,PM)作为油脂制取工业的重要副产品,富含蛋白质、多糖和酚类化合物等营养及功能成分。凭借其高蛋白含量,花生粕被认为是蛋白质回收和制备生物活性肽的绝佳原料。然而,受限于传统榨油工艺的高温过程,花生粕中蛋白质变性程度高,通常被用作饲料或直接丢弃,这不仅造成了环境污染,还降低了经济资源的利用率。近年来的研究表明,通过不同的加工处理方式,花生粕中的蛋白质可以得到有效利用[4]。目前,已有研究从大麦[5]、鹰嘴豆[6]、核桃[7]、绿豆[8]等多种植物蛋白中鉴定并纯化出了不同的铁螯合肽。
微生物发酵法因其水解效率高、产品质量稳定等多重优势,作为一种新型方法,在制备生物活性肽领域受到广泛关注。此外,发酵技术相较于酶解法,成本较低且能生产出具有较强铁亲和力的多肽[9]。然而,目前利用微生物发酵法从花生粕中制备金属螯合肽的报道较少。
因此,本研究采用红曲霉和枯草芽孢杆菌发酵法从花生粕中获得花生肽,与Fe2+结合制备肽铁螯合物。首先优化了花生肽与铁的螯合条件。然后,通过光谱学分析、氨基酸组成分析以及构象特征分析,深入探究了花生肽与亚铁离子的结合特性,并对花生肽铁螯合物的稳定性进行了初步研究。总之,本研究成功地建立了一种利用花生粕生产铁螯合肽的新方法。这些研究结果对提升花生粕的附加价值具有重要意义,并为开发用于预防和治疗缺铁症的花生肽铁螯合物提供了科学依据。
1 材料与方法
1.1 材料与试剂
花生粕,山东金胜粮油食品有限公司;枯草芽孢杆菌CICC10732、红曲霉CICC40704,中国工业微生物菌种保藏管理中心;FeCl2·4H2O,上海源叶生物科技有限公司;L-抗坏血酸、盐酸羟胺、邻菲啰啉,天津市科密欧化学试剂有限公司;无水乙醇,天津市天力化学试剂有限公司。
1.2 仪器与设备
SPX-250B-Z生化培养箱,上海博讯实业有限公司医疗设备厂;LGJ-18冷冻干燥机,北京四环科学仪器厂;S433D氨基酸分析仪,德国慕尼黑塞卡姆有限公司;Zetasizer Nano ZSP纳米粒度及zeta电位分析仪,英国Malvern公司;TU-1900紫外可见分光光度计,北京普析通用仪器有限公司;WQF-510傅里叶变换红外光谱仪,北京瑞丽分析仪器有限公司;Quanta 250 FEG扫描电子显微镜,美国FEI公司;SCL-10AVP 高效液相色谱,日本岛津公司。
1.3 实验方法
1.3.1 发酵花生粕水解物(fermented peanut meal hydrolysate, FPMH)的制备
枯草芽孢杆菌在LB培养基中培养18~24 h,温度37 ℃,转速180 r/min;红曲霉在PDB培养基中培养3~5 d,温度30 ℃,转速160 r/min。收集菌液并将最终浓度调整为107 CFU/mL。
花生粕粉碎后过80目筛,121 ℃灭菌20 min。发酵条件控制为:温度31 ℃,湿度65%,接种量6%。菌种比例为红曲霉与枯草芽孢杆菌2∶1,发酵过程持续96 h,期间每隔12 h取样1次。
发酵结束后,将样品置于60 ℃烘箱中干燥8 h,随后在-20 ℃下贮存。将2 g发酵花生粕粉末加入20 mL水中,室温下以120 r/min搅拌浸提1 h,随后以8 000 r/min离心30 min,收集FPMH。
1.3.2 水解物铁螯合物(fermented peanut meal hydrolysate iron chelate, FPMH-Fe)的制备
FPMH-Fe螯合物的制备参照FAN等[10]的方法,并略作修改。称取适量FPMH,配成溶液,并调节pH值至7.0。将FPMH溶液与FeCl2·4H2O和抗坏血酸按照3∶1的质量比混合均匀,置于一定温度的水浴锅中进行反应。反应完成后,向混合物中加入5倍体积的无水乙醇,使FPMH-Fe螯合物沉淀析出。随后,将溶液在9 703 r/min离心10 min,收集沉淀并进行冷冻干燥,最终得到FPMH-Fe螯合物。
1.3.3 单因素试验
根据影响螯合反应进程的因素,选择4个主要因素来优化FPMH的亚铁螯合能力,即多肽浓度、pH、温度和时间。基础反应条件为多肽质量浓度15 mg/mL,pH 7,温度40 ℃,反应时间30 min。
1.3.4 响应面试验
在单因素试验的基础上以螯合率为响应值,采用Box-Behnken中心组合进一步优化反应条件,响应面因素与水平见表1。
表1 响应面因素与水平
Table 1 Response surface factors and levels

编码因素水平-101A时间/min204060BpH678C温度/℃506070D多肽质量浓度/(mg/mL)51525
1.3.5 螯合活性测定
FPMH-Fe螯合物中铁含量的测定参照WU等[11]的方法,并略作修改。铁标准曲线绘制:分别取0、2、4、6、8、10 mL的10 μg/mL铁标准溶液置于50 mL容量瓶中,依次加入1 mL 100 g/L的盐酸羟胺溶液,2 mL 1.5 g/L的邻菲啰啉溶液,5 mL的乙酸乙酸钠溶液(pH值为5.0),定容到50 mL,摇匀,静置反应30 min,取200 μL置于96孔板中,测定其在510 nm处的吸光度。
取反应后的亚铁螯合物溶液5 mL,加入5倍的无水乙醇,静置2 h,6 861 r/min离心10 min,将沉淀置于酸性介质中将铁从螯合物中解离出来后用去离子水溶解定容至100 mL,按照标准曲线的步骤测定吸光度。铁螯合率和铁螯合产率分别根据公式(1)和公式(2)计算。
螯合率![]()
(1)
螯合产率![]()
(2)
式中:m0,加入反应体系中的总铁质量,mg;m1,FPMH-Fe 螯合物中的铁质量,mg;m2,FPMH-Fe螯合物的总质量,g。
1.3.6 水解度测定
参照程赞等[12]的方法,采用邻苯二甲醛(o-phthalaldehyde,OPA)法进行测定。将3 mL OPA试剂(现用现配)与400 μL待测样品混合,反应2 min后在340 nm处测定吸光度。根据公式(3)计算水解度:
水解度![]()
(3)
式中:h,水解的肽键数;htot,总肽键数。
1.3.7 分子质量分布
参照YAN等[9]的方法,并稍作修改。使用HPLC测量FPMH的分子质量分布。使用 TSK Gel 2000 SWXL 色谱柱(300 mm×7.8 mm,5 μm),流速为0.5 mL/min,色谱柱温度保持在25 ℃。流动相由0.1%(体积分数)三氟乙酸、45%(体积分数)乙腈和54.9%(体积分数)超纯水组成。过滤(使用0.22 μm滤膜)后,使用流动相制备2 mg/mL的FPMH。
1.3.8 傅里叶变换红外光谱测定
将FPMH、FPMH-Fe、FeCl2·4H2O以及FPMH与FeCl2·4H2O的物理混合物的冻干粉末分别与KBr按1∶100的质量比混合研磨,压制成薄片后,使用傅里叶变换红外光谱仪进行扫描分析。扫描范围为4 000~400 cm-1,以4 cm-1的分辨率进行64次扫描。
1.3.9 氨基酸分析
准确称取45 mg样品于20 mL厌氧管中,加入10 mL 6 mol/L的HCl和3~4滴苯酚,用高纯度N2吹5 min,立即拧紧盖子置于110 ℃水解22 h,冷却后,将溶液混匀并过滤,定容至100 mL,取适量滤液置于试管浓缩仪中蒸干,加入1 mL缓冲液溶解混匀,经0.22 μm滤膜后,转移至液相进样瓶中使用氨基酸分析仪分析水解物。
1.3.10 紫外可见吸收光谱学
将FPMH和FPMH-Fe粉末配制成0.2 mg/mL的溶液,使用紫外-可见分光光度计在190~400 nm波长进行全波长扫描。
1.3.11 圆二色光谱(circular dichroism,CD)
将FPMH和FPMH-Fe螯合物配制成0.2 mg/mL的溶液,然后使用CD仪测量。光谱扫描范围190~260 nm,扫描速度1 nm/s。然后用CDNN分析软件分析色谱数据并计算二级结构。
1.3.12 粒径和电位
将FPMH和FPMH-Fe螯合物配成0.5 mg/mL的溶液,采用纳米粒度及zeta电位分析仪,在固定散射角度90 °,25 ℃下平衡60 s,测定粒径、zeta电位和多分散性指数(polydispersity index,PDI)。
1.3.13 扫描电镜
取适量的FPMH及FPMH-Fe,经固定、喷金后分别在1 000×、5 000×和10 000×的放大倍数下观察样品表面形态特征。
1.3.14 稳定性
参照WU等[13]的方法,并稍作修改,将FPMH-Fe配制成1 mg/mL的溶液,用1 mol/L的HCl或NaOH溶液调节pH值至2.0、4.0、6.0、8.0和10.0,分别在25、40、55、70、85 ℃,静置1 h。加入5倍体积的无水乙醇,混合后在常温下放置1 h,然后在4 000×g转速下离心10 min。收集上清液,按照1.3.5节步骤测定其游离铁离子含量。游离铁含量的计算如公式(4)所示:
游离铁释放量![]()
(4)
式中:m1,测得的游离铁质量,mg;m0,FPMH-Fe螯合物的铁质量,mg。
1.4 统计分析
所有实验均重复测定3次,结果表示为“平均值±标准差”。使用SPSS 27.0进行统计分析,以Duncans多重比较法进行显著性差异分析,采用Origin 2024绘图。
2 结果与分析
2.1 水解度对螯合率的影响
金属螯合能力的差异可能源自于金属离子与肽结构之间的化学和物理性质的不同。水解度是发酵的一个重要指标,因为它与水解产物的功能直接相关[14]。然而,FPMH铁结合能力与水解度之间没有明显的线性关系,适当的水解对于获得具有高铁螯合能力的水解物至关重要。由图1-a可知,随着发酵时间的延长,FPMH的水解度呈现出先增加后逐渐稳定的趋势。FPMH的铁结合能力整体随着发酵时间的延长而增强,并在72 h达到峰值,随后略有下降。其原因可能是水解度过低,多肽的螯合位点暴露较少,导致与Fe2+结合不充分;然而水解度过高,大部分多肽易被进一步水解成氨基酸或者短肽,螯合位点被破坏,也不利于螯合反应的进行。
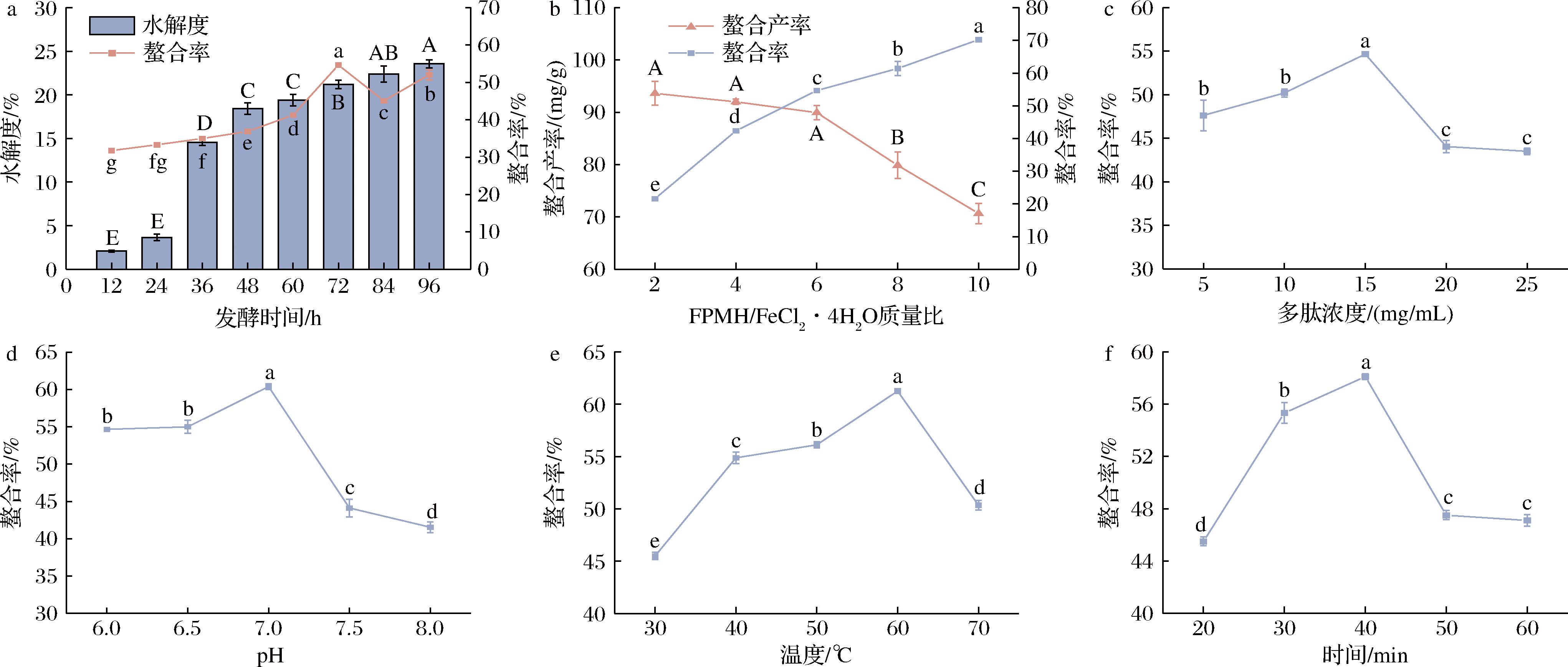
a-发酵时间对水解度和螯合率的影响;b-肽铁比对螯合率和螯合产率的影响;c-多肽浓度对螯合率的影响;d-pH对螯合率的影响;e-温度对螯合率的影响;f-时间对螯合率的影响
图1 肽铁螯合工艺参数优化
Fig.1 Optimization of peptide iron chelation process parameters
注:不同小写字母表示差异显著(P<0.05)(下同)。
2.2 肽铁比对螯合率及螯合产率的影响
如图1-b所示,当FPMH与Fe2+的质量比从2∶1调整至10∶1时,随着肽与铁比例的增加,铁离子螯合率从(21.61±0.31)%增加到(70.23±0.81)%,而螯合产率从(93.62±3.94) mg/g降低到(70.69±3.36) mg/g。由于多肽的铁螯合位点有限,导致其在铁离子浓度升高时配位不完全,从而使部分铁离子以游离态存在于溶液中。当肽铁的比例达到6∶1时,螯合率和螯合产率都达到了一个相对理想的平衡点,既能有效利用资源又避免浪费,同时保证螯合产率处于一个合理的水平。因此,选择肽铁比为6∶1来进行后续的实验。
2.3 单因素分析
2.3.1 多肽浓度对螯合率的影响
如图1-c所示,铁螯合率会随着溶液中多肽浓度的变化而变化。当溶液中多肽浓度增加时,Fe2+与多肽之间的接触面积可能因多肽分子间的聚集效应而减少,Fe2+与多肽结合位点之间的碰撞几率也随之降低[10]。肽分子之间对Fe2+的竞争加剧,从而导致单位质量的FPMH-Fe螯合产物所结合的Fe2+的量减少。
2.3.2 pH对螯合率的影响
图1-d展示了在不同pH值条件下进行螯合反应所得到的FPMH-Fe螯合物的铁螯合率。结果显示,在pH=7条件下,铁的螯合率最高,达到(60.38±0.67)%。而当pH值偏离中性,无论是升高还是降低,铁的螯合率均有所下降,这与ATHIRA等[15]的研究结果一致,即pH值的变化会影响肽的构象,并显著改变肽的结合能力。在酸性环境下,溶液中的H+会与Fe2+竞争肽中的金属位点结合。同时,肽中氨基酸的活性基团会发生质子化,从而降低它们对阳离子的亲和力。而在碱性环境下,Fe2+容易生成Fe(OH)2沉淀,从而抑制螯合反应的进行[16]。
2.3.3 温度对螯合率的影响
温度会对金属配体的相互作用造成影响。如图1-e所示,当温度从30 ℃升高至60 ℃时,铁螯合率明显升高,在60 ℃时达到(61.25±0.37)%。然而随着温度从60 ℃升高至70 ℃,螯合能力有所下降。这可能是由于花生粕发酵水解物中含有大分子多糖和包裹多肽的酯类。因此,适当的高温可以增强分子间的热运动,从而增加多肽与金属离子碰撞的机会[3]。但是,过高的温度会破坏多肽的结构使其功能丧失,从而不利于其螯合反应的进行。
2.3.4 时间对螯合率的影响
铁的螯合反应是一个快速过程,能够迅速达到平衡。如图1-f所示,在反应进行40 min时,螯合反应基本完成,此时螯合率达到(58.10±0.37)%。然而,随着反应时间的进一步延长,部分螯合物可能会发生解离。因此确定螯合时间为40 min。
2.4 响应面分析
2.4.1 回归模型分析
响应面试验设计及结果如表2所示。对选定的时间、pH、温度和多肽浓度4个因素进行线性回归拟合,可得二次多项回归方程模型:
表2 响应面试验设计及结果
Table 2 Response surface experimental design and results
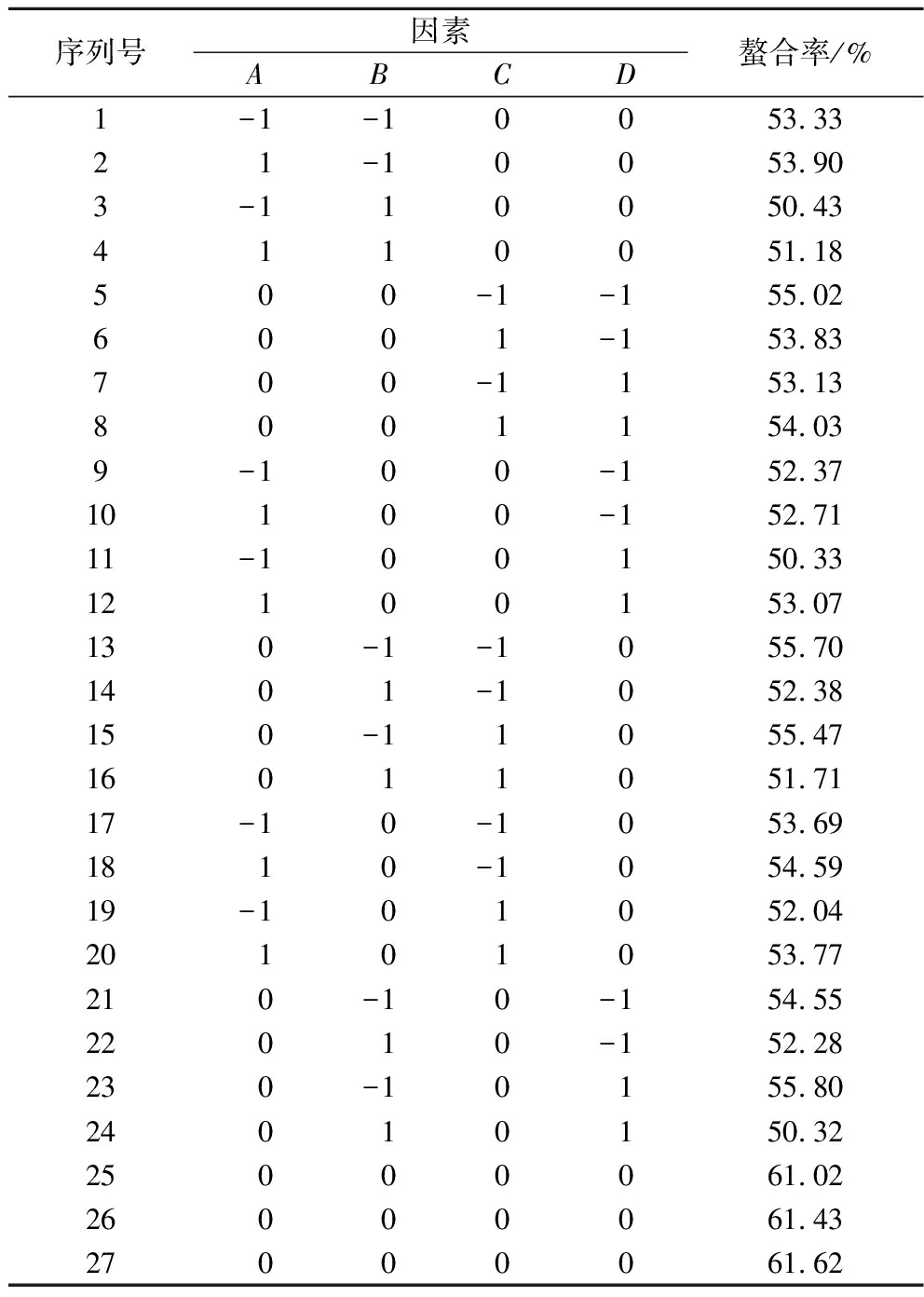
序列号因素ABCD螯合率/%1-1-10053.3321-10053.903-110050.434110051.18500-1-155.026001-153.83700-1153.138001154.039-100-152.3710100-152.7111-100150.3312100153.07130-1-1055.701401-1052.38150-11055.4716011051.7117-10-1053.691810-1054.5919-101052.0420101053.77210-10-154.5522010-152.28230-10155.8024010150.3225000061.0226000061.4327000061.62
Y=61.36+0.59A-1.70B-0.31C-0.34D+0.05AB+0.21AC+0.60AD-0.11BC-0.80BD+0.52CD-4.90A2-4.20B2-3.16C2-4.15D2
回归模型的方差分析见表3。此响应面的模型极显著,失拟项不显著,表明模型能较好地契合研究所选因素对螯合率的影响。回归方程![]() 两者数值比较接近,表明回归方程与实际实验适配度较高。
两者数值比较接近,表明回归方程与实际实验适配度较高。
表3 回归模型的方差分析
Table 3 ANOVA of the regression model
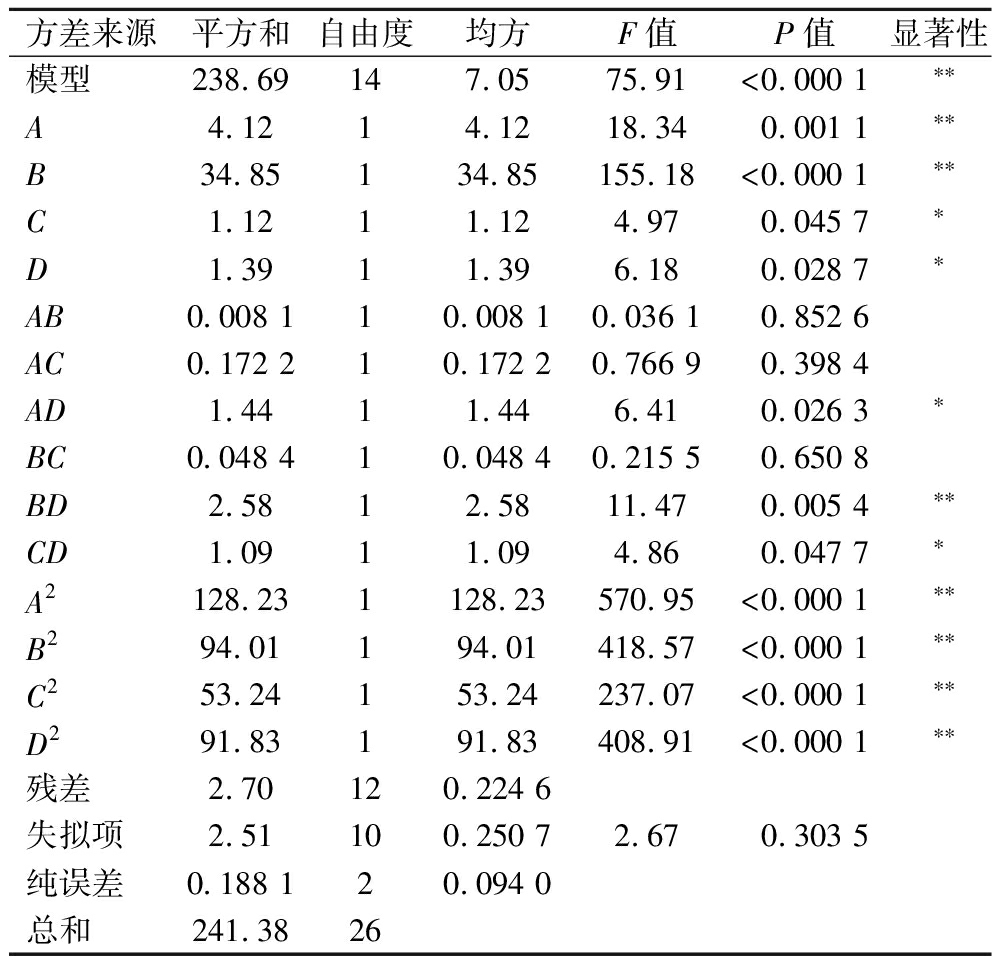
方差来源平方和自由度均方F值P值显著性模型238.69147.0575.91<0.000 1∗∗A4.1214.1218.340.001 1∗∗B34.85134.85155.18<0.000 1∗∗C1.1211.124.970.045 7∗D1.3911.396.180.028 7∗AB0.008 110.008 10.036 10.852 6AC0.172 210.172 20.766 90.398 4AD1.4411.446.410.026 3∗BC0.048 410.048 40.215 50.650 8BD2.5812.5811.470.005 4∗∗CD1.0911.094.860.047 7∗A2128.231128.23570.95<0.000 1∗∗B294.01194.01418.57<0.000 1∗∗C253.24153.24237.07<0.000 1∗∗D291.83191.83408.91<0.000 1∗∗残差2.70120.224 6失拟项2.51100.250 72.670.303 5纯误差0.188 120.094 0总和241.3826
注:*表示差异显著(P<0.05);**表示差异极显著(P<0.01)。
2.4.2 交互作用分析
由表3中显著性分析可得,时间与pH、时间与温度之间的交互作用不显著,时间与多肽浓度、温度与多肽浓度之间交互作用显著;pH与多肽浓度之间交互作用极显著。利用Design-Expert软件分析的得到最佳螯合条件为时间41.13 min、pH 6.8、温度59.56 ℃、多肽质量浓度14.8 mg/mL,预测螯合率达到61.55%。考虑到实际情况,将时间调整为41 min,温度调整为59.5 ℃,实测值[螯合率为(61.45±0.28)%]与预测值接近,代表模型契合度较高。
2.5 分子质量分布
图2展示了FPMH的分子质量分布情况,分子质量<1 000 Da的肽段占比达到(82.10±0.28)%,是FPMH的主要成分。表明FPMH主要由小分子多肽构成。多肽的分子质量与其对金属离子的螯合活性有关。一般来说,分子质量较小的肽由于其结构较为松散,更容易暴露出活性基团而有利于与Fe2+形成螯合物[17]。此外,较小体积的肽由于氨基和羧基的比例较高,可能会展现出更高的铁螯合活性[18]。SUN等[19]的报道显示,海参卵水解物的铁螯合能力随着分子质量的减小而显著增加。
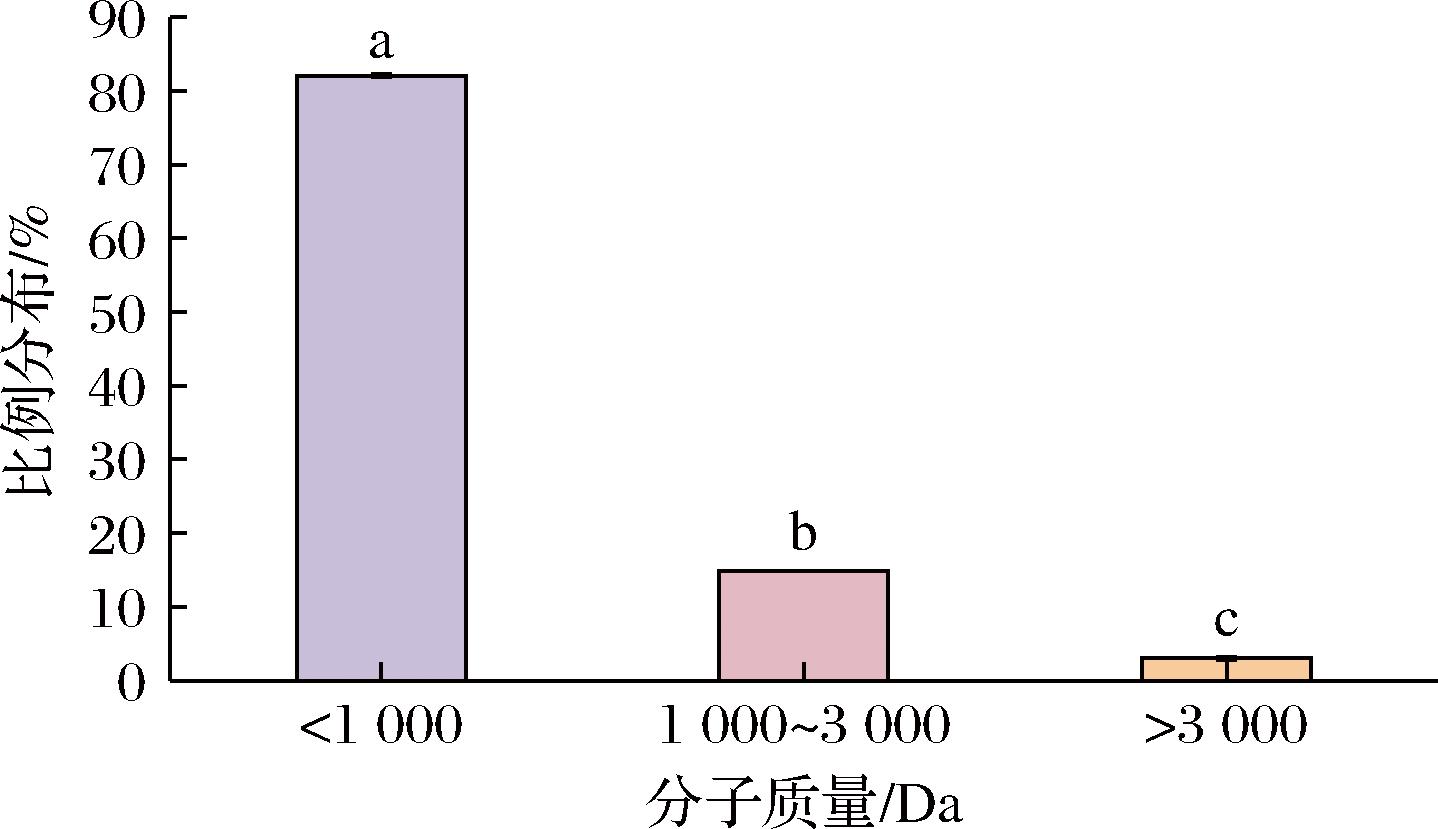
图2 分子质量分布
Fig.2 Molecular weight distribution
2.6 傅里叶变换红外光谱
红外光谱吸收峰的变化、增加和损失可以反映金属离子与肽中有机配体之间的相互作用。如图3所示,在FPMH-Fe螯合物的红外光谱分析中,指纹区和功能区的吸收峰的变化表明,Fe2+的存在可能引起了肽构象的显著变化,而这种变化与FeCl2以及FeCl2和FPMH的简单混合物存在明显差异。多肽和蛋白质的红外光谱与其他化合物的区别在于其特征性的酰胺I带(1 700~1 600 cm-1)和酰胺Ⅱ带(1 600~1 500 cm-1),这2条带是与酰胺基团相关的2个重要特征吸收带。其中,酰胺I带的吸收主要源于酰胺基团中C![]() O键的伸缩振动,而酰胺Ⅱ带的吸收则主要归因于N—H键的弯曲振动[15]。与FPMH相比,FPMH-Fe螯合物在铁络合后的吸收峰从1 642.36 cm-1向高波数移动(1 657.45 cm-1),表明C
O键的伸缩振动,而酰胺Ⅱ带的吸收则主要归因于N—H键的弯曲振动[15]。与FPMH相比,FPMH-Fe螯合物在铁络合后的吸收峰从1 642.36 cm-1向高波数移动(1 657.45 cm-1),表明C![]() O基团可能与Fe2+结合,从而生成了C—O—Fe键[19]。在1 600.27 cm-1处,FeCl2显示出一个显著的吸收峰,这可能源自其配位振动。区别于FPMH-Fe螯合物,当FeCl2与FPMH简单混合时,这一特征峰并未发生明显变化,表明其螯合物是一种与简单混合物不同的新物质。由于肽键的平面N—H变形,酰胺Ⅱ峰从1 541.77 cm-1移动到1 540.60 cm-1,这提示酰胺中的羰基和N—H基团可能参与了铁的结合反应[20]。此外,在3 292.85 cm-1处的高波段吸收峰可归因于N—H键的振动,而与铁螯合后,FPMH的特征峰蓝移至3 349.92 cm-1。这一变化可能是因为N原子能够提供电子对与铁离子形成配位键,从而取代了原有的氢键[19]。上述结果表明,FPMH与铁结合位点主要对应于羧基氧原子和氨基氮原子。
O基团可能与Fe2+结合,从而生成了C—O—Fe键[19]。在1 600.27 cm-1处,FeCl2显示出一个显著的吸收峰,这可能源自其配位振动。区别于FPMH-Fe螯合物,当FeCl2与FPMH简单混合时,这一特征峰并未发生明显变化,表明其螯合物是一种与简单混合物不同的新物质。由于肽键的平面N—H变形,酰胺Ⅱ峰从1 541.77 cm-1移动到1 540.60 cm-1,这提示酰胺中的羰基和N—H基团可能参与了铁的结合反应[20]。此外,在3 292.85 cm-1处的高波段吸收峰可归因于N—H键的振动,而与铁螯合后,FPMH的特征峰蓝移至3 349.92 cm-1。这一变化可能是因为N原子能够提供电子对与铁离子形成配位键,从而取代了原有的氢键[19]。上述结果表明,FPMH与铁结合位点主要对应于羧基氧原子和氨基氮原子。
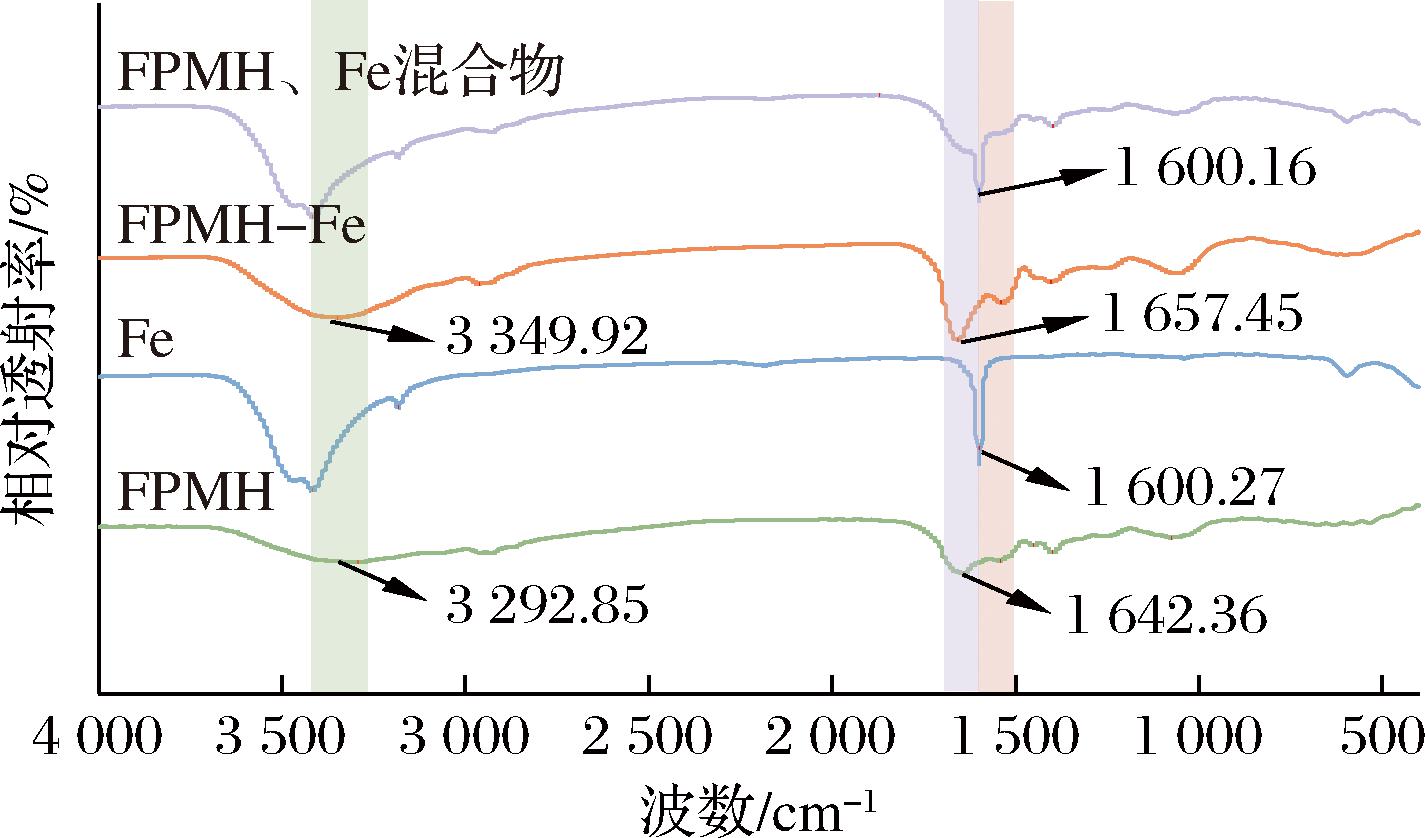
图3 FPMH、Fe混合物,FPMH-Fe,Fe和FPMH的红外光谱
Fig.3 Infrared spectra of FPMH,Fe mixtures, FPMH-Fe, Fe and FPMH
2.7 氨基酸分析
多肽的金属螯合能力受其氨基酸组成及其侧链基团特性的影响[21]。表4列出了花生粕(PM)、FPMH和FPMH-Fe的氨基酸组成。与PM相比,FPMH的氨基酸总量更高,表明发酵能提升花生粕的营养特性,并改变氨基酸比例。在FPMH中,Asp和Glu的含量显著高于其他氨基酸(P<0.05),且在与Fe2+螯合后,这2种氨基酸的相对含量均有所增加。CAETANO-SILVA等[22]从乳清蛋白水解物中分离纯化的肽段中,超过80%的肽段含有Asp,表明酸性氨基酸在金属螯合反应中发挥着重要作用。推测是因为羧基氧中的自由电子捐献给Fe2+空轨道,且去质子化之后的羧酸根离子(—COO-)可以与Fe2+通过配位作用结合,从而提升FPMH的铁结合能力[23]。此外,SUN等[19]的研究表明,His和Arg的含量与铁结合能力呈正相关性。其中,His因其含有N-咪唑环直接参与肽与金属离子的结合,而具有更高的结合能力。这与本研究中,FPMH与Fe2+结合后,His和Arg含量升高的结果一致。
表4 PM、FPMH和FPMH-Fe的氨基酸组成
Table 4 Amino acid composition of PM, FPMH, and FPMH-Fe
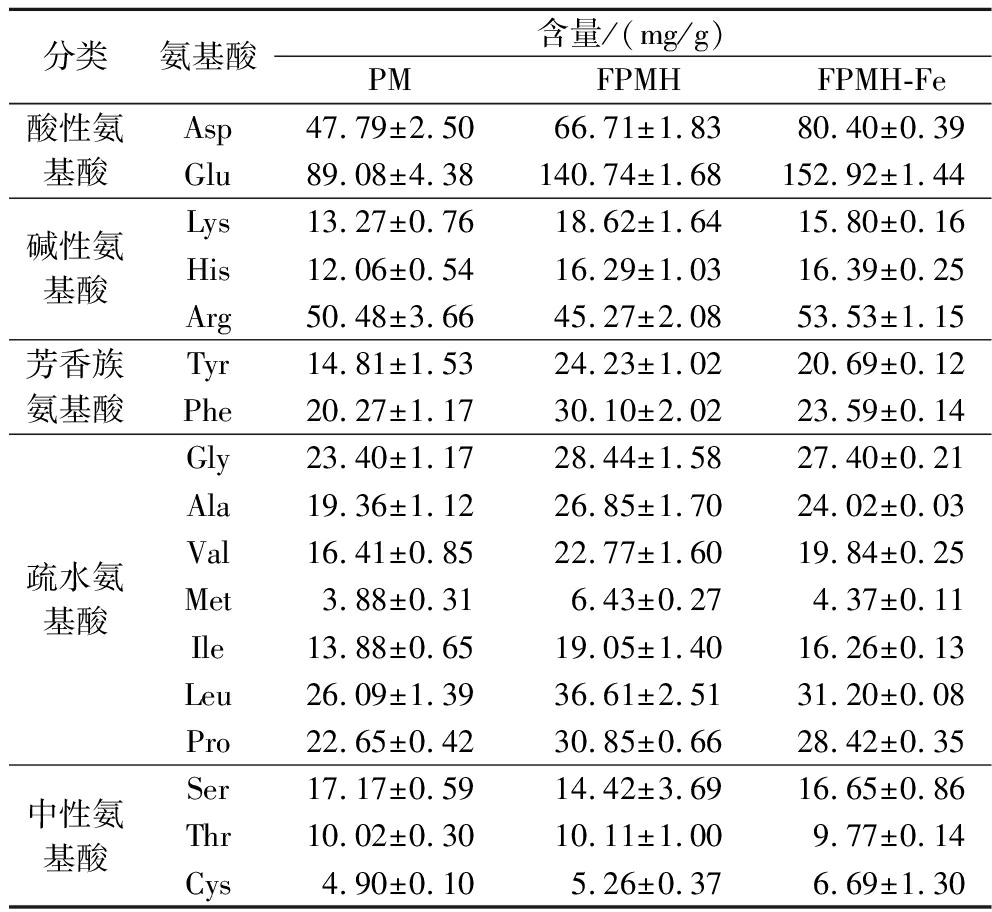
分类氨基酸含量/(mg/g)PMFPMHFPMH-Fe酸性氨基酸Asp47.79±2.5066.71±1.8380.40±0.39Glu89.08±4.38140.74±1.68152.92±1.44碱性氨基酸Lys13.27±0.7618.62±1.6415.80±0.16His12.06±0.5416.29±1.0316.39±0.25Arg50.48±3.6645.27±2.0853.53±1.15芳香族氨基酸Tyr14.81±1.5324.23±1.0220.69±0.12Phe20.27±1.1730.10±2.0223.59±0.14疏水氨基酸Gly23.40±1.1728.44±1.5827.40±0.21Ala19.36±1.1226.85±1.7024.02±0.03Val16.41±0.8522.77±1.6019.84±0.25Met3.88±0.316.43±0.274.37±0.11Ile13.88±0.6519.05±1.4016.26±0.13Leu26.09±1.3936.61±2.5131.20±0.08Pro22.65±0.4230.85±0.6628.42±0.35中性氨基酸Ser17.17±0.5914.42±3.6916.65±0.86Thr10.02±0.3010.11±1.009.77±0.14Cys4.90±0.105.26±0.376.69±1.30
2.8 紫外可见吸收光谱
如图4所示,通过紫外光谱扫描花生肽及其铁螯合物,花生肽的特征吸收峰出现在205 nm和271 nm处。205 nm的吸收峰主要归因于分子中羰基(C![]() O)的伸缩振动,而271 nm的吸收峰则主要是由于肽中的色氨酸、酪氨酸和苯丙氨酸等芳香族氨基酸所引起的紫外吸收特性[24]。随着添加不同比例的Fe2+,花生肽在205 nm处的最大吸收峰出现了不同程度的蓝移,250~300 nm附近的特征峰消失且吸收强度增加。在FPMH与Fe2+螯合过程中,芳香氨基酸的电荷迁移导致FPMH-Fe在271 nm处的吸收峰消失[15]。原吸光度峰移动或消失,提示FPMH-Fe螯合物形成了新的结构。
O)的伸缩振动,而271 nm的吸收峰则主要是由于肽中的色氨酸、酪氨酸和苯丙氨酸等芳香族氨基酸所引起的紫外吸收特性[24]。随着添加不同比例的Fe2+,花生肽在205 nm处的最大吸收峰出现了不同程度的蓝移,250~300 nm附近的特征峰消失且吸收强度增加。在FPMH与Fe2+螯合过程中,芳香氨基酸的电荷迁移导致FPMH-Fe在271 nm处的吸收峰消失[15]。原吸光度峰移动或消失,提示FPMH-Fe螯合物形成了新的结构。
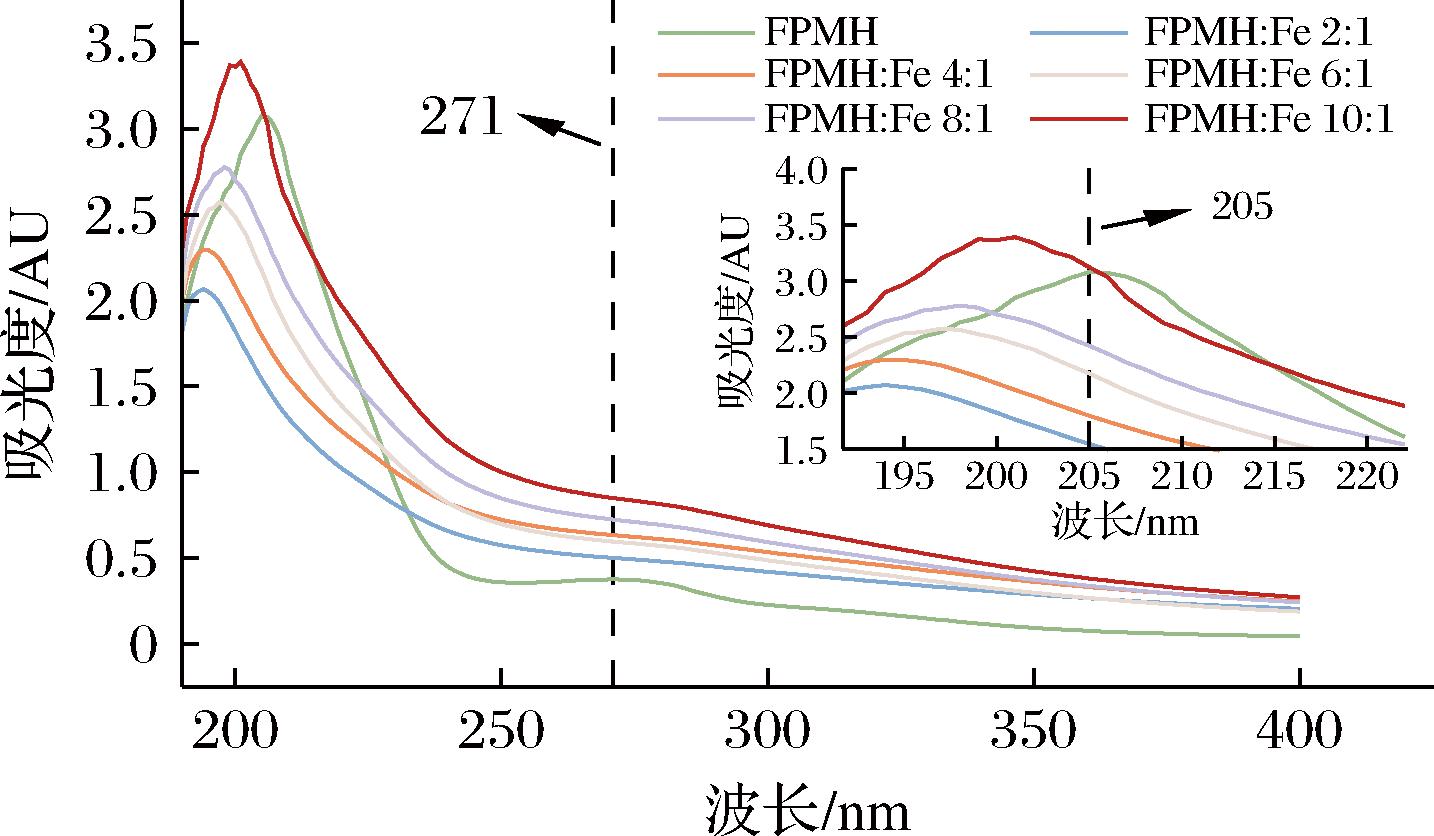
图4 不同肽铁比作用下的FPMH的紫外光谱
Fig.4 UV spectra of FPMH in the presence of different peptide-iron ratios
2.9 CD和二级结构分析
CD是研究“远紫外”光谱区(190~260 nm)蛋白质或肽二级结构的一种有效方法。图5展示了FPMH和FPMH-Fe的CD图。如图6所示,FPMH的二级结构由4种不同的构象组成,包括α-螺旋、β-折叠、β-转角和无规则卷曲。FPMH与Fe2+结合后,β-折叠与β-转角增加,α-螺旋与无规则卷曲减少。这表明Fe2+诱导了FPMH结构的转变,促进了多肽的折叠,形成了更加紧密的二级结构。这与先前的研究结果相符,即金属离子有助于β-折叠结构的形成,促进肽与铁的螯合[25-26]。
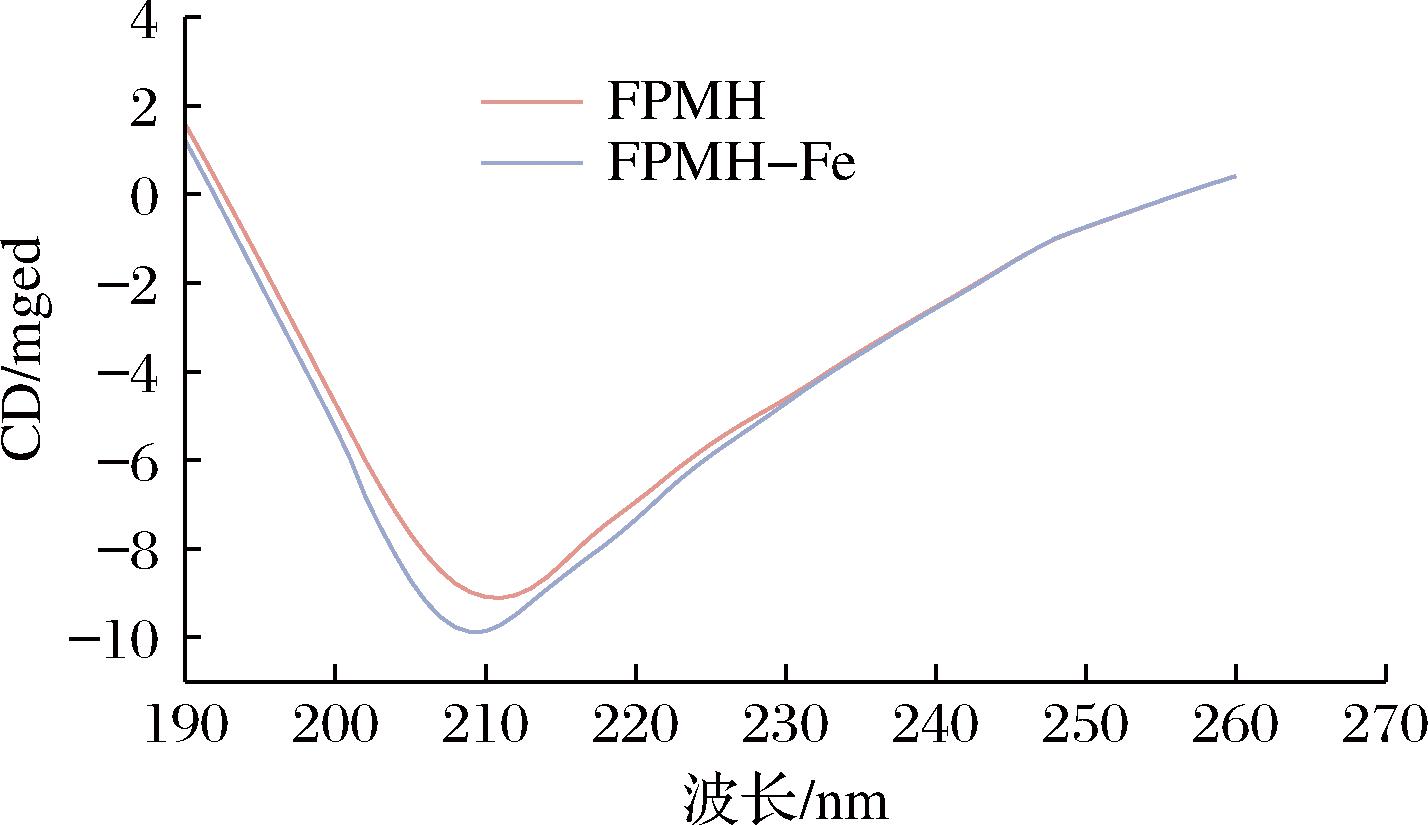
图5 FPMH和FPMH-Fe的CD
Fig.5 Circular dichroism spectra of FPMH and FPMH-Fe
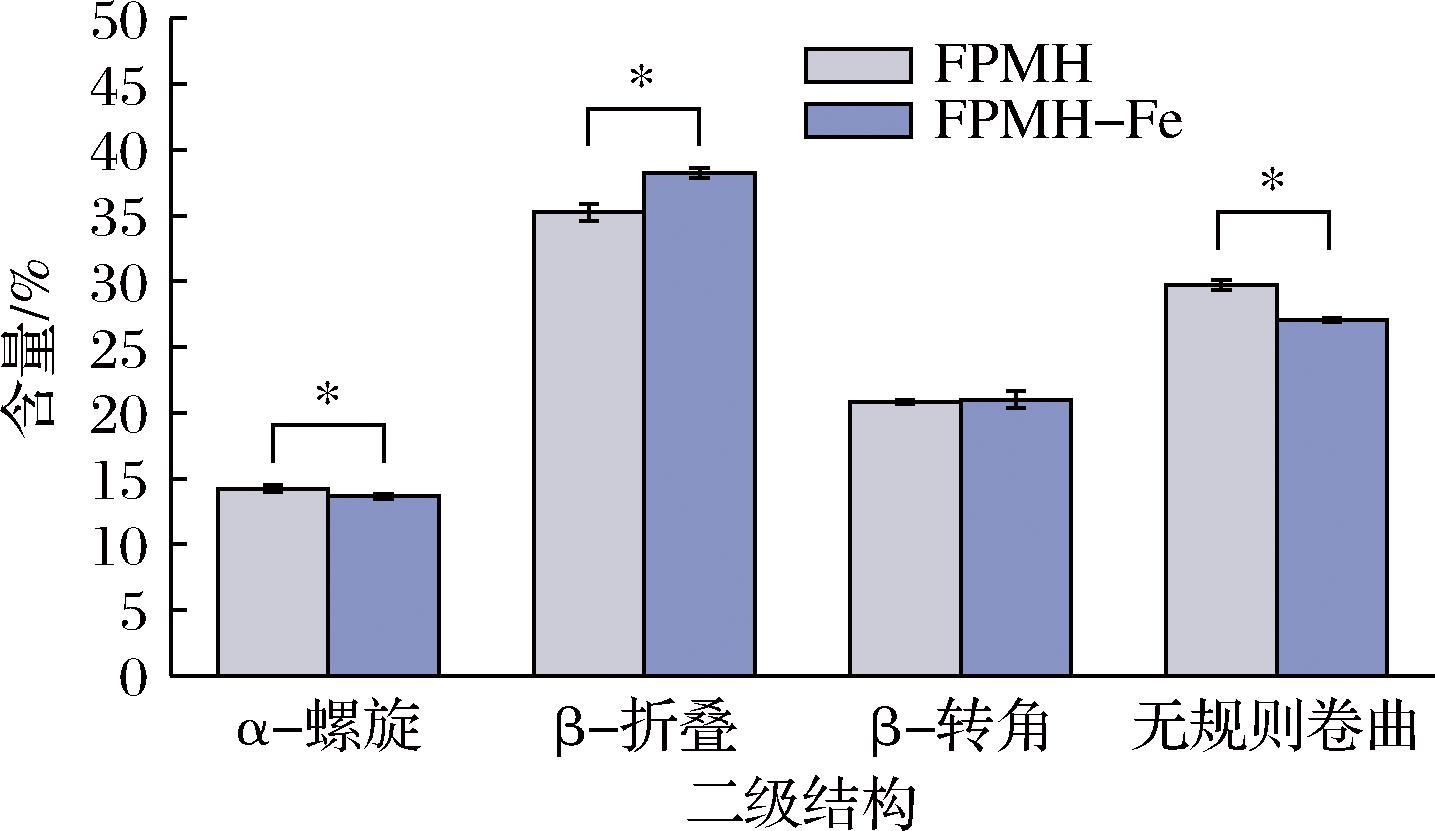
图6 FPMH和FPMH-Fe的二级结构
Fig.6 Secondary structure of FPMH and FPMH-Fe
注:*表示差异显著(P<0.05)。
2.10 粒径和电位
图7显示了FPMH和FPMH-Fe螯合物的粒径分布。FPMH在135.85 nm处出现了1个主峰值,而FPMH-Fe螯合物的主要粒度峰出现在407.16 nm处。与FPMH[(229.23±8.46) nm]相比,FPMH-Fe螯合物[(497.22±5.95) nm]的粒径显著增大(P<0.05)。这一现象可能是由于铁螯合诱导的肽聚集,此外单个Fe2+同时与FPMH的多个肽链结合也会使粒度分布增加[27]。结合上述CD和二级结构的结果,可以推断出Fe2+有利于FPMH形成β-折叠结构,并促进结构折叠,从而组装成纳米颗粒[26]。证实FPMH的分子结构在与铁结合之后发生了显著的变化。
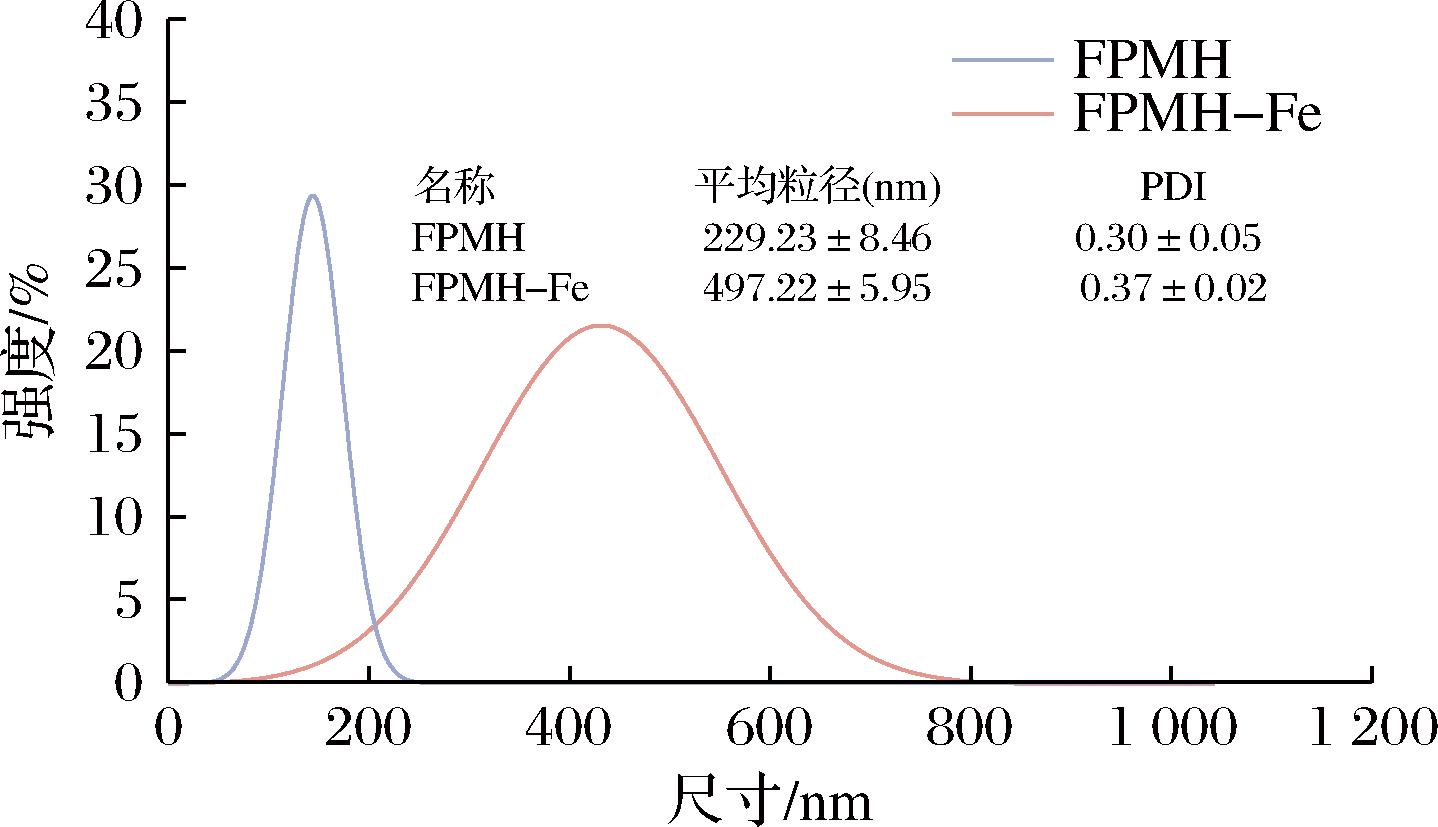
图7 FPMH和FPMH-Fe的粒径分布
Fig.7 Particle size distribution of FPMH and FPMH-Fe
Zeta电位可以反映分散系统中颗粒的表面电荷状态。如图8所示,FPMH的zeta电位绝对值较高,达到(-21.65±1.89) mV,这可能是由于微生物发酵作用促进了花生蛋白的大量水解,释放出低分子质量肽段,暴露疏水基团及活性氨基酸侧链,进而导致分散体系中净电荷的增加。除较小的肽段外,FPMH还含有大量的Asp和Glu等酸性氨基酸,这也会导致负电荷增加。然而,螯合物的形成导致FPMH表面负电荷减少,其电位上升至(-9.20±0.36) mV。电荷的增加表明Fe2+中和了多肽表面的负电荷,这证实了螯合反应中存在静电相互作用[28]。此外,Fe2+与带负电荷的分子[如羧基(—COO-)]的结合也是导致FPMH电位上升的原因之一。
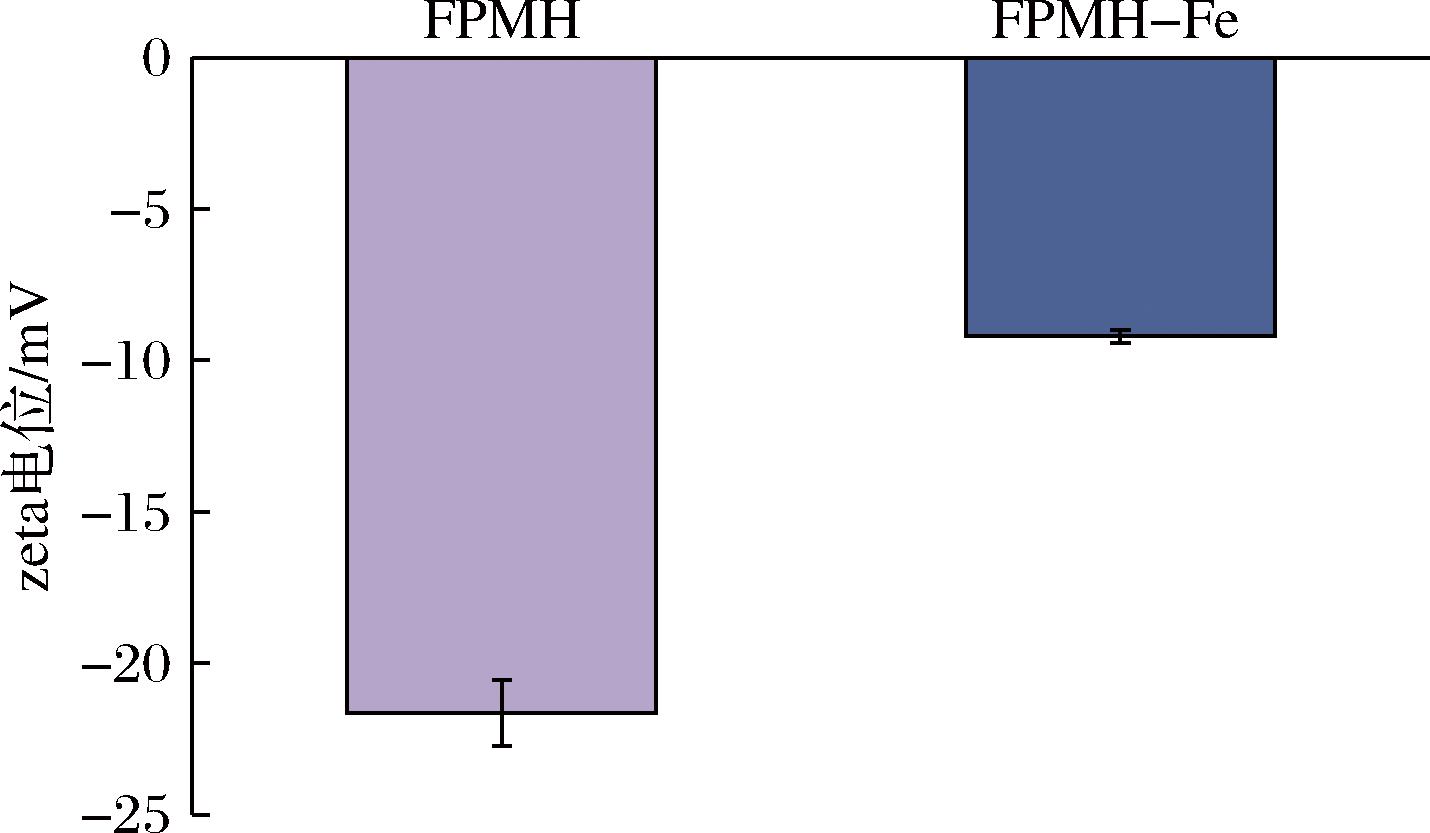
图8 FPMH和FPMH-Fe的zeta电位
Fig.8 Zeta potential of FPMH and FPMH-Fe
2.11 扫描电子显微镜
如图9所示,扫描电镜显示了FPMH和FPMH-Fe的微观形态差异。FPMH表面呈现坑洼不平的形态,且附着少量片状或块状颗粒,为多肽的典型特征。FPNH-Fe为表面粗糙且松散的的球状颗粒聚集物。其可能原因是,Fe2+与多肽的结合破坏了肽原有的致密结构,使肽链之间发生重组,形成了FPMH-Fe的致密结构。且Fe2+与多肽的官能团结合形成环状结构,肽链之间发生聚集,使FPMH-Fe螯合物表面呈现出许多多孔结构。这一结果与海参水解物与铁结合的研究结果类似[10]。

a-FPMH;b-FPMH-Fe
图9 不同放大倍数下的FPMH和FPMH-Fe的扫描电镜图片
Fig.9 SEM images of FPMH and FPMH-Fe at different magnifications
2.12 稳定性测试
如图10所示,随着pH值的升高,FPMH-Fe的游离铁释放量呈先降低后不变的总体趋势。在强酸性条件下(pH值为2),游离铁释放率达到最高值(53.58±1.47)%。这表明在较低的pH条件下,FPMH-Fe螯合物的稳定性较差,导致Fe2+从螯合物中解离出来。其可能原因是高浓度的H+能将肽从其与Fe2+的结合位点上置换出来[11]。而在接近中性和碱性条件下,FPMH-Fe螯合物表现出较高的稳定性,游离铁释放率均保持在较低水平(约7%)。
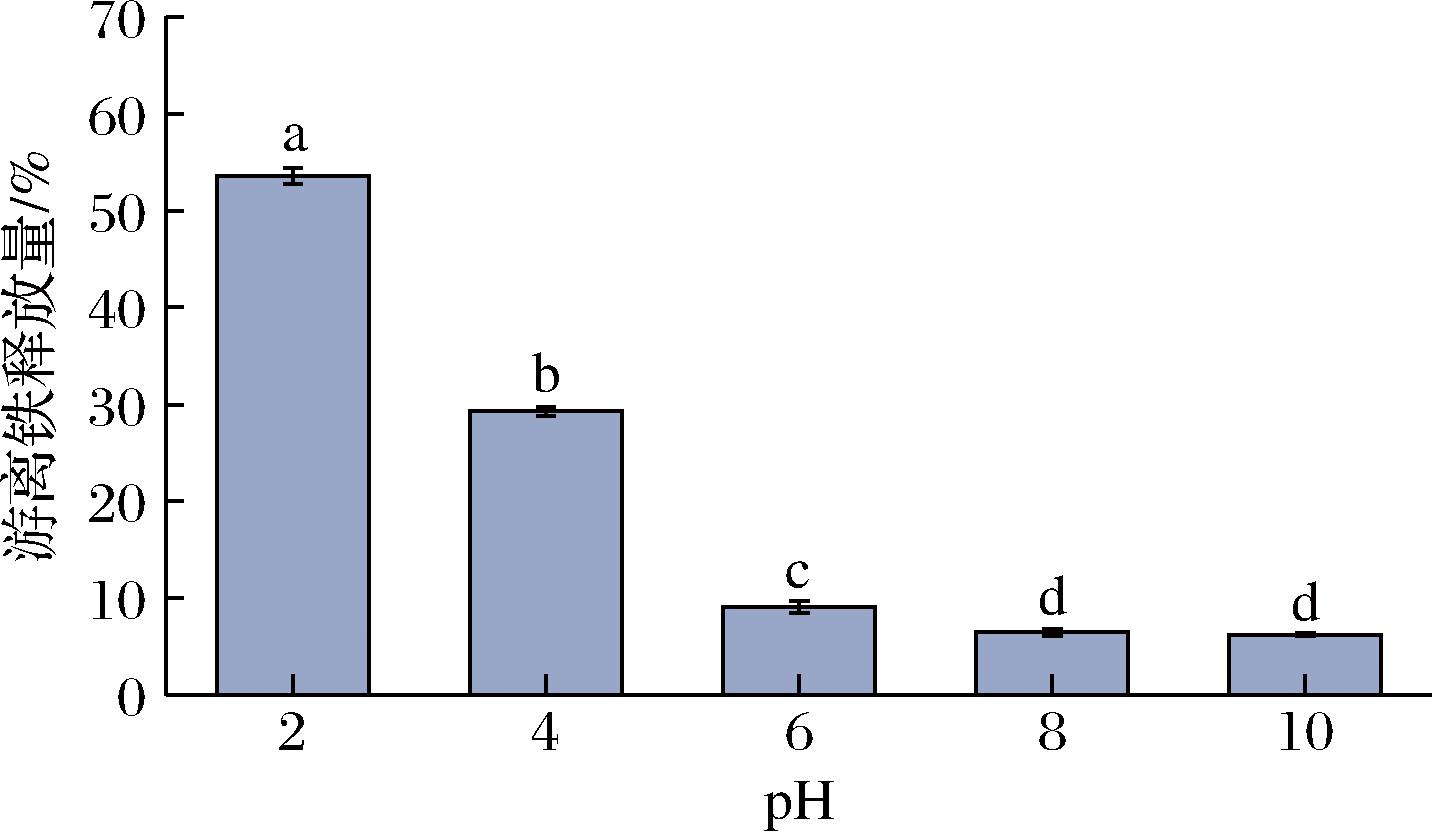
图10 pH对游离铁释放量的影响
Fig.10 Effect of pH on the release of free iron
如图11所示,在25~55 ℃,FPMH-Fe的游离铁释放率保持在较低水平,且不同组间无显著差异。随着温度升高,铁释放率呈上升趋势,温度达到70 ℃时,游离铁释放率为(14.24±1.58)%,仍处于较低水平;而当温度升高至85 ℃时,铁释放率达到最高值(42.17±1.16)%。这可能是因为高温加剧了分子间的热运动,导致螯合物的稳定性降低,从而使Fe2+更容易从螯合物中解离出来。
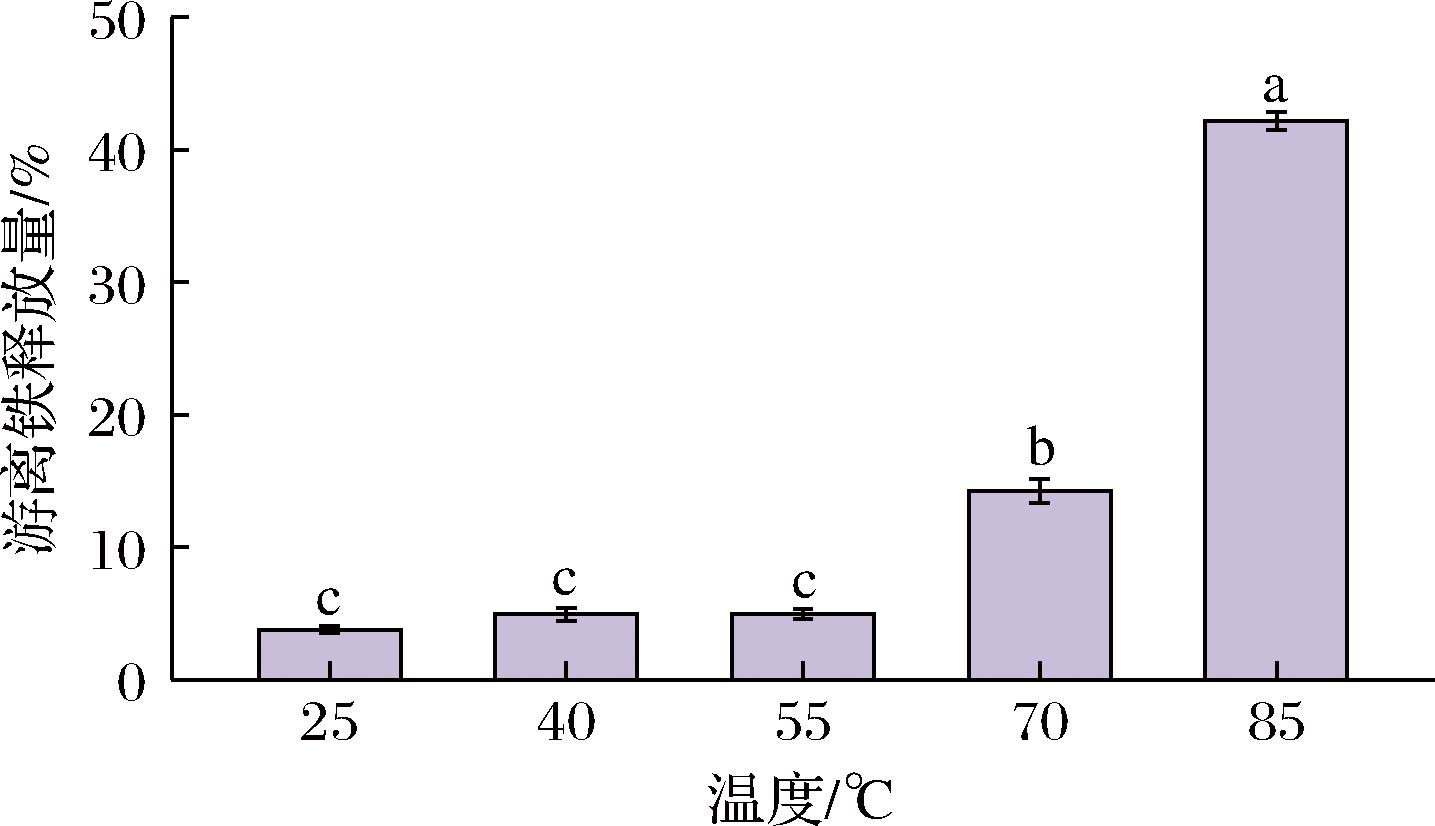
图11 温度对游离铁释放量的影响
Fig.11 Effect of temperature on free iron release
3 结论
在本研究中,经红曲霉和枯草芽孢杆菌发酵后的花生粕水解物具备与Fe2+结合的能力。形成的FPMH-Fe螯合物呈表面粗糙、松散的球状。zeta电位测量结果显示,这些多肽带有较高的负电荷。酸性氨基酸如Asp和Glu中带负电的羧酸基团是潜在的螯合位点且Fe2+可能中和了多肽表面的负电荷,因此肽铁螯合物的电位有所上升。红外光谱印证了FPMH与铁结合位点主要对应于羧基氧原子和氨基氮原子。此外,FPMH-Fe螯合物具有良好的耐热性和耐碱性。但在较低的pH值以及超过70 ℃的高温条件下,游离铁的释放量相对较高。本研究为制备新型铁补充剂提供了重要参考。
[1] CI X M, LIU R, SUN Y T, et al.A novel antioxidant iron-chelating peptide from yak skin:Analysis of the chelating mechanism and digestion stability in vitro[J].Journal of the Science of Food and Agriculture, 2024, 104(13):7907-7916.
[2] SUN L M, YU B, LUO Y H, et al.Effect of small peptide chelated iron on growth performance, immunity and intestinal health in weaned pigs[J].Porcine Health Management, 2023, 9(1):32.
[3] ZHANG Y J, DING X J, LI M Q.Preparation, characterization and in vitro stability of iron-chelating peptides from mung beans[J].Food Chemistry, 2021, 349:129101.
[4] ZHAO T, YING P F, ZHANG Y H, et al.Research advances in the high-value utilization of peanut meal resources and its hydrolysates:A review[J].Molecules, 2023, 28(19):6862.
[5] ECKERT E, LU L, UNSWORTH L D, et al.Biophysical and in vitro absorption studies of iron chelating peptide from barley proteins[J].Journal of Functional Foods, 2016, 25:291-301.
[6] ZHANG T, LI Y H, MIAO M, et al.Purification and characterisation of a new antioxidant peptide from chickpea (Cicer arietium L.) protein hydrolysates[J].Food Chemistry, 2011, 128(1):28-33.
[7] 林栋, 张咏清, 肖自芬, 等.核桃肽铁螯合物的制备及其结构表征[J].食品与发酵工业, 2025, 51(4):221-227;235.
LIN D, ZHANG Y Q, XIAO Z F, et al.Preparation and structural characterization of walnut peptide-ferrous chelate[J].Food and Fermentation Industries, 2025, 51(4):221-227;235.
[8] BUDSEEKOAD S, YUPANQUI C T, SIRINUPONG N, et al.Structural and functional characterization of calcium and iron-binding peptides from mung bean protein hydrolysate[J].Journal of Functional Foods, 2018, 49:333-341.
[9] YAN X, YUE Y, GUO B R, et al.Novel microbial fermentation for the preparation of iron-chelating scallop skirts peptides-its profile, identification, and possible binding mode[J].Food Chemistry, 2024, 451:139493.
[10] FAN C Z, GE X F, HAO J Y, et al.Identification of high iron-chelating peptides with unusual antioxidant effect from sea cucumbers and the possible binding mode[J].Food Chemistry, 2023, 399:133912.
[11] WU Y M, WANG Y, MA Z Z, et al.Novel insights into whey protein peptide-iron chelating agents:Structural characterization, in vitro stability and functional properties[J].Food Bioscience, 2024, 60:104317.
[12] 程赞, 赵晓燕, 张晓伟, 等.核桃分离蛋白酶解产物结构与功能的变化[J].中国油脂, 2022, 47(6):85-91.
CHENG Z, ZHAO X Y, ZHANG X W, et al.Changes of structure and function of enzymatic hydrolysates of walnut protein isolate[J].China Oils and Fats, 2022, 47(6):85-91.
[13] WU W M, HE L C, LIANG Y H, et al.Preparation process optimization of pig bone collagen peptide-calcium chelate using response surface methodology and its structural characterization and stability analysis[J].Food Chemistry, 2019, 284:80-89.
[14] LIU Y, WANG Z, KELIMU A, et al.Novel iron-chelating peptide from egg yolk:Preparation, characterization, and iron transportation[J].Food Chemistry, 2023, 18:100692.
[15] ATHIRA S, MANN B, SHARMA R, et al.Preparation and characterization of iron-chelating peptides from whey protein:An alternative approach for chemical iron fortification[J].Food Research International, 2021, 141:110133.
[16] WEI S S, HUO J Y, LIN J, et al.Egg yolk peptide-iron chelate:Preparation, conformational structure, chelating mechanism and stability in vitro[J].International Journal of Food Science &Technology, 2024, 59(7):4646-4659.
[17] TORRES-FUENTES C, ALAIZ M, VIOQUE J.Iron-chelating activity of chickpea protein hydrolysate peptides[J].Food Chemistry, 2012, 134(3):1585-1588.
[18] LI Y N, JIANG H, HUANG G R.Protein hydrolysates as promoters of non-haem iron absorption[J].Nutrients, 2017, 9(6):609.
[19] SUN N, CUI P B, JIN Z Q, et al.Contributions of molecular size, charge distribution, and specific amino acids to the iron-binding capacity of sea cucumber (Stichopus japonicus) ovum hydrolysates[J].Food Chemistry, 2017, 230:627-636.
[20] SI K, GONG T T, DING S Y, et al.Binding mechanism and bioavailability of a novel phosvitin phosphopeptide (Glu-Asp-Asp-pSer-pSer) calcium complex[J].Food Chemistry, 2023, 404:134567.
[21] LIN S T, HU X, LI L H, et al.Preparation, purification and identification of iron-chelating peptides derived from tilapia (Oreochromis niloticus) skin collagen and characterization of the peptide-iron complexes[J].LWT, 2021, 149:111796.
[22] CAETANO-SILVA M E, BERTOLDO-PACHECO M T, PAES-LEME A F, et al.Iron-binding peptides from whey protein hydrolysates:Evaluation, isolation and sequencing by LC-MS/MS[J].Food Research International, 2015, 71:132-139.
[23] LE VO T D, PHAM K T, VAN LE V M, et al.Evaluation of iron-binding capacity, amino acid composition, functional properties of Acetes japonicus proteolysate and identification of iron-binding peptides[J].Process Biochemistry, 2020, 91:374-386.
[24] BU G H, TI G H, ZHAO X L, et al.Isolation, identification, and chelation mechanism of ferrous-chelating peptide from peanut protein hydrolysate[J].Journal of the Science of Food and Agriculture, 2024, 104(15):9368-9378.
[25] ZHAO Q N, LIANG W, XIONG Z, et al.Digestion and absorption characteristics of iron-chelating silver carp scale collagen peptide and insights into their chelation mechanism[J].Food Research International, 2024, 190:114612.
[26] SUN N, WANG Y X, BAO Z J, et al.Calcium binding to herring egg phosphopeptides:Binding characteristics, conformational structure and intermolecular forces[J].Food Chemistry, 2020, 310:125867.
[27] DING X J, LI H L, XU M D, et al.Peptide composition analysis, structural characterization, and prediction of iron binding modes of small molecular weight peptides from mung bean[J].Food Research International, 2024, 175:113735.
[28] FAN C Z, WANG X T, SONG X W, et al.Identification of a novel walnut iron chelating peptide with potential high antioxidant activity and analysis of its possible binding sites[J].Foods, 2023, 12(1):226.