发芽糙米是稻谷脱壳后的糙米经过发芽至适当芽长的芽体,不仅能改善糙米的风味和口感,还能在保留丰富营养成分的基础上,进一步富集γ-氨基丁酸(γ-aminobutyric acid,GABA)等对人体有益的功能成分[1]。发芽糙米中富含GABA,GABA是一种天然存在的四碳、非蛋白质功能性氨基酸,在植物体内由谷氨酸脱羧酶(glutamic acid decarboxylase,GAD)催化和多胺降解合成[2],在预防老年痴呆方面具有显著作用。人在逐渐衰老时,脑内会出现氧化应激反应,产生的活性氧会攻击神经细胞的细胞膜和DNA,导致神经细胞损伤和死亡;同时,大脑中的乙酰胆碱酯酶(acetylcholinesterase,AChE)活性异常增高,导致乙酰胆碱水平下降,影响神经元之间的信号传递,可能会出现认知障碍等症状[3-4]。这两者正是老年人易患阿尔茨海默症(老年痴呆)的主要原因。GABA具有抗氧化活性和抑制AChE活性的功能,能帮助清除活性氧,降低其对神经细胞的氧化损伤,维持神经细胞的正常结构和功能,并且能够促进神经元信号传递,有助于提高认知能力,从而在预防老年痴呆方面发挥积极作用[5-6]。郑礼平等[7]合成了同时具有抗氧化活性和GABA增强活性的新型神经保护试剂,并证明该试剂具有神经保护作用。OKADA等[8]研究发现中老年女性患者若保持每日摄入一定量富含GABA的食物,对缓解抑郁症状及预防老年痴呆症具有积极作用。
该研究通过DPPH自由基、ABTS阳离子自由基及羟自由基(·OH)清除试验评价了发芽糙米GABA的体外抗氧化活性。基于酶动力学分析构建AChE抑制动力学模型,探究了发芽糙米GABA对AChE的抑制效果及类型。采用分子对接技术和分子动力学(molecular dynamics,MD)模拟探究GABA和AChE的相互作用,从分子层面揭示了发芽糙米GABA对AChE活性抑制机理,为基于该成分开发功能性食品提供了一定的理论依据。
1 材料与方法
1.1 材料与方法
碘化硫代乙酰胆碱(acetylthiocholine iodide,ATChI)、AChE、联硫代双硝基苯甲酸[5,5′-dithio bis-(2-nitrobenzoic acid),DTNB],上海源叶生物科技有限公司;GABA标准品(纯度≥98%),上海阿拉丁生化科技有限公司;ABTS、水溶性维生素E(Trolox)、3,5-二硝基水杨酸,罗恩试剂;DPPH,Sigma-Aldrich(上海)贸易有限公司;KH2PO4、Na2HPO4、H2O2、无水碳酸钠、K2S2O8、NaClO、酒石酸钾钠、氯酚、NaHSO3、苯酚、无水乙醇、CaCl2、硫酸亚铁、水杨酸、邻苯二甲醛(ortho phthalaldehyde,OPA)、四硼酸钠、β-巯基乙醇、抗坏血酸均为分析纯,天津永大化学试剂有限公司;实验用水为超纯水。
1.2 仪器与设备
ST3100型pH计,Ohaus(常州)仪器有限公司;LC-WB-8电热恒温水浴锅,力辰科技有限公司;LHS-150HC-I恒温恒湿培养箱,上海一恒科学仪器有限公司;MFOI-L1磁场催化光照培养,无锡英都斯特感应科技有限公司;RE52CS-1旋转水真空泵,上海亚荣生化仪器厂;MDJ-D02J1磨粉机,小熊家电有限公司;CL-80HTD超声波清洗机,济南克林有限公司;FA2204电子分析天平,上海菁海仪器有限公司;SZF-06A高速台式离心机,上海元析仪器有限公司;JC-2000酶标仪,赛默飞世尔科技有限公司;E2695高效液相色谱仪,美国Waters公司;VaCo·2-E真空冷冻干燥机,德国ZIRBUS技术有限公司。
1.3 试验方法
1.3.1 发芽糙米GABA的提取、纯化
将浸泡2 h的糙米放在强度为2.8 mT的交变磁场中处理68 min后,喷洒1 mmol/L CaCl2溶液于35 ℃发芽37 h。将发芽糙米放入80 ℃的烘箱烘干2 h进行酶灭活,并干燥至水分≤14%,粉碎至60目筛封装,冷藏备用。根据宁亚维等[9]的方法并稍作改进:将5.0 g发芽糙米粉加入到15 mL无水乙醇试管中,提取糙米中的黄色素,于60 ℃水浴保温2 h后,离心并弃去上清液,再加入20 mL纯水到沉淀物中,于40 ℃振荡水浴提取1 h,结束后离心并提取上清液,定容至25 mL,即得到发芽糙米GABA粗提液。参考杨胜远等[10]的方法对发芽糙米GABA粗提液进行纯化,并稍加修改:取40 mL发芽糙米GABA粗提取液,加入预处理后的732强酸型阳离子交换树脂2 g,在水浴恒温振荡器中37 ℃、120 r/min振荡24 h后过滤,用去离子水洗涤充分吸附后的树脂,加入40 mL 0.15 mol/L的Na2CO3溶液,在水浴恒温振荡器中37 ℃、120 r/min摇床振荡5 h,充分解吸后过滤并收集滤液,合并2次滤液即为发芽糙米GABA纯化液。
1.3.2 发芽糙米GABA质量浓度的测定
参考李雁琴[11]的方法采用HPLC测定纯化液中发芽糙米GABA的质量浓度:称取150 mg的OPA溶解于3 mL的甲醇中,加入27 mL的四硼酸钠缓冲液(0.4 mol/L,pH 9.4)、500 μL β-巯基乙醇和30 mg抗坏血酸,混合均匀制成衍生试剂。取1 mL纯化液按体积比为1∶1的比例与衍生试剂混合均匀后过0.22 μm滤膜,2 min后进样,以甲醇(A)和体积分数为0.10%甲酸溶液(B)为流动相,检测波长332 nm,流速0.8 mL/min,柱温30 ℃,进样量为10 μL,测定峰面积计算得发芽糙米GABA纯化液的质量浓度为0.38 mg/mL。
1.3.3 发芽糙米GABA体外抗氧化活性的测定
将发芽糙米GABA纯化液经冷冻干燥处理后,取适量粉末,用去离子水配制成质量浓度为0、0.05、0.10、0.20、0.40、0.80 mg/mL的样品液,进行对自由基的清除能力的试验,并以Trolox和GABA标准品作为阳性对照。
1.3.3.1 DPPH自由基清除能力的测定
参照MOYO等[12]的方法,稍有改动。用无水乙醇配制0.1 mmol/L DPPH溶液,将2.0 mL发芽糙米GABA样品液加入到2.0 mL DPPH溶液中,混匀后避光30 min,于517 nm波长处测其吸光度值。按公式(1)计算DPPH自由基清除率:
DPPH自由基清除率![]()
(1)
式中:Ax,2.0 mL样品液加2.0 mL DPPH溶液的吸光度值;Ay,2.0 mL样品液加2.0 mL无水乙醇的吸光度值;Az,2.0 mL纯水加2.0 mL DPPH溶液的吸光度值。
1.3.3.2 ABTS阳离子自由基清除能力的测定
参考 MOYO等[12]的方法,稍作修改。将2.6 mmol/L K2S2O8溶液加入到7 mmol/L ABTS溶液中,并避光反应16 h后,即得ABTS阳离子自由基储备液,使用前用乙醇(体积分数为70%)对其进行稀释,使其在734 nm波长处的吸光度值为0.70。将0.5 mL 发芽糙米GABA样品液加到3.0 mL ABTS阳离子自由基溶液中,避光反应30 min,于波长734 nm测其吸光度值。按公式(2)计算ABTS阳离子自由基清除率:
ABTS阳离子自由基清除率![]()
(2)
式中:Ax,0.5 mL样品液加3.0 mL ABTS阳离子自由基试液的吸光度值;Ay,0.5 mL样品液加3.0 mL 70%乙醇的吸光度值;Az,0.5 mL纯水加3.0 mL ABTS阳离子自由基试液的吸光度值。
1.3.3.3 ·OH清除能力
参考薛山等[13]的方法,将1 mL 发芽糙米GABA样品液、1 mL 9 mmol/L FeSO4溶液、1 mL 9 mmol/L的水杨酸-乙醇溶液摇匀放置10 min,再加入1 mL 8.8 mmol/L H2O2溶液,摇匀后,将其置于37 ℃水浴中30 min,在510 nm波长处测其吸光度值。按公式(3)计算·OH的清除率:
羟自由基清除率![]()
(3)
式中:Ax,1 mL样品液加1 mL H2O2溶液的吸光度值;Ay,1 mL样品液加1 mL纯水的吸光度值;Az,1 mL纯水加1 mL H2O2溶液的吸光度值。
1.3.4 发芽糙米GABA对AChE的抑制作用
1.3.4.1 发芽糙米GABA对AChE的抑制活性试验
用硫代乙酰胆碱-联硫代双硝基苯甲酸法测定AChE的活性[14]。
对照组AChE活性的测定:将2.0 mL pH值为7.4的磷酸盐缓冲液、50 μL 1 U/mL AChE和200 μL 0.002 mol/L的DTNB溶液(溶剂为pH 7.4的磷酸盐缓冲液)混合,于37 ℃水浴15 min,再加入100 μL 0.015 mol/L的ATChI溶液(溶剂为pH 7.4的磷酸盐缓冲液),并用pH 7.4的磷酸缓冲液定容到2.5 mL,摇匀后于37 ℃水浴6 min,以纯水作为参比,于412 nm波长处测其吸光度值。以pH 7.4的磷酸缓冲液代替AChE使用液做空白实验,测得试剂空白值(Az)。
抑制AChE活性测定:配制发芽糙米GABA质量浓度为0.25、0.5、1、1.5、2.5、3.5 mg/mL,加入AChE溶液和100 μL发芽糙米GABA样品液,按照对照组AChE活性测定步骤,于412 nm波长处测得加入发芽糙米GABA抑制剂后的吸光度值(A)。通过公式(4)计算AChE抑制率:
AChE活性抑制率![]()
(4)
式中:Ax,加GABA样品液的吸光度值;Ay,用磷酸盐缓冲液代替AChE溶液测得的吸光度值;Az,用纯水代替GABA样液测得的吸光度值。
1.3.4.2 发芽糙米GABA对AChE抑制动力学模型的构建
配制浓度为0、0.2、0.4、0.6、0.8、1.0 U/mL的AChE溶液。按照1.3.3.1节中的方法,保持底物ATChI溶液浓度为0.015 mol/L,分别测定不同浓度AChE溶液与不同质量浓度发芽糙米GABA(0、0.5、1.5、3.5 mg/mL)的酶促反应速率。通过构建酶浓度-反应速率曲线,根据斜率变化特征确定其抑制模式。
通过Lineweaver-Burk双倒数曲线解析抑制机制:配制浓度为2.5、5.0、10.0、12.5、15.0 mmol/L的底物ATChI溶液。根据1.3.3.1节中的方法,保持AChE浓度为1 U/mL,分别测定不同底物浓度S和不同质量浓度发芽糙米GABA(0、0.5、1.5、3.5 mg/mL)反应的吸光度值,计算酶促反应速率V。以1/S作为横坐标,1/V作为纵坐标进行线性拟合,通过截距与斜率的变化特征判断抑制类型。
1.3.4.3 GABA与AChE的分子对接
利用分子对接模拟技术,进一步解析GABA在AChE活性中心的结合位点。
1)预处理
从RCSB PDB数据库(https://www.rcsb)中获取AChE 3D晶体结构(PDB ID:1EVE)和GABA结构(PDB ID:6HUP)。
2)分子对接
使用MOE 2019进行分子对接实验,对接共采集30个构象;使用MOE算法进行构象采样和打分,根据结合位点选取最优构象。相互作用图使用MOE软件绘制,结合示意图使用PyMol绘制。
1.3.4.4 GABA与AChE的MD模拟
该研究通过MD模拟技术来探究蛋白质-小分子复合物的相互作用机制及构象稳定性,采用Gromacs 2022作为动力学模拟软件进行100 ns的MD模拟。基于Amber 99 sb-ilnd力场参数构建AChE拓扑文件,配体分子则通过Amber 20软件经GAFF力场参数生成拓扑文件。采用TIP3P水模型建立水盒子,确保蛋白与盒子边缘距离≥1.2 nm,通过添加Na+/Cl-离子平衡体系电荷。执行50 000步最陡下降法,依次对其进行NVT和NPT系综平衡,在300 K恒温和1 bar恒压条件下开展100 ns的MD模拟,设置10 Å为非键相互作用截断半径。
1.4 数据处理
所有实验都经过3组平行测定,并计算出均值和标准差;运用SPSS For Windows软件进行方差分析,运用Origin Pro 2021软件绘图。
2 结果与分析
2.1 发芽糙米GABA抗氧化性的研究
发芽糙米GABA对DPPH自由基有一定的清除能力,如图1-a所示,DPPH自由基的清除率与发芽糙米GABA质量浓度呈正相关,当发芽糙米GABA质量浓度为0.8 mg/mL时,对DPPH自由基的清除率为92.71%,接近于该质量浓度下Trolox的清除率(94.71%),发芽糙米GABA的半数抑制浓度(half inhibitory concentration,IC50)为0.082 mg/mL,这表明发芽糙米GABA具有较好的DPPH自由基清除能力。
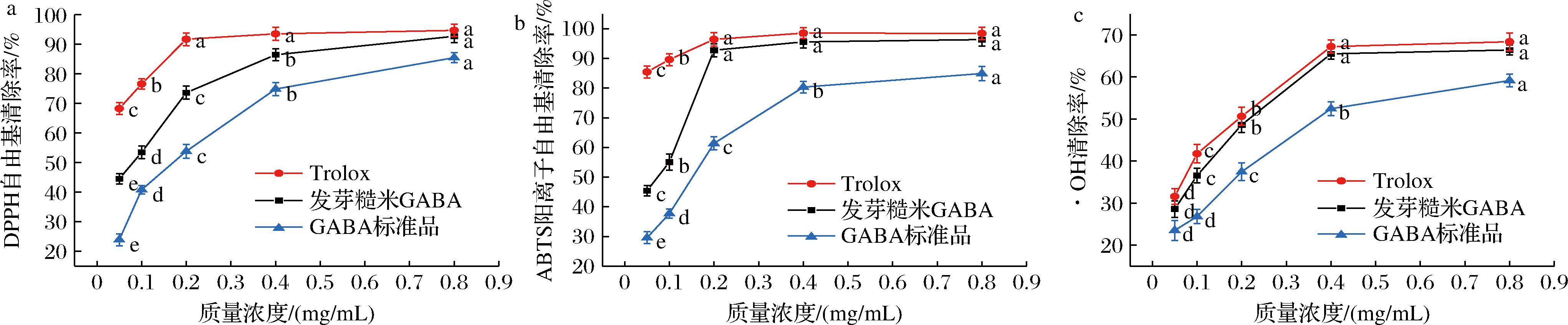
a-DPPH自由基清除率;b-ABTS阳离子自由基清除率;c-·OH清除率
图1 发芽糙米GABA的质量浓度对抗氧化活性的影响
Fig.1 Effect of GABA concentration on antioxidant activity in germinated brown rice
注:不同小写字母表示不同处理间差异显著(P<0.05)(下同)。
发芽糙米GABA对ABTS阳离子自由基有很好的清除能力,如图1-b所示,当发芽糙米GABA质量浓度达到0.2 mg/mL时,自由基清除率停止升高并且与Trolox的清除能力几乎相同。发芽糙米GABA质量浓度为0.8 mg/mL时对ABTS阳离子自由基的清除能力达到最大值96.35%,接近于同质量浓度Trolox水平(97.76%)。发芽糙米GABA的IC50值为0.075 mg/mL,说明发芽糙米GABA对ABTS阳离子自由基表现出更好的清除能力。这是因为GABA的分子结构有1个羟基和1个氨基,二者能够向自由基传递质子,与自由基发生反应后,将其转化为更稳定或惰性状态,从而有效阻断自由基的链式反应[15-16]。由图1-c可知,在发芽糙米GABA为0.4 mg/mL时对·OH清除率趋于平缓,在0.8 mg/mL时达到最高66.42%,但都略低于Trolox对·OH清除率,发芽糙米GABA的IC50值为0.216 mg/mL,表明发芽糙米GABA具有较好的清除·OH的能力,发芽糙米GABA及Trolox的IC50值分别为0.22、0.20 mg/mL。由图1可知GABA标准品对于DPPH自由基、ABTS阳离子自由基、·OH清除的IC50值分别为0.17、0.15、0.36 mg/mL,均高于发芽糙米GABA,可能由于发芽糙米GABA提取液虽经过分离、纯化但体系中仍含有少量其他抗氧化成分,如多酚、酚酸等,这些成分与发芽糙米GABA产生协同作用,共同提高了体系自由基清除效率。
2.2 发芽糙米GABA对AChE的抑制活性及动力学研究
2.2.1 发芽糙米GABA对AChE活性的抑制
AChE在生物神经传导中起到关键作用,能够使神经突触部位的乙酰胆碱水解成乙酸和胆碱,如果酶活性过高会影响神经元的信号传递,因此抑制AChE的活性可以改善阿尔茨海默症患者的认知功能、记忆力和行动能力等[17]。如图2所示,发芽糙米GABA对AChE的抑制率随GABA质量浓度的增大而增大,当发芽糙米GABA质量浓度为3.5 mg/mL时,对AChE的抑制率为59.77%,但发芽糙米GABA对酶活性的抑制率始终低于多奈哌齐。通过计算多奈哌齐、发芽糙米GABA和GABA标准品的IC50值分别为0.74、2.49、3.3 mg/mL。相较于结构单一的GABA标准品,发芽糙米中的GABA可能与多酚、其他氨基酸等其他天然成分产生协同作用,并通过与糖类、蛋白质等形成复合物或发生化学修饰,进而增强其抑制AChE活性的能力。尽管发芽糙米GABA对AChE活性的抑制要低于阳性对照药物多奈哌齐,但其具有天然、健康、安全的特性,仍是一类优良的AChE抑制剂。
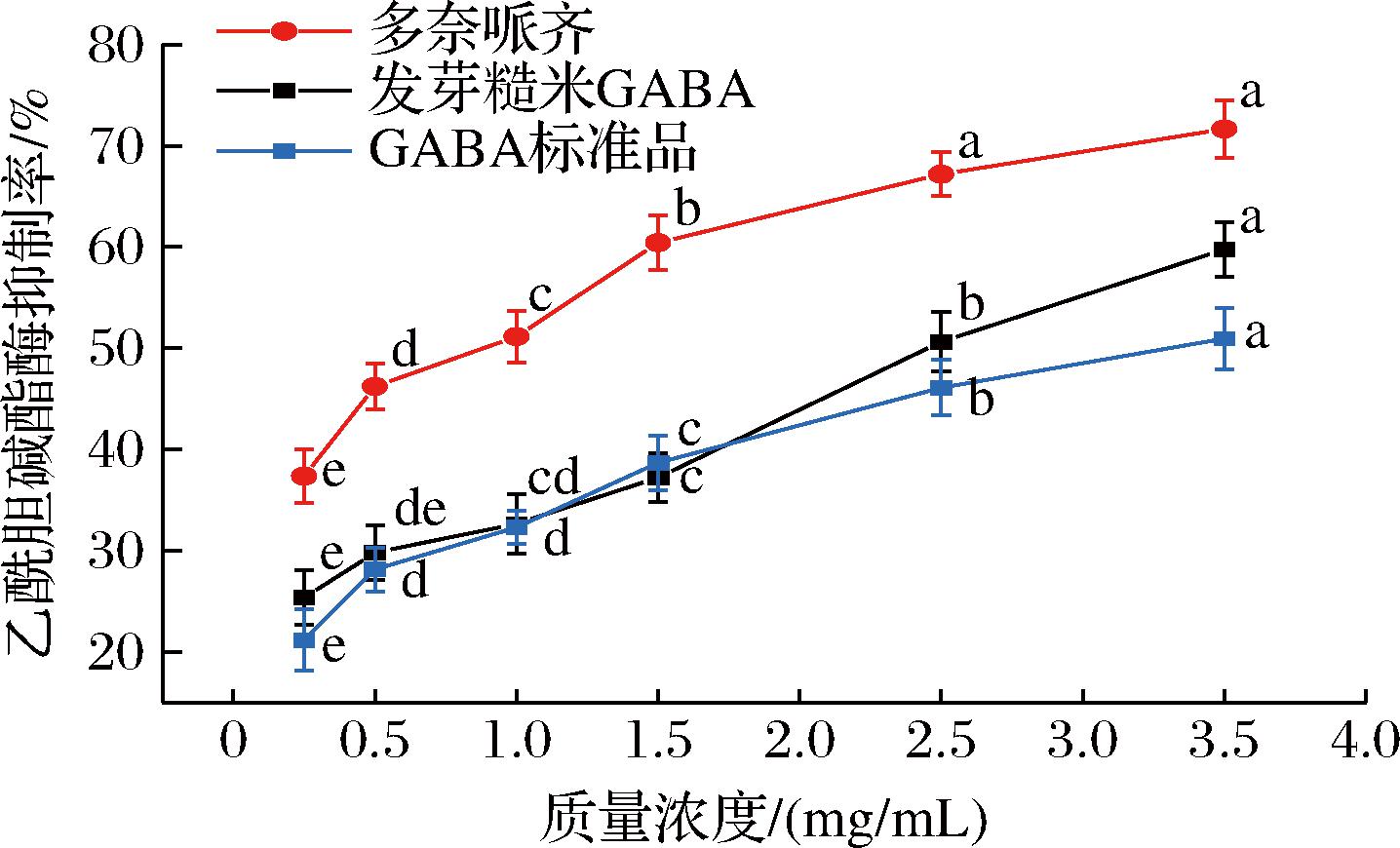
图2 发芽糙米GABA对AChE活性的抑制效果
Fig.2 Inhibition effect of GABA on AChE activity in germinated brown rice
2.2.2 发芽糙米GABA对AChE的抑制动力学分析
在不同质量浓度的发芽糙米GABA抑制剂条件下AChE浓度与反应速率的关系如图3所示,所得直线均基本通过原点。随着GABA质量浓度的增加,直线的斜率在不断降低,说明发芽糙米GABA对AChE的抑制作用是可逆性抑制。表明发芽糙米GABA与AChE的作用未引起酶蛋白变性,抑制剂以非共价键与AChE分子发生可逆性结合,进而造成酶活性降低或丧失。
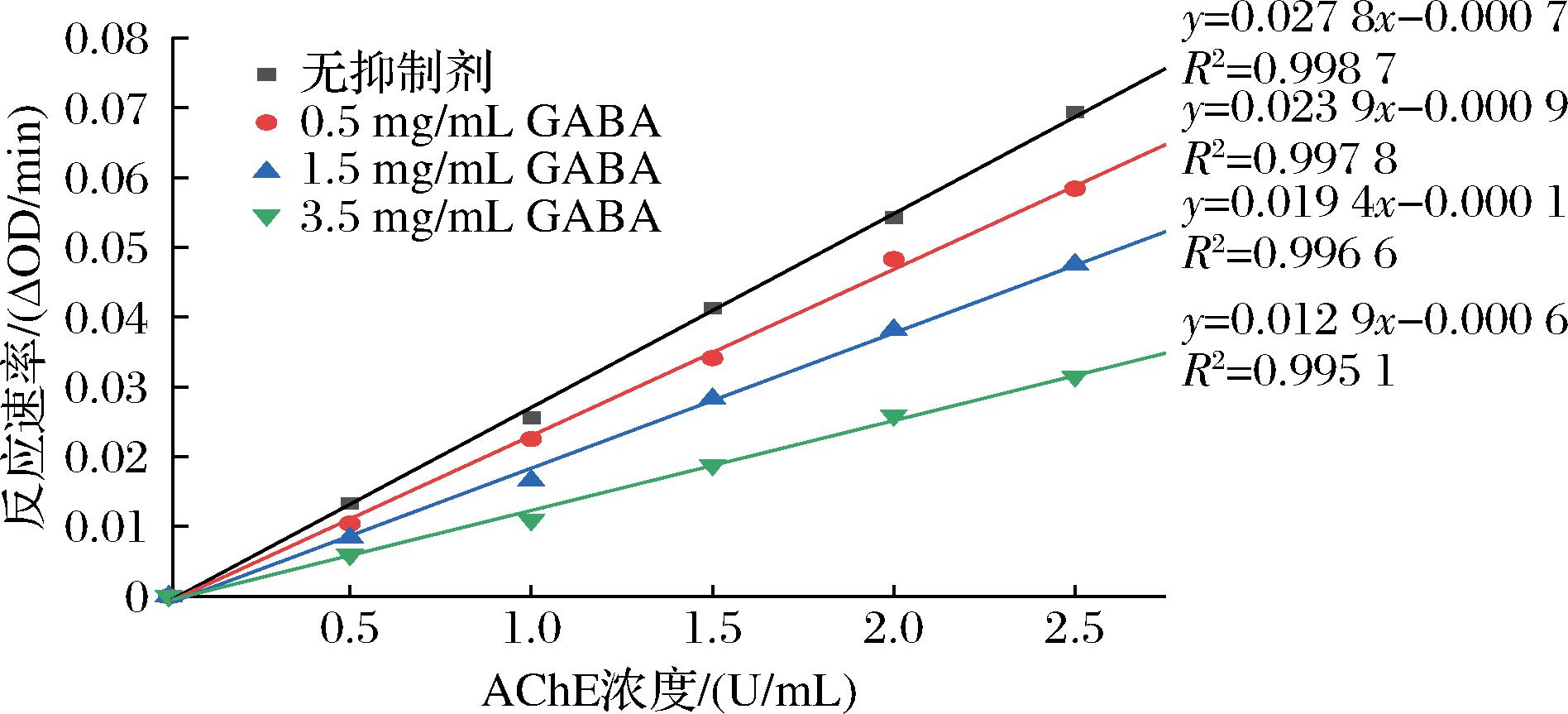
图3 发芽糙米GABA对AChE的抑制类型
Fig.3 Inhibition of acetylcholinesterase by GABA in germinated brown rice
如图4所示,直线斜率随发芽糙米GABA质量浓度的增大而增大,且4条直线相交于x轴上同一点,空白对照组和添加质量浓度为0.5、1.5、3.5 mg/mL发芽糙米GABA样品组的Km值分别为23.48、23.38、21.50和21.70,Km值几乎不变;最大反应速率Vmax分别为0.104、0.075、0.054、0.038 ΔOD/min,Vmax值减小,说明GABA对AChE的抑制类型属于非竞争性抑制。
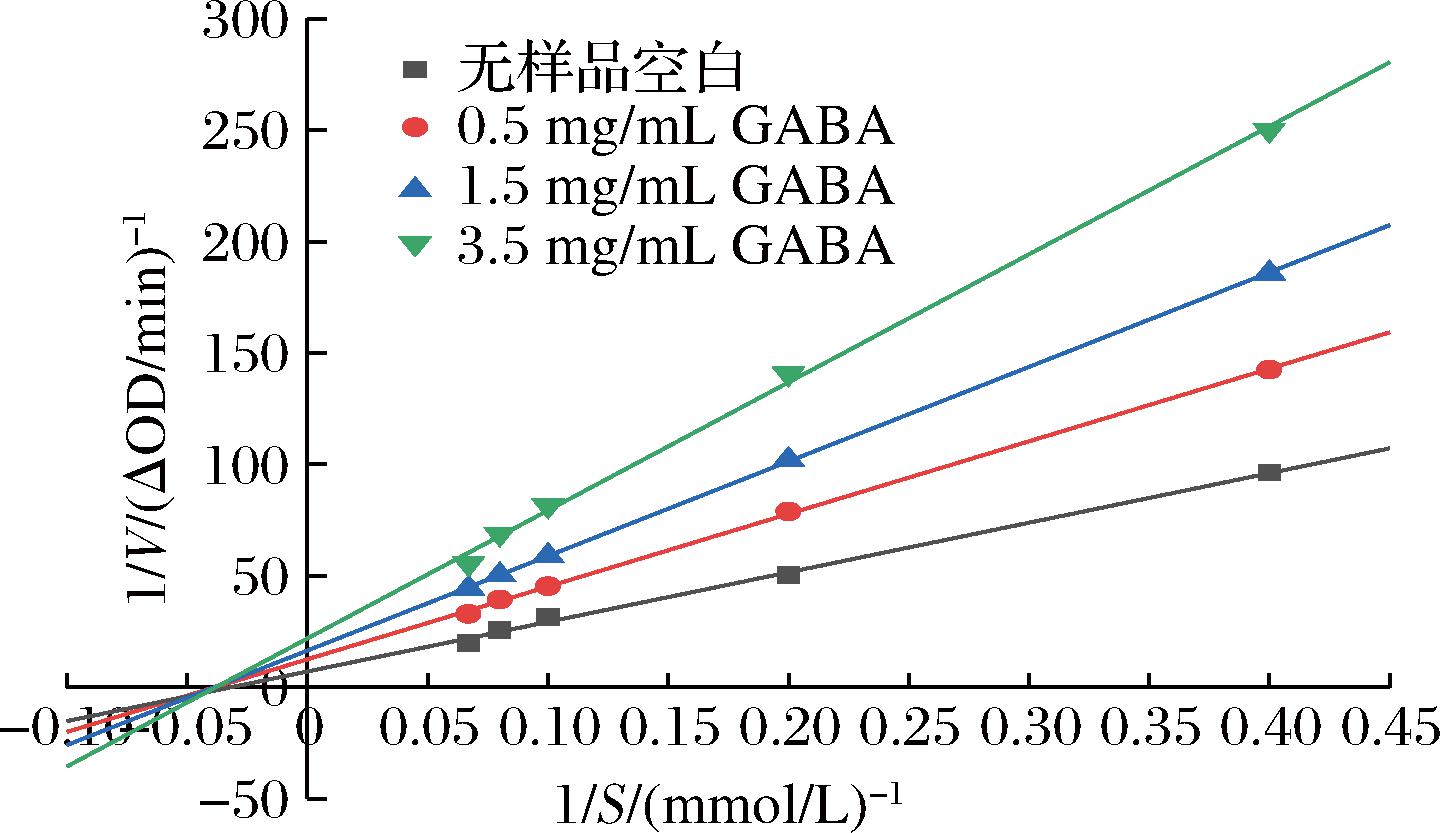
图4 发芽糙米GABA对AChE抑制作用的Lineweaver-Burk曲线
Fig.4 Lineweaver-Burk curve of GABA’s inhibitory effect on AChE in germinated brown rice
综上所述,发芽糙米GABA对AChE抑制类型属于可逆非竞争性抑制,这可能是由于GABA不与底物竞争酶的结合位点,不干扰酶-底物结合,而是与酶、酶-底物复合物结合[18]。
2.2.3 GABA与AChE分子对接结果分析
通过MM-GBSA计算分析,筛选出GABA与AChE对接得分最高的结果如表1所示,GABA与AChE的结合能为-5.37 kcal/mol,结合自由能小于-5.0 kcal/mol表示有较好的结合活性,故GABA与AChE可以形成稳定的复合物,与2.2.2节中实验结果相符。
表1 分子对接的分数表
Table 1 Molecular docking scores
抑制剂靶点结合自由能/(kcal/mol)GABAAChE-5.37
对接的构象结果如图5可知,GABA结合到AChE蛋白的活性口袋的表面,GABA能够与AChE的活性位点(Glu199、Ser200、Gly123、Glu118等)结合,如与AChE蛋白残基Tyr130可以形成1个键长为3.3的氢键,与残基Ser122、Glu199、His440等形成2个氢键,氢键是GABA与AChE相互作用的主要作用力,能够稳定分子间的相互作用,并影响分子的构象和功能[19];同时GABA还可以与AChE蛋白残基Gly117、Leu127、Trp84形成疏水作用力。
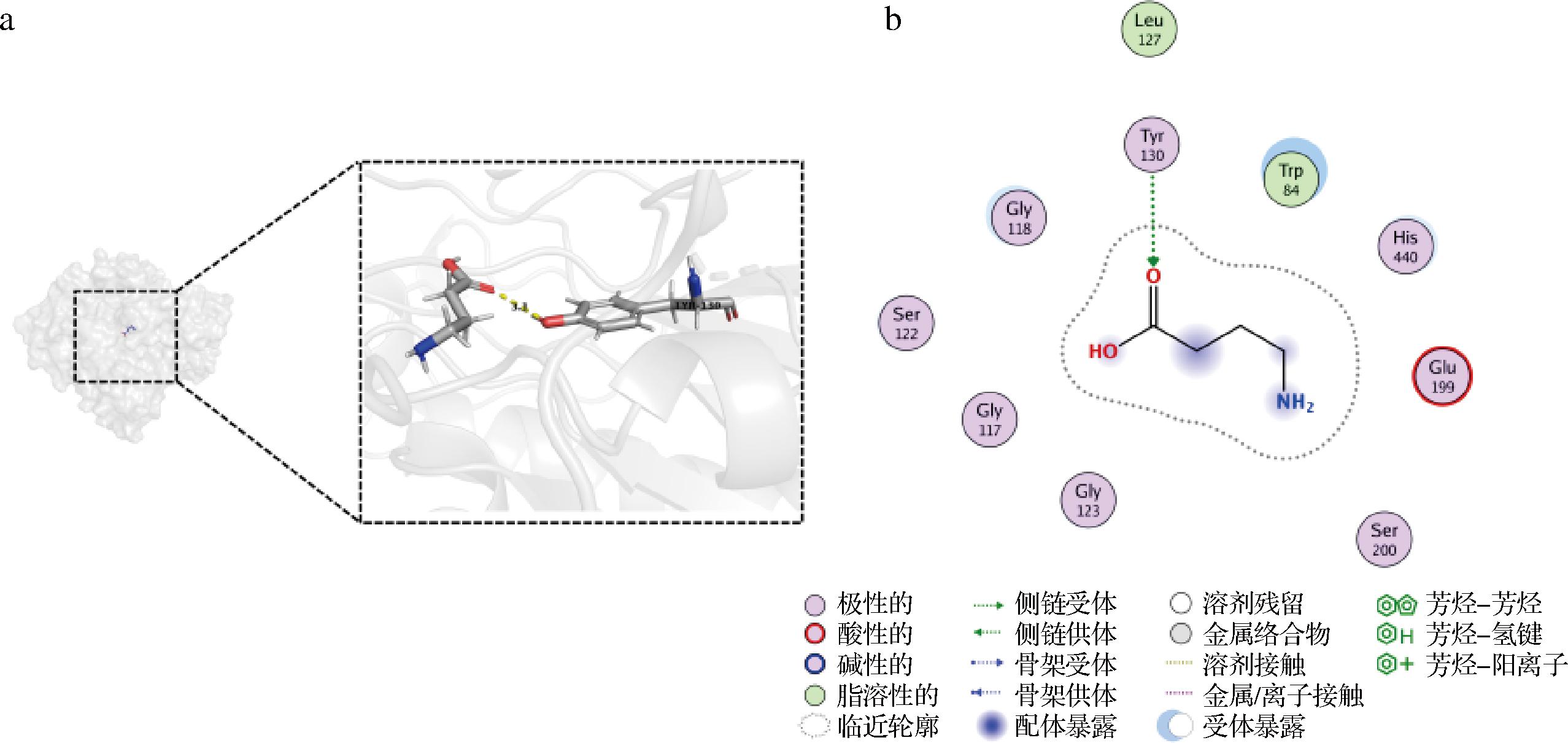
a-3D;b-2D
图5 GABA与AChE分子对接3D、2D图
Fig.5 3D and 2D diagrams of GABA docking with AChE molecules
2.2.4 MD模拟分析
将GABA与AChE进行100 ns的MD模拟分析,并通过Gromacs内置分析模块对模拟轨迹进行数据分析[20]。
1)GABA与AChE的回转半径(radius of gyration,Rg)、均方根偏差(root mean square error,RMSD)、均方根波动(root mean square fluctuation,RMSF)分析
RMSD可以被用来观察体系在模拟过程中相对于初始结构的蛋白质整体构象变化。其值越大表明蛋白在体系中的结构变化越大。而Rg用于评价体系结构的紧密程度。该值越大表示蛋白质越松散,该值越小表示蛋白质越紧密。AChE与GABA的Rg和RMSD结果分别如图6-a和图6-b所示,RMSD值在模拟的前20 ns发生略微波动,但随着模拟时间延长,RMSD值波动幅度变小,逐渐趋于稳定[21]。在100 ns模拟中,复合物体系的Rg值为2.283 85~ 2.359 62 nm;结合RMSD和Rg数据来看,体系在100 ns模拟中,体系趋于稳定,收敛。
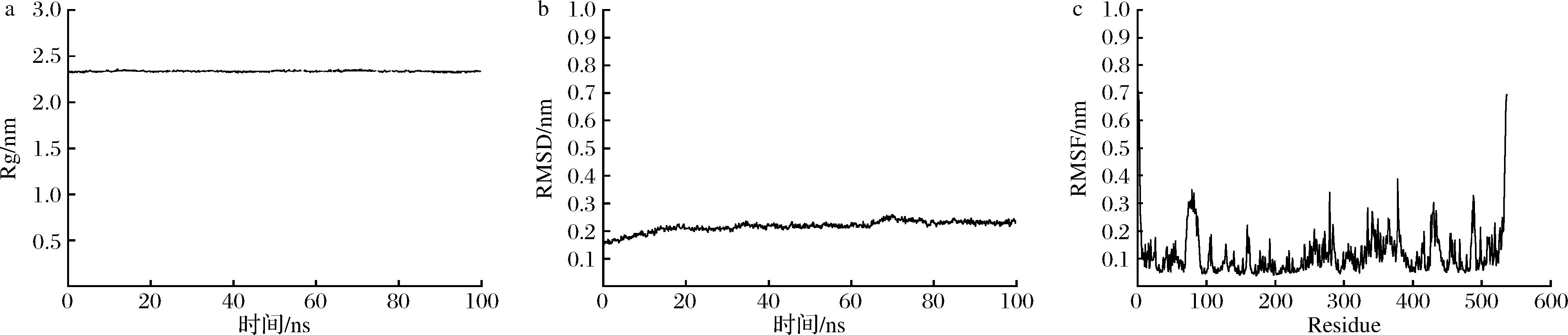
a-Rg;b-RMSD;c-RMSF
图6 GABA与AChE之间的Rg、RMSD及RMSF变化情况图
Fig.6 Rg, RMSD, and RMSF changes between GABA and AChE
RMSF可以观察体系在模拟过程中局部氨基酸残基位点结构波动的情况[22]。该值越大表明该位置残基越柔性[23]。RMSF结果如图6-c所示,GABA与AChE的平均RMSF值为1.257 Å,GABA与AChE结合后,在79、279、378、430、488号附近AChE氨基酸残基波动远大于其他残基,说明这些残基区域表现出较高的结构灵活性。
2)GABA与AChE相互作用分析
在整个模拟过程中,蛋白与配体的相互作用可以分为4种:氢键、水桥、疏水作用和离子桥[24]。如图7-a所示,100 ns MD模拟中,AChE蛋白和GABA可以形成氢键相互作用,氢键数量为0~5,氢键的平均数量为1.187 8±1.020 1。溶剂可及表面积(solvent accessible surface area,SASA)是指生物大分子(如蛋白质)表面能被溶剂分子接触到的面积,而计算SASA可以帮助了解蛋白质表面的疏水区域分布,在蛋白质折叠和相互作用过程中,疏水界面的变化情况如图7-b所示,SASA为215~235,表明GABA和AChE蛋白的结合存在疏水作用。
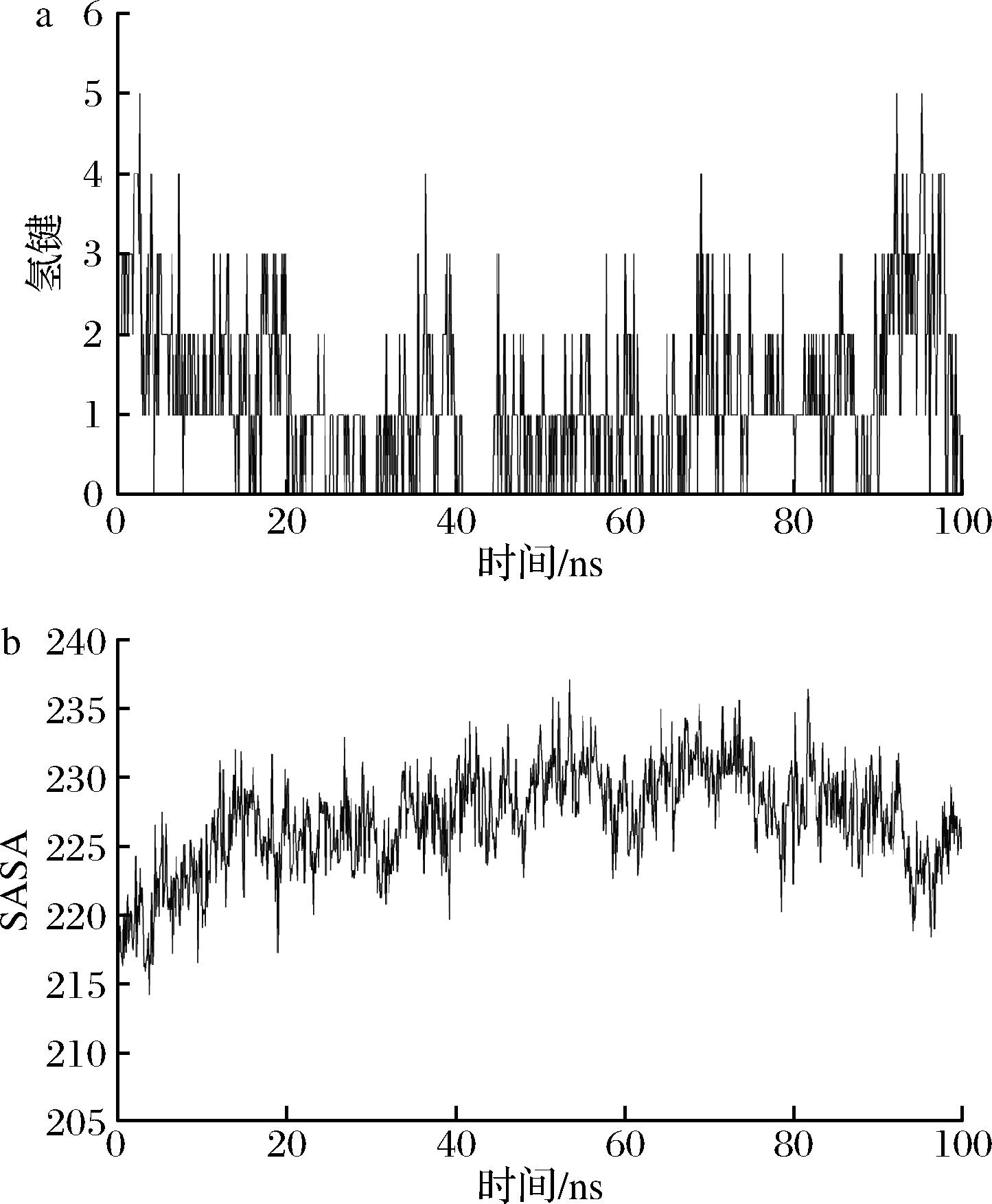
a-氢键;b-SASA
图7 GABA与AChE互作图谱
Fig.7 Interaction diagram between GABA and AChE
残基能量分解体现了每一个残基对蛋白配体结合的贡献,通过GABA-AChE体系的结合自由能如图8-a所示,气相自由能是范德华力和静电相互作用力综合计算所得,气相自由能为负值,说明了在气相环境下GABA与AChE具有自发结合的趋势[20]。其中范德华力和静电相互作用力都小于0,说明了范德华力、静电相互作用力都有利于维持蛋白小分子体系三维结构的结合。同时溶剂化能中的表面能为负值,但是数值较小,而广义玻恩能为正数,表明极性溶剂不利于其结合。通过气象自由能与溶剂化能的关系,最终的总结合自由能为(-6.2±3.86) kcal/mol,意味着结合过程会使系统的自由能降低,GABA-AChE体系倾向于形成更稳定的复合物,这种结合有利于生物分子执行特定的生物学功能[25]。如图8-b所示,在残基体现上主要由Trp84参与对GABA与AChE结合的贡献。
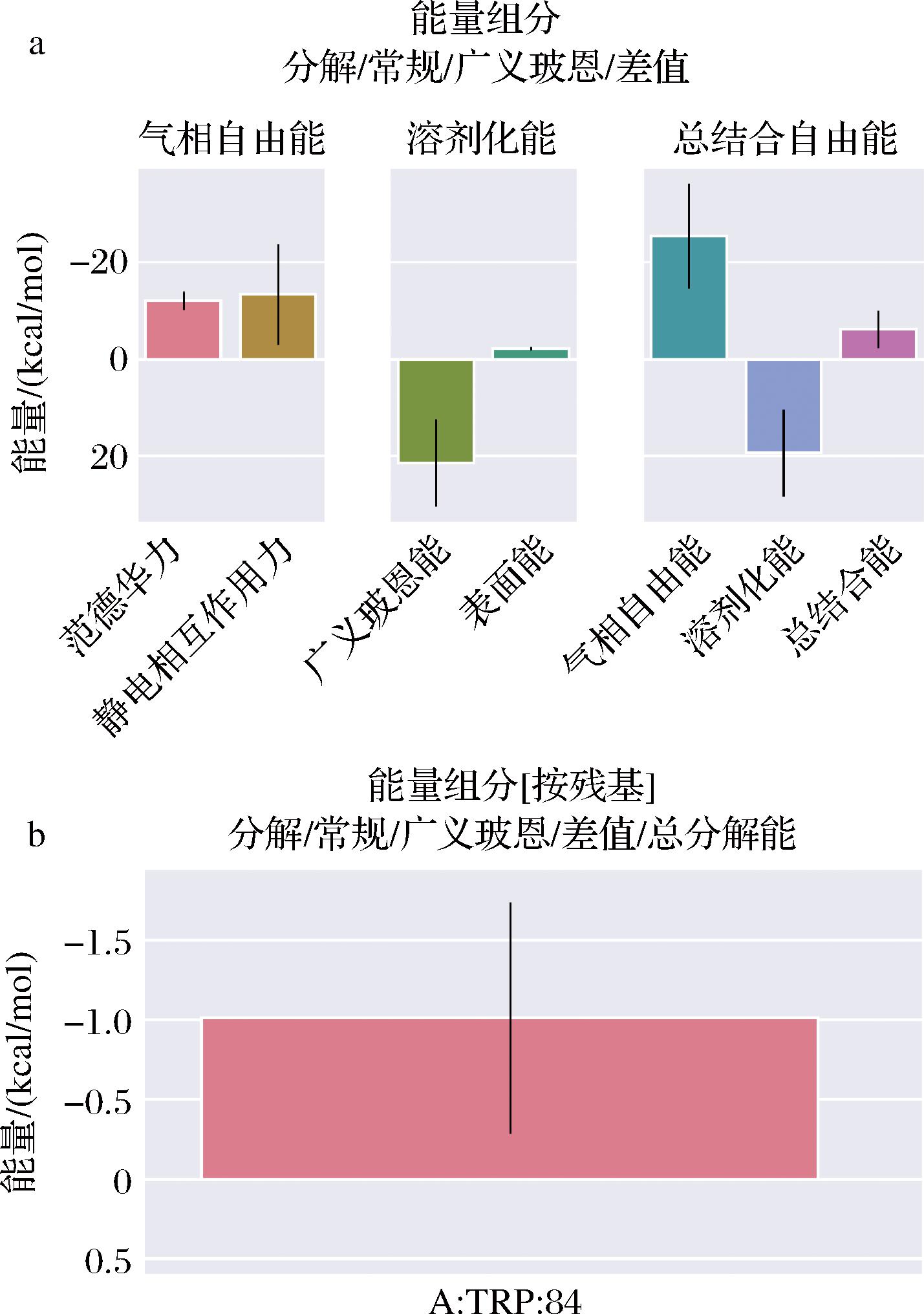
a-属性分解图;b-残基分解图
图8 GABA-AChE体系的结合能分解示意图
Fig.8 Schematic diagram of the binding energy decomposition of the GABA-AChE system
3 结论
本研究以DPPH自由基、ABTS阳离子自由基和·OH清除能力为指标研究了发芽糙米GABA的抗氧化能力,发芽糙米GABA的DPPH自由基、ABTS阳离子自由基和·OH清除能力的IC50值分别0.082、0.075、0.216 mg/mL,说明发芽糙米GABA具有很好的抗氧化能力,有利于延缓人体组织细胞因氧化应激引发的衰老。通过酶抑制试验研究了发芽糙米GABA对AChE的抑制作用,其抑制率为59.77%,IC50值为2.49 mg/mL,说明发芽糙米GABA对AChE有较好的抑制效果;通过酶促动力学模型分析了发芽糙米GABA对AChE的抑制类型为可逆非竞争性抑制。通过分子对接及分子动力学模拟分析了发芽糙米GABA与抑制AChE的机制,考察了该分子系统的动态行为,GABA主要通过氢键和疏水作用与AChE的7个氨基酸残基结合,结合自由能较低,结合相对稳定,可有效抑制AChE的活性,揭示了发芽糙米GABA对AChE具有抑制作用的微观机理。总而言之,发芽糙米GABA不但可以作为新型的抗氧化剂,减弱神经细胞的氧化应激损伤,还可以作为AChE的抑制剂,抑制神经递质代谢酶,在缓解抑郁症状及预防阿尔茨海默症的功能性食品开发中具有积极应用价值。
[1] 牟敦山, 杨笑难, 蒋超, 等.糙米营养特性及加工技术研究进展[J].粮食问题研究, 2024(5):30-33;44.
MOU D S, YANG X N, JIANG C, et al.Research progress on nutritional characteristics and processing technology of brown rice[J].Grain Issues Research, 2024(5):30-33;44.
[2] 符琼, 周文化, 黄卫文, 等.发芽糙米生物活性物质及生理功能研究进展[J].食品工业科技, 2019, 40(14):325-333.
FU Q, ZHOU W H, HUANG W W, et al.Research progress on bioactive substances and physiological function of germinated brown rice[J].Science and Technology of Food Industry, 2019, 40(14):325-333.
[3] DOS SANTOS MOREIRA N C, DE FREITAS LIMA J E B, MARCHIORI M F, et al.Neuroprotective effects of cholinesterase inhibitors:Current scenario in therapies for Alzheimer’s disease and future perspectives[J].Journal of Alzheimer’s Disease Reports, 2022, 6(1):177-193.
[4] MAJIDAZAR R, REZAZADEH-GAVGANI E, SADIGH-ETEGHAD S, et al.Pharmacotherapy of Alzheimer’s disease:An overview of systematic reviews[J].European Journal of Clinical Pharmacology, 2022, 78(10):1567-1587.
[5] KHAN T, WASEEM R, SHAHID M, et al.Recent advancement in therapeutic strategies for Alzheimer’s disease:Insights from clinical trials[J].Ageing Research Reviews, 2023, 92:102113.
[6] CHEONG S L, TIEW J K, FONG Y H, et al.Current pharmacotherapy and multi-target approaches for Alzheimer’s disease[J].Pharmaceuticals, 2022, 15(12):1560.
[7] 郑礼平, 王玉婷, 倪罗番, 等.兼具抗氧化和γ-氨基丁酸增强活性的多功能抗脑卒中化合物[J].南京医科大学学报(自然科学版), 2022, 42(5):644-649.
ZHENG L P, WANG Y T, NI L F, et al.Multifunctional anti-stroke compounds with both antioxidant and γ-aminobutyric acid enhancing activity[J].Journal of Nanjing Medical University (Natural Sciences), 2022, 42(5):644-649.
[8] OKADA T, SUGISHITA T, MURAKAMI T, et al.Effect of the defatted rice germ enriched with GABA for sleeplessness, depression, autonomic disorder by oral administration[J].Nippon Shokuhin Kagaku Kogaku Kaishi, 2000, 47(8):596-603.
[9] 宁亚维, 刘祥贵, 王志新, 等.小米糙米发芽富集γ-氨基丁酸[J].食品与生物技术学报, 2019, 38(1):53-57.
NING Y W, LIU X G, WANG Z X, et al.Improve γ-aminobutyric acid content by the germination of brown foxtail millet[J].Journal of Food Science and Biotechnology, 2019, 38(1):53-57.
[10] 杨胜远, 邓宝君, 谭微珠.戊糖片球菌发酵番茄富集γ-氨基丁酸工艺条件优化[J].食品研究与开发, 2024, 45(19):113-120.
YANG S Y, DENG B J, TAN W Z.Optimization of fermentation conditions for enriching γ-aminobutyric acid in tomato by Pediococcus pentosaceus[J].Food Research and Development, 2024, 45(19):113-120.
[11] 李雁琴. 红枣中GABA检测方法优化及其变化规律的研究[D].阿拉尔:塔里木大学, 2020.
LI Y Q.Study on the optimization of γ-aminobutyric acid detection method and in variation rule in jujube[D].Alaer:Tarim University, 2020.
[12] MOYO B, OYEDEMI S, MASIKA P J, et al.Polyphenolic content and antioxidant properties of Moringa oleifera leaf extracts and enzymatic activity of liver from goats supplemented with Moringa oleifera leaves/sunflower seed cake[J].Meat Science, 2012, 91(4):441-447.
[13] 薛山, 赵昕源, 胡潘虹.Plackett-Burman试验结合Box-Behnken响应面法优化琯溪蜜柚海绵层水溶性抗氧化膳食纤维猪肉丸加工配方[J].食品工业科技, 2024, 45(10):176-186.
XUE S, ZHAO X Y, HU P H.Plackett-burman test combined with box-behnken response surface method to optimize the formulation of pork meatball added with soluble antioxidant dietary fiber from sponge layer of Guanxi pomelo[J].Science and Technology of Food Industry, 2024, 45(10):176-186.
[14] 刘琼玉, 周培疆, 陈岩.氯酚对乙酰胆碱酯酶的抑制作用及其动力学研究[J].武汉大学学报(理学版), 2010, 56(5):542-546.
LIU Q Y, ZHOU P J, CHEN Y.Inhibition effect of chlorophenols on acetylcholinesterase and its kinetics[J].Journal of Wuhan University (Natural Science Edition), 2010, 56(5):542-546.
[15] YANG D S, ZHANG L P, GAO S, et al.Effects of grape seed proanthocyanidin on the conformation and functional properties of lamb myofibrillar protein under hydroxyl radical-induced oxidative stress[J].LWT, 2025, 222:117625.
[16] SHEN S G, JIA S R, WU Y K, et al.Effect of culture conditions on the physicochemical properties and antioxidant activities of polysaccharides from Nostoc flagelliforme[J].Carbohydrate Polymers, 2018, 198:426-433.
[17] 梁志满. 乙酰胆碱酯酶特异性适配子对阿尔茨海默症转基因小鼠模型的作用研究[D].广州:南方医科大学, 2019.
LIANG Z M.The effects of acetylcholinesterase-specific aptamer on Alzheimer’s disease transgenic model[D].Guangzhou:Southern Medical University, 2019.
[18] YA AR Ü, DEMIR Y, GÖNÜL
AR Ü, DEMIR Y, GÖNÜL ![]() et al.Novel schiff base sulfonate derivatives as carbonic anhydrase and acetylcholinesterase inhibitors:Synthesis, biological activity, and molecular docking insights[J].Chemistry &Biodiversity, 2025, 22(5):e202402893.
et al.Novel schiff base sulfonate derivatives as carbonic anhydrase and acetylcholinesterase inhibitors:Synthesis, biological activity, and molecular docking insights[J].Chemistry &Biodiversity, 2025, 22(5):e202402893.
[19] BATHULA S, SANKARANARAYANAN M, MALGIJA B, et al.2-amino thiazole derivatives as prospective aurora kinase inhibitors against breast cancer:QSAR, ADMET prediction, molecular docking, and molecular dynamic simulation studies[J].ACS Omega, 2023, 8(46):44287-44311.
[20] 李泽飞, 王平.基于分子对接与分子动力学模拟探讨生慧颗粒有效成分对γ氨基丁酸A型受体与乙酰胆碱酯酶的作用机制[J].中华中医药杂志, 2024, 39(1):157-162.
LI Z F, WANG P.Discussion on the mechanism of Shenghui Granule acting on GABAaR and AChE based on molecular docking and molecular dynamics simulation[J].China Journal of Traditional Chinese Medicine and Pharmacy, 2024, 39(1):157-162.
[21] 郭妍, 郭怡琳, 刘柏平, 等.基于分子动力学模拟与实验验证探讨黄芩素抑制PD-1/PD-L1相互作用的分子机制[J].食品工业科技, 2024, 45(2):40-47.
GUO Y, GUO Y L, LIU B P, et al.Mechanism of baicalein inhibiting the PD-1/PD-L1 interaction based on molecular dynamics simulation and experiment research[J].Science and Technology of Food Industry, 2024, 45(2):40-47.
[22] LUAN J S, HU B C, WANG S Z, et al.Selectivity mechanism of BCL-XL/2 inhibition through in silico investigation[J].Physical Chemistry Chemical Physics, 2022, 24(28):17105-17115.
[23] LIN X Q, LI X, LIN X B.A review on applications of computational methods in drug screening and design[J].Molecules, 2020, 25(6):1375.
[24] SAJID ALI M, SINGH E, MUTHUKUMARAN J, et al.Non-steroidal anti-inflammatory drug effect on the binding of plasma protein with antibiotic drug ceftazidime:Spectroscopic and in silico investigation[J].International Journal of Molecular Sciences, 2023, 24(19):14811.
[25] 张志森. Jarzynski Equality计算自由能在生物大分子体系中的应用[D].杭州:浙江大学, 2014.
ZHANG Z S.Free energy calculation by Jarzynski Equality for biomolecular complex[D].Hangzhou:Zhejiang University, 2014.