蜂胶是植物树脂和蜜蜂唾液分泌物的混合物[1],主要成分为树脂(50%)、蜡和脂肪酸(30%)、芳香族化合物和精油(10%)、花粉(5%)以及矿物和有机化合物(5%),是重要生物活性物质的来源,可减少食品中添加剂的使用或降低治疗药物的浓度[2]。蜂胶提取物(propolis extract,PE)是在除蜡后得到的有效成分[3],鉴定出超过850种化合物[4],包括黄酮类、酚酸类、萜类、氨基酸及维生素等[5],常用溶剂(水、乙醇或者油)提取或超临界萃取,其中乙醇法PE存在风味残留和安全隐患,这在一定程度上限制了其在食品中的应用[6];水提法PE能更好地保护生物活性物质,更高效地抑制自由基产生[7],显著降低肿瘤细胞的生长和增殖[8]。尽管PE具有显著的健康作用,但其水溶性低、稳定性不足[9],且研究表明PE对食品感官接受度的最高添加量≤0.5%[10]。为此,利用各种载体(如纳米颗粒、脂质体、乳剂和多糖)去包埋PE[11],可防止因热、氧化和紫外线而导致活性物质的降解[12],提高溶解度和生物利用度,还可以掩盖不良气味和味道[13],有助于PE的高值化应用。
羧甲基壳聚糖(carboxymethyl chitosan,CMCS)是一种线性大分子结构的水溶性壳聚糖(chitosan,CS)衍生物,具有良好的水溶性和生物相容性的特性,对一些生物活性物质有很好的保护和缓释作用[14]。研究发现,CMCS(2%)和凹凸棒黏土(0.15%)(均为质量分数)协同可对精油进行包封和缓释,提高抑菌活性并延长抑菌时间[15]。此外,β-环糊精(β-cyclodextrin,β-CD)是一种外部相对亲水、内部由于C—H的屏蔽作用而疏水的环状低聚糖,可与活性分子通过疏水作用力和氢键以包合物的形式存在,通过提高疏水分子的稳定性或水溶性有效实现活性分子的共载[16]。研究表明,β-CD为壁材的分子包合方法可以有效地保护蜂胶中的生物活性化合物,得到具有抑制胃癌细胞系癌细胞增殖能力的微粒[17]。CMCS的阳离子特性和β-CD的阴离子特性[18]使其能够通过静电相互作用自组装形成共载体系,在活性物质包埋方面潜力巨大[19]。利用β-CD将β-胡萝卜素包埋在空腔中,然后通过—NH2和—OH基团与CS形成氢键,可构成双重包埋体系实现对β-胡萝卜素的保护[20]。β-CD和2种不同的水溶性壳聚糖衍生物(盐酸壳聚糖和CMCS)自组装成共载体系,通过双重包埋花青素,提高了稳定性[21]。CS和透明质酸作为壁材料,包埋PE后提高了溶解性和稳定性[22]。然而,对于CMCS/β-CD协同包埋PE的相关研究尚未涉及。
因此,本研究以蜂胶水提取物为研究对象,采用自组装法制备了CMCS/β-CD-PE共载体系,并进行制备条件优化,利用形貌表征和结构分析探究共载体系的形成机理,以期为PE的广泛应用奠定基础。
1 材料与方法
1.1 材料与试剂
PE,重庆昂科生物科技有限公司;β-CD,天津希恩思奥普德科技有限公司;CMCS,上海麦克林生化科技有限公司。
1.2 仪器与设备
A101色差仪,美国科诺工业有限公司;场发射扫描电子显微镜(scanning electron microscopy,SEM),英国卡尔蔡司公司;透射电子显微镜(transmission electron microscopy,TEM),日本HITACHI公司;原子力显微镜(atomic force microscope,AFM),法国HORIBA FRANCE SASTGL-16公司;马尔文激光粒度仪,英国马尔文公司;Spectrum 100红外光谱仪(Fourier infrared spectrometer,FTIR),美国Perkin-Elmer公司;X射线衍射仪(X-ray diffraction,XRD),荷兰帕纳特公司;差式扫描量热仪(differential scanning calorimetry,DSC),美国珀金埃尔默公司。
1.3 实验方法
1.3.1 CMCS/β-CD-PE共载体系制备
β-CD、PE和CMCS共载体系主要通过自组装方法制备[12]。1)不同添加顺序的共载体系制备。首先将CMCS和β-CD粉末分别溶于去离子水中,充分搅拌至完全溶解,使得CMCS和β-CD的质量浓度均为12 g/L。然后将PE粉末添加到上述溶液中,持续搅拌30 min,所得样品记为CMCS-PE和β-CD-PE,其中PE的质量浓度为5 g/L;将CMCS和β-CD溶液等体积混合,持续搅拌30 min,所得样品记为CMCS/β-CD。分别取等体积的β-CD和CMCS溶液加入CMCS-PE和CD-PE溶液中,充分搅拌30 min,得到CMCS-PE-β-CD和β-CD-PE-CMCS共载体系;将PE粉末加入到CMCS/β-CD溶液中,得到CMCS/β-CD-PE共载体系。作为对照组,将PE粉末直接溶解在水中,样品记为W-PE。
2)不同质量浓度的CMCS/β-CD-PE共载体系制备。固定β-CD的质量浓度为12 g/L,将不同质量浓度的CMCS溶液(2、4、12、36、72 g/L)等体积加入β-CD溶液中,持续搅拌30 min,使得CMCS和β-CD的比例分别为1∶6、1∶3、1∶1、3∶1和6∶1,在不同比例下添加不同浓度的PE粉末(1.25、2.5、5、10、20 g/L)后搅拌30 min,得到CMCS/β-CD-PE(1-5)共载体系,探究不同CMCS/β-CD比例和PE浓度对CMCS/β-CD-PE共载体系色泽的影响。
1.3.2 CMCS/β-CD-PE共载体系的稳定性和色泽
1.3.2.1 添加顺序对CMCS/β-CD-PE共载体系稳定性的影响
将所得到的CMCS-PE、CD-PE、W-PE、CMCS-PE-β-CD、β-CD-PE-CMCS和CMCS-β-CD-PE 6组样品在4 ℃下贮存10 d后,观察不同物质共载PE后的稳定性。
1.3.2.2 不同质量浓度对CMCS/β-CD-PE共载体系色泽的影响
CIE Lab色度学参数包括L*、a*和b*,由色度计在室内光照下记录CMCS/β-CD-PE溶液的色泽。所有测量均至少进行3次。
1.3.3 CMCS/β-CD-PE共载体系的形貌表征
1.3.3.1 SEM表征
冻干后的CMCS/β-CD-PE共载体系以及各组分固体粉末,通过场发射扫描电子显微镜记录上述样品的SEM图像,以了解其形态特征。将待测样品镀金以获得优异的导电效果,并在微观水平上重复观察3次。
1.3.3.2 TEM表征
将10 μL新鲜配制的CMCS/β-CD-PE溶液,滴加至50目的碳涂层铜网上,随后用磷钨酸溶液染色5 min,待自然干燥后即可进行检测。
1.3.3.3 AFM表征
借助Veeco Nanoscope V Multimode 8扫描探针显微镜对样品进行AFM观察。在机器扫描之前,需取10 μL CMCS/β-CD-PE溶液小心地滴在光滑的云母片上,静置风干后,采用接触模式来捕捉其形态。
1.3.4 CMCS/β-CD/PE共载体系的结构表征
1.3.4.1 Zeta电位和粒径
在25 ℃条件下,使用纳米激光粒度仪测量在CMCS/β-CD-PE溶液的zeta电位与粒径。为了避免多粒子效应,样品溶液用相应pH值的去离子水稀释20倍以测定zeta电位[19]。
1.3.4.2 FTIR
首先扫描背景,然后将CMCS/β-CD-PE冻干样品放在平台上,使用衰减全反射模式收集光谱,使用FTIR仪在4 000~400 cm-1波数范围内扫描样品。
1.3.4.3 XRD
检测CMCS/β-CD-PE冻干复合样品的XRD光谱。以2 °/min的扫描速度在2θ范围为5°~60°采集谱图[21]。
1.3.4.4 DSC
将CMCS/β-CD-PE冻干粉末置于密封的铝锅中,以10 ℃/min的升温速率从30 ℃迅速加热至230 ℃,同时通入20 mL/min的N2进行保护。样品图谱信息借助DSC记录并分析。
1.3.5 数据处理
试验设3次重复,结果以“平均值±标准差”表示。数据采用SPSS进行统计分析,均值间采用Duncan多重比较,显著性水平为P<0.05;采用Origin 2024作图。
2 结果与分析
2.1 CMCS、β-CD和PE共载体系的工艺优化
2.1.1 添加顺序对CMCS/β-CD-PE共载体系稳定性的影响
将CMCS和β-CD以不同添加顺序包埋PE,4 ℃条件下静置10 d。由图1-a可知,0 d的W-PE显示明显沉淀、β-CD-PE显示轻微沉淀,CMCS-PE和CMCS/β-CD-PE、β-CD-PE-CMCS、CMCS-PE-β-CD均表现稳定。如图1-b可知,4 ℃条件下贮存10 d的W-PE、β-CD-PE、CMCS-PE、β-CD-PE-CMCS和CMCS-PE-β-CD表现出明显的沉淀和聚集,而CMCS/β-CD-PE的稳定性良好,且倒置后流动性也较好。贮存稳定性的差异可能是由于亲脂性的PE不能很好地分散在β-CD溶液和水中[23],但是可以很好地溶解在CMCS中[24];这与EBADI等[25]将PE添加到CS溶液中的稳定性研究结果一致;且在杨萌[26]利用壳聚糖季铵盐/β-CD以及CMCS/γ-CD递送体系对蛋清肽和姜黄素进行包埋后的稳定性研究得到进一步验证。因此,CMCS/β-CD-PE共载物体系的添加顺序设置为CMCS→β-CD→PE。

a-0 d;b-10 d
图1 CMCS/β-CD-PE共载体系的添加顺序优化
Fig.1 Optimization of the addition sequence of the CMCS/β-CD-PE co-loading system
注:图1-a和图1-b从左到右依次为CMCS/PE-β-CD、β-CD-PE-CMCS、CMCS/β-CD-PE、W-PE、β-CD-PE、CMCS-PE。
2.1.2 不同CMCS和PE质量浓度对CMCS/β-CD-PE共载体系色泽的影响
由于PE中含有丰富的多酚类化合物,而多酚类化合物具有多个生色团(如C![]() C和C
C和C![]() O),这些生色团具有较强的紫外光吸收能力,这非常有利于保护富含蛋白质和脂质的食品免受光诱导的氧化变质,并且当PE的添加量增加时,样品的黄色加深[25]。因此进一步研究了CMCS和PE质量浓度对CMCS/β-CD-PE共载体系色泽的影响。
O),这些生色团具有较强的紫外光吸收能力,这非常有利于保护富含蛋白质和脂质的食品免受光诱导的氧化变质,并且当PE的添加量增加时,样品的黄色加深[25]。因此进一步研究了CMCS和PE质量浓度对CMCS/β-CD-PE共载体系色泽的影响。
由图2可知,当CMCS/β-CD质量比为1∶1时,CMCS/β-CD-PE样品的a*和b*值总体上高于其他样品,这可能归因于β-CD和CMCS复合物对PE的充分包埋。从整体上看,a*和b*均随着PE含量的增加而增加,但是在PE质量浓度达到5 g/L时,随着PE浓度的进一步增加,它们减少或趋于不变,这可能是由于PE过量,无法彻底包埋,从而聚集或者沉淀,导致a*和b*值降低。而随着PE浓度的增加,L*呈现逐渐降低的趋势[20]。综合来看,CMCS/β-CD-PE3比CMCS/β-CD-PE1、CMCS/β-CD-PE2、CMCS/β-CD-PE4和CMCS/β-CD-PE5有更令人满意的颜色参数。此外,在图2-f中,5 g/L质量浓度的CMCS/β-CD-PE3共载体系比PE水溶液有着更加稳定的色泽,10 d后也未发生沉淀。因此,最终选择用于进一步研究的PE质量浓度为5 g/L, CMCS∶β-CD比例为1∶1。

a-CMCS∶β-CD=1∶3;b-CMCS∶β-CD=1∶2;c-CMCS∶β-CD=1∶1;d-CMCS∶β-CD=2∶1;e-CMCS∶β-CD=3∶1;f-CMCS/β-CD-PE共载体系色泽
图2 不同CMCS和PE添加量对共载体系色泽的影响
Fig.2 Effects of different addition amounts of CMCS and PE on the color of the co-loading system
注:图2-f中从左到右依次为CMCS/β-CD-PE中PE添加量1.25、2.5、5、10、20 g/L(CMCS∶β-CD=1∶1)和5 g/L PE水溶液。不同小写字母表示差异显著(P<0.05)(下同)。
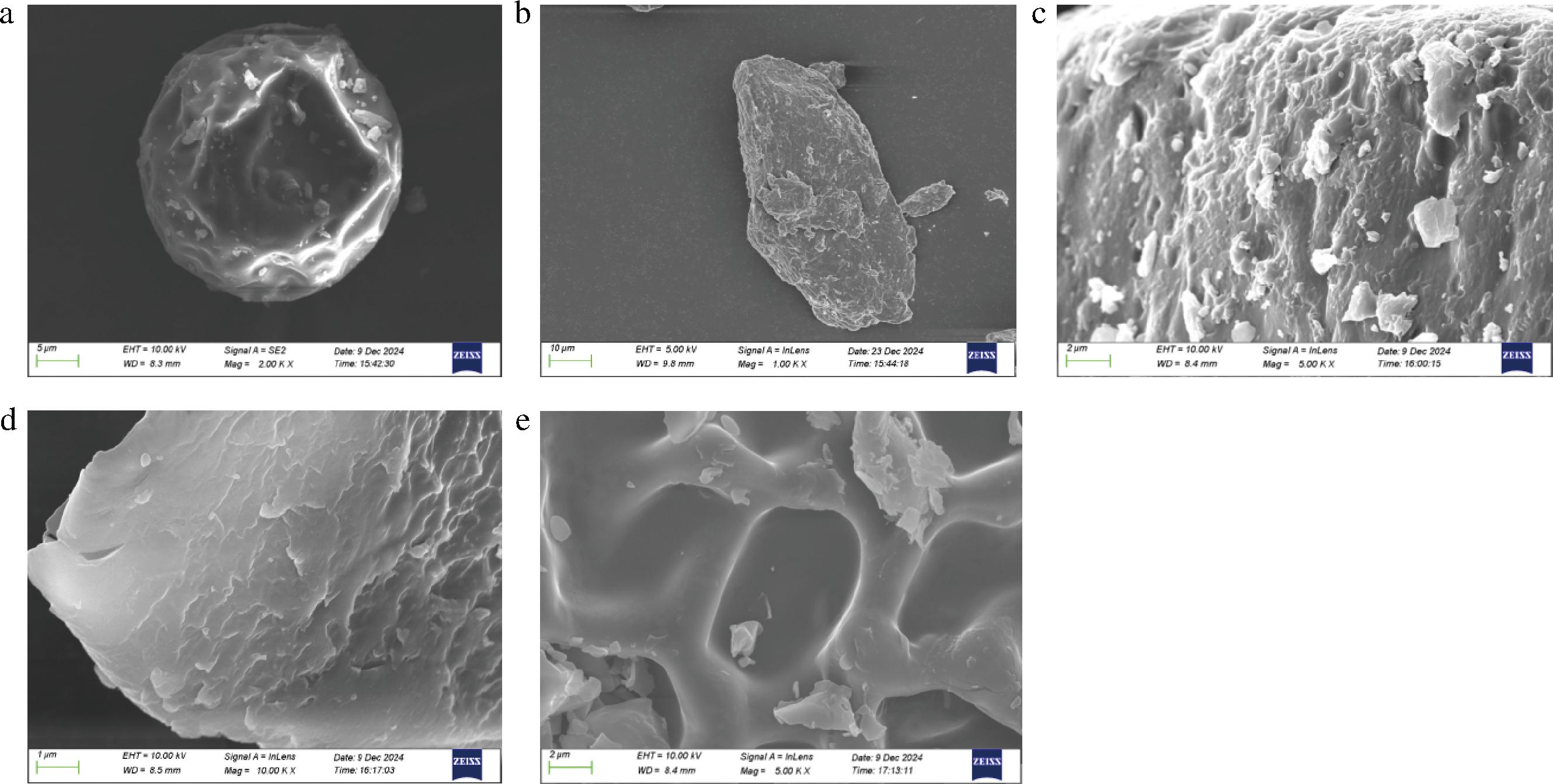
a-PE;b-CMCS;c-β-CD;d-CMCS/β-CD;e-CMCS/β-CD-PE
图3 PE、CMCS、β-CD、CMCS/β-CD和CMCS/β-CD-PE的SEM图像
Fig.3 SEM images of PE, CMCS, β-CD, CMCS/β-CD, and the CMCS/β-CD-PE
2.2 CMCS/β-CD-PE共载体系的形貌表征
2.2.1 SEM分析
如图3所示,CMCS、β-CD和PE单一组分的形态各异。β-CD呈现大颗粒并伴有团簇现象,表面光滑且边缘略显隆起,凸显β-CD在复合物中的主导地位。CMCS则表现出不规则的结构,表面排列方式不同,颗粒较大,多为碎片化结构;CMCS/β-CD具有相似的外观,表面有许多不规则片状结构,有些地方有类似β-CD的凸起,证明两者的结合;PE则显示大尺寸的球形晶体,表面多有凹状结构,附着许多微小结构、比较圆润;研究发现,掺入PE后,一些CS膜中会出现一些孔隙或裂纹,这些孔洞或裂纹的形成是由于PE与膜基质之间的相容性较低,从而影响膜的阻隔性和机械性能[26]。与单一组分相比,CMCS/β-CD-PE显示带有许多微小的薄片,表面比其他样品光滑得多,还有许多圆润的小坑,具有各组分的部分特征,且形态结构和晶体性质发生了巨大变化[27],这可能是形成包涵复合物的迹象。
2.2.2 TEM分析
TEM图像如图4所示。PE水溶液表现出许多球状和方块状,而CMCS表现出片状不规则结构,这与SEM的结果一致,而β-CD 的微观结构则表现出结晶状态,具有不规则的方块状结构,这是因为 β-CD 内部的C—H基团形成了非极性疏水空腔,而外部的极性伯羟基则对水分子具有吸引作用,赋予了 β-CD 独特的“外亲水、内疏水”的结构特性,这与李亚娟等[19]的研究结果一致。当其与CMCS结合之后,则呈现出相对比较规则且分散均匀的类球形结构,说明在氢键和空间位阻影响下,CMCS吸附交错在β-CD的表面,降低其结晶性[21]。而在加入PE后,CMCS/β-CD-PE表现出较大的块状结构和球状,具有PE的部分特征,进一步说明三者的成功共载。CORREA-PACHECO等[28]在观察可食性蜂胶-壳聚糖纳米颗粒膜时,发现PE在与CS结合后也会形成白色的圆点和较大聚合物。

a-PE;b-CMCS;c-β-CD;d-CMCS/β-CD;e-CMCS/β-CD-PE
图4 PE、CMCS、β-CD、CMCS/β-CD和CMCS/β-CD-PE共载体系的TEM图像
Fig.4 TEM images of PE, CMCS, β-CD, and of the co-loading systems CMCS/β-CD and CMCS/β-CD-PE
2.2.3 AFM分析
如图5所示,PE、CMCS和β-CD的高度分别在-1.52~11.28、-3.6~14.91、-2.92~17.25 nm,表面均有一定的粗糙度;而相比于CMCS/β-CD(43.63 nm),CMCS/β-CD-PE(7.12 nm)则呈现出更加有序而紧凑的三维结构,且其表面粗糙度明显降低,表明其结构上发生了显著变化,证明了CMCS/β-CD共载体系对PE包埋成功。有研究发现蜂胶的加入使得薄膜样品的表面变得更加均匀[29]。然而,通过AFM 分析得到的样品粒径结果存在显著性差异。这种现象可能主要归因于 AFM 样品制备过程(如干燥过程)中共载体系内多组分水化层减少[30]。与此同时,显著的粒径差异也在一定程度上预示着PE作为共载成分吸附于体系内层的可能。

a-PE;b-CMCS;c-β-CD;d-CMCS/β-CD;e-CMCS/β-CD-PE
图5 PE、CMCS、β-CD、CMCS/β-CD和CMCS/β-CD-PE的AFM图像
Fig.5 AFM images of PE, CMCS, β-CD, CMCS/β-CD and CMCS/β-CD-PE
2.3 CMCS/β-CD-PE共载体系的结构表征分析
2.3.1 zeta电位和粒径分析
如图6-a所示,CMCS/β-CD-PE共载体系的zeta电位值保持在-30 mV左右,较为稳定。Zeta电位随着共载体系的形成,展现出三者的结合规律,这可能是由于共载体系中更多的—NH3+基团的CMCS增强了静电排斥力[24]。此外,为了进一步证明CMCS/β-CD/PE共载体系的形成,分别测定了各个分散体系的粒径。结果如图6-b所示,单一组分PE、β-CD和CMCS的粒径分别为805.4、372.2、4 150.3 nm,而形成CMCS/β-CD-PE后其粒径增加为4 778.3 nm,说明CMCS/β-CD对PE包埋成功。LIU等[21]测得包埋ACN的β-CD-CHC/CMC纳米复合物具有较小的粒径(333.86 nm)和zeta电位(+45.97 mV);李亚娟等[19]测得β-CD、CHC及β-CD/CHC分散体系的粒径为2.88、1.92、3.53 μm,具有与本实验相似的结果;而PANT等[31]将麦芽糊精作为壁材、真空干燥制备的蜂胶粉末超过90%的颗粒粒径在89.34 μm左右,再次证明了本实验结果的科学合理性。
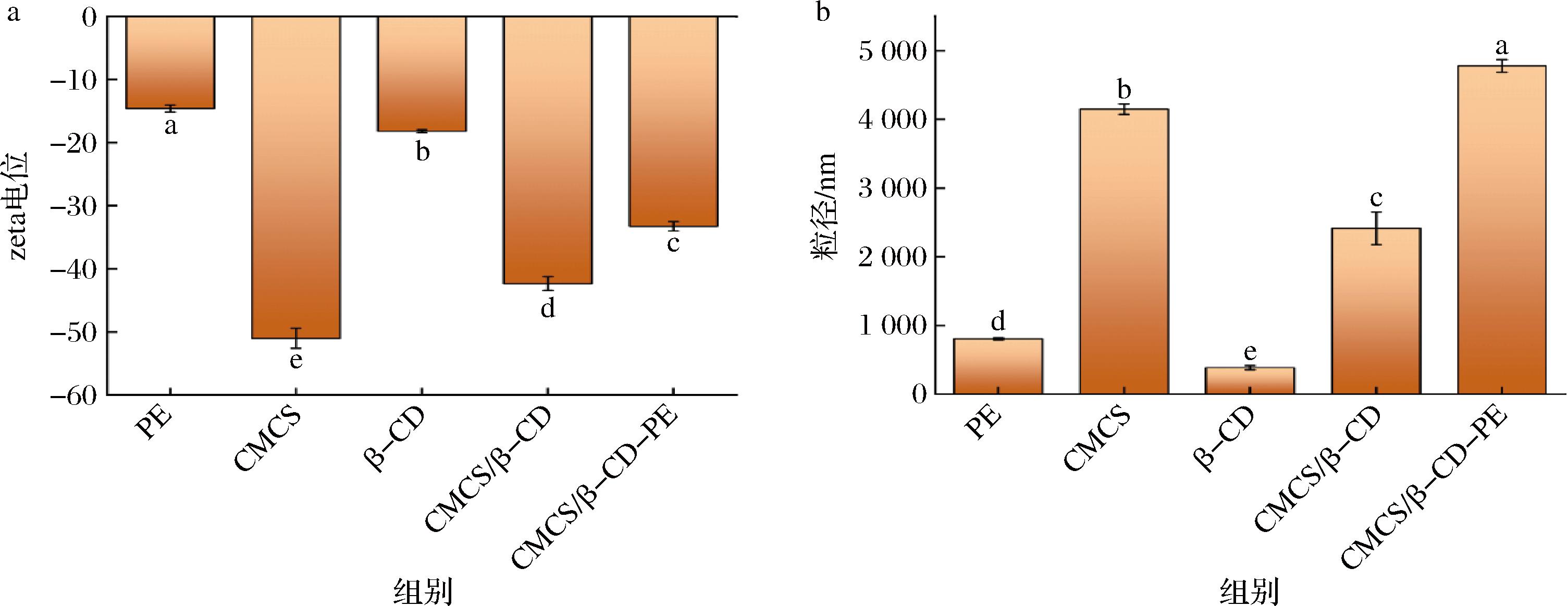
a-zeta电位;b-粒径
图6 PE、CMCS、β-CD、CMCS/β-CD和CMCS/β-CD-PE的zeta电位和粒径
Fig.6 Zeta potential and particle size of PE, CMCS, β-CD, CMCS/β-CD, and CMCS/β-CD-PE
2.3.2 FTIR分析
通过FTIR来进一步探究共载体系内多组分间相互作用类型及机制。如图7-a所示,PE在3 304 cm-1处出现峰值,这与羟基(O—H)和氨基(N—H)基团的拉伸有关,可能是由多酚、碳水化合物,或者蛋白质和水引起[31]。位于2 924 cm-1的峰与C—H键的不对称拉伸振动、游离氨基酸的NH3+带拉伸振动以及羧酸的相应振动有关;而1 652、1 596 cm-1处的峰则归因于PE中类黄酮和脂质成分的C![]() O键和C
O键和C![]() C键的对称振动,以及N—H键的变形振动。DE OLIVEIRA CARDOSO等[32]报道的PE中在1 300~1 000 cm-1的光谱区域描述了由醚、酯、醇和羧酸引起的C—O的拉伸和C—OH基团的弯曲,这主要与PE中的酚酸和类黄酮有关。而519 cm-1附近的峰值与环畸变有关。β-CD的特征峰在3 200~3 500 cm-1范围内呈现为宽峰,这与O—H伸缩振动有关[19]。此外,β-CD在2 923、1 411、1 022 cm-1处的特征峰分别代表饱和烷烃(—CH3)的伸缩振动、O—H弯曲振动和C—O—C的伸缩振动;在CMCS光谱中,位于3 354 cm-1处的峰对应于氢键O—H或N—H伸缩振动,1 587、1 409 cm-1处为羧基的非对称和对称伸缩振动吸收峰,1 055 cm-1处为葡萄糖环中C—O—C的伸缩振动吸收峰;当β-CD与CMCS结合后,β-CD在3 303 cm-1处的特征峰明显增强,同时CMCS在1 587、1 409 cm-1处的峰强度明显降低。此外,CMCS位于1 055 cm-1特征峰在β-CD/CMCS复合颗粒中移动到1 026 cm-1,这些实验结果表明,氢键与静电相互作用在β-CD与CMCS复合颗粒的形成过程中起着至关重要的作用。
C键的对称振动,以及N—H键的变形振动。DE OLIVEIRA CARDOSO等[32]报道的PE中在1 300~1 000 cm-1的光谱区域描述了由醚、酯、醇和羧酸引起的C—O的拉伸和C—OH基团的弯曲,这主要与PE中的酚酸和类黄酮有关。而519 cm-1附近的峰值与环畸变有关。β-CD的特征峰在3 200~3 500 cm-1范围内呈现为宽峰,这与O—H伸缩振动有关[19]。此外,β-CD在2 923、1 411、1 022 cm-1处的特征峰分别代表饱和烷烃(—CH3)的伸缩振动、O—H弯曲振动和C—O—C的伸缩振动;在CMCS光谱中,位于3 354 cm-1处的峰对应于氢键O—H或N—H伸缩振动,1 587、1 409 cm-1处为羧基的非对称和对称伸缩振动吸收峰,1 055 cm-1处为葡萄糖环中C—O—C的伸缩振动吸收峰;当β-CD与CMCS结合后,β-CD在3 303 cm-1处的特征峰明显增强,同时CMCS在1 587、1 409 cm-1处的峰强度明显降低。此外,CMCS位于1 055 cm-1特征峰在β-CD/CMCS复合颗粒中移动到1 026 cm-1,这些实验结果表明,氢键与静电相互作用在β-CD与CMCS复合颗粒的形成过程中起着至关重要的作用。
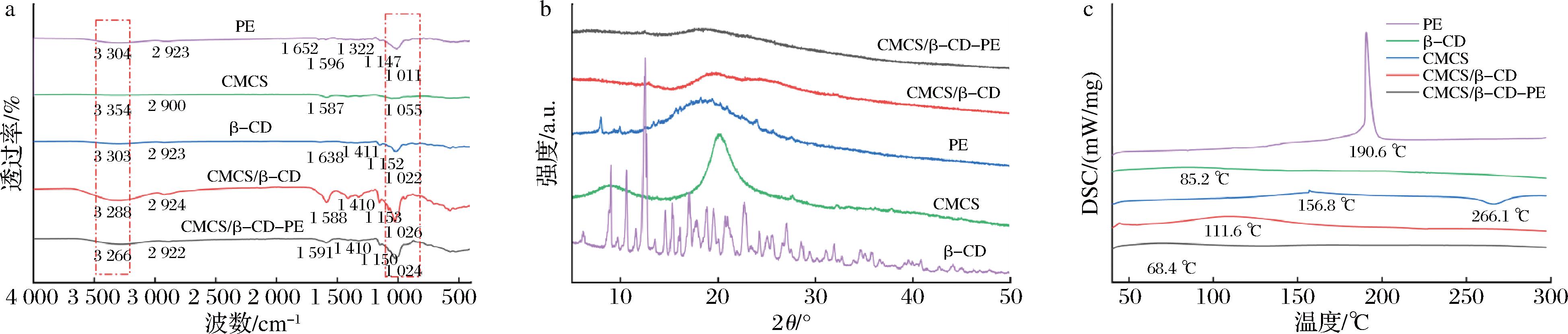
a-FTIR谱图;b-XRD谱图;c-DSC谱图
图7 PE、β-CD、CMCS、CMCS/β-CD和CMCS/β-CD-PE共载体系的FTIR谱图、XRD谱图和DSC谱图
Fig.7 FTIR spectra, XRD patterns, and DSC curves of the co-loading systems of PE, β-CD, CMCS, CMCS/β-CD, and CMCS/β-CD-PE
β-CD/CMCS和CMCS/β-CD-PE共载体系具有非常相似的FTIR光谱,没有额外的峰出现,证明了共载体系各组分间是没有新的共价键形成的物理相互作用[33]。并且,在CMCS/β-CD-PE的光谱中,3 304、1 652 cm-1处的峰相比于PE明显增强,PE在1 652 cm-1处的特征峰消失,1 011 cm-1处的峰在CMCS/β-CD-PE中移动到1 024 cm-1,这表明PE可能通过疏水相互作用和范德华力相互作用被包埋到CMCS/β-CD复合物中,因此,PE原有的红外特征很可能被β-CD或CMCS的光谱所掩盖或干扰,难以直接观测。CMCS/β-CD-PE体系中较宽的O—H谱带(3 200~3 500 cm-1)和峰强度的增强,进一步分析可能是由于β-CD的—OH和CMCS的—NH2基团之间的氢键作用,或者这些基团的伸缩频率存在重叠。这与杨萌[26]自组装构建的壳聚糖季胺盐/β-CD以及CMCS/γ-CD递送体系有着类似的结构,CMCS和β-CD之间的强相互作用促进了PE的稳定包埋,形成具有高强度的氢键、静电相互作用和更多的无定形、高效的共载结构。
2.3.3 XRD分析
借助XRD可以更好地阐明PE在共载体系中的包埋效果。如图7-b所示,β-CD呈现出典型笼型结晶谱图和特征峰[19](2θ=10.61°、12.51°有反射),而CMCS和PE分别在20.19°和18.56°有很强的反射,表明其为无定形态[20]。在CMCS/β-CD的谱图中,与β-CD相对应的特征峰存在被掩盖或强度降低的现象,这进一步表明CMCS能够以无定形态的结构环绕在β-CD周围。值得关注的是,PE的特征峰在CMCS/β-CD-PE中显著降低,一些噪音也完全消失,这一现象可能是共载体系对于活性物质(PE)的有效包埋。此外,CMCS/β-CD-PE相比于各单一物质表现出更宽峰,这意味着各物质的晶体结构被破坏,相发生变化[34]。结晶度的降低可能是由于PE能够渗透到共载体系网络中,与生物聚合物链形成强的分子间相互作用,破坏了生物聚合物的有序结晶结构[26]。原因总结如下:1)PE发生分离,以分子形式进入到β-CD的疏水腔中,形成包埋复合物;2)CMCS的存在进一步限制这些PE分子,抑制其结晶并在共载系统中形成无定形态。
2.3.4 DSC分析
DSC可用于评估复合物的热稳定性。如图7-c所示,β-CD的曲线显示85 ℃处有最大吸热峰,CMCS在156 ℃有最大吸收峰,PE的吸热峰出现在190 ℃,这一结果表明PE具有较高的热稳定性。对于β-CD来说,与CMCS结合后的吸热峰转移到更高的温度(111.6 ℃),增强了β-CD的热稳定性。CMCS/β-CD-PE共载体系的吸热峰在68 ℃处,而PE的特征峰消失,表明PE可能进入CMCS/β-CD的空腔形成包合物[21]。多项研究表明,加入PE后,一些胶膜的玻璃化转变温度(Tg)和熔融温度(Tm)均有所下降,相比于不添加PE的薄膜,含有PE的薄膜具有更低的热性能,因为PE会严重破坏聚合物链构象的完整性[26]。因此CMCS/β-CD可以有效共载PE。
2.4 CMCS/β-CD-PE共载体系形成机理分析
根据上述结果,本研究提出了CMCS/β-CD共载PE的机理,如图8所示。
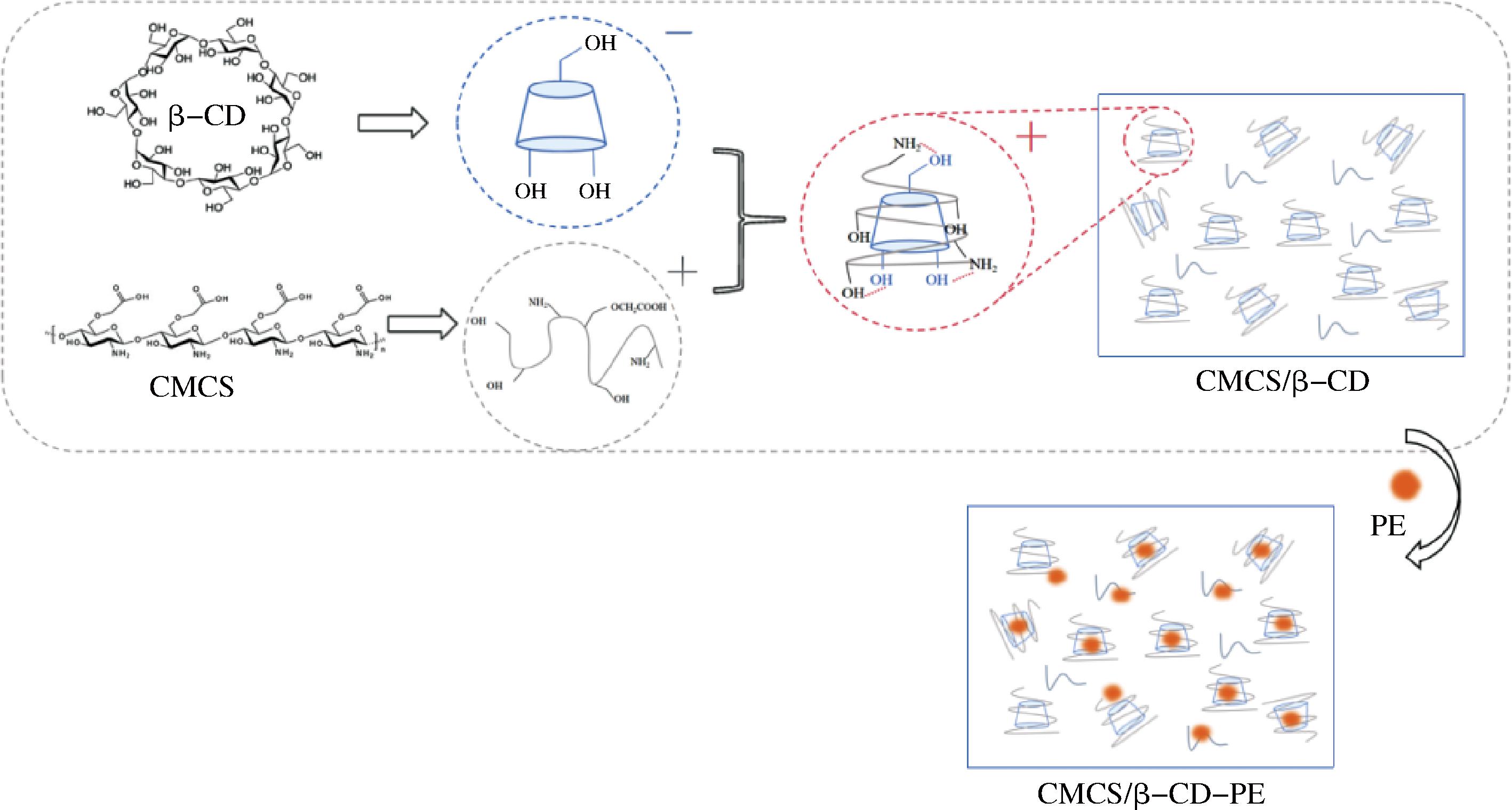
图8 CMCS/β-CD-PE共载原理图
Fig.8 Schematic diagram of the co-loading mechanism of CMCS/β-CD-PE
β-CD作为一类带正电的天然环状分子,具有内疏水、外亲水的圆台结构,使其具备共载亲水和疏水小分子活性物质的能力。而CMCS作为一种带负电的链状结构,因同时具有—NH2 和—COOH,使其有着极佳的生物相容性和水溶性,可以通过氢键相互作用和静电相互作用与β-CD结合,相互缠绕形成三维网络结构。负载PE后,PE中的疏水成分(如萜类、脂溶性黄酮)可嵌入CMCS的疏水微区或被其形成的纳米结构包裹还有可能进入β-CD疏水空腔中,形成稳定的共载体系,有效实现对PE的双重包埋。
3 结论与讨论
本研究通过调控CMCS、β-CD和PE之间的添加顺序和质量浓度制备了CMCS/β-CD-PE共载体系,成功实现对PE的包埋。结果表明,当三者的添加顺序为CMCS→β-CD→PE、CMCS和β-CD比例为1∶1以及PE质量浓度为5 g/L时,所形成的CMCS/β-CD-PE共载体系最稳定。这归因于CMCS和β-CD之间交联缠绕形成三维网络,在氢键、疏水相互作用和静电相互作用的共同作用下实现对PE的有效包埋,提高了稳定性。这项研究可以为扩大PE在食品、制药和化妆品领域的应用提供有用的信息,并且可为基于CMCS/β-CD共载体系对其他生物活性物质的包埋提供理论参考。
[1] SANTOS L M, FONSECA M S, SOKOLONSKI A R, et al.Propolis:Types, composition, biological activities, and veterinary product patent prospecting[J].Journal of the Science of Food and Agriculture, 2020, 100(4):1369-1382.
[2] TAVARES L, SMAOUI S, LIMA P S, et al.Propolis:Encapsulation and application in the food and pharmaceutical industries[J].Trends in Food Science &Technology, 2022, 127:169-180.
[3] 彭正菊, 谌迪, 张岑, 等.蜂胶油提物的制备及抗氧化活性研究[J].浙江农业学报, 2024, 36(10):2338-2346.
PENG Z J, CHEN D, ZHANG C, et al.Preparation and antioxidant activity of propolis oil extracts[J].Acta Agriculturae Zhejiangensis, 2024, 36(10):2338-2346.
[4] KASOTE D, BANKOVA V, VILJOEN A M.Propolis:Chemical diversity and challenges in quality control[J].Phytochemistry Reviews, 2022, 21(6):1887-1911.
[5] PANT K, SHARMA A, CHOPRA H K, et al.Impact of biodiversification on propolis composition, functionality, and application in foods as natural preservative:A review[J].Food Control, 2024, 155:110097.
[6] KUBILIENE L, LAUGALIENE V, PAVILONIS A, et al.Alternative preparation of propolis extracts:Comparison of their composition and biological activities[J].BMC Complementary and Alternative Medicine, 2015, 15:156.
[7] OR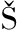 OLI
OLI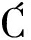 N, BA
N, BA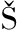 I
I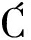 I.Immunomodulation by water-soluble derivative of propolis:A factor of antitumor reactivity[J].Journal of Ethnopharmacology, 2003, 84(2-3):265-273.
I.Immunomodulation by water-soluble derivative of propolis:A factor of antitumor reactivity[J].Journal of Ethnopharmacology, 2003, 84(2-3):265-273.
[8] CARVALHO A A, FINGER D, MACHADO C S, et al.In vivo antitumoural activity and composition of an oil extract of Brazilian propolis[J].Food Chemistry, 2011, 126(3):1239-1245.
[9] DO NASCIMENTO T G, DE ALMEIDA C P, DA CONCEIÇ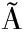 O M M, et al.Caseinates loaded with Brazilian red propolis extract:Preparation, protein-flavonoids interaction, antioxidant and antibacterial activities[J].Journal of Thermal Analysis and Calorimetry, 2022, 147(2):1329-1343.
O M M, et al.Caseinates loaded with Brazilian red propolis extract:Preparation, protein-flavonoids interaction, antioxidant and antibacterial activities[J].Journal of Thermal Analysis and Calorimetry, 2022, 147(2):1329-1343.
[10] POBIEGA K, KRA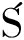 NIEWSKA K, GNIEWOSZ M.Application of propolis in antimicrobial and antioxidative protection of food quality-A review[J].Trends in Food Science &Technology, 2019, 83:53-62.
NIEWSKA K, GNIEWOSZ M.Application of propolis in antimicrobial and antioxidative protection of food quality-A review[J].Trends in Food Science &Technology, 2019, 83:53-62.
[11] 唐宏刚, 肖朝耿, 陈黎洪, 等.高压均质法制备O/W型蜂胶纳米乳液的研究[J].浙江农业学报, 2013, 25(3):619-622.
TANG H G, XIAO C G, CHEN L H, et al.Preparation of propolis oil-in-water nano-emulsion by high-pressure homogenization[J].Acta Agriculturae Zhejiangensis, 2013, 25(3):619-622.
[12] FANG Z X, BHANDARI B.Encapsulation of polyphenols-a review[J].Trends in Food Science &Technology, 2010, 21(10):510-523.
[13] TAVARES L, SANTOS L, ZAPATA NORE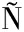 A C P.Bioactive compounds of garlic:A comprehensive review of encapsulation technologies, characterization of the encapsulated garlic compounds and their industrial applicability[J].Trends in Food Science &Technology, 2021, 114:232-244.
A C P.Bioactive compounds of garlic:A comprehensive review of encapsulation technologies, characterization of the encapsulated garlic compounds and their industrial applicability[J].Trends in Food Science &Technology, 2021, 114:232-244.
[14] 郑会娟. 羧甲基壳聚糖包覆的中链脂肪酸纳米脂质体的制备及其性质研究[D].南昌:南昌大学, 2012.
ZHENG H J.Preparation and properties of medium-chain fatty acid nanoliposomes coated with carboxymethyl chitosan[D].Nanchang:Nanchang University, 2012.
[15] 史沛青, 郑艳茹, 陈晖, 等.改性凹凸棒黏土/羧甲基壳聚糖协同稳定桉叶精油Pickering乳液制备及缓释抑菌性能[J].食品科学, 2022, 43(18):47-54.
SHI P Q, ZHENG Y R, CHEN H, et al.Preparation and sustained-release antibacterial activity of eucalyptus leaf essential oil Pickering emulsion stabilized by modified attapulgite nanoparticles and carboxymethyl chitosan[J].Food Science, 2022, 43(18):47-54.
[16] ASTRAY G, GONZALEZ-BARREIRO C, MEJUTO J C, et al.A review on the use of cyclodextrins in foods[J].Food Hydrocolloids, 2009, 23(7):1631-1640.
[17] CATCHPOLE O, MITCHELL K, BLOOR S, et al.Anti-gastrointestinal cancer activity of cyclodextrin-encapsulated propolis[J].Journal of Functional Foods, 2018, 41:1-8.
[18] 钱晓晴, 王立敏, 张文, 等.壳聚糖基Pickering乳液及其在食品中的应用[J].食品科学, 2023, 44(21):386-395.
QIAN X Q, WANG L M, ZHANG W, et al.Advances in chitosan-based Pickering emulsions and their food applications[J].Food Science, 2023, 44(21):386-395.
[19] 李亚娟, 张镭译, 张婷, 等.蛋清肽和姜黄素协同增强多糖基高内相Pickering乳液的界面结构实现活性保护[J].食品科学, 2024, 45(21):20-28.
LI Y J, ZHANG L Y, ZHANG T, et al.Egg white peptide and curcumin synergistically enhance the interfacial structure of polysaccharide-based high internal phase Pickering emulsions, which in turn improve their bioaccessibility[J].Food Science, 2024, 45(21):20-28.
[20] WANG H X, HU L D, PENG L, et al.Dual encapsulation of β-carotene by β-cyclodextrin and chitosan for 3D printing application[J].Food Chemistry, 2022, 378:132088.
[21] LIU R R, WANG X H, YANG L X, et al.Coordinated encapsulation by β-cyclodextrin and chitosan derivatives improves the stability of anthocyanins[J].International Journal of Biological Macromolecules, 2023, 242:125060.
[22] KIM D H, JEONG E W, BAEK Y, et al.Development of propolis extract-loaded nanoparticles with chitosan and hyaluronic acid for improving solubility and stability[J].LWT, 2023, 181:114738.
[23] SHAKOURY N, ALIYARI M A, SALAMI M, et al.Encapsulation of propolis extract in whey protein nanoparticles[J].LWT, 2022, 158:113138.
[24] JIE Y L, CHEN F S, ZHU T W, et al.High internal phase emulsions stabilized solely by carboxymethyl chitosan[J].Food Hydrocolloids, 2022, 127:107554.
[25] EBADI Z, KHODANAZARY A, HOSSEINI S M, et al.The shelf life extension of refrigerated Nemipterus japonicus fillets by chitosan coating incorporated with propolis extract[J].International Journal of Biological Macromolecules, 2019, 139:94-102.
[26] 杨萌. 共载蛋清肽和姜黄素的两亲性自组装递送体系构建及效用评价[D].长春:吉林大学, 2023.
YANG M.Construction and utility evaluation of amphiphilic self-assembly delivery system co-carrying egg white peptide and curcumin[D].Changchun:Jilin University, 2023.
[27] YONG H M, LIU J.Active packaging films and edible coatings based on polyphenol‐rich propolis extract:A review[J].Comprehensive Reviews in Food Science and Food Safety, 2021, 20(2):2106-2145.
[28] CORREA-PACHECO Z N, BAUTISTA-BA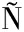 OS S, DE LORENA RAMOS-GARC
OS S, DE LORENA RAMOS-GARC A M, et al.Physicochemical characterization and antimicrobial activity of edible propolis-chitosan nanoparticle films[J].Progress in Organic Coatings, 2019, 137:105326.
A M, et al.Physicochemical characterization and antimicrobial activity of edible propolis-chitosan nanoparticle films[J].Progress in Organic Coatings, 2019, 137:105326.
[29] ZHANG Q Y, YANG A, TAN W H, et al.Development, physicochemical properties, and antibacterial activity of propolis microcapsules[J].Foods, 2023, 12(17):3191.
[30] LI X Q, FAN L P, LI J W.Extrusion-based 3D printing of high internal phase emulsions stabilized by co-assembled β-cyclodextrin and chitosan[J].Food Hydrocolloids, 2023, 134:108036.
[31] PANT K, THAKUR M, CHOPRA H K, et al.Encapsulated bee propolis powder:Drying process optimization and physicochemical characterization[J].LWT, 2022, 155:112956.
[32] DE OLIVEIRA CARDOSO E, CONTI B J, SANTIAGO K B, et al.Phenolic compounds alone or in combination may be involved in propolis effects on human monocytes[J].The Journal of Pharmacy and Pharmacology, 2017, 69(1):99-108.
[33] TAVARES L, SANTOS L, NORE A C P Z.Microencapsulation of organosulfur compounds from garlic oil using β-cyclodextrin and complex of soy protein isolate and chitosan as wall materials:A comparative study[J].Powder Technology, 2021, 390:103-111.
A C P Z.Microencapsulation of organosulfur compounds from garlic oil using β-cyclodextrin and complex of soy protein isolate and chitosan as wall materials:A comparative study[J].Powder Technology, 2021, 390:103-111.
[34] GAMAL MOHAMED M, MENG T S, KUO S W.Intrinsic water-soluble benzoxazine-functionalized cyclodextrin and its formation of inclusion complex with polymer[J].Polymer, 2021, 226:123827.