山桐子(Idesia polycarpa Maxim.)是落叶乔木,属于大风子科山桐子属,又被称为山梧桐、水冬瓜、油葡萄和树上油库[1]等,在中国多分布在秦岭和淮河以南等地,以其高含油量和高脂质含量而闻名。山桐子粕是山桐子油脂提取后的副产物,富含蛋白质(12.92%)、粗纤维(27.16%)和铁(503.24 mg/kg)等多种营养成分[2];同时山桐子中总糖含量约为12.53%~15.49%[3]。目前已有从山桐子粕中提取蛋白质和多糖的研究。例如,杨文清等[4]优化了碱溶酸沉提取山桐子粕蛋白质的工艺,并证明其具有优良的抗氧化活性;此外,将山桐子粕蛋白质应用于可食用薄膜和水果涂层的制备,发现蛋白质浓度与薄膜抗拉强度和断裂伸长率呈正相关,且蛋白质涂层能有效延缓甜樱桃果实的衰老。同时,使用复合蛋白酶对山桐子粕蛋白质进行酶消化,并采用超滤和葡萄糖凝胶色谱从蛋白质水解物中分离出具有抗氧化活性的肽[5]。ZHANG等[6]发现与微波干燥、红外干燥和热风干燥相比,采用微波真空干燥制备的山桐子粕多糖具有较高的糖醛酸含量和独特的三螺旋结构,增强了多糖的抗氧化活性和α-糖苷酶抑制力,且能有效延缓糖化反应。此外,SHI等[7]采用超声波结合三相分区同步提取山桐子粕中的蛋白质、多糖和脂质,此方法蛋白质提取率为5.03%,多糖提取率为10.03%,经组分分析发现,提取的蛋白质富含谷氨酸、天冬氨酸和丝氨酸;多糖组分则以RG-I果胶为主,对α-葡萄糖苷酶和糖化反应表现出较强的热稳定性和抑制作用。
在食品加工领域,已被证实与单独蛋白质或多糖相比,使用蛋白质-多糖非共价复合物表现出更强的性能。例如,由乳铁蛋白和阿拉伯树胶形成的静电复合物较单独乳铁蛋白和阿拉伯树胶具有更高的界面吸附和乳化能力[8]。此外,将海藻酸钠引入大豆分离蛋白体系后,蛋白质的结构更加松散且稳定,从而显著提升了乳化、发泡和抗氧化性能[9]。ZHANG等[10]基于非共价相互作用制备了大豆分离蛋白-κ卡拉胶复合凝胶,发现与κ-卡拉胶水凝胶相比,大豆分离蛋白的加入不仅能够加快复合凝胶的形成,使其结构更加坚韧致密,而且具有一定的缓释性能。
现有研究多聚焦于蛋白质和多糖的单独提取,其中碱提法是蛋白质和多糖提取中常用的方法。考虑到植物细胞壁对有效成分溶出的阻碍作用,由此本研究采用纤维素酶辅助碱提的方式,得到山桐子粕蛋白质-多糖复合物,并探究纤维素酶添加量对其理化与功能特性的影响,旨在为山桐子粕中营养成分的提取与利用提供理论参考和数据支持。
1 材料与方法
1.1 材料与试剂
山桐子粕(蛋白质8.41%、不溶性膳食纤维36.58%、脂肪10.51%),国家林业草原山桐子加工与综合利用工程技术研究中心;纤维素酶(来源于李氏木霉、酶活力400 U/mg,最适pH 4.80,最适温度50 ℃),上海源叶生物科技有限公司;大豆油,中国粮油食品有限公司;8-苯胺基-1-萘磺酸(8-anilino-1-naphthalenesulfonic acid,ANS)、3,5-二硝基水杨酸(3,5-dinitrosalicylic acid,DNS)、十二烷基硫酸钠(sodium dodecyl sulfate,SDS),德国Sigma公司;其他化学试剂均为分析纯。
1.2 仪器与设备
H1750R高速冷冻离心机,湖南湘仪离心机仪器有限公司;T18型高速分散机,德国IKA公司;F-7100荧光分光光度计,日本日立公司;LGJ-18真空冷冻干燥机,北京松源华兴科技发展有限公司;纳米粒度及Zeta电位分析仪,马尔文帕纳科技有限公司;QM-3SP2型行星式球磨机,南京南大仪器有限公司。
1.3 实验方法
1.3.1 脱脂、超微粉碎山桐子粕的制备
高温压榨山桐子粕,经初步粉碎、过60目筛后,利用石油醚浸提2 h,重复2次,自然干燥得到脱脂山桐子粕,将脱脂粕和研磨球(不锈钢球,直径为6 mm),按照料球比1∶8(质量比),放入行星式齿轮球磨机进行研磨,总体积不超过研磨罐体积的2/3,设置频率40 Hz,6 h研磨后,制得脱脂、超微粉碎山桐子粕。
1.3.2 山桐子粕蛋白质-多糖复合物的共提取制备
称取一定量经脱脂、超微粉碎6 h后的山桐子粕,按照山桐子粕与去离子水料液比1∶20(g∶mL)混合,并充分搅拌溶解。用1 mol/L的盐酸调节溶液pH为4.80,分别加入1%、2%、3%、4%和5%(质量分数)的纤维素酶,在50 ℃条件下磁力搅拌酶解50 min,酶解结束后调节pH至中性,在90 ℃温度下加热10 min进行灭酶处理后、取出,将溶液冷却至室温,用2 mol/L的NaOH调节pH至12,在50 ℃温度下磁力搅拌2 h。4 000×g离心20 min,重复2次,收集上清液。上清液经5 000 Da超滤膜进行超滤分离,在超滤过程中,控制压力为0.2 Pa,并加入50倍样本体积的水洗脱出上清液中的盐与小分子等杂质,最后将浓缩液冷冻干燥得蛋白质-多糖复合物。
1.3.3 基本组成成分测定
在样品蛋白质含量测定时,由于纤维素酶添加会引入蛋白质,使用仅添加纤维素酶的实验组,扣除纤维素酶本身对样品蛋白质含量的影响。样品蛋白质含量的测定参照GB 5009.5—2016《食品安全国家标准 食品中蛋白质的测定》燃烧法。
总糖含量的测定参照李宝花[11]的方法,并稍作修改。精确称取干燥至恒重的待测样品,配制成1 mg/mL的待测溶液,各取1 mL于试管中,之后各加入1 mL体积分数为5%的苯酚溶液和5 mL的浓硫酸,振荡摇匀,冷却至室温,在490 nm处测定吸光度。以葡萄糖标准溶液绘制标准曲线(y=9.036 7x-0.017 8,R2=0.997 1)。通过标准曲线计算总糖含量。
灰分含量的测定参照GB 5009.4—2016《食品安全国家标准 食品中灰分的测定》550 ℃烘烤法。
还原糖含量的测定参照李秀清等[12]的方法,并稍作修改。精确称取干燥至恒重的待测样品,配制成1 mg/mL的待测溶液,将样品稀释至合适的浓度,各取1 mL至试管中,每管分别加入配制好的DNS溶液150 μL、去离子水2.15 mL,混匀。重复3组。将上述试管在沸水中加热反应5 min,自然冷却至室温,在540 nm处测定每管溶液吸光度,以葡萄糖标准液绘制标准曲线(y=7.603 8x-0.013 2,R2=0.999 9)。根据标准曲线计算还原糖含量。
总酚含量测定参照ZHANG等[13]的方法,并稍作修改。准确称量待测样品0.5 g(精确至0.000 1 g),加入去离子水充分溶解制成待测溶液,将待测液稀释至合适的浓度,吸取1 mL待测液于10 mL离心管中,分别加水6 mL后摇匀;再分别加入0.5 mL福林酚试剂,充分摇匀,静置1 min;加入1.5 mL质量分数20%的Na2CO3溶液,用去离子水定容至10.0 mL;避光反应60 min,在765 nm下测定吸光度值,以没食子酸溶液标准液绘制标准曲线(y=119.552 4x+0.001 5,R2=0.998 3)。根据标准曲线计算总酚含量。
总黄酮含量测定参考罗争琴[14]的方法,并稍作修改。准确称量待测样品0.5 g(精确至0.000 1 g),加入去离子水充分溶解制成待测溶液,将待测液稀释至合适的浓度,吸取1 mL黄酮待测液于10 mL离心管中,分别加入2.0、1.8、1.6、1.4、1.2、1.0、0.8、0.6 mL 体积分数为60%的乙醇溶液;再加入0.3 mL质量分数为5%的NaNO2溶液摇匀,放置8 min;加入0.3 mL质量分数为10%的Al(NO3)3溶液,放置6 min;加入4.0 mL质量分数为4%的NaOH溶液,加入体积分数为60%的乙醇溶液定容,摇匀,放置12 min;于510 nm测定吸光度值。以芦丁标准溶液绘制标准曲线(y=11.780 6x+0.001 4,R2=0.999 7)。根据标准曲线计算黄酮含量。
1.3.4 粒径和电位的测定
参考文献[15-16]的方法,并稍作修改。将山桐子粕复合物溶于水中,配成质量浓度为1 mg/mL的复合物溶液,在25 ℃下测定复合物样品的粒径;将山桐子粕复合物粉、用去离子水溶解制成4 mg/mL的溶液测定其电位。
1.3.5 溶解度的测定
根据徐之涵[17]的方法测定,并稍作修改。称取一定量的山桐子粕复合物样品,用去离子水配制成10 mg/mL的溶液,8 000×g离心10 min,取1 mL的上清液加入5 mL的考马斯亮蓝溶液,振荡混匀,避光反应5 min,在595 nm处测量吸光度值,代入标准曲线中计算上清液中的蛋白质含量。溶解度的计算如公式(1)所示:
溶解度![]()
(1)
1.3.6 持水力的测定
参考QIAO等[18]的方法,并稍作修改。分别准确称取0.5 g(精确到0.000 1 g)6组复合物粉末至10 mL干燥洁净离心管中,加入8 mL蒸馏水,在室温下静置4 h,离心(3 000×g、15 min),去除上层液体,用吸水纸将离心管壁附着的多余水分吸干,称量记录离心管和样品湿重。持水力计算如公式(2)所示:
持水力![]()
(2)
式中:m1,山桐子粕复合物粉末的质量,g;m2,干燥离心管的质量,g;m3,离心管与样品湿重的质量,g。
1.3.7 持油力的测定
参考QIAO等[18]的方法,稍作修改。分别准确称取0.5 g(精确到0.000 1 g)6组复合物粉末至10 mL干燥洁净离心管中,加入8 mL大豆油,在室温下静置4 h后,离心(3 000×g、15 min),去除上层液体,用吸油纸将离心管壁附着的多余油渍吸干,称量记录离心管和样品湿重。持油力计算如公式(3)所示:
持油力![]()
(3)
式中:N1,山桐子粕复合物粉末的质量,g;N2,干燥离心管的质量,g;N3,离心管与样品湿重的质量,g。
1.3.8 表面疏水性的测定
参考ZHAN等[19]的方法,使用ANS荧光探针法。根据复合物中的蛋白质含量,用pH=7的PBS缓冲液(0.01 mol/L)将山桐子粕复合物样品配制成不同浓度梯度的蛋白质溶液,取4 mL样品与20 μL 8 mmol/L 的ANS试剂漩涡混匀,避光反应15 min,使用荧光分光光度计测定荧光强度,设置激光波长和发射波长分别为390、470 nm,以蛋白质浓度梯度为横坐标,荧光强度为纵坐标作图,斜率即为表面疏水性指数。
1.3.9 乳化活性(emulsifying activity index,EAI)及乳化稳定性(emulsifying stability index,ESI)的测定
参考ZHANG等[20]的方法,并稍作修改。量取15 mL 10 mg/mL的山桐子粕复合物溶液,加入5 mL的大豆油,使用高速分散机,10 000 r/min均质2 min。均质结束后立即从底部吸取50 μL的初级乳化液,并向其中加入5 mL质量分数为0.1%的SDS溶液。以质量分数为0.1%的SDS溶液为空白对照,使用分光光度计在500 nm处测定吸光度值A0。同样方法测定静置10 min后的吸光度值A10。EAI和ESI计算如公式(4)、公式(5)所示:
(4)
(5)
式中:T,2.303;N,稀释因子,100;φ,油相比例,0.25;c,溶液质量浓度,mg/mL;A0,乳液0 min时测定的吸光度值;A10,乳液10 min时测定的吸光度值。
1.3.10 主成分分析(principal component analysis,PCA)
首先对测定指标数据进行标准化处理,以消除各指标量纲差异的影响。基于特征值>1的原则筛选主成分,采用方差最大化正交旋转方法计算主成分载荷矩阵。接着计算各主成分的特征值、方差贡献率及累计方差贡献率,以及函数表达式与特征向量。以各主成分的方差贡献率作为权重系数,建立主成分综合评价函数模型。根据特征向量中载荷较高的指标确定主成分的生物学意义,通过综合评价模型计算各样品的主成分综合得分并进行排序,分析不同处理组样品间的相关性。
1.4 数据处理
每组实验至少重复3次,结果均表示为“平均值±标准差”(n=3),使用SPSS 22.0数据软件进行ANOVA显著性分析;通过Duncan的多重范围考察各平均值间差异是否显著;使用Origin 2021软件进行绘图。
2 结果与分析
2.1 基本组成成分分析
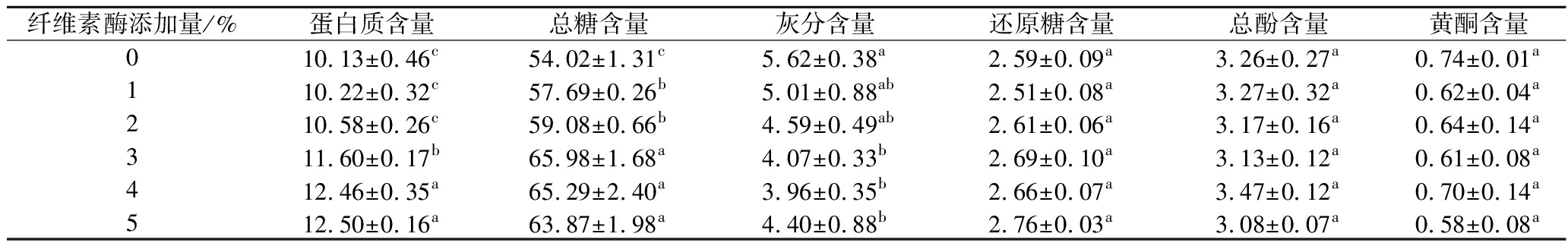
由表1可知,总糖为复合物中的主要成分,其含量在54.02%~65.98%;其次是蛋白质,含量为10.13%~12.50%;灰分含量居第3位,为3.96%~5.62%。与对照组(纤维素酶添加量为0%)相比,随着纤维素酶添加量的增加,复合物中蛋白质和多糖(即总糖)含量呈上升趋势。一方面,纤维素酶可破坏植物细胞壁结构,使细胞内的蛋白质与多糖成分更易溶出;另一方面,酶解作用可能分解与复合物紧密结合的其他杂质成分,释放原本呈结合状态的蛋白质或多糖。随着酶量的进一步增加,即当添加量>3%时,蛋白质和多糖含量变化趋势趋于稳定,表明此时大部分蛋白质和多糖成分已被充分释放。此外,本研究发现,纤维素酶添加量对复合物中还原糖、总酚和黄酮的含量并未产生显著影响(P>0.05)。
表1 蛋白质-多糖复合物的基本组成成分 单位:%
Table 1 Basic components of protein-polysaccharide complexes
纤维素酶添加量/%蛋白质含量总糖含量灰分含量还原糖含量总酚含量黄酮含量010.13±0.46c54.02±1.31c5.62±0.38a2.59±0.09a3.26±0.27a0.74±0.01a110.22±0.32c57.69±0.26b5.01±0.88ab2.51±0.08a3.27±0.32a0.62±0.04a210.58±0.26c59.08±0.66b4.59±0.49ab2.61±0.06a3.17±0.16a0.64±0.14a311.60±0.17b65.98±1.68a4.07±0.33b2.69±0.10a3.13±0.12a0.61±0.08a412.46±0.35a65.29±2.40a3.96±0.35b2.66±0.07a3.47±0.12a0.70±0.14a512.50±0.16a63.87±1.98a4.40±0.88b2.76±0.03a3.08±0.07a0.58±0.08a
注:每列不同小写字母表示有显著差异(P<0.05)。
2.2 粒径
粒径可以初步反映复合物的稳定性。由图1可知,经纤维素酶辅助提取后的蛋白质-多糖复合物粒径显著减小(P<0.05)。当纤维素酶添加量由0%增加至3%时,复合物的粒径逐渐降低,其中酶添加量为3%时粒径最小,较对照组降低了66.85%(P<0.05)。这可能是由于纤维素酶对大分子多糖的水解作用,即酶解反应可将多糖分解为小分子单糖[21],减少了其在蛋白质表面的吸附聚集,从而降低了复合物平均粒径。在ZHAO等[22]研究海藻酸钠和肌原纤维蛋白相互作用时也发现了类似的现象,可能是因为多糖含量的增加使黏度增加,会产生空间位阻效应,抑制大分子聚集形成,进而减小粒径[23]。然而,当纤维素酶添加量继续增至4%时,复合物的平均粒径略有增大(P<0.05),这可能是由于提取的复合物中蛋白质浓度显著增加,过高的蛋白质浓度阻碍了多糖完全吸附到蛋白质颗粒的表面,形成桥接絮凝现象,削弱了蛋白质和多糖之间的静电相互作用,促进了颗粒的聚集,因此粒径增大[24]。XU等[25]研究发现,随着玉米醇溶蛋白浓度的增加,玉米醇溶蛋白和果胶复合物的粒径也增大。
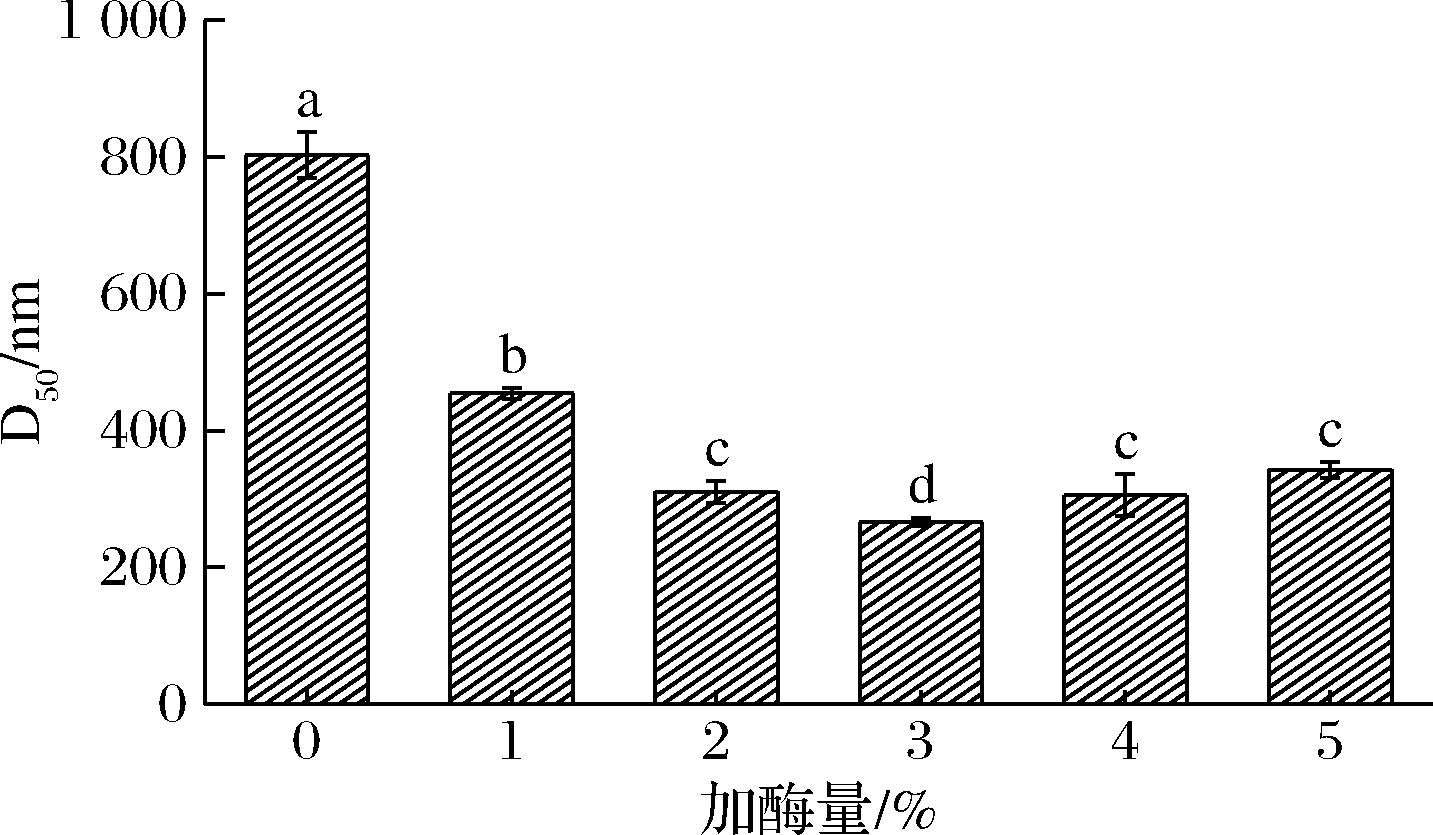
图1 纤维素酶添加量对蛋白质-多糖复合物粒径的影响
Fig.1 Effect of cellulase addition on the particle size of protein-polysaccharide complexes
注:不同小写字母表示有显著差异(P<0.05)(下同)。
2.3 电位
电位代表分散体系中带电粒子的表面电荷密度,用来表示溶液的稳定性,在复合物的研究中还可通过该指标研究粒子电荷对蛋白质-多糖相互作用的影响[26]。如图2所示,经纤维素酶辅助提取后的蛋白质-多糖复合物电位绝对值显著增加(P<0.05),说明纤维素酶辅助提取制得的山桐子粕蛋白质-多糖复合物具有更高的稳定性。当纤维素酶添加量由0%增加至3%时,复合物的电位绝对值逐渐升高,其中3%添加量的电位绝对值最大,较对照组增加约31.72%(P<0.05),这可能是由于复合物中蛋白质和多糖含量的增加会引入更多的负电荷,导致复合物表面的负电荷量增加,与蛋白质颗粒之间的静电斥力增加[25],阻碍了颗粒聚集,复合物溶液更为稳定。ZHANG等[27]发现随着结冷胶浓度的增加,结冷胶与酪蛋白复合物的电位绝对值也增加。随着加酶量由3%增加至5%,复合物的电位绝对值呈减小趋势,这可能是由于提取的复合物中蛋白质浓度显著增加(P<0.05),过高的蛋白质浓度会使生物分子之间产生强大的电荷屏蔽效应[28],导致整体电荷密度降低,因此电位绝对值减小。
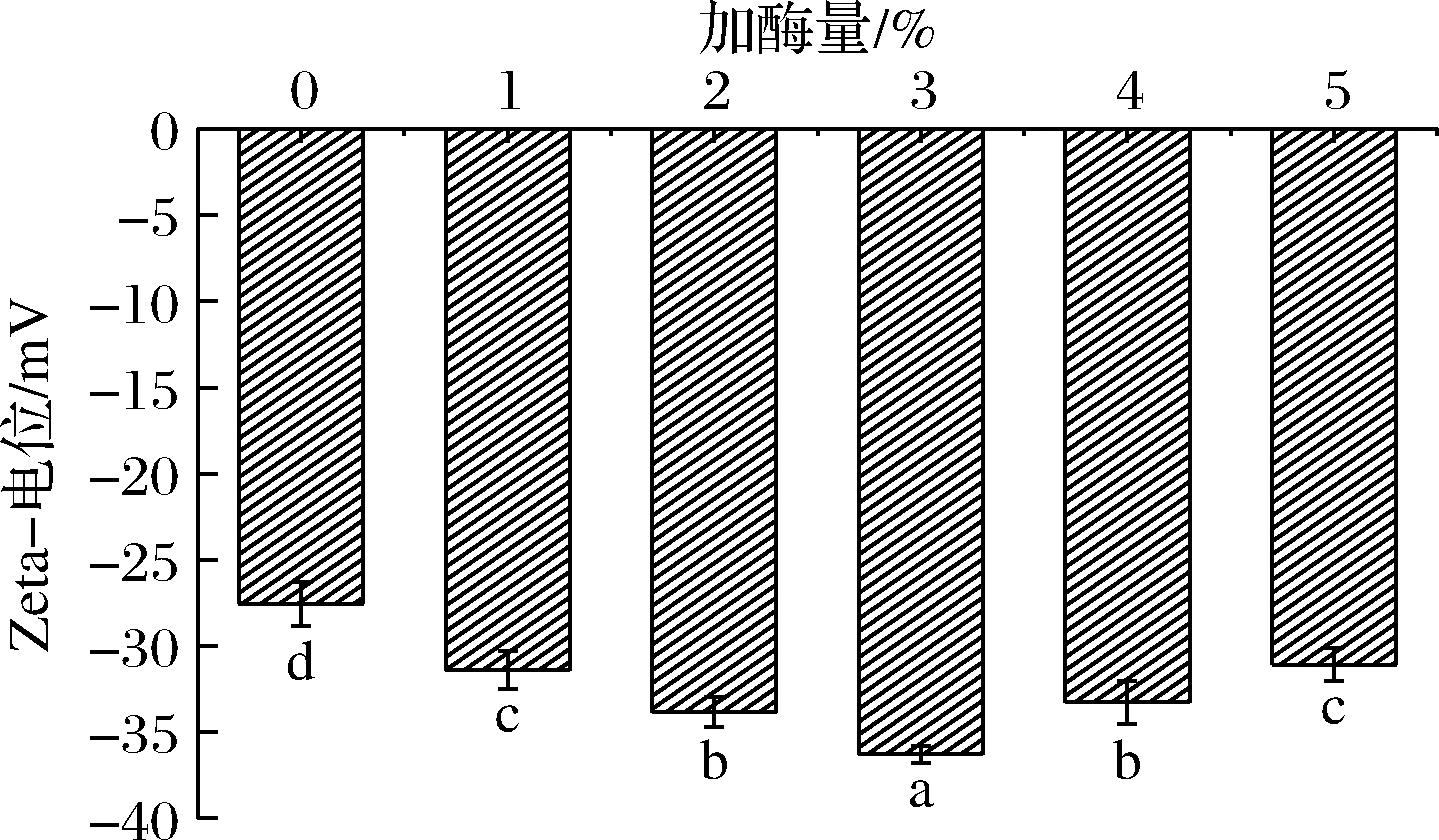
图2 纤维素酶添加量对蛋白质-多糖复合物电位的影响
Fig.2 Effect of cellulase addition on the potential of protein-polysaccharide complexes
2.4 持水力
如图3所示,加入纤维素酶后得到的蛋白质-多糖复合物的持水力整体呈现显著增加的趋势(P<0.05)。当纤维素酶添加量增加至3%时,复合物的持水力最大,较对照组提升了74.70%。持水力改善可能是由于羟基的强大活性以及多糖的亲水性[29],纤维素酶催化降解纤维素后释放出的多糖链段中,大量羟基基团展现出强大的活性,其作为极性官能团能够通过氢键与水分子形成高强度的结合网络,从而显著提升体系对水分的束缚能力。朱常月[30]在酪蛋白和壳聚糖复合物中也发现类似现象,即多糖的存在会显著增加蛋白质的持水力。
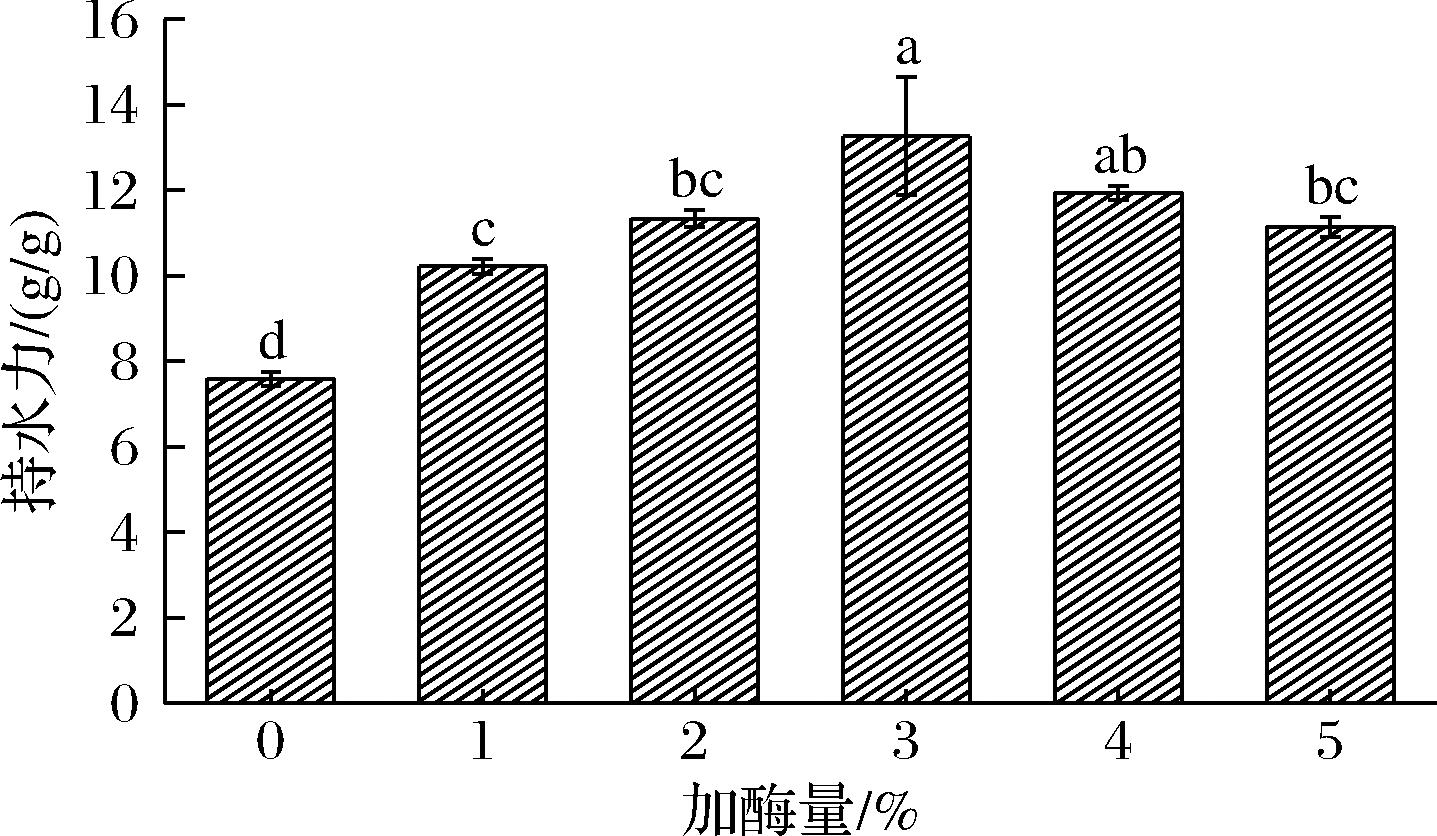
图3 纤维素酶添加量对蛋白质-多糖复合物持水力的影响
Fig.3 Effect of cellulase addition on water-holding capacity of protein-polysaccharide complexes
2.5 持油力
如图4所示,加入纤维素酶后得到的蛋白质-多糖复合物的持油力整体呈显著增加趋势(P<0.05)。当纤维素酶添加量由0%增加至3%时,复合物的持油力逐渐升高,3%时最大,较对照组提升了53.91%。较小的粒径和更均匀的分散性可能导致与油的接触面积增大,从而获得优异的持油力[31]。GAO等[32]也发现具有较小粒径的多糖会与油有更大的接触面积,并增强物理捕捉能力,使持油力增大。
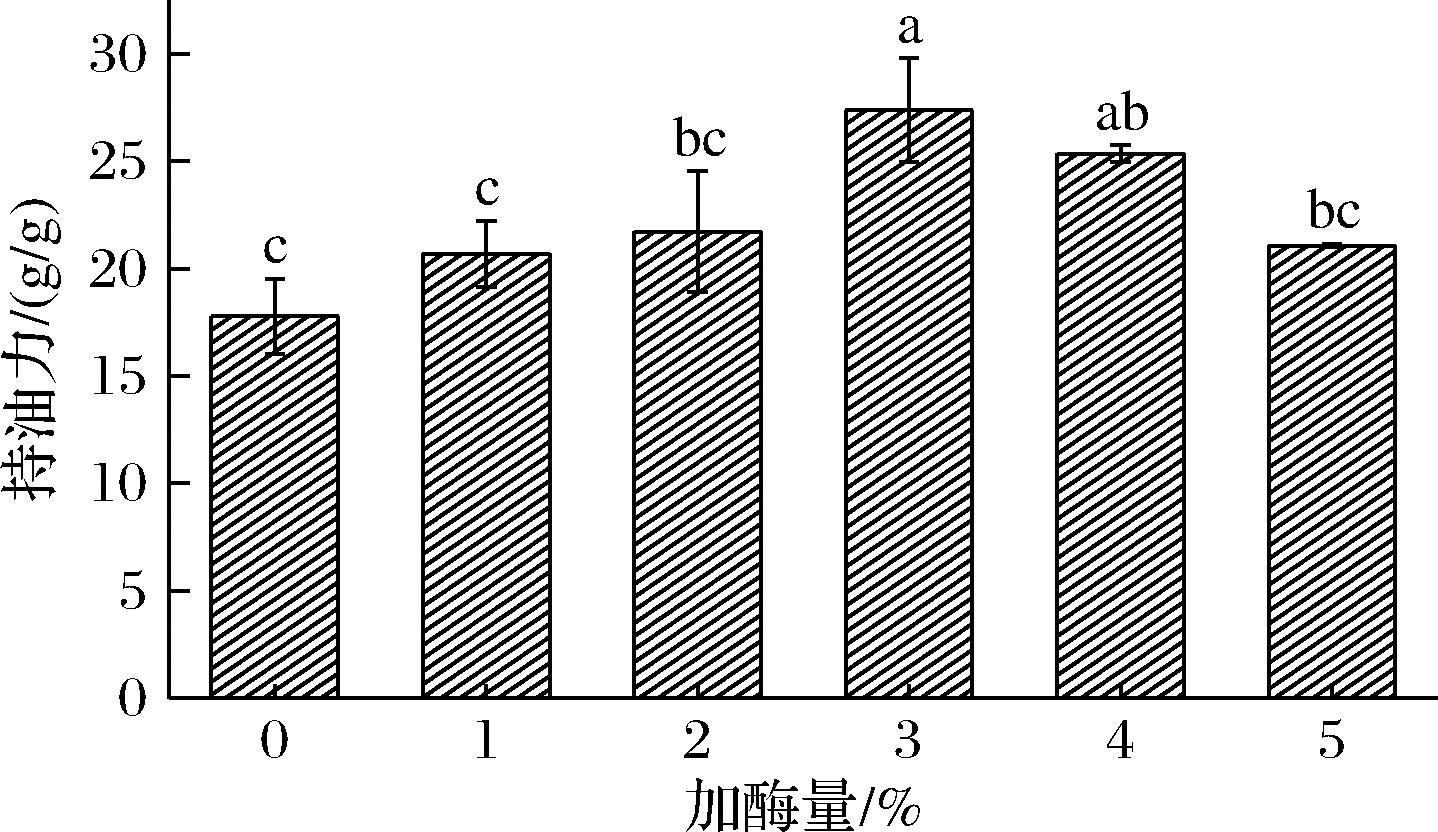
图4 纤维素酶添加量对蛋白质-多糖复合物持油力的影响
Fig.4 Effect of cellulase addition on oil-holding capacity of protein-polysaccharide complexes
2.6 表面疏水性
表面疏水性可用于表征蛋白质的空间构象和蛋白质分子表面疏水基团的相对含量,尤其是疏水残基的暴露程度[33],与蛋白质的溶解度和乳化性能等密切相关。由图5可知,与未添加纤维素酶空白组相比,添加不同剂量纤维素酶会使复合物的表面疏水性呈现先下降后升高的趋势(P<0.05),在纤维素酶添加量为3%时,表面疏水性达到最小值,多糖含量最高,此时复合物的亲水性最强(图3),亲水基团增多会掩盖蛋白质的疏水基团,从而使表面疏水性降低[34]。FANG等[35]研究发现,添加卡拉胶会使大豆分离蛋白的表面疏水性降低。
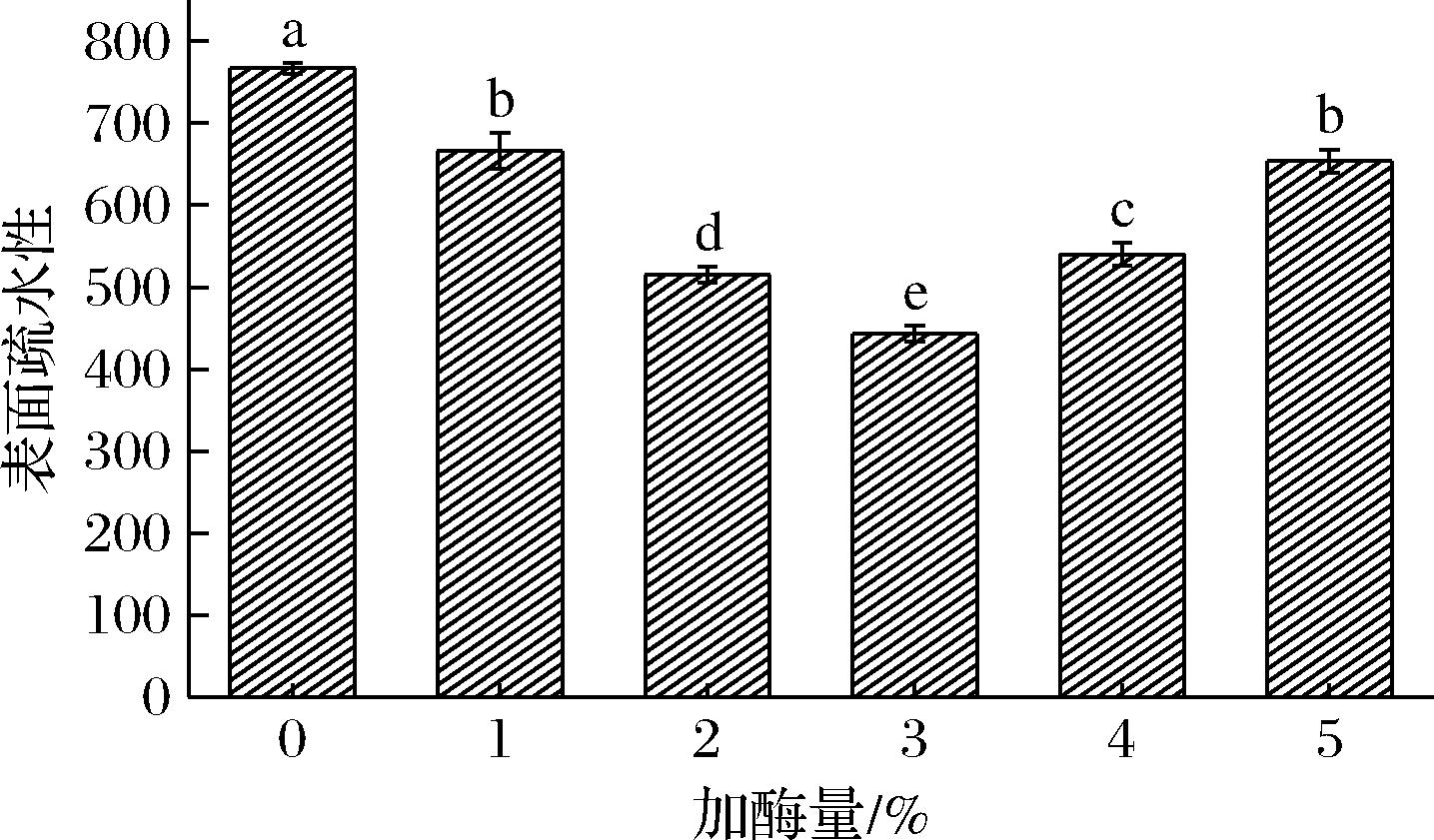
图5 纤维素酶添加量对蛋白质-多糖复合物表面疏水性的影响
Fig.5 Effect of cellulase addition on the surface hydrophobicity of protein-polysaccharide complexes
2.7 溶解度
如图6所示,加入纤维素酶后得到的蛋白质-多糖复合物的溶解度整体呈显著增加趋势(P<0.05)。与WANG等[36]的报道一致,即甜茶多糖添加量的增加会显著改善甜茶多糖和乳清分离蛋白复合体系的溶解度。本研究中,当纤维素酶添加量为3%时,溶解度最强,较对照组提升了36.22%。这是因为纤维素酶添加量为3%时复合物的亲水性最强(图3),具有最多的亲水基团,所以溶解度最大。但随着添加量继续增加至4%,其溶解度呈下降趋势,主要是因为亲水基团减少。
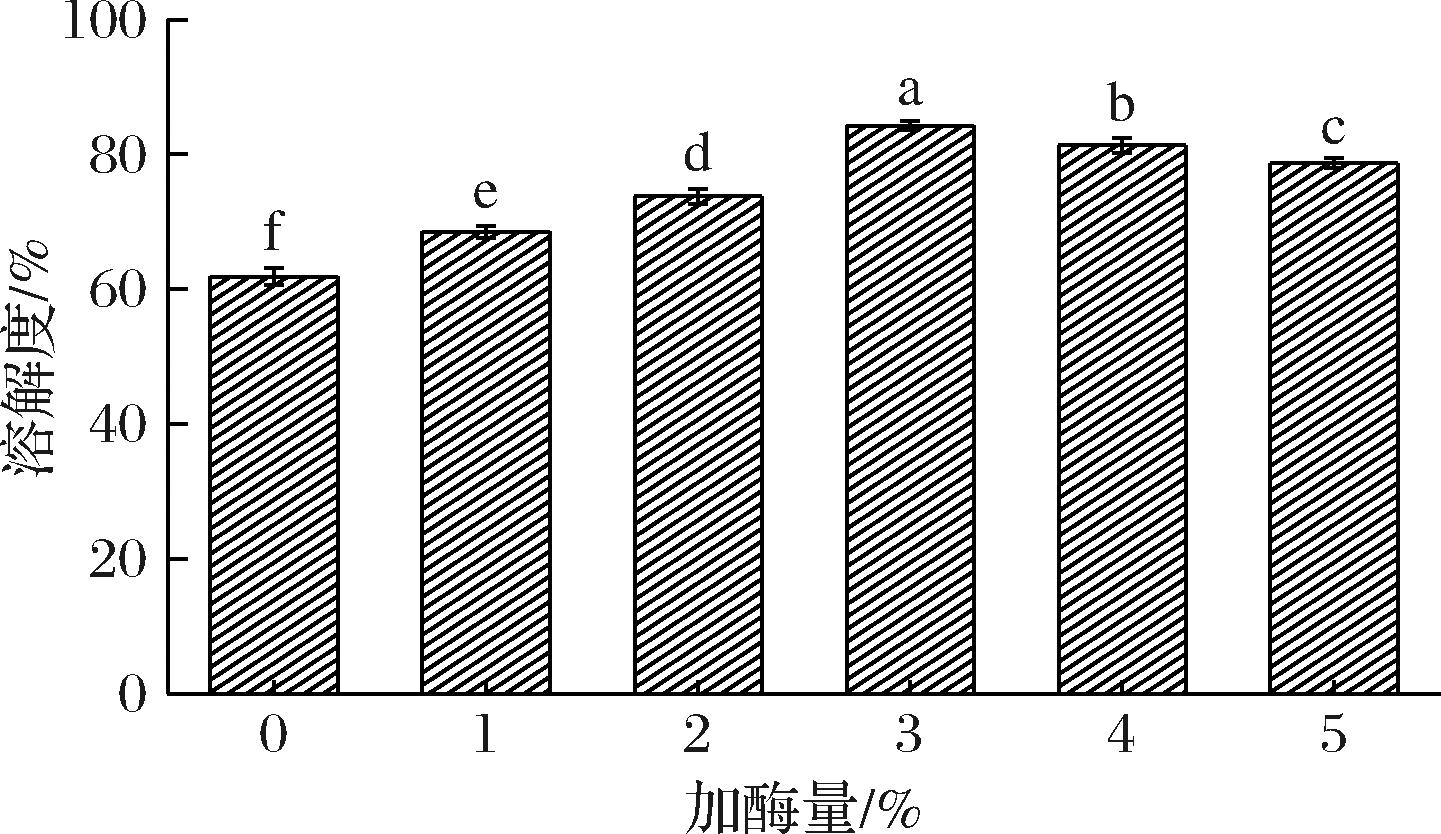
图6 纤维素酶添加量对蛋白质-多糖复合物溶解度的影响
Fig.6 Effect of cellulase addition on the solubility of protein-polysaccharide complexes
2.8 乳化特性
EAI是指蛋白质和多糖在油水界面吸附形成乳化层的能力,ESI形容液滴在乳液中的稳定性,多糖和蛋白质等生物大分子的乳化特性主要取决于其亲水性、表面疏水性和分子大小等[37]。
由图7-a可知,与未添加纤维素酶制得的复合物相比,加入纤维素酶后得到的蛋白质-多糖复合物的EAI呈现先升高后降低的趋势(P<0.05),且在3%添加量时EAI最高,较对照组增加了7.32%。这可能是由于随着纤维素酶添加量增加至3%,复合物的粒径逐渐减小(图1),且在3%时粒径最小,拥有更大的比表面积,有利于复合物在油-水界面快速吸附[38],表现出EAI提高。而随着纤维素酶添加量增加至4%,EAI显著降低,是由于此条件下复合物粒径增大(图1),与油-水界面吸附面积减小。

a-EAI;b-ESI
图7 纤维素酶添加量对蛋白质-多糖复合物乳化特性的影响
Fig.7 Effect of cellulase addition on emulsifying properties of protein-polysaccharide complexes
由图7-b可知,经纤维素酶处理后的蛋白质-多糖复合物的ESI整体呈显著增加趋势(P<0.05),这可能与多糖含量的增加有关,有研究表明多糖可通过静电相互作用吸附在油滴表面,并形成保护层,通过空间位阻效应使液滴碰撞后不易聚集[39],进而提升油滴的稳定性。当纤维素酶添加量由0%增加至3%时,复合物的ESI逐渐升高,3%时最大,较对照组提升了58.00%。这是因为在纤维素酶添加量为3%时,山桐子粕蛋白质-多糖复合物的持油力最强(图4),能更有效地降低油-水界面张力,使油滴更易分散成小颗粒,减少因界面能过高导致的聚结。但随着添加量继续增加至4%,其ESI呈下降趋势,与亲油性下降有关。
2.9 PCA
利用PCA对不同纤维素酶添加量提取得到的山桐子粕蛋白质-多糖复合物的理化性质进行综合评价。如图8所示,PC1和PC2的方差贡献率分别为81.4%和14.3%,累计贡献率为95.7%。具体而言,PC1的相关指标为多糖含量、粒径、电位、持水力、持油力、溶解度和乳化稳定性;PC2的相关指标为蛋白含量和EAI。在PCA的载荷图中,变量间在载荷图上的夹角可以反映变量的潜在相关性,即当夹角为锐角时,说明呈现正相关,且夹角越小,相关性越强;当夹角接近直角时,说明2个变量间几乎没有相关性;当夹角接近180°时,说明2个变量之间存在较强的负相关关系。由图8可知,多糖含量与其他变量间形成的夹角均小于蛋白质含量与其他变量间形成的夹角;此外,多糖含量与PC1的夹角小于蛋白质含量与PC1的夹角,说明多糖含量与PC1的相关性较强。综上所述,与蛋白质含量对复合物的性质影响效果相比,多糖含量的影响效果较大,即蛋白质-多糖复合物中多糖含量对复合物性质的贡献更大。
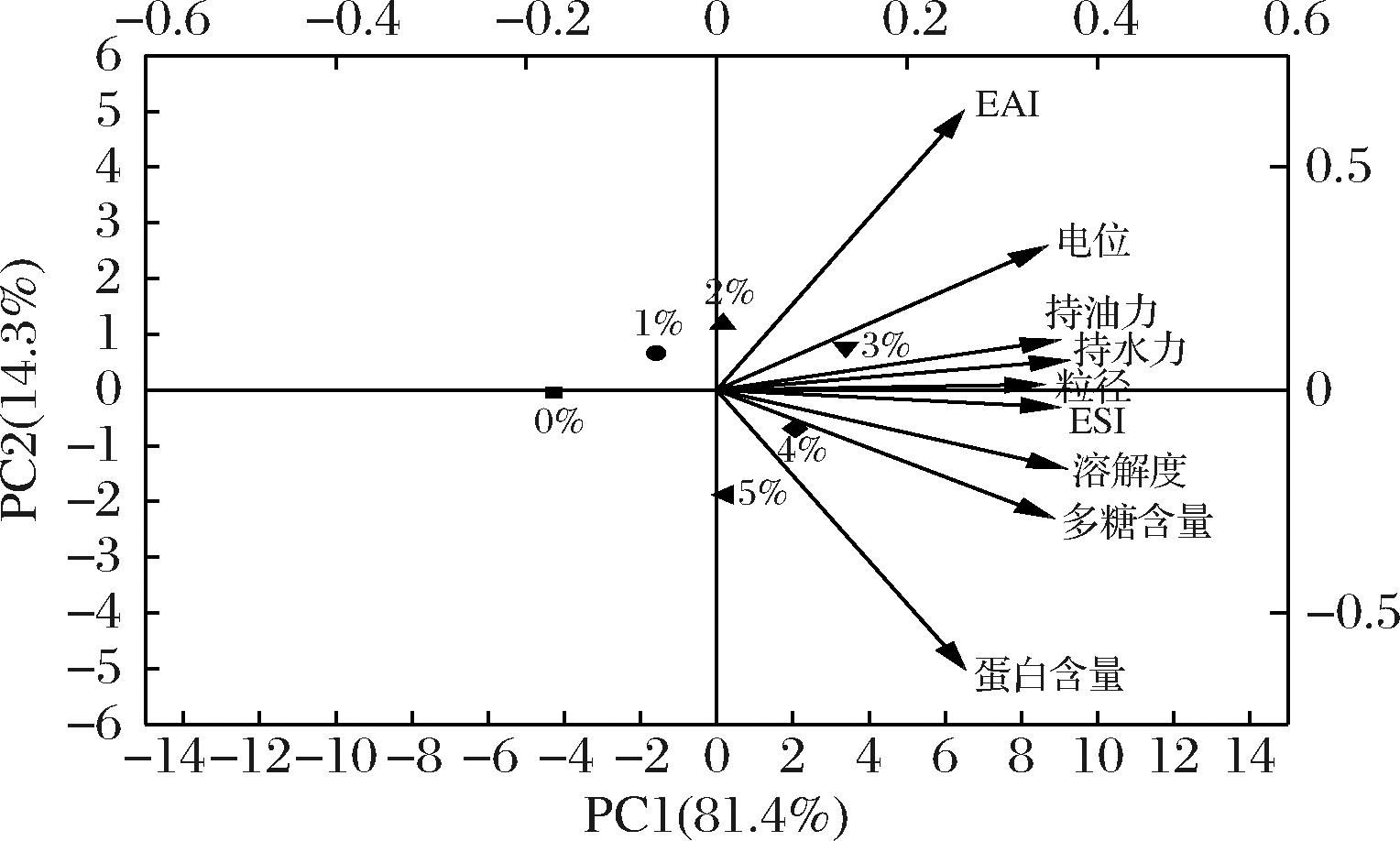
图8 不同纤维素酶添加量提取得到的蛋白质-多糖复合物的PCA
Fig.8 PCA of protein-polysaccharide complexes obtained by extraction with different cellulase additions
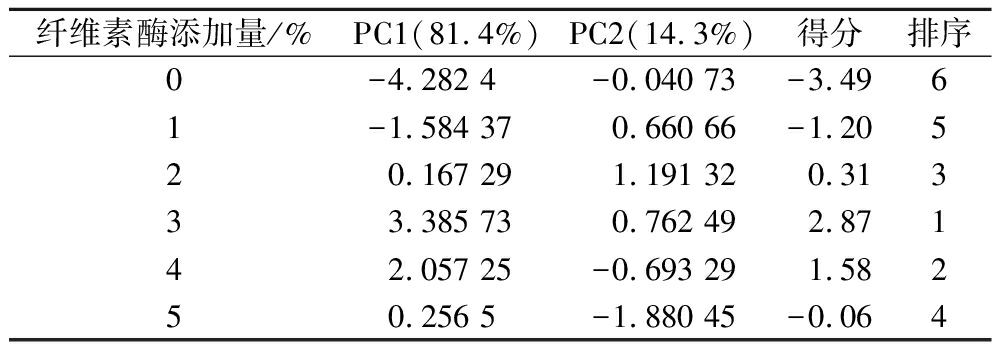
由表2可知,当纤维素酶添加量为3%时,山桐子粕蛋白质-多糖复合物的PCA得分最高,为2.87。这表明当纤维素酶添加量为3%时,提取得到的山桐子粕蛋白质-多糖复合物的理化功能特性最佳。
表2 纤维素酶添加量对蛋白质-多糖复合物PCA得分的影响
Table 2 Effect of cellulase addition on the PCA score of protein-polysaccharide complexes
纤维素酶添加量/%PC1(81.4%)PC2(14.3%)得分排序0-4.282 4 -0.040 73-3.4961-1.584 370.660 66-1.20520.167 291.191 320.31333.385 730.762 492.87142.057 25-0.693 291.58250.256 5-1.880 45-0.064
3 结论
本研究利用纤维素酶辅助碱溶的提取方式从山桐子粕中获得了蛋白质-多糖复合物,并探究了纤维素酶添加量对山桐子粕蛋白质-多糖复合物理化及功能特性的影响。结果表明,与未添加纤维素酶的对照组相比,纤维素酶处理显著提高了复合物中蛋白质和总糖含量(P<0.05),其中总糖含量为54.02%~65.98%,蛋白质含量为10.13%~12.50%。此外,适量纤维素酶处理使蛋白质-多糖复合物的粒径显著减小,电位绝对值增大,这表明纤维素酶辅助提取有助于提升蛋白质-多糖复合物的稳定性。在功能特性方面,随着纤维素酶添加量的增加,蛋白质-多糖复合物的溶解度、持水力、持油力、EAI和ESI均呈现先增加后降低的趋势。PCA显示,当纤维素酶添加量为3%时,山桐子粕蛋白质-多糖复合物显示出最佳的理化与功能特性。综上,纤维素酶辅助提取可有效改善山桐子粕蛋白质-多糖复合物的功能特性,其可作为功能性基料应用于食品工业中,为山桐子粕的高附加值利用提供理论与数据支撑。
[1] RANA S, LIU Z.Study on the pattern of vegetative growth in young dioecious trees of Idesia polycarpa Maxim[J].Trees, 2021, 35(1):69-80.
[2] 杨静, 张娟, 李浪, 等.毛叶山桐子粕的营养价值及重金属元素含量分析[J].动物营养学报, 2020, 32(11):5482-5490.
YANG J, ZHANG J, LI L, et al.Analysis of nutritional value and heavy metal element contents in Idesia polycarpa meal[J].Chinese Journal of Animal Nutrition, 2020, 32(11):5482-5490.
[3] 邹康, 常云鹤, 宋明发, 等.不同产地山桐子果实成分及脂肪酸组成分析与评价[J/OL].中国油脂, 2023.https://link.cnki.net/doi/10.19902/j.cnki.zgyz.1003-7969.230342.
ZOU K, CHANG Y H, SONG M F, et al.Analysis and evaluation of fruit composition and fatty acid composition of Idesia polycarpa Maxim from Different Geographic Regions[J/OL].China Oils and Fats, 2023.https://link.cnki.net/doi/10.19902/j.cnki.zgyz.1003-7969.230342.
[4] 杨文清, 罗凯, 陈耀兵.山桐子蛋白提取工艺优化及功能特性研究[J].中国粮油学报, 2024, 39(3):89-97.
YANG W Q, LUO K, CHEN Y B.Optimization of extraction process and functional properties of Idesia polycarpa Maxim.protein[J].Journal of the Chinese Cereals and Oils Association, 2024, 39(3):89-97.
[5] DOU L, ZHANG Z M, YANG W Q, et al.Separation and purification of antioxidant peptides from Idesia polycarpa Maxim.cake meal and study of conformational relationship between them[J].Food Science &Nutrition, 2024, 12(9):6206-6225.
[6] ZHANG Q Q, HUANG R S, WANG L S, et al.Comparative study on the effects of different drying technologies on the structural characteristics and biological activities of polysaccharides from Idesia polycarpa Maxim cake meal[J].Food Chemistry, 2025, 26:102348.
[7] SHI X, ZHANG Q Q, YANG J T, et al.Simultaneous extraction of oil, protein and polysaccharide from Idesia polycarpa Maxim cake meal using ultrasound combined with three phase partitioning[J].Ultrasonics Sonochemistry, 2024, 110:107043.
[8] CHENG C, WU Z H, WANG Y, et al.Tunable high internal phase emulsions (HIPEs) formulated using lactoferrin-gum Arabic complexes[J].Food Hydrocolloids, 2021, 113:106445.
[9] ZHANG Z F, LI T R, ZHANG Y B, et al.Effect of polysaccharides on conformational changes and functional properties of protein-polyphenol binary complexes:A comparative study[J].International Journal of Biological Macromolecules, 2023, 253:126890.
[10] ZHANG Q, GU L P, SU Y J, et al.Development of soy protein isolate/κ-carrageenan composite hydrogels as a delivery system for hydrophilic compounds:Monascus yellow[J].International Journal of Biological Macromolecules, 2021, 172:281-288.
[11] 李宝花. 黄山石耳多糖的提取纯化及其体外模拟消化的研究[D].南京:南京农业大学, 2020.
LI B H.Study on the extraction,purification and in vitro simulated digestion of polysaccharides from the umbilicaria of Huangshan[D].Nanjing:Nanjing Agricultural University, 2020.
[12] 李秀清, 纪宝玉, 裴莉昕, 等.槐米的红外快速鉴别与总黄酮、总酚酸、还原糖含量测定[J].中国食品添加剂, 2024, 35(8):200-207.
LI X Q, JI B Y, PEI L X, et al.Rapid infrared identification and determination of total flavonoids, total phenolic acids and reducing sugars in Sophora japonica flower buds[J].China Food Additives, 2024, 35(8):200-207.
[13] ZHANG J, WANG Y D, XUE Q W, et al.The effect of ultra-high pretreatment on free, esterified and insoluble-bound phenolics from mango leaves and their antioxidant and cytoprotective activities[J].Food Chemistry, 2022, 368:130864.
[14] 罗争琴. 淡竹叶总黄酮提取工艺优化及抗炎作用研究[D].贵州:贵州大学, 2025.
LUO Z Q.Optimization of the extraction process and anti-inflammatory effects of total flavonoids in Tempranillo leaves[D].Guizhou:Guizhou University, 2025.
[15] CHEN X Y, GUO M Z, SANG Y X, et al.Effect of ball-milling treatment on the structure, physicochemical properties and allergenicity of proteins from oyster (Crassostrea gigas)[J].LWT, 2022, 166:113803.
[16] WU Y, ESKIN N A M, CUI W, et al.Emulsifying properties of water soluble yellow mustard mucilage:A comparative study with gum Arabic and Citrus pectin[J].Food Hydrocolloids, 2015, 47:191-196.
[17] 徐之涵. 糯米蛋白冷冻球磨与酶解联合改性研究[D].安徽:安徽农业大学, 2024.
XU Z H.Study on the combined modification of glutinous rice protein by freezing ball milling and enzymatic hydrolysis[D].Anhui:Anhui Agricultural University, 2024.
[18] QIAO C C, ZENG F K, WU N N, et al.Functional, physicochemical and structural properties of soluble dietary fiber from rice bran with extrusion cooking treatment[J].Food Hydrocolloids, 2021, 121:107057.
[19] ZHAN F C, SHI M Q, WANG Y T, et al.Effect of freeze-drying on interaction and functional properties of pea protein isolate/soy soluble polysaccharides complexes[J].Journal of Molecular Liquids, 2019, 285:658-667.
[20] ZHANG R Y, CORSTENS M, LUO Z S, et al.Effect of pH on the emulsifying performance of protein-polysaccharide complexes[J].Journal of the Science of Food and Agriculture, 2024, 104(12):7649-7655.
[21] 林燕, 张伟, 华鑫怡, 等.纤维素酶水解能力的影响因素及纤维素结构变化研究[J].食品与发酵工业, 2012, 38(4):39-43.
LIN Y, ZHANG W, HUA X Y, et al.Study on the factors affecting enzymatic hydrolysis capability and the structural changes of cellulose[J].Food and Fermentation Industries, 2012, 38(4):39-43.
[22] ZHAO N, ZOU H N, SUN S, et al.The interaction between sodium alginate and myofibrillar proteins:The rheological and emulsifying properties of their mixture[J].International Journal of Biological Macromolecules, 2020, 161:1545-1551.
[23] LANEUVILLE S I, PAQUIN P, TURGEON S L.Effect of preparation conditions on the characteristics of whey protein:Xanthan gum complexes[J].Food Hydrocolloids, 2000, 14(4):305-314.
[24] GUO J H, XU C, NENG X Y, et al.Encapsulation of Lactiplantibacillus plantarum in W/O/W emulsion stabilized with whey protein isolate and konjac glucomannan complex[J].Carbohydrate Polymers, 2025, 361:123661.
[25] XU C, GUO J H, CHANG B Y, et al.Study on encapsulation of Lactobacillus plantarum 23-1 in W/O/W emulsion stabilized by pectin and zein particle complex[J].International Journal of Biological Macromolecules, 2024, 279:135346.
[26] BURKEN O, SOMMER S.Evaluation of protein-polysaccharide interactions through ζ-potential and particle size measurements to assess their functionality in wine[J].Journal of Food Science, 2024, 89(10):6413-6424.
[27] ZHANG C Y, CHU H, GAO L, et al.Encapsulation of Lactiplantibacillus plantarum with casein-gellan gum emulsions to enhance its storage, pasteurization, and gastrointestinal survival[J].Food Chemistry, 2025, 462:140909.
[28] LIANG Z Q, CHU H, HOU Z Q, et al.W/O/W emulsions stabilized with whey protein concentrate and pectin:Effects on storage, pasteurization, and gastrointestinal viability of Lacticaseibacillus rhamnosus[J].International Journal of Biological Macromolecules, 2023, 232:123477.
[29] JIN G G, ZHANG M, WANG X R, et al.Characteristics of exopolysaccharides - egg white protein composite gel and its application in low - fat sausage[J].Food Chemistry, 2025, 26:102290.
[30] 朱常月. 壳聚糖降解物与两种蛋白的酶法糖基化交联及产物性质[D].哈尔滨:东北农业大学, 2016.
ZH C Y.Enzymatic glycosylation and crosslinking of two proteins witn a degraded chitosan and some properties of the products[D].Harbin:Northeast Agricultural University, 2016.
[31] REN M D, HOU Y R, PENG D L, et al.Ultrasonic/compound enzyme extraction, comparative characterisation and biological activity of Lonicera macranthoides polysaccharides[J].Ultrasonics Sonochemistry, 2025, 114:107259.
[32] GAO S, LI W P, YIN M P, et al.A comparative study on physicochemical properties and biological activities of polysaccharides from Coreopsis tinctoria buds obtained by different methods[J].Foods, 2025, 14(7):1168.
[33] LIU M Y, SHAN S, GAO X, et al.The effect of sweet tea polysaccharide on the physicochemical and structural properties of whey protein isolate gels[J].International Journal of Biological Macromolecules, 2023, 240:124344.
[34] BENICHOU A, ASERIN A, LUTZ R, et al.Formation and characterization of amphiphilic conjugates of whey protein isolate (WPI)/xanthan to improve surface activity[J].Food Hydrocolloids, 2007, 21(3):379-391.
[35] FANG Q, XU T H, SU R H, et al.Composite gel based on κ-carrageenan-soybean isolate protein/soy protein fibrils:Focus on structural differences and gel properties[J].International Journal of Biological Macromolecules, 2025, 307:142274.
[36] WANG H L, ZHANG J R, RAO P F, et al.Mechanistic insights into the interaction of Lycium barbarum polysaccharide with whey protein isolate:Functional and structural characterization[J].Food Chemistry, 2025, 463:141080.
[37] TIAN Y, SHENG Y N, WU T, et al.Effects of cavitation jet combined with ultrasound, alkaline hydrogen peroxide and Bacillus subtilis treatment on the properties of dietary fiber[J].Food Bioscience, 2024, 59:103895.
[38] LUO W W, XU H Y, GANTUMUR M A, et al.Ball milling-ultrasound modification of citrus fiber-carrageenan complex for improving functional properties of salted egg white[J].Food Biophysics, 2025, 20(2):66.
[39] FERNANDEZ-AVILA C, TRUJILLO A J.Ultra-High Pressure Homogenization improves oxidative stability and interfacial properties of soy protein isolate-stabilized emulsions[J].Food Chemistry, 2016, 209:104-113.