甘薯[Ipomoea batatas (L.) Lam.]是全球重要粮饲及工业原料作物,在中国栽培超400年,种植面积和产量居世界前列[1-2]。伴随《“健康中国2030”规划纲要》推进,富含多酚、黄酮等功能成分的甘薯成为研究热点[3]。甘薯加工中占块根10%~15%的薯皮常被丢弃,既浪费资源又污染环境[4-5]。甘薯皮多酚含量高于块根内部,含绿原酸等多种活性成分[6-8],开发利用对提升产业附加值意义重大。
多酚类物质提取是甘薯皮功能研究与产业化应用的基础。溶剂萃取、超声波辅助、微波辅助等传统方法已广泛用于甘薯皮多酚提取[9]。如响应面法优化超声波提取可提高得率,超声波-微波协同能缩短时间、提升绿原酸提取效率。但因提取原理与作用机制不同,各方法所得提取物中多酚成分、含量及活性存在显著差异[10-11]。溶剂极性影响溶解,超声波通过机械破碎与空化效应改变细胞通透性,微波依赖热效应加速溶出[12-13]。这些差异干扰提取物质量控制与后续开发,因此系统解析不同提取方法对甘薯皮多酚代谢物谱的影响,是优化工艺、精准开发活性成分的关键。
目前,甘薯皮多酚研究多局限于单一成分定量(如绿原酸、总多酚)或简单生物活性评价(抗氧化、抑菌),缺乏对提取物多元代谢物的全面分析[14]。传统HPLC、GC-MS等检测技术虽可定量特定成分,但难以覆盖复杂体系中的微量及未知代谢物[15-16]。非靶向代谢组学通过LC-MS、核磁共振等技术,能对生物样本小分子代谢物进行系统性无偏分析,已在植物逆境响应、农产品品质评估及中药成分解析等领域广泛应用[17],例如成功解析芍药不同部位的芍药苷、黄酮类等差异代谢物[18]。不过在甘薯研究中,代谢组学虽已用于块根多酚及叶片提取工艺研究,但针对甘薯皮多酚提取方法对代谢物谱影响的研究尚少。值得关注的是,多酚生物活性与其结构多样性及成分协同作用紧密相连,如绿原酸通过细胞膜损伤、酶活性抑制和基因表达调控发挥抑菌作用,总多酚抗氧化能力不仅取决于含量,还与单体组成比例相关[19];且不同提取方法会改变提取物活性成分构成,高温易导致多酚氧化分解,超声波可促进结合态多酚释放[20-21]。因此,单一成分定量或总指标难以全面评价提取效果,可采用非靶向代谢组学技术来剖析提取方法和代谢物谱间的关联。
本研究运用非靶向代谢组学方法开展相关工作,对比水提、超声波辅助醇提和维生素C辅助醇提3种方法提取甘薯皮多酚的效应差异。通过LC-MS检测与多元统计,筛选特征代谢物,剖析不同方法对成分的影响,为工艺优化提供依据,为甘薯皮资源的开发再利用提供理论依据。
1 材料与方法
1.1 材料与试剂
供试材料:新鲜甘薯,安徽省六安市当地超市,选消费者购买量居多的品种。
试剂:甲醇、甲酸(色谱纯);实验用水;其余试剂均为分析纯。
1.2 仪器与设备
AB Triple TOF 6600质谱仪,美国AB SCIEX公司;Agilent 1260 Infinity Ⅱ液相色谱仪,美国安捷伦科技有限公司;HR/T20MM立式高速冷冻离心机,湖南赫西仪器装备有限公司;Scientz-100F真空冷冻干燥,宁波新芝生物科技股份有限公司;MM400研磨仪,德国RETSCH公司。
1.3 实验方法
1.3.1 样品酚类物质提取
新鲜甘薯经清水冲洗后,用削皮刀均匀削取表皮(厚度≤1 mm,避免薯肉混入),切块后于-80 ℃预冷冻24 h。随后转移至真空冷冻干燥机(冷阱温度-50 ℃,真空度≤10 Pa)进行72 h三循环冻干。干燥样品经粉碎机研磨后过100目筛,获得均质粉末,密封保存于干燥器中备用。分别采用水提法、超声波辅助醇提法和维生素C辅助醇提法进行提取同样质量的甘薯皮粉。
水提法参考REN等[22]的方法,稍微修改,按照料液比1∶35(g∶mL)称量甘薯皮粉于蒸馏水中,60 ℃水浴60 min,4 ℃、8 000 r/min离心10 min。抽滤得多酚提取物,备用。
超声波辅助醇提法参考TSVETKOV等[23]的方法,稍作修改,按照料液比1∶15(g∶mL)称量甘薯皮粉于体积分数65%的乙醇中,60 ℃水浴50 min,4 ℃、8 000 r/min离心10 min。抽滤得多酚提取物,备用。
维生素C辅助醇提法参考PODLOUCK 等[24]的方法,稍作修改,按照料液比1∶30(g∶mL)称量甘薯皮粉于蒸馏水中,同时加入60 μL含0.4 mg/mL维生素C的体积分数2%乙醇溶液,60 ℃水浴50 min,4 ℃、8 000 r/min离心10 min。抽滤得多酚提取物,备用。
等[24]的方法,稍作修改,按照料液比1∶30(g∶mL)称量甘薯皮粉于蒸馏水中,同时加入60 μL含0.4 mg/mL维生素C的体积分数2%乙醇溶液,60 ℃水浴50 min,4 ℃、8 000 r/min离心10 min。抽滤得多酚提取物,备用。
1.3.2 LC-MS分析
上述提取样品经真空冷冻干燥63 h后在研磨仪中30 Hz,1.5 min研磨成粉末,精确称取50 mg,加入1 200 μL -20 ℃预冷的体积分数70%甲醇水内标提取液(含250 μg/mL标准品,标准品为体积分数98%的2-氯苯丙氨酸),涡旋6次(每次30 s,间隔30 min),12 000 r/min离心3 min,上清液经0.22 μm滤膜过滤后进样。
色谱分离采用Waters ACQUITY UPLC HSS T3柱(1.8 μm,2.1 mm×100 mm),柱温40 ℃,流速0.40 mL/min,进样量4 μL;流动相A(体积分数0.1%甲酸水)与B(体积分数0.1%甲酸乙腈)梯度洗脱:0 min(95% A),5 min(35% A),6 min(1% A),7.5 min(1% A),7.6 min(95% A),10 min(95% A)。质谱采集采用AB TripleTOF 6600质谱仪,ESI正/负离子模式:正模式(离子化电压5 000 V,源温550 ℃,碰撞能量10 V/30 V),负模式(电压-4 000 V,其余同正模式)。
1.4 数据处理
测试数据借助ProteoWizard工具实现测试数据到mzML格式的转换,完成格式转换后,使用XCMS软件进行峰提取与校正操作(缺失值过滤>50%,KNN/SVR填充校正),通过自建库及公共库(MetDNA)鉴定代谢物(综合评分>0.5,QC~CV<0.5),合并正负模式数据得最终分析结果,依据标准化处理后所提取的相对峰面积,能够得出代谢物的相对定量结果。
在多元统计分析环节,借助代谢组学数据处理软件metaX对原始数据实施转换操作,随后开展主成分分析(principal component analysis,PCA)与正交偏最小二乘法判别分析(orthogonal partial least squares discriminant analysis, OPLS-DA),从而获取代谢物的变量权重值(variable importance in projection,VIP)。单变量分析部分,基于t检验计算各代谢物在2组间的P值,同时算出代谢物在2组间的差异倍数(fold change,FC)值。运用R包Pheatmap绘制聚类热图,在此过程中采用z-score标准化方法对代谢物数据进行归一化处理。火山图通过R包ggplot2绘制,该图能够综合代谢物的VIP值、FC值和P值这3个参数,以筛选出目标代谢物。利用R语言的cor()函数开展差异代谢物之间的相关性分析,借助cor.mtest ()函数进行显著性统计,规定P<0.05为具有统计学显著性。KEGG富集图使用R语言ggplot2包绘制,当代谢途径的P<0.05时,判定该代谢途径呈显著富集状态。
2 结果与分析
2.1 离子色谱图分析
可对不同质控(quality control,QC)样本的质谱检测分析总离子流图(total ion chromatogram,TIC)开展重叠展示分析,以此判断代谢物提取与检测的重复性,如图1所示,所有QC样品的峰面积和保留时间的重叠度均较高,说明仪器稳定性强,实验数据可靠。
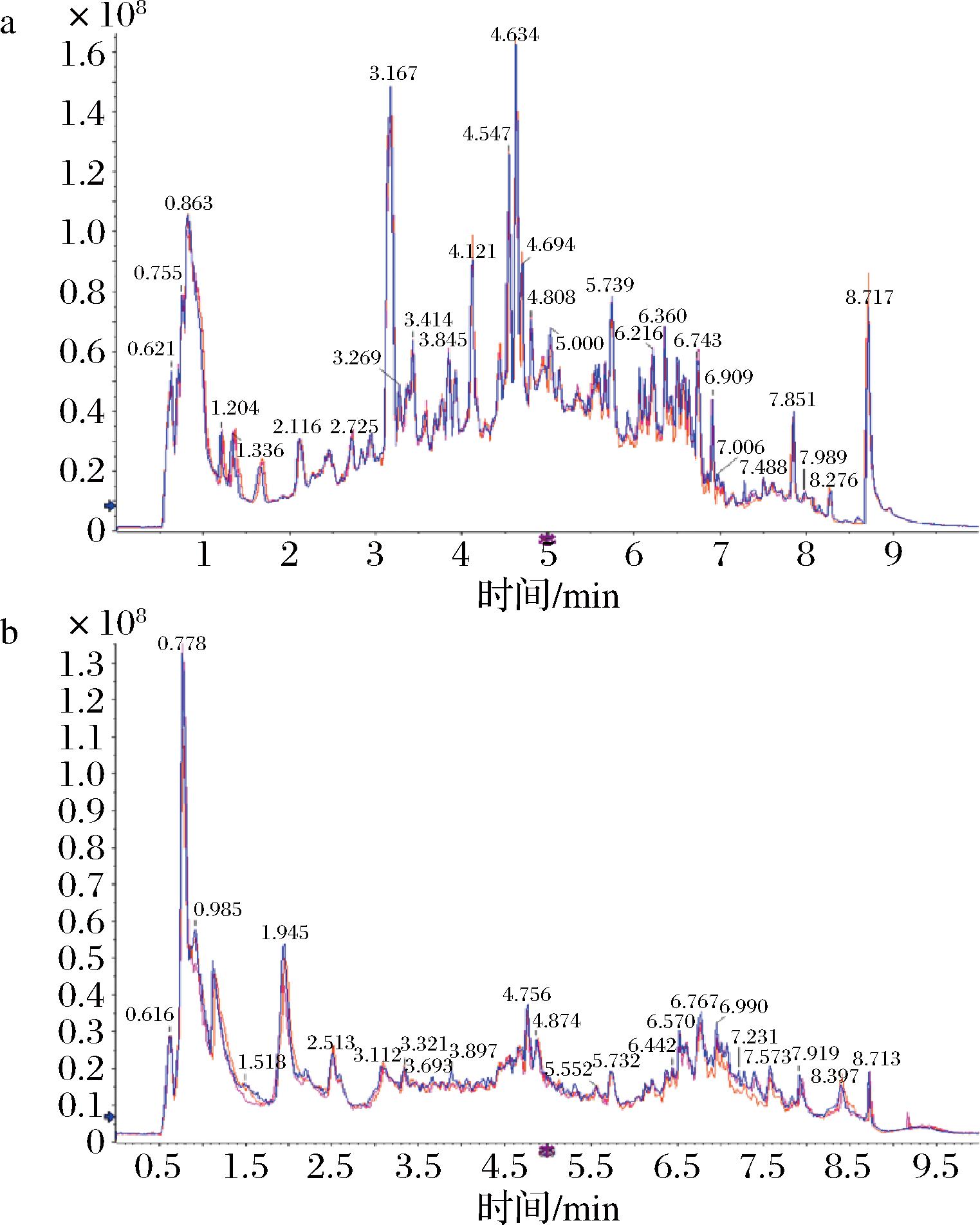
a-正离子模式;b-负离子模式
图1 正、负离子模式下QC 样本的TIC
Fig.1 TIC of QC sample in positive and negative ion mode
2.2 甘薯皮不同提取方法代谢物定量检测
如图2-a所示,在3个样品中都是酚酸类含量最多,其次是黄酮类。整体而言,超声波辅助醇提的样品中,提取出多酚类化合物的总含量是最多的,其中酚酸类占比64.68%。而水提和维生素C辅助醇提的样品,多酚类物质的总量显著低于超声波辅助醇提的样品。但黄酮类的占比明显高于超声波辅助醇提的样品。在超声波辅助醇提样品中类黄酮占28.62%,而在水提和维生素C辅助醇提的样品中,类黄酮占比达37.80%和37.40%。这说明不同的提取方法,得到的化合物存在差异。
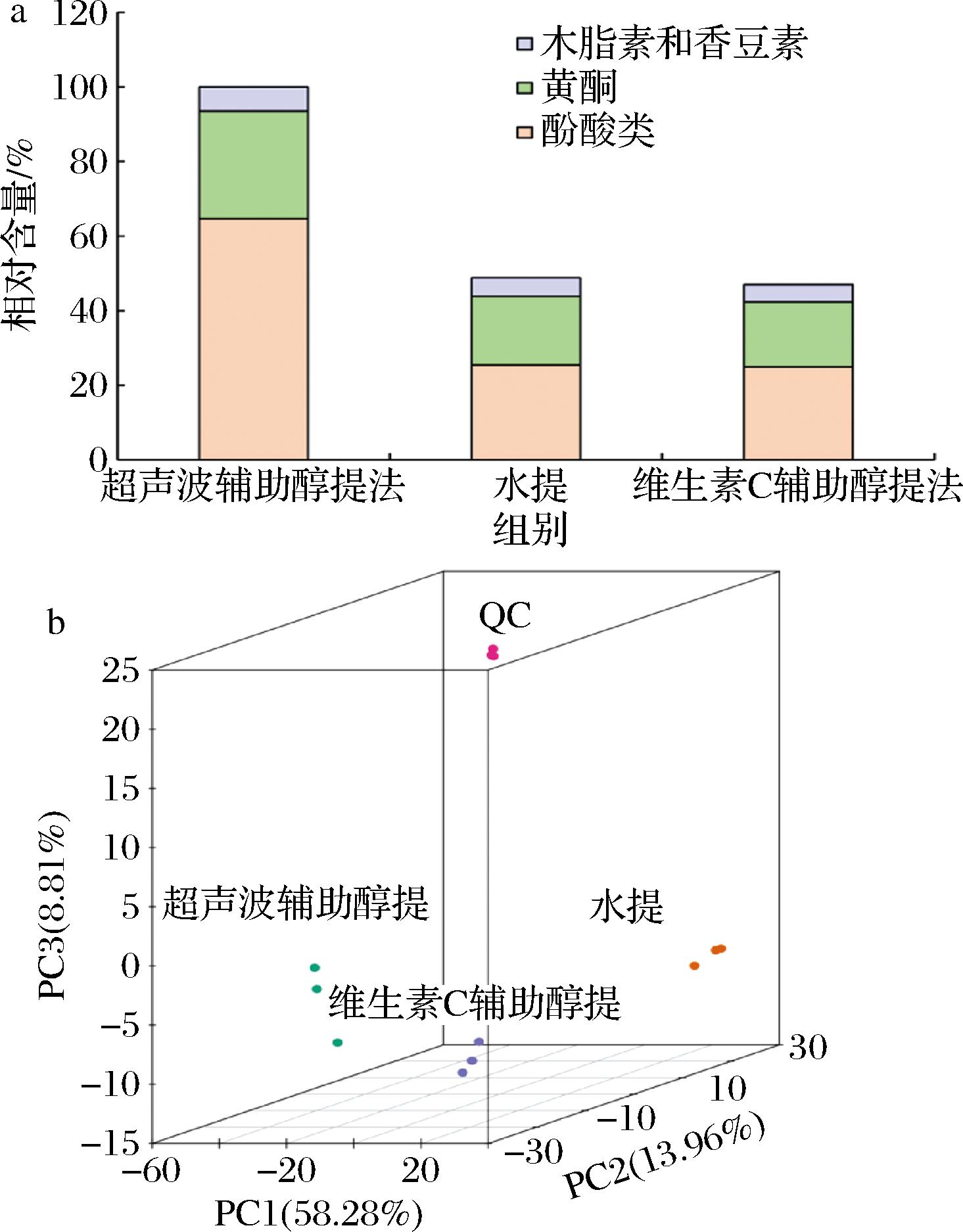
a-代谢物含量分布图;b-PCA三维图
图2 甘薯皮不同提取方法鉴定出的代谢物含量分布图和PCA三维图
Fig.2 Content analysis of metabolite profiles in sweet potato peels using different extraction methods and three dimensional diagram of PCA
为了解样品之间的整体代谢差异以及同一组内样品的变异性,对9个样品进行PCA。如图2-b所示,3组样品在三维主成分空间中分布较为分散,说明样本在PCA所提取的综合变量特征上存在明显差异,可能意味着不同组样本在原始数据的变量特征上有本质区别。水提组样本相对聚集,说明组内样本在这些主成分所反映的特征上具有相似性,稳定性较好;而超声波辅助醇提、维生素C辅助醇提2组组间分散,表明存在较大异质性。
2.3 代谢物功能及分类注释
基于KEGG、HMDB、LIPID MAPS等数据库信息,对鉴定到的代谢物开展功能与分类注释工作,旨在明晰不同代谢物的功能特性及分类状况。在KEGG通路分析图里,经注释的代谢物总数达1 632个。其中,新陈代谢通路涵盖的代谢物数量相对较多,主要注释结果如下:脂质代谢相关代谢物有434个,氨基酸代谢相关代谢物为379个,碳水化合物代谢相关代谢物是179个,辅因子和维生素代谢相关代谢物为177个,核苷酸代谢相关代谢物有109个(图3-a)。在HMDB数据库注释结果中,共涉及1 669个代谢物,主要涵盖以下类别:脂质及类脂质分子(459个)、有机酸及其衍生物(373个)、杂环化合物(180个)、苯环类化合物(168个),以及苯丙素类与聚酮类化合物(148个)(图3-b)。在LIPID MAPS数据库中注释到236个代谢物,其中脂肪酰基类130个,甘油脂类11个,甘油磷脂类76个,聚酮类5个,异戊烯醇脂类1个和鞘脂类12个(图3-c)。
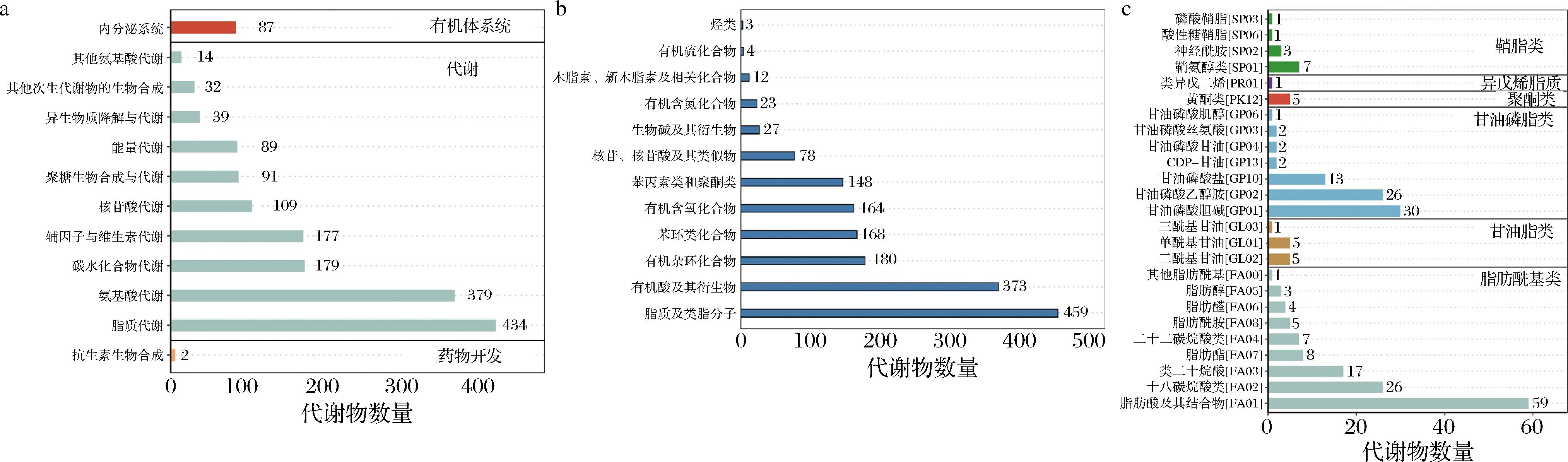
a-KEGG通路分析图;b-HMDB数据库注释分析图;c-LIPID MAPS数据库注释分析图
图3 代谢物功能及分类注释图
Fig.3 Function and classification annotation diagram of metabolites
2.4 差异代谢物筛选和分析
OPLS-DA模型得分图中,以预测主成分为横坐标,从横坐标方向能够观察到组间差异;以正交主成分为纵坐标,从纵坐标方向可了解组内差异;百分比代表着该成分对数据集的解释程度。图中每1个点都代表1个样品,同一组的样品采用相同颜色标识。由得分图4-A1~图4-A3可知,3组样品两两比较均有明显的分离,但水提组样本相对聚集,说明水提组代谢物之间差异较小;而超声波辅助醇提和维生素C辅助醇提2组组间相对分散,表明超声波辅助醇提和维生素C辅助醇提2组代谢物之间差异性较大。
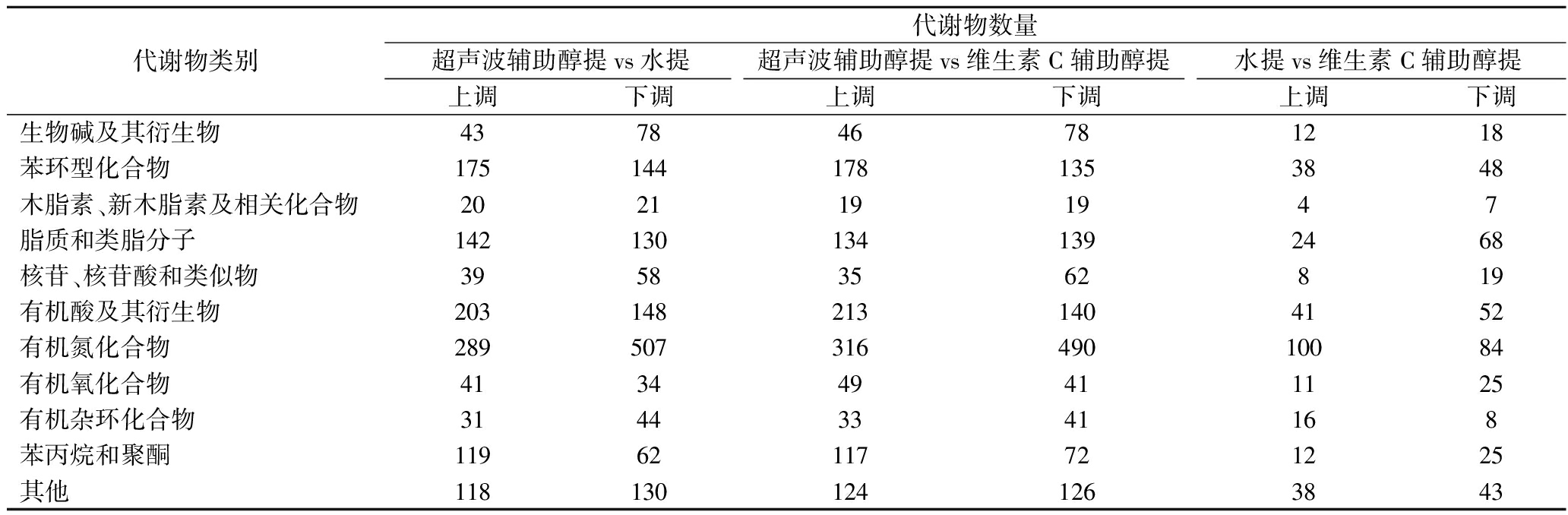
表1 代谢物在各部位差异表达情况
Table 1 Differential expression of metabolites in different parts
代谢物类别代谢物数量超声波辅助醇提vs水提超声波辅助醇提vs维生素C辅助醇提水提vs维生素C辅助醇提上调下调上调下调上调下调生物碱及其衍生物437846781218苯环型化合物1751441781353848木脂素、新木脂素及相关化合物2021191947脂质和类脂分子1421301341392468核苷、核苷酸和类似物39583562819有机酸及其衍生物2031482131404152有机氮化合物28950731649010084有机氧化合物413449411125有机杂环化合物31443341168苯丙烷和聚酮11962117721225其他1181301241263843
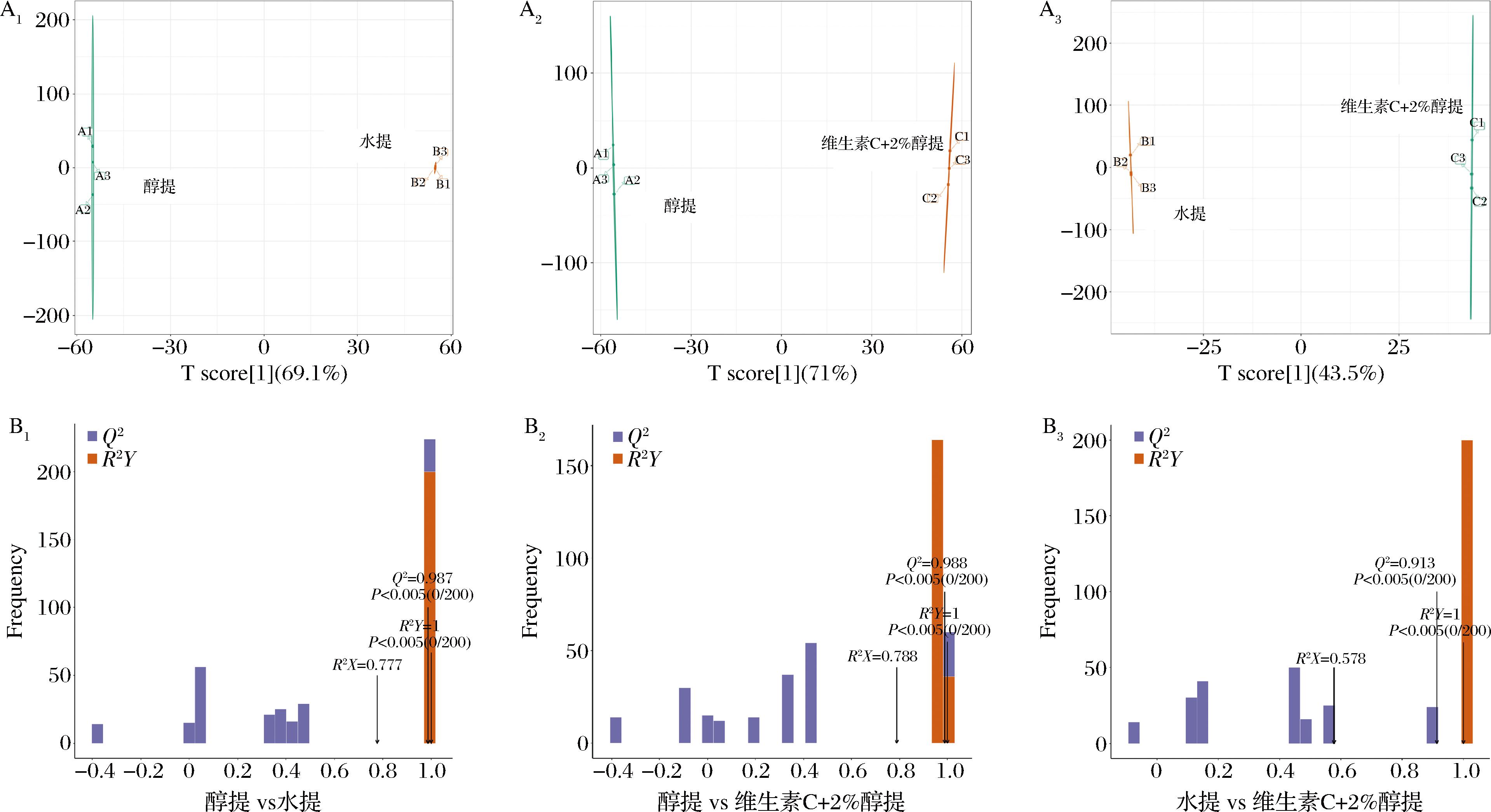
A1-超声波辅助醇提法vs水提得分图;A2-超声波辅助醇提法vs维生素C辅助醇提法得分图;A3-水提vs维生素C辅助醇提法得分图;B1-超声波辅助醇提法vs水提验证图;B2-超声波辅助醇提法vs维生素C辅助醇提法验证图;B3-水提vs维生素C辅助醇提法验证图
图4 OPLS-DA 得分图和检验图
Fig.4 OPLS-DA score diagram and permutation test diagram
对于OPLS-DA模型导出的指标,只有在模型没有过拟合的情况下才更具说服力。采用R2X,R2Y和Q2对OPLS-DA模型进行了评估,在模型评估中,R2X和R2Y分别代表所构建模型对X矩阵和Y矩阵的解释程度,Q2用于衡量模型的预测能力。一般来说,这3项指标越趋近于1,表明模型的稳定性和可靠性越强。当Q2>0.5时,可判定该模型有效;若Q2>0.9,则说明模型表现优异。图4-B1~图4-B3为OPLS-DA验证图,如图所示,均符合P<0.05,模型最佳,结果稳定可靠。
用韦恩图表示甘薯皮不同提取方法鉴定出的代谢物数量,可发现多组间的差异代谢物,如图5-A所示。甘薯皮不同提取方法鉴出的代谢物分别是:超声波辅助醇提中1 603种,水提中1 462种,维生素C辅助醇提中1 629种,三者共有的代谢物有442种,各部位中独有的代谢物数量分别是:超声波辅助醇提中350种,水提中215种,维生素C辅助醇提中209种。水提和超声波辅助醇提、超声波辅助醇提和维生素C辅助醇提、水提和维生素C辅助醇提共有代谢数量分别是884、1 051和910种。
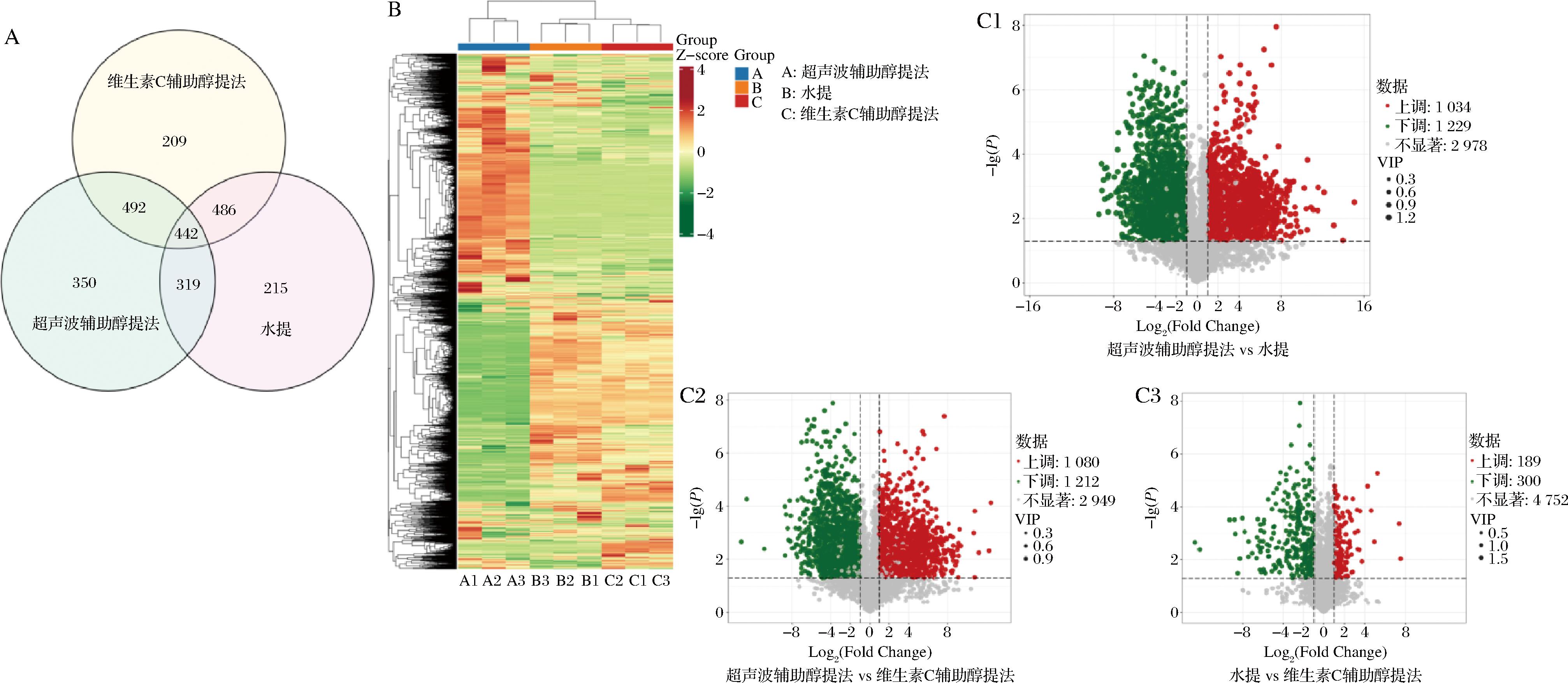
A-代谢物韦恩图;B-差异代谢物聚类热图;C1-超声波辅助醇提法vs水提差异代谢物火山图;C2-超声波辅助醇提法vs维生素C辅助醇提法差异代谢物火山图;C3-水提vs维生素C辅助醇提法差异代谢物火山图
图5 代谢物韦恩图,差异代谢物聚类热图,差异代谢物火山图
Fig.5 Venn diagram of metabolites, cluster heatmap of differential metabolites, and volcanic map of differential metabolites
基于VIP>1.0,FC>1.2或FC<0.833且P<0.05的筛选标准,差异代谢物的组间筛选结果如图5-B聚类热图所示。图中横向坐标标注为样品名称,纵向坐标对应差异代谢物信息,Group栏为样本分组标识。热图通过不同颜色对标准化处理后的代谢物相对含量进行可视化呈现,其中红色区域表示高含量,绿色区域表示低含量。聚类枝越短代表相似性越高。在对聚类热图的分析可知,不同提取方法的代谢谱存在不同的分组模式。从聚类层面看,水提和维生素C辅助醇提代谢物种类相似度较高,从代谢物丰度层面看,超声波辅助醇提中代谢物主要集中在红色高表达区域,而水提和维生素C辅助醇提中代谢物主要集中在绿色低表达区域,说明大多数差异代谢物在超声波辅助醇提中的表达量高于水提和维生素C辅助醇提中。
通过差异代谢物火山图(图5-C1~图5-C3)可直观显示差异代谢物的整体分布情况。在超声波辅助醇提vs水提中有2 263种差异代谢物,其中1 034种上调、1 229种下调;在超声波辅助醇提vs维生素C辅助醇提中有2 292种差异代谢物,其中1 080种上调、1 212种下调;在水提vs维生素C辅助醇提中有489种代谢物,其中189种上调、300种下调;不同提取方法差异代谢物上下调的具体数量如表1所示。
针对上述分类,对不同提取方式中差异较大的化合物进行分析。脂质和类脂分子、苯环型化合物、有机酸及其衍生物和有机氮化合物在总差异代谢物中占比最大。超声波辅助醇提vs水提中上调物质多为有机酸及其衍生物、苯环型化合物及苯丙烷和聚酮化合物,主要差异化合物为1-棕榈酰甘油磷酸胆碱(FC=33 832.64)、酸藤子酚(FC=15 836.24)、2-苄基琥珀酸(FC=4 582.52)、灯盏花素A(FC=3 057.31)等,下调物质多为生物碱及其衍生物和有机氮化合物,主要化合物为Val-Arg-Glu-Glu(FC=0.001)、腺苷-3′-5′-环单磷酸水合物(FC=0.002)、野靛苷(FC=0.002)和洋地黄毒苷(FC=0.002)等。
超声波辅助醇提vs维生素C辅助醇提中上调物质多为有机酸及其衍生物、苯环型化合物及苯丙烷和聚酮化合物,主要差异化合物为印楝沙兰林(FC=5 064.83)、槐酮(FC=2 384.55)、1-咖啡酰奎宁酸(FC=1 807.03)、酸藤子酚(FC=1 793.40)、2-苄基琥珀酸(FC=614.12)等。下调物质多为生物碱及其衍生物和有机氮化合物,主要化合物为腺苷-3′-5′-环单磷酸水合物(FC=0.000 1)、甲酰胺菌素B(FC=0.000 2)、野靛苷(FC=0.000 5)、Val-Arg-Glu-Glu(FC=0.002)等。
水提vs维生素C辅助醇提中上调物质多为有机氮化合物,主要差异化合物为乳-N-岩藻糖-戊糖I(FC=183.95)、α-D-半乳糖胺1-磷酸(FC=166.34)。下调物质多为脂质和类脂分子,主要差异物为甲酰胺菌素B(FC=0.000 2)、15S-羟基-8Z,11Z,13E-十八碳三烯酸(FC=0.002)、3-(3,4-二甲氧基苯基)-7-羟基-4H-苯并吡喃-4-酮(FC=0.002)、8-羟基-9E,11Z,14Z-十八碳三烯酸(FC=0.002)和松油酸甲酯(FC=0.002)等。
对酚酸类化合物成分进行分析,代谢物差异较大(FC>2)物质结果见表2,超声波辅助醇提方法中1-咖啡酰奎宁酸、3-甲氧基儿茶酚、2-(2,4-二羟基苯基)-2-羟基乙酸、10-副姜油酮、异绿原酸C、多米芬、1,3-O-双咖啡酰奎宁酸(洋蓟酸)、4-O-咖啡酰奎宁酸甲酯、绿原酸(3-O-咖啡酰奎宁酸)、3,4-二羟基苯乙烯、菊苣酸、O-双(2-氨基乙氧基)苯、对香豆醇、异绿原酸B、阿格努赛德、3,4,5-三甲氧基苯甲酸和咖啡酸含量较水提和维生素C辅助醇提更高。水提方法中8-副姜油酮、降二氢辣椒酯和8-姜酚含量较维生素C辅助醇提更高。槭苷元G和连翘酯苷A在超声波辅助醇提和水提中含量差异更大。
表2 酚酸类关键代谢物
Table 2 Key metabolites of phenolic acids
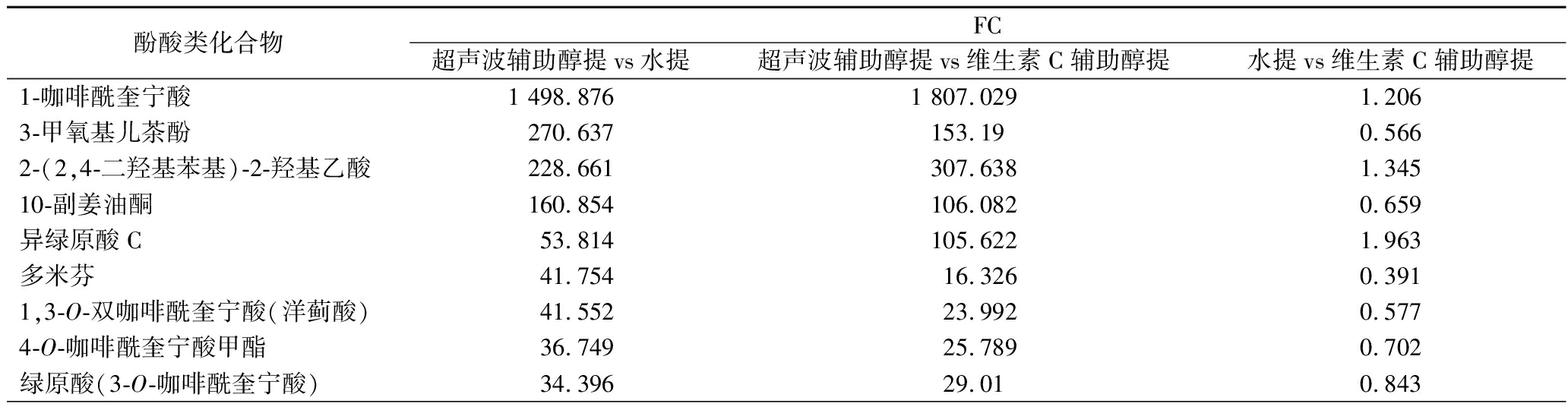
酚酸类化合物FC超声波辅助醇提vs水提超声波辅助醇提vs维生素C辅助醇提水提vs维生素C辅助醇提1-咖啡酰奎宁酸1 498.8761 807.0291.2063-甲氧基儿茶酚270.637153.190.5662-(2,4-二羟基苯基)-2-羟基乙酸228.661307.6381.34510-副姜油酮160.854106.0820.659异绿原酸C53.814105.6221.963多米芬41.75416.3260.3911,3-O-双咖啡酰奎宁酸(洋蓟酸)41.55223.9920.5774-O-咖啡酰奎宁酸甲酯36.74925.7890.702绿原酸(3-O-咖啡酰奎宁酸)34.39629.010.843
续表2
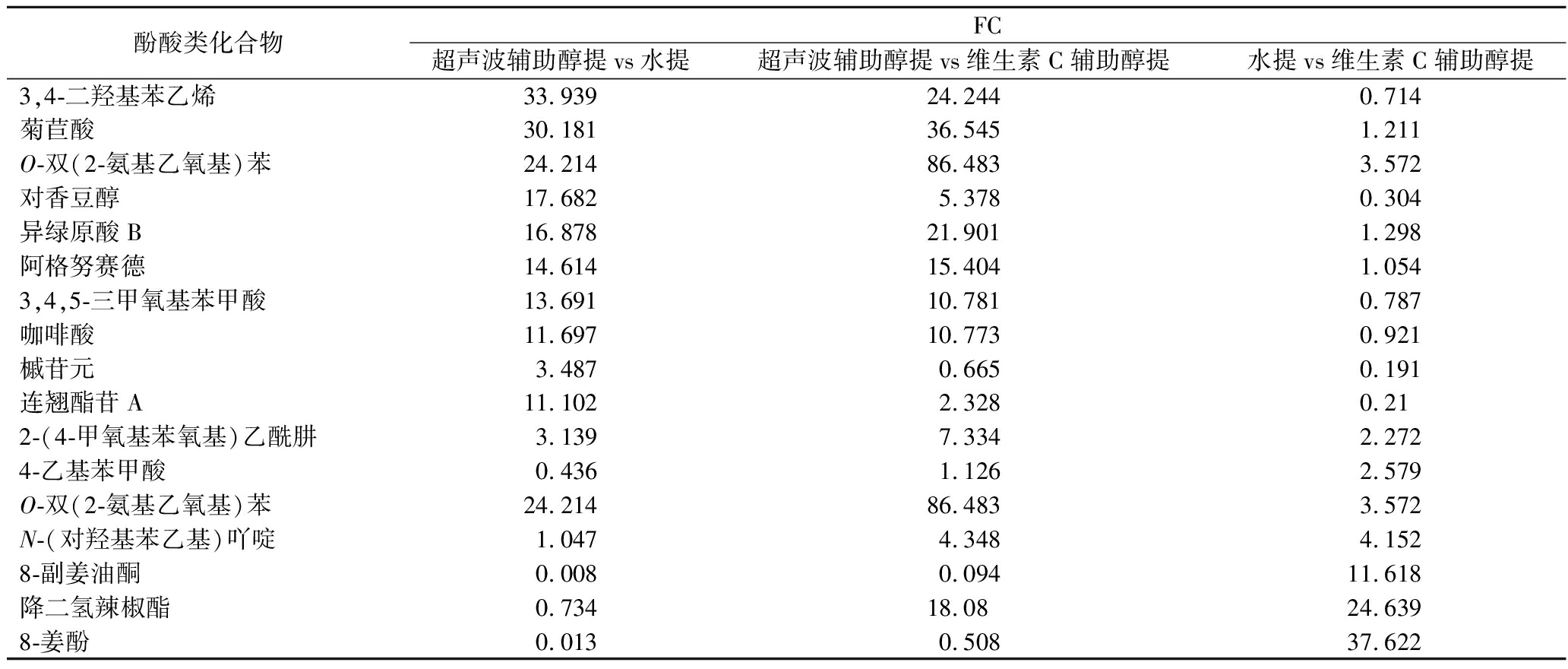
酚酸类化合物FC超声波辅助醇提vs水提超声波辅助醇提vs维生素C辅助醇提水提vs维生素C辅助醇提3,4-二羟基苯乙烯33.93924.2440.714菊苣酸30.18136.5451.211O-双(2-氨基乙氧基)苯24.21486.4833.572对香豆醇17.6825.3780.304异绿原酸B16.87821.9011.298阿格努赛德14.61415.4041.0543,4,5-三甲氧基苯甲酸13.69110.7810.787咖啡酸11.69710.7730.921槭苷元 3.4870.6650.191连翘酯苷A11.1022.3280.212-(4-甲氧基苯氧基)乙酰肼3.1397.3342.2724-乙基苯甲酸0.4361.1262.579O-双(2-氨基乙氧基)苯24.21486.4833.572N-(对羟基苯乙基)吖啶1.0474.3484.1528-副姜油酮0.0080.09411.618降二氢辣椒酯0.73418.0824.6398-姜酚0.0130.50837.622
2.5 差异代谢物KEGG富集
利用KEGG数据库对水提、超声波辅助醇提和维生素C辅助醇提方法提取的差异代谢物进行通路分析,前25条富集程度最大的代谢通路如图6所示,在这些比较组中,超声波辅助醇提和水提的主要差异代谢通路基本一致。
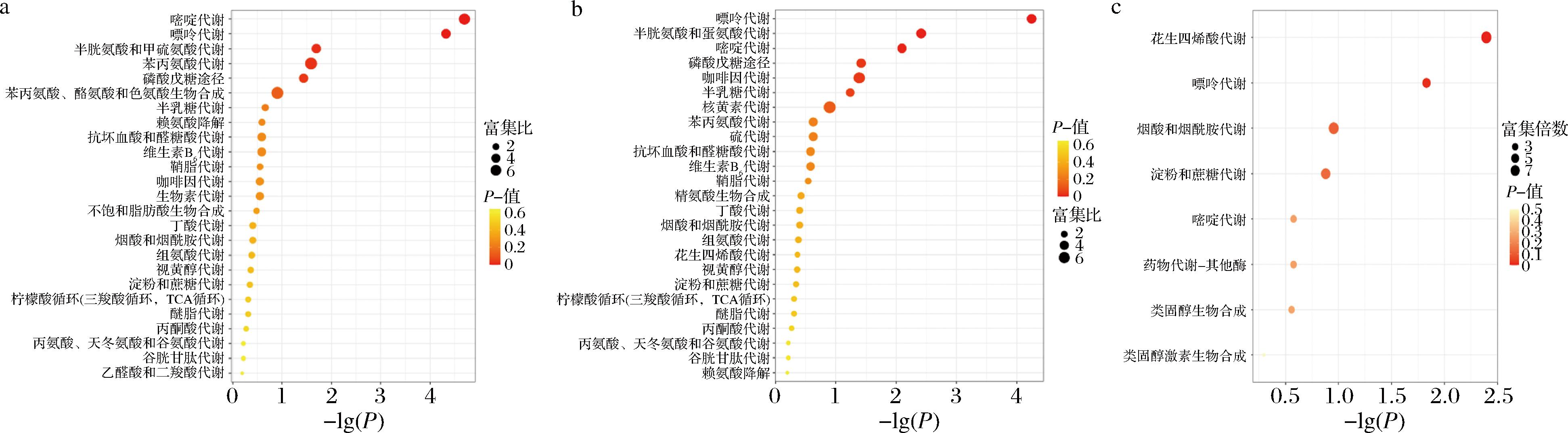
a-超声波辅助醇提法vs水提;b-超声波辅助醇提法vs维生素C辅助醇提法;c-水提vs维生素C辅助醇提法
图6 差异代谢物KEGG 富集图
Fig.6 KEGG enrichment of differential metabolites
在超声波辅助醇提vs水提中,共将2 263个差异代谢物注释至32条代谢通路。其中,有5条代谢通路呈现显著差异(P<0.05),分别为嘧啶代谢、嘌呤代谢、半胱氨酸和甲硫氨酸代谢、苯丙氨酸代谢以及磷酸戊糖途径。上述代谢途径共涉及130种差异代谢物,上调的差异代谢物有2′-脱氧胞苷-5′-单磷酸、槲皮素、吐根碱等89种,下调的有罂粟碱、4-羟基鞘氨醇等41种。嘧啶代谢通路涉及11种差异代谢物,2′-脱氧胞苷-5′-单磷酸、5-羟甲基脱氧胞苷等在醇提vs水提中上调,胞苷、2′-脱氧胞苷5′-三磷酸、胸苷、胞嘧啶、胞苷-5′-单磷酸、胞苷-5′-二磷酸、假尿苷、5-甲基胞嘧啶、尿嘧啶核苷在醇提vs水提中下调。嘌呤代谢通路涉及27种差异代谢物,腺苷-5′-二磷酸、ADP核糖等11种代谢物上调,腺苷-3′-5′-环单磷酸水合物、鸟嘌呤等16种代谢物下调。半胱氨酸和甲硫氨酸代谢涉及5种差异代谢物,包括L-胱硫醚、1-脱氧-D-木酮糖-5-磷酸、N-甲酰蛋氨酸、3-甲硫基丙酸、5-脱氧-5-甲硫腺苷,均在超声波辅助醇提vs水提中上调。苯丙氨酸代谢途径涉及2种差异代谢物,苯乙酸上调,苯丙酮酸下调。磷酸戊糖途径涉及3种差异代谢物,包括6-磷酸葡萄糖酸、D-果糖-1,6-二磷酸、核糖1-磷酸均下调。
在超声波辅助醇提vs维生素C辅助醇提中,将2 292个差异代谢物注释到34条代谢通路上,其中差异显著的代谢通路有5条(P<0.05),研究涉及嘌呤代谢、半胱氨酸与甲硫氨酸代谢、嘧啶代谢、磷酸戊糖代谢及咖啡因代谢等多条代谢通路。上述代谢途径中共包含178种差异代谢物,上调的差异代谢物有2-羟基戊二酸、腺苷-5′-二磷酸等87种,下调的有罂粟碱、反式-草木犀苷呤等91种。嘌呤代谢涉及25种差异代谢物,其中尿素、2′-脱氧腺苷-5′-磷酸等10种代谢物上调,2′-脱氧腺苷、腺苷-5′-单磷酸等15种代谢物下调。半胱氨酸和甲硫氨酸代谢涉及6种差异代谢物,包括1-脱氧-D-木酮糖-5-磷酸、L-胱硫醚、3-甲硫基丙酸、N-甲酰蛋氨酸、5-脱氧-5-甲硫腺苷5种代谢物上调,S-甲基-5-硫代-D-核糖-1-磷酸下调。嘧啶代谢途径涉及8种差异代谢物,其中尿素上调,假尿苷、胞苷-5′-二磷酸等7种代谢物下调。磷酸戊糖代谢途径涉及3种差异代谢物,其中2-酮-3-脱氧-D-葡萄糖酸上调,核糖1-磷酸和6-磷酸葡萄糖酸下调。咖啡因代谢途径涉及2种差异代谢物,1-甲基尿酸上调,7-甲基黄嘌呤下调。
在水提vs维生素C辅助醇提中,本研究对489个差异代谢物进行代谢通路注释,共映射至8条代谢通路。其中,2条代谢通路呈现显著差异(P<0.05),分别为花生四烯酸代谢通路与嘌呤代谢途径。这2条通路共涉及43种差异代谢物,上调的差异代谢物有角鲨烯二磷酸、苦杏仁苷等14种,下调的有腺苷、对香豆醇等29种。花生四烯酸代谢途径涉及3种差异代谢物,包括20-羟基-5Z,8Z,11Z,14Z-二十碳四烯酸、5S-氢过氧-6E,8Z,11Z,14Z-二十碳四烯酸和5,6-二羟基-8Z,11Z,14Z-二十碳三烯酸。嘌呤代谢涉及6种差异代谢物,包括2′-脱氧腺苷-5′-磷酸上调,腺苷-5′-单磷酸和腺嘌呤等5种代谢物下调。
3 结论与讨论
本研究采用非靶向代谢组学技术,对水提、超声波辅助醇提和维生素C辅助醇提3种方法提取的甘薯皮多酚进行代谢物分析,共鉴定出401种酚类物质。PCA显示水提组样本聚集稳定,超声波辅助醇提与维生素C辅助醇提组异质性大;OPLS-DA验证组间差异显著,3组比较分别筛选到2 263、2 292、489种差异代谢物,主要富集于脂质、氨基酸和碳水化合物代谢通路。其中,超声波辅助醇提对酚酸(如1-咖啡酰奎宁酸、绿原酸)和类黄酮提取效果更优,维生素C辅助醇提可平衡成分多样性与稳定性。KEGG分析表明,差异代谢物主要分布于嘌呤代谢、半胱氨酸和甲硫氨酸代谢等通路。本研究从代谢层面揭示了不同提取方法对甘薯皮多酚成分的影响,为甘薯皮资源的高值化利用及提取工艺优化提供了理论支撑。
传统甘薯皮多酚提取研究多局限于单一成分定量或活性评价,缺乏对代谢物谱的系统解析。本研究首次通过非靶向代谢组学技术,全面揭示了不同提取方法对甘薯皮多酚成分的影响,发现超声波辅助醇提和维生素C辅助醇提在成分多样性上存在显著差异,而维生素C的引入可有效调节提取物的稳定性。这一结果为解释不同提取工艺下多酚活性差异提供了物质基础,也验证了代谢组学技术在植物提取物质量控制中的适用性。此外,研究发现的差异代谢物富集通路(如嘌呤代谢、脂质代谢),为深入探索多酚提取的作用机制提供了新方向,对推动甘薯皮功能成分的精准开发具有重要意义。
[1] 王欣, 李强, 曹清河, 等.中国甘薯产业和种业发展现状与未来展望[J].中国农业科学, 2021, 54(3):483-492.
WANG X, LI Q, CAO Q H, et al.Current status and future prospective of sweet potato production and seed industry in China[J].Scientia Agricultura Sinica, 2021, 54(3):483-492.
[2] 马代夫, 李强, 曹清河, 等.中国甘薯产业及产业技术的发展与展望[J].江苏农业学报, 2012, 28(5):969-973.
MA D F, LI Q, CAO Q H, et al.Development and prospect of sweet potato industry and its technologies in China[J].Jiangsu Journal of Agricultural Sciences, 2012, 28(5):969-973.
[3] 高志远, 胡亚亚, 韩美坤, 等.甘薯块根多酚高效测定技术优化与应用[J].中国粮油学报, 2021, 36(11):49-56.
GAO Z Y, HU Y Y, HAN M K, et al.Optimization and application of efficient determination technique for polyphenol in sweet potato tubers[J].Journal of the Chinese Cereals and Oils Association, 2021, 36(11):49-56.
[4] 蒋新龙, 王海, 张玲丹.超声-微波协同提取甘薯皮绿原酸及其微胶囊化工艺优化研究[J].中国粮油学报, 2021, 36(10):138-143.
JIANG X L, WANG H, ZHANG L D.Extraction of chlorogenic acid from sweet potato skin by ultrasonic microwave synergistic and optimization of microencapsulation process[J].Journal of the Chinese Cereals and Oils Association, 2021, 36(10):138-143.
[5] 于章龙, 刘瑞, 孙元琳, 等.甘薯多酚氧化酶酶学性质及电解水对其酶活力抑制效果[J].食品工业, 2021, 42(6):61-65.
YU Z L, LIU R, SUN Y L, et al.The enzymatic properties of polyphenol oxidase from sweet potato and the inhibitory effect of electrolyzed water on its enzyme activity[J].The Food Industry, 2021, 42(6):61-65.
[6] 胡康棣, 彭湘君, 姚改芳, 等.不同耐贮性甘薯的抗氧化特性差异[J].江苏农业科学, 2021, 49(16):162-168.
HU K D, PENG X J, YAO G F, et al.Study on difference of antioxidant characteristics of sweet potatoes with different storability[J].Jiangsu Agricultural Sciences, 2021, 49(16):162-168.
[7] 孔秀林, 张文婷, 孙健, 等.甘薯叶片中多酚类物质的提取及抗氧化活性研究[J].江苏师范大学学报(自然科学版), 2018, 36(2):34-37;41.
KONG X L, ZHANG W T, SUN J, et al.Study on the extraction and antioxidant activity of polyphenols from sweet potato leaves[J].Journal of Jiangsu Normal University(Natural Science Edition), 2018, 36(2): 34-37; 41.
[8] 忻晓庭, 潘悠优, 陆国权, 等.响应面法优化甘薯皮多酚超声提取工艺[J].江苏师范大学学报(自然科学版), 2018, 36(1):26-29;32.
XIN X T, PAN Y Y, LU G Q, et al.Optimization of ultrasonic-assisted extraction technology of polyphenols from sweet potato peel by response surface methodogy[J].Journal of Jiangsu Normal University (Natural Science Edition), 2018, 36(1):26-29;32.
[9] 张文婷, 孔秀林, 孙健, 等.响应面法优化甘薯叶片多酚提取工艺[J].核农学报, 2018, 32(12):2397-2405.
ZHANG W T, KONG X L, SUN J, et al.Optimization of extraction process of polyphenols from sweet potato leaves by response surface methodology[J].Journal of Nuclear Agricultural Sciences, 2018, 32(12):2397-2405.
[10] 林锦裕, 杨秀敏, 陈泽豪, 等.不同甘薯皮多酚提取液抑菌性的对比探究[J].湖南农业科学, 2019(5):92-94.
LIN J Y, YANG X M, CHEN Z H, et al.Contrast of bacteriostasis of polyphenol extracts from different sweet potato peels[J].Hunan Agricultural Sciences, 2019(5):92-94.
[11] 张佳鑫, 梁思琪, 肖强, 等.黄精总黄酮提取工艺优化及抗氧化活性分析[J].湖北林业科技, 2024, 53(1):37-44.
ZHANG J X, LIANG S Q, XIAO Q, et al.Extraction and antioxidant activity analysis of total flavonoids of Polygonatum sibiricum[J].Hubei Forestry Science and Technology, 2024, 53(1):37-44.
[12] CAJKA T, VACLAVIKOVA M, DZUMAN Z, et al.Rapid LC-MS-based metabolomics method to study the fusarium infection of barley[J].Journal of Separation Science, 2014, 37(8):912-919.
[13] 龚成胜, 王述彬, 刘金兵, 等.瓜果类蔬菜代谢组学研究进展[J].中国蔬菜, 2024(3):23-31.
GONG C S, WANG S B, LIU J B, et al.Research progress of metabonomics in melon and fruit vegetables[J].China Vegetables, 2024(3):23-31.
[14] 张芬, 何守魁, 刘金宝, 等.绿原酸对食源性致病菌抑菌机理的研究进展[J].食品与发酵科技, 2024, 60(5):102-107.
ZHANG F, HE S K, LIU J B, et al.Advances in research on the antibacterial mechanism of chlorogenic acid against foodborne pathogens[J].Sichuan Food and Fermentation, 2024, 60(5):102-107.
[15] LI H L, GAO X, XU F L, et al.Chemical composition and antioxidant activities of essential oil from Paeonia lactiflora flowers[J].Journal of Northwest A&F University (Natural Science Edition), 2017, 45:204-210.
[16] 闫慧娇, 王志伟, 赵恒强, 等.菏泽牡丹花HPLC特征图谱研究及8种成分的测定[J].中草药, 2017, 48(9):1866-1871.
YAN H J, WANG Z W, ZHAO H Q, et al.Study on HPLC digital fingerprint of Paeonia suffruticosa and determination of eight components[J].Chinese Traditional and Herbal Drugs, 2017, 48(9):1866-1871.
[17] 张凡忠, 刘小红, 章初龙, 等.植物响应病原真菌的代谢组学研究进展[J].中国细胞生物学学报, 2016, 38(4):434-440.
ZHANG F Z, LIU X H, ZHANG C L, et al.Progresses of metabolomics in plants response to plant pathogenic fungi[J].Chinese Journal of Cell Biology, 2016, 38(4):434-440.
[18] 张璐哲,赵文双,孟兆青,等.基于非靶向代谢组学的芍药不同部位代谢物差异性分析[J].天然产物研究与开发,2025,37(5):795-806.
ZHANG L Z, ZHAO W S, MENG Z Q, et al. Differential analysis of metabolites in different parts of Paeonia lactiflora Pall. based on non-targeted metabolomics[J]. Natural Product Research and Development, 2025,37(5):795-806.
[19] 胡潇漓, 高昌, 黄平.高效液相色谱法同时测定金银花口服液中6种成分含量[J].中国药业, 2024, 33(19):101-103.
HU X L, GAO C, HUANG P.Simultaneous determination of six components in Jinyinhua oral liquid by HPLC[J].China Pharmaceuticals, 2024, 33(19):101-103.
[20] 何佳丽, 胡恩明, 王纪辉, 等.核桃叶及其乙醇提取物化学成分分析[J].食品与机械, 2024, 40(6):164-169.
HE J L, HU E M, WANG J H, et al.Chemical composition analysis of walnut leaves and their ethanol extracts[J].Food &Machinery, 2024, 40(6):164-169.
[21] 张露, 程鑫鹏, 邓梅, 等.丹皮乙醇提取物的抗氧化和抗糖尿病活性研究[J].天然产物研究与开发, 2024, 36(5):762-770.
ZHANG L, CHENG X P, DENG M, et al.Antidiabetic and antioxidant activities of ethanol extracts from Moutan Cortex[J].Natural Product Research and Development, 2024, 36(5):762-770.
[22] REN Y Y, MAKHELE M, ZHOU J J, et al.Extraction, purification, component analysis and bioactivity of polyphenols from wampee[J].Process Biochemistry, 2025, 150:318-327.
[23] TSVETKOV D E, DMITRENOK A S, TSVETKOV Y E, et al.Polyphenolic components of extracts from the knot wood of plum “Renklod sinii” (Renclode blue)[J].Russian Chemical Bulletin, 2024, 73(12):3768-3774.
[24] PODLOUCK P, POLI
P, POLI ENSK
ENSK I, JIRSA O.Effect of the extraction solvent and method on the determination of the total polyphenol content in different common buckwheat (Fagopyrum esculentum Moench) varieties[J].Food &Nutrition Research, 2025, 69.DOI:10.29219/fnr.v69.9834.
I, JIRSA O.Effect of the extraction solvent and method on the determination of the total polyphenol content in different common buckwheat (Fagopyrum esculentum Moench) varieties[J].Food &Nutrition Research, 2025, 69.DOI:10.29219/fnr.v69.9834.