牡蛎是我国产量最大的养殖贝类,2023年产量达到667万t,占全国贝类总产量40%以上[1]。作为重要的海洋资源,牡蛎具有“海洋牛奶”的美称,滋味鲜美,具有较高的营养价值。牡蛎烹饪方式包括蒸制、水煮、烘烤等,热加工方式对其理化性质具有重要影响,具体表现为蛋白质的聚集、变性与氧化,脂肪的氧化分解等,并进一步影响其风味[2]。JIANG等[3]研究表明,与烘烤和油炸相比,蒸制牡蛎具有更高的蛋白消化率和矿物质(锌、铁)生物利用度,而蒸制与烘烤牡蛎生成的潜在危害物质晚期糖基化终产物(advanced glycation end products,AGEs)均低于油炸牡蛎;林玉锋等[4]比较了蒸制、水煮、微波和焙烤等方式对牡蛎品质的影响,发现焙烤牡蛎具有最接近生牡蛎的硬度、弹性,但其蛋白含量下降程度较大;蒸制牡蛎的氨基酸等营养成分流失最少,但其硬度较大。
近年来,蒸汽辅助烘烤(steam assisted roasting)作为一种新型烹饪方式,因其结合蒸制与焙烤的技术优势而受到关注。蒸汽辅助烘烤是在空气对流烘烤的基础上,引入过热蒸汽辅助加热的烹饪手段[5]。MORA等[6]分别采用35%、88%蒸汽量在100 ℃的烤箱温度下烘烤火鸡肉,以火鸡肉中心温度达74 ℃为终点,发现与不添加蒸汽相比,蒸汽辅助烘烤显著缩短火鸡肉达到烹饪终点所需时间,火鸡肉的剪切力降低、具有较高的含水量及水分迁移速率,其中35%蒸汽量烘烤火鸡肉得率更高、嫩度更佳。此外还有关于蒸汽辅助烘烤对牛肉[7]、菠菜[8]品质影响的研究,均表明蒸汽辅助烘烤能使其获得更佳的食用品质。目前,尚未有将蒸汽辅助烘烤应用于牡蛎烹饪方面的研究。因此,本研究旨在探讨不同烹饪方式、不同蒸汽量对烘烤牡蛎理化性质与风味品质的影响。
1 材料与方法
1.1 材料与试剂
鲜活太平洋牡蛎(Crassostrea gigas),青岛市黄岛区;Bradford蛋白浓度检测试剂盒,北京索莱宝科技有限公司;BOXBIO羰基含量试剂盒,北京盒子生工科技有限公司;其余化学试剂均为国产分析纯。
1.2 仪器与设备
JO-E-T61型食品接触用万能蒸烤箱,广州市英联斯特餐饮设备有限公司;NPPUI TR230型多通路温度巡检仪,东莞市横河电子仪器有限公司;T18 basic高速均质分散机,德国艾卡仪器设备有限公司;AB135-型精密电子天平,瑞士梅特勒托利多公司;Synergy H4型多功能酶标仪,美国Bio-tek公司;FlavourSpec气相离子迁移谱联用仪,德国G.A.S仪器有限公司。
1.3 实验方法
1.3.1 样品准备与烹饪
选择尺寸接近12 cm×5 cm×3 cm,外壳完整,形状接近的牡蛎,清洗后沥干。待进行烹饪实验时,去除牡蛎上壳,并将其分为3组,对照组在万能蒸烤箱的烤模式下,实验组分别在蒸烤模式(25%蒸汽量、50%蒸汽量)进行烘烤(烘烤温度均为200 ℃),所获得样品分别命名为NS(无蒸汽)、LS(低蒸汽量)与HS(高蒸汽量)。使用多通路温度巡检仪监测其中心温度变化,记录每种烘烤方式使牡蛎中心温度达65、70、75 ℃时间,后续按照所得时间进行烹饪。烘烤完成后,将牡蛎肉取下并置于-20 ℃保藏备用。
1.3.2 烹饪损失率测定
在烘烤开始前,先将牡蛎肉从壳中取下,用吸水纸吸干水分,称取其烹饪前质量m1;然后放回其下壳中,按照1.3.1节中的方式进行烘烤,称取烘烤完成后的质量m2。烹饪损失率的计算如公式(1)所示:
烹饪损失率![]()
(1)
1.3.3 感官评价
参考GB/T 37062—2018《水产品感官评价指南》的方法制定牡蛎质地、形态、气味、滋味以及整体喜好度的感官评价表,评价标准如表1所示。选择10位经训练的感官评价员参与实验,测试者年龄均在22~28岁之间。
表1 牡蛎感官评价标准
Table 1 Criteria for sensory evaluation of steam-assisted roasted oysters

评价项目描述得分质地质地较硬0~3质地稍软4~6质地柔软7~10形态严重收缩0~3轻度收缩4~6饱满多汁7~10清香(气味)清香味较弱0~3清香味一般4~6清香味较强7~10肉香(气味)肉香味较弱0~3肉香味一般4~6肉香味较强7~10鲜味(滋味)鲜味较弱0~3鲜味一般4~6鲜味较强7~10甜味(滋味)甜味较弱0~3甜味一般4~6甜味较强7~10整体喜好度较难接受0~3可接受4~6较喜爱7~10
1.3.4 可溶性蛋白含量及羰基含量测定
分别提取烘烤牡蛎的水溶性蛋白和盐溶性蛋白。参考焦云爽等[9]方法并稍作修改,称取约2.0 g牡蛎样品于50 mL离心管中,加入20 mL预冷至4 ℃的0.02 mol/L磷酸盐缓冲液(pH 7.0),高速匀浆1 min,4 ℃下5 000 r/min离心15 min,重复1次并合并上清液,即为水溶性蛋白样品;在沉淀中加入20 mL预冷至4 ℃的0.02 mol/L磷酸盐缓冲液(0.45 mol/L KCl,pH 7.0),然后在4 ℃ 6 000 r/min离心25 min,重复1次,将上清液合并,得到盐溶性蛋白样品。
采用Bradford蛋白浓度试剂盒分别测定水溶性、盐溶性蛋白样品中的蛋白含量。使用BOXBIO羰基含量试剂盒测定水溶性蛋白样品中的羰基含量,结果以μmol/g protein表示。
1.3.5 硫代巴比妥酸反应物(thiobarbituric acid reactive substances,TBARS)值测定
参考国家标准GB 5009.181—2016《食品安全国家标准 食品中丙二醛的测定》,建立标准曲线,样品的TBARS值的计算如公式(2)所示:
(2)
式中:c,从标准曲线中得到的试样溶液中丙二醛的浓度,μg/mL;V,试样溶液定容体积mL;m,最终试样溶液所代表的试样质量,g。
1.3.6 席夫碱与荧光AGEs含量测定
席夫碱含量测定参考李奥[10]的方法并稍作修改。称取2.0 g牡蛎样品,加入10倍体积20 mmol/L的磷酸缓冲液(pH 6.5),高速匀浆1 min,4 ℃下8 000 r/min离心15 min,取上清液,使用荧光分光光度计检测。检测条件:激发波长360 nm,发射波长400~600 nm,检测间隔1 nm,狭缝宽度5 nm。荧光AGEs含量测定参考ZHANG等[11]的方法并稍作修改,称取2.0 g牡蛎样品,加入10倍体积20 mmol/L的磷酸缓冲液(pH 8.2),高速匀浆1 min,随后在55 ℃水浴中振荡60 min,4 ℃下8 000 r/min离心15 min,取上清液,使用荧光分光光度计进行检测。检测条件:激发波长325 nm,发射波长350~600 nm,检测间隔1 nm,狭缝宽度5 nm。
1.3.7 基于气相色谱-离子迁移谱(gas chromatography-ion mobility spectrometry,GC-IMS)的挥发性风味分析
样品前处理参考赵玲等[12]的方法并稍作修改。取2.0 g样品,加入2.0 mL饱和NaCl溶液,60 ℃下孵育20 min,进样针温度80 ℃。通过GC×IMS library search软件进行挥发性化合物定性分析,生成指纹图谱并进行主成分分析(principal component analysis,PCA)。
1.3.8 数据处理与分析
所有实验均重复3次,取平均值。采用Excel软件记录和处理实验数据,数据以“平均值±标准差”表示,采用SPSS软件进行Duncan差异显著性分析,P<0.05表示差异显著,采用Origin软件绘制图表。
2 结果与分析
2.1 感官评价
蒸汽辅助烘烤方式对牡蛎外观形态的影响如表2所示,其中各组牡蛎均保持完整的形态,但随着烹饪中心温度的升高,牡蛎肉质呈现更大程度的收缩。
表2 蒸汽辅助烘烤得到牡蛎的外观
Table 2 Product appearance of steam-assisted roasted oysters
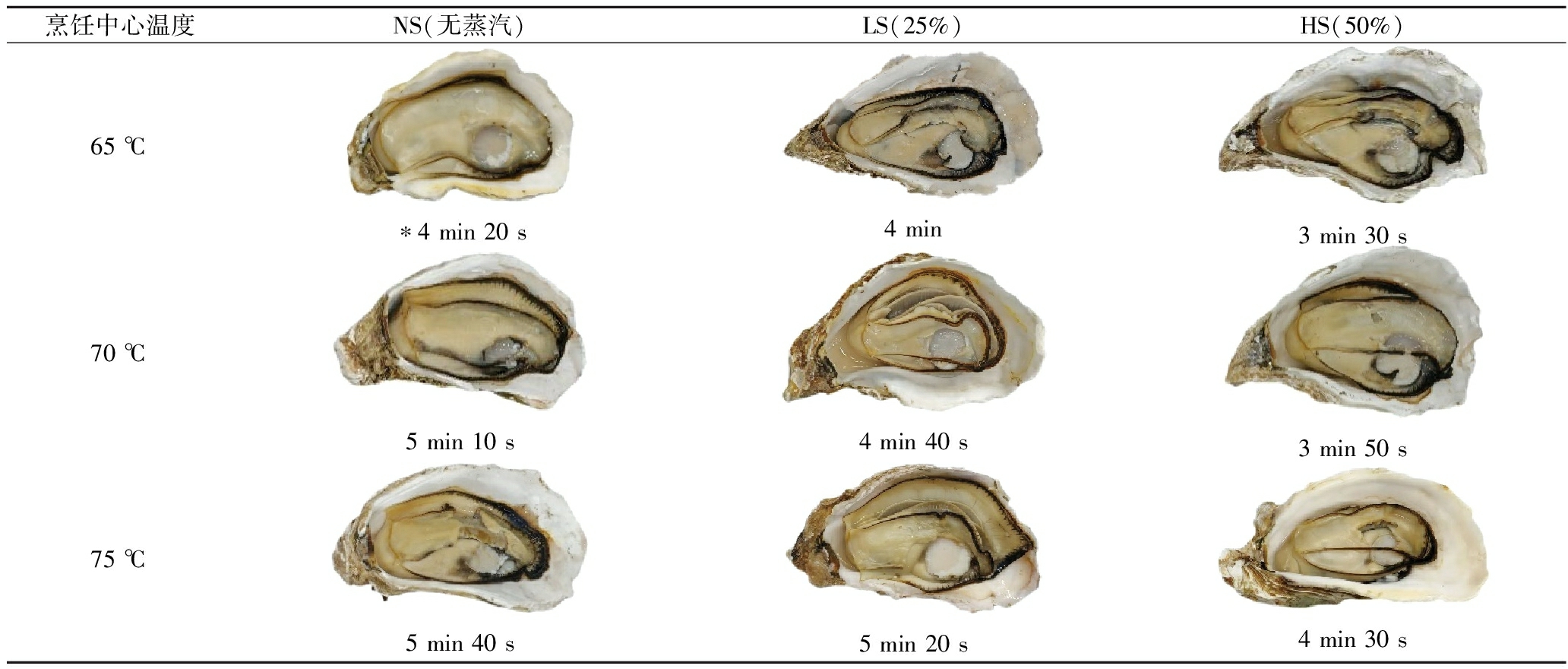
烹饪中心温度NS(无蒸汽)LS(25%)HS(50%)65 ℃∗4 min 20 s4 min3 min 30 s70 ℃5 min 10 s4 min 40 s3 min 50 s75 ℃5 min 40 s5 min 20 s4 min 30 s
注:*表示样品到达对应中心温度所需时间(精确到10 s)。
蒸汽辅助烘烤方式对牡蛎感官评分如图1所示。LS-75 ℃、HS-70 ℃与NS-75 ℃具有较高的喜好度评分,其中LS-75 ℃在鲜味、咸味、肉香味3项指标评分较高,而HS-70 ℃在清香味这一指标评分最高。烹饪中心温度升高使牡蛎肉香味与喜好度评分较高,可能与烹饪过程中牡蛎的风味变化有关;蒸汽量增大使牡蛎形态、光泽评分提升,可能由于湿热环境不利于牡蛎产生结壳;烹饪中心温度升高以及蒸汽量增大使牡蛎质地、形态得分降低,可能与烹饪造成的汁液流失有关。
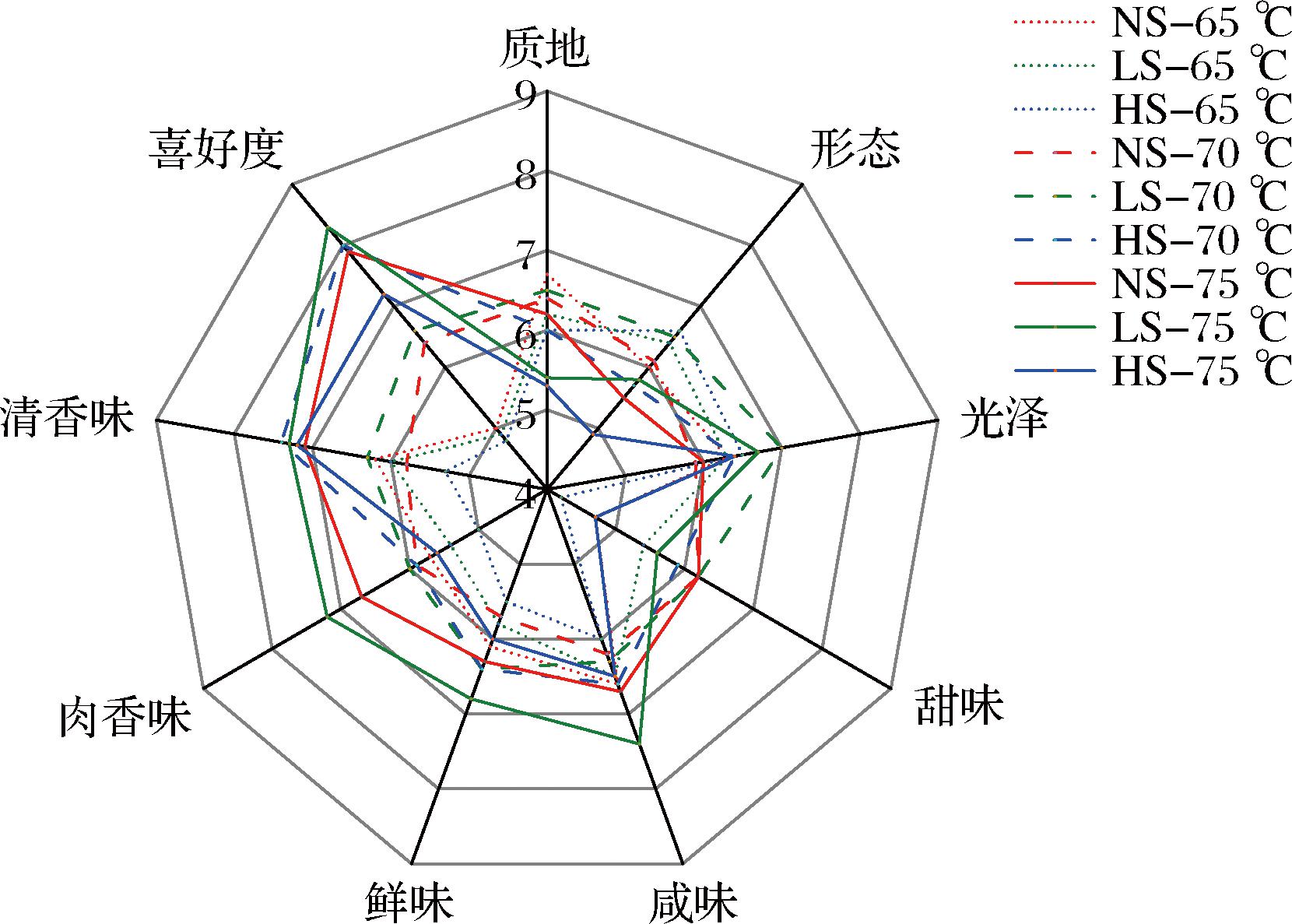
图1 蒸汽辅助烘烤牡蛎的感官评分
Fig.1 Sensory scoring of steam-assisted roasted oysters
2.2 烹饪损失率
牡蛎含水量高,且通常以其活体状态烹饪,其在热加工中易出现应激性的汁液流失[12]。蒸汽辅助烘烤牡蛎的烹饪损失率如图2所示。牡蛎的烹饪损失率随烹饪中心温度提高呈不显著的增大趋势(P>0.05),仅LS-75 ℃烹饪损失率显著大于LS-65 ℃与LS-70 ℃(P<0.05);除HS-70 ℃外,蒸汽辅助烘烤均使牡蛎烹饪损失率显著增加(P<0.05),这可能由于蒸汽阻碍牡蛎烘烤过程中表面结壳,从而无法阻止其水分溢出[13]。
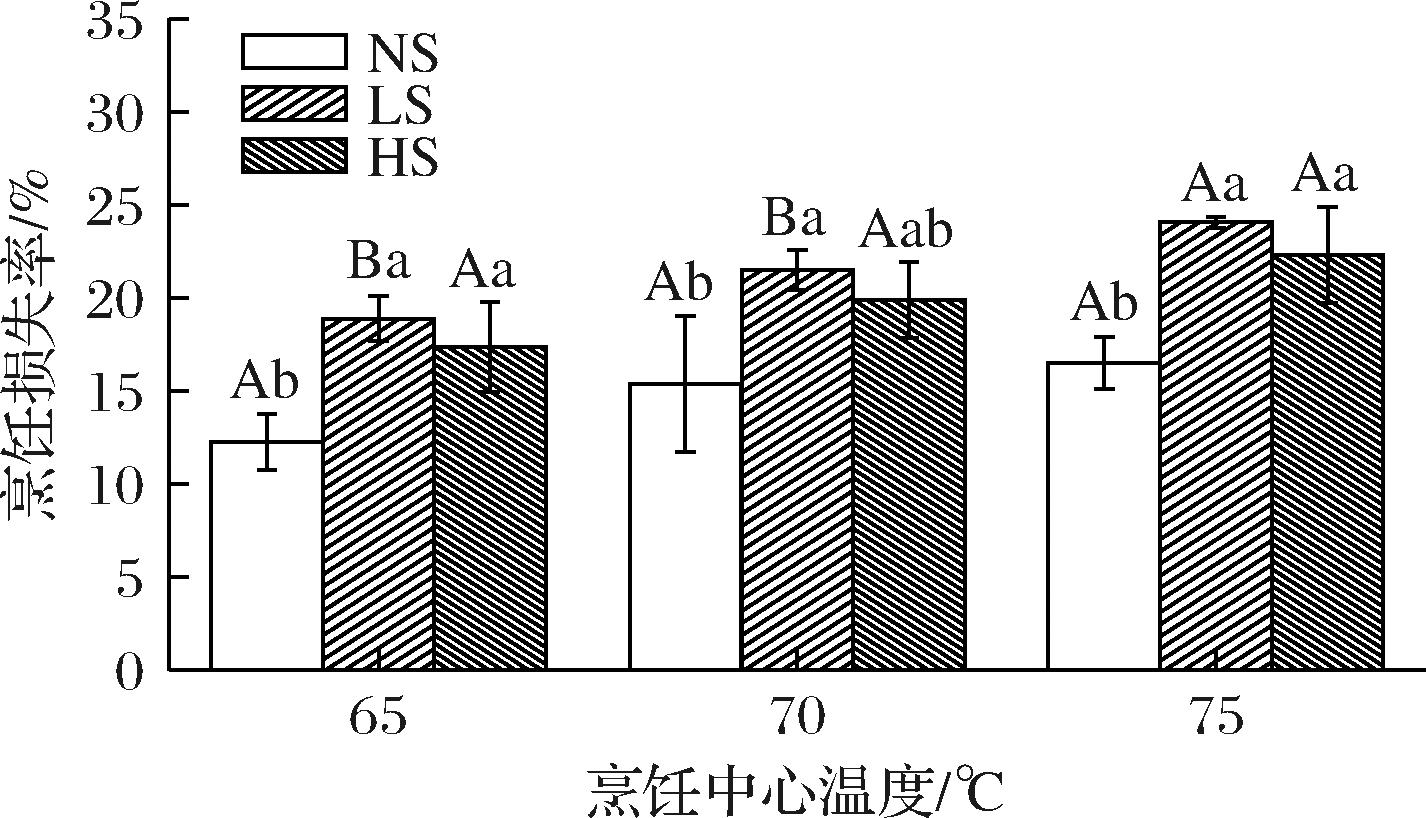
图2 蒸汽辅助烘烤牡蛎的烹饪损失率
Fig.2 Cooking loss rate of steam-assisted roasted oysters
注:大小写字母分别代表不同烹饪中心温度与不同烹饪方式之间的差异显著性(下同)。
2.3 水溶性及盐溶性蛋白含量
可溶性蛋白含量对肉类、水产品蛋白的持水力有潜在影响,可作为其熟制程度的指标[14]。如图3所示,牡蛎水溶性蛋白、盐溶性蛋白含量随烹饪中心温度的升高分别呈先下降后稳定与持续下降的趋势;进一步达到75 ℃时,水溶性蛋白含量则无显著变化。蒸汽辅助烘烤在各个烹饪中心温度的水溶性与盐溶性蛋白含量均较对照低15%~40%,其中HS组牡蛎仅盐溶性蛋白在烹饪中心温度达到65、75 ℃时显著小于LS组(P<0.05)。以上结果表明蒸汽能够促进牡蛎烹饪过程中蛋白质含量下降,推测蒸汽可能具有促进蛋白质变性的作用。
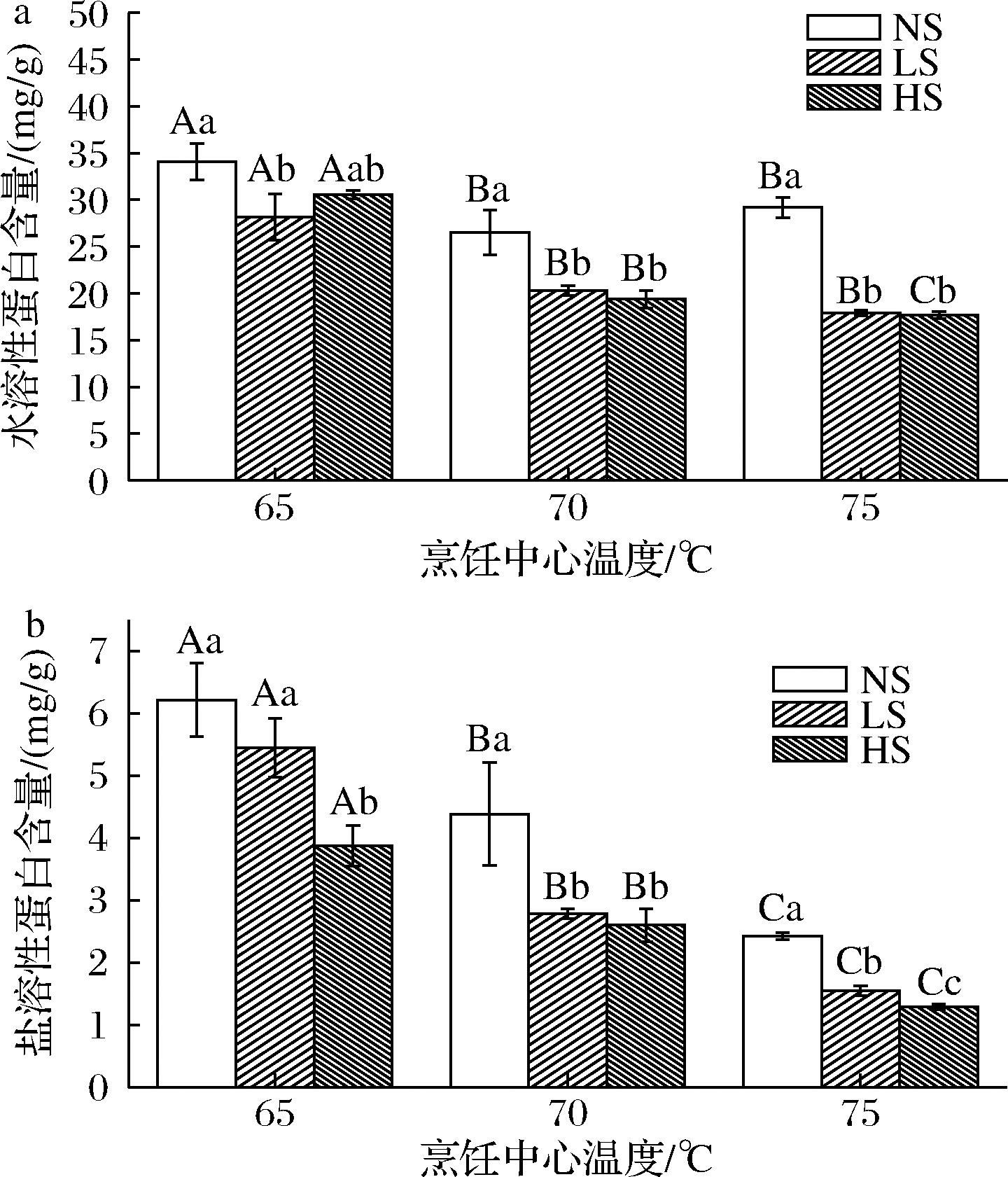
a-水溶性蛋白含量;b-盐溶性蛋白含量
图3 蒸汽辅助烘烤牡蛎水溶性蛋白及盐溶性蛋白的含量
Fig.3 Contents of water-soluble protein and salt-soluble protein in steam-assisted roasted oysters
2.4 羰基含量
在食品热加工过程中,脂肪氧化产物攻击蛋白质侧链并形成羰基,因此羰基是衡量蛋白氧化程度的重要指标[15]。如图4所示,随烹饪中心温度提高,各组牡蛎的羰基含量均显著提高,说明烘烤使牡蛎蛋白氧化程度增加;在65 ℃的烹饪中心温度下,蒸汽辅助烘烤使牡蛎羰基含量显著降低(P<0.05),而烹饪中心温度达到70、75 ℃时,蒸汽辅助烘烤则使牡蛎羰基含量分别产生30%~40%的显著提升(P<0.05),不同烹饪中心温度下LS与HS组均无显著差异(P>0.05)。蒸汽辅助烘烤对牡蛎蛋白羰基的形成可能具有先抑制后促进的作用,推测在较低的烹饪中心温度下,蒸汽相较烘烤对牡蛎传热的贡献更大,因此蒸汽辅助烘烤的传热方式更接近于蒸制,而蒸制是使动物蛋白羰基化程度较小的热处理方式之一[16],而烹饪中心温度较高时,蒸汽促进蛋白氧化,推测较高的湿度可能促进了氧化反应。
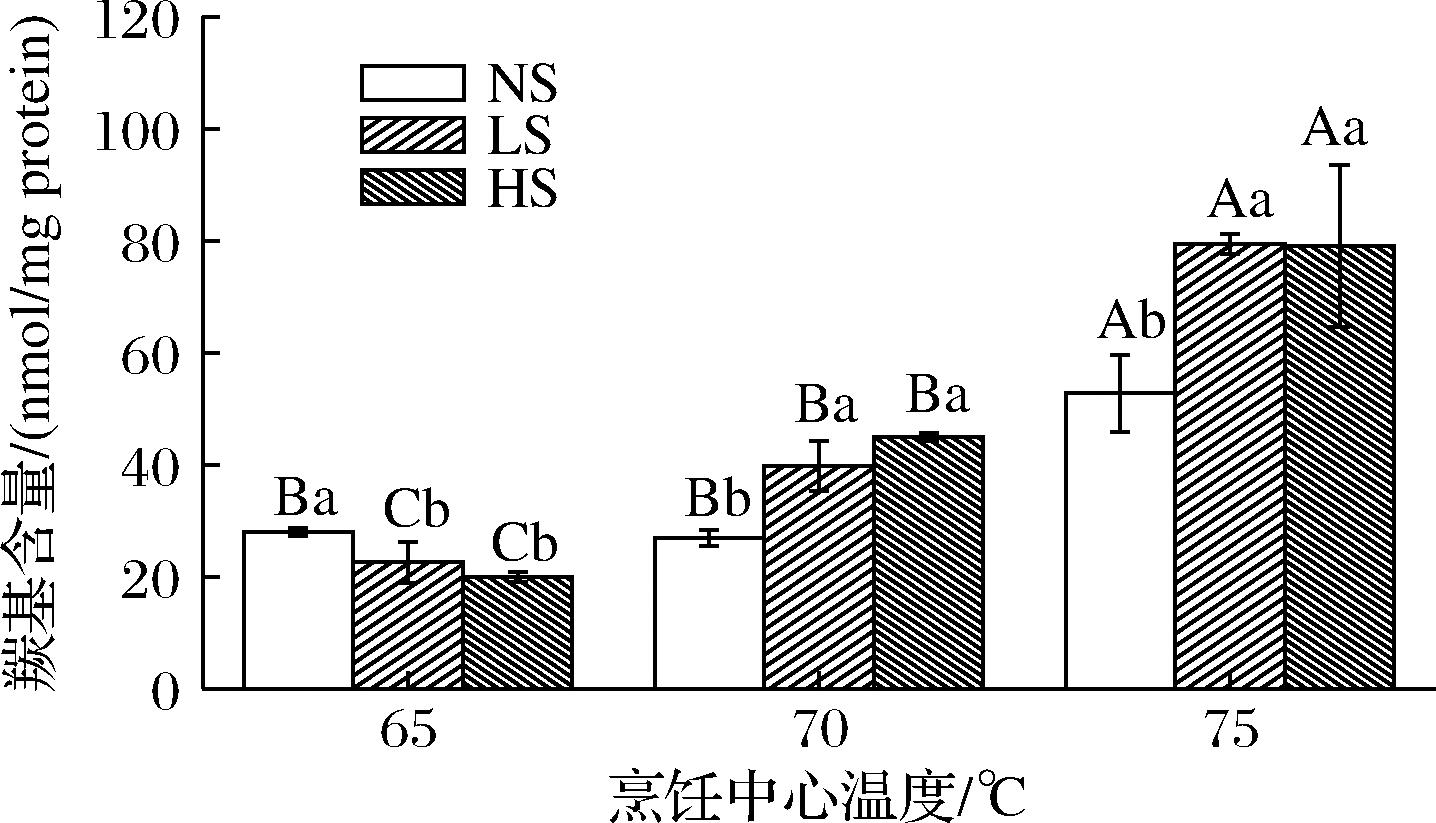
图4 蒸汽辅助烘烤牡蛎的羰基含量
Fig.4 Carbonyl content of steam-assisted roasted oysters
2.5 TBARS值
食品中的脂肪氧化会产生丙二醛(malondialdehyde,MDA),因此其含量(即TBARS值)常用于描述食品中脂肪的氧化程度[17]。如图5所示,随着烹饪中心温度从65 ℃升至70 ℃,不同烹饪方式牡蛎的TBARS值显著增加2倍以上;进一步提升至75 ℃,不同烹饪方式牡蛎的TBARS值继续显著增加但程度较小。在同一烹饪中心温度下,牡蛎TBARS值随蒸汽量增加而显著增加,说明蒸汽辅助烘烤对牡蛎脂肪氧化有促进作用。FENG等[14]研究蒸汽辅助烘烤牛肉得到类似的结果,并推测可能由于蒸汽在牡蛎肉表面凝结成液滴,从而增大传热系数所致。脂肪氧化会产生更丰富的醛、酮等风味物质,但过度氧化会导致其营养价值降低[15]。
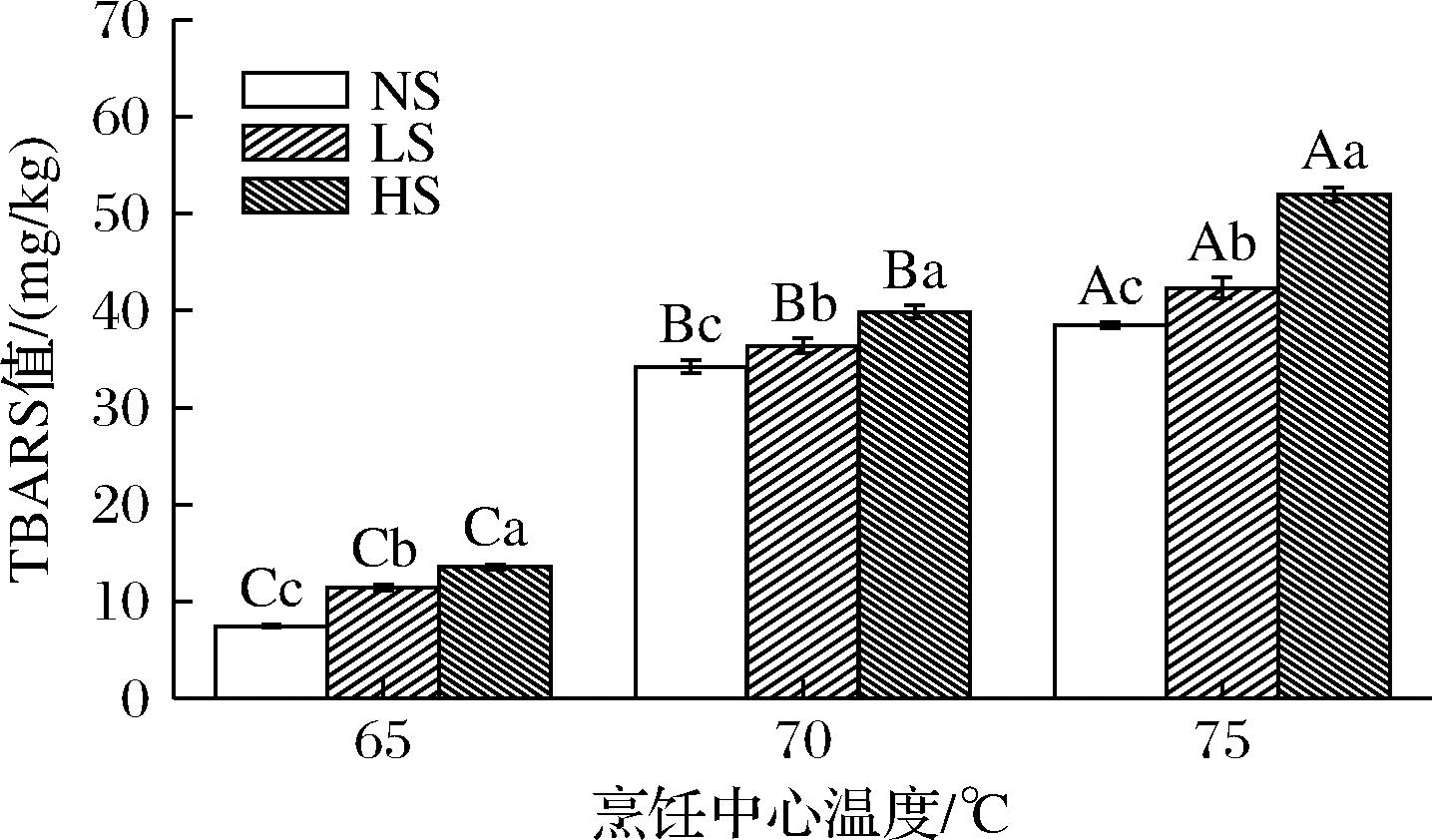
图5 蒸汽辅助烘烤牡蛎的TBARS值
Fig.5 TBARS of steam-assisted roasted oysters
2.6 席夫碱与荧光AGEs含量
席夫碱与荧光AGEs均为水产品烹饪过程中的美拉德反应产物,分别生成于美拉德反应的初始阶段和终末阶段,均具有较强的荧光特性[18]。实验分别使用360 nm与325 nm的激发波长检测席夫碱与荧光AGEs的荧光强度,以表征其含量。席夫碱荧光强度如图6-a所示,本研究分别在440 nm和520 nm处观察到2个明显的荧光峰,这与JIANG等[3]的研究一致;结果显示,当牡蛎烹饪中心温度达到65、70 ℃时,与LS和HS组牡蛎相比,NS组均荧光强度较小,说明相对于传统烘烤,蒸汽辅助烘烤对美拉德反应的早期阶段可能有一定抑制作用;烹饪中心温度达到75 ℃时,LS组的席夫碱含量最高,而NS与HS组牡蛎的席夫碱含量呈下降趋势,并均低于LS组,推测由于产生的席夫碱参与美拉德反应到下一阶段的Amadori重排当中[19]。
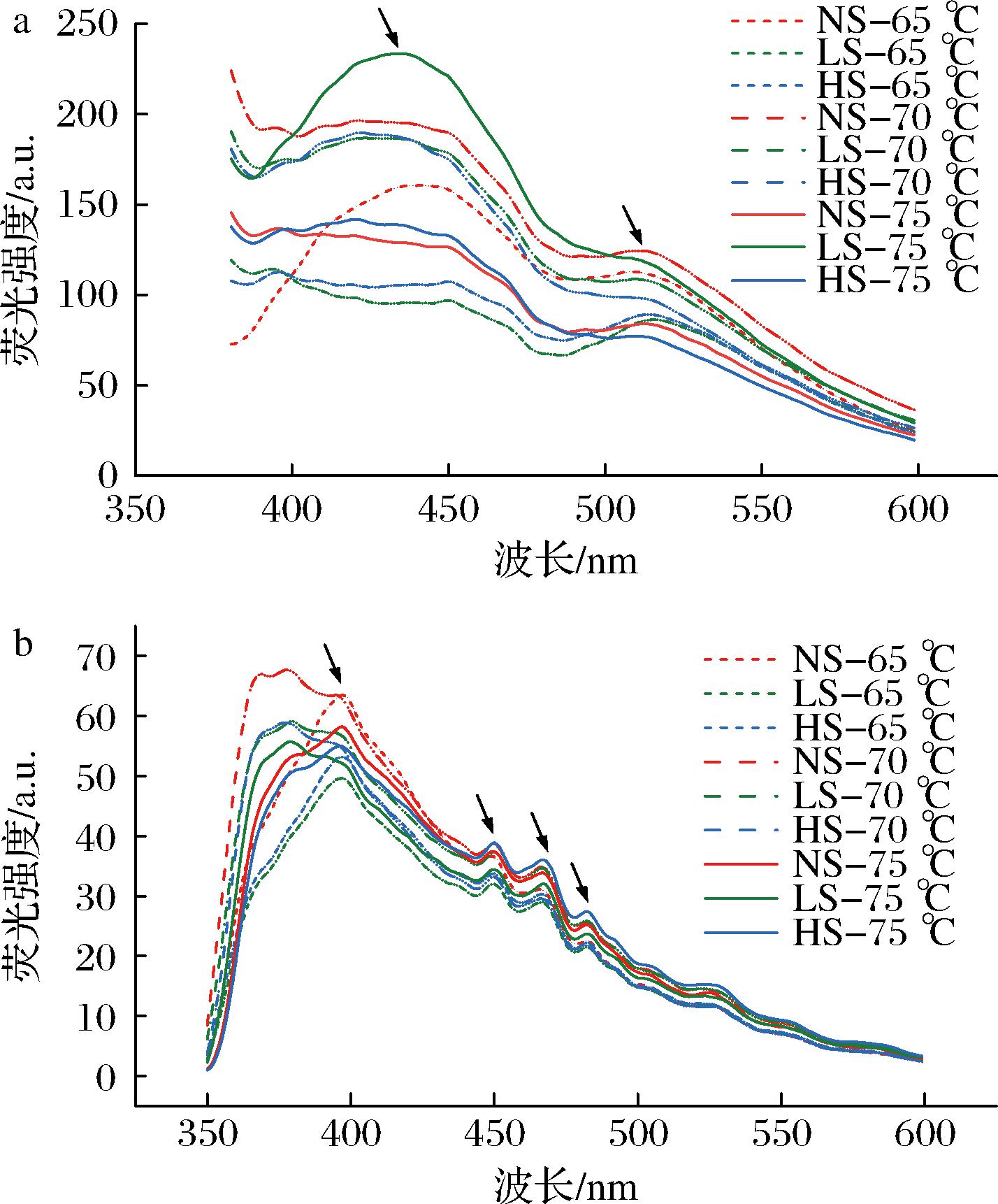
a-席夫碱(激发波长:360 nm);b-荧光AGEs(激发波长:325 nm)
图6 不同处理条件下蒸汽辅助烘烤牡蛎的席夫碱与荧光AGEs荧光强度变化
Fig.6 The fluorescence of the Schiff bass and AGEs under various cooking conditions steam-assisted roasted oysters
荧光AGEs含量如图6-b所示。荧光AGEs在发射波长约为400、450、470及480 nm处产生多个荧光发射。以400 nm处的荧光发射峰为参考,结果显示,在所有烹饪中心温度下,LS组与HS组的荧光强度均低于NS组,进一步证明蒸汽辅助烘烤可抑制牡蛎烹饪过程中的美拉德反应。类似地,3种烹饪方式产生的荧光AGEs含量均随烹饪中心温度的增长呈现先增后减的趋势,这与胡本伦等[20]对油炸鱼饼的研究呈相同趋势,推测可能由于烹饪中心温度较高时生成的荧光AGEs发生聚集、交联等化学反应,可溶性下降导致难以被检测到。
2.7 挥发性风味物质
使用GC-IMS风味分析仪对牡蛎样品的挥发性风味化合物进行鉴定,如图7所示,共检出40种挥发性风味物质,其中包括11种醛,10种酮,9种醇,5种酯类和3种烯,此外还有呋喃、吡嗪类各1种。指纹图谱显示,随着烹饪中心温度升高,大多数醛、酮类物质的信号强度呈现显著上升趋势,如正己醛、(E,E)-2,4-庚二烯醛、2-庚酮等。醛类是脂肪自动氧化降解和不饱和脂肪酸中碳碳双键的氧化产物[21-22],由于具有令人愉悦的气味,如奶油味、水果味、青草味,且阈值低[23],是水产品形成烘烤香气的主要贡献者[24],其中(E,E)-2,4-庚二烯醛是太平洋牡蛎的特征风味物质,该物质特有的坚果香气与脂香对牡蛎整体风具有决定性作用[25];酮类主要来自ω-3不饱和脂肪酸(如二十五碳烯酸、二十二碳六烯酸)的热氧化,以及氨基酸的Strecker降解产物等美拉德反应中间产物[22],是烘烤肉类脂肪味与焦香味的主要来源,本研究检测到2-庚酮、2,3-戊二酮、1-辛烯-3-酮等典型组分,其中2-庚酮、2,3-戊二酮等贡献烘烤肉类脂肪的焦香特征[26];醇类物质来源于醛类、酮类物质的还原及脂质的氧化,其中1-辛烯-3-醇为典型的蘑菇味化合物,是水产品的腥味来源之一[27]。本研究检测到正己醇、正戊醇等直链醇,其中正己醇与牡蛎特征性的青草味高度相关。
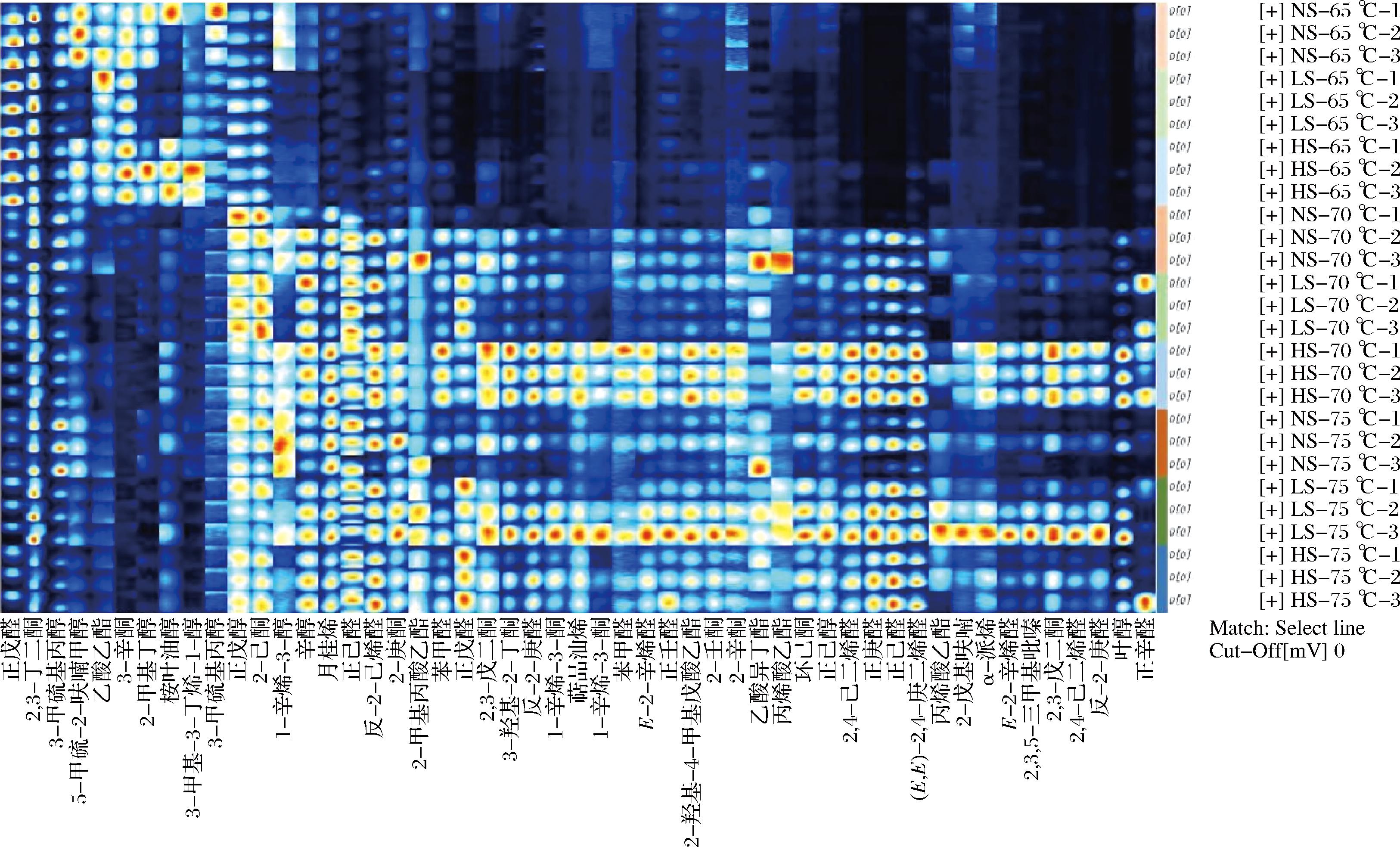
图7 蒸汽辅助烘烤牡蛎的挥发性风味物质指纹图谱
Fig.7 Fingerprint of volatile flavor substances in steam-assisted roasted oysters
在70、75 ℃的烹饪中心温度下,相比对照,蒸汽辅助烘烤使牡蛎产生了更丰富的挥发性风味化合物,其中HS-70 ℃和LS-75 ℃可认为是产生挥发性风味物质最丰富的处理组,而值得注意的是,HS-75 ℃样品并未产生最丰富的挥发性风味物质,这意味着当烘烤程度和蒸汽量同时达到最大时,其挥发性风味物质含量下降,这与郭迅等[15]对牡蛎蒸煮过程中的挥发性风味的研究结果相似,后者结果表明,牡蛎蒸煮过程中产生的醛、酮类物质整体呈先增后减的趋势,推测可能由于生成的挥发性物质进一步降解导致。
PCA结果如图8所示,结果表明,当牡蛎的烹饪中心温度达65 ℃时,不同的烹饪方式对牡蛎的挥发性风味影响相近;值得注意的是,NS-75 ℃与LS-70 ℃,以及LS-75 ℃与HS-70 ℃的挥发性风味特征较为近似,推测可能由于蒸汽通过促进蛋白、脂质氧化,促使牡蛎的挥发性风味在更低的烹饪中心温度下趋近成熟状态,这与前文的牡蛎蛋白羰基含量和TBARS值的测定结果一致。
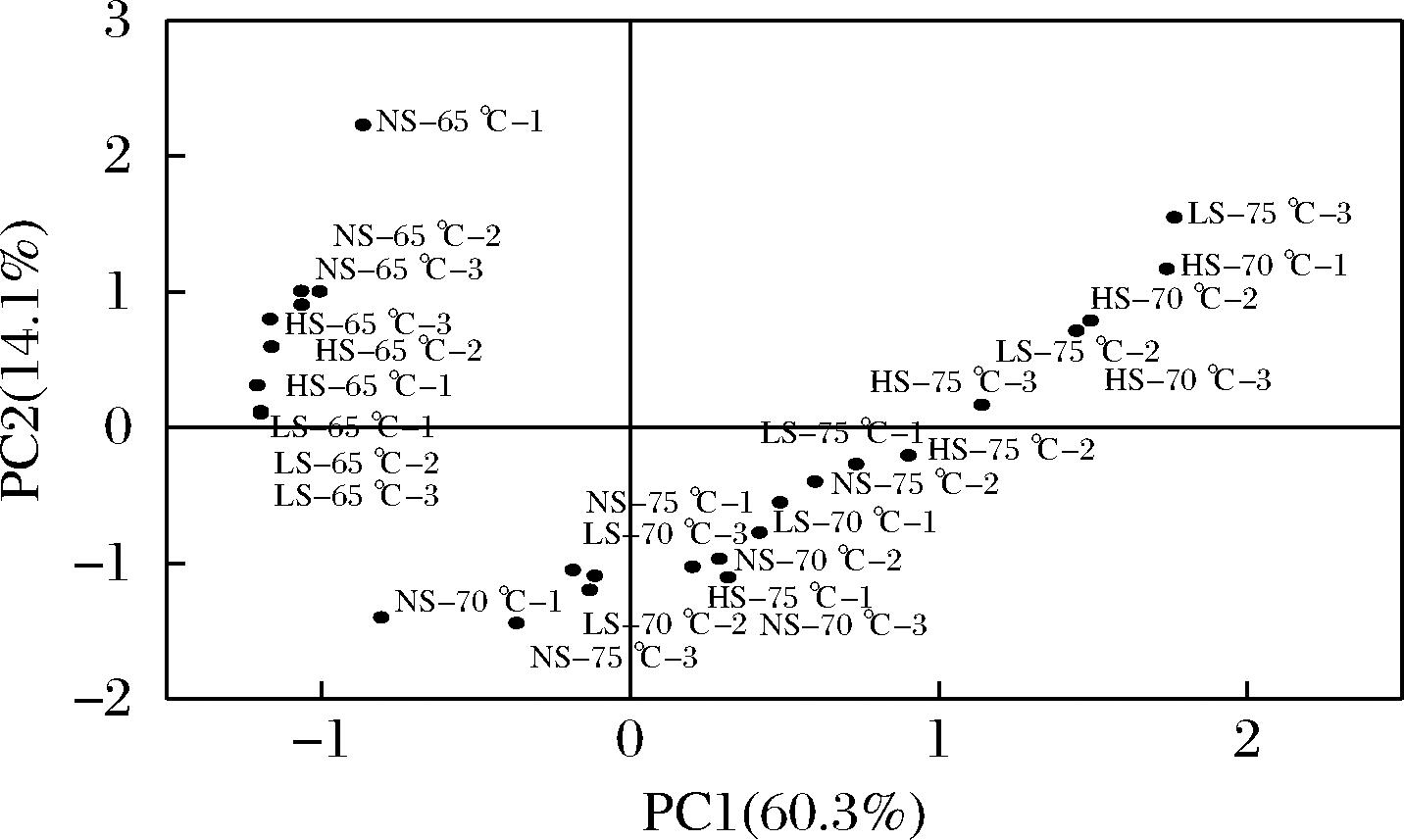
图8 蒸汽辅助烘烤牡蛎的挥发性风味物质主成分分析
Fig.8 PCA of volatile flavor compounds in steam-assisted roasted oysters
3 结论与讨论
本文研究了蒸汽辅助烘烤对牡蛎理化性质、风味和感官品质的影响。结果表明,相比于传统烤箱烘烤,蒸汽辅助烘烤能够缩短烹饪所需时间,但使牡蛎的烹饪损失率增加;蒸汽辅助烘烤使感官评分中的形态、光泽评分升高;达到同一烹饪中心温度时,蒸汽辅助烘烤一定程度上促进牡蛎蛋白质和脂肪的氧化,同时减少席夫碱与荧光AGEs两种美拉德反应产物的产生;蒸汽辅助烘烤牡蛎产生了更为丰富的醛、等挥发性风味物质。可通过蒸汽辅助烘烤,使用50%蒸汽量并将烹饪中心温度控制在70 ℃,从而得到风味、感官品质较好的产品,同时避免蛋白、脂肪过度氧化的负面影响。本研究可为新型烹饪方式在水产品加工中的应用提供参考。
[1] 王丹. 中国渔业统计年鉴:2024[M].北京:中国农业出版社, 2024.
WANG D.2024 China Fishery Statistical Yearbook[M].Beijing:China Agriculture Press, 2024.
[2] FENG C S, TIAN L, JIAO Y D, et al.The effect of steam cooking on the proteolysis of Pacific oyster (Crassostrea gigas) proteins:Digestibility, allergenicity, and bioactivity[J].Food Chemistry, 2022, 379:132160.
[3] JIANG S S, FENG X, ZHANG F, et al.Effects of cooking methods on the Maillard reaction products, digestibility, and mineral bioaccessibility of Pacific oysters (Crassostrea gigas)[J].LWT, 2021, 141:110943.
[4] 林玉锋, 黄后培, 刘嘉怡, 等.不同烹饪方式对牡蛎蛋白质营养品质的影响[J].食品科技, 2020, 45(7):143-151.
LIN Y F, HUANG H P, LIU J Y, et al.Effect of different cooking methods on the nutritional quality of oyster protein[J].Food Science and Technology, 2020, 45(7):143-151.
[5] BARBANTI D, PASQUINI M.Influence of cooking conditions on cooking loss and tenderness of raw and marinated chicken breast meat[J].LWT-Food Science and Technology, 2005, 38(8):895-901.
[6] MORA B, CURTI E, VITTADINI E, et al.Effect of different air/steam convection cooking methods on Turkey breast meat:Physical characterization, water status and sensory properties[J].Meat Science, 2011, 88(3):489-497.
[7] ISLEROGLU H, KEMERLI T, KAYMAK-ERTEKIN F.Effect of steam-assisted hybrid cooking on textural quality characteristics, cooking loss, and free moisture content of beef[J].International Journal of Food Properties, 2015, 18(2):403-414.
[8] ISLEROGLU H, SAKIN-YILMAZER M, KEMERLI-KALBARAN T, et al.Kinetics of colour, chlorophyll, and ascorbic acid content in spinach baked in different types of oven[J].International Journal of Food Properties, 2017, 20(11):2456-2465.
[9] 焦云爽, 王月月, 姜鹏飞, 等.解冻方式对南极磷虾滑品质的影响[J].食品工业科技, 2025, 46(5):309-317.
JIAO Y S, WANG Y Y, JIANG P F, et al.Effect of Different thawing methods on quality changes of prepared Antarctic krill paste[J].Science and Technology of Food Industry, 2025, 46(5):309-317.
[10] 李奥. 多酚烃基酯对油炸牡蛎抗氧化的构效关系及机制[D].大连:大连工业大学:2021.
LI A.The antioxidative structure-activity relationship and mechanism of polyphenol alkyl esters in the process of oyster frying[D].Dalian:Dalian Polytechnic University, 2021.
[11] ZHANG S Q, ZHOU P C, HAN P, et al.Formation of Nε-carboxymethyl-lysine and Nε-carboxyethyl-lysine in heated fish myofibrillar proteins with glucose:Relationship with its protein structural characterization[J].Foods, 2023, 12(5):1039.
[12] 赵玲, 胡梦月, 曹荣, 等.蓝鳍金枪鱼不同部位肌肉的营养与主要风味分析[J].渔业科学进展, 2023, 44(1):219-227.
ZHAO L, HU M Y, CAO R, et al.Analysis of nutrition and major flavor of different muscle parts of Thunnus thynnus[J].Progress in Fishery Sciences, 2023, 44(1):219-227.
[13] MENEZES E A, OLIVEIRA A F, FRANÇA C J, et al.Bioaccessibility of Ca, Cu, Fe, Mg, Zn, and crude protein in beef, pork and chicken after thermal processing[J].Food Chemistry, 2018, 240:75-83.
[14] FENG R H, BAO Y L, LIU D M, et al.Steam-assisted roasting inhibits formation of heterocyclic aromatic amines and alters volatile flavour profile of beef steak[J].International Journal of Food Science &Technology, 2020, 55(9):3061-3072.
[15] 郭迅, 曾名湧, 董士远.牡蛎蒸煮过程中的品质变化[J].食品科学, 2021, 42(5):24-31.
GUO X, ZENG M Y, DONG S Y.Quality changes of oysters during steaming[J].Food Science, 2021, 42(5):24-31.
[16] YU M M, FAN Y C, ZHANG X R, et al.Effect of boiling on texture of abalone muscles and its mechanism based on proteomic techniques[J].Food Chemistry, 2022, 388:133014.
[17] 胡吕霖, 任思婕, 沈清, 等.不同烹饪方式及体外模拟消化环境对鲟鱼蛋白质氧化及消化性的影响[J].食品科学, 2018, 39(20):63-70.
HU L L, REN S J, SHEN Q, et al.Effect of different cooking treatments and in vitro digestion on protein oxidation and digestibility of sturgeon fillets[J].Food Science, 2018, 39(20):63-70.
[18] HU L L, REN S J, SHEN Q, et al.Proteomic study of the effect of different cooking methods on protein oxidation in fish fillets[J].RSC Advances, 2017, 7(44):27496-27505.
[19] SHARMA C, KAUR A, THIND S S, et al.Advanced glycation end-products (AGEs):An emerging concern for processed food industries[J].Journal of Food Science and Technology, 2015, 52(12):7561-7576.
[20] 胡本伦, 武润琳, 孙靖雯, 等.炸制过程中油脂氧化对鱼饼中晚期糖基化终末产物生成的影响[J].中国油脂, 2023, 48(10):81-86.
HU B L, WU R L, SUN J W, et al.Effect of oil oxidation on formation of advanced glycation end products in fish cakes during frying process[J].China Oils and Fats, 2023, 48(10):81-86.
[21] CHAO P C, HSU C C, YIN M C.Analysis of glycative products in sauces and sauce-treated foods[J].Food Chemistry, 2009, 113(1):262-266.
[22] BI S J, XUE C H, WEN Y Q, et al.Comparative study between triploid and diploid oysters (Crassostrea gigas) on non-volatile and volatile compounds[J].LWT, 2023, 179:114654.
[23] VAN HOUCKE J, MEDINA I, LINSSEN J, et al.Biochemical and volatile organic compound profile of European flat oyster (Ostrea edulis) and Pacific cupped oyster (Crassostrea gigas) cultivated in the Eastern Scheldt and Lake Grevelingen, the Netherlands[J].Food Control, 2016, 68:200-207.
[24] CHEN T Y, LI C S, HUANG H, et al.Identification of key physicochemical properties and volatile flavor compounds for the sensory formation of roasted tilapia[J].Food Chemistry, 2024, 460:140636.
[25] LIU S, XU H Q, JIAN S S, et al.Molecular basis of taste and micronutrient content in Kumamoto oysters (Crassostrea sikamea) and Portuguese oysters (Crassostrea angulata) from Xiangshan Bay[J].Frontiers in Physiology, 2021, 12:713736.
[26] LIU H, MA J R, PAN T, et al.Effects of roasting by charcoal, electric, microwave and superheated steam methods on (non)volatile compounds in oyster cuts of roasted lamb[J].Meat Science, 2021, 172:108324.
[27] 杨要芳, 王治军, 宋春勇, 等.热风干制对牡蛎特征风味的影响[J].食品与发酵工业, 2025, 51(7):316-326.
YANG Y F, WANG Z J, SONG C Y, et al.Effect of hot air drying on the characteristic flavor of oysters[J].Food and Fermentation Industries, 2025, 51(7):316-326.