构树(Broussonetia papyrifera)为桑科构属落叶乔木,其叶片(构叶)具有悠久的药食同源应用历史。构叶味甘性凉,富含黄酮和酚类等活性成分,具有凉血、利水等药用功效[1]。食用记载最早见于《毛诗草木鸟兽虫鱼疏》,其中提到“其叶初生可以为茹”。《救荒本草》进一步详述其烹制方法:“采嫩叶炸熟,换水浸洗淘净,以油盐调食。”目前开发的构树叶主要产品包括构叶面、构叶饼干、构叶饮料及构叶茶等,兼具独特风味与营养价值[2]。此外,构叶粗蛋白含量高且氨基酸组成均衡,经发酵后可作为优质饲料,可提升畜禽免疫力并改善肉质[3]。然而,构叶含有单宁等抗营养因子,可能影响其适口性[4];同时,鲜嫩构叶及其加工品因含水量和粗蛋白含量高,在贮藏过程中易引发虫蛀、霉变等问题,导致营养成分流失、货架期缩短[5]。此类问题不仅影响构叶品质,更威胁民众健康。因此,对构叶进行灭菌处理对保障其质量至关重要。
传统食品保鲜技术如高温灭菌或使用化学防腐剂可能会破坏构叶中的营养成分,并且存在化学残留的风险[6]。相比之下,电子束辐照(electron beam irradiation,EBI)作为一种冷灭菌技术,在食品加工中显示出显著优势:适量的EBI能有效杀死病原菌和腐败菌,将微生物数量降低到安全标准以下,同时还具备降解单宁和延长食品保质期的特点[7]。目前,针对构叶的EBI灭菌工艺研究报道较少,辐照对其品质的影响作用尚不明确,导致关键工艺参数缺乏理论依据。
本研究通过探究不同剂量EBI对构叶营养组分、微生物数量、总酚和黄酮等活性物质、单宁含量及抗氧化能力的综合影响,旨在阐明EBI对构叶品质的作用规律,为构叶贮藏加工的辐照工艺提供科学依据。
1 材料与方法
1.1 样品采集
于2024年6月25日在贵州贵阳采集构叶,迅速带入实验室进行包装。
1.2 试验设计
构叶设0、8、10、15、20 kGy 5个不同吸收剂量,以未辐照的构叶做对照,每个剂量设3个重复。样品采用带透气膜聚乙烯袋(规格:20 cm×30 cm;2个直径1 cm透气膜)进行包装,每袋样品100 g。采用贵州雷大辐照科技有限公司的10 MeV、20 kW电子加速器进行辐照加工,束流2 mA,传送带速率分别为3 m/min 和4 m/min。
1.3 材料与试剂
乙腈、甲酸、水(均为色谱纯),赛默飞世尔科技(中国)有限公司;甲酸铵(质谱纯)、氨基酸标准品(纯度>98%)、BC4755-100T/48S DPPH自由基清除能力、BC4775-100T/48S ABTS阳离子自由基清除能力、BC1310总抗氧能力检测试剂盒,北京索莱宝科技有限公司;福林酚溶液(纯度>99%),上海源叶生物科技有限公司;聚乙烯袋、透气膜,贵州鑫盛瑞生物科技有限公司;G0119W单宁含量试剂盒、G01256W48羟自由基清除能力试剂盒,苏州格锐思生物科技有限公司。
1.4 仪器与设备
GR60SA高压灭菌锅,厦门致微仪器有限公司;IGS60恒温培养箱,德国赛默飞世尔科技公司;WGL-125B鼓风干燥箱,天津泰斯特仪器有限公司;FW100高速粉碎机,天津泰斯特仪器有限公司;Rapid N exceed杜马斯定氮仪,德国元素Elementar公司;ANKOM-2000i纤维分析仪,美国ANKOM科技公司;QTRAP® 6500+质谱仪,美国AB SCIEX公司。
1.5 试验方法
1.5.1 营养成分分析
称取20.0 g样品,置于65 ℃鼓风干燥箱中烘干至恒重,计算干物质含量(dry matter,DM)。烘干样品用小型高速粉碎机粉碎过1 mm筛。采用硫酸-蒽酮比色法测定水溶性碳水化合物含量,采用杜马斯定氮仪测定粗蛋白含量,采用全自动纤维分析仪测定中性洗涤纤维和酸性洗涤纤维含量,结果以干物质基础表示[8]。
1.5.2 氨基酸含量测定
采用ExionLC AD液相系统与QTRAP® 6500+质谱仪联用对样本氨基酸含量进行分析,该分析由上海美吉生物医药科技有限公司完成。标准品配制:精确称取21种氨基酸标品各10 mg,加0.1 mol/L HCl溶液溶解并定容至1 mL,涡旋混匀,即标准品储备溶液。色谱条件:AdvanceBio MS Spent Media(2.1 mm×50 mm, 2.7 μm)色谱柱,柱温40 ℃,进样量1 μL,流速0.5 mL/min。质谱条件:采用正模式检测,帘式气体35 psi,碰撞气体为中等强度,雾化气和辅助气均为50 psi。离子喷雾电压+5 500 V,离子源温度550 ℃[9]。
1.5.3 活性成分及抗营养因子测定
总黄酮含量采用NaNO2-Al(NO3)3-NaOH 显色法测定[10]。总酚含量采用福林酚法[11]进行测定;单宁含量:采用单宁含量试剂盒(G0119W)测定。
1.5.4 抗氧化活性测定
采用DPPH自由基清除能力、ABTS阳离子自由基清除能力和总抗氧能力(total antioxidant capacity,T-AOC)检测试剂盒检测样品的DPPH自由基清除能力、ABTS阳离子自由基清除能力和T-AOC;采用羟自由基清除能力试剂盒检测样品的羟自由基(·OH)清除能力。
1.5.5 微生物数量测定
称取10.0 g样品,加入90 mL无菌生理盐水(质量分数0.85%),4 ℃、150 r/min振荡1 h后吸取1 mL菌液用于微生物计数,对滤液进行梯度稀释,采用平板培养法对乳酸菌、酵母菌、霉菌、肠杆菌及好氧菌的数量进行微生物计数[8]。微生物数据以lg CFU/g表示,并以构叶鲜重(fresh weight,FW)为基础。
1.6 数据处理
采用SAS 9.3(SAS Institute Inc.Cary, NC)软件对试验数据进行单因素方差分析(Ono-way ANOVA),结果表示为“平均值±标准差”,并用Tukey’s多重比较来分析数据平均值之间的差异(P<0.05),使用Origin 2024软件绘图。
2 结果与分析
2.1 辐照处理对构叶营养成分及微生物数量的影响
由表1可知,EBI对构叶DM、中性洗涤纤维、酸性洗涤纤维、水溶性碳水化合物及粗蛋白含量均无显著影响(P>0.05),这一现象与黄芪、杜仲叶及玉米等植物材料的辐照研究结果一致[12-14]。构叶营养成分的稳定性可能与其水分结合状态及低剂量辐照对细胞壁的物理保护有关[15-16]。
表1 不同辐照剂量处理对构叶营养品质及微生物数量的影响
Table 1 Effects of different radiation doses on nutrient quality and microbial quantity of B.papyrifera leaves
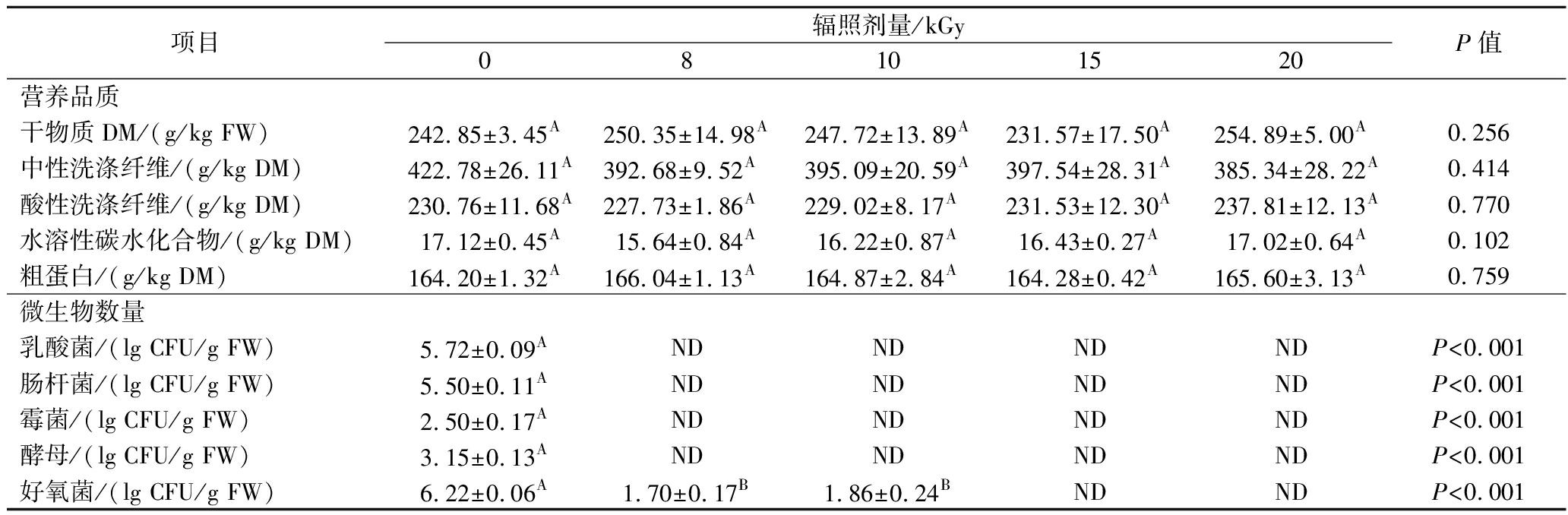
项目辐照剂量/kGy08101520P值营养品质干物质DM/(g/kg FW)242.85±3.45A250.35±14.98A247.72±13.89A231.57±17.50A254.89±5.00A0.256中性洗涤纤维/(g/kg DM)422.78±26.11A392.68±9.52A395.09±20.59A397.54±28.31A385.34±28.22A0.414酸性洗涤纤维/(g/kg DM)230.76±11.68A227.73±1.86A229.02±8.17A231.53±12.30A237.81±12.13A0.770水溶性碳水化合物/(g/kg DM)17.12±0.45A15.64±0.84A16.22±0.87A16.43±0.27A17.02±0.64A0.102粗蛋白/(g/kg DM)164.20±1.32A166.04±1.13A164.87±2.84A164.28±0.42A165.60±3.13A0.759微生物数量乳酸菌/(lg CFU/g FW)5.72±0.09ANDNDNDNDP<0.001肠杆菌/(lg CFU/g FW)5.50±0.11ANDNDNDNDP<0.001霉菌/(lg CFU/g FW)2.50±0.17ANDNDNDNDP<0.001酵母/(lg CFU/g FW)3.15±0.13ANDNDNDNDP<0.001好氧菌/(lg CFU/g FW)6.22±0.06A1.70±0.17B1.86±0.24BNDNDP<0.001
注:同行数据不同字母表示差异显著(P<0.05);ND表示未检出(下同)。
EBI对构叶中微生物的灭活效应呈现显著剂量依赖性规律。随着辐照剂量从0 kGy提升至8 kGy,乳酸菌、肠杆菌、霉菌及酵母数量呈指数级下降并被完全灭活,其原因可能为高能电子束直接破坏微生物DNA双链结构并抑制关键酶活性[17]。黄芪经4~8 kGy EBI可彻底杀灭需氧菌、霉菌和酵母菌[12],杜仲叶研究显示仅需4 kGy剂量即可达到同等灭菌效果[13],表明材料特性与微生物群落组成的差异会显著影响辐照剂量需求。BA则展现出更强的辐照抗性,在8~10 kGy剂量下仍残存1.70~1.86 lg CFU/g FW,这可能与其形成芽孢和细胞壁结构更复杂密切相关[18]。当剂量提升至15~20 kGy时,构叶中所有微生物均被彻底灭活,这一剂量规律为辐照技术在构叶灭菌中的应用提供了理论参考。
2.2 辐照处理对构叶氨基酸含量的影响
氨基酸是蛋白质的基本构成物质,由表2可知,构叶中含有18种氨基酸,EBI对构叶甘氨酸含量无显著影响(P>0.05),可能因为甘氨酸是唯一不含侧链的氨基酸(仅含氨基和羧酸基团),其分子结构简单且化学键稳定,相较于芳香族氨基酸甘氨酸的化学键对辐照诱导的自由基攻击具有更强的抗性[19]。
表2 不同辐照剂量处理对构叶氨基酸含量的影响 单位:mg/kg DM
Table 2 Effects of different irradiation doses on amino acid content in B.papyrifera leaves
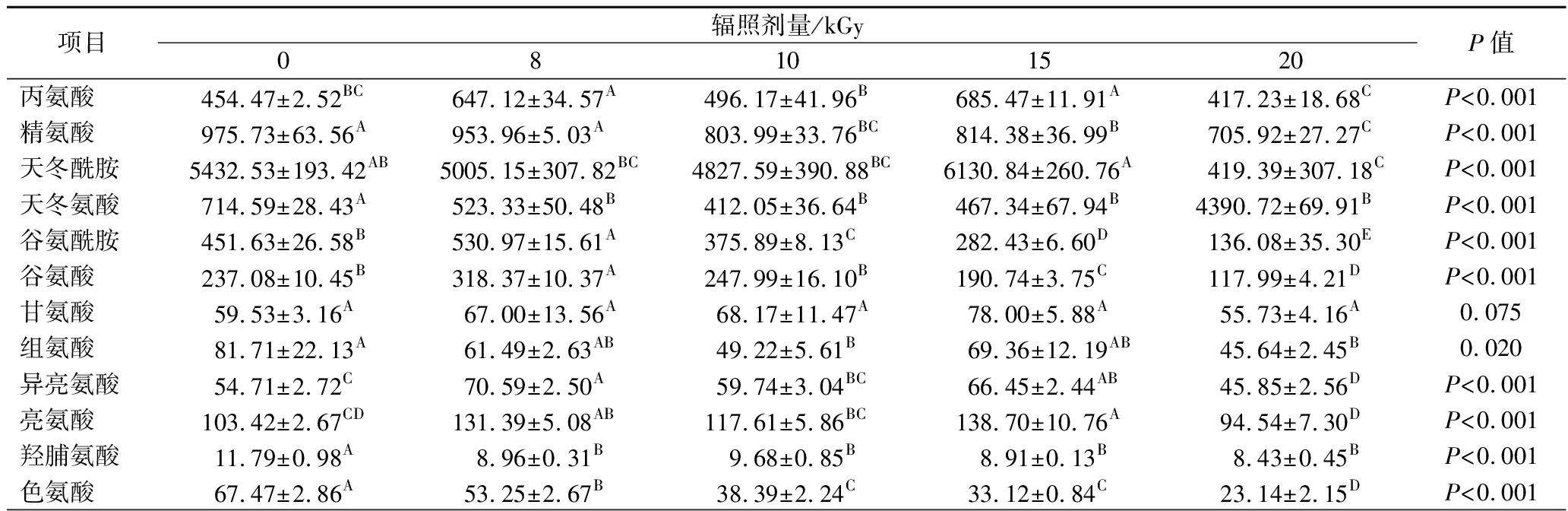
项目辐照剂量/kGy08101520P值丙氨酸454.47±2.52BC647.12±34.57A496.17±41.96B685.47±11.91A417.23±18.68CP<0.001精氨酸975.73±63.56A953.96±5.03A803.99±33.76BC814.38±36.99B705.92±27.27CP<0.001天冬酰胺5432.53±193.42AB5005.15±307.82BC4827.59±390.88BC6130.84±260.76A419.39±307.18CP<0.001天冬氨酸714.59±28.43A523.33±50.48B412.05±36.64B467.34±67.94B4390.72±69.91BP<0.001谷氨酰胺451.63±26.58B530.97±15.61A375.89±8.13C282.43±6.60D136.08±35.30EP<0.001谷氨酸237.08±10.45B318.37±10.37A247.99±16.10B190.74±3.75C117.99±4.21DP<0.001甘氨酸59.53±3.16A67.00±13.56A68.17±11.47A78.00±5.88A55.73±4.16A0.075组氨酸81.71±22.13A61.49±2.63AB49.22±5.61B69.36±12.19AB45.64±2.45B0.020异亮氨酸54.71±2.72C70.59±2.50A59.74±3.04BC66.45±2.44AB45.85±2.56DP<0.001亮氨酸103.42±2.67CD131.39±5.08AB117.61±5.86BC138.70±10.76A94.54±7.30DP<0.001羟脯氨酸11.79±0.98A8.96±0.31B9.68±0.85B8.91±0.13B8.43±0.45BP<0.001色氨酸67.47±2.86A53.25±2.67B38.39±2.24C33.12±0.84C23.14±2.15DP<0.001
续表2

项目辐照剂量/kGy08101520P值赖氨酸98.10±7.63C151.33±21.31A140.32±14.25AB165.47±18.42A110.85±7.45BC0.001苯丙氨酸38.89±0.46B50.76±2.64A41.29±2.24B53.35±2.70A37.71±2.17BP<0.001脯氨酸742.12±18.75AB690.51±29.73BC662.06±34.12CD791.80±3.14A593.93±40.56DP<0.001苏氨酸150.48±12.69B181.59±1.38A152.66±5.38B146.84±4.92B117.50±2.90CP<0.001酪氨酸42.47±1.46A24.08±3.96B15.71±0.94C18.55±0.22BC13.85±1.84CP<0.001缬氨酸114.97±3.43B150.03±6.84A127.88±6.76B128.21±6.72B91.45±3.84CP<0.001
EBI(0~20 kGy)对构叶中除甘氨酸外的所有氨基酸组成均有显著影响(P<0.05)。色氨酸含量随剂量增加持续下降,这可能归因于其苯环结构对辐照自由基高度敏感,易发生氧化断裂[20]。谷氨酰胺、谷氨酸及苏氨酸的含量在8 kGy时因蛋白质二级结构破坏而短暂上升[21],但在8 kGy以上剂量时,则因其羧基或β-羟基发生氧化降解而下降[22-23]。精氨酸、天冬酰胺、天冬氨酸、组氨酸、脯氨酸和酪氨酸含量在15 kGy及羟脯氨酸含量在10 kGy出现短暂上升,推测与辐照诱导的蛋白质交联暂时保护作用有关[24]。而当剂量达到20 kGy时,交联结构被破坏并伴随氧化分解,最终导致其含量下降[25]。丙氨酸、异亮氨酸、亮氨酸、赖氨酸、苯丙氨酸和缬氨酸的含量随辐照剂量增加呈现非线性波动:在低剂量(0~8 kGy)下可能因ROS激活抗氧化系统而上升[21],随后在剂量升高至8~10 kGy时,抗氧化能力耗尽及支链氨基酸β-羟基氧化导致其含量下降[26];在10~15 kGy辐照范围下,蛋白质降解释放氨基酸,但同时自由基链式反应加剧,最终生成大量酮酸、挥发性醛类等终产物,导致含量复杂变化,最终在20 kGy时含量整体下降[27]。
有研究发现EBI对玉米(3~5 kGy)和扒鸡(6.5 kGy)氨基酸总量无显著影响[14,28],证实在<8 kGy剂量范围内辐照对氨基酸的稳定性具有普适性,而>8 kGy可能会显著影响氨基酸含量变化,该剂量规律为辐照技术在构叶加工中的应用提供了科学参考。
2.3 辐照处理对构叶构叶活性物质及单宁含量的影响
由图1可知,辐照强度显著影响构叶总黄酮、总酚及单宁含量(P<0.05)。未辐照组总黄酮含量为15.31 g/kg DM,随辐照剂量增加呈线性下降至20 kGy时的1.74 g/kg。这一趋势与EBI诱导黄酮类化合物氧化降解的机制一致,可能与自由基直接攻击黄酮骨架的C环导致羟基化或断裂有关[29]。程竹林等[16]发现枸杞黄酮含量在0~10 kGy辐照剂量下持续下降,印证了辐照对黄酮类化合物的破坏效应。而黄芪在4~10 kGy剂量下黄酮含量亦保持稳定[12],这表明不同植物材料中的黄酮类化合物对辐照的敏感性存在差异。
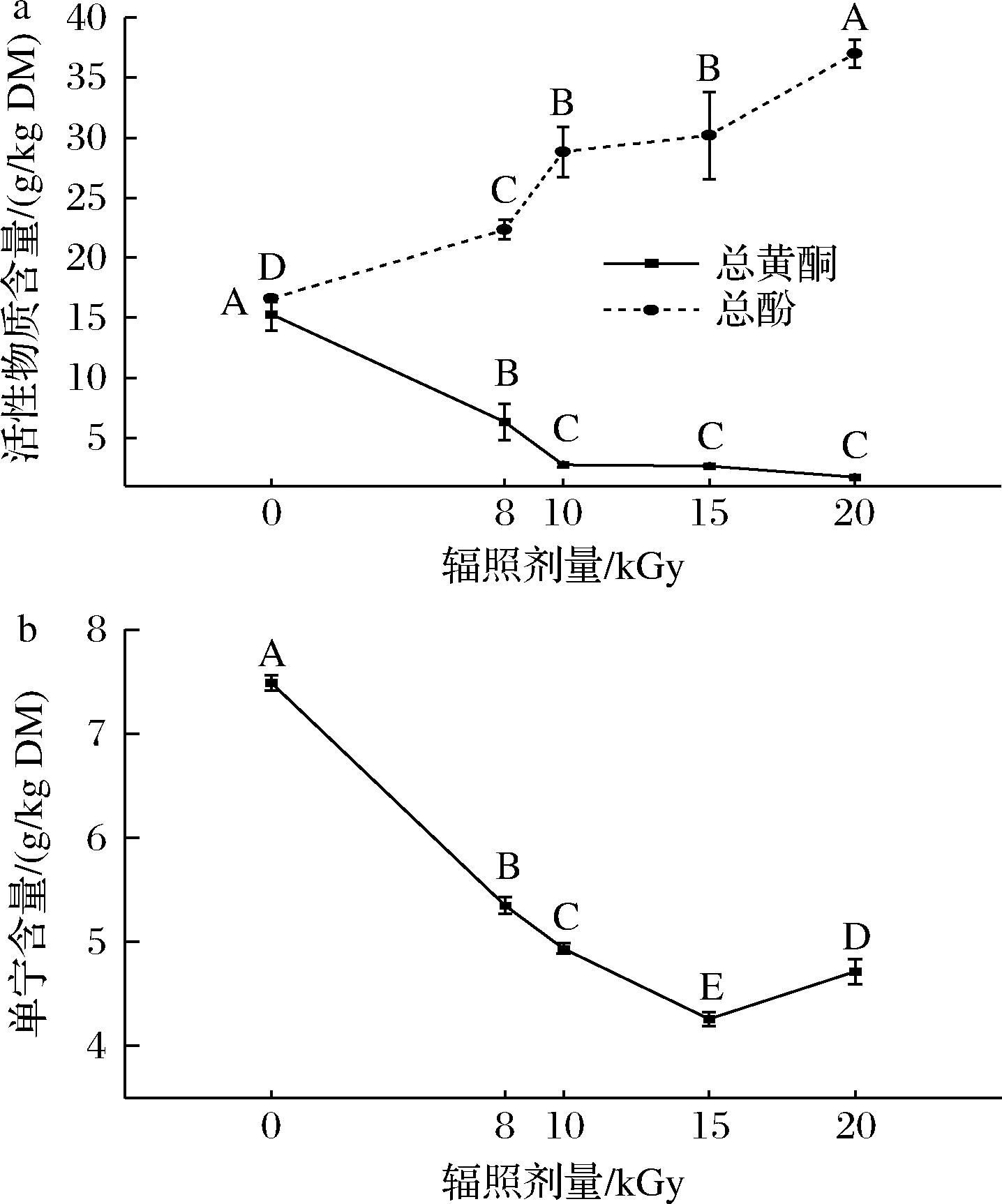
a-活性物质;b-单宁
图1 不同辐照剂量处理对构叶活性物质及单宁含量的影响
Fig.1 Effects of different radiation doses on active substances and tannin content in B.papyrifera leaves
注:不同字母表示差异显著(P<0.05)(下同)。
未辐照组构叶总酚含量为16.29 g/kg DM,随辐照剂量增加显著上升至20 kGy时的36.99 g/kg DM。该现象提示辐照促进酚类物质积累可能有两方面因素:一方面,EBI激活苯丙烷代谢通路关键酶(如苯丙氨酸解氨酶)促进酚类前体合成[30];另一方面,辐照诱导的膜脂过氧化可破坏细胞膜通透性,促进结合态酚类物质的溶出[31]。
构叶单宁含量在EBI下呈现非线性变化:未辐照组为7.49 g/kg DM,在15 kGy剂量时降至最低值4.26 g/kg DM,20 kGy时小幅回升至5.2 g/kg DM。15 kGy可能为氧化降解与保护性缩合反应的动态平衡阈值:<15 kGy辐照产生的·OH优先攻击单宁酚羟基和共轭双键,导致缩合型单宁的氧化断裂[32];而>15 kGy辐照可能形成稳定的寡聚态中间体“亚缩合单宁”,这类结构通过非酶促聚合抵抗自由基攻击,从而减缓降解速率[33]。
2.4 辐照处理对构叶抗氧化活性的影响
由图2可知,构叶的ABTS阳离子自由基和DPPH自由基清除能力随辐照剂量(0~20 kGy)增加均呈显著剂量依赖性下降(P<0.05),在20 kGy时分别降至23.32%和2.43%。该同步下降现象很可能与高剂量辐照诱导的活性氧(reactive oxygen species,ROS)爆发及抗氧化成分结构破坏有关:高能电子束产生的·OH自由基直接攻击抗氧化物质的共轭双键或羟基,导致自由基生成速率超过内源性抗氧化系统的清除阈值,引发系统性失衡使其清除能力持续降低[34]。尽管辐照过程中总酚含量有所增加,但由于其清除机制主要依赖电子转移(electron transfer,ET),而同时降解的黄酮类物质兼具ET与氢原子转移功能,因此总酚的积累难以完全弥补黄酮损失对ABTS阳离子自由基/DPPH自由基清除能力造成的负面影响[35-36]。
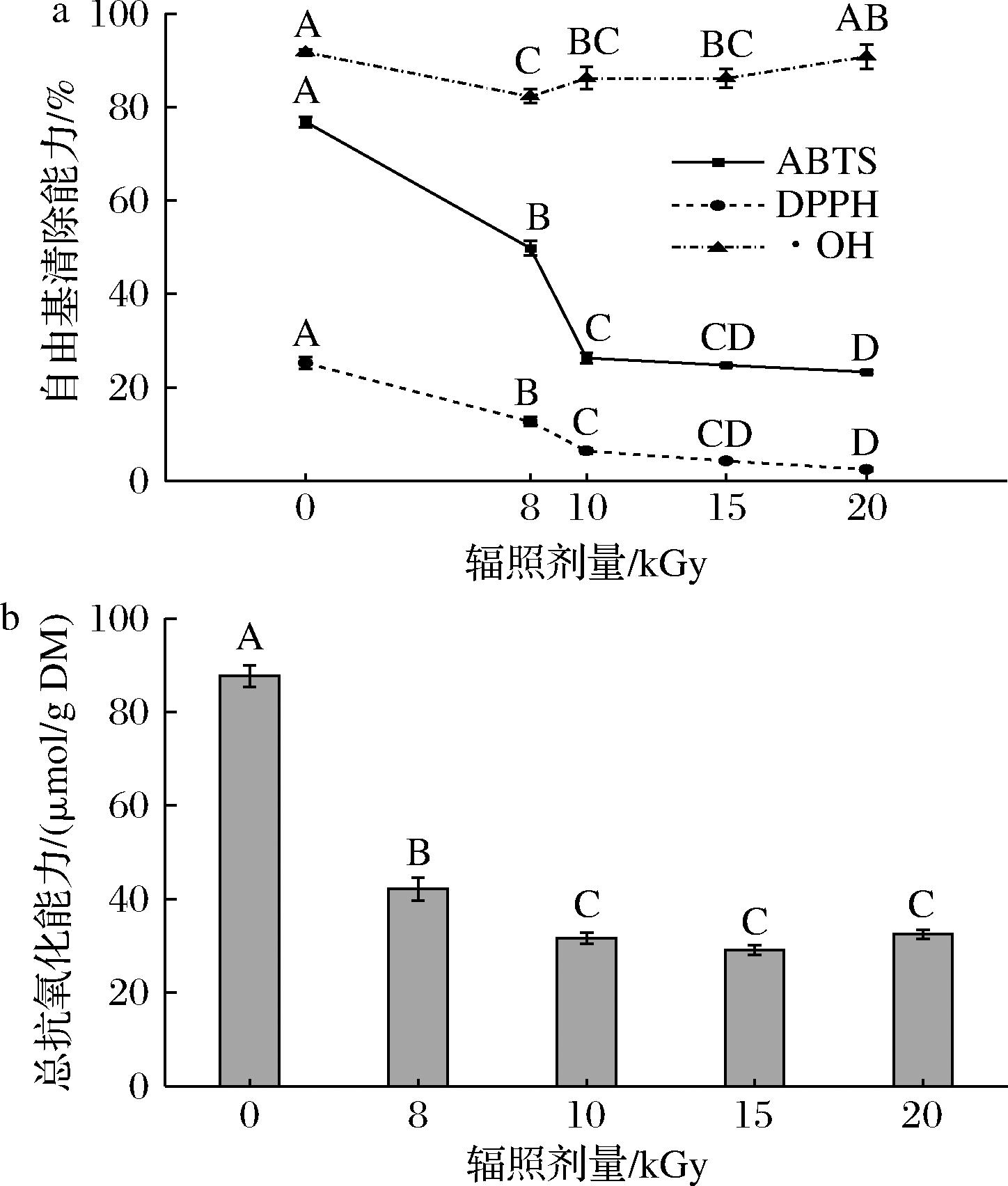
a-自由基清除能力;b-总抗氧化能力
图2 不同辐照剂量处理对构叶抗氧化活性的影响
Fig.2 Effects of different radiation doses on antioxidant activity of B.papyrifera leaves
·OH清除能力呈现先降后升的趋势。在0~8 kGy剂量区间,清除能力下降10.22%,这可能与ABTS阳离子自由基、DPPH自由基清除率下降原因类似,即辐照初期·OH对抗氧化物质的攻击导致清除能力受损[34]。而在8 kGy以上剂量时,清除能力出现上升,这可能与辐照触发的抗氧化酶(如谷胱甘肽还原酶)活性短暂上调以及高剂量辐照破坏细胞膜脂结构,促进结合态酚类物质释放有关[37-38]。T-AOC在辐照后整体下降,与ABTS和DPPH的趋势一致。T-AOC在15 kGy时达最低值(29.10 μmol/g DM),这很可能反映了酶促系统(SOD/CAT)与非酶系统(维生素C、谷胱甘肽)协同保护作用的减弱及黄酮持续降解的影响[39]。而在20 kGy时T-AOC小幅回升可能与高剂量辐照诱导的膜损伤及结合态酚释放有关[40]。
3 结论
在0~20 kGy EBI范围内,构叶的主要营养成分保持稳定,但单宁含量有所下降。其抗氧化性能呈现下降趋势,具体表现为ABTS阳离子与DPPH自由基清除能力降低、总抗氧化活性减弱。从营养保存角度考虑,当构叶需保持氨基酸结构完整时,建议将辐照剂量控制在8 kGy以内;若以灭菌效果为首要目标,则适宜采用15~20 kGy的辐照剂量。本研究的主要局限在于未能细致划分0~8 kGy的低剂量辐照区间,以致无法精准确定既能有效抑制构叶病原微生物,又能最大限度保留有益菌群及其抗氧化功能的最佳辐照参数。后续研究需建立更为精细的剂量梯度,全面评估对构叶不同微生物及抗氧化活性的作用规律。
[1] 秦超燕, 宁带连.构树化学成分及药理作用研究进展[J].世界最新医学信息文摘, 2019, 19(96):66-67.
QIN C Y, NING D L.Research progress on chemical constituents and pharmacological effects of Broussonetia papyrifera[J].World Latest Medicine Information, 2019, 19(96):66-67.
[2] 胡艳敏, 熊伟, 沈世华.舌尖上的杂交构树[J].生命世界, 2018(10):32-35.
HU Y M, XIONG W, SHEN S H.Hybrid Broussonetia papyrifera on the tip of the tongue[J].Life World, 2018(10):32-35.
[3] 蔡玉, 陈国顺, 支喜军, 等.构树发酵饲料在猪禽养殖中的应用研究进展[J].畜牧兽医杂志, 2019, 38(1):41-45.
CAI Y, CHEN G S, ZHI X J, et al.Research progress on the application of Broussonetia papyrifera fermented feed in pigs and poultry breeding[J].Journal of Animal Science and Veterinary Medicine, 2019, 38(1):41-45.
[4] HE Q, ZHOU W, CHEN X Y, et al.Chemical and bacterial composition of Broussonetia papyrifera leaves ensiled at two ensiling densities with or without Lactobacillus plantarum[J].Journal of Cleaner Production, 2021, 329:129792.
[5] 卢伟,侯茂林,黎家文.植物营养对植食性昆虫行为与发育的影响[C].科技创新与绿色植保—中国植物保护学会2006学术年会论文集.昆明:中国植物保护学会,2006.
LU W, HOU M L, LI J W.The influence of plant nutrition on the behavior and development of herbivorous Insects[C].Technological Innovation and Green Plant Protection- Proceedings of the 2006 Academic Annual Conference of the Chinese Society for Plant Protection.Kunming:Chinese Society for Plant Protection,2006.
[6] WANG S, LIN S Y, LI S, et al.Effects of different thermal sterilization conditions on the quality of ready-to-eat shrimp based on specific sterilization intensity[J].Food Chemistry, 2024, 450:139359.
[7] 崔龙, 李庆鹏, 周瑞琴, 等.电子束辐照对饼粕类饲料中抗营养因子的影响[J].核农学报, 2017, 31(4):696-701.
CUI L, LI Q P, ZHOU R Q, et al.Effect of electron beam irradiation on anti-nutrition factors in cake meal feed[J].Journal of Nuclear Agricultural Sciences, 2017, 31(4):696-701.
[8] 杨鑫. 海拔梯度对高山嵩草和燕麦叶际微生物及其发酵特性的影响研究[D].南京:南京农业大学, 2022.
YANG X.Effects of altitude gradient on phyllospheric microorganisms and their fermentation characteristics of Kobresia pygmafa and Avena sativa L.[D].Nanjing:Nanjing Agricultural University, 2022.
[9] FERRÉ S, GONZ LEZ-RUIZ V, GUILLARME D, et al.Analytical strategies for the determination of amino acids:Past, present and future trends[J].Journal of Chromatography B, 2019, 1132:121819.
LEZ-RUIZ V, GUILLARME D, et al.Analytical strategies for the determination of amino acids:Past, present and future trends[J].Journal of Chromatography B, 2019, 1132:121819.
[10] 李金芳, 张守芳, 李丽丹, 等.NaNO2-Al(NO3)3-NaOH比色法测定乳苣不同部位总黄酮含量研究[J].食品与营养科学, 2022, 11(1):36-43.
LI J F, ZHANG S F, LI L D, et al.Determination of total flavonoids in different parts of Chicory by NaNO2-Al(NO3)3-NaOH colorimetry[J].Journal of Food and Nutrition Science, 2022, 11(1):36-43.
[11] LI X C, WU X T, HUANG L.Correlation between antioxidant activities and phenolic contents of radix Angelicae sinensis (Danggui)[J].Molecules, 2009, 14(12):5349-5361.
[12] 王良才, 王海军, 刘秉坤, 等.高能电子束辐照灭菌对黄芪品质的影响[J].核农学报, 2025, 39(5):953-960.
WANG L C, WANG H J, LIU B K, et al. Effects of high energy electron beam irradiation sterilization on quality of astragali radix[J].Journal of Nuclear Agricultural Sciences, 2025, 39(5):953-960.
[13] 唐艺文, 陈谦, 王钢, 等.高能电子束辐照对杜仲叶品质的影响研究[J].核农学报, 2023, 37(5):962-970.
TANG Y W, CHEN Q, WANG G, et al.Effect of electron-beam irradiation on quality of Eucommia ulmoides leaves[J].Journal of Nuclear Agricultural Sciences, 2023, 37(5):962-970.
[14] 郭东权, 王娴, 董威杰, 等.电子束辐照对玉米品质及赭曲霉毒素A降解效果的探讨[J].中国粮油学报, 2018, 33(5):76-81.
GUO D Q, WANG X, DONG W J, et al.Effects of electron beam irradiation on corn quality and degradation of ochratoxin A[J].Journal of the Chinese Cereals and Oils Association, 2018, 33(5):76-81.
[15] 陈晓平, 金玉, 孟岩, 等.高能电子束对大米食用品质的影响[J].食品科学, 2016, 37(3):71-74.
CHEN X P, JIN Y, MENG Y, et al.Effect of high-energy electron beam irradiation on eating quality of rice[J].Food Science, 2016, 37(3):71-74.
[16] 程竹林, 王晓雨, 任贵平, 等.电子束辐照对干枸杞生虫及品质的影响[J].现代食品科技, 2023, 39(2):221-228.
CHENG Z L, WANG X Y, REN G P, et al.Effects of electron beam irradiation on the infestation and quality of dried goji (Lycium barbarum)[J].Modern Food Science &Technology, 2023, 39(2):221-228.
[17] 何凯锋, 陈秀金, 臧鹏, 等.辐照杀菌技术对食品品质的影响及控制研究进展[J].食品与发酵工业, 2023, 49(10):299-305.
HE K F, CHEN X J, ZANG P, et al.Research progress on effect of irradiation sterilization on food quality and its control[J].Food and Fermentation Industries, 2023, 49(10):299-305.
[18] SHARMA P, VENUGOPAL A P, SUTAR P P, et al.Mechanism of microbial spore inactivation through electromagnetic radiations:A review[J].Journal of Future Foods, 2024, 4(4):324-334.
[19] FANG F, SUN X, LIU Y X, et al.γ-Ray driven aqueous-phase methane conversions into complex molecules up to glycine[J].Angewandte Chemie-International Edition, 2025, 64(1):e202413296.
[20] 苟小军, 杨艳, 杨晓露, 等.色氨酸代谢研究进展[J].医学研究杂志, 2021, 50(3):126-128.
GOU X J, YANG Y, YANG X L, et al.Research progress of tryptophan metabolism[J].Journal of Medical Research, 2021, 50(3):126-128.
[21] 王甜, 吴锐霄, 杨春杰, 等.不同电子束辐照处理对传统镇巴腊肉品质的影响[J].肉类研究, 2022, 36(10):16-23.
WANG T, WU R X, YANG C J, et al.Effects of electron beam irradiation on the quality of traditional Zhenba smoked cured meat[J].Meat Research, 2022, 36(10):16-23.
[22] MINKOFF B B, BRUCKBAUER S T, SABAT G, et al.Covalent modification of amino acids and peptides induced by ionizing radiation from an electron beam linear accelerator used in radiotherapy[J].Radiation Research, 2019, 191(5):447-459.
[23] 顾可飞, 陈志军.电子束辐照对氨基酸与蛋白质结构的影响[J].辐射研究与辐射工艺学报, 2019, 37(2):33-40.
GU K F, CHEN Z J.Influence of electron-beam irradiation on amino acids and protein structure[J].Journal of Radiation Research and Radiation Processing, 2019, 37(2):33-40.
[24] 耿胜荣, 程薇, 廖涛, 等.γ射线和电子束辐照对牛血清蛋白结构的影响[J].现代食品科技, 2016, 32(12):211-217;253.
GENG S R, CHENG W, LIAO T, et al.Effects of γ-rays and electron beam irradiation on bovine serum albumin structure[J].Modern Food Science and Technology, 2016, 32(12):211-217;253.
[25] ZHANG J, WANG T, YANG C J, et al.Integrated proteomics and metabolomics analysis revealed the mechanisms underlying the effect of irradiation on the fat quality of Chinese bacon[J].Food Chemistry, 2023, 413:135385.
[26] ZHANG Y Q, KONG Y F, XU W J, et al.Electron beam irradiation alters the physicochemical properties of chickpea proteins and the peptidomic profile of its digest[J].Molecules,2023, 28(16):6161.
[27] JIA W, WU X Y.Potential biomarkers analysis and protein internal mechanisms by cold plasma treatment:Is proteomics effective to elucidate protein-protein interaction network and biochemical pathway?[J].Food Chemistry, 2023, 426:136664.
[28] 胡鹏, 张奇志, 邓鹏, 等.辐照对扒鸡氨基酸及感官品质的影响[J].核农学报, 2011, 25(3):506-509.
HU P, ZHANG Q Z, DENG P, et al.Effect of irradiation on amino acid and sensory quality of braised chicken[J].Acta Agriculturae Nucleatae Sinica, 2011, 25(3):506-509.
[29] NEM ANU M R, KIKUCHI I S, DE JESUS ANDREOLI PINTO T, et al.Electron beam irradiation of Matricaria chamomilla L.for microbial decontamination[J].Nuclear Instruments and Methods in Physics Research Section B:Beam Interactions with Materials and Atoms, 2008, 266(10):2520-2523.
ANU M R, KIKUCHI I S, DE JESUS ANDREOLI PINTO T, et al.Electron beam irradiation of Matricaria chamomilla L.for microbial decontamination[J].Nuclear Instruments and Methods in Physics Research Section B:Beam Interactions with Materials and Atoms, 2008, 266(10):2520-2523.
[30] ZHENG Q, TIAN W H, WANG S S, et al.Electron beam irradiation maintains postharvest quality of Actinidia arguta by regulating the cell wall, starch degradation, and antioxidant capacity[J].Postharvest Biology and Technology, 2025, 223:113442.
[31] 燕欣悦, 胡风庆, 宁崇, 等.电子束辐照技术对食品品质的影响及在食品中的应用研究进展[J].食品与机械, 2025, 41(2):216-225.
YAN X Y, HU F Q, NING C, et al.Research progress on the effect of electron beam irradiation technology on food quality and its application in food[J].Food &Machinery, 2025, 41(2):216-225.
[32] DWINANDHA D, ELSAMADONY M, GAO R J, et al.Interpretable machine learning and reactomics assisted isotopically labeled FT-ICR-MS for exploring the reactivity and transformation of natural organic matter during ultraviolet photolysis[J].Environmental Science &Technology, 2024, 58(1):816-825.
[33] YU K J, DIXON R A, DUAN C Q.A role for ascorbate conjugates of (+)-catechin in proanthocyanidin polymerization[J].Nature Communications, 2022, 13(1):3425.
[34] HOU D H, WANG C L, YU J T, et al. Effects of electron beam irradiation on the postharvest quality characteristics of winter jujube (Zizyphus jujuba mill.cv.Dalidongzao)[J].Journal of Future Foods, 2025, 5(2):153-161.
[35] VO Q V, NAM P C, THONG N M, et al.Antioxidant motifs in flavonoids:O—H versus C—H bond dissociation[J].ACS Omega, 2019, 4(5):8935-8942.
[36] PLATZER M, KIESE S, TYBUSSEK T, et al.Radical scavenging mechanisms of phenolic compounds:A quantitative structure-property relationship (QSPR) study[J].Frontiers in Nutrition, 2022,9:882458.
[37] 金梦阳, 危文亮.60Coγ射线辐照对续随子保护酶活性的影响[J].核农学报, 2008, 22(5):569-572;580.
JIN M Y, WEI W L.The effects of 60Co γ-rays irradiation on the activity of protective enzymes in caper spurge (Euphorbia lathyris L.)seedlings[J].Acta Agriculturae Nucleatae Sinica, 2008, 22(5):569-572;580.
[38] 徐攀, 贾鑫, 高鹏, 等.基于正交偏最小二乘判别分析电子束辐照对黄精抗氧化活性的影响[J].食品安全质量检测学报, 2023, 14(12):274-282.
XU P, JIA X, GAO P, et al.Analysis of the effect of electron beam irradiation on antioxidant activity of Polygonati rhizoma based on orthogonal partial least squares-discriminant[J].Journal of Food Safety &Quality, 2023, 14(12):274-282.
[39] 王冠, 岳鑫颖, 吕春茂, 等.60Co-γ射线辐照对榛子鲜果采后生理及脂质营养的影响[J].食品科学, 2023, 44(15):212-219.
WANG G, YUE X Y, LYU C M, et al.Effect of60Co-γ Irradiation on postharvest physiology and lipid nutrition of fresh hazelnuts[J].Food Science, 2023, 44(15):212-219.
[40] 司婧, 张红.12C6+离子束辐照番茄种子当代效应[J].原子核物理评论, 2011, 28(3):349-353.
SI J, ZHANG H.Effects of irradiation with12C6+ion beam on M1 characters of Lycopersicon esculentum Mill.[J].Nuclear Physics Review, 2011, 28(3):349-353.