L-高丝氨酸是一种重要的非蛋白质氨基酸,具有多种生理功能,在饲料、医药、化工和农业等领域具有广泛应用[1]。L-高丝氨酸作为天冬氨酸家族氨基酸,是生物体合成L-苏氨酸和L-蛋氨酸等必需氨基酸的重要前体物质,在细胞的生理活动和代谢调控中发挥着关键作用[2]。研究表明,L-高丝氨酸能够诱导动植物的免疫反应,增强其免疫力,从而促进生长发育[3]。L-高丝氨酸分子结构中包含有氨基和羟基等活性基团,赋予其多样的化学反应特性,使其成为重要的C4平台化合物,用于合成2,4-二羟基丁酸、γ-丁内酯、1,3-丙二醇等多种高附加值化学品[4-5]。随着对L-高丝氨酸应用研究的不断深入,L-高丝氨酸的应用潜力不断被挖掘与拓展。最近,L-高丝氨酸还被开发作为关键前体合成广谱除草剂L-草铵膦,是实现光学纯L-草铵膦绿色合成的重要路径[1]。
目前,L-高丝氨酸的合成方法主要包括化学合成法和生物合成法。化学合成法通常以L-蛋氨酸为原料,合成过程存在反应路径复杂、生产成本高及环境污染严重等问题,难以满足绿色、高效的大规模工业化生产要求[6]。近年来,随着合成生物学和代谢工程技术的迅速发展,微生物发酵法凭借其原料廉价、过程环保及可持续性强等优势,成为L-高丝氨酸绿色制造的重要途径,受到了研究人员的广泛关注[6]。目前,关于L-高丝氨酸微生物合成的研究主要集中在大肠杆菌(Escherichia coli)模型菌株上。例如,ZHANG等[7]以E.coli为宿主,通过增强L-高丝氨酸合成路径、敲除相关降解通路以及促进产物外排等代谢工程策略,成功构建了高效的L-高丝氨酸生产菌株,发酵产量达到60.1 g/L。LIU等[8]通过耦合调控L-高丝氨酸合成途径和细胞分离过程,进一步将E.coli中L-高丝氨酸的合成水平提高至101.31 g/L。谷氨酸棒杆菌(Corynebacterium glutamicum)作为一种重要的食品安全级工业微生物,已成功应用于氨基酸、有机酸和核苷酸等多种化合物的生物制造,在发酵生产L-高丝氨酸方面具有巨大潜力[9]。最近,LI等[10-11]通过调控C.glutamicum的代谢流,构建了C.glutamicum L-高丝氨酸生产底盘细胞,并进一步通过调控辅因子供应策略,将L-高丝氨酸产量提高至63.5 g/L。尽管如此,目前通过代谢改造C.glutamicum生产L-高丝氨酸的研究相对较少,当前获得的产量和得率相对较低,无法满足工业化应用需求。
L-高丝氨酸的生产水平、生产强度和转化率是影响其工业化应用潜力的关键指标。在微生物中,L-高丝氨酸的合成主要依赖2条途径,即AspC途径(aspartate aminotransferase pathway)和AspA途径(aspartate ammonia-lyase pathway)[1,12]。这2条途径均以草酰乙酸(oxaloacetate, OAA)为关键代谢中间物。在AspC途径中,OAA在天冬氨酸转氨酶(aspartate aminotransferase,AspC)的催化下生成天冬氨酸,随后通过下游反应合成L-高丝氨酸。该路径具有较高的理论转化效率,每1 mol葡萄糖可生成2 mol L-高丝氨酸,是目前L-高丝氨酸生物合成的主要路径。而在AspA途径中,OAA首先进入三羧酸(tricarboxylic acid,TCA)循环,生成延胡索酸,再由天冬氨酸裂解酶(aspartate ammonia-lyase,AspA)催化生成天冬氨酸,并进一步进入L-高丝氨酸合成流程。AspA途径由于与TCA循环密切相关,更有利于细胞的能量代谢和平衡生长。因此,通过合理平衡AspC与AspA 2条途径的代谢通量,能够有效实现细胞生长与产物合成之间的动态协调,进而提高L-高丝氨酸的发酵产量与原料利用率。鉴于C.glutamicum在氨基酸工业生产中的显著优势以及其良好的遗传可操控性,本研究以C.glutamicum为宿主菌株,围绕L-高丝氨酸的高效合成需求,通过AspC与AspA双通路通量协同调控、前体合成强化以及辅因子代谢平衡等策略,构建具备工业化潜力的L-高丝氨酸高效合成微生物细胞工厂,为实现L-高丝氨酸工业化绿色生物制造提供重要的研究基础和理论依据。
1 材料与方法
1.1 材料
1.1.1 菌种和质粒
本研究中E. coli DH5α由本实验室保藏,主要用于质粒构建。C.glutamicum ATCC13032由本实验室保藏,主要作为L-高丝氨酸生产底盘细胞。温度敏感敲除质粒pCRD206由本实验室保藏,主要用于C.glutamicum染色体上基因的敲除和敲入。所用菌株与质粒见表1。
表1 本研究所用质粒与菌株
Table 1 Plasmids and strains used in this study
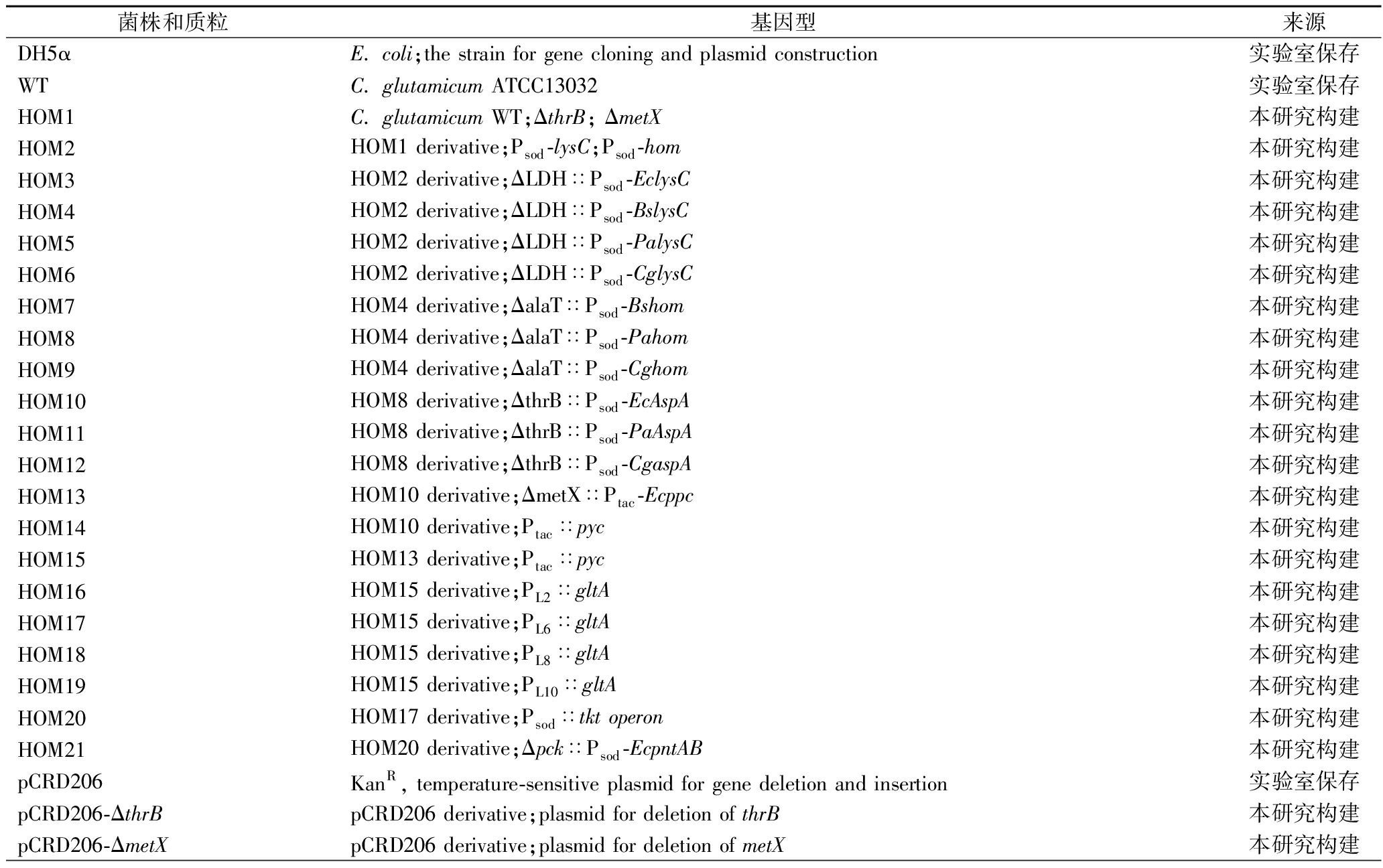
菌株和质粒基因型来源DH5αE. coli;the strain for gene cloning and plasmid construction实验室保存WTC. glutamicum ATCC13032实验室保存HOM1C. glutamicum WT;ΔthrB; ΔmetX本研究构建HOM2HOM1 derivative;Psod-lysC;Psod-hom本研究构建HOM3HOM2 derivative;ΔLDH∷Psod-EclysC本研究构建HOM4HOM2 derivative;ΔLDH∷Psod-BslysC本研究构建HOM5HOM2 derivative;ΔLDH∷Psod-PalysC本研究构建HOM6HOM2 derivative;ΔLDH∷Psod-CglysC本研究构建HOM7HOM4 derivative;ΔalaT∷Psod-Bshom本研究构建HOM8HOM4 derivative;ΔalaT∷Psod-Pahom本研究构建HOM9HOM4 derivative;ΔalaT∷Psod-Cghom本研究构建HOM10HOM8 derivative;ΔthrB∷Psod-EcAspA本研究构建HOM11HOM8 derivative;ΔthrB∷Psod-PaAspA本研究构建HOM12HOM8 derivative;ΔthrB∷Psod-CgaspA本研究构建HOM13HOM10 derivative;ΔmetX∷Ptac-Ecppc本研究构建HOM14HOM10 derivative;Ptac∷pyc本研究构建HOM15HOM13 derivative;Ptac∷pyc本研究构建HOM16HOM15 derivative;PL2∷gltA本研究构建HOM17HOM15 derivative;PL6∷gltA本研究构建HOM18HOM15 derivative;PL8∷gltA本研究构建HOM19HOM15 derivative;PL10∷gltA本研究构建HOM20HOM17 derivative;Psod∷tkt operon本研究构建HOM21HOM20 derivative;Δpck∷Psod-EcpntAB本研究构建pCRD206KanR, temperature-sensitive plasmid for gene deletion and insertion实验室保存pCRD206-ΔthrBpCRD206 derivative;plasmid for deletion of thrB本研究构建pCRD206-ΔmetXpCRD206 derivative;plasmid for deletion of metX本研究构建
续表1
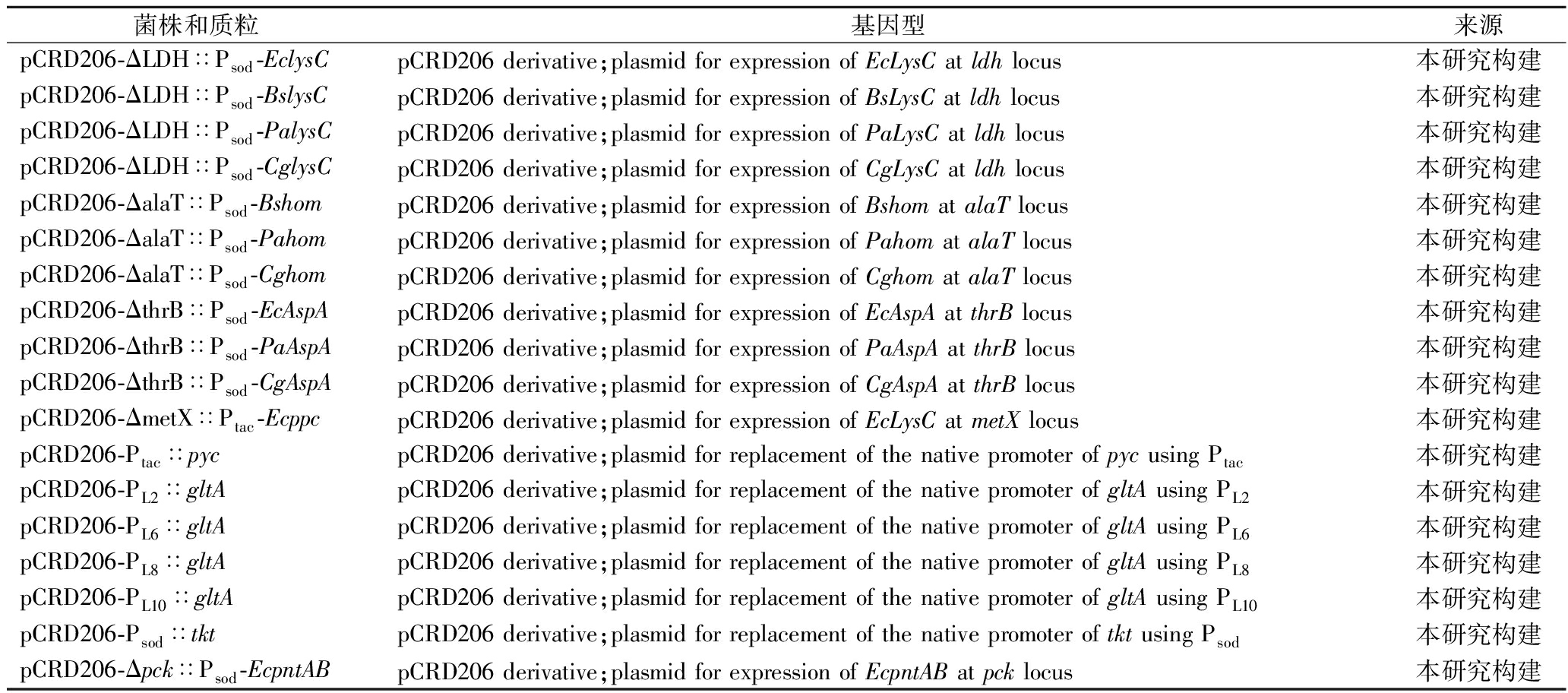
菌株和质粒基因型来源pCRD206-ΔLDH∷Psod-EclysCpCRD206 derivative;plasmid for expression of EcLysC at ldh locus本研究构建pCRD206-ΔLDH∷Psod-BslysCpCRD206 derivative;plasmid for expression of BsLysC at ldh locus本研究构建pCRD206-ΔLDH∷Psod-PalysCpCRD206 derivative;plasmid for expression of PaLysC at ldh locus本研究构建pCRD206-ΔLDH∷Psod-CglysCpCRD206 derivative;plasmid for expression of CgLysC at ldh locus本研究构建pCRD206-ΔalaT∷Psod-BshompCRD206 derivative;plasmid for expression of Bshom at alaT locus本研究构建pCRD206-ΔalaT∷Psod-PahompCRD206 derivative;plasmid for expression of Pahom at alaT locus本研究构建pCRD206-ΔalaT∷Psod-CghompCRD206 derivative;plasmid for expression of Cghom at alaT locus本研究构建pCRD206-ΔthrB∷Psod-EcAspApCRD206 derivative;plasmid for expression of EcAspA at thrB locus本研究构建pCRD206-ΔthrB∷Psod-PaAspApCRD206 derivative;plasmid for expression of PaAspA at thrB locus本研究构建pCRD206-ΔthrB∷Psod-CgAspApCRD206 derivative;plasmid for expression of CgAspA at thrB locus本研究构建pCRD206-ΔmetX∷Ptac-EcppcpCRD206 derivative;plasmid for expression of EcLysC at metX locus本研究构建pCRD206-Ptac∷pycpCRD206 derivative;plasmid for replacement of the native promoter of pyc using Ptac本研究构建pCRD206-PL2∷gltApCRD206 derivative;plasmid for replacement of the native promoter of gltA using PL2本研究构建pCRD206-PL6∷gltApCRD206 derivative;plasmid for replacement of the native promoter of gltA using PL6本研究构建pCRD206-PL8∷gltApCRD206 derivative;plasmid for replacement of the native promoter of gltA using PL8本研究构建pCRD206-PL10∷gltApCRD206 derivative;plasmid for replacement of the native promoter of gltA using PL10本研究构建pCRD206-Psod∷tktpCRD206 derivative;plasmid for replacement of the native promoter of tkt using Psod本研究构建pCRD206-Δpck∷Psod-EcpntABpCRD206 derivative;plasmid for expression of EcpntAB at pck locus本研究构建
1.1.2 试剂
限制性内切酶、T4 DNA连接酶、Phusion DNA聚合酶,Thermo Fisher公司;ClonExpress MultiS One Step Cloning Kit质粒无缝克隆试剂盒,南京诺唯赞生物科技有限公司;质粒提取试剂盒、胶回收试剂盒、RNA-prep Pure Cell/Bacteria Kit,天根生化科技有限公司。
1.1.3 培养基
LB培养基(g/L):酵母提取物5、胰蛋白胨10、NaCl 5。
LBHIS培养基(g/L):酵母提取物2.5、胰蛋白胨5、脑心浸液18.5、D-山梨醇91、NaCl 5。
种子培养基(g/L):葡萄糖30、玉米浆30、MgSO4 0.5、KH2PO4 1、(NH4)2SO4 5、pH 7.0。
发酵培养基(g/L):葡萄糖70,玉米浆20,乙酸钾0.5,KH2PO4 0.5,MgSO4 0.5,(NH4)2SO4 20,H3PO4 0.225 mL/L,FeSO4-柠檬酸0.55 mL/L(FeSO4·7H2O 20 g/L,柠檬酸18.14 g/L),维生素溶液7 mL/L(生物素300 mg/L,维生素B1 500 mg/L,泛酸钙盐2 g/L,烟酰胺 600 mg/L),pH 7.0。
1.1.4 仪器与设备
TC-XP-D型PCR基因扩增仪、NanoDrop 2000分光光度计,美国赛默飞世尔科技公司;ZWY-211C振荡培养箱,美国精骐有限公司;Scientz-IID超声破碎仪,宁波新芝公司;5810R高速冷冻离心机,德国Eppendorf公司。Synergy NEO2多功能酶标仪,美国伯腾仪器有限公司;1260高效液相色谱仪,美国Agilent公司。
1.2 实验方法
1.2.1 质粒构建
本研究采用温度敏感穿梭质粒pCRD206对C.glutamicum进行基因敲除和敲入[13]。使用Phusion DNA聚合酶,以菌株基因组为模版,分别扩增获得目的基因DNA片段和上下游同源片段。质粒骨架 pCRD206 经BamHI和XbaI双酶切线性化后,采用ClonExpress MultiS One Step Cloning Kit无缝克隆试剂盒将上述获得的DNA片段连接起来,构建重组质粒。
1.2.2 C.glutamicum基因敲除和插入
利用同源重组技术对C.glutamicum中的基因进行敲除和敲入[13]。将上述构建的重组质粒电转化至C.glutamicum感受态细胞,涂布于含有25 μg/L卡那霉素的固体LBHIS培养基中,25 ℃培养24 h。挑取单菌落接种至含有25 μg/L卡那霉素的液体LBHIS培养基中,37 ℃培养12 h,筛选质粒发生首次同源重组并整合至染色体的阳性菌株。随后,将筛选得到的重组菌转接至含蔗糖的无抗培养基中进行反向筛选,以促使质粒发生第二次重组并从染色体中剔除。通过菌落PCR验证获得目的基因敲除或敲入的C.glutamicum工程菌株。
1.2.3 胞内NADPH测定
将重组菌株接种于发酵培养基中,于对数生长期取样,并将菌液稀释至 OD600= 1。使用PBS洗涤菌体2次后,置于冰水浴中超声波破碎20 min。破碎液在4 ℃、6 000 r/min条件下离心20 min,收集上清液用于胞内NADPH含量的测定。检测使用上海碧云天公司提供的 NADP+/NADPH 检测试剂盒,按照说明书操作完成测定。
1.2.4 酶活性测试
天冬氨酸激酶活性按照文献报道双酶偶联法进行测定[14]。天冬氨酸激酶催化天冬氨酸生成天冬氨酸-4-磷酸,后者经天冬氨酸半醛脱氢酶催化下生成天冬氨酸半醛,并伴随NADPH消耗。因此,通过监测340 nm波长下NADPH吸光度的变化可间接测定天冬氨酸激酶的酶活性。酶活性检测体系为:100 mmol/L Tris-HCl(pH 7.5),10 mmol/L天冬氨酸,5 mmol/L ATP,2 mmol/L MgSO4,1 mmol/L NADPH,0.5 μg天冬氨酸半醛脱氢酶以及适量天冬氨酸激酶。酶活性单位定义为每分钟消耗1 μmol/L NADPH 所用的酶量(1 U)。
1.2.5 基因表达强度分析
本研究采用实时荧光定量PCR(quantitative real-time polymerase chain reaction, RT-qPCR)技术分析目的基因的表达强度。以16S rRNA 作为内参基因,使用 SYBR GREEN Realtime PCR Master Mix(TOYOBO, Japan)进行目的基因的表达分析。
1.2.6 L-高丝氨酸工程菌株的发酵测试
摇瓶发酵:将单菌落接种至LBHIS培养基中,在32 ℃、220 r/min条件下过夜培养,随后按1%的接种量接种至种子培养基中,在相同条件下培养16 h。将种子培养基按照初始OD600=1接种至含有25 mL发酵培养基的250 mL三角瓶中,在32 ℃、220 r/min条件下继续培养60 h。
发酵罐发酵:将种子培养基以5%的接种量接种至发酵罐中,培养温度32 ℃,发酵培养60 h。发酵过程中采用25%(体积分数)氨水控制发酵体系的pH值维持在7.0,并通过搅拌速率和通气量维持溶氧浓度为30%。采用葡萄糖生物传感分析仪检测发酵罐中葡萄糖的浓度,当发酵体系中葡萄糖质量浓度低于5 g/L时,流加600 g/L葡萄糖溶液,通过调节流加速度,控制发酵液中葡萄糖质量浓度在5 g/L以下。
1.2.7 L-高丝氨酸浓度检测
使用分光光度计测定发酵液中菌体的生长情况(OD600),使用高效液相色谱仪测定发酵液中L-高丝氨酸的含量。色谱柱为Agilent ZORBAX Eclipse AAA色谱柱(4.6 mm×150 mm,5 μm)。流动相A相:40 mmol/L NaH2PO4溶液(pH=7.8),B相:乙腈∶甲醇∶水=45∶45∶10(体积比),流速2.0 mL/min,检测波长338 nm,柱温40 ℃。
1.2.8 统计分析
样本均采用3个独立重复实验。使用SPSS统计软件进行双侧Student t检验,分析实验组之间的统计学显著差异。
2 结果与分析
2.1 C.glutamicum L-高丝氨酸生物合成底盘细胞的构建
L-高丝氨酸的合成以L-天冬氨酸为前体,其生成存在2条主要途径:在AspC途径中,草酰乙酸经AspC催化直接生成天冬氨酸;而在AspA途径中,草酰乙酸经TCA循环生成延胡索酸,再经AspA催化生成天冬氨酸。随后,天冬氨酸通过由天冬氨酸激酶(LysC)、天冬氨酸半醛脱氢酶(Asd)和高丝氨酸脱氢酶(Hom)催化的共同下游步骤转化为L-高丝氨酸。L-高丝氨酸作为关键代谢节点,是合成L-苏氨酸和L-蛋氨酸的直接前体,因此在细胞内通常被快速消耗而不会大量积累(图1)。
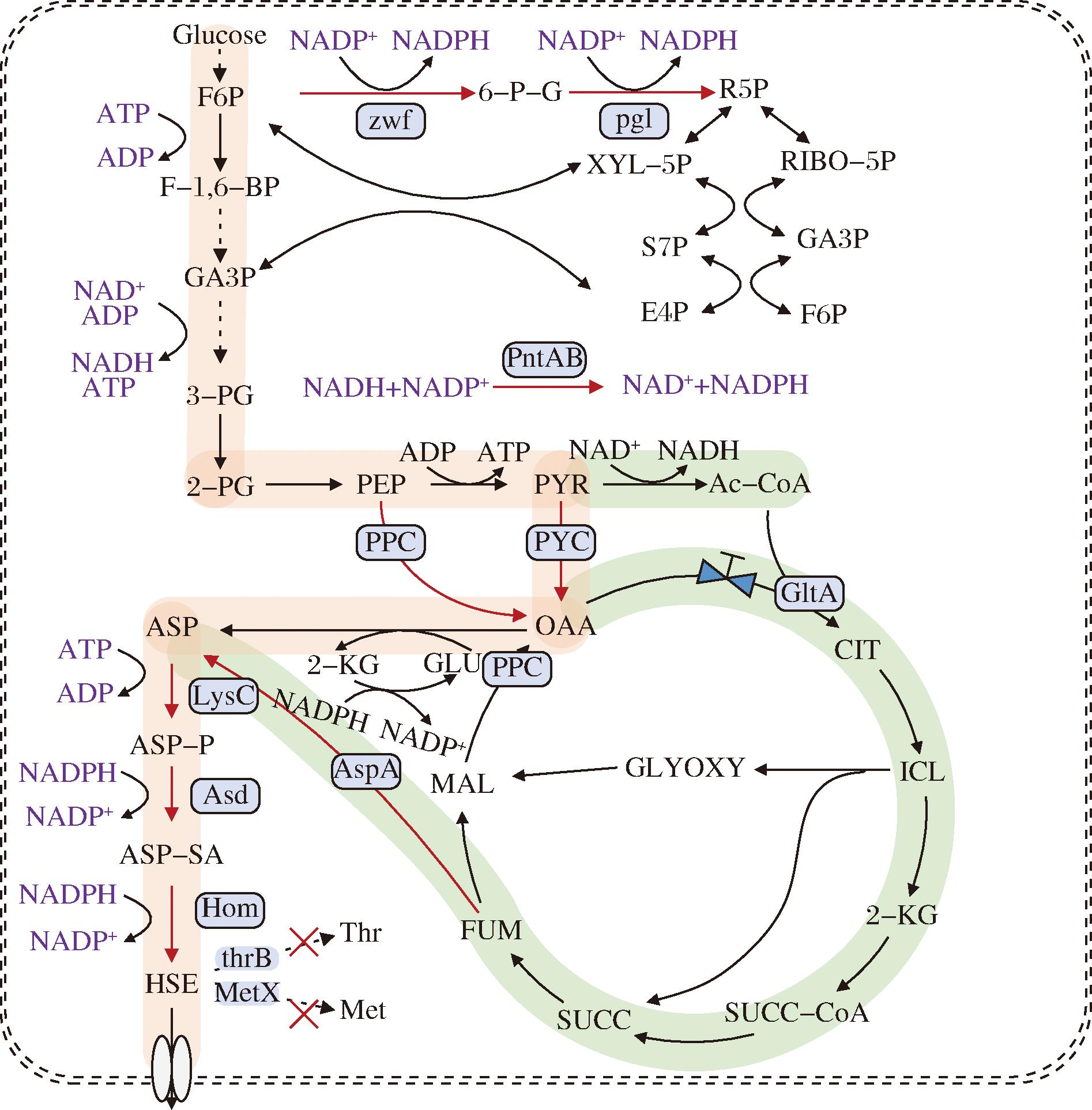
图1 基于双途径代谢工程改造C.glutamicum生产L-高丝氨酸示意图
Fig.1 Schematic diagram for engineering of C.glutamicum based on the dual pathway for L-homoserine production
注:红色箭头表示基因过表达;红色“X”表示基因敲除;红色底纹代表AspC途径;绿色底纹代表ApsA途径。
基于上述认识,本研究以C.glutamicum ATCC13032为宿主,通过阻断L-高丝氨酸的降解路径并增强其合成通量,构建L-高丝氨酸合成底盘菌株。L-高丝氨酸激酶(homoserine kinase,ThrB)和高丝氨酸乙酰转移酶(homoserine acetyltransferase,MetX)是催化L-高丝氨酸进入L-苏氨酸和L-蛋氨酸合成途径的关键催化酶,因此本研究首先敲除了高丝氨酸激酶和高丝氨酸乙酰转移酶编码基因thrB和metX,阻断了L-高丝氨酸的下游降解途径,构建了重组菌株HOM1。在此基础上,进一步使用强启动子Psod过表达L-高丝氨酸合成途径中的关键酶天冬氨酸激酶和高丝氨酸脱氢酶编码基因lysC和hom,构建了重组菌株HOM2。对上述工程菌株进行摇瓶发酵分析发现,HOM1与HOM2的生物量与野生型菌株相比并未表现出显著差异。而且工程菌株HOM1和HOM2分别积累了1.25 g/L与4.12 g/L的L-高丝氨酸,相较于起始菌株(0.24 g/L),产量分别提高了5.2倍和17.16倍(图2)。结果表明,通过敲除关键降解途径并强化L-高丝氨酸的合成通量,可显著提升其在胞内的积累水平,成功构建了具有L-高丝氨酸生产能力的底盘菌株。
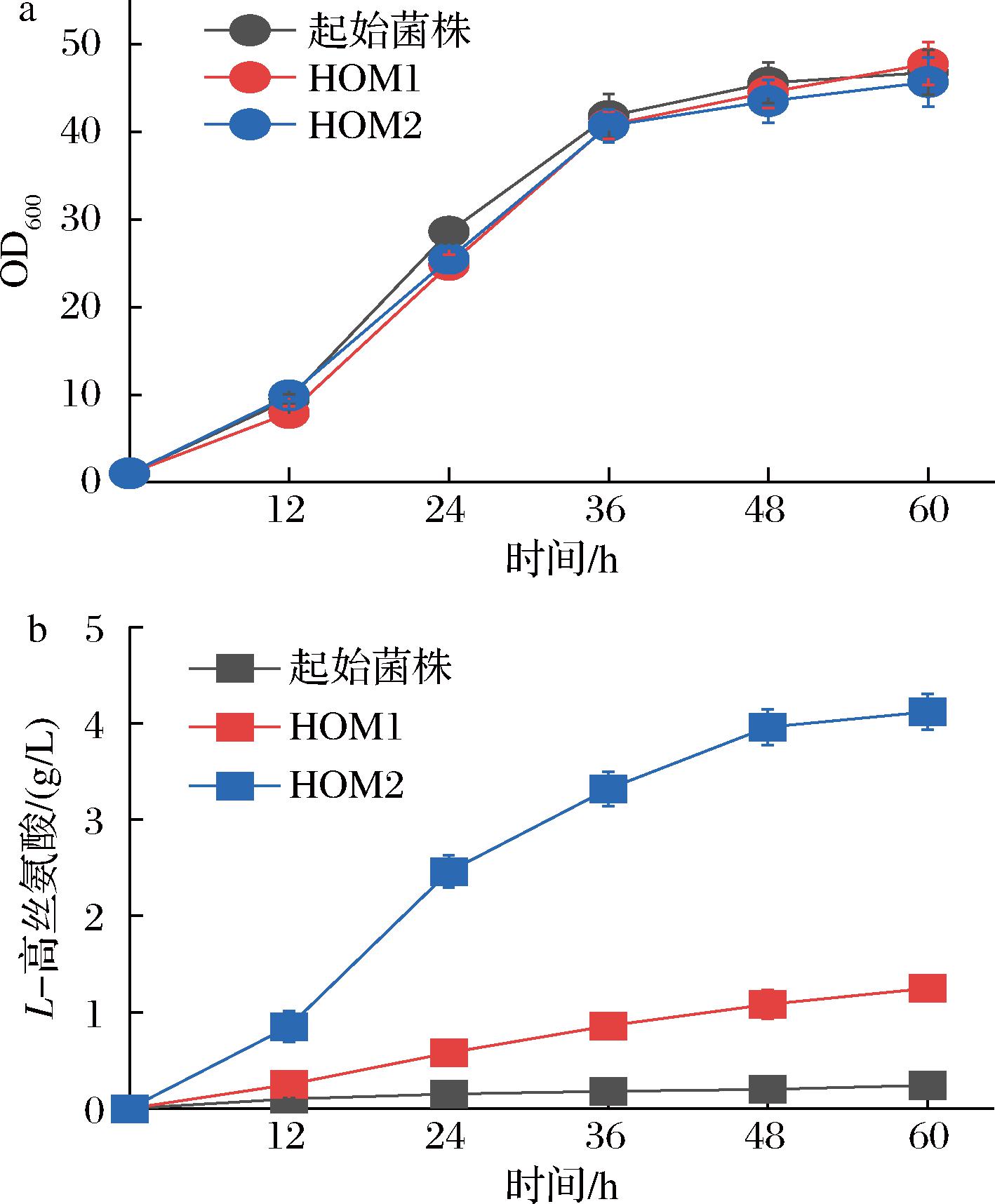
a-L-高丝氨酸重组菌株的生长轮廓曲线;b-重组菌株的L-高丝氨酸生产
图2 重组菌株的生物量和L-高丝氨酸产量
Fig.2 Biomass and L-homoserine production of recombinant strains
2.2 L-高丝氨酸双合成途径重构与优化
2.2.1 重构AspC途径提高L-高丝氨酸合成
AspC途径是 L-高丝氨酸合成的主要代谢路径,其代谢通量的高低直接影响最终产物的积累水平。因此,本研究针对AspC途径进行重构与强化,以提高其整体催化效率。天冬氨酸激酶(aspartate kinase,LysC)是AspC路径中的关键限速酶,催化L-天冬氨酸转化为天冬氨酸磷酸,并进入下游的L-高丝氨酸合成路径。为增强该途径代谢流,本研究在C.glutamicum L-高丝氨酸合成底盘细胞的基础上,进一步强化天冬氨酸激酶的表达。本研究通过文献分析和数据库检索[1,12],从常见工业微生物中筛选了多个具有高效催化活性的lysC基因,包括来源于E.coli、枯草芽孢杆菌(Bacillus subtilis)、铜绿假单胞菌(Pseudomonas aeruginosa)及C.glutamicum自身的lysC基因,分别采用强启动子Psod在底盘菌株HOM2的染色体上整合表达,构建重组菌株HOM3、HOM4、HOM5和HOM6。摇瓶发酵结果表明,上述获得4个重组菌株的L-高丝氨酸含量均有不同程度的提高,其中表达来源于Bacillus subtilis BSlysC基因的重组菌株HOM4的产量最高达到4.76 g/L,比对照菌株HOM2提高了15.53%(图3)。进一步通过酶活性测试发现,HOM4中天冬氨酸激酶活性高于其他菌株,说明提高天冬氨酸激酶活性能增强L-高丝氨酸的合成通量,促进L-高丝氨酸的合成。
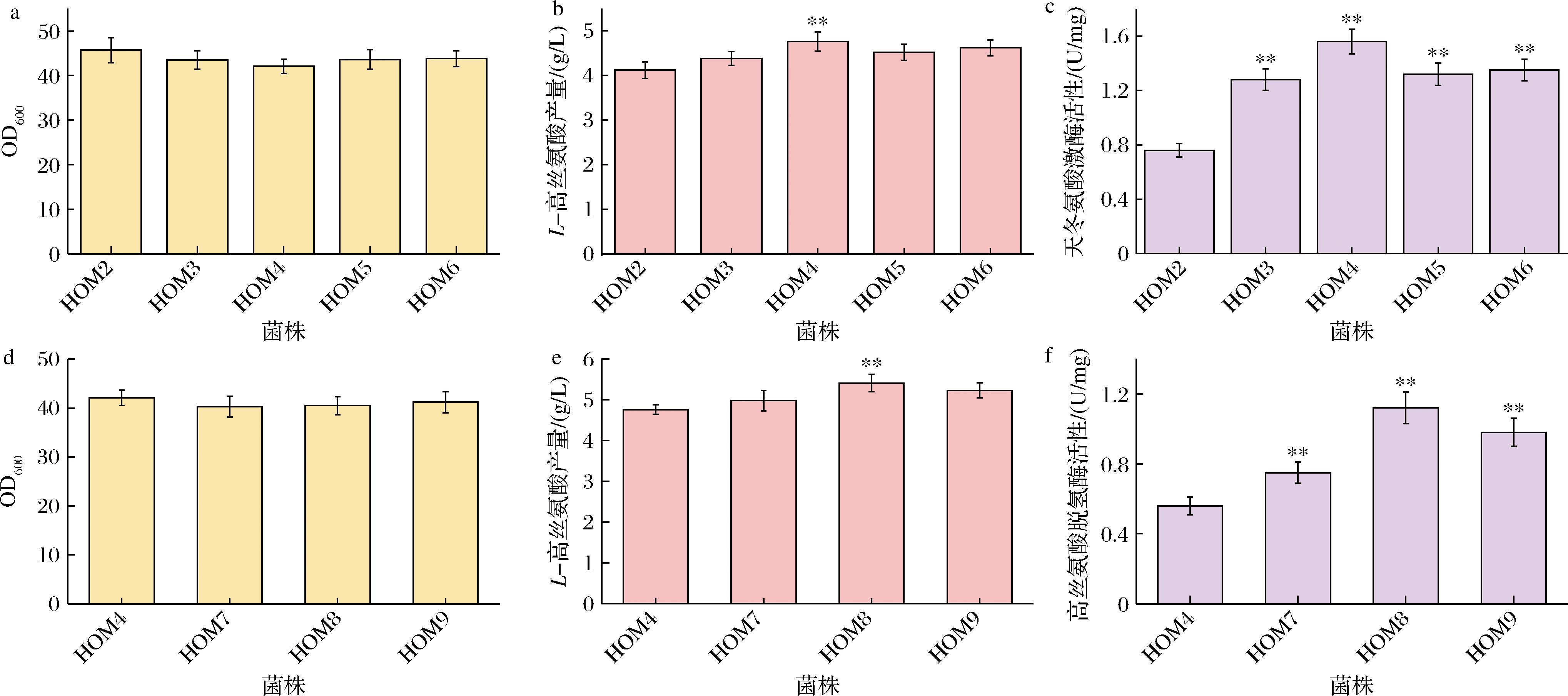
a-重组菌株的生物量;b-重组菌株的L-高丝氨酸产量;c-重组菌株天冬氨酸激酶活性测定;d-重组菌株的生物量;e-重组菌株的L-高丝氨酸产量;f-重组菌株L-高丝氨酸脱氢酶活性测定
图3 AspC途径重构提高C.glutamicum L-高丝氨酸合成能力
Fig.3 Reconstruction of AspC synthetic pathway to enhance L-homoserine synthesis in C.glutamicum
注:*表示P<0.05,**表示P<0.01(下同)。
高丝氨酸脱氢酶是L-高丝氨酸生物合成的最后一步,催化天冬氨酸半醛生成L-高丝氨酸,是合成L-高丝氨酸的另一个关键限速步骤。因此,本研究在HOM4工程菌株的基础上,进一步强化表达高丝氨酸脱氢酶,提高L-高丝氨酸的合成效率。本研究比较分析了不同来源的高丝氨酸脱氢酶对L-高丝氨酸合成的影响,包括来源于B.subtilis、P.aeruginosa以及C.glutamicum自身的高丝氨酸脱氢酶hom基因,并使用强启动子Psod进行强化表达,构建了重组菌株HOM7、HOM8、HOM9。由于E.coli中高丝氨酸脱氢酶编码基因thrA和metL为双功能酶[12],同时存在天冬氨酸激酶活性,不利于实现独立调控,因此未被纳入后续分析。如图3所示,构建的3个重组菌株L-高丝氨酸的产量比对照菌株HOM4均有一定的提高,其中表达来源于P.aeruginosa Pahom基因的工程菌种HOM8的L-高丝氨酸含量达到5.41 g/L,比对照菌株HOM4提高了13.65%。同时,酶活性测定发现,HOM8中高丝氨酸脱氢酶活性高于其他重组菌株的酶活性,进一步证明高丝氨酸脱氢酶是调控L-高丝氨酸合成速率的关键酶,增强其活性有助于提高最终产物的积累。
2.2.2 重构AspA途径提高L-高丝氨酸合成
AspA能够催化延胡索酸生产L-天冬氨酸,是生产L-高丝氨酸的另一条关键途径[1]。为进一步增强L-天冬氨酸的前体供给能力,本研究在HOM8重组菌株的基础上强化表达AspA途径。从常见工业菌株中克隆了具有高效催化活性的AspA,包括来源于E.coli[1]、P.aeruginosa[15]和C.glutamicum的aspA基因,并在强启动子Psod的驱动下实现其高水平表达,分别构建了重组菌株HOM10、HOM11和HOM12。摇瓶发酵结果表明,HOM10表现出最高的L-高丝氨酸生产能力,其产量达到5.86 g/L,比对照菌株HOM8提高了8.31%。而且HOM10的生物量水平与HOM8基本相当,表明该策略在不影响细胞生长的前提下,有效提高了目标产物的合成能力(图4)。综上结果表明,增强AspA途径中天冬氨酸裂氨酶的表达水平,能够提高L-天冬氨酸的合成速率,从而进一步推动L-高丝氨酸的积累,为进一步提升产量提供了有效的策略支持。
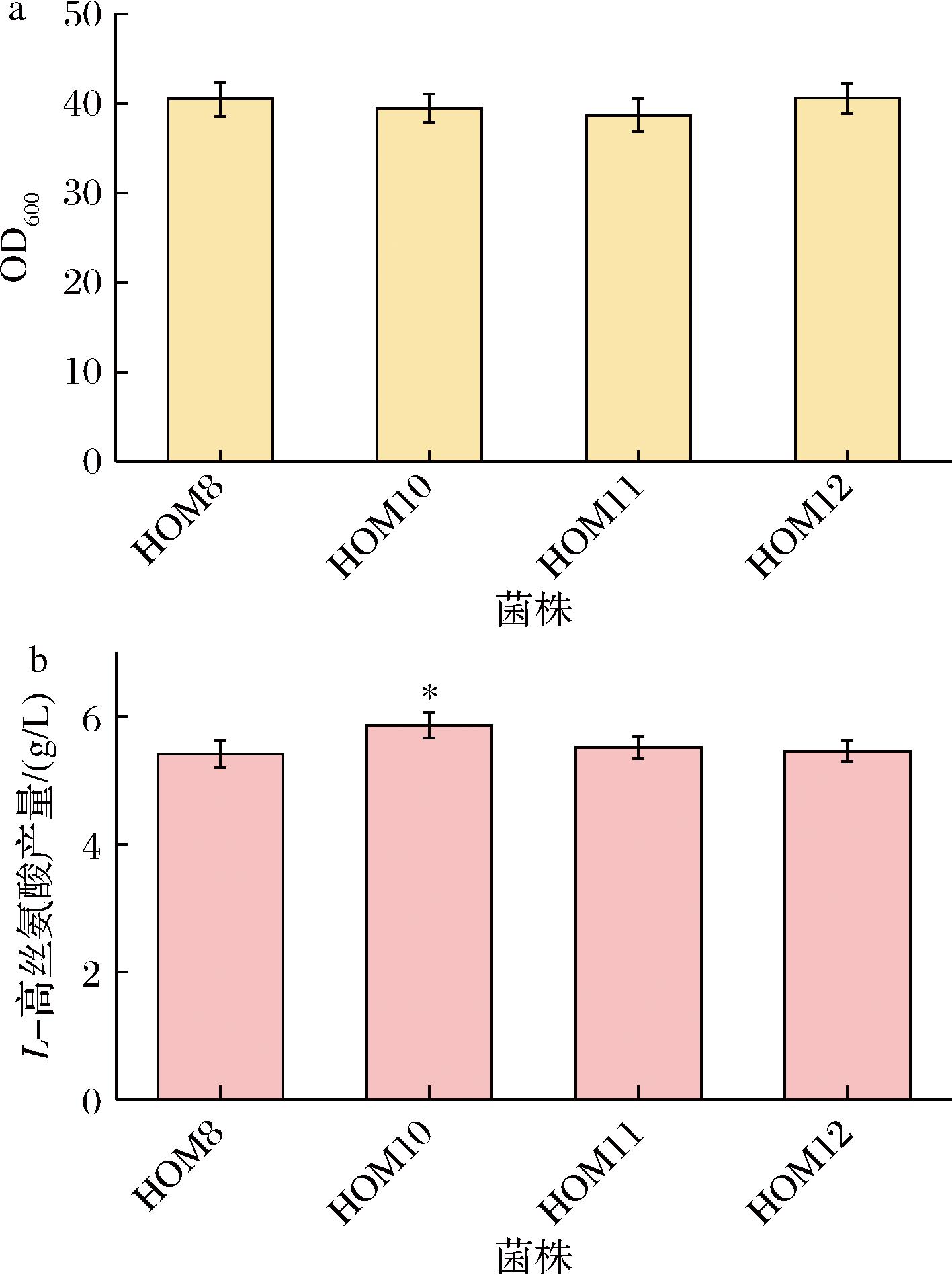
a-生物量;b-L-高丝氨酸产量
图4 AspA途径重构促进C.glutamicum L-高丝氨酸的合成
Fig.4 AspA pathway reconstruction promotes the synthesis of L-homoserine in C.glutamicum
2.3 前体合成调控提高L-高丝氨酸合成能力
OAA是L-高丝氨酸生物合成的关键前体物质,其供给水平直接影响了L-高丝氨酸的合成效率[16]。在微生物中,OAA主要通过2条途径生成:一条由丙酮酸羧化酶(pyruvate carboxylase,PYC)催化丙酮酸合成,另一条由磷酸烯醇式丙酮酸羧化酶(phosphoenolpyruvate carboxylase,PPC)催化磷酸烯醇式丙酮酸生成。这2条羧化反应均可固定1个CO2分子,不仅提高了碳原子的利用效率,还有助于减少碳排放,从而提升目标产物的得率。为增强OAA的前体供给能力,在HOM10菌株的基础上,利用强启动子Ptac分别表达来源于E.coli的ppc和来源于C.glutamicum自身的pyc基因,分别构建了重组菌株HOM13和HOM14。摇瓶发酵结果分析显示,HOM13和HOM14的生长能力比对照菌株HOM10略有下降,推测可能由于部分碳代谢流被引导至L-高丝氨酸的合成途径,从而削弱了对细胞生长所需碳源的供给。而且HOM13和HOM14在L-高丝氨酸的合成方面均表现出显著提升,其产量分别为6.48 g/L和6.65 g/L,较HOM10分别提高了10.58%与13.48%(图5)。在此基础上,进一步将PPC与PYC两个合成路径进行组合强化,构建重组菌株HOM15。发酵测试结果表明,HOM15的L-高丝氨酸产量达到6.98 g/L,较HOM10提高了19.11%(图5-b)。上述结果表明,通过协调强化PPC与PYC两条OAA合成路径,能显著提升OAA的前体供给能力,从而增强了L-高丝氨酸的合成通量,促进了L-高丝氨酸的高效积累。
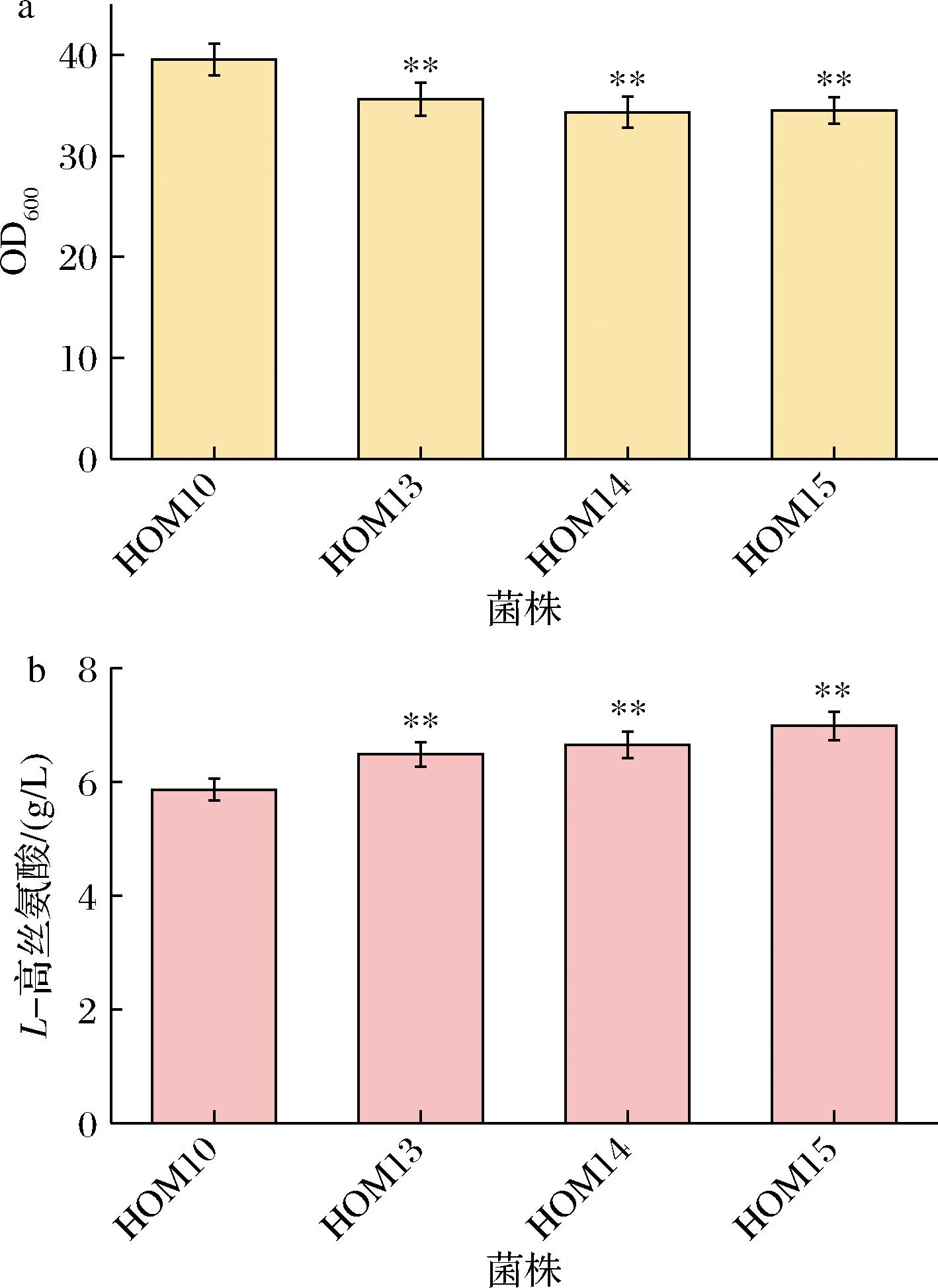
a-生物量;b-L-高丝氨酸产量
图5 前体合成调控提高C.glutamicum L-高丝氨酸的合成能力
Fig.5 Regulation of precursor synthesis to enhance the L-homoserine synthesis in C.glutamicum
2.4 双途径平衡调控促进L-高丝氨酸合成
本研究在C.glutamicum中通过重构ApsC和ApsA途径,实现了L-高丝氨酸的生物合成。值得注意的是,AspC途径是L-高丝氨酸生物合成的主要路径,具有较高的理论产物得率,每1 mol葡萄糖可合成2 mol L-高丝氨酸;然而,该途径依赖大量NADPH作为还原力来源,易受到胞内NADPH供给不足的限制。AspA途径需经由TCA 循环,得率显著低于AspC途径,每1 mol葡萄糖理论上合成1 mol L-高丝氨酸,但是该路径与细胞的正常生长和能量代谢紧密耦合。因此,合理平衡2条代谢通路的通量分配,有助于缓解细胞生长与产物合成之间在碳源利用上的竞争,从而提升细胞工厂的合成效率和生产能力。柠檬酸合成酶(citrate synthase,GltA)是OAA进入TCA循环的限速酶,是调控AspC与AspA路径之间代谢流的关键节点。基于此,本研究在工程菌株HOM15的基础上,从启动子文库中选择了4个不同强度的启动子PL2、PL6、PL8和PL10[17],对gltA基因的表达进行精细调控,分别构建了重组菌株HOM16、HOM17、HOM18和HOM19。摇瓶发酵结果表明,当使用最低启动子强度(PL2)调控gltA表达时,重组菌株HOM16的细胞生长显著受抑,同时L-高丝氨酸产量明显下降,表明AspA通路通量的过度抑制削弱了TCA循环活性,进而限制了细胞增殖及代谢能力。相比之下,当采用启动子PL6调控gltA表达时,重组菌株HOM17的L-高丝氨酸产量达到8.56 g/L,较对照菌株HOM15提升22.64%,尽管其生物量略有下降,但总体代谢效率得到显著优化(图6)。RT-qPCR分析显示,HOM17中gltA基因的表达水平约为对照菌株的52.8%,进一步验证了中等强度表达可在保证细胞生长的前提下,有效调控AspC与AspA途径间的代谢分配。综上所述,适度调控关键酶gltA的表达水平,可实现对AspC与AspA双通路代谢流的精准调控,有效协调细胞生长与目标产物合成之间的碳代谢平衡,进而促进L-高丝氨酸的高效合成。
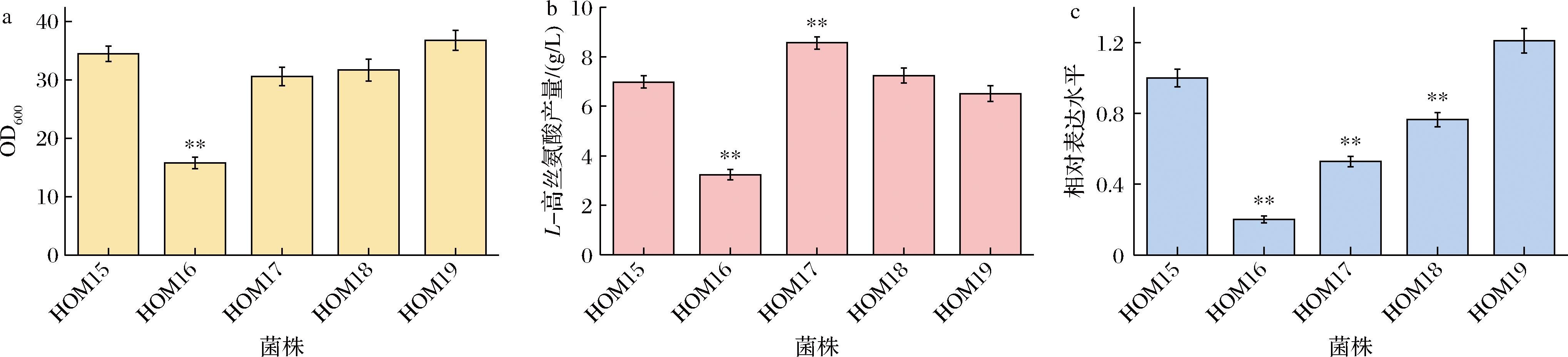
a-生物量;b-L-高丝氨酸产量;c-RT-PCR测定重组菌株gltA的表达水平
图6 双途径平衡调控促进L-高丝氨酸合成
Fig.6 Dual pathway balanced regulation promotes L-homoserine synthesis
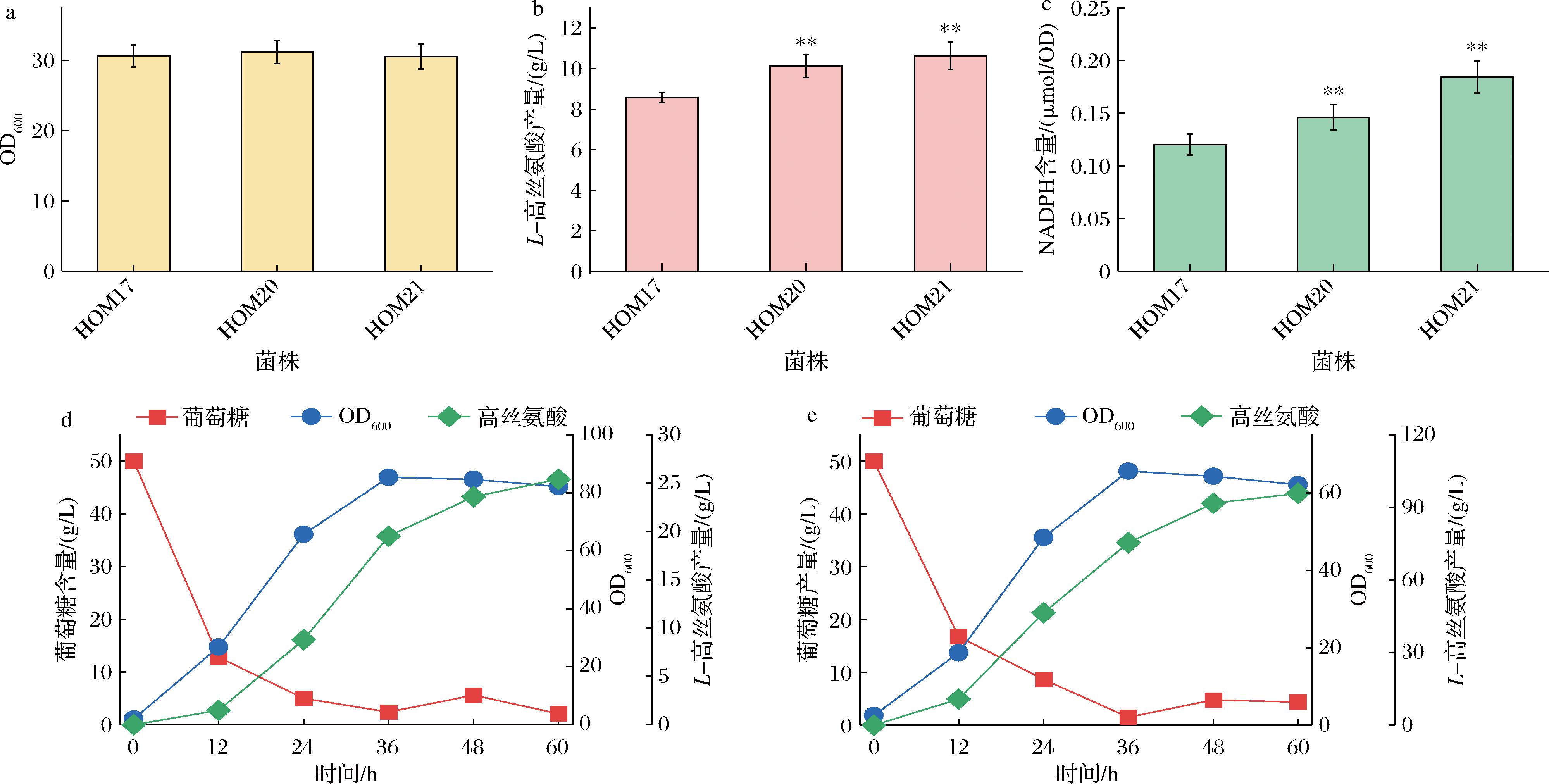
a-生物量;b-L-高丝氨酸产量;c-NADPH含量测定;d-L-高丝氨酸生产底盘菌株HOM2发酵罐轮廓分析;e-L-高丝氨酸工程菌株HOM21发酵罐轮廓分析
图7 辅因子工程强化L-高丝氨酸的生产水平
Fig.7 Cofactor engineering to enhance the L-homoserine production
2.5 辅因子工程强化L-高丝氨酸的生产水平
L-高丝氨酸合成途径中需要消耗大量的辅因子NADPH,构成了限制其合成效率的关键因素。尤其是在AspC途径中,每合成1 mol L-高丝氨酸需要消耗3 mol NADPH,胞内NADPH的再生能力成为影响产物合成水平的核心限制瓶颈。在微生物中,磷酸戊糖途径是NADPH再生的主要代谢通路之一。在C.glutamicum中,磷酸戊糖途径受到转酮酶(transketolase,TKT)操纵子的调控。因此,本研究在工程菌株HOM17的基础上,使用强启动子Psod替换了TKT操纵子的启动子,增强磷酸戊糖途径通量,构建了工程菌株HOM20。如图7所示,HOM20的L-高丝氨酸的发酵产量达到10.12 g/L,比对照菌株HOM17提高了18.22%。在此基础上,为进一步强化NADPH的再生能力,在重组菌株HOM20中,使用强启动子Ptac过表达了来源于E.coli的吡啶核苷酸转氢酶基因(pyridine nucleotide transhydrogenase,pntAB),将胞内过量的NADH转化为NADPH,从而进一步增强还原力供应,获得了工程菌株HOM21。如图7所示,工程菌株HOM21胞内的NADPH含量比对照菌株HOM17提高了45.75%,说明通过调控磷酸戊糖途径和吡啶核苷酸转氢酶途径能够有效提高胞内NADPH的再生能力。而且工程菌株HOM21的L-高丝氨酸产量达到10.63 g/L,比对照菌株HOM17提高了24.18%。上述结果表明,提高胞内辅因子的平衡再生能力能够为L-高丝氨酸的生物合成提供有效驱动力,从而显著提高L-高丝氨酸合成能力。
在此基础上,对最终构建L-高丝氨酸合成菌株HOM21进行5 L发酵罐规模测试。发酵动力学结果如图7所示,HOM21的生长速率比对照菌株HOM2略有降低,细胞生长在36 h达到稳定期,OD600达到65.6,比对照菌株HOM2(OD600 =85.3)降低了23.1%。而且,HOM21的L-高丝氨酸产量随发酵时间持续上升,在60 h时达到最高水平,L-高丝氨酸产量达到95.8 g/L,远高于对照菌株HOM2的25.4 g/L,是对照菌株HOM2的3.77倍。同时,L-高丝氨酸的生产强度为1.6 g/(L·h),葡萄糖转化率为0.45 g/g,是目前已报道的利用C.glutamicum生产L-高丝氨酸的先进水平。
3 结论与讨论
L-高丝氨酸是一种重要的非蛋白质氨基酸,不仅在体内具有重要的生理功能,同时也是合成L-草铵膦等多种精细化工产品的重要中间体。微生物发酵法因其具有环境友好、成本低廉等优势,已成为L-高丝氨酸绿色合成的重要技术路线。近年来,随着L-高丝氨酸市场需求的持续增长,研究者围绕其生物合成开展了大量代谢工程相关研究。然而,当前所构建的工程菌株在产量与转化效率方面仍存在明显不足,限制了L-高丝氨酸的工业化生产进程。C.glutamicum是一种食品安全级工业微生物,具备发酵生产多种氨基酸的良好基础,具有作为L-高丝氨酸生产宿主的广阔应用前景。但目前针对该菌种在L-高丝氨酸合成方面的研究仍相对有限。为此,本研究基于代谢工程策略,对C.glutamicum 的L-高丝氨酸合成途径进行了系统改造,通过重构并协调AspC与AspA双合成路径、强化前体物质供给能力、优化NADPH辅因子的再生平衡,成功构建了高效L-高丝氨酸合成细胞工厂。最终获得的工程菌株发酵产量达95.8 g/L,生产强度为1.6 g/(L·h),葡萄糖转化率为0.45 g/g,达到目前基于C.glutamicum生产L-高丝氨酸的先进水平。本研究不仅验证了C.glutamicum在L-高丝氨酸高效生物合成中的应用潜力,同时系统揭示了影响其合成效率的关键限速步骤与调控机制,为实现L-高丝氨酸的绿色工业化制造提供了坚实的理论基础与工程借鉴。
[1] MU Q X, ZHANG S S, MAO X J, et al.Highly efficient production of L-homoserine in Escherichia coli by engineering a redox balance route[J].Metabolic Engineering, 2021, 67:321-329.
[2] CAI M M, ZHAO Z Q, LI X F, et al.Development of a nonauxotrophic L-homoserine hyperproducer in Escherichia coli by systems metabolic engineering[J].Metabolic Engineering, 2022, 73:270-279.
[3] VAN DAMME M, ZEILMAKER T, ELBERSE J, et al.Downy mildew resistance in Arabidopsis by mutation of HOMOSERINE KINASE[J].The Plant Cell, 2009, 21(7):2179-2189.
[4] HONG K K, KIM J H, YOON J H, et al.O-Succinyl-L-homoserine-based C4-chemical production:Succinic acid, homoserine lactone, γ-butyrolactone, γ-butyrolactone derivatives, and 1, 4-butanediol[J].Journal of Industrial Microbiology &Biotechnology, 2014, 41(10):1517-1524.
[5] ZHONG W Q, ZHANG Y, WU W J, et al.Metabolic engineering of a homoserine-derived non-natural pathway for the de novo production of 1, 3-propanediol from glucose[J].ACS Synthetic Biology, 2019, 8(3):587-595.
[6] SUN Y J, WU J P, XU J Q, et al.Metabolic engineering of Escherichia coli for the production of L-homoserine[J].Microbial Cell Factories, 2024, 1(3):223-230.
[7] ZHANG Y, WEI M H, ZHAO G H, et al.High-level production of L-homoserine using a non-induced, non-auxotrophic Escherichia coli chassis through metabolic engineering[J].Bioresource Technology, 2021, 327:124814.
[8] LIU Z F, CAI M M, ZHOU S Q, et al.High-efficient production of L-homoserine in Escherichia coli through engineering synthetic pathway combined with regulating cell division[J].Bioresource Technology, 2023, 389:129828.
[9] LI M H, LI H, ZHANG X, et al.Metabolic engineering of Corynebacterium glutamicum:Unlocking its potential as a key cell factory platform for organic acid production[J].Biotechnology Advances, 2024, 77:108475.
[10] LI N, LI L H, YU S Q, et al.Dual-channel glycolysis balances cofactor supply for L-homoserine biosynthesis in Corynebacterium glutamicum[J].Bioresource Technology, 2023, 369:128473.
[11] LI N, WANG M, YU S Q, et al.Optimization of CRISPR-Cas9 through promoter replacement and efficient production of L-homoserine in Corynebacterium glutamicum[J].Biotechnology Journal, 2021, 16(8):2100093.
[12] CHEN Y Y, HUANG L G, YU T, et al.Balancing the AspC and AspA pathways of Escherichia coli by systematic metabolic engineering strategy for high-efficient L-homoserine production[J].ACS Synthetic Biology, 2024, 13(8):2457-2469.
[13] WEI L, ZHAO J H, WANG Y R, et al.Engineering of Corynebacterium glutamicum for high-level γ-aminobutyric acid production from glycerol by dynamic metabolic control[J].Metabolic Engineering, 2022, 69:134-146.
[14] ISOGAI S, TAKAGI H.Enhancement of lysine biosynthesis confers high-temperature stress tolerance to Escherichia coli cells[J].Applied Microbiology and Biotechnology, 2021, 105(18):6899-6908.
[15] LI G Q, LU C D.Molecular characterization and regulation of operons for asparagine and aspartate uptake and utilization in Pseudomonas aeruginosa[J].Microbiology, 2018, 164(2):205-216.
[16] WANG Y S, BAI Y L, ZENG Q, et al.Recent advances in the metabolic engineering and physiological opportunities for microbial synthesis of L-aspartic acid family amino acids:A review[J].International Journal of Biological Macromolecules, 2023, 253:126916.
[17] WEI L, XU N, WANG Y R, et al.Promoter library-based module combination (PLMC) technology for optimization of threonine biosynthesis in Corynebacterium glutamicum[J].Applied Microbiology and Biotechnology, 2018, 102(9):4117-4130.