葡萄酒中的单宁主要来源于葡萄籽和葡萄皮,由苯丙氨酸聚合通过代谢途径生物合成[1-2]。单宁的化学特性(聚合度、聚合单体等)直接决定了葡萄酒涩感[3-4]。过强的涩感可能会掩盖葡萄酒中的其他风味成分,而涩感不足则可能导致葡萄酒口感寡淡,酒体单薄[5]。根据美国材料实验协会(American Society for Testing and Materials)2004年的定义[6],涩感是一种复杂的感官体验,表现为上皮细胞在接触某些物质(如明矾或单宁)时发生的收缩、紧绷或起皱。尽管关于涩感形成机制仍存在诸多争议,但普遍认为,由单宁引起的涩感主要是由于其与唾液中的蛋白质结合后形成的沉淀所致[7]。由于单宁对红葡萄酒涩感的巨大贡献及其分子鉴定的复杂性,几十年来红葡萄酒中单宁的表征在葡萄酒化学领域引起了人们的强烈关注。单宁由多种黄烷-3-醇单体组成,主要包括(表)儿茶素、(表)棓儿茶素和(表)儿茶素没食子酸酯等[8]。这些黄烷醇单元间连接方式大多以B型连接。在酿酒过程中,单宁可能会发生氧化、缩合、羟基化和重排等复杂反应[9-10],但目前关于红葡萄酒酿造过程中单宁变化对涩感的影响还缺乏全面解释[3,11]。
随着计算化学和分子模拟技术的飞速发展[12],分子对接被广泛应用于葡萄酒领域,帮助研究人员深入理解葡萄酒中关键化学成分与口腔内唾液蛋白或其他大分子物质之间的相互作用模式和结合强度[13]。不仅为理解涩感等复杂口腔感知的感知机制提供了新的视角,也为预测不同单宁结构对整体风味特征可能产生的影响、筛选能够改善葡萄酒口感或提升酒体稳定性的潜在成分提供了重要的理论依据和技术手段[14-15]。然而,尽管分子对接在探索分子间相互作用方面显示出巨大潜力,但是目前系统性地利用分子对接技术,结合酿造过程中单宁组分和结构的动态变化,来阐释其与红葡萄酒涩感感知演变之间关系的研究仍相对有限。
本研究基于超高效液相色谱四极杆飞行时间质谱联用(ultra performance liquid chromatography quadrupole time-of-flight mass spectrometry,UPLC-Q-TOF)非靶向代谢组学及分子对接技术探究红葡萄酒酿造过程中单宁及涩感感知变化。在工业规模酿酒过程中收集了3个阶段(浸渍、发酵和陈酿)的12个连续关键点的葡萄酒样品。使用Folin-Ciocalteu法分析红葡萄酒总酚含量,通过间苯三酚裂解法对红葡萄酒单宁组分进行表征。利用UPLC-Q-TOF、定量描述分析(quantitative descriptiveanalysis,QDA)对赤霞珠红葡萄酒的单宁及涩感感知变化进行研究,通过分子对接技术探究涩感变化机理。为揭示红葡萄酒酿造过程中单宁复杂结构演变对涩感感知变化的影响提供了一定的理论基础。
1 材料与方法
1.1 材料与试剂
赤霞珠葡萄果实于2021年葡萄采收期采集自宁夏贺兰山东麓产区葡萄园(北纬38°28′,东经106°12′)。葡萄汁可溶性固形物含量27.20 °BrX,可滴定酸含量5.00 g/L(以酒石酸计),pH 3.49,卫生状况良好。
儿茶素、表儿茶素、棓儿茶素、表棓儿茶素(纯度均≥99.0%)、表儿茶素没食子酸酯、表棓儿茶素没食子酸酯(纯度均≥98.1%),中国食品药品研究院;间苯三酚(HPLC级),上海麦克林生化科技有限公司;甲酸、甲醇(均为LC-MS级),赛默飞世尔科技公司;LC-MS级超纯水,霍尼韦尔国际公司;Folin-Ciocalteu溶液(BR),Phygene生物技术有限公司。
1.2 仪器与设备
AQ C18亲水系列SPE固相萃取柱,天津博纳艾杰尔科技有限公司;VP2C隔膜真空泵、EV400旋转蒸发仪,北京莱伯泰科仪器股份有限公司;57030-U SUPELCO标准型12管固相萃取装置,北京飞美斯分析科技有限公司;Agilent1290-G6546A UPLC-ESI-Q-TOF电喷雾液质联用飞行时间质谱、HPH-C18 UHPLC column(2.1 mm×100 mm, 1.9 μm),美国安捷伦科技有限公司。
1.3 实验方法
1.3.1 红葡萄酒酿造
本研究以赤霞珠葡萄为原料,在工业规模上进行酿造红葡萄酒。葡萄除梗后经人工分拣去除病果和未成熟果,新鲜葡萄破碎后加入20 t不锈钢发酵罐,入罐时添加偏重亚硫酸钾(SO2,50 mg/L)和果胶酶(35 mg/L)。在5~8 ℃下进行3~6 d冷浸渍。冷浸渍结束后加入250 mg/L的酿酒酵母(D254)启动酒精发酵,发酵温度维持在22~25 ℃,酒精发酵结束后去除皮渣。在分离出的葡萄酒中添加10 mg/L乳酸菌进行苹果酸-乳酸发酵。苹果酸-乳酸发酵结束后进行装瓶(750 mL),装瓶前将SO2质量浓度调整至20 mg/L,装瓶后置于酒窖中贮存,温度16 ℃,相对湿度75%,直到指定取样时间进行取样。
在葡萄酒酿造的3个阶段(浸渍阶段、发酵阶段和陈酿阶段)的12个关键时间点取样。具体取样点包括:葡萄入罐(G1)、冷浸渍降温前(G2)、冷浸渍结束(G3)、升温阶段(G4)、酒精发酵开始(AF1)、酒精发酵比重至1(AF2)、苹果酸-乳酸发酵开始(MLF1)、苹果酸-乳酸发酵结束(MLF2)、陈酿3个月(Age3)、陈酿6个月(Age6)、陈酿9个月(Age9)和陈酿12个月(Age12)。每次取样贮存在-20 ℃的冰箱中。
1.3.2 理化指标测定
测定pH值、可滴定酸度、酒精度,方法参照GB/T 15038—2006《葡萄酒、果酒通用分析方法(含第1号修改单)》。残糖测量通过全自动分析仪。总酚测定参照VIGNAULT等[16]的方法,标准曲线为0.3 g/L梯度稀释的没食子酸溶液,标准曲线方程为y=27.62x+2.07(R2=0.999 7)。所有分析均重复3次。
1.3.3 单宁组分测定
根据KENNEDY等[17]的方法,吸取2.5 mL红葡萄酒在<40 ℃下旋转蒸发至干燥。用10 mL蒸馏水稀释旋蒸至干的红葡萄酒备用。在抽真空条件下激活SPE固相萃取柱,将10 mL稀释过的红葡萄酒完全吸入固相萃取柱内,先用50 mL水冲洗柱子以洗去样品中的糖类和有机酸,之后用50 mL甲醇将样品洗脱并收集。将所得组分旋转蒸发至干燥,复溶于1 mL甲醇当中作为样品液备用。吸取200 μL反应液(2.5 g间苯三酚、0.5 g抗坏血酸、493 μL盐酸)与20 μL样品液充分混合,然后置于50 ℃烘箱中反应20 min,反应结束后加入1 mL终止液(无水乙酸钠328 mg,定容在100 mL蒸馏水中,浓度为40 mmol/L)混匀,最后经过0.22 μm滤膜过滤后用UPLC-ESI-Q-TOF检测。间苯三酚裂解反应、裂解单宁质荷比和终结单元与延伸单元离子流色谱图信息如图1所示。
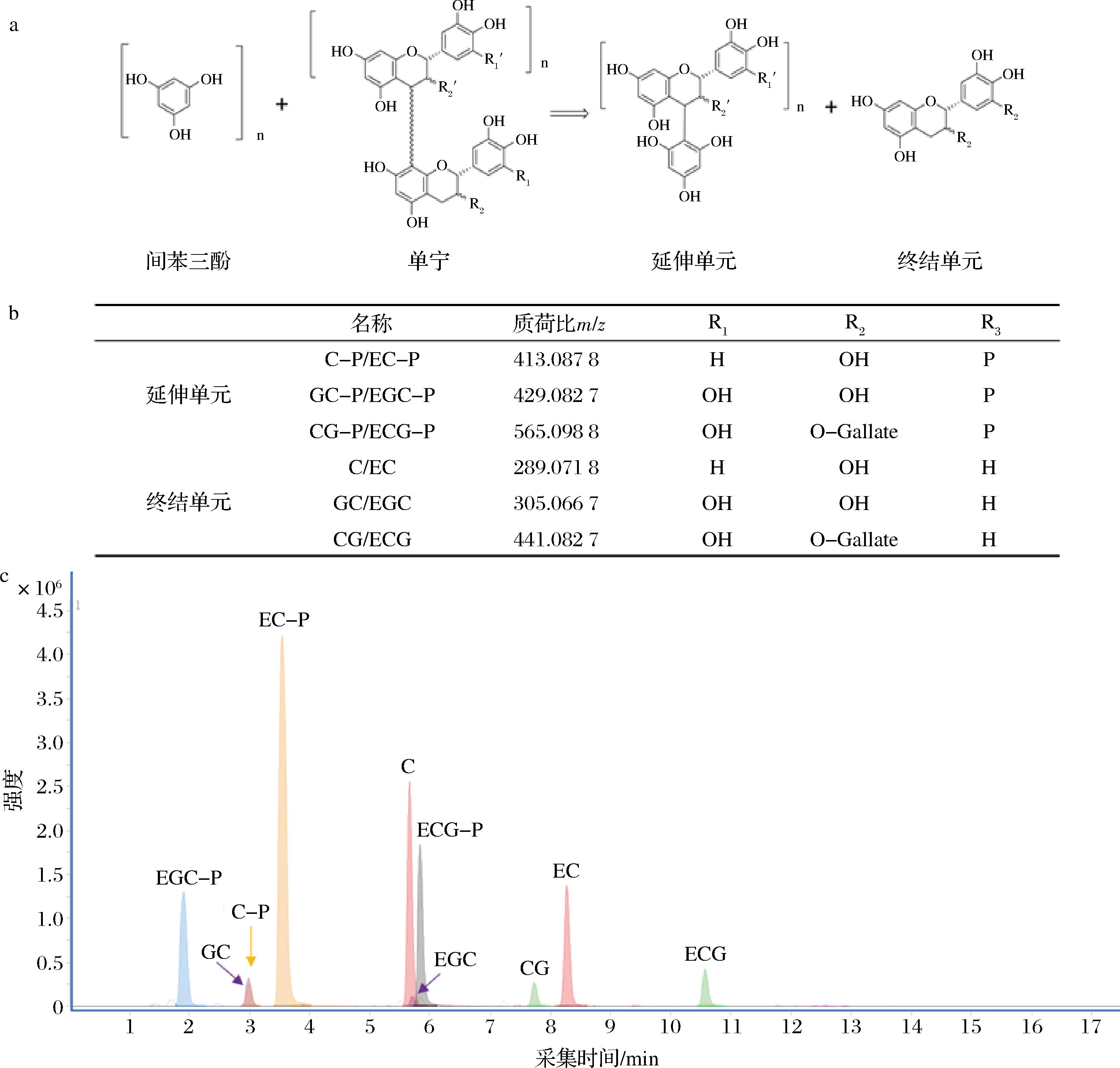
a-间苯三酚裂解反应;b-间苯三酚反应裂解后单宁物质单体结构与质荷比信息;c-终结单元与延伸单元组合提取离子流色谱图
图1 基于间苯三酚裂解法的单宁组分分析
Fig.1 Tannin composition analysis by phloroglucinolysis
注:儿茶素(catechin, C);表儿茶素(epicatechin, EC);棓儿茶素(gallocatechin, GC);表棓儿茶素(epigallocatechin, EGC);儿茶素没食子酸酯(catechin gallate, CG);表儿茶素没食子酸酯(epicatechin gallate,ECG);间苯三酚加合物(phloroglucinol adduct, P)。
UPLC-ESI-Q-TOF的方法参照MA等[1]并略做修改。经过修改后最终条件如下,LC的条件:流动相A为含0.1%甲酸的水溶液,B为含0.1%甲酸的甲醇溶液,流速0.3 mL/min。线性梯度为:0~1 min,10%B;1~4 min,10%~20%B;4~10 min,20%~32%B;10~14 min,32%~100%B;之后用100%的B相溶液冲洗柱子3 min,在下一次进样前用初始条件平衡柱子3 min,进样量1 μL;MS的条件:质谱仪工作在2 GHz扩展动态范围内(m/z 3 200 Th)。雾化器压力和流量分别设置为25 psi和9 L/min。干燥气体温度300 ℃。鞘气气体流量和温度设定为11 L/min和350 ℃。Fragmentation、Skimmer、OCT和毛细管电压在分别为150、65、750、4 000 V。所有分析在负离子模式下进行。标准曲线使用儿茶素标准品半定量,公式为y=233 477x+5 950.5(R2=0.999 8)。
1.3.4 单宁非靶向代谢组的测定
将样本解冻并用0.22 μm滤膜过滤后,使用UPLC-Q-TOF进行检测。LC和MS条件均与1.3.3节相同。新的线性梯度如下:0~1.9 min 5% B;1.9~3.8 min 5%~10% B;3.8~5.6 min 10% B;5.6~7.5 min 10%~12% B;7.5~8.2 min 12%~14% B;8.2~15.6 min 14%~25% B;15.6~19.6 min 25%~65% B;19.6~20 min 65%~100% B,并在运行结束后保持3 min,总运行时间23 min。基于之前的方法[18],使用(-)-表儿茶素的峰面积标准曲线半定量地确定所有单宁的浓度。单体和二聚体使用(-)-表儿茶素标准曲线y=451 612x+42 134(R2=0.996 5);三聚体到五聚体使用(-)-表儿茶素标准曲线y=806 789x+2 998.8(R2=0.999 5)。所有分析均重复3次。
1.3.5 涩感感官分析
从宁夏大学葡萄酒研究中心招募10名品鉴小组成员(年龄22~30岁,包括6名女性和4名男性),小组成员均为葡萄酒及相关专业博士和硕士研究生,有至少2年以上葡萄酒感官分析经验,熟悉葡萄酒及涩感品鉴,味觉功能正常,身体健康,无吸烟史。所有品鉴小组成员均签署了书面知情同意书,符合《赫尔辛基宣言》的要求[19],并经宁夏大学科学技术伦理委员会批准。
涩感强度培训采用三角品尝法[20],使用不同浓度的商业单宁溶液(葡萄皮提取,Vinitan Advance,Lamothe-Abelt,法国)作为涩感强度溶液进行培训。培训中,小组成员对标有随机三位码的黑色标准品鉴杯中的6组质量浓度由低到高的单宁溶液(1.0、2.0、3.0、4.0、5.0、6.0 g/L)进行区分,从每组3杯(2杯溶液相同,1杯不同)中分辨出不同的溶液,并对6组中分辨出的6个不同质量浓度的溶液进行涩感强度评分并由低到高进行排序。
各取样点样品涩感强度评估采用QDA方法[21],3个阶段12个取样点样品随机编号,对涩感强度从低到高进行0~10评分,每次评估后提供水和饼干用于清除口腔中残留的涩感,每个样品重复评估3次。
1.3.6 单宁与唾液蛋白分子对接
使用AutoDock Vina 1.2.3软件对不同结构单宁与胰腺α-淀粉酶(panreatic alpha-amylase,PAA)进行分子对接研究[12]。受体选择PAA(PDB ID:1HNY),该结构是从RCSB PDB(https://www.rcsb.org/structure/1HNY)获取,并使用AutoDock Tools 1.5.7进行预处理,包括去除蛋白结构中水分子及其他非蛋白分子、添加氢原子、计算电荷。所有配体在ChemDraw 20.0中绘制,经Chem3D 20.0处理,并在MM2力场下进行能量最小化。以PAA共结晶配体的位置为对接中心,对接的彻底性设为8,能量范围设为3。每次对接运行产生9种构象及其对应得分。采用PyMOL 2.5.5对分子对接结果进行可视化,运用Protein-Ligand Interaction Profiler(PLIP)工具分析蛋白-配体相互作用[13, 22-23]。分析重点涵盖结合能、疏水作用、氢键、π-阳离子相互作用和π-堆叠等关键相互作用类型。
1.3.7 数据处理
使用Excel 2016收集汇总数据,使用R 4.4.1进行统计分析,通过多个R包进行数据处理和统计检验(其中Agricolae包进行单因素方差分析和最小显著差异检验)来比较显著性差异,显著性水平设定为0.05。结果使用Origin 2024b软件进行可视化。
2 结果与分析
2.1 红葡萄酒基本理化指标分析
赤霞珠红葡萄酒pH值为3.55,残糖含量为4.26 g/L,可滴定酸含量为7.10 g/L(以酒石酸计),酒精度为15.60%vol。指标均符合GB/T 15038—2006《葡萄酒、果酒通用分析方法(含第1号修改单)》对干红葡萄酒的要求。
赤霞珠红葡萄酒酿造过程中总酚含量发生显著变化(P<0.05)。如图2所示,在入罐到AF结束(比重降至1)时,总酚含量从起始的701.17 mg/L,显著上升至2 331.86 mg/L,苹果酸-乳酸发酵及陈酿期间,总酚含量有显著的下降趋势,但变化幅度不大,从峰值2 331.86 mg/L下降至1 959.51 mg/L后回升至2 247.43 mg/L。
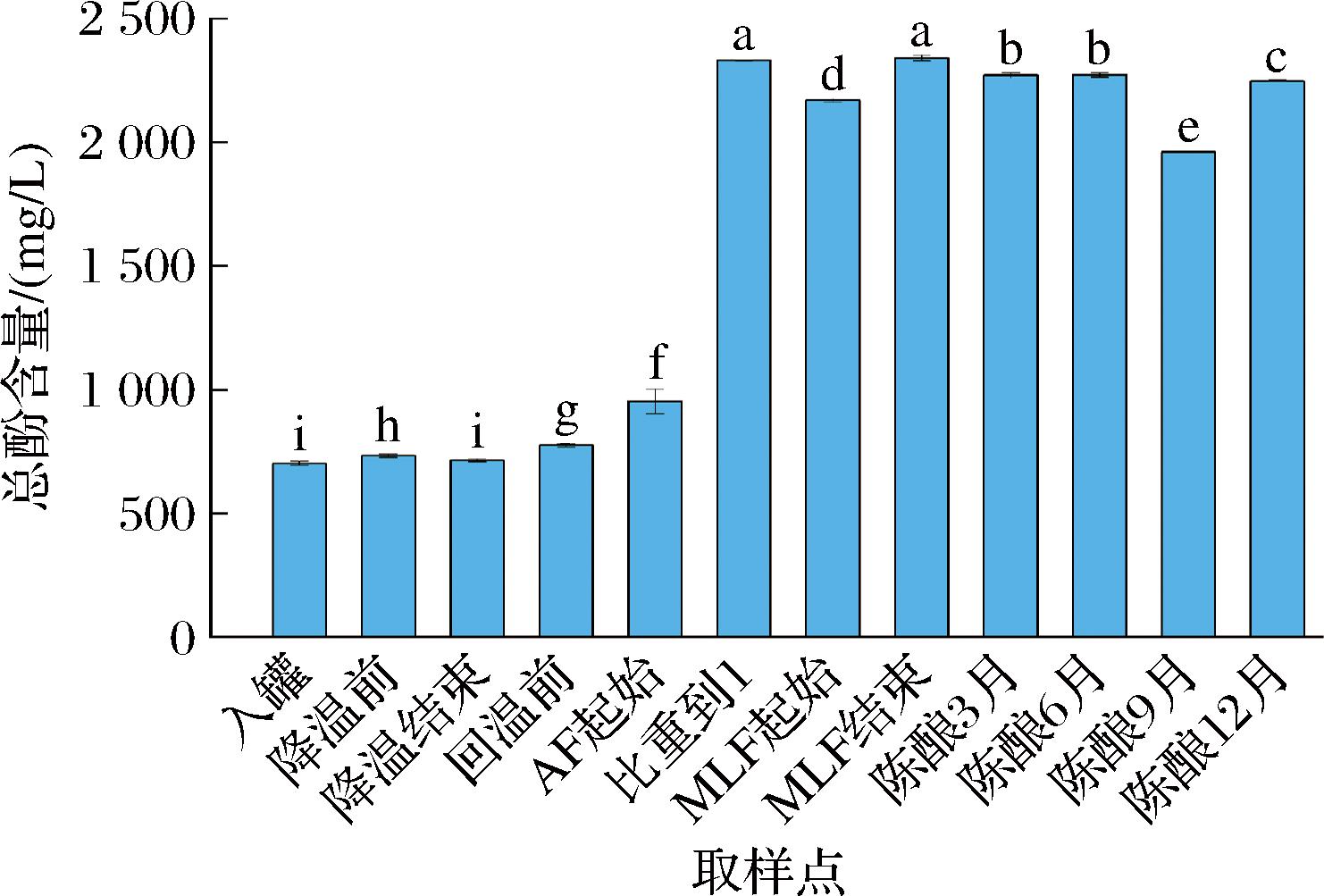
图2 红葡萄酒酿造过程中总酚含量变化
Fig.2 Evolution of total phenolic content during red wine winemaking
注:不同字母表示显著性差异(P<0.05)(下同)。
2.2 红葡萄酒酿造过程中单宁组分变化分析
如图3所示,儿茶素没食子酸酯类单宁百分比整体呈现上升趋势,在MLF2达到峰值(14%),随后缓慢下降。棓儿茶素类单宁百分比也呈现上升趋势,在AF2达到峰值(19%)后,在MLF2略微下降(12%)后趋于稳定。儿茶素类单宁整体呈下降趋势。3种类型单宁中,儿茶素类单宁含量最高。
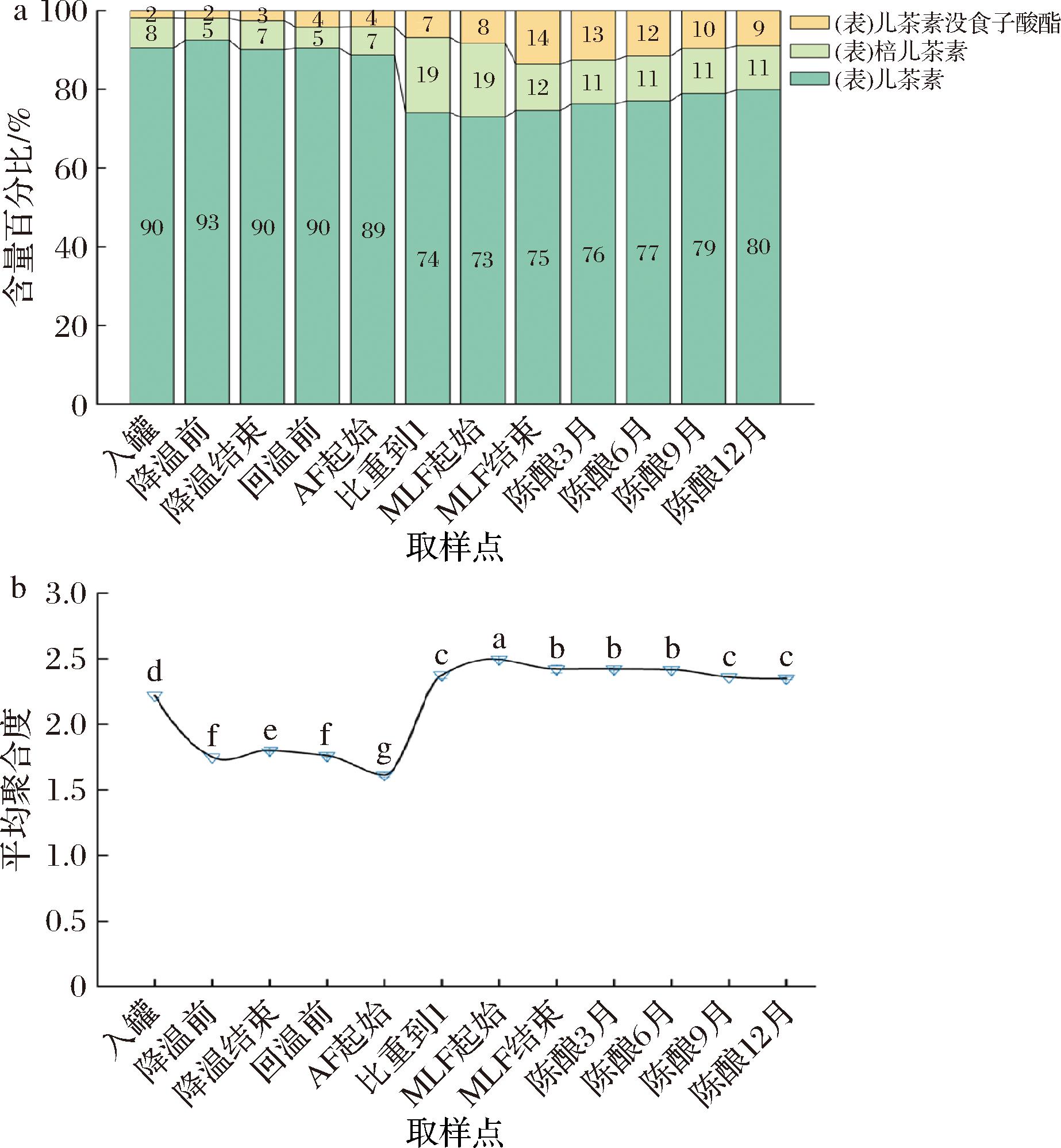
a-不同类型单宁比例变化;b-平均聚合度变化
图3 红葡萄酒酿造过程中单宁组分变化
Fig.3 Evolution of tannin composition during red wine winemaking
对赤霞珠红葡萄酒酿造过程中12个取样点样品平均聚合度检测显示,G1到AF1阶段聚合度持续下降,AF2显著提升在MLF1达到峰值后趋于平稳。
2.3 红葡萄酒酿造过程的单宁分子UPLC-Q-TOF非靶向代谢组分析
基于SONG等[24]的方法,对107种已鉴定的单宁分子进行热图分析,儿茶素类单宁变化趋势如图4-a所示,主要分3类。第1类先上升,在苹果酸-乳酸发酵结束左右达到峰值后在后续陈酿期间又呈现下降趋势,此类占多数,其中具体代表物质有DP1-1、DP1-2、DP2-1、DP2-3、DP2-4、DP3-3、DP3-6、DP3-7、DP3-8、DP3-9、DP4-3、DP4-5、DP4-6、DP5-1、DP5-2、DP5-3、DP5-4。第2类先上升,然后在苹果酸-乳酸发酵结束左右到达峰值但是并未呈现出明显的下降趋势而是一直保持在峰值处波动的现象,代表物质有DP2-5、DP2-6、DP3-2、DP3-4、DP4-1。第3类物质在整个过程中呈现持续上升的趋势,例如DP2-2、DP3-1、DP3-5、DP4-2、DP4-4。
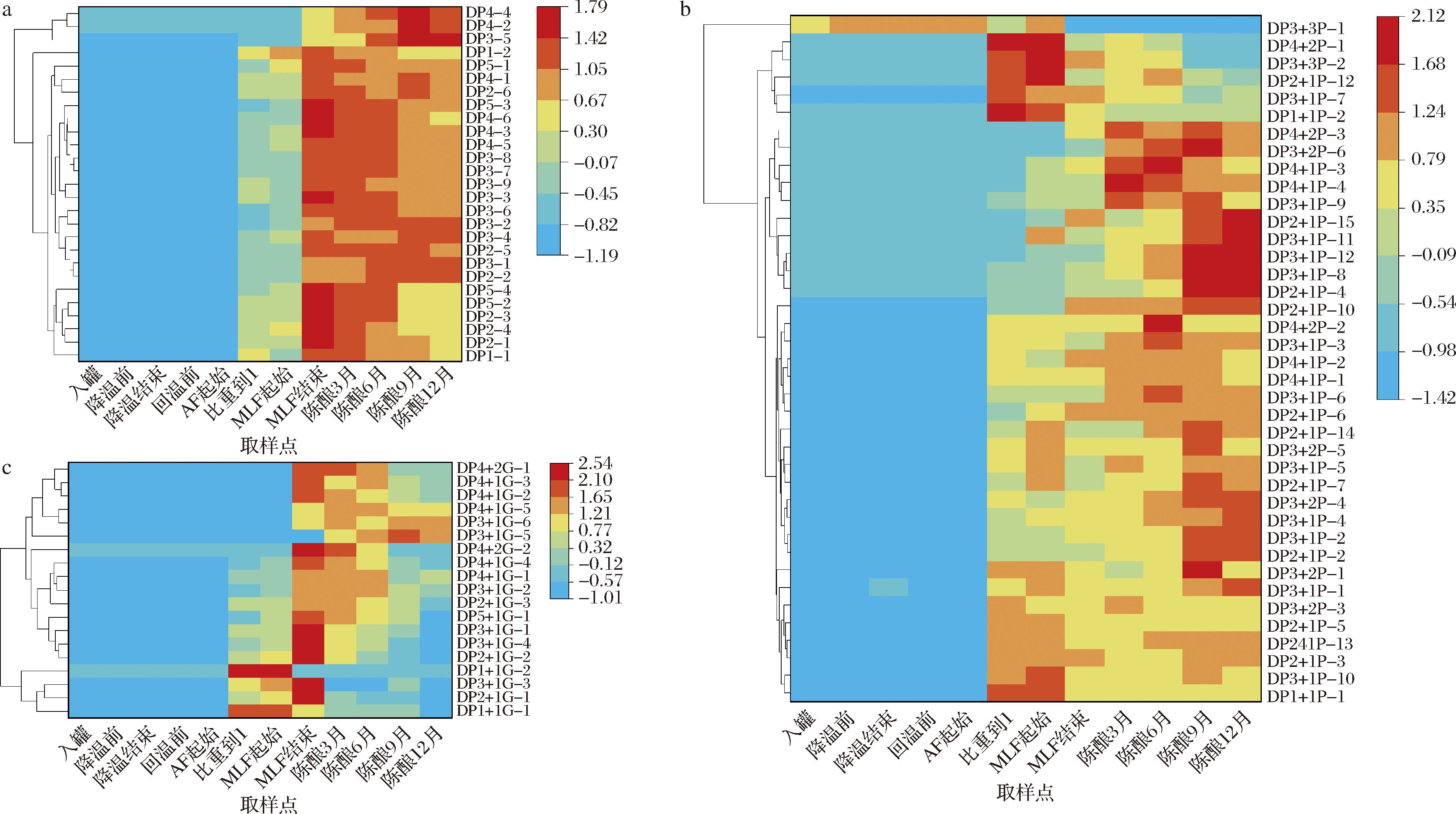
a-儿茶素类单宁;b-棓儿茶素类单宁;c-儿茶素没食子酸酯类单宁
图4 红葡萄酒酿造过程中单宁含量变化
Fig.4 Evolution of tannin content during red wine winemaking
注:单宁命名规则为聚合度+聚合单体数量-编号,编号代表该质荷比下物质在色谱峰中的保留时间排序。
棓儿茶素类单宁变化趋势如图4-b所示,也可分为3类。第1类上升后又下降的,该类物质又可分为2小类,其中峰值出现在苹果酸-乳酸发酵起始左右时的物质有DP1+1P-1、DP1+1P-2、DP2+1P-5、DP2+1P-12、DP2+1P-13、DP3+1P-10、DP3+1P-7、DP3+2P-3、DP3+3P-2、DP4+2P-1;峰值稍稍靠后出现在陈酿6月左右时的物质有DP3+1P-9、DP3+2P-6、DP4+1P-3、DP4+1P-4、DP4+2P-3。第2类物质先上升然后约在苹果酸-乳酸发酵结束时到达峰值然后呈现波动趋势,其代表物质有DP2+1P-3、DP2+1P-6、DP2+1P-7、DP2+1P-13、DP2+1P-14、DP3+1P-3、DP3+1P-5、DP3+1P-6、DP3+2P-5、DP4+1P-1、DP4+1P-2。第3类物质在整个过程中呈现持续上升的趋势,其代表物质有DP2+1P-2、DP2+1P-4、DP2+1P-10、DP2+1P-15、DP3+1P-1、DP3+1P-2、DP3+1P-4、DP3+1P-8、DP3+1P-11、DP3+1P-12、DP3+2P-1、DP3+2P-4。
儿茶素没食子酸酯类单宁变化趋势如图4-c,分为2类。第1类先上升后下降趋势的物质占大多数,其中峰值在苹果酸-乳酸发酵结束左右的物质占大多数包括DP1+1G-1、DP1+1G-2、DP2+1G-2、DP2+1G-3、DP3+1G-1、DP3+1G-2、DP3+1G-4、DP4+1G-1、DP4+1G-2、DP4+1G-3、DP4+1G-4、DP4+1G-5、DP4+2G-1、DP4+2G-2、DP5+1G-1仅有2种物质峰值出现在比重到1处,为DP1+1G-1、DP1+1G-2。另第2类上升后呈现较为稳定的物质也有2种,分别是DP3+1G-5和DP3+1G-6。
2.4 红葡萄酒酿造过程中涩感演变分析
QDA结果显示,赤霞珠红葡萄酒酿造过程中各取样点涩感强度有显著性差异,结果如图5所示。浸渍阶段(G1、G2、G3、G4)涩感强度整体呈现上升趋势,涩感强度评分从1.16上升到2.33,无显著性差异。发酵阶段涩感强度评分显著提高,苹果酸-乳酸发酵阶段(MLF1、MLF2)显著高于酒精发酵阶段(AF1、AF2)。陈酿各阶段(Age3、Age6、Age9、Age12)涩感强度评分无显著性差异,在Age12到达峰值6.92。
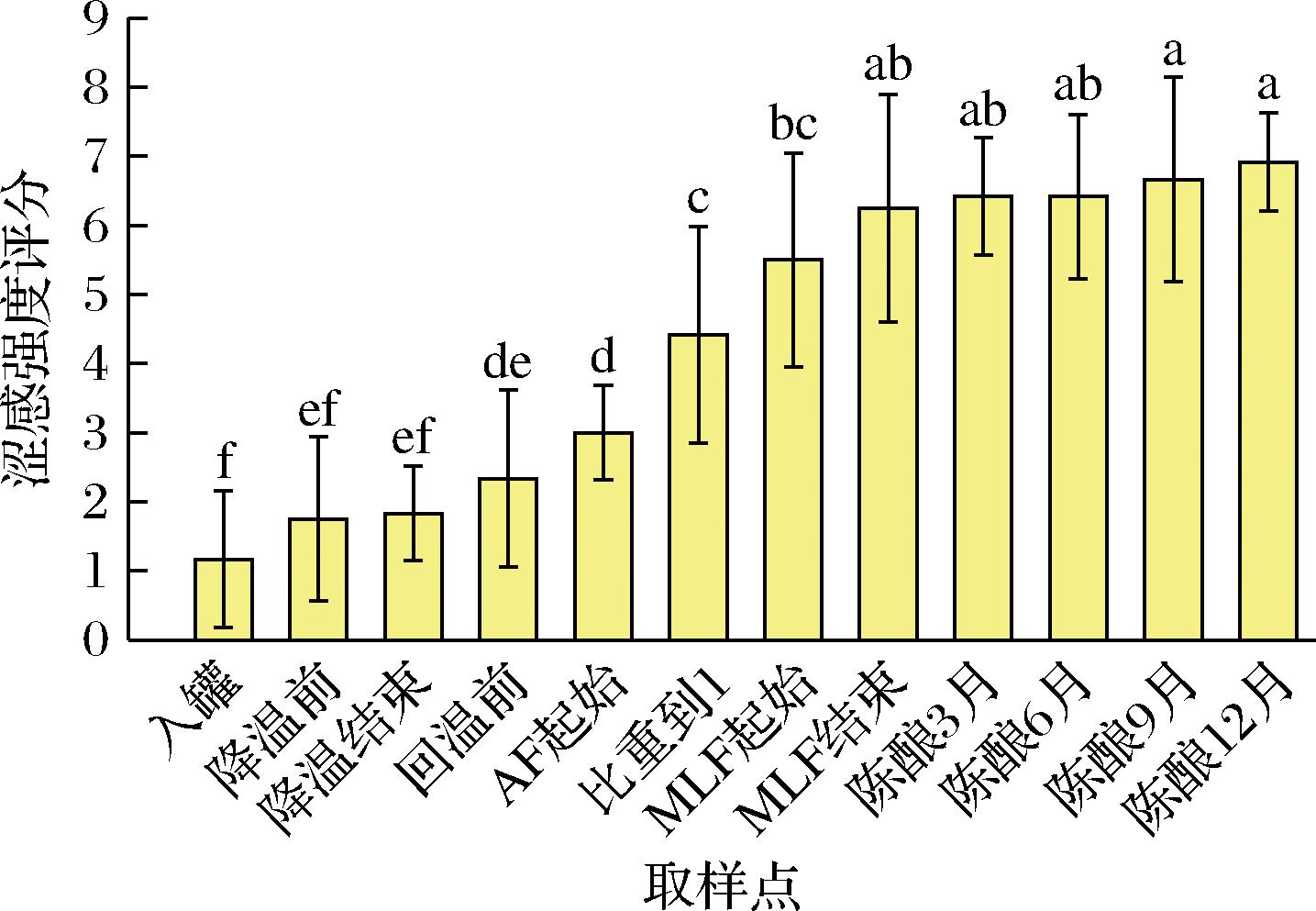
图5 红葡萄酒酿造过程中涩感强度变化
Fig.5 Evolution of astringency intensity during red wine winemaking
2.5 不同结构单宁与唾液蛋白相互作用机理分子模拟探究
儿茶素类单宁与胰腺α-淀粉酶分子对接结果如图6所示,使用绝对结合能直观表示结合强度的变化。随着聚合度增加,结合强度逐渐增加,在DP1时,绝对结合能为7.2 kcal/mol,在DP3时,达到9.4 kcal/mol的峰值,表现出最强的结合强度。疏水作用和氢键数量随着聚合度的增加而增加,氢键数量从DP1的2个增加到DP3的7个。疏水作用从DP1的3个增加到DP3的4个。π-堆叠数量DP2和DP3均为2。相互作用中氢键占主导地位,其次是疏水相互作用。
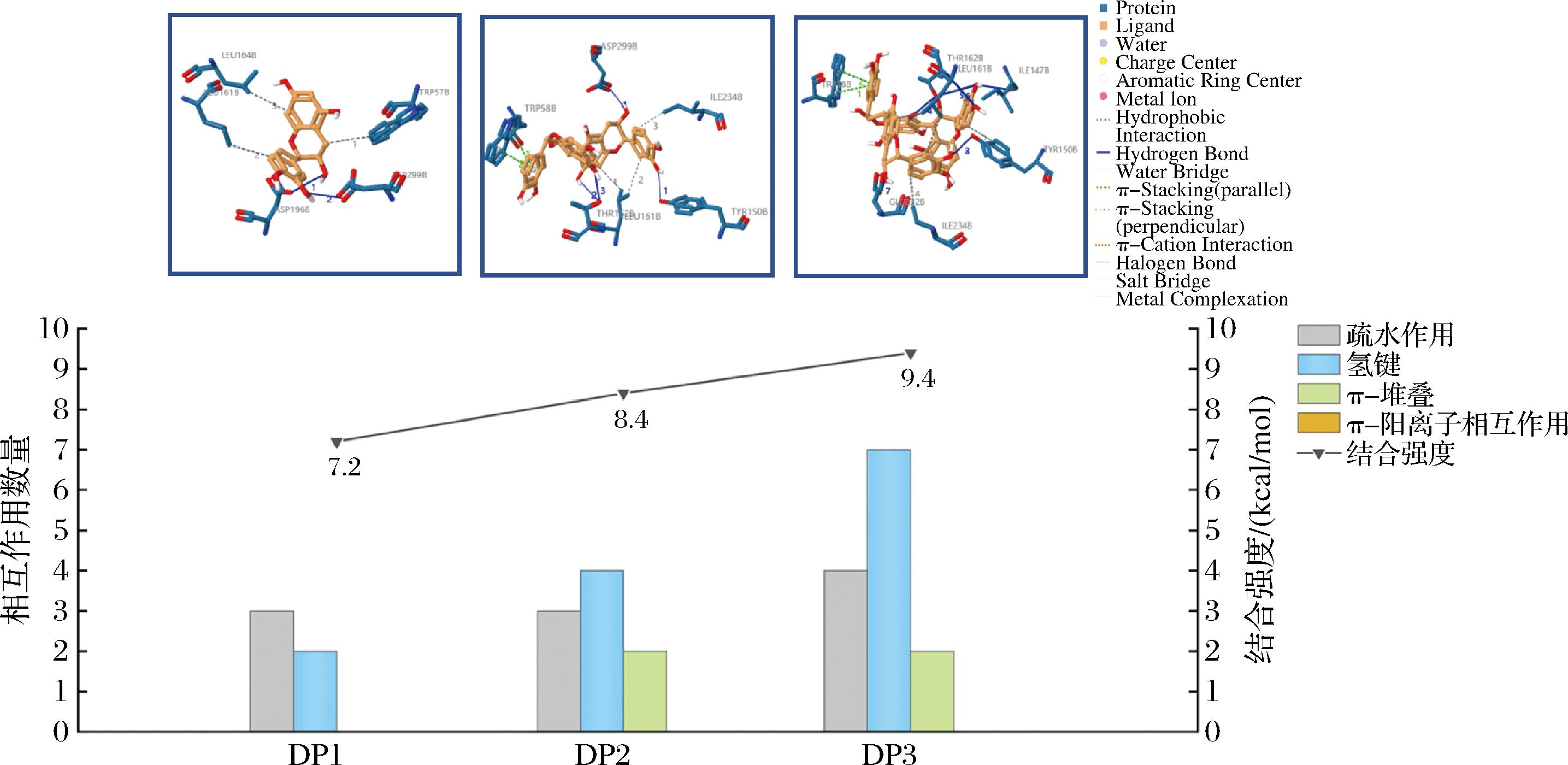
图6 不同聚合度的儿茶素类单宁与胰腺α-淀粉酶相互作用分析
Fig.6 Interaction analysis of catechin-type tannins with PAA at different degrees of polymerization
棓儿茶素类单宁与胰腺α-淀粉酶分子对接结果如图7所示,二聚体棓儿茶素单宁随着原花翠素比例(P)增加,结合强度略微降低。在DP2时,绝对结合能为8.4 kcal/mol,在DP2+2P时,略微降低到8.2 kcal/mol。疏水作用数量随着原花翠素比例增加,从DP2、DP2+1P的3个到DP2+2P的4个。氢键和π-堆叠数量随着原花翠素比例增加而减少,氢键数量从DP2的4个减少到DP2+2P的3个。π-堆叠数量从DP2、DP2+1P的2个减少到DP2+2P的1个。相互作用中疏水相互作用占主导地位,其次是氢键。
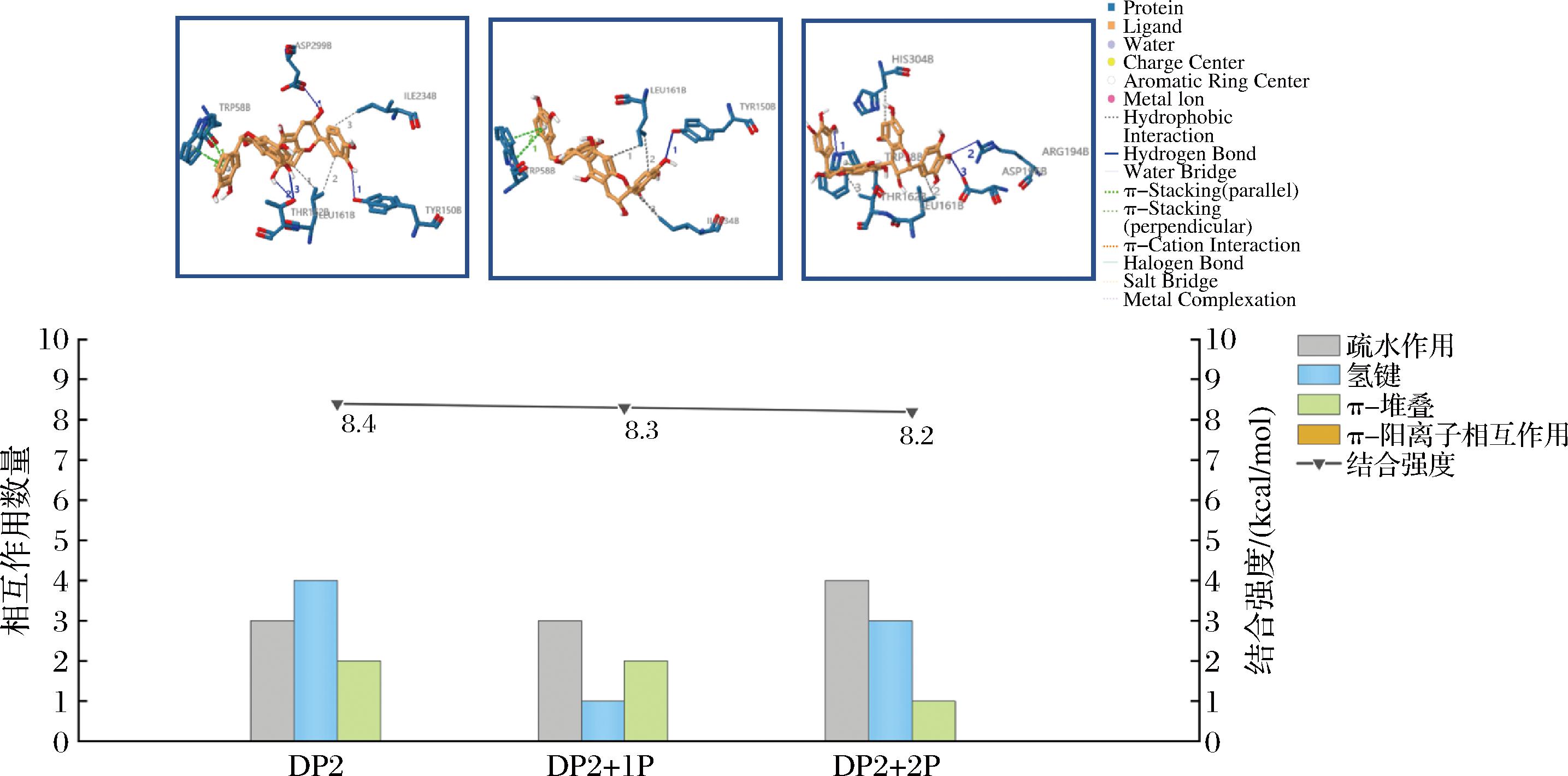
图7 不同原花翠素比例的棓儿茶素类单宁与胰腺α-淀粉酶相互作用分析
Fig.7 Interaction analysis of prodelphinidin-type tannins with PAA at different procyanidin proportions
儿茶素没食子酸酯类单宁与胰腺α-淀粉酶分子对接结果如图8所示,二聚体儿茶素没食子酸酯单宁随着没食子酸酯化程度(G)增加,结合强度逐渐增加。在DP2时,绝对结合能为8.4 kcal/mol,在DP2+2G时,达到9.7 kcal/mol的峰值,表现出最强的结合强度。疏水作用和氢键数量随着没食子酸酯化程度增加而增加,氢键数量从DP2的4个增加到DP2+2G的6个,DP2+1G时达到峰值7个。疏水作用从DP2的3个增加到DP2+2G的7个。π-堆叠数量随着没食子酸酯化程度增加而略微减少,DP2的π-堆叠数量为2,在DP2+1G和DP2+2G减少到1个。在DP2+2G还存在π-阳离子相互作用,在与胰腺α-淀粉酶结合过程中提供更强的结合能力。相互作用中氢键占主导地位,其次是疏水作用。
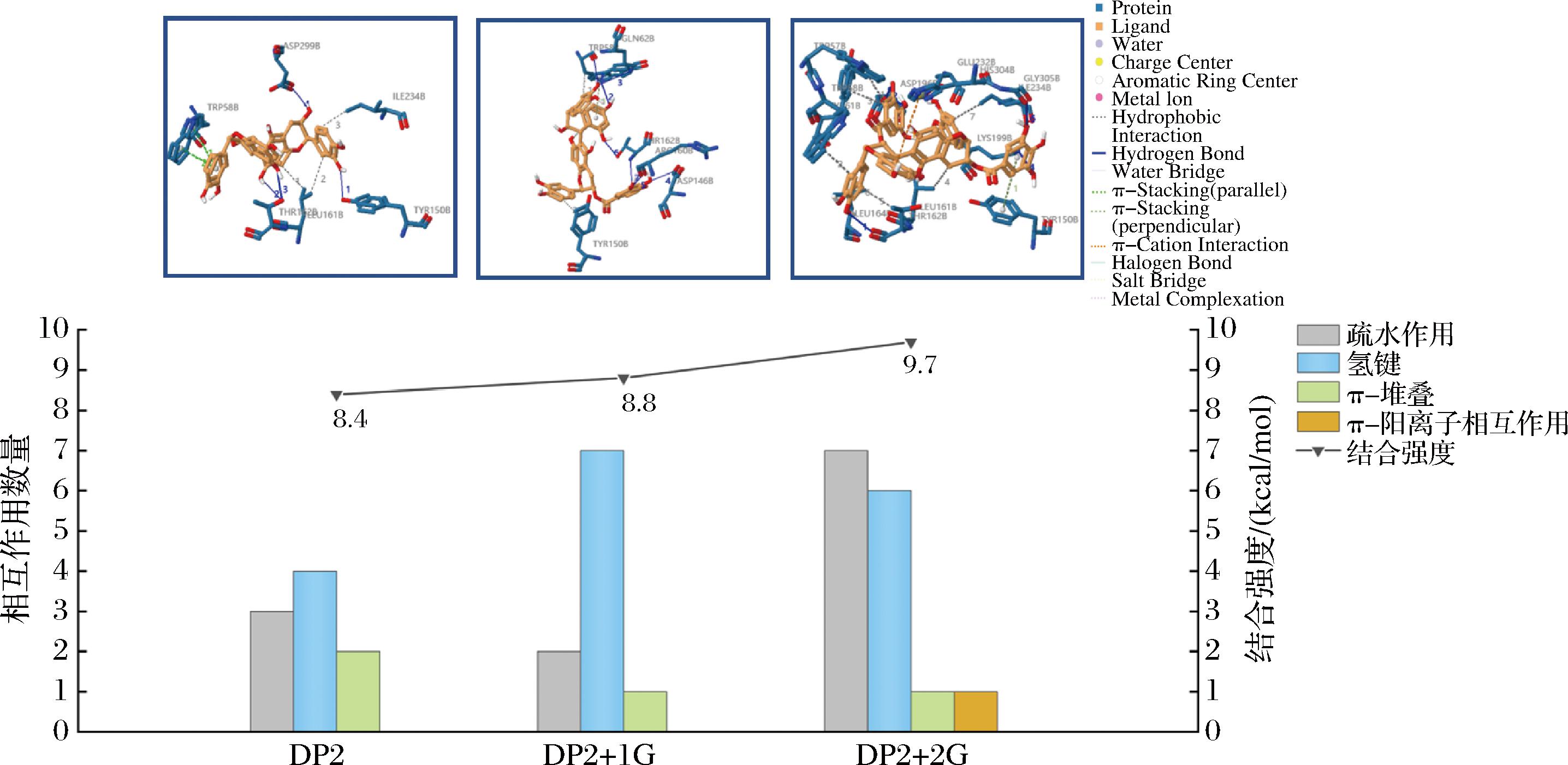
图8 不同酯化程度的儿茶素没食子酸酯类单宁与胰腺α-淀粉酶相互作用分析
Fig.8 Interaction analysis of catechin gallate-type tannins with PAA at different degrees of galloylation
3 讨论
在赤霞珠红葡萄酒酿造过程中总酚含量变化显著,与浸渍阶段相比,发酵和陈酿阶段含量显著升高。这与之前的研究结果一致[25],由于冷浸渍过程中葡萄醪的环境条件(无乙醇、低温、无酶活性等),只有少量酚类物质被浸提到葡萄汁中。随着环境条件(pH、酒精度和温度)的改变,大量酚类物质在发酵及陈酿过程中被浸提出来,总酚含量显著提高。陈酿过程中总酚含量在陈酿9个月时下降。这一现象可能是因为在陈酿9个月时瓶储环境温度升高,提高了酚类物质与多糖、花色苷等组分形成不溶性复合物的反应速率。此外,还可能是因为在对该取样点取样测量时,由于葡萄酒样品未被充分摇匀,偶然测量误差对该取样点测量结果产生影响。
在整个酿造过程中各类型单宁变化明显,儿茶素类单宁在酿酒过程中呈下降趋势,棓儿茶素类单宁和儿茶素没食子酸酯类单宁呈上升趋势后趋于稳定[26]。儿茶素类单宁比例下降可能是因为其结构不稳定,在酿酒过程中易发生氧化、降解和聚合反应。相反,棓儿茶素类单宁和儿茶素没食子酸酯类单宁表现出更好的稳定性,不易被氧化分解,因此在酿酒过程中比例逐渐增加[3]。平均聚合度在酒精发酵过程中快速增长,在苹果酸-乳酸发酵阶段达到峰值,在陈酿阶段趋于稳定。BOIDO等[27]认为,这一趋势可能是因为在发酵过程中,随着酒精度、温度升高等因素影响,促进了聚合反应的发生,导致平均聚合度显著上升。在陈酿阶段,随着陈酿时间延长,单宁结构趋于稳定,平均聚合度趋于平稳。
红葡萄酒酿造过程的单宁分子UPLC-Q-TOF非靶向代谢组学分析中。儿茶素类单宁的演变呈现多样性。大部分儿茶素类单宁(如DP1-1、DP2-1等)表现为先升高,在苹果酸-乳酸发酵结束左右达到峰值后于陈酿中下降的趋势,可能是因为浸渍过程中升高随后伴随着氧化、聚合及沉淀等转化损耗逐渐降低[28-29]。少数单宁(如DP2-5、DP4-1等)在达到峰值后保持相对稳定,可能源于其结构的稳定性或达到了生成与转化的动态平衡。部分单宁(如DP2-2、DP4-2等)在整个酿造及陈酿过程中持续上升,主要是通过小分子前体的聚合反应不断生成,形成了更复杂的结构[30]。棓儿茶素类单宁的变化趋势同样复杂。部分物质(如DP1+1P-1、DP2+1P-5等)峰值出现在苹果酸-乳酸发酵起始左右便开始下降,可能与其较高的反应活性和较早的转化有关。而另一些(如DP3+1P-9、DP4+1P-3等)峰值则出现在陈酿6个月,表明形成较晚或初期相对稳定。部分棓儿茶素类单宁(如DP2+1P-3、DP3+1P-3等)也表现出先升高后趋于稳定的模式。此外,持续上升的种类(如DP2+1P-2、DP3+1P-1等)表明含有棓儿茶素单元的更复杂单宁仍在不断形成中。棓儿茶素类单宁B环更多的羟基对氧化或亲电取代反应有更高的易感性。因此更容易转化为更复杂的聚合结构中。儿茶素没食子酸酯类单宁大多数与儿茶素类相似,趋势呈现先升后降(峰值在苹果酸-乳酸发酵结束左右),少数在酒精发酵结束时即达峰值,同样温度的升高和酒精度逐渐增加是关键因素。乙醇作为有机溶剂,显著增强了酚类物质从葡萄皮和籽中的浸渍效果。温度升高则进一步加速了分子的扩散和溶解过程。极少数呈现先升后稳的没食子酰化单宁,可能是因为没食子酰基的存在显著修饰了单宁分子的极性和空间构象。在葡萄酒陈酿环境下,因为其特定的三维结构可能使得易于水解的酯键、易于氧化的酚羟基或易于参与聚合反应的位点被有效保护,不易被其他反应物接触到,对水解、氧化及进一步聚合等转化途径表现出显著抗性[31]。
在红葡萄酒酿造过程中,基于QDA感官分析结果表明,涩感强度具有阶段性特征,呈现发酵阶段显著增长后在陈酿阶段趋于稳定的趋势。葡萄破碎后入罐时间点表现出最弱的涩感强度,基本理化指标分析中总酚含量同样处于最低水平,与较低的涩感强度感知具有一致性。但表现出较高的平均聚合度,MA等[18]研究表明聚合度与唾液蛋白结合能力呈现正相关,与感官分析中低涩感强度不符。这一现象可能是因为该取样点单宁组分中较高的棓儿茶素类单宁比例。分子对接结果表明,随着原花翠素比例增加,棓儿茶素类单宁与胰腺α-淀粉酶结合强度略微降低,氢键和π-堆叠数量减少,导致涩感强度降低。发酵阶段,总酚含量与平均聚合度均显著升高,分子对接结果进一步表明,随着单宁聚合度升高,其与胰腺α-淀粉酶间结合强度增强,疏水相互作用、氢键、π-堆叠等非共价相互作用数量增加。同时发酵阶段儿茶素没食子酸酯类单宁比例也大幅提高,分子对接结果表明,相同聚合度下,没食子酸酯化程度增加,单宁与胰腺α-淀粉酶间结合强度大幅增强,疏水作用、氢键数量增加。与感官层面涩感强度显著升高表现出一致性。在陈酿阶段,尽管感官评分结果表明,涩感强度评分略有升高,但并未表现出显著性差异(P>0.05)。这一现象可能是因为单宁组分分析中陈酿阶段(表)儿茶素比例逐渐升高,同时代谢组学结果表明DP3-1、DP3-3、DP3-4、DP3-5等儿茶素类单宁随着陈酿进行逐渐积累,DP1-1、DP1-2、DP2-3等儿茶素类单宁含量逐渐降低。分子对接结果表明,随着儿茶素聚合度升高,单宁与胰腺α-淀粉酶间结合强度大幅增强,涩感强度增加。这些结果共同表明,赤霞珠红葡萄酒瓶中陈酿12个月时单宁的转化尚处于复杂阶段,葡萄酒中较高聚合度的单宁水解程度较低,单体及较低聚合度的单宁含量不足以引起涩感强度显著降低。
4 结论
本研究通过UPLC-Q-TOF非靶向代谢组学分析了赤霞珠红葡萄酒酿造过程12个关键点单宁及涩感感知变化,并通过分子对接技术探究涩感变化机理。结果表明:红葡萄酒酿造过程中总酚含量与涩感强度均在发酵阶段显著增加,在陈酿阶段趋于稳定。单宁组分变化结果表明,不同类型单宁在酿造过程中呈现复杂动态演变,儿茶素类单宁比例最高,整体呈现下降趋势,而棓儿茶素类和儿茶素没食子酸酯类单宁则表现为先升高在发酵阶段达到峰值(分别为19%和14%)后趋于稳定。单宁的平均聚合度在酒精发酵期间迅速上升,并在苹果酸-乳酸发酵开始时达到峰值,随后在陈酿阶段维持相对稳定;非靶向代谢组学分析结果表明儿茶素类单宁的演变呈现多样性:大部分(DP1-1、DP2-1等)表现为先升高,在苹果酸-乳酸发酵结束左右达到峰值后于陈酿中下降;少数(DP2-5、DP4-1等)在达到峰值后保持相对稳定;部分(DP2-2、DP4-2等)在整个酿造及陈酿过程中持续上升。棓儿茶素类单宁的变化趋势复杂:部分物质(DP1+1P-1、DP2+1P-5等)峰值出现在苹果酸-乳酸发酵起始左右并开始下降;另一些(DP3+1P-9、DP4+1P-3等)峰值出现在陈酿6个月;部分(DP2+1P-3、DP3+1P-3等)表现为先升高后趋于稳定;持续上升的种类(如DP2+1P-2、DP3+1P-1等)也被观察到。儿茶素没食子酸酯类单宁大多数(DP1+1G-1、DP2+1G-1等)与儿茶素类相似,趋势呈现先升后降(峰值在苹果酸-乳酸发酵结束左右),少数在酒精发酵结束时即达峰值。极少数呈现先升后稳的趋势;分子对接结果表明单宁与胰腺α-淀粉酶间相互作用主要以氢键和疏水相互作用为主,儿茶素类单宁随聚合度增加结合强度逐渐增强,棓儿茶素类单宁随原花翠素比例增加结合强度略微降低,儿茶素没食子酸酯类单宁随酯化程度增加结合强度大幅增加。研究结果为揭示红葡萄酒酿造过程中单宁复杂结构演变对涩感感知变化的影响提供了一定的理论基础。
[1] MA W, WAFFO-TÉGUO P, JOURDES M, et al.First evidence of epicatechin vanillate in grape seed and red wine[J].Food Chemistry, 2018, 259:304-310.
[2] YU K J, DIXON R A, DUAN C Q.A role for ascorbate conjugates of (+)-catechin in proanthocyanidin polymerization[J].Nature Communications, 2022, 13(1):3425.
[3] MA W, GUO A Q, ZHANG Y L, et al.A review on astringency and bitterness perception of tannins in wine[J].Trends in Food Science &Technology, 2014, 40(1):6-19.
[4] 张云伟, 白天华, 王礼, 等.葡萄酒加工废弃物的资源化利用研究进展[J].食品与发酵工业, 2024, 50(1):302-310.
ZHANG Y W, BAI T H, WANG L, et al.Recent advances on resource utilization of wine wastes[J].Food and Fermentation Industries, 2024, 50(1):302-310.
[5] GAWEL R.Red wine astringency:A review[J].Australian Journal of Grape and Wine Research, 1998, 4(2):74-95.
[6] WANG S Y, SMYTH H E, OLARTE MANTILLA S M, et al.Astringency and its sub-qualities:A review of astringency mechanisms and methods for measuring saliva lubrication[J].Chemical Senses, 2024, 49:bjae016.
[7] RAMOS-PINEDA A M, CARPENTER G H, GARC A-ESTÉVEZ I, et al.Influence of chemical species on polyphenol-protein interactions related to wine astringency[J].Journal of Agricultural and Food Chemistry, 2020, 68(10):2948-2954.
A-ESTÉVEZ I, et al.Influence of chemical species on polyphenol-protein interactions related to wine astringency[J].Journal of Agricultural and Food Chemistry, 2020, 68(10):2948-2954.
[8] DELCAMBRE A, SAUCIER C.Identification of new flavan-3-ol monoglycosides by UHPLC-ESI-Q-TOF in grapes and wine[J].Journal of Mass Spectrometry, 2012, 47(6):727-736.
[9] ZENG L M, TEISS DRE P L, JOURDES M.Structures of polymeric pigments in red wine and their derived quantification markers revealed by high-resolution quadrupole time-of-flight mass spectrometry[J].Rapid Communications in Mass Spectrometry, 2016, 30(1):81-88.
DRE P L, JOURDES M.Structures of polymeric pigments in red wine and their derived quantification markers revealed by high-resolution quadrupole time-of-flight mass spectrometry[J].Rapid Communications in Mass Spectrometry, 2016, 30(1):81-88.
[10] LI S Y, DUAN C Q.Astringency, bitterness and color changes in dry red wines before and during oak barrel aging:An updated phenolic perspective review[J].Critical Reviews in Food Science and Nutrition, 2019, 59(12):1840-1867.
[11] PAISSONI M A, MOTTA G, GIACOSA S, et al.Mouthfeel subqualities in wines:A current insight on sensory descriptors and physical-chemical markers[J].Comprehensive Reviews in Food Science and Food Safety, 2023, 22(4):3328-3365.
[12] TROTT O, OLSON A J.AutoDock Vina:Improving the speed and accuracy of docking with a new scoring function, efficient optimization, and multithreading[J].Journal of Computational Chemistry, 2010, 31(2):455-461.
[13] ZHAO Q H, DU G R, WANG S N, et al.Investigating the role of tartaric acid in wine astringency[J].Food Chemistry, 2023, 403:134385.
[14] 孙晓涵, 张雪, 石宝晖, 等.葡萄酒中非生物代谢来源有害物质的研究进展[J].食品与发酵工业, 2024, 50(5):334-340.
SUN X H, ZHANG X, SHI B H, et al.Advances in the study of harmful substances of non-biological metabolic origin in wine[J].Food and Fermentation Industries, 2024, 50(5):334-340.
[15] PU D D, MENG R X, QIAO K N, et al.Electronic tongue, proton-transfer-reaction mass spectrometry, spectral analysis, and molecular docking characterization for determining the effect of α-amylase on flavor perception[J].Food Research International, 2024, 181:114078.
[16] VIGNAULT A, GONZ LEZ-CENTENO M R, PASCUAL O, et al.Chemical characterization, antioxidant properties and oxygen consumption rate of 36 commercial oenological tannins in a model wine solution[J].Food Chemistry, 2018, 268:210-219.
LEZ-CENTENO M R, PASCUAL O, et al.Chemical characterization, antioxidant properties and oxygen consumption rate of 36 commercial oenological tannins in a model wine solution[J].Food Chemistry, 2018, 268:210-219.
[17] KENNEDY J A, JONES G P.Analysis of proanthocyanidin cleavage products following acid-catalysis in the presence of excess phloroglucinol[J].Journal of Agricultural and Food Chemistry, 2001, 49(4):1740-1746.
[18] MA W, WAFFO-TEGUO P, JOURDES M, et al.Chemical affinity between tannin size and salivary protein binding abilities:Implications for wine astringency[J].PLoS One, 2016, 11(8):e0161095.
[19] MORRIS K.Revising the declaration of Helsinki[J].Lancet, 2013, 381(9881):1889-1890.
[20] GAMBUTI A, RINALDI A, PESSINA R, et al.Evaluation of aglianico grape skin and seed polyphenol astringency by SDS-PAGE electrophoresis of salivary proteins after the binding reaction[J].Food Chemistry, 2006, 97(4):614-620.
[21] DEHLHOLM C, BROCKHOFF P B, MEINERT L, et al.Rapid descriptive sensory methods-comparison of free multiple sorting, partial napping, napping, flash profiling and conventional profiling[J].Food Quality and Preference, 2012, 26(2):267-277.
[22] ADASME M F, LINNEMANN K L, BOLZ S N, et al.PLIP 2021:Expanding the scope of the protein-ligand interaction profiler to DNA and RNA[J].Nucleic Acids Research, 2021, 49(W1):W530-W534.
[23] CUI Z Y, ZHANG N L, ZHOU T X, et al.Conserved sites and recognition mechanisms of T1R1 and T2R14 receptors revealed by ensemble docking and molecular descriptors and fingerprints combined with machine learning[J].Journal of Agricultural and Food Chemistry, 2023, 71(14):5630-5645.
[24] SONG L N, SUN X H, SHI B H, et al.Chemosensory analysis of condensed tannins and their astringency perception in Marselan, Cabernet Sauvignon and Merlot red wine during winemaking[J].LWT, 2024, 212:116983.
[25] CHIRA K, JOURDES M, TEISSEDRE P L.Cabernet sauvignon red wine astringency quality control by tannin characterization and polymerization during storage[J].European Food Research and Technology, 2012, 234(2):253-261.
[26] GONZALO-DIAGO A, DIZY M, FERN NDEZ-ZURBANO P.Taste and mouthfeel properties of red wines proanthocyanidins and their relation to the chemical composition[J].Journal of Agricultural and Food Chemistry, 2013, 61(37):8861-8870.
NDEZ-ZURBANO P.Taste and mouthfeel properties of red wines proanthocyanidins and their relation to the chemical composition[J].Journal of Agricultural and Food Chemistry, 2013, 61(37):8861-8870.
[27] BOIDO E, GARC A-MARINO M, DELLACASSA E, et al.Characterisation and evolution of grape polyphenol profiles of Vitis vinifera L.cv.Tannat during ripening and vinification[J].Australian Journal of Grape and Wine Research, 2011, 17(3):383-393.
A-MARINO M, DELLACASSA E, et al.Characterisation and evolution of grape polyphenol profiles of Vitis vinifera L.cv.Tannat during ripening and vinification[J].Australian Journal of Grape and Wine Research, 2011, 17(3):383-393.
[28] CASASSA L F, HARBERTSON J F.Extraction, evolution, and sensory impact of phenolic compounds during red wine maceration[J].Annual Review of Food Science and Technology, 2014, 5:83-109.
[29] DESHAIES S, GARCIA F, SUC L, et al.Study of the oxidative evolution of tannins during Syrah red wines ageing by tandem mass spectrometry[J].Food Chemistry, 2022, 385:132538.
[30] CHEYNIER V, DUE AS-PATON M, SALAS E, et al.Structure and properties of wine pigments and tannins[J].American Journal of Enology and Viticulture, 2006, 57(3):298-305.
AS-PATON M, SALAS E, et al.Structure and properties of wine pigments and tannins[J].American Journal of Enology and Viticulture, 2006, 57(3):298-305.
[31] FABRE S, PINAUD N, FOUQUET É, et al.Colloidal behavior of wine galloylated tannins[J].Comptes Rendus Chimie, 2010, 13(5):561-565.