全谷物作为健康膳食的重要组成部分,其富含的膳食纤维、维生素及植物化学物质在慢性疾病预防中具有独特优势[1]。尤为值得注意的是,全谷物中多酚类物质因其抗氧化、抗炎等生理功能成为研究热点,但天然存在的结合态多酚因其结构复杂性导致生物可及性不足,严重制约其功能发挥[2]。近年来,微生物发酵技术通过靶向调控多酚转化路径,为破解这一难题提供了创新突破口。
发酵技术在提升全谷物食品的营养价值和健康功效方面展现出巨大潜力。它不仅能改善产品的品质和感官特性,还能通过降低血糖值、调节多酚含量及其生物可及性,增强多酚的生物利用度。在发酵过程中,微生物利用其代谢酶系对多酚等生物活性物质进行转化,通过水解、甲基化、糖基化和酯化等反应改变多酚的分子结构,增加其溶解性,提高生物利用度[3],并可能进一步生成新的生物活性物质。
多酚的生物利用度常因其结构复杂性和生物可及性受限。探究发酵中天然多酚的转化机制,可深化对微生物影响多酚结构与功能的理解,为开发高生物利用度的多酚产品提供科学依据。借助发酵调控多酚生物转化,并利用多组学技术系统解析其机制,能设计开发具有特定健康益处的全谷物功能食品。这不仅为发酵全谷物中天然多酚的生物转化提供了理论支持,也为我国全谷物食品产业的技术创新和消费者对保健功能食品的需求满足提供了帮助,进而推动产业进步和满足大众健康需求。
1 全谷物及其天然多酚
1.1 全谷物中多酚的结构与分类
全谷物是指未经精细加工,或虽经碾磨、粉碎、压片等处理,但依然保留完整谷粒的麸皮、胚乳、胚芽及其天然营养成分的谷物。作为植物次生代谢产物的天然多酚,在全谷物中展现出显著的多样性,其种类、含量及分布受谷物品种、基因型及环境条件影响。
全谷物中多酚类物质的多样性如图1所示,主要包括酚酸类和类黄酮化合物两大类别。其中酚酸类占比超80%,分为C6-C1骨架的羟基苯甲酸和C6-C3骨架的羟基肉桂酸衍生物。羟基苯甲酸类的香草酸和原儿茶酸在燕麦和黑麦中含量较高;羟基肉桂酸类的阿魏酸和对香豆酸则主要富集于麸皮和糊粉层[4]。小麦麸皮中阿魏酸含量可达干重的0.5%~1.5%,其与阿拉伯木聚糖酯键结合形成细胞壁重要组分。此外,麸皮组织的次级代谢产物呈空间特异性分布,类黄酮物质中的槲皮素、山柰酚等黄酮醇以及芹菜素等黄酮主要集中在胚芽和种皮区域[5]。
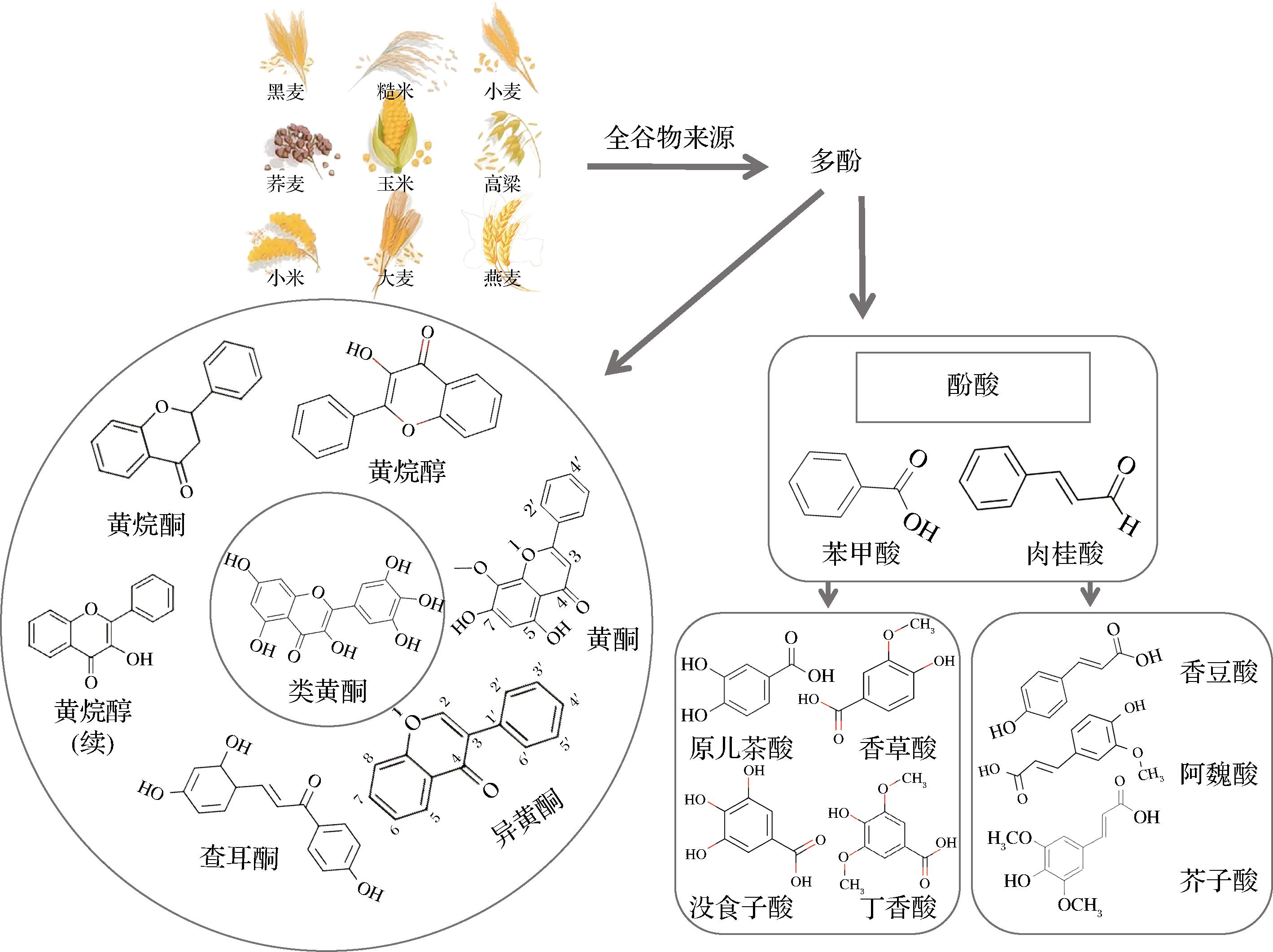
图1 全谷物中多酚类物质的分类
Fig.1 Classification of polyphenols in whole grains
1.2 天然多酚的存在形式及其主要生物活性
全谷物中的天然多酚主要分为酚酸类和类黄酮化合物。如表1所示,多酚以游离态和结合态形式存在,其中结合态占比高达70%~90%。游离态多酚主要包括阿魏酸、对香豆酸、咖啡酸、原儿茶酸及槲皮素等;结合态多酚则多为糖苷衍生物或与细胞壁结合的酚酸。不同的谷物具有独特成分,如荞麦含芦丁,玉米和高粱含矢车菊素-3-O-葡萄糖苷,而燕麦以芦丁和绿原酸为主[21]。酚酸类化合物通过酯键、醚键或糖苷键与细胞壁多糖结合,其生物活性与结构密切相关。例如,3-甲氧基-4-羟基肉桂酸的邻位甲氧基和羟基可协同清除自由基,其抗氧化能力显著强于香豆酸[22]。类黄酮化合物则以C6-C3-C6骨架为特征,B环羟基化程度决定其抑制α-葡萄糖苷酶的能力,进而调控餐后血糖。糖基化修饰虽增强水溶性,但会降低肠道吸收率[23]。微生物发酵通过β-葡萄糖苷酶水解糖苷键释放高活性苷元,显著提升其抗炎和抗肿瘤潜力,因此加工方式对生物利用度至关重要。
表1 全谷物中多酚的组成和存在形式
Table 1 Composition and forms of polyphenols present in whole grains

谷物物种游离态多酚结合态多酚参考文献黑麦阿魏酸、对香豆酸、咖啡酸、香草酸、原儿茶酸、芹菜素、木犀草素、山奈酚、槲皮素阿魏酸、对香豆酸、芥子酸、咖啡酸、香草酸、丁香酸、芹菜素-7-O-葡萄糖苷、木犀草素-7-O-葡萄糖苷、柚皮素[6-7]糙米阿魏酸、咖啡酸、丁香酸、原儿茶酸、绿原酸、香豆酸、水杨酸、邻香豆酸、丁香酚、2,4-二羟基苯甲醛,芥子酸、2-羟基肉桂酸、槲皮素、山奈酚、异鼠李素阿魏酸、绿原酸、咖啡酸、丁香酸、香草酸、对香豆酸、对羟基苯甲酸、丁香酚、原儿茶酸、邻香豆酸,2,4-二羟基苯甲醛、芥子酸、槲皮素-3-O-葡萄糖苷、山奈酚-3-O-葡萄糖苷、矢车菊素-3-O-葡萄糖苷[8-9]小麦没食子酸、原儿茶酸、绿原酸、咖啡酸、丁香酸、阿魏酸、香草酸、对香豆酸、对羟基苯甲酸、槲皮素、山奈酚、芹菜素没食子酸、丁香酸、阿魏酸、香草酸、对香豆酸、异戊酸、槲皮素-3-O-葡萄糖苷、山奈酚-3-O-葡萄糖苷、芹菜素-6-C-葡萄糖苷、柚皮素[10-11]荞麦咖啡酸、对香豆酸、阿魏酸、原儿茶酸、介子酸、芦丁、槲皮素、山奈酚、异槲皮苷阿魏酸、对香豆酸、咖啡酸、原儿茶酸、香草酸、芥子酸、槲皮素-3-O-葡萄糖苷、黄酮醇阿魏酸酯[12-13]玉米阿魏酸,咖啡酸,没食子酸,对香豆酸,邻香豆酸,槲皮素、山奈酚、杨梅素阿魏酸、咖啡酸、对香豆酸、对羟基苯甲酸、紫丁香酸、原儿茶酸、槲皮素-3-O-葡萄糖苷、山奈酚-3-O-葡萄糖苷、异鼠李素-3-O-芸香糖苷、矢车菊素-3-O-葡萄糖苷[14-15]高粱阿魏酸、对香豆酸、咖啡酸、原儿茶酸、介子酸、槲皮素、山奈酚、异鼠李素、芹菜素阿魏酸、对香豆酸、咖啡酸、原儿茶酸、介子酸、香草酸、槲皮素-3-O-葡萄糖苷、山奈酚-3-O-葡萄糖苷、异鼠李素-3-O-芸香糖苷、矢车菊素-3-O-葡萄糖苷[16]
续表1

谷物物种游离态多酚结合态多酚参考文献小米阿魏酸、对香豆酸、咖啡酸、原儿茶酸、香草酸、槲皮素、山奈酚、异鼠李素、木犀草素阿魏酸、对香豆酸、芥子酸、咖啡酸、原儿茶酸、香草酸、槲皮素-3-O-葡萄糖苷、山奈酚-3-O-葡萄糖苷、异鼠李素-3-O-芸香糖苷、柚皮素[17-18]大麦阿魏酸、对香豆酸、咖啡酸、香草酸、槲皮素、山奈酚、芹菜素阿魏酸、对香豆酸、芥子酸、咖啡酸、原儿茶酸、香草酸、槲皮素-3-O-葡萄糖苷、山奈酚-3-O-葡萄糖苷、芹菜素-6-C-葡萄糖苷、柚皮素[19]燕麦绿原酸、咖啡酸、胡萝卜酸、香草酸、对香豆酸、对羟基苯甲酸、2,4-二羟基苯甲醛、芥子酸、绿原酸、阿魏酸、芦丁、槲皮素、异鼠李素、山奈酚咖啡酸、丁香酸、香草酸、对香豆酸、对羟基苯甲酸、2,4-二羟基苯甲醛、芥子酸、绿原酸、阿魏酸、槲皮素-3-O-葡萄糖苷、山奈酚-3-O-芸香糖苷、柚皮素[20]
天然多酚的生理功能与其存在形式和基质互作密切相关。抗氧化活性源于酚羟基供氢或电子能力,如燕麦中阿魏酸酯化阿拉伯木聚糖占总酚酸的60%~70%,发酵后释放的游离阿魏酸可抑制低密度脂蛋白氧化,降低动脉粥样硬化风险[24];荞麦芦丁水解产物槲皮素通过激活AMPK通路改善胰岛素敏感性,并抑制α-葡萄糖苷酶延缓糖吸收;黑麦烷基间苯二酚则通过线粒体途径诱导结肠癌细胞凋亡。多酚与膳食纤维、蛋白质的相互作用也影响其生物可及性。小麦麸皮中的阿魏酸与阿拉伯木聚糖通过酯键交联,需微生物的阿魏酸酯酶解离;而燕麦β-葡聚糖通过氢键包裹多酚以抵抗胃酸降解;而蛋白酶可水解多酚-蛋白质复合物释放游离多酚。这种基质-多酚-微生物的三元互作机制,为开发高生物利用度功能食品提供了理论支撑。
2 发酵对全谷物中多酚的影响
2.1 发酵菌种对多酚成分及生物可及性的影响
全谷物中的多酚需在消化过程中释放为可吸收形式以发挥健康效益,其肠道吸收程度称为生物可及性,进入体循环的比例则定义为生物利用度。由于天然多酚的溶解性和稳定性较低,其生物可及性通常受限。发酵菌种通过分泌特异性酶系统,可同时实现多酚结构转化与细胞壁降解,显著提升其生物可及性。如表2所示,谷物经发酵处理后,其总多酚含量呈现显著提升趋势。其中,小麦、玉米、高粱等谷物的多酚含量增幅普遍超过60%,而黑米在发酵过程中多酚含量的绝对值增长尤为突出。这一变化主要归因于微生物的代谢活动:乳酸菌与酵母菌能够通过水解结合态酚酸或降解单宁的方式,促使多酚释放;霉菌则可分解玉米细胞壁,释放其中的酚酸成分;在黑米发酵过程中,乳酸菌介导的花青素糖苷水解过程,进一步提升了游离多酚的含量。此外,在燕麦发酵体系中,芽孢杆菌通过协同β-葡聚糖的降解过程,有效促进了酚酸的释放。这些现象表明,发酵过程能够借助微生物的特异性代谢机制,显著增强谷物中多酚类物质的生物可利用性。ZIELI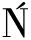 SKI等[29]研究发现乳酸菌发酵荞麦饼干的总多酚及黄酮含量显著高于未发酵样品,且总多酚生物可及性明显增强。但液态发酵中,副干酪乳酪杆菌和戊糖片球菌分别使总多酚含量下降23.0%和32.0%,铁离子还原抗氧化能力(ferric ion reducing antioxidant power,FRAP)与氧自由基吸收能力(oxygen radical absorbance capacity,ORAC)值亦显著降低。相反,芽孢菌发酵苦荞可使槲皮素和山奈酚含量分别增至初始值的5.8倍和37.4倍,同时促进肠道变形菌门生长,并与菌群丰度呈正相关。固态发酵中,冠突散囊菌处理甜荞后,总多酚含量与抗氧化活性同步提升[30],而苦荞面团发酵虽导致总黄酮下降,但游离糖苷配基及结合态芦丁增加。
SKI等[29]研究发现乳酸菌发酵荞麦饼干的总多酚及黄酮含量显著高于未发酵样品,且总多酚生物可及性明显增强。但液态发酵中,副干酪乳酪杆菌和戊糖片球菌分别使总多酚含量下降23.0%和32.0%,铁离子还原抗氧化能力(ferric ion reducing antioxidant power,FRAP)与氧自由基吸收能力(oxygen radical absorbance capacity,ORAC)值亦显著降低。相反,芽孢菌发酵苦荞可使槲皮素和山奈酚含量分别增至初始值的5.8倍和37.4倍,同时促进肠道变形菌门生长,并与菌群丰度呈正相关。固态发酵中,冠突散囊菌处理甜荞后,总多酚含量与抗氧化活性同步提升[30],而苦荞面团发酵虽导致总黄酮下降,但游离糖苷配基及结合态芦丁增加。
表2 主要谷物发酵后的总多酚含量变化[25-28]
Table 2 Changes in total polyphenol content after fermentation of major cereals[25-28]
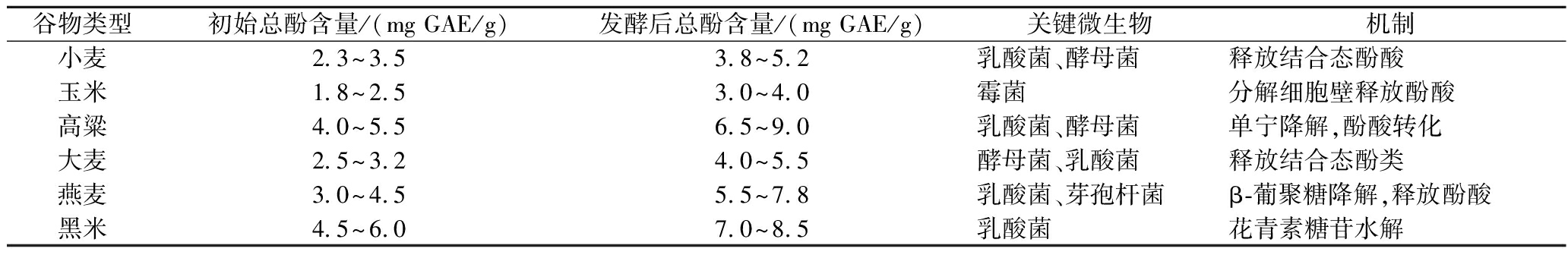
谷物类型初始总酚含量/(mg GAE/g)发酵后总酚含量/(mg GAE/g)关键微生物机制小麦2.3~3.53.8~5.2乳酸菌、酵母菌释放结合态酚酸玉米1.8~2.53.0~4.0霉菌分解细胞壁释放酚酸高粱4.0~5.56.5~9.0乳酸菌、酵母菌单宁降解,酚酸转化大麦2.5~3.24.0~5.5酵母菌、乳酸菌释放结合态酚类燕麦3.0~4.55.5~7.8乳酸菌、芽孢杆菌β-葡聚糖降解,释放酚酸黑米4.5~6.07.0~8.5乳酸菌花青素糖苷水解
如图2-a所示,菌种通过酶系释放或修饰酚酸。乳酸菌分泌阿魏酸酯酶和β-葡萄糖苷酶,水解结合态阿魏酸、对香豆酸,并利用脱羧酶将咖啡酸、原儿茶酸转化为抗氧化活性更强的二氢咖啡酸及儿茶酚[31];黑曲霉则通过β-氧化途径将阿魏酸降解为间羟基苯甲酸和对羟基苯甲酸,并进一步脱羧生成香草醛和香草酸[32]。此外,玫瑰乳杆菌和短乳杆菌通过脱羧酶将羟基肉桂酸转化为苯酚衍生物[33],而酿酒酵母通过裂解酶将香豆酸、阿魏酸转化为香草醛等脂溶性代谢物,提升吸收率[34]。如图2-b所示,菌种通过糖苷键水解与结构修饰优化活性。酵母菌通过α-鼠李糖苷酶与α-糖苷酶级联催化,将荞麦芦丁水解为异槲皮苷和槲皮素苷元,后者肠道吸收率提高3~5倍[35];曲霉属则通过脱羟基酶与去糖基酶将芦丁转化为山奈酚-3-葡萄糖苷及游离山奈酚,增强抗炎与降糖活性[36]。部分菌种还可通过甲基化或羟基化修饰黄酮骨架,调控其与靶标蛋白的亲和力。例如,干酪乳酪杆菌和嗜酸乳杆菌发酵红高粱时,β-葡萄糖苷酶活性使糖苷配基/糖基化比率提高5~10倍,而枯草芽孢杆菌通过纤维素酶协同释放结合态黄酮。上述转化不仅释放了结合态多酚,还通过生成高活性代谢物提升了生物可及性。微生物代谢产物可协同稳定多酚结构,形成“酶解-转化-增效”的级联机制,为开发高功能活性的发酵谷物制品提供理论支撑。
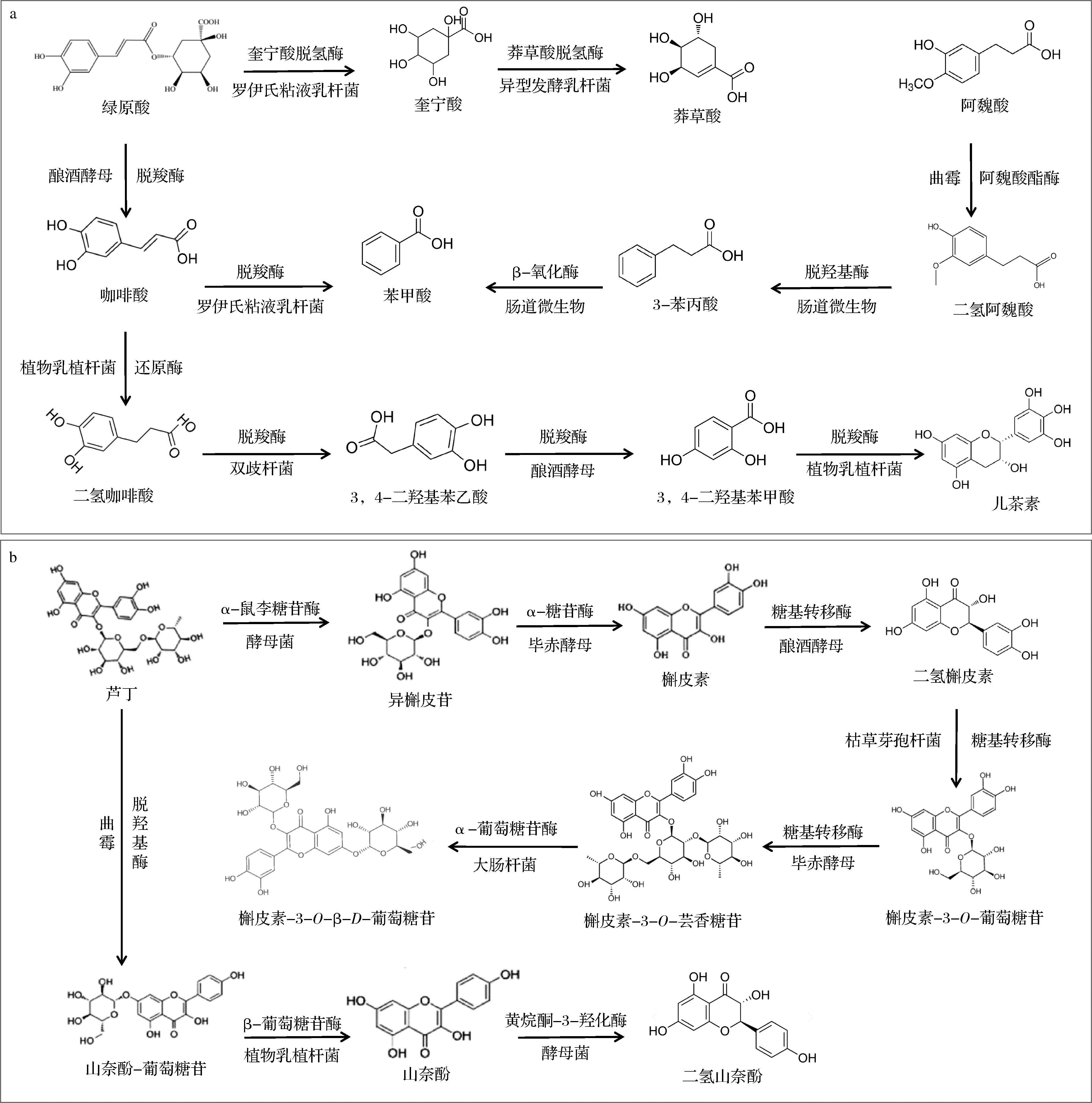
a-酚酸转化机制;b-黄酮修饰途径
图2 全谷物中多酚类物质在微生物发酵过程中的转化与降解途径
Fig.2 Transformation and degradation pathways of polyphenols in whole grains during microbial fermentation
2.2 发酵条件对多酚成分的及生物可及性的影响
发酵条件(温度、时间、菌种组合)通过调控微生物代谢活性及酶促反应动力学,直接影响多酚的转化效率与生物可及性。其中,温度通过调控酶活性与微生物生长速率,深刻影响着多酚释放与降解的动态平衡。在25~40 ℃的中低温区间,纤维素酶、β-葡萄糖苷酶等细胞壁降解酶的催化活性显著增强,促使多酚释放速率与温度呈正相关关系,进而提升多酚的生物可及性。当温度攀升至45 ℃以上,β-葡萄糖苷酶等热敏感型酶会因高温变性失活,致使黄酮苷水解效率骤降40%~60%[37]。同时,不同菌种对温度的适应性差异显著。以小麦发酵为例,枯草芽孢杆菌在33 ℃时多酚释放量较39 ℃下的植物乳植杆菌低12%~15%,但其黄酮苷保留率却高出20%[38],这充分表明菌种的合理选择能够对多酚转化类型实现特异性调控。适宜的发酵温度是优化多酚转化和生成的关键因素,维持在一个最佳范围内能够有效地促进多酚的合成,同时避免过高温度带来的负面影响。不同的菌种适宜的发酵温度不同,过高或过低的温度都可能影响发酵过程中酶的活性,进而影响多酚的转化效率和类型[33]。
发酵时间同样对多酚的生物可及性有着不可忽视的影响。研究证实,不同菌种对同种谷物的多酚转化效率存在显著差异。以高粱发酵为例,枯草芽孢杆菌在第5天总酚含量达峰值(6.8 mg GAE/g),而植物乳植杆菌仅需3 d即可实现相近水平(6.5 mg GAE/g),且后者黄酮苷元生成量较前者高出1.3倍[38],直观体现了菌株代谢路径的特异性。在薏仁米发酵过程中,植物乳植杆菌和干酪乳酪杆菌分别于60、48 h达到总多酚含量最大值[33],这进一步表明菌种特性对多酚转化进程的决定性作用。
发酵时长对多酚转化至关重要:时间过短会导致转化不充分,过长则可能引发多酚降解。以枯草芽孢杆菌发酵为例,在对数生长期,菌株代谢旺盛,多酚含量随发酵产物积累持续上升,至第5天稳定期时达到峰值;进入衰亡期后,多酚因被分解利用导致其含量下降[38]。
此外,菌种组合的协同效应显著影响多酚转化效率。燕麦发酵中,芽孢杆菌与乳酸菌协同作用加速β-葡聚糖降解,释放更多酚酸;黑米发酵则依赖单一乳酸菌主导的花青素糖苷水解机制,展现出菌种专一性的独特优势[27-30]。因此,精准匹配菌种组合与发酵参数,可针对目标多酚类型优化转化路径,从而最大化其营养价值与功能特性。
3 多组学技术解析发酵过程中多酚生物转化机制
3.1 酶催化作用
酶作为生物催化剂,凭借其高度底物特异性在发酵多酚生物转化中发挥关键作用,通过定向催化反应决定终产物的结构和功能特性。多酚生物转化可分为释放与转化2个动态过程。释放是指在发酵过程中,由于酶的作用,原本与蛋白质、纤维素等大分子物质结合或嵌在细胞壁结构中的多酚被释放出来,成为游离态或多酚含量增加的形式。转化则指多酚在酶的作用下发生化学结构的变化,生成新的化合物或衍生物(图2)。
在谷物发酵过程中,微生物产生的水解酶可分解细胞壁并切断酚类物质的化学键,释放出不溶态结合多酚,转化为可溶形式以提高生物可及性(图2)。乳酸菌的β-葡萄糖苷酶通过水解糖苷键去除吡喃糖残基;植物乳植杆菌Bgl3家族酶利用Glu-X-X-Glu基序特异性水解黄酮苷的β-1,4糖苷键,其催化效率受底物构象影响,对异黄酮苷活性更高。多酚还可经还原反应转化,如儿茶素还原酶将儿茶素转为黄酮类[39],植物乳植杆菌与双歧杆菌发酵黑米时,花色苷转化为游离酚类,芍药素重构为香草酸,矢车菊素-3-葡萄糖苷分解为矢车菊素。此外,糖基转移酶通过糖基化修饰(如结合核苷酸激活的二磷酸糖供体形成糖苷键)及羟基引入等作用增强多酚活性。管玉格[40]研究发现,发酵可提升总酚含量,西兰花发酵后根皮酸增至624 μg/g,同时生成香草酸、4-乙烯基愈创木酚等活性分子,显著提高多酚的生物利用度。
多组学技术的整合应用(图3)为解析多酚转化网络提供了系统的研究框架。宏基因组学可鉴定发酵微生物中编码关键酶的功能基因簇,植物乳植杆菌发酵黑麦过程中,羟基肉桂酸脱羧酶基因的上调与香草酸、4-乙烯基愈创木酚的积累呈强正相关,揭示其为核心调控靶点,从传统酸面团中筛选的野生型戊糖片球菌携带独特的阿魏酸酯酶基因簇[41];转录组学通过分析特定发酵阶段的基因表达谱,揭示水解酶或氧化还原酶的动态调控网络,动态追踪发酵过程中羟基肉桂酸脱羧酶基因的表达上调,与香草酸、4-乙烯基愈创木酚的积累高度同步,锁定其为核心调控靶点;宏蛋白质组学则可直接检测酶的表达水平及翻译后修饰状态,验证其催化活性与多酚转化的关联性,植物乳植杆菌Bgl3酶的糖基化修饰可增强其对异黄酮苷的水解活性;代谢组学通过追踪多酚衍生物的动态变化,构建底物-产物代谢流图谱[42]。GAUR等[43]结合宏基因组和代谢组学分析,发现植物乳植杆菌发酵过程中,花色苷降解关键基因的上调与香草酸等小分子酚酸的积累高度同步,阐明菌株特异性代谢路径。这种多维度数据整合不仅能够精准定位驱动多酚转化的核心酶系,还可通过机器学习模型预测最优发酵条件,实现产物定向调控。
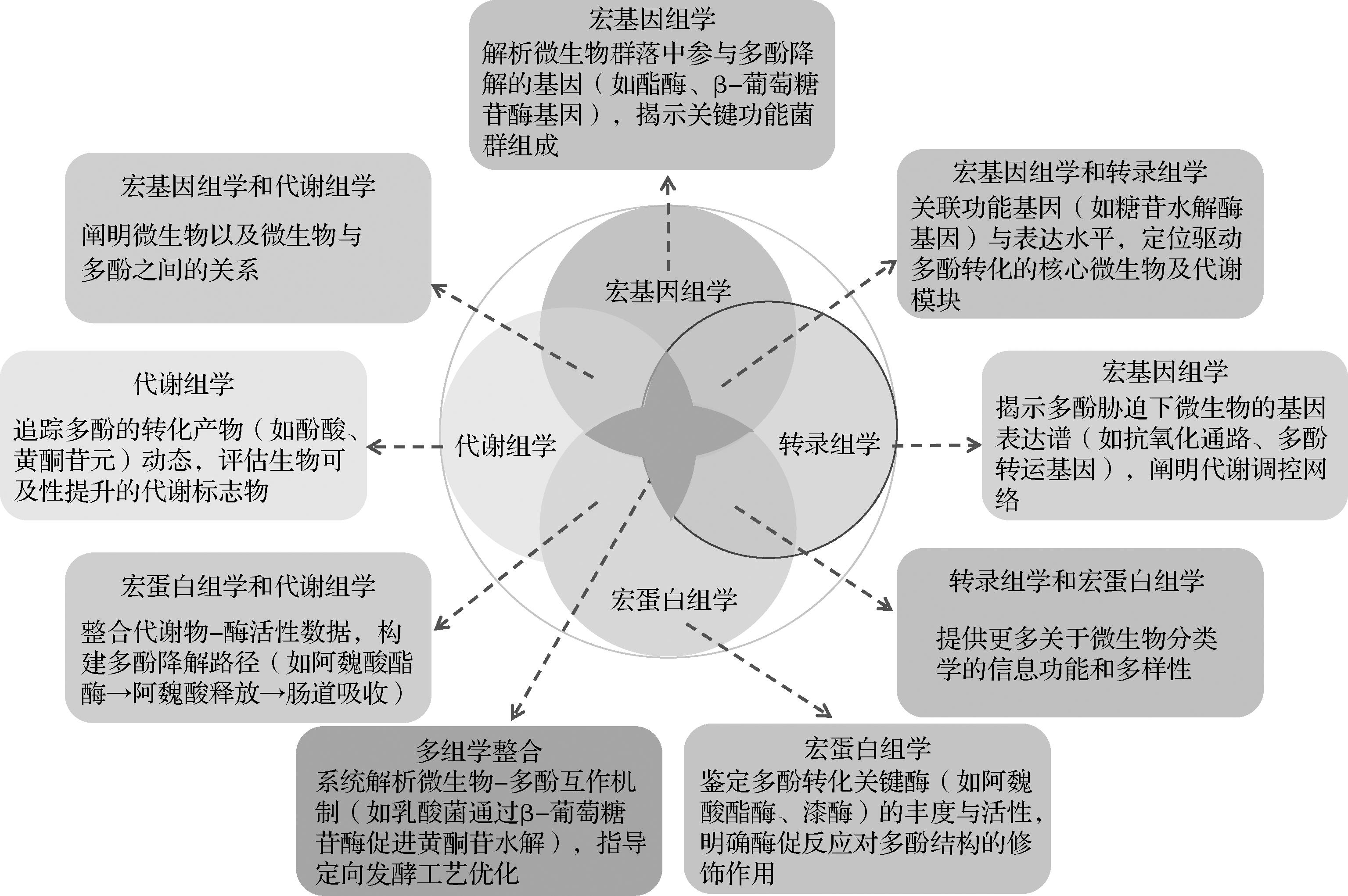
图3 阐明发酵的机制:整合多组学技术解析全谷物多酚的代谢转化
Fig.3 Elucidating the mechanisms of fermentation:Integrating multi-omics techniques to resolve metabolic
transformation of whole grain polyphenols
酶催化多酚转化机制的核心在于酶-底物特异性互作驱动的分子重构,该过程产生的有机酸等副产物还可协同促进多酚释放。这种精准的生物催化体系不仅深化了我们对天然产物代谢的理解,更为食品功能因子增效、药物前体合成及生物制造工艺革新提供了技术支撑。
3.2 微生物代谢产物作用
微生物的代谢产物(如有机酸、细菌素和维生素)能够调节自身的代谢途径,从而影响多酚类物质的转化和生物可及性。一方面通过直接参与生化反应,另一方面通过调控微生物群落结构。实验数据表明,乳酸菌发酵可以显著提高苦荞粉中总黄酮的含量[提升率达(42±3.6)%],该现象与代谢产物的协同作用直接相关[44]。具体而言,微生物在发酵过程中产生的酸性或碱性物质会改变环境的pH值,而pH的变化会直接影响多酚类物质的化学性质和酶活性,进而影响其转化。
在发酵过程中产生的有机酸,如乳酸和醋酸,能够降低环境pH值,进而影响多酚类化合物的稳定性,促使其发生结构变化。全谷物发酵实验中,当人为添加乳酸使体系pH值从6.0降至4.5时,多酚的结构异构化速率提升了35%,黄烷醇向黄烷酮的转化率显著增加[45]。在酸性环境中,多酚类化合物中的羟基(—OH)会发生质子化,形成带正电的羟基(—OH2+),这会改变多酚的电子分布和反应性[46]。此外,多酚的羟基还可与有机酸发生酯化反应,生成酚酸酯,从而改变多酚的溶解性和生物活性。酸性条件可能导致多酚类化合物的结构异构化,代谢组学分析显示,乳酸积累导致pH值降至4.5时,黄烷酮合酶活性上调,促使黄烷醇异构化为黄烷酮。通过整合代谢组学和宏蛋白质组学技术,研究人员能够动态监测pH依赖性多酚异构体的丰度变化,并关联关键异构酶的活性波动。ZHAO等[47]结合转录组和代谢组数据,发现乳酸菌在低pH条件下上调质子转运相关基因,同时促进黄烷酮的积累,揭示了pH调控多酚转化的跨膜质子耦合机制。因此,在食品发酵过程中,控制环境的pH值对于保持多酚类化合物的稳定性和功能特性至关重要。
细菌素是一类由细菌生成的具有抗菌活性的蛋白质或肽,能够抑制有害细菌的生长,为乳酸菌提供更有利的生长环境,并间接促进多酚类化合物的转化。使用细菌素合成基因簇敲除的植物乳植杆菌突变株进行发酵时,多酚底物的无效消耗恢复至对照组水平,而添加纯化乳酸链球菌素可使目标产物得率提升41%[48-49]。由乳酸链球菌产生的乳酸链球菌素,是一种广泛应用的细菌素。宏基因组学鉴定了植物乳植杆菌中细菌素合成基因簇与多酚氧化酶基因的共表达模块,能够抑制多种革兰氏阳性菌(葡萄球菌、链球菌和李斯特菌)和部分革兰氏阴性菌(大肠杆菌和沙门氏菌),使得多酚底物无效消耗减少60%。这些细菌素的作用机制多样,包括破坏细菌细胞壁、形成离子通道导致细胞膜去极化、抑制细菌蛋白质合成等。宏基因组学和宏蛋白质组学分析表明,细菌素的合成与多酚转化存在协同调控关系。TANG等[50]通过比较宏基因组学鉴定了植物乳植杆菌中细菌素合成基因簇与多酚氧化酶基因的共表达模块,进一步通过代谢流分析证实,抑制竞争性微生物可减少多酚底物的无效消耗,从而提高目标产物的得率。通过抑制有害菌的生长,乳酸菌可以在食品发酵过程中占据优势,从而创造一个有利于其生长的环境。在这种环境中,乳酸菌通过各种酶的作用促进多酚类化合物的降解,提高多酚的生物可及性。
维生素如维生素B群,可能在多酚类化合物的代谢过程中起到辅酶的作用,影响其转化途径。在维生素B2合成缺陷型菌株中,漆酶活性下降67%,而外源补充黄素腺嘌呤二核苷酸(flavin adenine dinucleotide,FAD)(0.1~1.0 mmol/L)可使多酚转化效率恢复至野生型水平。单细胞代谢通量分析显示,维生素B2浓度每增加0.1 mmol/L,黄烷酮合成途径的碳通量占比可提升15%。通过CRISPR干扰技术构建维生素响应型启动子调控的多酚氧化酶工程菌株,证实维生素浓度与酶活性存在剂量依赖关系[51]。空间代谢组学结合单细胞转录组学发现,维生素B2的局部浓度梯度与漆酶活性区域重叠,证实其通过FAD辅酶激活多酚氧化还原反应。维生素作为辅酶不仅可以加速多酚的代谢过程,还可以调节相关酶的活性,影响多酚的代谢路径。多组学技术的联用为解析维生素介导的代谢调控网络提供了新思路。空间代谢组学可定位发酵体系中维生素B2的分布热点,并与转录组数据中多酚氧化还原酶的表达区域重叠,提示维生素的局部浓度梯度对酶活性的空间特异性调控[52]。此外,合成生物学结合蛋白质工程手段,已能够基于多组学数据设计维生素依赖型多酚转化酶,实现代谢途径的定向优化。总之,微生物代谢产物通过直接参与化学反应或者调节微生物群落,显著影响多酚的转化途径,从而影响多酚的生物可及性。有机酸通过质子耦合机制驱动化学转化,细菌素通过生态位重塑优化代谢路径,维生素通过空间特异性调控增强酶效率,说明代谢产物不仅是发酵过程的必然产物,更是多酚转化的主动调控者。
3.3 细胞间相互作用
发酵过程中细胞间的相互作用对多酚的转化具有重要影响。在发酵过程中,不同种类的微生物相互作用,能够改变微生物群落结构。一些微生物可能具备将多酚转化为更易利用或更具生物活性的化合物的能力,而群落的动态变化会进一步影响这种转化的效率和最终产物。通过宏基因组学与代谢组学的联合分析,研究人员能够解析微生物互作网络与多酚代谢产物的关联性。SHANGPLIANG等[53]利用宏基因组组装技术重建发酵体系中微生物的功能基因组,结合代谢组学数据发现,乳酸菌与酵母菌的共生关系通过乙酸交叉喂养机制,显著提高黄酮苷的降解效率。这种跨物种代谢互作的揭示,为定向调控菌群结构以优化多酚转化提供了理论依据。
细胞通过释放信号分子进行通讯,这些信号分子可以影响细胞内酶的活性,进而调控多酚的生物转化过程。胰岛素和糖皮质激素等可以影响动物细胞内酶的活性,调控多酚的代谢。这些激素可以调节基因表达,从而影响酶的合成。细胞因子是细胞间通讯的小分子蛋白质,它们可以调节免疫反应和炎症过程,间接影响多酚转化酶的活性。单细胞转录组学与空间蛋白质组学技术的结合,可精准定位信号分子对多酚代谢酶的调控靶点。STASZEK等[54]通过单细胞测序发现,发酵体系中特定乳酸菌亚群在接触植物乳植杆菌素后,其多酚氧化酶编码基因的表达量上调2.3倍,同时胞内FAD辅酶水平增加,表明细菌素通过细胞间信号传递激活维生素依赖的酶促反应。
在微生物群落中,不同种类的微生物可以通过细胞间相互作用影响多酚的生物转化。真菌能够产生分解木质素和纤维素的酶,如多酚氧化酶和漆酶,这些酶能够将植物细胞壁中的多酚类物质降解成较小的分子[55]。细菌随后可以利用这些较小的分子作为碳源和能量来源进行生长和代谢,肠杆菌属能够利用降解后的单宁酸或黄酮类化合物。基于宏转录组学和代谢流分析的多组学整合模型,能够动态追踪真菌-细菌协同代谢路径。KANG等[56]通过时间序列转录组数据锁定真菌漆酶基因的表达峰值期,并利用同位素标记代谢流追踪技术证实,此阶段释放的香豆酸被相邻的芽孢杆菌优先吸收,进而通过β-酮己二酸途径转化为具有抗氧化活性的苯丙素衍生物。细胞间的信号传递可以调控多酚代谢途径中关键酶的表达和活性,从而影响多酚的转化路径。
细胞间的相互作用通过信号传递和微生物群落的动态变化影响多酚的生物转化。多组学技术的系统整合(如微生物互作网络建模、机器学习驱动的菌群设计)正在突破传统研究的局限性,能够从分子-细胞-群落多层级解析多酚转化的调控枢纽。深入了解这些相互作用能够有助于揭示细胞通过信号分子调控多酚的生物转化机制,以便更好地控制和利用多酚的生物转化过程。
4 多组学技术解析发酵过程中多酚生物转化机制
全谷物富含多酚,但生物可及性通常较低,微生物发酵能够提升多酚的生物可及性,增强其功能活性,并改善风味。发酵过程中多酚的生物转化和生物可及性的提高是由发酵条件、菌种特性和微生物代谢共同驱动的复杂过程。多组学技术的应用揭示了多酚从释放到代谢的全链条机制,为精准调控发酵过程提供了理论依据。未来研究中,需进一步解析多酚转化的动态代谢网络,例如通过时空分辨代谢组学定位关键中间产物,结合酶工程手段优化多酚转化酶的催化效率与底物特异性。此外,通过合成生物学构建“代谢开关”,利用pH或代谢产物浓度反馈调控细菌素、有机酸的合成基因簇,可实现多酚转化的动态平衡。通过对这一过程的深入理解和精确控制,优化全谷物食品的发酵,提升其营养价值,为人类健康提供更加有效的植物化学保护。这不仅体现了发酵技术的科学价值,也展现了传统食品加工与现代生物科技相结合的巨大潜力。
未来研究将围绕多维度技术创新,系统优化谷物发酵策略以提升多酚生物利用价值。在发酵条件调控层面,将借助机器学习构建pH动态调控模型,精准捕捉发酵过程中环境参数变化对微生物代谢的影响;同时基于菌群互作网络理论,设计共生发酵体系,实现菌种间的优势互补。在发酵介质优化方面,通过添加功能性预生物质,定向富集产酶菌株,为多酚高效转化创造有利条件。在评估方法革新上,将聚焦开发更精准的多酚生物可及性评估技术。一方面,深化体外模拟胃肠道消化模型研究,构建整合肠道微生物共培养系统的动态吸收评估平台,模拟体内真实消化环境;另一方面,结合动物模型实验与人体临床试验,从多尺度验证多酚的生物利用度,为功能性食品研发提供可靠数据支撑。基于对多酚-微生物互作机制的深入解析,靶向递送技术将成为重要突破口。通过开发包埋发酵菌株的纳米载体,保护菌株活性,提升其在肠道环境中的定殖效率,持续发挥多酚转化效应。在功能性食品开发领域,CRISPR基因编辑技术将用于强化乳酸菌β-葡萄糖苷酶表达,精准水解多酚糖苷键,提高活性苷元释放率;同时,“智能发酵菌剂”的设计可根据宿主代谢表型,自适应调节多酚代谢通路,实现对慢性疾病的精准预防与治疗。通过上述技术路径,有望开发出一系列具有特定健康功效的全谷物发酵食品,推动功能性食品产业的创新发展。
[1] 中国食品报. 全谷物产业向“新”发展[EB/OL].2024-08-28.https://www.cnfood.cn/article id=1828360863528222722.
China Food Newspaper.Whole grain industry goes “New”[EB/OL].2024-08-28.https://www.cnfood.cn/article id=1828360863528222722.
[2] 胡文凯, 王艳丽, 彭镰心, 等.谷物膳食纤维和酚类物质结合对肠道健康影响的研究进展[J].保鲜与加工, 2024, 24(9):147-156.
HU W K, WANG Y L, PENG L X, et al.Research progress on the effects of cereal dietary fiber and phenolic substances on gut health[J].Storage and Process, 2024, 24(9):147-156.
[3] 吕俊丽, 侯丽丽, 杨昊鹏, 等.发芽对莜麦多酚及抗氧化活性生物可及性的影响[J].中国食品学报, 2024, 24(6):33-43.
LYU J L, HOU L L, YANG H P, et al.Effects of germination on bioaccessibility of polyphenols and antioxidant activities of naked oats[J].Journal of Chinese Institute of Food Science and Technology, 2024, 24(6):33-43.
[4] DA SILVA A P G, SGANZERLA W G, JOHN O D, et al.A comprehensive review of the classification, sources, biosynthesis, and biological properties of hydroxybenzoic and hydroxycinnamic acids[J].Phytochemistry Reviews, 2025, 24(2):1061-1090.
[5] EL HOUSSNI I, ZAHIDI A, KHEDID K, et al.Nutrient and anti-nutrient composition of durum, soft and red wheat landraces:Implications for nutrition and mineral bioavailability[J].Journal of Agriculture and Food Research, 2024, 15:101078.
[6] 章灏, 王立, 李言.黑小麦麸皮中多酚类物质的纯化工艺优化及成分分析[J].粮油食品科技, 2024, 32(1):28-35;12.
ZHANG H, WANG L, LI Y.Purification process optimization and composition analysis of polyphenols from black wheat bran[J].Science and Technology of Cereals, Oils and Foods, 2024, 32(1):28-35;12.
[7] 冯芝英. 全谷物糙米结合态酚类物质结构表征及其肠道微生物代谢特征研究[D].广州:华南农业大学, 2021.
FENG Z Y.Structural characterisation of phenolics in the bound state of whole grain brown rice and their metabolic profile in intestinal microorganisms[D].Guangzhou:South China Agricultural University, 2021.
[8] 叶玲旭, 刘兴训, 周素梅, 等.不同颜色糙米的酚类物质组成及抗氧化活性分析[J].食品与发酵工业, 2016, 42(9):75-80.
YE L X, LIU X X, ZHOU S M, et al.Phenolic compounds and antioxidant activity of brown rice in different color of bran[J].Food and Fermentation Industries, 2016, 42(9):75-80.
[9] 吕京京, 李璐, 张娜.植物性食物中结合多酚的释放及功能活性的研究进展[J].食品工业科技, 2025, 46(4):404-413.
LYU J J, LI L, ZHANG N.Research progress on the release and functional activity of bound polyphenols in plant foods[J].Science and Technology of Food Industry, 2025, 46(4):404-413.
[10] 刘富明, 母婷婷, 王彩霞, 等.蓝色和紫色小麦多酚提取物的体外抗氧化活性评价[J].食品与发酵工业, 2019, 45(9):202-206.
LIU F M, MU T T, WANG C X, et al.Evaluation of in vitro antioxidant activities of polyphenol extracts from blue and purple wheat[J].Food and Fermentation Industries, 2019, 45(9):202-206.
[11] 刘琴, 张薇娜, 朱媛媛, 等.不同产地苦荞籽粒中多酚的组成、分布及抗氧化性比较[J].中国农业科学, 2014, 47(14):2840-2852.
LIU Q, ZHANG W N, ZHU Y Y, et al.Comparison of the constitutions, distribution, and antioxidant activities of polyphenols from different varieties of Tartary buckwheat seed produced from different regions of China[J].Scientia Agricultura Sinica, 2014, 47(14):2840-2852.
[12] 杨红叶, 杨联芝, 柴岩, 等.甜荞和苦荞籽中多酚存在形式与抗氧化活性的研究[J].食品工业科技, 2011, 32(5):90-94;97.
YANG H Y, YANG L Z, CHAI Y, et al.Comparison of antioxidant activity and the content of free and bound phenolics in common buckwheat and Tartary buckwheat particles[J].Science and Technology of Food Industry, 2011, 32(5):90-94;97.
[13] 田晓闽, 陈利容, 孙琳琳, 等.鲜食玉米酚类化合物含量及体外功能活性研究[J].食品科技, 2023, 48(4):223-229.
TIAN X M, CHEN L R, SUN L L, et al.The content and in vitro functional activity of phenolic compounds in fresh corn[J].Food Science and Technology, 2023, 48(4):223-229.
[14] 何鑫怡. 甜玉米多酚提取物抗氧化和抗衰老活性研究[D].重庆:西南大学, 2024.
HE X Y.Research on antioxidant and anti-aging activities of sweet corn polyphenol extract[D].Chongqing:Southwest University, 2024.
[15] 刘文义. 不同品种高粱中酚类物质的分离鉴定以及差异性分析[D].天津:天津大学, 2020.
LIU W Y.Separation and identification of phenolics in different varieties of sorghum and differential analysis[D].Tianjin:Tianjin University, 2020.
[16] 王雅楠, 白云飞, 刘昕桐, 等.加工方式对小米多酚含量影响研究进展[J].食品研究与开发, 2023, 44(14):219-224.
WANG Y N, BAI Y F, LIU X T, et al.Effects of processing methods on the content of millet polyphenols[J].Food Research and Development, 2023, 44(14):219-224.
[17] 闫巧珍. 小米多酚提取、分离纯化、组分分析及生物活性的研究[D].太原:山西农业大学, 2020.
YAN Q Z.Research on extraction, separation and purification, component analysis and biological activity of millet polyphenols[D].Taiyuan:Shanxi Agricultural University, 2020.
[18] 翟玮玮, 侯会绒, 孙兆远.四种谷物中多酚含量的测定及抗氧化特性研究[J].食品工业科技, 2012, 33(24):150-153.
ZHAI W W, HOU H R, SUN Z Y.Detection of phenols content and antioxidant activity of four grains[J].Science and Technology of Food Industry, 2012, 33(24):150-153.
[19] 陈露露. 燕麦活性物质的研究综述[J].现代食品, 2024, 30(4):139-141.
CHEN L L.A review of research on active substances in oats[J].Modern Food, 2024, 30(4):139-141.
[20] 贺馨怡, 李晓, 申家乐, 等.富含多酚的燕麦发芽条件优化及多酚差异代谢物分析[J].湘潭大学学报(自然科学版), 2023, 45(3):120-130.
HE X Y, LI X, SHEN J L, et al.Optimization of germination conditions and analysis of differential metabolites of oats enriched with polyphenols[J].Journal of Xiangtan University (Natural Science Edition), 2023, 45(3):120-130.
[21] LI Y, ZHANG W J, HUANG Y F, et al.Exogenous silicon improved the cell wall stability by activating non-structural carbohydrates and structural carbohydrates metabolism in salt and drought stressed Glycyrrhiza uralensis stem[J].International Journal of Biological Macromolecules, 2024, 283:137817.
[22] 马玉辉, 谭斌, 吕莹果, 等.谷物多酚降糖降脂作用的研究进展[J].中国粮油学报, 2024, 39(8):200-209.
MA Y H, TAN B, LYU Y G, et al.Research progress on hypoglycemic and lipid-lowering effects of grain polyphenols[J].Journal of the Chinese Cereals and Oils Association, 2024, 39(8):200-209.
[23] OTHMAN Z A, WAN GHAZALI W S, NOORDIN L, et al.Phenolic compounds and the anti-atherogenic effect of bee bread in high-fat diet-induced obese rats[J].Antioxidants, 2020, 9(1):33.
[24] GUMUL D, BERSKI W.The polyphenol profile and antioxidant potential of irradiated rye grains[J].International Journal of Food Science, 2021, 2021(1):8870754.
[25] GIL J V, ESTEBAN-MU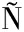 OZ A, FERN
OZ A, FERN NDEZ-ESPINAR M T.Changes in the polyphenolic profile and antioxidant activity of wheat bread after incorporating quinoa flour[J].Antioxidants, 2022, 11(1):33.
NDEZ-ESPINAR M T.Changes in the polyphenolic profile and antioxidant activity of wheat bread after incorporating quinoa flour[J].Antioxidants, 2022, 11(1):33.
[26] AKBARI M, RAZAVI S H, KHODAIYAN F, et al.Fermented corn bran:A by-product with improved total phenolic content and antioxidant activity[J].LWT, 2023, 184:115090.
[27] ARUNA C R, RATNAVATHI C V, SUGUNA M, et al.Genetic variability and GxE interactions for total polyphenol content and antioxidant activity in white and red sorghums (Sorghum bicolor)[J].Plant Breeding, 2020, 139(1):119-130.
[28] CHAIYASUT C, PENGKUMSRI N, SIRILUN S, et al.Assessment of changes in the content of anthocyanins, phenolic acids, and antioxidant property of Saccharomyces cerevisiae mediated fermented black rice bran[J].AMB Express, 2017, 7(1):114.
[29] ZIELI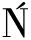 SKI H, WICZKOWSKI W, TOPOLSKA J, et al.Bioaccessibility of phenolic acids and flavonoids from buckwheat biscuits prepared from flours fermented by lactic acid bacteria[J].Molecules, 2022, 27(19):6628.
SKI H, WICZKOWSKI W, TOPOLSKA J, et al.Bioaccessibility of phenolic acids and flavonoids from buckwheat biscuits prepared from flours fermented by lactic acid bacteria[J].Molecules, 2022, 27(19):6628.
[30] XIAO Y, WU X, YAO X S, et al.Metabolite profiling, antioxidant and α-glucosidase inhibitory activities of buckwheat processed by solid-state fermentation with Eurotium cristatum YL-1[J].Food Research International, 2021, 143:110262.
[31] MPOFU E, CHAKRABORTY J, SUZUKI-MINAKUCHI C, et al.Biotransformation of monocyclic phenolic compounds by Bacillus licheniformis TAB7[J].Microorganisms, 2020, 8(1):26.
[32] WANG J X, LIANG J D, GAO S.Biodegradation of lignin monomers vanillic, p-coumaric, and syringic acid by the bacterial strain, Sphingobacterium sp.HY-H[J].Current Microbiology, 2018, 75(9):1156-1164.
[33] LOMASCOLO A, ODINOT E, VILLENEUVE P, et al.Challenges and advances in biotechnological approaches for the synthesis of canolol and other vinylphenols from biobased p-hydroxycinnamic acids:A review[J].Biotechnology for Biofuels and Bioproducts, 2023, 16(1):173.
[34] KAWAZOE M, TAKAHASHI K, TOKUE Y, et al.Catabolic system of 5-formylferulic acid, a downstream metabolite of a β-5-type lignin-derived dimer, in Sphingobium lignivorans SYK-6[J].Journal of Agricultural and Food Chemistry, 2023, 71(49):19663-19671.
[35] PACHL P, KAPE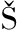 OV
OV J, BRYNDA J, et al.Rutinosidase from Aspergillus niger:Crystal structure and insight into the enzymatic activity[J].The FEBS Journal, 2020, 287(15):3315-3327.
J, BRYNDA J, et al.Rutinosidase from Aspergillus niger:Crystal structure and insight into the enzymatic activity[J].The FEBS Journal, 2020, 287(15):3315-3327.
[36] HERRERA-ROCHA K M, ROCHA-GUZM N N E, GALLEGOS-INFANTE J A, et al.Phenolic acids and flavonoids in acetonic extract from quince (Cydonia oblonga Mill.):Nutraceuticals with antioxidant and anti-inflammatory potential[J].Molecules, 2022, 27(8):2462.
N N E, GALLEGOS-INFANTE J A, et al.Phenolic acids and flavonoids in acetonic extract from quince (Cydonia oblonga Mill.):Nutraceuticals with antioxidant and anti-inflammatory potential[J].Molecules, 2022, 27(8):2462.
[37] 陈林林, 张海鹏, 李伟, 等.谷物多酚提取及影响和改善其生物活性利用技术的研究进展[J].中国调味品, 2024, 49(5):205-212.
CHEN L L, ZHANG H P, LI W, et al.Advances in technologies for extracting polyphenols from cereals, influencing and improving their bioactivity utilization[J].China Condiment, 2024, 49(5):205-212.
[38] 吕海鹏, 王梦琪, 张悦, 等.普洱茶后发酵过程中多酚类成分生物转化的研究进展[J].食品科学, 2018, 39(23):306-312.
LYU H P, WANG M Q, ZHANG Y, et al.Recent advances in research on biotransformation of polypheonls during Pu-erh tea pile fermentation[J].Food Science, 2018, 39(23):306-312.
[39] 陈俊婕, 劳颖仪, 陈晓维, 等.茶多酚的功能活性及稳态化研究进展[J].中国果菜, 2024, 44(8):25-31.
CHEN J J, LAO Y Y, CHEN X W, et al.Research progress on functional activity and stabilization of tea polyphenols[J].China Fruit &Vegetable, 2024, 44(8):25-31.
[40] 管玉格. 鲜切西兰花酚类物质生物合成机制及其抗氧化活性的研究[D].大连:大连理工大学, 2021.
GUAN Y G.Studies on the mechanism of phenolic biosynthesis and its antioxidant activity in fresh-cut broccoli florets[D].Dalian:Dalian University of Technology, 2021.
[41] 王昌禄, 王旭锋, 丁成芳, 等.组学技术在红曲霉研究中应用的进展[J].食品科学技术学报, 2023, 41(5):14-23.
WANG C L, WANG X F, DING C F, et al.Application progress of omics technology in Monascus sp.research[J].Journal of Food Science and Technology, 2023, 41(5):14-23.
[42] WALSH L H, COAKLEY M, WALSH A M, et al.Bioinformatic approaches for studying the microbiome of fermented food[J].Critical Reviews in Microbiology, 2023, 49(6):693-725.
[43] GAUR G, OH J H, FILANNINO P, et al.Genetic determinants of hydroxycinnamic acid metabolism in heterofermentative lactobacilli[J].Applied and Environmental Microbiology, 2020, 86(5):e02461-19.
[44] REN Y H, WU S S, XIA Y, et al.Probiotic-fermented black Tartary buckwheat alleviates hyperlipidemia and gut microbiota dysbiosis in rats fed with a high-fat diet[J].Food &Function, 2021, 12(13):6045-6057.
[45] LEONARD W, ZHANG P Z, YING D Y, et al.Fermentation transforms the phenolic profiles and bioactivities of plant-based foods[J].Biotechnology Advances, 2021, 49:107763.
[46] 吴妙鸿, 邱珊莲, 林宝妹, 等.嘉宝果叶片多酚提取物的微生物转化及其对抗氧化活性的影响[J].江苏农业科学, 2021, 49(24):184-189.
WU M H, QIU S L, LIN B M, et al.Microbial transformation of polyphenols extract from Myrciaria cauliflora leaves and its effect on antioxidant activity[J].Jiangsu Agricultural Sciences, 2021, 49(24):184-189.
[47] ZHAO C R, YOU Z L, BAI L.Fungal plasma membrane H+-ATPase:Structure, mechanism, and drug discovery[J].Journal of Fungi, 2024, 10(4):273.
[48] ZHAO K, QIU L, TAO X Y, et al.Genome analysis for cholesterol-lowing action and bacteriocin production of Lactiplantibacillus plantarum WLPL21 and ZDY04 from traditional Chinese fermented foods[J].Microorganisms, 2024, 12(1):181.
[49] SUN X Q, KONG L Y, YUAN J W, et al.Regulatory mechanism of plnC in Lactiplantibacillus plantarum B1 on Plantaricin biosynthesis[J].Food Bioscience, 2024, 62:105355.
[50] TANG X Y.Synthetic biology to revive microbial natural product discovery[J].mLife, 2023, 2(2):123-125.
[51] TANG L X, WANG Y X, PENG M Y, et al.Fungal laccase and its production, immobilization, and application:A review[J].Mycosystema, 2023, 42(9).
[52] LIU J H, HUANG R R, SONG Q Q, et al.Combinational antibacterial activity of nisin and 3-phenyllactic acid and their co-production by engineered Lactococcus lactis[J].Frontiers in Bioengineering and Biotechnology, 2021, 9:612105.
[53] SHANGPLIANG H N J, TAMANG J P.Metagenomics and metagenome-assembled genomes mining of health benefits in jalebi batter, a naturally fermented cereal-based food of India[J].Food Research International, 2023, 172:113130.
[54] STASZEK P, KRASUSKA U, BEDERSKA-B ASZCZYK M, et al.Canavanine increases the content of phenolic compounds in tomato (Solanum lycopersicum L.) roots[J].Plants, 2020, 9(11):1595.
ASZCZYK M, et al.Canavanine increases the content of phenolic compounds in tomato (Solanum lycopersicum L.) roots[J].Plants, 2020, 9(11):1595.
[55] 杨艳, 杨荣玲, 邹宇晓, 等.肠道微生物菌群生物转化天然多酚类化合物研究进展[J].食品科学, 2014, 35(17):319-325.
YANG Y, YANG R L, ZOU Y X, et al.Recent advances in biotransformation of natural polyphenols by gut microflora[J].Food Science, 2014, 35(17):319-325.
[56] KANG M, CHOI Y, KIM H, et al.Single-cell RNA-sequencing of Nicotiana attenuata Corolla cells reveals the biosynthetic pathway of a floral scent[J].New Phytologist, 2022, 234(2):527-544.