食源性肽是指通过蛋白质的酶解或发酵,从食物中提取的生物活性短肽[1],具有抗氧化、抗炎和免疫调节等多种生理调节作用[2],在功能性食品和营养保健品领域具有广阔的应用前景。目前,其来源主要包括动物蛋白(如乳蛋白、鱼蛋白)和植物蛋白(如大豆蛋白、豌豆蛋白等)。近年来,植物源肽因其天然、低致敏性和环保特性,受到广泛关注。然而,我国食源性肽产业仍以初级加工和直接食用为主,深加工和高附加值产品开发利用尚不充分[3]。因此,推动食源性肽的深加工和功能开发,对于提升其商业价值和市场竞争力至关重要。
相比于完整蛋白质,食源性肽分子质量小,更易被人体消化吸收,可迅速进入血液循环,发挥其生理功能[4]。但其稳定性易受pH、温度和氧化等因素影响,易在加工和储存过程中酶解,限制了工业化应用[5]。因此,优化酶水解工艺及改进配方成为提高食源性肽稳定性和功能性的重要研究方向。
食源性肽的生物功能取决于核心肽段的序列和结构特征[6]。不同的酶水解工艺产生的肽段组成各异,特定功能(如抗氧化、抗炎)可能与富含特定氨基酸(如精氨酸、组氨酸或半胱氨酸)的肽段相关。通过现代质谱技术、氨基酸序列分析和分子对接等方法,可精确鉴定功能性核心肽段,结合定向酶解和肽段筛选,可以进一步提高食源性肽的功能特性和市场竞争力[7]。
本文综述了食源性肽的利用现状及深加工必要性,阐述了食源性肽在稳定性及消化吸收方面的优势,重点阐述了食源性肽的生理功能及核心肽段的鉴定研究进展,为食源性肽在食品、营养保健及医药领域的应用奠定基础。
1 食源性肽稳定性研究进展
1.1 物理化学稳定性
食源性肽通常由疏水相互作用、盐桥和氢键等非共价作用力维持其三维结构,从而保持较高的稳定性[8]。然而,在食品加工或消化过程中,肽易受环境因素影响发生降解,形成结构更为“动态”的新生肽。
不同氨基酸残基对环境因素(如温度、pH值和盐浓度)的敏感性存在差异。热处理会改变肽的二级结构,导致聚集并丧失活性。pH值变化可能会导致肽的电离特性发生改变,从而引发电子转移,导致活性降低。在碱性条件下,某些氨基酸(如神经氨酸、丝氨酸和半胱氨酸)对pH波动较为敏感,表现出较低的稳定性[9-10]。高盐环境下,氨基酸残基侧链的离子相互作用会导致肽的结构发生变化,从而降低其生物活性[11-12]。
氨基酸序列对食源性肽的稳定性至关重要。GURUPRASAD等[13]研究了蛋白质的稳定性与其二肽成分之间的相关性,发现部分二肽含量及结构在不稳定蛋白质中的发生频率明显不同于稳定蛋白质。如从Kluyveromyces marxianus蛋白水解物中纯化分离的VLSTSFPPK肽段,若将脯氨酸替换为半胱氨酸、酪氨酸或组氨酸,生成的新肽VLSTSFCPK、VLSTSFYPK和VLSTSFHPK,在高盐处理后抗氧化活性显著下降,说明半胱氨酸等残基在盐溶液中易发生构象变化,导致稳定性降低[14]。
此外,疏水性残基间作用力对热稳定性有重要影响。研究发现,KLTWQELYQLKYKGI在高温下表现出较高的热稳定性,但当第10位的亮氨酸替换为苯丙氨酸或缬氨酸,热稳定性明显下降(Tm从78.3 ℃到40 ℃左右),主要因疏水相互作用受扰,肽分子核心结构解构[15]。
二级结构类型亦影响食源性肽的热稳定性。ASADUZZAMAN等[16]以及UDENIGWE等[17]研究均表明,β片结构比例高的肽对热处理更敏感,稳定性较差。如肽VLSTSFCPK中β片结构比例较高,因而热稳定性低于同源肽。
综上所述,食源性肽的物理化学稳定性主要受氨基酸序列、空间构象及非共价作用力共同调控,且易受加工温度、pH值及盐浓度等因素干扰。未来可聚焦于氨基酸序列与稳定性关联解析、位点改造优化、标准化加工与消化模拟体系建立及分子动力学模拟辅助机制阐明,以提升功能肽在极端条件下的稳定性与应用价值。
1.2 代谢稳定性
食源性肽的生物活性效应与其在体内的吸收动力学及代谢稳定性存在显著相关性。研究表明,肽在胃肠道环境中需经历多阶段酶解过程,仅少量肽段能以完整或修饰形式穿越肠上皮屏障进入体循环,进而发挥其靶向生理调控功能[18-19]。
在小肠中,特别是空肠段,食源性肽吸收主要依赖4种转运机制吸收:细胞旁路扩散、跨细胞被动扩散、转胞吞作用及载体介导主动运输[20-21]。肽转运蛋白1(peptide transporter1,PepT1)介导的载体转运在二肽和三肽跨膜吸收中尤为重要,可有效避免肽酶水解。PepT1依赖电化学质子梯度及结构特异性识别完成H+/肽复合物转运[22]。然而,即便完成肠道吸收,食源性肽仍易受血清肽酶降解,导致系统生物利用度有限[23]。
肽在体内活性维持需同时具备固有生物活性及对消化酶的耐受性。如表1所示,3类主要消化酶底物识别机制存在显著差异,直接影响食源性肽的降解动力学:胃蛋白酶对芳香族氨基酸富集肽段降解迅速,而胰蛋白酶对含碱性残基肽段具有较高切割效率,而胰凝乳蛋白酶对芳香环与大型疏水残基有较强识别性,导致疏水性肽在肠相消化中稳定性较差。
表1 主要蛋白酶的切割特性比较
Table 1 Comparison of cleavage characteristics of major proteases
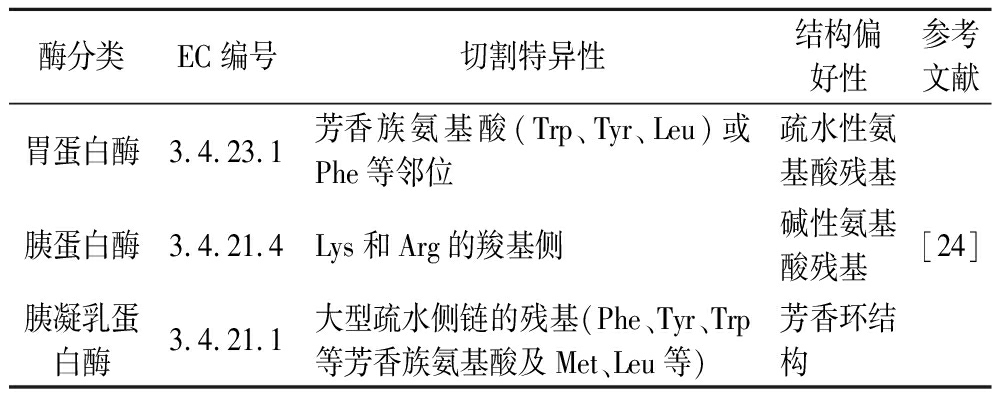
酶分类EC编号切割特异性结构偏好性参考文献胃蛋白酶3.4.23.1芳香族氨基酸(Trp、Tyr、Leu)或Phe等邻位疏水性氨基酸残基胰蛋白酶3.4.21.4Lys和Arg的羧基侧碱性氨基酸残基胰凝乳蛋白酶3.4.21.1大型疏水侧链的残基(Phe、Tyr、Trp等芳香族氨基酸及Met、Leu等)芳香环结构[24]
当前,体外模拟消化-质谱联用技术已成为评估肽消化稳定性的金标准,可实现超滤耦合超高效液相色谱串联质谱动态定量,揭示氨基酸残基贡献度解析结构-稳定性关系[25]。研究发现,>3 kDa酪蛋白肽在肠相更易降解,而富含酸性残基或具有疏水核心结构的肽段则表现出较好的酶抗性[26-27]。特别是脯氨酸效应备受关注,其环状结构限制酶切位点可及性,使富含Pro或Glu的肽段对胃肠蛋白酶更具耐受性[28]。
此外,消化条件对肽稳定性影响显著。如表2所示,不同研究组模拟胃消化条件存在多维参数差异。
表2 代表性体外胃消化实验参数比较
Table 2 Comparison of parameters of representative in vitro gastric digestion experiments
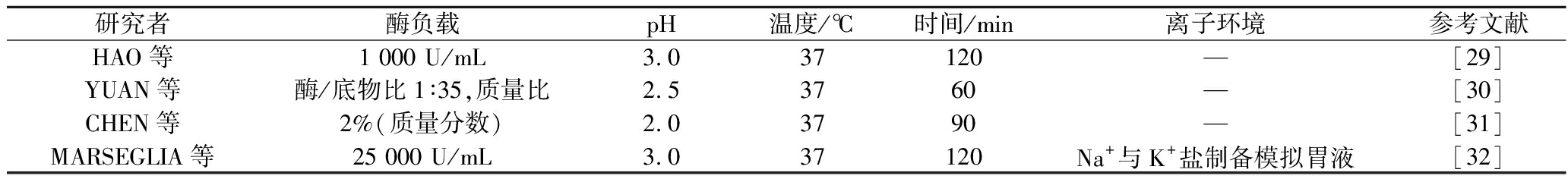
研究者酶负载pH温度/℃时间/min离子环境参考文献HAO等1 000 U/mL3.037 120—[29]YUAN等酶/底物比1∶35,质量比2.53760—[30]CHEN等2%(质量分数)2.03790—[31]MARSEGLIA等25 000 U/mL3.037120Na+与K+盐制备模拟胃液[32]
注:“—”表示原文献中未提及体外胃消化实验的离子环境。
当pH值从2.0升至3.0时,相同肽段降解速率常数降低1.8~2.3倍,主要因胃蛋白酶活性中心His残基质子化状态变化(pKa=4.5)。此外,离子环境差异(如Na+/K+存在与否)可调节酶构象动力学,导致酶活波动达35%(P<0.05),强调模拟生理离子强度的必要性。
尽管稳定性通常采用残留率量化,但受酶活性单位换算、离子强度及固液比标准化缺失影响,不同研究间的残留率存在一定偏差。这提示未来研究需要建立统一的体外消化评估指南。
1.3 贮藏与加工过程中的稳定性
在食品加工和贮藏过程中,外部环境因素对食源性肽的稳定性与生物活性具有重要影响。加工过程中所涉及的热力学应力、光辐射及机械处理等物理因素等,导致肽或其前体蛋白的空间构象发生改变,从而衰减其生物活性功能。此外,肽-基质相互作用(如美拉德反应、非共价复合物形成)会进一步改变其结构-活性关系。因此,建立基于质量源于设计(quality by design,QbD)理念的工艺优化策略,对维持食源性肽在食品体系中的功能稳定性具有重要应用价值[32]。
具体而言,温度变化是加工与贮藏过程中最常见且影响显著的因素之一。MIRZAEI等[14]研究发现,小米麸皮肽在不同巴氏杀菌条件下(63 ℃加热30 min、69 ℃加热30 min、75 ℃加热10 min、80 ℃加热25 s及100 ℃加热12 s)均能保持较好的抗氧化活性,部分肽段如RGLLLPSMSNAP、CFMTY和CTGTPYC在100 ℃持续加热15 min后依然具备较强的ABTS阳离子自由基清除能力,但加热至30 min则活性显著下降,表明高温长时间处理会破坏肽段关键功能结构,导致活性丧失。类似地,XU等[33]报道,100 ℃加热45~60 min显著降低了豌豆低聚肽的溶解度,主要归因于热诱导的构象重排、疏水基团暴露及肽链聚集,进一步影响其理化稳定性。
除了温度外,pH值作为加工体系和胃肠道消化环境中的重要变量,同样对肽的稳定性产生显著影响。XU等[33]发现,CFMTY肽在pH 2.0~8.0时抗氧化活性较为稳定,但在pH 10.0碱性环境下,RGLLLPSMSNAP肽段的ABTS阳离子清除能力明显下降,推测碱性条件通过影响肽电离状态、电子转移或构象变化,抑制其生物活性。
此外,贮藏环境中的水分活度、氧气含量及添加剂种类与浓度亦会调控肽的稳定性与活性表现。XU等[33]指出,常规质量浓度(2~4 mg/mL)糖和盐对RGLLLPSMSNAP、CFMTY和CTGTPYC肽段活性无显著影响,但高盐环境(6 mg/mL)会削弱其ABTS阳离子自由基清除能力,可能是高盐诱导构象变化或促进肽链聚集,而氧气暴露则易引发肽链氧化降解,降低其生物活性,低氧贮藏可有效延缓活性衰减[34]。此外,PÉREZ-GREGORIO等[35]报道,植物多酚类化合物可与肽形成酚-肽共轭物,适量添加有助于增强肽稳定性,但过量或特定结构的多酚易导致沉淀或络合,反而削弱肽的功能特性。
综上,食品加工与贮藏过程中的多因素协同作用显著影响食源性肽的结构稳定性与功能表达。合理优化热力学条件、pH值、氧气水平及基质环境,并基于QbD理念构建工艺优化策略,将有助于提升食源性肽在实际食品体系中的应用效果与生物活性保持能力。
2 食源性肽中特征肽段的鉴定方法及技术
特征肽段的精准鉴定是功能蛋白质组学研究中的关键科学问题,尤其在复杂食品基质中活性肽的结构解析与功能关联研究中具有决定性作用。目前,常用方法主要包括液相色谱、质谱及其联用技术,如液相色谱-质谱和液相色谱-串联质谱,在肽段的精确性与序列分析中发挥核心作用。
液相色谱-质谱技术融合了液相色谱的分离能力与质谱的高灵敏度检测优势,广泛应用于复杂样品中化合物的分离与鉴定,通过测定分子质量等关键信息实现肽段初步解析[36]。
液相色谱-串联质谱技术在此基础上引入MS/MS碎裂模式,获取更详细的氨基酸序列信息,是当前食源性肽研究中应用最广泛的序列解析方法,具备高准确度、良好特异性与灵敏度,适用于复杂肽混合物的分析[36]。
飞行时间质谱作为高分辨率、快速响应的质谱技术,通过测定离子飞行时间计算质量-电荷比,适用于高通量肽段筛选与初步鉴定[37]。
综上所述,液相色谱-串联质谱技术凭借优异的灵敏度与准确性,已成为当前食源性肽功能肽段鉴定的主流方法,多项研究已利用该技术成功解析了来源于多种食物蛋白的活性肽段,表3列举了近年来部分典型食源性肽段。
表3 食源性肽中特征肽段的鉴定
Table 3 Identification of characteristic peptide segments in foodborne peptides

续表3

鉴定技术原料肽段参考文献凝胶渗透色谱和反相高效液相色谱绿豆FLVNPDDNENL、FLVNP-DDNENLRIIKDNVISEIPTEVLDL[38]液相色谱-串联质谱牛奶QEPVLGPVRGPFP、YPFPGPIPN[39]反相高效能液相色谱大米蛋白YGIYPR[40]
3 食源性肽的功能特性与应用
食源性肽是由食物蛋白在水解过程中生成的生物活性肽,因其丰富的氨基酸序列和独特的理化特性,展现出多种有益的生理功能。研究表明,食源性肽不仅具有显著的抗炎和血管紧张素转换酶(angiotensin converting enzyme,ACE)抑制活性,还表现出良好的抗氧化、免疫调节、抗癌、降糖及改善肠道功能等多重生物活性(如图1所示)。这些功能主要源于其特定的氨基酸序列和疏水性结构,能够通过多种信号通路参与生理调节和疾病防治。以下将分别阐述食源性肽在不同生理功能中的具体作用机制与研究进展。
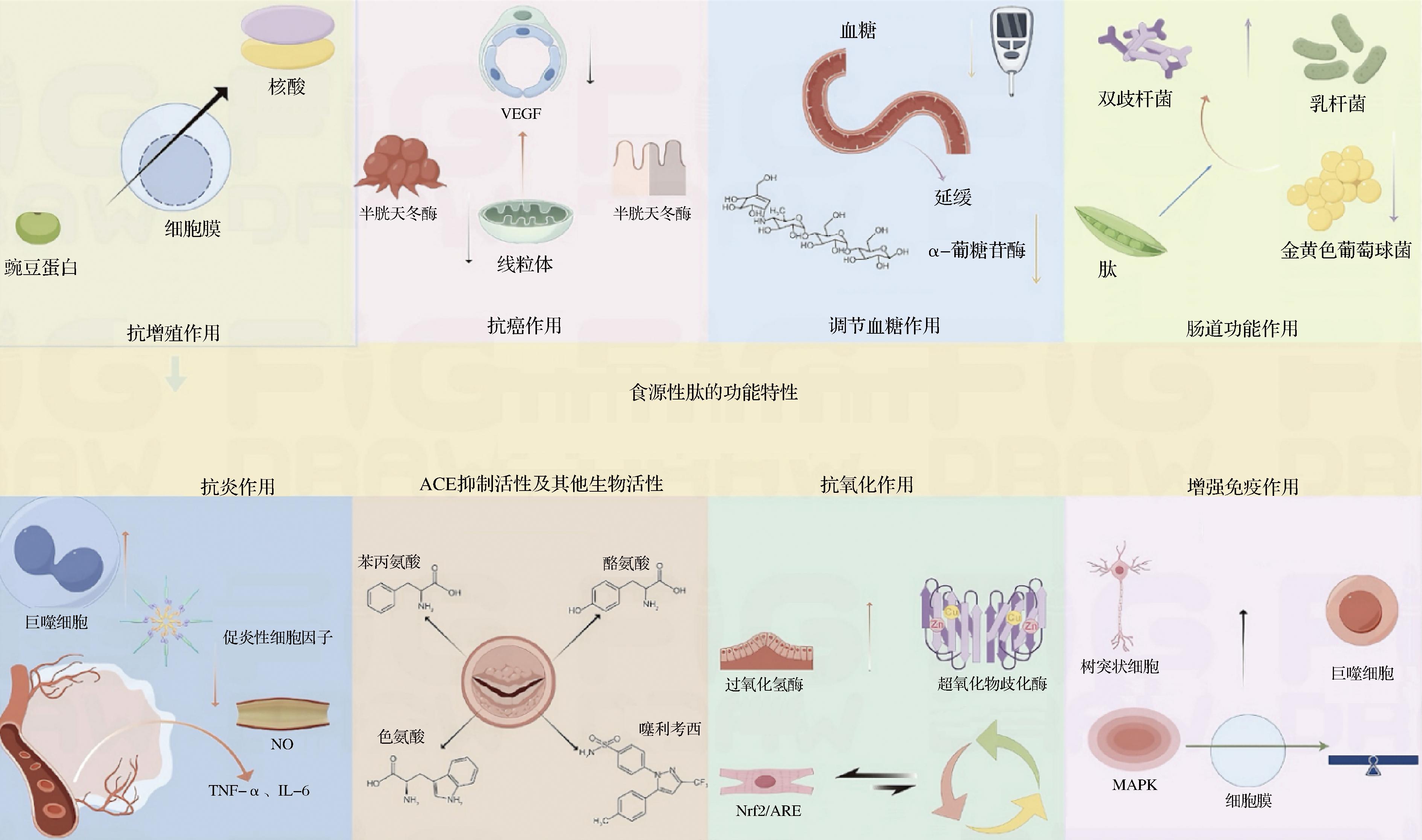
图1 食源性肽的功能特性(Figdraw制图)
Fig.1 Functional characteristics of food-derived peptides(Figdraw drawing)
注:VEGF:血管内皮生长因子;TNF-α:肿瘤坏死因子-α;IL-6:白细胞介素-6;MAPK:丝裂原活化蛋白激酶;Nrf2/ARE:核因子相关因子2/抗氧化反应元件。
3.1 抗炎作用
炎症是机体应对外界有害因素(如病原体感染、组织损伤及有害刺激)的生物防御反应,旨在限制损伤并促进受损组织修复与再生。适度的炎症有助于维持机体稳态,但若失去调控并持续存在,则可能发展为慢性炎症,进而诱发动脉粥样硬化、2型糖尿病、皮肤病以及衰老相关疾病等[41]。
调节氧化应激与炎症反应:食源性肽具有良好抗氧化能力,能够降低活性氧(reative oxygen species,ROS)水平,减轻DNA损伤及脂质过氧化,并下调炎症因子表达,改善癌症微环境,从而抑制肿瘤发生。
近年来,研究表明部分食源性肽具有显著的抗炎活性,已在多种体内外炎症模型中得到验证[42]。其抗炎机制主要包括对炎症信号通路的干预、促炎因子的抑制以及免疫细胞功能的调控。如NF-κB信号通路是调控炎症反应的核心通路之一,参与肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)、IL-6、IL-1β、NO及前列腺素2等多种促炎因子的转录调控[43]。其经典通路由膜受体、IκB激酶复合物(IκB kinase complex,IKK)、IκBα蛋白及NF-κB二聚体组成。当细胞受到脂多糖(lipopolysaccharide,LPS)、促炎因子或ROS刺激时,IKK激活IκBα磷酸化并降解,释放NF-κB p65亚基转移入核,结合靶基因启动子,促进炎症相关基因表达[44]。已有研究表明,食源性活性肽可通过抑制IκBα和p65磷酸化,阻断NF-κB信号通路活化,从而降低促炎因子表达,发挥抗炎作用[45]。同时,已有研究证实,食源性肽可通过抑制激酶级联磷酸化反应,从而降低TNF-α、IL-6等促炎介质的表达。此外,部分肽段可增强巨噬细胞吞噬能力,并在适度释放NO和促炎细胞因子的基础上,实现对免疫反应的双向调控[46]。
氨基酸组成及理化性质是影响食源性肽抗炎活性的关键因素。富含亮氨酸和异亮氨酸的肽段可通过调控激酶磷酸化通路,有效缓解炎症反应;而疏水性较强的肽段可通过与细胞膜相互作用,改变细胞膜表面电荷,抑制LPS诱导的炎症反应[47]。特别是当肽段N端含有疏水性氨基酸残基时,其抗炎效果更为显著[48]。此外,富含正电荷的氨基酸(如赖氨酸、精氨酸和组氨酸)的食源性肽也被证实具有较强的抗压能力,这类氨基酸有助于肽段与靶细胞膜表面相互作用,增强其对炎症信号通路的干预能力[49-50]。
3.2 ACE抑制活性及其他生物活性
高血压是由多种内外因素共同引发的慢性疾病,其主要发病机制与肾素-血管紧张素系统异常激活密切相关。ACE通过催化血管紧张素I转化为血管紧张素II,从而引起血管收缩、血压升高及钠潴留等生理反应。因此,抑制ACE活性已成为治疗高血压的重要靶点之一。ACE是经典肾素-血管紧张素-醛固酮系统中核心降压靶点,其催化血管紧张素I转化为血管紧张素II,同时降解缓激肽,诱导血管收缩及血压升高[51]。食源性ACE抑制肽通过直接与ACE活性中心结合或阻断其催化活性,发挥降压作用[3]。部分研究还发现,ACE抑制肽可间接影响NO/cGMP信号途径,促进血管舒张[52]。
近年来,食源性肽因其天然、安全及多功能特性,逐渐成为ACE抑制剂的潜在替代物。研究表明,黄豌豆蛋白水解产物及花园豌豆衍生的多肽均在体外展现出良好的ACE抑制活性,且部分肽段同时具有抗氧化、降胆固醇、抗菌及抗肿瘤等多重生物活性[53]。结构特性决定了食源性肽的ACE抑制能力。多数活性肽由2~10个氨基酸残基组成,富含脯氨酸、赖氨酸、精氨酸以及疏水性氨基酸的短链肽段,在多项研究中被证实具有抗菌、免疫调节、ACE抑制、血管活性以及神经调节等功能特性[54]。ACE抑制肽通常以线性结构存在,依靠关键氨基酸残基与ACE活性中心结合,阻断酶促反应[54-56]。特别是C端含脯氨酸、苯丙氨酸、色氨酸、酪氨酸和精氨酸残基的肽段,通过氢键、疏水作用及静电相互作用与ACE形成稳定复合物,从而有效抑制其催化活性[57-58]。
3.3 抗氧化作用
氧化应激是指机体内ROS或活性氮水平异常升高,超过内源性抗氧化防御系统调控能力,引发细胞损伤、脂质过氧化及DNA损伤等病理反应的重要机制,与心血管疾病、糖尿病、肿瘤及神经退行性疾病等密切相关。因此,增强机体的抗氧化能力,降低自由基诱导的氧化损伤,对于维持细胞稳态及预防相关疾病至关重要。
研究证实,食源性肽在清除自由基、金属离子螯合及调节氧化应激信号通路方面展现出良好的抗氧化潜力[59-60]。常用的体外抗氧化能力评价方法(如DPPH自由基清除能力、铁离子还原抗氧化能力及β-胡萝卜素-亚油酸漂白法等),均表明食源性肽在不同模型中展现出显著的抗氧化活性[61-62]。这些生物活性使得食源性肽在减缓氧化损伤、延缓衰老及预防与氧化应激相关疾病方面具有重要应用前景。在机制研究方面,食源性肽的抗氧化活性与其氨基酸组成及序列特征密切相关。富含含硫氨基酸(半胱氨酸、蛋氨酸)、芳香族氨基酸(酪氨酸、色氨酸)及带正电荷氨基酸(赖氨酸、精氨酸)肽段,表现出较强自由基清除及抗氧化酶调节活性[63]。其中,含硫氨基酸通过提供巯基(—SH)与自由基直接反应,而芳香族氨基酸可稳定自由基中间体,部分短肽还能激活Nrf2/ARE信号通路,上调超氧化物歧化酶、过氧化氢酶及谷胱甘肽过氧化物酶等抗氧化酶的表达,提升细胞氧化防御能力。目前,Keap1/Nrf2/ARE是食源性肽抗氧化作用研究最多的信号通路。当细胞处于氧化应激状态时,Nrf2从Keap1抑制复合物中释放,转位至细胞核,与抗氧化反应元件结合,激活下游抗氧化酶如超氧化物歧化酶、谷胱甘肽过氧化物酶、NAD(P)H:醌氧化还原酶1及血红素加氧酶-1等的表达,从而清除ROS,维持细胞内氧化还原稳态[64-65]。大量研究表明,多种来源的食源性肽如玉米、豆类、乳清蛋白和海洋蛋白水解物均可通过激活Nrf2通路,缓解氧化损伤[66]。
3.4 增强免疫作用
免疫系统是机体维持内环境稳定、抵御病原微生物和清除异常细胞的重要防御机制,免疫系统功能紊乱易诱发感染、慢性炎症及自身免疫性疾病。目前用于治疗免疫相关疾病的药物往往存在副作用较大或不适合长期使用的问题。因此,寻找安全有效的免疫调节手段成为研究的热点。
多项研究证实,食源性肽可通过调节免疫相关因子的表达和分泌,改善机体免疫稳态,在预防和缓解免疫相关疾病中发挥积极作用[67]。在免疫调节机制方面,研究发现食源性肽能够通过抑制NO的合成,减少过度的炎症反应,同时通过增强促炎细胞因子(如TNF-α和IL-6)的分泌,刺激免疫反应,从而增强机体的免疫防御能力[68]。
在信号通路方面,MAPK家族(ERK、JNK和p38)参与细胞的增殖、分化、凋亡和免疫调控。食源性肽可通过激活ERK或抑制JNK、p38途径,调节巨噬细胞、T细胞和NK细胞功能,增强免疫反应[69-70]。例如,Mytilus edulis蛋白水解物能显著上调RAW264.7巨噬细胞中的ERK磷酸化水平,促进NO和IL-6等免疫因子的分泌[71]。
JAK/STAT是另一条经典免疫信号通路,调节细胞对细胞因子的应答。当细胞因子与其受体结合后,JAK激酶被活化,磷酸化STAT蛋白,形成二聚体转位入核,调节免疫相关基因表达。多项研究表明,食源性肽可通过上调JAK/STAT途径,促进NK细胞活性和巨噬细胞吞噬功能,增强非特异性免疫反应[72]。
3.5 抗癌作用
胃肠道癌症是全球发病率和致死率均居前列的恶性肿瘤类型,发病涉及慢性炎症、遗传易感性、不良饮食习惯及病原微生物感染等因素。其异常增殖和侵袭能力是疾病恶化和转移的关键。目前临床常用的抗癌治疗手段主要包括化疗、放疗和靶向治疗等,但存在较大的副作用,如非靶向性损伤正常组织、诱导耐药性及引发免疫抑制等问题。因此,开发天然来源、安全性高且具有良好靶向作用的抗癌功能成分,已成为当代癌症防治研究的重要方向。
近年来,食源性肽在抗胃肠道癌症方面表现出良好的生物活性,尤其在抑制癌细胞增殖和诱导凋亡方面具有显著作用。植物来源的活性肽由于来源丰富、结构多样、毒性较低,成为癌症辅助治疗或功能食品开发的重要候选物。
抗癌肽(anticancer peptides,ACPs)通过多途径发挥抗肿瘤作用,主要机制包括膜破坏、线粒体凋亡及信号通路调节。ACPs富含正电荷和疏水性氨基酸残基,可选择性结合癌细胞膜表面带负电的磷脂成分,破坏膜结构完整性,诱导细胞裂解或坏死。同时,部分ACPs可激活线粒体凋亡通路,促进细胞内ROS积聚,诱导线粒体膜电位丧失,释放细胞色素C,依次激活Caspase-9和Caspase-3,诱导细胞程序性死亡。此外,ACPs还能通过抑制PI3K/Akt、NF-κB等促存活信号通路,阻断下游Bcl-2、mTOR活化,促进癌细胞凋亡并抑制迁移侵袭。这些多靶点、复合型机制使ACPs在抗药性肿瘤治疗中展现出良好应用前景[68]。
食源性肽的抗癌作用机制主要包括以下几个方面[68]:
抑制癌细胞增殖:部分肽段可调控细胞周期相关蛋白(如cyclin D1和CDK4)表达,阻断细胞周期进程,同时干扰PI3K/Akt、MAPK等信号通路激活,抑制与细胞生长信号传导过程。
诱导癌细胞凋亡:富含疏水性及带正电荷氨基酸残基(如亮氨酸、赖氨酸、精氨酸等)的食源性肽,可激活线粒体依赖性凋亡通路,显著提高Caspase-3和Caspase-9等表达,抑制抗凋亡蛋白Bcl-2表达、促进促凋亡蛋白Bax表达,诱导癌细胞程序性凋亡。
抑制肿瘤血管生成:部分食源性肽可抑制血管内皮生长因子及其受体表达,阻断肿瘤新生血管形成,间接限制肿瘤扩增与转移能力。
抑制癌细胞迁移与侵袭:食源性肽被证实可通过下调基质金属蛋白酶(MMP-2和MMP-9)活性,限制癌细胞对基质的降解过程,从而有效抑制其迁移和侵袭行为。
综上所述,食源性肽可通过多靶点、多通路调控,展现出良好的抗癌潜力,为癌症辅助治疗及功能食品研发提供了分子基础。但当前研究仍多局限于体外模型,缺乏系统性体内药效学评价及作用机制验证,未来应重点围绕其体内稳定性、靶向性及安全性开展深入研究,推动其在癌症防治中的应用转化。
3.6 调节血糖作用
糖尿病是一种以血糖代谢紊乱为特征的慢性代谢性疾病,其主要病理机制由胰岛素分泌不足或胰岛素抵抗引起[73]。长期高血糖可引发胰岛β细胞功能障碍,促进氧化应激反应和慢性炎症反应的发生,进而导致糖尿病视网膜病变、肾病和神经病变等微血管并发症[73]。除药物及胰岛素治疗外,开发安全、天然及多靶点的功能活性成分成为防治的研究热点。研究表明,食源性肽在调节血糖水平、改善胰岛功能及胰岛素敏感性方面具有良好的生物活性[73]。来源于植物蛋白(如大豆、豌豆)及动物蛋白(如乳清、鱼类)的活性肽,可通过多靶点机制发挥降糖作用。例如,部分食源性肽可通过抑制α-葡萄糖苷酶和二肽基肽酶-4等关键酶活性,延缓糖类物质的分解与吸收,降低餐后血糖水平。α-淀粉酶和α-葡萄糖苷酶是控制淀粉消化速率、调节餐后血糖水平的关键消化酶。食源性非酚类化合物(如多糖、肽类和有机酸)可通过抑制这2种酶的活性,延缓淀粉水解,降低葡萄糖释放速率,从而缓解血糖波动。例如,桑叶提取物中的1-脱氧野尻霉素对α-葡萄糖苷酶表现出强效抑制作用,玫瑰茄中的花色苷和有机酸亦能显著抑制α-淀粉酶活性,有助于餐后血糖调控[74]。
3.7 肠道功能作用
肠道菌群是人体内数量最多、种类最丰富的微生态系统,广泛参与宿主的营养吸收、免疫调节和屏障功能维持等生理过程。菌群组成紊乱易诱发炎症性肠病、代谢综合征及自身免疫性疾病等[75]。不良饮食结构、抗生素滥用及慢性疾病状态等均可破坏肠道微生态平衡,导致有害菌增殖,从而引发肠道屏障功能受损和系统性炎症反应。因此,调节肠道菌群结构、恢复其稳态已成为提升肠道健康、预防慢性疾病的重要策略。研究发现,食源性肽具有良好的肠道调节功能,可通过多种机制维持肠道菌群稳态。例如,豌豆肽在体外研究中表现出抑制特定有害菌(如大肠杆菌、金黄色葡萄球菌)生长的能力,具有一定的抗感染作用[76]。此外,某些食源性肽还可促进益生菌(如双歧杆菌、乳酸杆菌)的增殖,增强肠道屏障功能,调节黏膜免疫反应,改善肠道微环境。其在维持肠道微生态平衡、防治肠道相关疾病方面展现出广阔的应用前景。
肠道慢性炎症是炎症性肠病发病的核心病理机制,涉及氧化应激、细胞凋亡、肠屏障功能障碍及肠道微生态失衡等多重因素。食源性肽可通过多靶点机制调节肠道免疫稳态,缓解炎症反应。例如,乳清蛋白肽可降低促炎因子TNF-α、IL-6表达,促进IL-10等抗炎因子释放,改善结肠组织病理损伤。同时,部分食源性肽能增强紧密连接蛋白(ZO-1、occludin)表达,修复肠黏膜屏障,抑制肠道细胞凋亡,并通过调节NF-κB和MAPK信号通路,降低氧化应激水平,从而发挥抗炎症性肠病作用[72]。
4 结论
食源性肽作为一类具有重要生物活性的功能成分,近年来受到了广泛关注。本文系统综述了食源性肽的来源、功能特性、稳定性研究、代谢吸收机制、核心肽段的鉴定方法及其在功能性食品中的应用。研究表明,食源性肽不仅在降血压、抗氧化、抗炎、免疫调节等方面展现出显著的生物学活性,还在改善代谢综合征和促进肠道健康方面具有潜在的应用价值。尽管食源性肽在功能性食品领域的应用前景广阔,但仍存在一些挑战。例如,食源性肽在体内的稳定性及其生物利用度受到胃肠道消化和吸收过程的影响。此外,功能性肽段的精确鉴定与合成、结构-功能关系的深入解析以及工业化生产技术的优化仍需进一步探索。未来的研究应致力于通过现代组学和生物信息学手段,深入挖掘食源性肽的结构与功能特性,开发高效稳定的制备与应用技术,从而推动食源性肽在促进健康和疾病预防领域的广泛应用。
[1] KORHONEN H, PIHLANTO A.Bioactive peptides:Production and functionality[J].International Dairy Journal, 2006, 16(9):945-960.
[2] 陈心瑷, 翟兴月, 佟长青, 等.生物活性肽和肠道菌群相互作用研究进展[J].食品安全质量检测学报, 2022, 13(4):1044-1049.
CHEN X A, ZHAI X Y, TONG C Q, et al.Research progress on interaction between bioactive peptides and gut microbiota[J].Journal of Food Safety &Quality, 2022, 13(4):1044-1049.
[3] UDENIGWE C C, ALUKO R E.Food protein-derived bioactive peptides:Production, processing, and potential health benefits[J].Journal of Food Science, 2012, 77(1):R11-R24.
[4] MINE Y, LI-CHAN E, JIANG B. Bioactive Proteins and Peptides as Functional Foods and Nutraceuticals[M]. Ames, IA: Wiley, 2010.
[5] G MEZ-GUILLÉN M C, GIMÉNEZ B, L
MEZ-GUILLÉN M C, GIMÉNEZ B, L PEZ-CABALLERO M E, et al.Functional and bioactive properties of collagen and gelatin from alternative sources:A review[J].Food Hydrocolloids, 2011, 25(8):1813-1827.
PEZ-CABALLERO M E, et al.Functional and bioactive properties of collagen and gelatin from alternative sources:A review[J].Food Hydrocolloids, 2011, 25(8):1813-1827.
[6] UDENIGWE C C.Bioinformatics approaches, prospects and challenges of food bioactive peptide research[J].Trends in Food Science &Technology, 2014, 36(2):137-143.
[7] NONGONIERMA A B, FITZGERALD R J.Strategies for the discovery, identification and validation of milk protein-derived bioactive peptides[J].Trends in Food Science &Technology, 2016, 50:26-43.
[8] D’ADDIO S M, BOTHE J R, NERI C, et al.New and evolving techniques for the characterization of peptide therapeutics[J].Journal of Pharmaceutical Sciences, 2016, 105(10):2989-3006.
[9] L PEZ-S
PEZ-S NCHEZ J, PONCE-ALQUICIRA E, PEDROZA-ISLAS R, et al.Effects of heat and pH treatments and in vitro digestion on the biological activity of protein hydrolysates of Amaranthus hypochondriacus L.grain[J].Journal of Food Science and Technology, 2016, 53(12):4298-4307.
NCHEZ J, PONCE-ALQUICIRA E, PEDROZA-ISLAS R, et al.Effects of heat and pH treatments and in vitro digestion on the biological activity of protein hydrolysates of Amaranthus hypochondriacus L.grain[J].Journal of Food Science and Technology, 2016, 53(12):4298-4307.
[10] WANG X Q, YU H H, XING R E, et al.Optimization of the extraction and stability of antioxidative peptides from mackerel (Pneumatophorus japonicus) protein[J].BioMed Research International, 2017, 2017:6837285.
[11] ZHU C Z, ZHANG W G, KANG Z L, et al.Stability of an antioxidant peptide extracted from Jinhua ham[J].Meat Science, 2014, 96(2):783-789.
[12] 邹颖玲,王桂瑛,王雪峰,等.火腿中生物活性肽的研究进展[J].食品研究与开发,2020,41(6):205-210.
ZOU Y L, WANG G Y, WANG X F, et al.Review of bioactive peptides derived from dry-cured ham[J].Food Research and Development, 2020, 41(6):205-210.
[13] GURUPRASAD K, REDDY B V, PANDIT M W.Correlation between stability of a protein and its dipeptide composition:A novel approach for predicting in vivo stability of a protein from its primary sequence[J].Protein Engineering, 1990, 4(2):155-161.
[14] MIRZAEI M, MIRDAMADI S, SAFAVI M, et al.The stability of antioxidant and ACE-inhibitory peptides as influenced by peptide sequences[J].LWT, 2020, 130:109710.
[15] DE ROSA L, DIANA D, DI STASI R, et al.Probing the helical stability in a VEGF-mimetic peptide[J].Bioorganic Chemistry, 2021, 116:105379.
[16] ASADUZZAMAN A K M, CHUN B S.Recovery of functional materials with thermally stable antioxidative properties in squid muscle hydrolyzates by subcritical water[J].Journal of Food Science and Technology, 2015, 52(2):793-802.
[17] UDENIGWE C C, FOGLIANO V.Food matrix interaction and bioavailability of bioactive peptides:Two faces of the same coin[J].Journal of Functional Foods, 2017, 35:9-12.
[18] KARA M.Influence of physiological and chemical factors on the absorption of bioactive peptides[J].International Journal of Food Science &Technology, 2019, 54(5):1486-1496.
M.Influence of physiological and chemical factors on the absorption of bioactive peptides[J].International Journal of Food Science &Technology, 2019, 54(5):1486-1496.
[19] BHANDARI D, RAFIQ S, GAT Y, et al.A review on bioactive peptides:Physiological functions, bioavailability and safety[J].International Journal of Peptide Research and Therapeutics, 2020, 26(1):139-150.
[20] XU Q B, HONG H, WU J P, et al.Bioavailability of bioactive peptides derived from food proteins across the intestinal epithelial membrane:A review[J].Trends in Food Science &Technology, 2019, 86:399-411.
[21] JAKUBCZYK A, KARA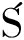 M, RYBCZY
M, RYBCZY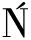 SKA-TKACZYK K, et al.Current trends of bioactive peptides-new sources and therapeutic effect[J].Foods, 2020, 9(7):846.
SKA-TKACZYK K, et al.Current trends of bioactive peptides-new sources and therapeutic effect[J].Foods, 2020, 9(7):846.
[22] SHEN W L, MATSUI T.Intestinal absorption of small peptides:A review[J].International Journal of Food Science &Technology, 2019, 54(6):1942-1948.
[23] DALIRI E, OH D, LEE B.Bioactive peptides[J].Foods, 2017, 6(5):32.
[24] WANG B, XIE N N, LI B.Influence of peptide characteristics on their stability, intestinal transport, and in vitro bioavailability:A review[J].Journal of Food Biochemistry, 2019, 43(1):e12571.
[25] MIRZAEI M, SHAVANDI A, MIRDAMADI S, et al.Bioactive peptides from yeast:A comparative review on production methods, bioactivity, structure-function relationship, and stability[J].Trends in Food Science &Technology, 2021, 118:297-315.
[26] PICARIELLO G, FERRANTI P, FIERRO O, et al.Peptides surviving the simulated gastrointestinal digestion of milk proteins:Biological and toxicological implications[J].Journal of Chromatography B, 2010, 878(3-4):295-308.
[27] XIE N N, WANG B, JIANG L P, et al.Hydrophobicity exerts different effects on bioavailability and stability of antioxidant peptide fractions from casein during simulated gastrointestinal digestion and Caco-2 cell absorption[J].Food Research International, 2015, 76:518-526.
[28] SAVOIE L, AGUDELO R A, GAUTHIER S F, et al.In vitro determination of the release kinetics of peptides and free amino acids during the digestion of food proteins[J].Journal of AOAC INTERNATIONAL, 2005, 88(3):935-948.
[29] HAO L, GAO X C, ZHOU T Y, et al.Angiotensin I-converting enzyme (ACE) inhibitory and antioxidant activity of umami peptides after in vitro gastrointestinal digestion[J].Journal of Agricultural and Food Chemistry, 2020, 68(31):8232-8241.
[30] YUAN L, SUN L P, ZHUANG Y L.Preparation and identification of novel inhibitory angiotensin-I-converting enzyme peptides from tilapia skin gelatin hydrolysates:Inhibition kinetics and molecular docking[J].Food &Function, 2018, 9(10):5251-5259.
[31] CHEN M, LI B.The effect of molecular weights on the survivability of casein-derived antioxidant peptides after the simulated gastrointestinal digestion[J].Innovative Food Science &Emerging Technologies, 2012, 16:341-348.
[32] MARSEGLIA A, DELLAFIORA L, PRANDI B, et al.Simulated gastrointestinal digestion of cocoa:Detection of resistant peptides and in silico/in vitro prediction of their ace inhibitory activity[J].Nutrients, 2019, 11(5):985.
[33] XU B F, WANG X Y, ZHENG Y J, et al.Novel antioxidant peptides identified in millet bran glutelin-2 hydrolysates:Purification, in silico characterization and security prediction, and stability profiles under different food processing conditions[J].LWT, 2022, 164:113634.
[34] WONG F C, XIAO J B, ONG M G, et al.Identification and characterization of antioxidant peptides from hydrolysate of blue-spotted stingray and their stability against thermal, pH and simulated gastrointestinal digestion treatments[J].Food Chemistry, 2019, 271:614-622.
[35] PÉREZ-GREGORIO R, SOARES S, MATEUS N, et al.Bioactive peptides and dietary polyphenols:Two sides of the same coin[J].Molecules, 2020, 25(15):3443.
[36] WANG X Q, YU H H, XING R E, et al.Characterization, preparation, and purification of marine bioactive peptides[J].BioMed Research International, 2017, 2017:9746720.
[37] PEKOV S, INDEYKINA M, POPOV I, et al.Application of MALDI-TOF/TOF-MS for relative quantitation of α- and β-Asp7 isoforms of amyloid-β peptide[J].European Journal of Mass Spectrometry, 2018, 24(1):141-144.
[38] ZHAO L L, LIU X H, WANG S P, et al.Research progress on fermentation-produced plant-derived bioactive peptides[J].Frontiers in Pharmacology, 2024, 15:1438947.
[39] CUI Q, DUAN Y Q, ZHANG M J, et al.Peptide profiles and antioxidant capacity of extensive hydrolysates of milk protein concentrate[J].Journal of Dairy Science, 2022, 105(10):7972-7985.
[40] XU Z, MAO T M, HUANG L, et al.Purification and identification immunomodulatory peptide from rice protein hydrolysates[J].Food and Agricultural Immunology, 2019, 30(1):150-162.
[41] CHAKRABARTI S, JAHANDIDEH F, WU J P.Food-derived bioactive peptides on inflammation and oxidative stress[J].BioMed Research International, 2014, 2014:608979.
[42] ZHANG S H, REN M, ZENG X F, et al.Leucine stimulates ASCT2 amino acid transporter expression in porcine jejunal epithelial cell line (IPEC-J2) through PI3K/Akt/mTOR and ERK signaling pathways[J].Amino Acids, 2014, 46(12):2633-2642.
[43] KIM Y S, AHN C B, JE J Y.Anti-inflammatory action of high molecular weight Mytilus edulis hydrolysates fraction in LPS-induced RAW264.7 macrophage via NF-κB and MAPK pathways[J].Food Chemistry, 2016, 202:9-14.
[44] FAN X L, ZHANG Y H, DONG H Q, et al.Trilobatin attenuates the LPS-mediated inflammatory response by suppressing the NF-κB signaling pathway[J].Food Chemistry, 2015, 166:609-615.
[45] LI T G, GAO D X, DU M, et al.Casein glycomacropeptide hydrolysates inhibit PGE2 production and COX2 expression in LPS-stimulated RAW264.7 macrophage cells via Akt mediated NF-κB and MAPK pathways[J].Food &Function, 2018, 9(4):2524-2532.
[46] LIU H, WANG J P, LIU Y J, et al.Characterisation of functional pea protein hydrolysates and their immunomodulatory activity[J].International Journal of Food Science &Technology, 2024, 59(5):3317-3330.
[47] SINGH S, DATTA A, SCHMIDTCHEN A, et al.Tryptophan end-tagging for promoted lipopolysaccharide interactions and anti-inflammatory effects[J].Scientific Reports, 2017, 7:212.
[48] LIU H, LI B.Separation and identification of collagen peptides derived from enzymatic hydrolysate of Salmo salar skin and their anti-inflammatory activity in lipopolysaccharide (LPS)-induced RAW264.7 inflammatory model[J].Journal of Food Biochemistry, 2022, 46(7):e14122.
[49] CHEN X H, SUN L L, LI D L, et al.Green tea peptides ameliorate diabetic nephropathy by inhibiting the TGF-β/Smad signaling pathway in mice[J].Food &Function, 2022, 13(6):3258-3270.
[50] SAISAVOEY T, SANGTANOO P, CHANCHAO C P, et al.Identification of novel anti-inflammatory peptides from bee pollen (Apis mellifera) hydrolysate in lipopolysaccharide-stimulated RAW264.7 macrophages[J].Journal of Apicultural Research, 2021, 60(2):280-289.
[51] WU Q, LUO F J, WANG X L, et al.Angiotensin I-converting enzyme inhibitory peptide:An emerging candidate for vascular dysfunction therapy[J].Critical Reviews in Biotechnology, 2022, 42(5):736-755.
[52] DE LEO F, PANARESE S, GALLERANI R, et al.Angiotensin converting enzyme (ACE) inhibitory peptides:Production and implementation of functional food[J].Current Pharmaceutical Design, 2009, 15(31):3622-3643.
[53] NDIAYE F, VUONG T, DUARTE J, et al.Anti-oxidant, anti-inflammatory and immunomodulating properties of an enzymatic protein hydrolysate from yellow field pea seeds[J].European Journal of Nutrition, 2012, 51(1):29-37.
[54] CARBONARO M, MASELLI P, NUCARA A.Structural aspects of legume proteins and nutraceutical properties[J].Food Research International, 2015, 76:19-30.
[55] NATESH R, SCHWAGER S L U, STURROCK E D, et al.Crystal structure of the human angiotensin-converting enzyme-lisinopril complex[J].Nature, 2003, 421(6922):551-554.
[56] BHUYAN B J, MUGESH G.Antioxidant activity of peptide-based angiotensin converting enzyme inhibitors[J].Organic &Biomolecular Chemistry, 2012, 10(11):2237-2247.
[57] WU J P, ALUKO R E, NAKAI S.Structural requirements of Angiotensin I-converting enzyme inhibitory peptides:Quantitative structure-activity relationship study of di- and tripeptides[J].Journal of Agricultural and Food Chemistry, 2006, 54(3):732-738.
[58] KAMRAN F, REDDY N.Bioactive peptides from legumes:Functional and nutraceutical potential[J].Recent Advances in Food Science, 2018, 1(3):134-149.
[59] 吴宝森, 孙玥晖, 刘姝韵, 等.火腿中抗氧化肽的研究进展[J].食品安全质量检测学报, 2016,7(12):4809-4814.
WU B S, SUN Y H, LIU S Y, et al.Research progress of antioxidant peptides in ham[J].Journal of Food Safety &Quality, 2016,7(12):4809-4814.
[60] 郑召君, 武如娟, 张日俊.动物源性抗氧化肽的生物学功能及与其结构的关系[J].动物营养学报, 2015,27(4):1034-1040.
ZHENG Z J, WUR J, ZHANG R J.Biological functions of animal-derived antioxidative peptides and its relationship with the peptides structure[J].Chinese Journal of Animal Nutrition, 2015, 27(4):1034-1040.
[61] LEMUS-CONEJO A, VILLANUEVA-LAZO A, MARTIN M E, et al.Sacha inchi (Plukenetia volubilis L.) protein hydrolysate as a new ingredient of functional foods[J].Foods, 2024, 13(13):2045.
[62] 王乐, 成晓瑜, 马晓钟, 等.金华火腿加热烹饪和体外模拟消化后粗肽抗氧化和ACE抑制活性比较研究[J].肉类研究, 2018, 32(1):16-22.
WANG L, CHENG X Y, MA X Z, et al.Comparison of antioxidant and angiotensin converting enzyme inhibitory activities of crude peptide extract from Jinhua ham after cooking and in vitro simulated gastrointestinal digestion[J].Meat Research,2018, 32(1):16-22.
[63] 李丽,杨兰芬,杨金燕,等.生物活性肽抗氧化作用的研究进展[J].工业微生物,2025,55(1):43-45.
LI L,YANG L F,YANG J Y, et al.Research progress on the antioxidant effect of bioactive peptides[J].Industrial Microbiology, 2025, 55(1):43-45.
[64] KENSLER T W, WAKABAYASHI N, BISWAL S.Cell survival responses to environmental stresses via the Keap1-Nrf2-ARE pathway[J].Annual Review of Pharmacology and Toxicology, 2007, 47:89-116.
[65] HE R, WANG Y J, YANG Y J, et al.Rapeseed protein-derived ACE inhibitory peptides LY, RALP and GHS show antioxidant and anti-inflammatory effects on spontaneously hypertensive rats[J].Journal of Functional Foods, 2019, 55:211-219.
[66] ZHANG R Q, REN Y K, REN T Q, et al.Marine-derived antioxidants:A comprehensive review of their therapeutic potential in oxidative stress-associated diseases[J].Marine Drugs, 2025, 23(6):223.
[67] SANGEETHA VIJAYAN P, XAVIER J, VALAPPIL M P.A review of immune modulators and immunotherapy in infectious diseases[J].Molecular and Cellular Biochemistry, 2024, 479(8):1937-1955.
[68] NOROUZI P, MIRMOHAMMADI M, HOUSHDAR TEHRANI M H.Anticancer peptides mechanisms, simple and complex[J].Chemico-Biological Interactions, 2022, 368:110194.
[69] COSKUN M, OLSEN J, SEIDELIN J B, et al.MAP kinases in inflammatory bowel disease[J].Clinica Chimica Acta, 2011, 412(7-8):513-520.
[70] KYRIAKIS J M, AVRUCH J.Mammalian MAPK signal transduction pathways activated by stress and inflammation:A 10-year update[J].Physiological Reviews, 2012, 92(2):689-737.
[71] RIVERA-JIMÉNEZ J, BERRAQUERO-GARC A C, PÉREZ-G
A C, PÉREZ-G LVEZ R, et al.Peptides and protein hydrolysates exhibiting anti-inflammatory activity:Sources, structural features and modulation mechanisms[J].Food &Function, 2022, 13(24):12510-12540.
LVEZ R, et al.Peptides and protein hydrolysates exhibiting anti-inflammatory activity:Sources, structural features and modulation mechanisms[J].Food &Function, 2022, 13(24):12510-12540.
[72] ZHU W Y, REN L Y, ZHANG L, et al.The potential of food protein-derived bioactive peptides against chronic intestinal inflammation[J].Mediators of Inflammation, 2020, 2020:6817156.
[73] DENG X, PENG D D, YAO Y F, et al.Optogenetic therapeutic strategies for diabetes mellitus[J].Journal of Diabetes, 2024, 16(6):e13557.
[74] JAHANDIDEH F, BOURQUE S L, WU J P.A comprehensive review on the glucoregulatory properties of food-derived bioactive peptides[J].Food Chemistry:X, 2022, 13:100222.
[75] ZHOU Y C, ZHANG D D, CHENG H, et al.Repairing gut barrier by traditional Chinese medicine:Roles of gut microbiota[J].Frontiers in Cellular and Infection Microbiology, 2024, 14:1389925.
[76] WIJESEKARA T, ABEYRATHNE E D N S, AHN D U.Effect of bioactive peptides on gut microbiota and their relations to human health[J].Foods, 2024, 13(12):1853.