花色苷是一类水溶性色素,是果蔬及其制品(如葡萄酒等)的主要呈色物质。花色苷拥有典型的C6(A环)-C3(C环)-C6(B环)碳骨架结构,其中含氧杂环(C环)的存在增强了花色苷稳定性,也为与其他分子的相互作用提供了可能[1]。花色苷是葡萄酒中的主要呈色物质,目前已在葡萄酒中发现了300多种花色苷,主要分为单体花色苷、酰化花色苷及吡喃花色苷(pyranoanthocyanins,PACN)3类[2]。葡萄酒发酵初期,果皮和果实中的单体花色苷,能够赋予葡萄酒紫红色调,而单体花色苷在发酵过程中不稳定,会随发酵时间的延长而逐渐减少[3]。在发酵过程中,单体花色苷会与阿魏酸、香豆酸、咖啡酸等有机酸酰化生成酰基化花色苷,其在酸性条件下稳定性更好,从而赋予葡萄酒更加稳定的颜色[4]。到酿酒后期的成熟阶段,单体花色苷,尤其是酰基化花色苷,又会与乙醛、乙烯基酚、α-酮戊二酸、丙酮酸等物质发生加环反应形成PACN[5],此时葡萄酒的颜色也从鲜艳的宝石红色或紫红色逐渐过渡为陈酿酒特有的砖红色[6]。
PACN通过保护花色苷C环免受水的亲核攻击,显著抑制其水解过程,从而弥补单体花色苷稳定性差的缺陷;此外,PACN还能与其他有机酸、多酚等物质发生加成、缩合等反应,形成分子质量更大的聚合花色苷,通过增强分子结构的复杂性提升整体稳定性[7-8]。目前,涉及PACN的研究较少,这可能与中国葡萄酒产业的发展起步比较晚有关。与通过酰化、酯化等手段对花色苷进行结构修饰以增强稳定性和功能活性的方法相比,PACN的发现有效弥补了传统修饰中转化效率低、步骤繁琐及选择性差等局限[9]。作为新型花色苷衍生物,PACN不仅保留了单体花色苷的抗氧化、抗菌、抗过敏、抗肿瘤等多种生物活性,还克服了其易受pH、光照、温度及金属离子等因素影响而降解的缺点[10-12],在具备更高稳定性的同时,还能丰富自然界的颜色多样性[13]。因此,本文对PACN的结构、稳定性、生物活性和应用等方面进行了综述,旨在为PACN的开发和利用提供参考。
1 PACN结构及颜色特征
花色苷化学本质是糖基化花青素,是2-苯并吡喃或黄烊盐离子的多羟基以及甲氧基衍生物,结构为C6(A环)-C3(C环)-C6(B环)型黄酮骨架及2个芳香环和1个含氧杂环,具有抗过敏、抗氧化、抗肿瘤、抗菌等多种功能[1]。花色苷能与其他化合物生成花色苷衍生物,该类衍生物大致分为PACN和非PACN两大类。其中,PACN在花色苷结构的C4和C5位的羟基之间有1个额外的吡喃D环(图1)[14],在清除自由基、抗炎、抗乳腺癌、抗氧化和缓解糖尿病等方面有较好的效果,具有较高的生物活性[15]。此外,PACN对陈酿红酒颜色贡献颇大,在发酵过程中促进红酒颜色由紫红色向砖红色转变,提升了红酒的品质和口感[14]。与花色苷前体的辅因子不同,形成PACN的结构特点和颜色特征也有所差异,可分为8类,如表1和图2所示。
表1 PACN的8大类型及颜色[16]
Table 1 Types and colors of PACN[16]

类型反应底物颜色第一代PACNVitisin B 型花色苷花色苷+乙醛橙色Vitisin A 型花色苷花色苷+丙酮酸橙红色甲基PACN花色苷+丙酮酸或花色苷+乙酰乙酸橙黄色黄烷醇PACN花色苷+黄烷醇橙红色酚基PACN(含Pinotin型)花色苷+羟基肉桂酸类橙红色第二代PACNPortisins型PACN花色苷+乙醛+丙酮酸+黄烷醇或花色苷+丙酮酸+乙烯基苯酚/氨基肉桂酸+间苯三酚深蓝色或紫红色内酯型(吡喃酮型)PACNVitisin A+水黄色PACN二聚体Vitisin A+甲基PACN蓝绿色
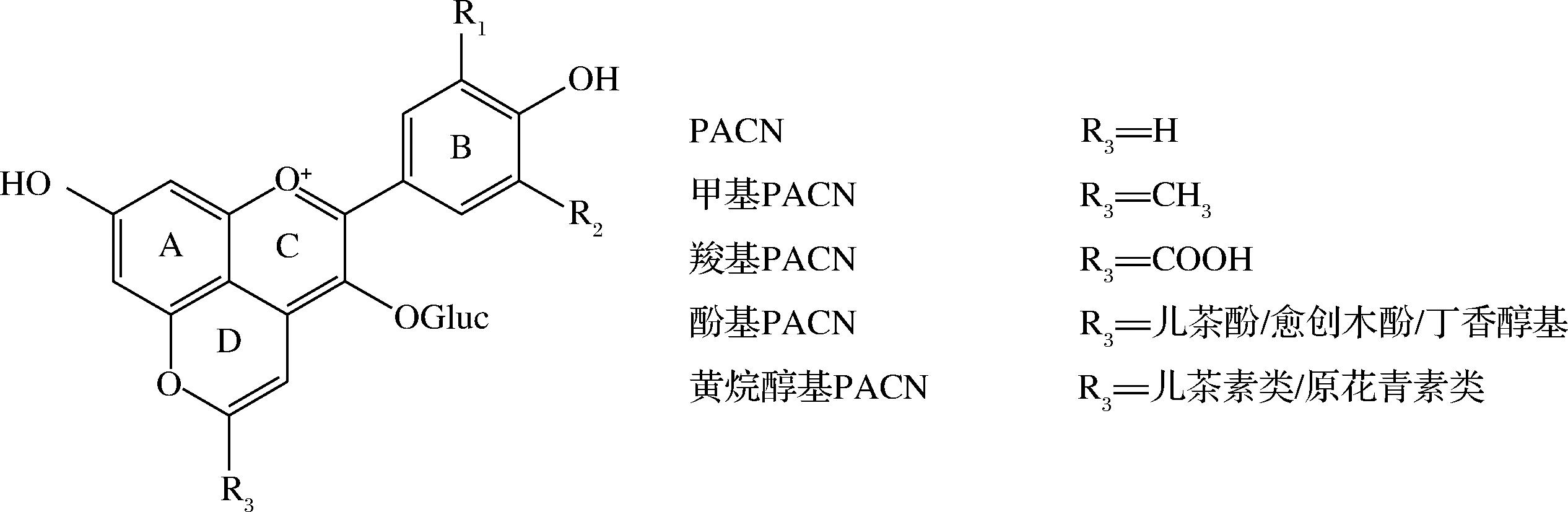
图1 PACN基本结构[15]
Fig.1 Basic structure of PACN[15]
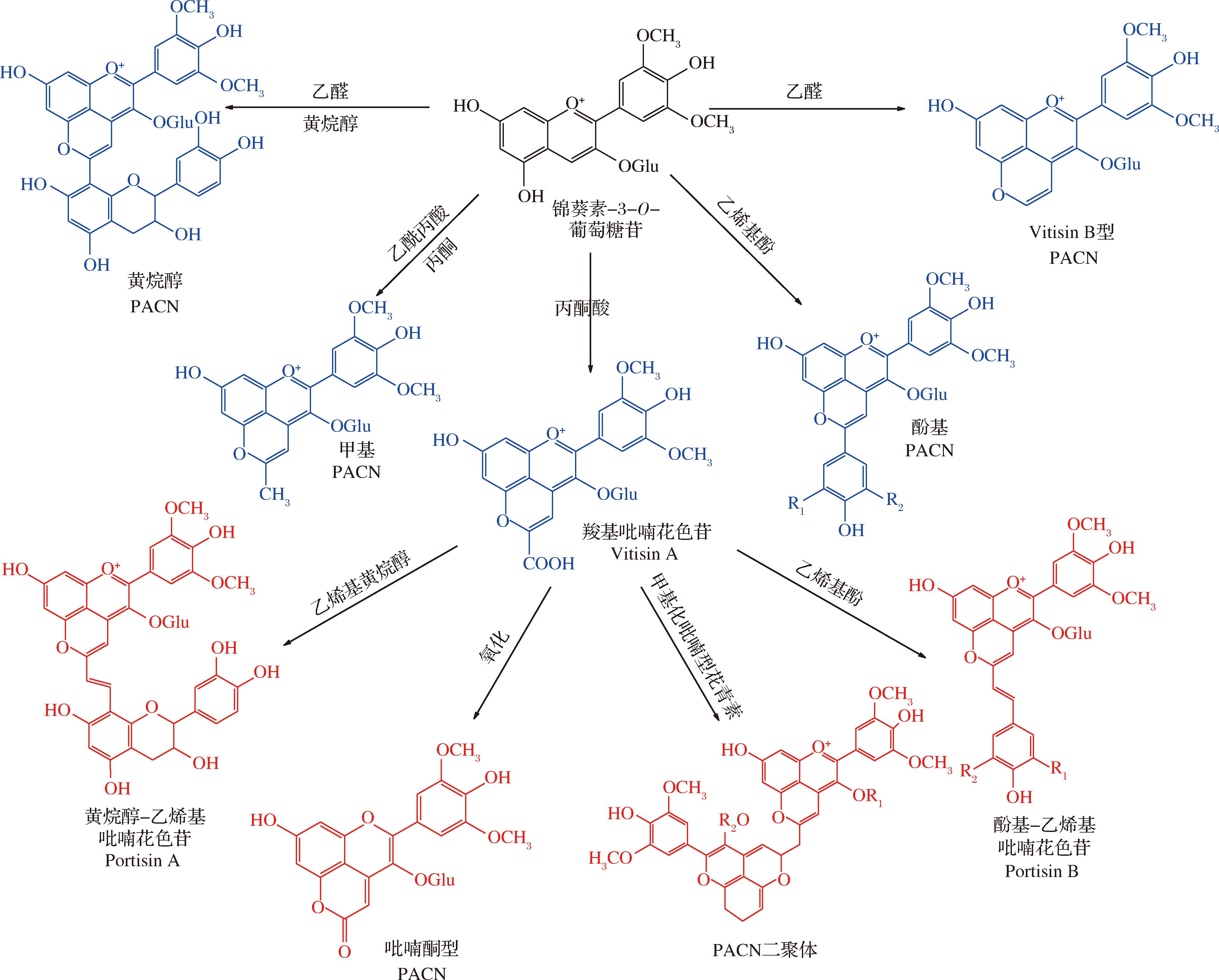
图2 八类PACN形成过程[15]
Fig.2 Formation process of eight types of PACN[15]
1.1 第一代PACN
1.1.1 甲基型与Vitisins型PACN
Vitisins型PACN是最早研究的PACN之一,其中乙醛与单体花色苷反应产物Vitisin B结构最为简单,仅增多了1个吡喃D环[15,17]。Vitisin A比Vitisin B略微复杂,是锦葵素-3-O-葡萄糖苷(Mv-3-glu, M3G)与烯醇化丙酮酸反应,在C4、C5位处形成1个以M3G为核心并附带1个羟基乙烯基和酮基的吡喃环,最早于长时间存放的葡萄皮及陈酿红酒中被发现[18]。而甲基型PACN是在Vitisins型PACN的C10位上多了1个甲基,是花色苷与乙醛乙酸的产物。值得注意的是,甲基型PACN与Vitisins型PACN相比只是C10上多了1个甲基,但在颜色上有明显不同。两者相比单体花色苷均发生了蓝移,但甲基PACN蓝移更加显著,并呈现出更显著的黄色[19]。它们的形成机制类似,以Vitisin A形成机制为例(图3),在酸性环境下羧基可烯醇化,带电负性的甲基与M3G的C4位(正电性)发生加成缩合随后又脱水氧化形成新的吡喃环[15]。此外,OLIVERIA等[20]发现,在水溶液中甲基PACN呈现出4种不同形态结构,未质子化的甲基PACN在碱性条件下会转变为呈黄色的新结构,但该过程不可逆(图4)。
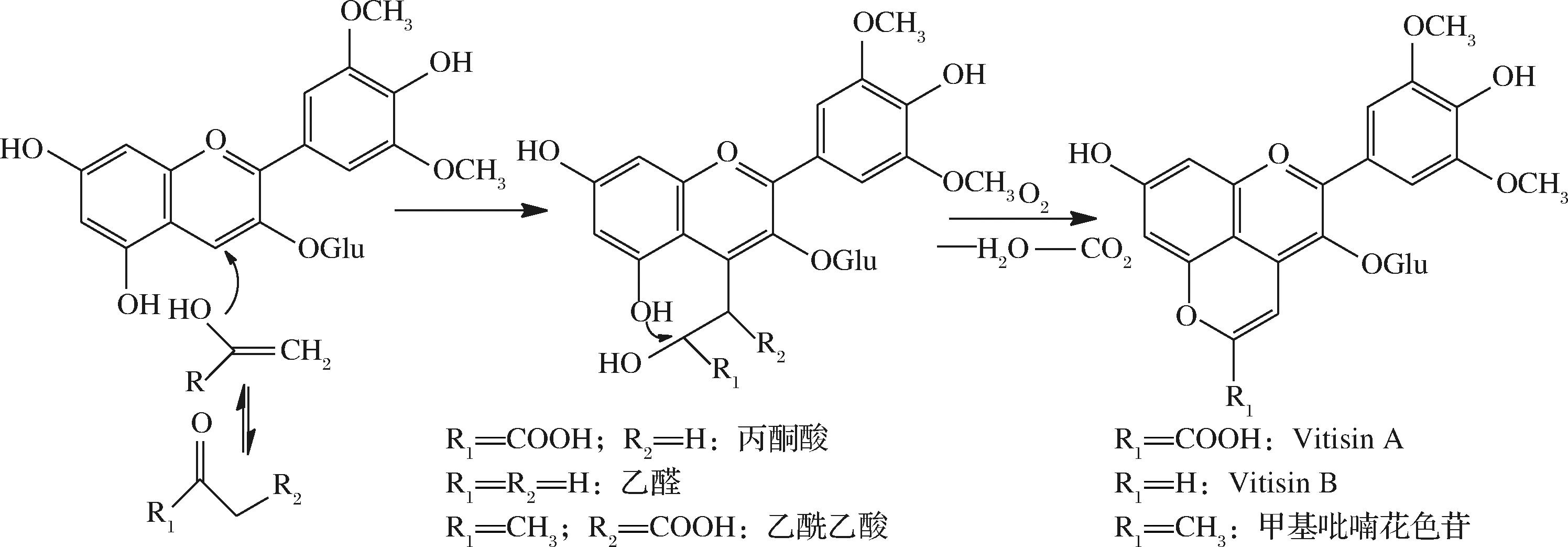
图3 Vitisin A型PACN与甲基型PACN的形成过程[15]
Fig.3 Formation process of Vitisin A-type PACN and methyl PACN[15]
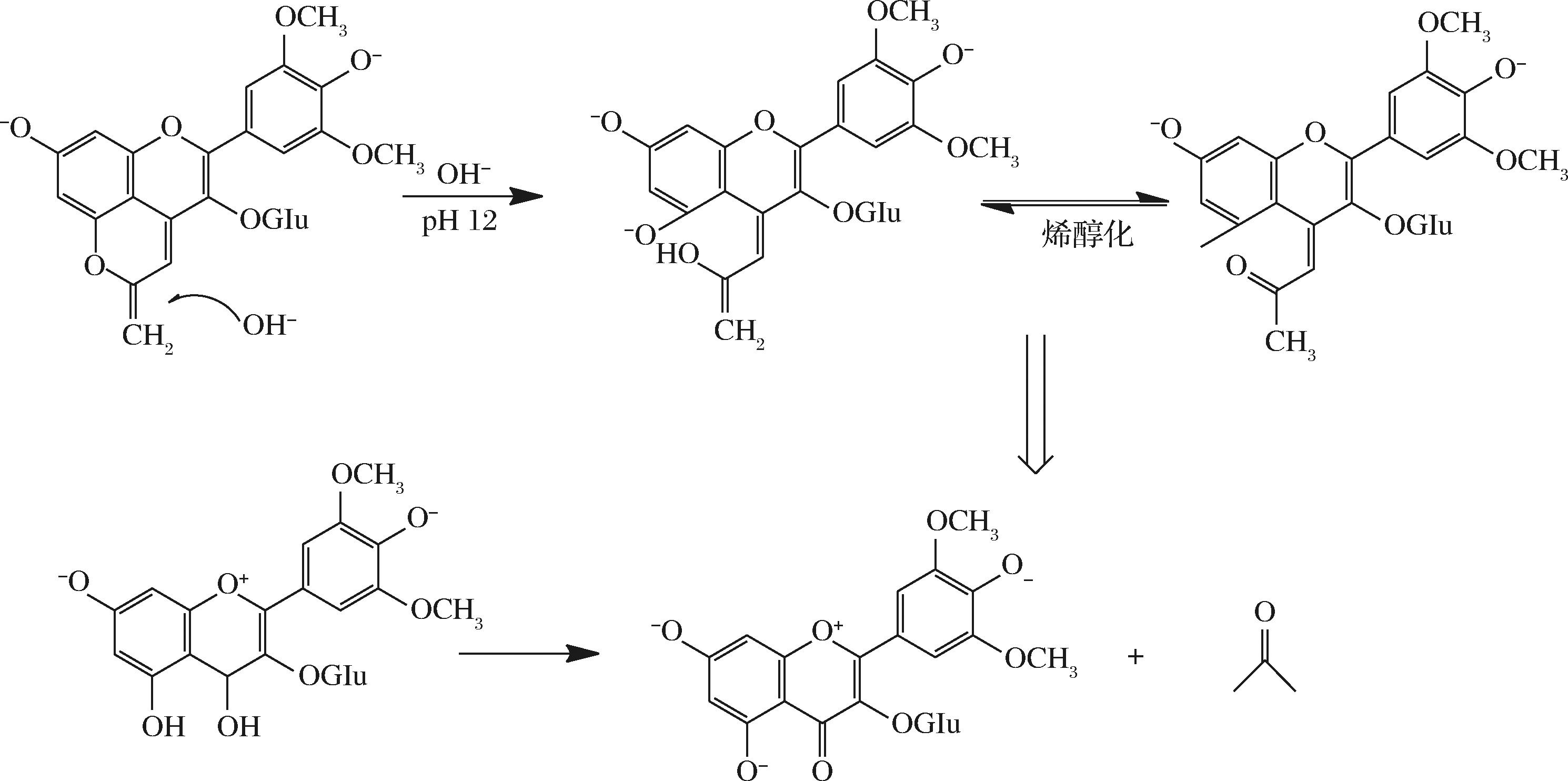
图4 甲基型PACN在碱性条件下结构变化假设[20]
Fig.4 Hypothesis on the structural changes of methyl PACN under alkaline conditions[20]
1.1.2 黄烷醇型PACN
1997年FRANCIA-ARICHA等[21]发现在乙醛介导下的黄烷-3-醇黄烷醇类物质会与M3G反应生成新的物质,并将该物质定义为黄烷醇PACN,它是由花色苷C4、C5位羟基与8-乙烯基黄烷醇的乙烯基之间产生环化加成反应形成(图5)[15]。其中乙烯基黄烷醇型PACN同Vitisins型PACN相似,最大吸收波长也发生了蓝移,呈现为红橙色[15]。HE等[22]探索了不同花色苷的结构特性,发现黄烷醇PACN在强酸至中性条件下都具有很高的颜色强度,尤其在pH值为3.6时达到最高。这种情况的发生可能是因为PACN中的儿茶素的吡喃环与吡喃鎓生色团之间交叠并发生相互作用,结构呈现出封闭“笼型”结构[22]。
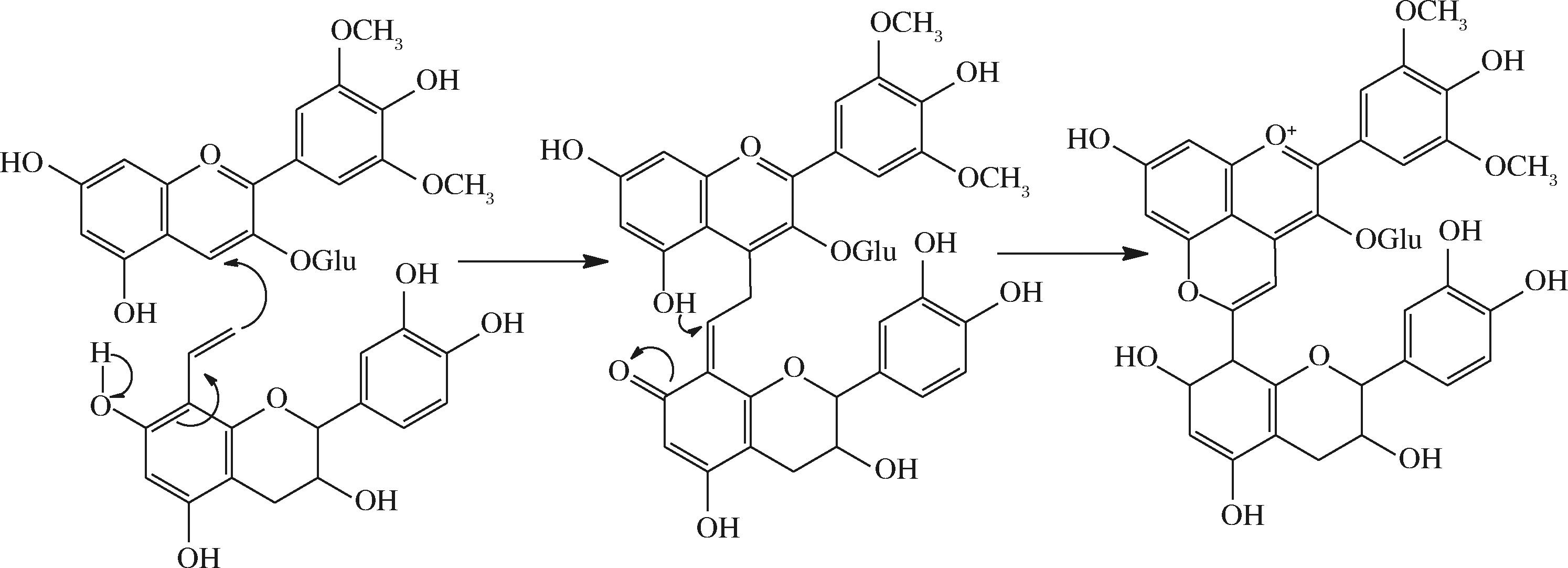
图5 黄烷醇型PACN的形成过程[23]
Fig.5 Formation of flavano-PACN[23]
1.1.3 酚基PACN
学者在葡萄酒研究中发现了一种具有蓝移吸收光谱且呈黄色的色素,经鉴定该物质是3-对香豆酰葡萄糖苷和M3G分别与葡萄酒中非黄烷醇成分缩合形成的酚基PACN(Pinotin),其形成机制为:M3G与乙烯基苯酚(对香豆酸脱羧产物)在花色苷C4和C5位点发生环加成与氧化反应(图6)[24]。研究表明,葡萄酒中的羟基肉桂酸类物质(如阿魏酸、芥子酸、咖啡酸等)可通过脱羧生成4-乙烯基苯酚,进而与单体花色苷发生共价结合形成酚基PACN。在此过程中,酚酸小分子通过分子内辅色、分子间辅色和自缔合等方式对花色苷发挥辅色作用,其形成的超分子结构能干扰水分子对黄烊盐阳离子的亲核攻击,从而有效提升花色苷结构在环境中的相对稳定性[25-26]。此外,研究发现M3G能直接与咖啡酸反应生成新的色素,研究者将生成的PACN命名为Pinotin A。Pinotin A在葡萄酒中的含量不同于其他成分。例如,1~2年内含量较低,但随着时间的延长大部分第一代花色苷逐渐降解,到4~6年后Pinotin A含量会大幅度增加,该现象发生的机理目前尚未有研究说明[27]。
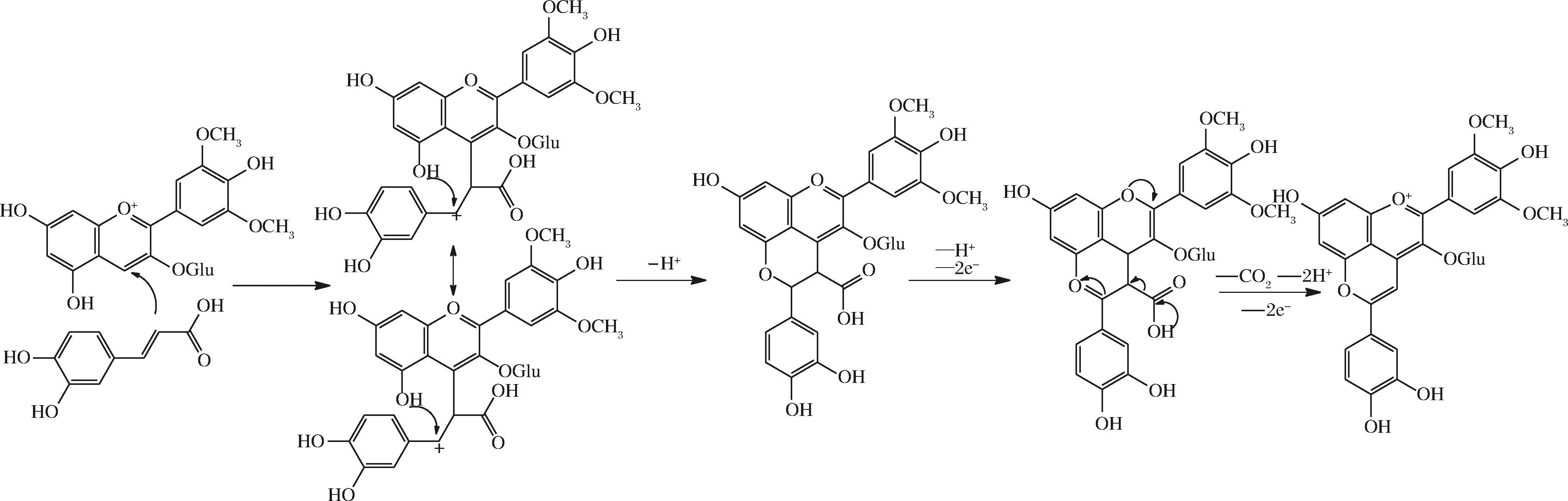
图6 酚基PACN的形成过程[24]
Fig.6 Formation process of hydroxyphenol-PACN[24]
1.2 第二代PACN
1.2.1 Portisins型PACN
2003年Portisins型PACN首次在波特酒中被分离鉴定出来,是由乙烯基苯酚化合物和Vitisin A的C10位发生反应缩合而成[27](图7)。Portisin型PACN是花色苷中重要的一类,其吸收光谱与Vitisins和Pinotin相反。其中,Portisin A的最大吸收光谱高达570 nm,呈现蓝色色调,π电子的拓展共轭会赋予Portisin A更高的稳定性,这可能是其产生独特色调的原因[27-28]。除此之外,研究人员在陈酿的波特酒中发现PACN-乙烯基-羟基肉桂酸类物质(Portisin B),其最大吸收波长红移波长达到540 nm。Portisin B是由羟基肉桂酸的C![]() C对Vitisin A具有亲电性质的C10部位发生亲核攻击,再脱去甲酸氧化形成[28] (图7)。值得注意的是,Portisin B具有独特的颜色特性,具体表现为在-10 ℃其颜色由蓝色转变为红色[29]。由于温度变化会导致其振动能量的改变,具体体现为随温度下降而减小,而低温下结晶排列的有序性会促使水与可溶性羟基的相互作用,进而增强相关的振动频率,因此振动频率的增强能够弥补由于温度下降振动能量的降低,最终在基态能量上表现为增加的趋势,这与颜色的变化趋势相似可能是该颜色发生变化的潜在机制[15]。
C对Vitisin A具有亲电性质的C10部位发生亲核攻击,再脱去甲酸氧化形成[28] (图7)。值得注意的是,Portisin B具有独特的颜色特性,具体表现为在-10 ℃其颜色由蓝色转变为红色[29]。由于温度变化会导致其振动能量的改变,具体体现为随温度下降而减小,而低温下结晶排列的有序性会促使水与可溶性羟基的相互作用,进而增强相关的振动频率,因此振动频率的增强能够弥补由于温度下降振动能量的降低,最终在基态能量上表现为增加的趋势,这与颜色的变化趋势相似可能是该颜色发生变化的潜在机制[15]。
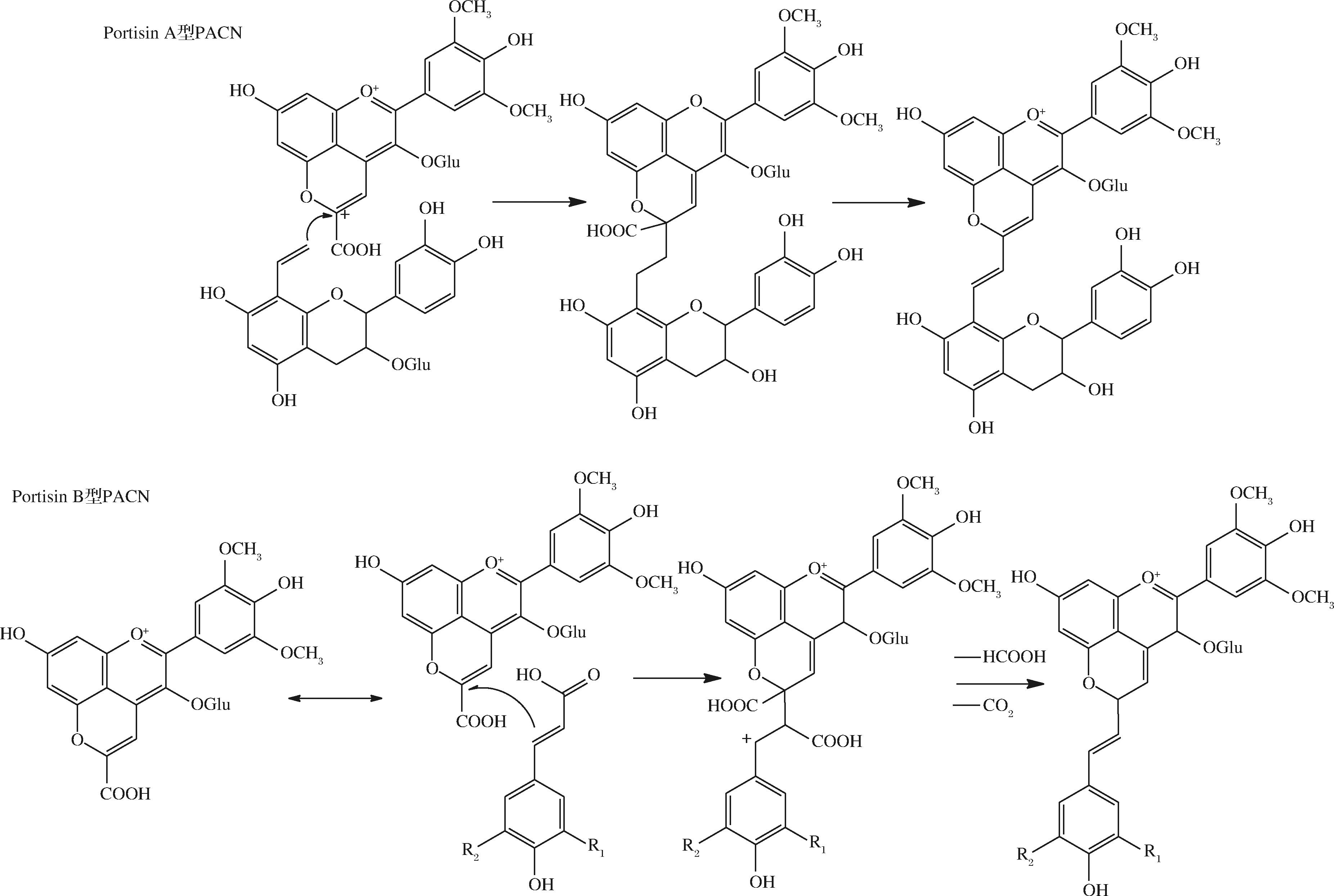
图7 Portisin型花色苷形成过程[28]
Fig.7 Formation process of Portisin-type flavonoid[28]
1.2.2 内酯型(吡喃酮型)PACN
在红酒中还存在其他类型的花色苷衍生物,如内酯型(吡喃酮型)(Oxovitisin)PACN,它是由Vitisin A上具有亲电特性的C10位受到水分子攻击形成半缩醛,随后半缩醛脱羧将羟基氧化成吡喃-2-酮再脱水形成的(图8)[30]。这些物质在红酒中含量很低,结构与Vitisin B相似,是原吡喃环上的一个氢原子被氧原子替换而形成,属于Vitisin A的环氧化产物。例如,HE等[30]在陈酿的波特酒中发现的Oxovitisin,其最大吸收波长仅为373 nm,呈现出橙黄色。
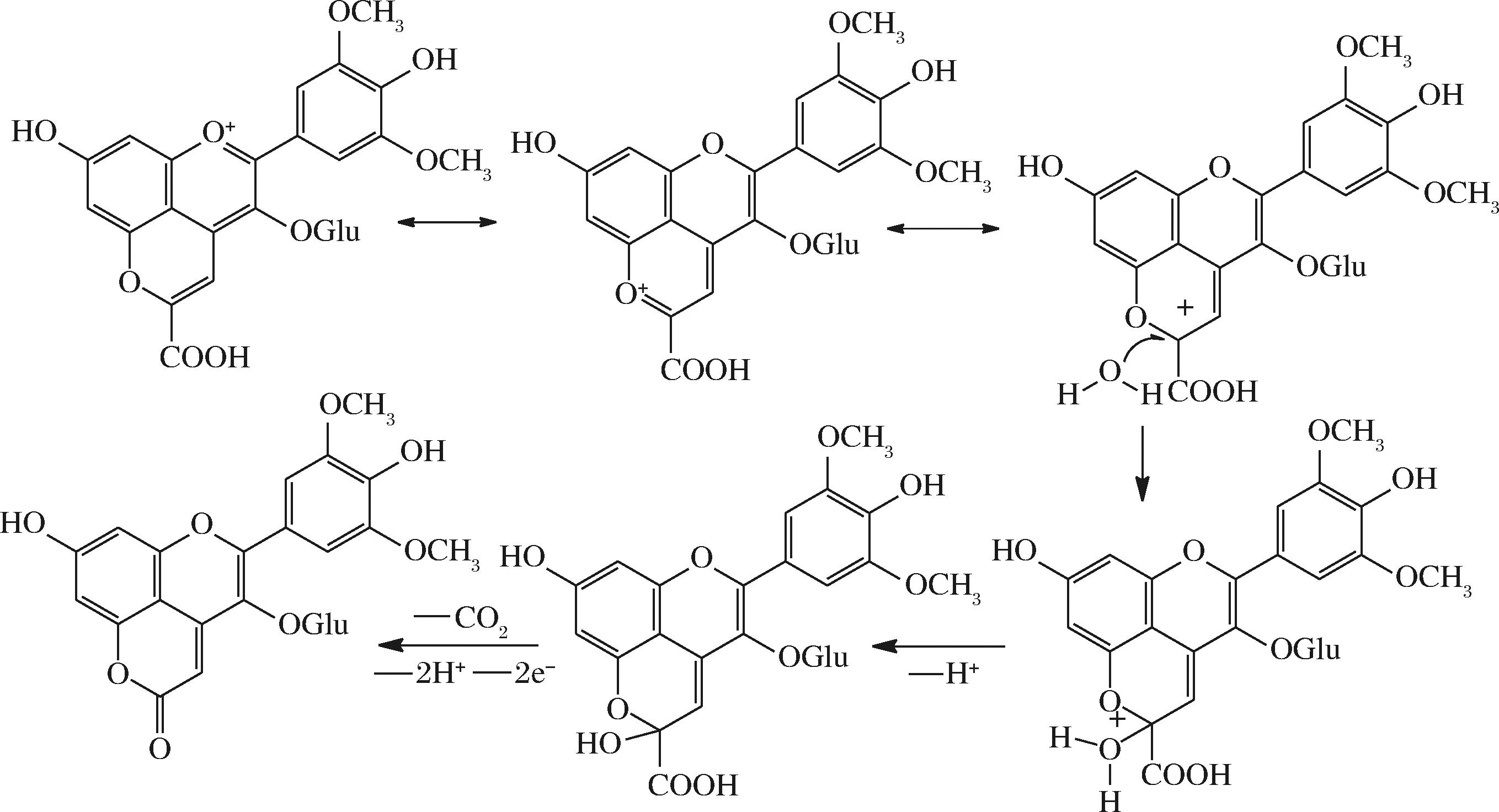
图8 内酯型(吡喃酮型)PACN的形成过程[30]
Fig.8 Formation process of PACN (Oxovitisins)[30]
1.2.3 PACN二聚体
除上述吡喃酮型花色苷外,PACN二聚体也存在于红酒中,但其含量较低,且多数在波特酒及合成模拟溶液中被检测到,在普通葡萄酒或红酒中的相关报道较少。其形成机制存在2种理论解释:其一,甲基PACN的C10位通过甲基去质子化生成亚甲基,该亚甲基借助双键结构对Vitisin A亲电的C10位点发起亲核攻击,形成由亚甲基连接的双PACN中间体,随后经进一步氧化脱去一分子甲酸,最终生成蓝绿色的PACN二聚体(图9)[31];其二,有研究认为PACN二聚体的形成源于2种前体物质通过π电子云相互作用生成电荷转移复合物,再经自由基反应或离子反应缩合脱去甲酸完成聚合[32]。
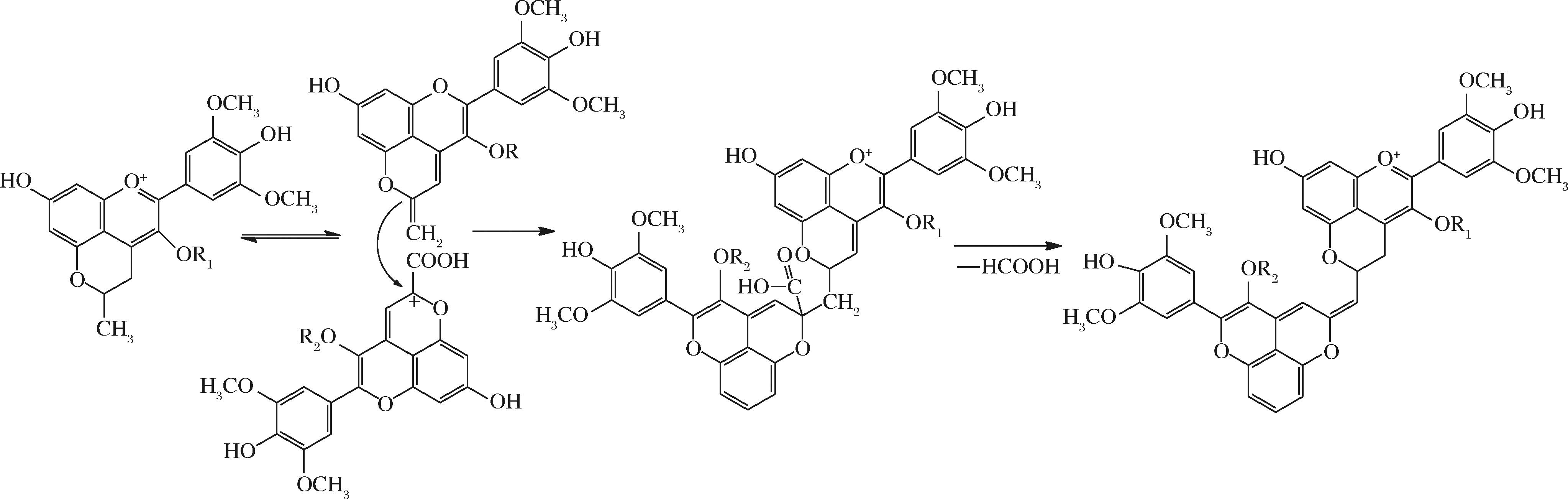
图9 PACN二聚体的形成过程[31]
Fig.9 Formation process of PACN dimers[31]
2 PACN稳定性
受光照、SO2、pH、温度等因素影响,花色苷容易分解,但PACN的吡喃D环能够保护其免受水的亲核攻击,从而表现出对pH、SO2和温度等的更强的抵抗力[13]。因此,探讨不同环境下PACN的变化对PACN的开发应用具有重要意义。
2.1 pH对PACN稳定性的影响
PACN相比单体花色苷具有更强的稳定性。两者颜色对比如表2所示:当pH为1~5时,单体花色苷色度下降80%左右,而PACN几乎没有波动[33]。例如,pH为3.6~4.5时,M3G结构向无色甲醇假碱和查耳酮转变,其颜色由红色逐渐褪至无色。相反,以M3G为前体的6种PACN在相同pH条件下均能保持原来的色泽,并且与pH=1时的色泽强度相差不大,证明PACN的稳定性更好[34]。这可能与其结构中容易被水亲核进攻的C4位点被取代并生成吡喃环有关,避免了其形成无色的半缩醛结构[22]。
表2 PACN与单体花色苷颜色对比[37]
Table 2 Color comparison of PACN and prototypical anthocyanidins[37]
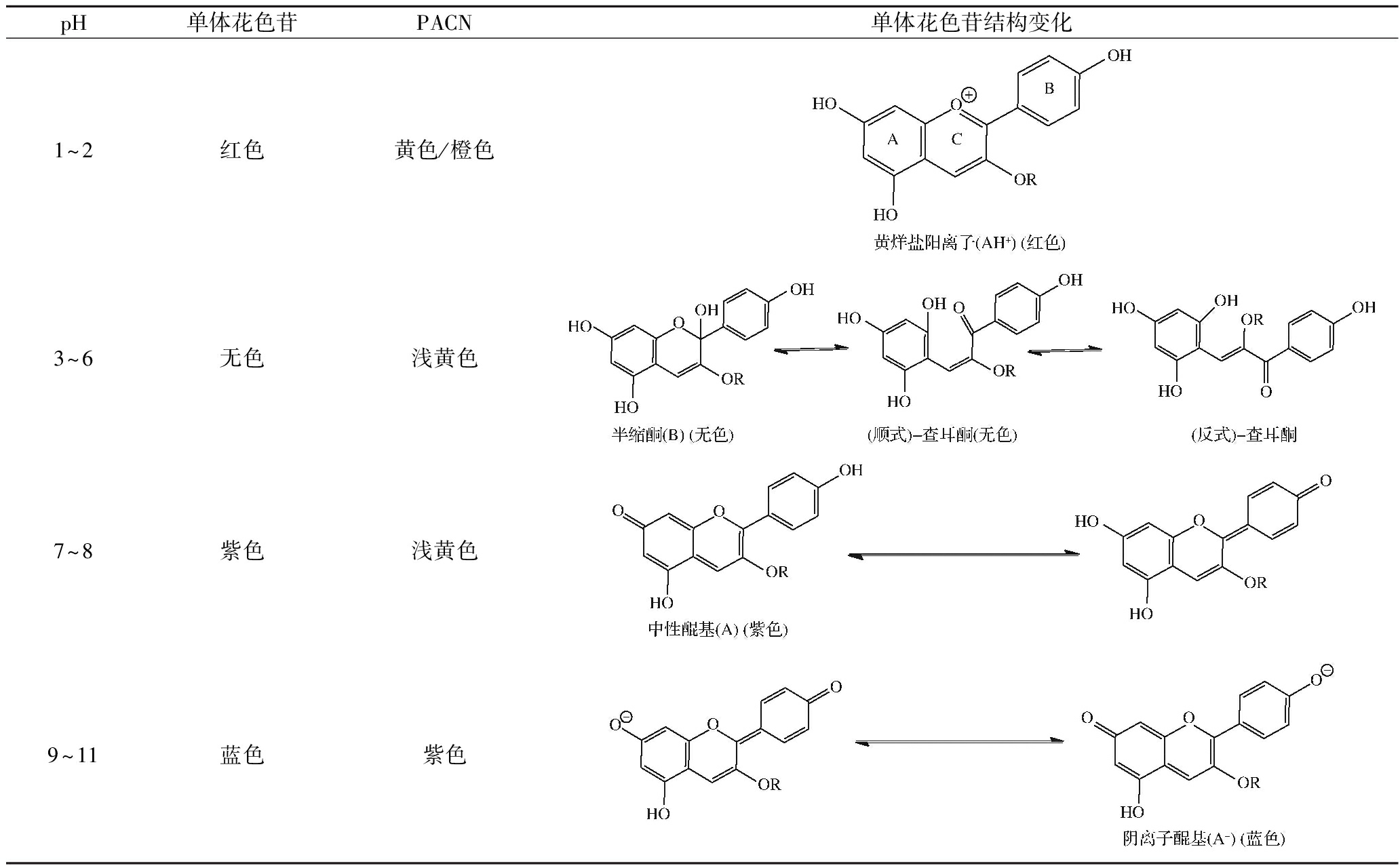
pH单体花色苷PACN单体花色苷结构变化1~2红色黄色/橙色3~6无色浅黄色7~8紫色浅黄色9~11蓝色紫色
此外,单体花色苷随pH的变化会呈现出“红色-无色-紫色-蓝色”的变化,其原因是花色苷不稳定(如上文所述)易受pH影响,从而导致花色苷结构发生转变。但PACN的色泽在不同pH条件下变化较小。例如,SUN等[34]研究了香豆酸、丙酮、丙酮酸、咖啡酸、芥子酸、阿魏酸与M3G合成的6种PACN,发现它们在较高的pH下均表现出较好的pH耐受性和稳定性。邝敏杰[35]研究发现Vitisins 型吡喃型在酸性至中性pH范围内的颜色较为稳定,而甲基型PACN在pH 1.0~7.0内颜色变化较小,该结果说明PACN能够提高花色苷对pH的耐受能力。随着pH的升高,PACN颜色也会发生改变,如在中性条件下原本橙红色的Vitisin A会逐渐转变为红色色调[35]。这是因为随着pH的不断升高,其结构中C4′和C7位点羟基中的质子会发生转移,促使溶液中出现醌式双阴离子碱和醌式阴离子碱结构的花色苷,从而使颜色发生变化[36]。
2.2 SO2对PACN稳定性的影响
PACN等衍生物质的生成,受到了发酵体系、花色苷、SO2、丙酮酸浓度等的影响。关于SO2的影响,BAKKER等[38]研究发现,Vitisins型PACN衍生物比单体花色苷具有更强的抵抗SO2漂白的作用。而HE等[22]也得出类似结果,他们对pH、贮存时间及SO2对黄烷醇-PACN稳定性的影响展开了详细研究,发现在pH值不变的情况下,黄烷醇-PACN的稳定性远高于单体花色苷,并且表现出对SO2较好的抵抗作用。其原因是PACN具有很强的抵抗水和酸性亚硫酸盐亲核攻击的能力[15]。这说明PACN的确能够提高花色苷稳定性,并且这种能力随着发酵时间的延长而更加明显。
2.3 温度对PACN稳定性的影响
除上述影响因素外,温度对PACN的形成同样至关重要:其不仅会影响花色苷的稳定性,还对花色苷的色泽与含量产生显著作用。例如,VOSS等[39]研究了3种10-儿茶酚基型PACN与对应单体花色苷在稳定性上的差异,结果发现在90 ℃下加热4.5 h后,单体花色苷吸光度值下降了64%,色度下降超过30%,而3种PACN的最大吸光度值仅下降10%,且其色度仅下降5%。此外,有研究发现Portisin B从低温条件转移至室温条件下时,其颜色会发生红移[28]。上述结果说明PACN相较于单体花色苷具有更好的稳定性。除颜色变化外,研究人员还发现PACN的含量会随温度波动而改变。例如,Vitisins型PACN的含量随温度升高呈先增后降的趋势:当温度升至27 ℃时含量达到峰值,超过该温度后则逐渐下降[40]。这可能是因为随着发酵温度的升高,丙酮酸和乙醛的含量增多,从而促使PACN含量升高。当温度进一步升高时,PACN的前体反应物二甲花翠素-3-O-葡萄糖苷发生降解,从而导致其含量降低[40]。值得注意的是,有研究结果显示M3G、矢车菊素-3-O-葡萄糖苷(cyanidin-3-O-glucoside,C3G)和芍药素-3-O-葡萄糖苷3种花色苷形成的苯酚PACN热稳定性均高于单体花色苷,说明吡喃结构是花色苷热稳定性提高的原因,而不是由于单体花色苷不同[39]。因此,PACN具有巨大的应用潜能。
2.4 光照对PACN稳定性的影响
光照会促使单体花色苷降解为2,4,6-三羟基苯甲醛和苯甲酸等产物[41]。然而,研究人员测定了光照条件下PACN和单体花色苷的颜色、抗SO2能力、稳定性及基本花色苷含量,结果发现PACN在光照下其稳定性、色度、抗SO2能力及基本花色苷含量均优于单体花色苷,且避光处理优于光照处理,表明PACN能提高花色苷稳定性[2]。其原因可能是PACN中吡喃D环的形成导致结构更加稳定不易受到胁迫。
3 PACN功能活性
3.1 抗氧化活性
由于单体花色苷结构不稳定且易分解,而PACN中新形成的D环结构可通过保护花色苷骨架免受水的亲核攻击,从而显著提升其稳定性;且通过多种检测方法证实,PACN的生物活性也随之发生改变(表3)。前期研究证实,PACN的抗氧化活性显著优于单体花色苷。例如,以M3G为原型衍生的6种PACN抗氧化能力均强于M3G,其中,Poinotin A的抗氧化活性表现最为突出[33]。此外,罗海霞[42]通过合成Pinotin A、Vitisin A、甲基 PACN、Mv-3-glu-4-乙烯基愈创木酚、Mv-3-glu-4-乙烯基丁香醇和 Mv-3-glu-4-乙烯基苯酚6种PACN,对比其与M3G的抗氧化活性,结果显示,PACN对ABTS阳离子自由基的清除能力显著更强,抗氧化效果更为优异。此外,甲基PACN对DPPH自由基和羟自由基的清除能力随浓度升高而增强,均表现出良好的抗氧化潜力[34]。但并非所有PACN的抗氧化都强于单体花色苷,例如研究人员将吡喃酮型花色苷衍生物(Oxovitisin A)与前体羧基PACN(Vitisin A)、M3G及甲基PACN进行DPPH、ABTS阳离子自由基清除实验和铁氧还原力(ferric reducing antioxidant power,FRAP)测试,实验结果显示:M3G的自由基清除能力最强,Vitisin A次之,而Oxovitisin A的抗氧化活性最差[43]。
表3 不同PACN的功能活性测定方法[47]
Table 3 Functional activity assay of different PACNs[47]
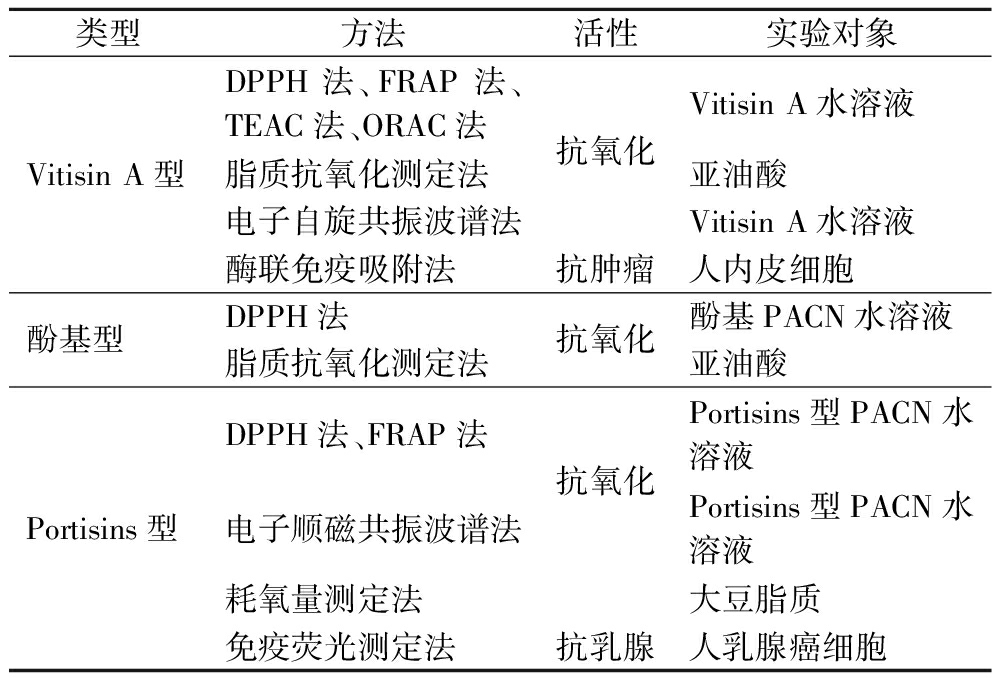
类型方法活性实验对象Vitisin A型DPPH法、FRAP法、TEAC法、ORAC法脂质抗氧化测定法电子自旋共振波谱法酶联免疫吸附法抗氧化抗肿瘤Vitisin A水溶液亚油酸Vitisin A水溶液人内皮细胞酚基型DPPH法脂质抗氧化测定法抗氧化酚基PACN水溶液亚油酸Portisins型DPPH法、FRAP法电子顺磁共振波谱法耗氧量测定法免疫荧光测定法抗氧化抗乳腺Portisins型PACN水溶液Portisins型PACN水溶液大豆脂质人乳腺癌细胞
注:ORAC法-氧化自由基吸收能力测定法;TEAC法-Trolox当量抗氧化能力。
另一方面,PACN因结构变化导致其抗氧化能力与酰基化花色苷存在差异。例如,酰基化花色苷与天然单体花色苷清除DPPH自由基的半抑制浓度(half inhibitory concentration, IC50)值分别为4.451 μg/mL和22.919 μg/mL,而PACN类物质中Vitisin A与Oxovitisin A的IC50值分别为25.925 μg/mL和56.808 μg/mL,表明PACN虽具备一定抗氧化能力,但酰基化花色苷对DPPH自由基的清除效果更优[44]。此外,ABTS阳离子自由基清除实验的结果与上述结论相似,进一步证实酰基化花色苷的抗氧化活性强于PACN[43-44]。花色苷对自由基的清除能力主要与其共轭结构和羟基数目有关,尤其是A环上C5位、C7位和B环上C3′、C4′、C5′位的羟基[45-46]。PACN对DDPH等自由基清除能力较弱主要原因是其结构上链接的羟基数量较少,导致其给电子能力较差。
与之相反,在清除超氧阴离子和H2O2时,Oxovitisin A与Vitisin A表现出更优的效果,这是由于多酚类物质通过酚羟基解离出氢离子,与活性氧自由基结合转化为稳定分子结构所致[43]。此外,Oxovitisin A的分子结构特征进一步强化了其抗氧化能力:1)B环C4、C3位的甲氧基与A、C、D环形成平衡结构;2)B环通过C环C3、C2位的共轭双键与Oxovitisin A主体平面共轭,扩大了分子的共轭体系,促进电子离域并稳定反应中间体;3)吡喃环与非氧鎓离子结构的存在,共同赋予其更高的抗氧化活性[43]。此外,红酒中部分PACN是经由酰基化而形成的,其结构较酰基化花色苷更为复杂,稳定性也较酰基化花色苷更好,因此具有更高的抗氧化能力。
3.2 抗癌作用
前期研究显示,Oxovitisin A在抗乳腺癌细胞(MCF-7)实验中表现出显著优于单体花色苷M3G的抑制效果,这可能与PACN环上的取代基促进物质吸收转运有关[43]。进一步研究还发现,PACN的D环取代基类型与其功能活性存在明确相关性,活性强弱顺序为羰基>羧基>甲基;其中,Oxovitisin A因在胃壁具有最快的转运吸收速率,可更快发挥生物活性[43]。上述结果除母环上链接的糖苷和B环上取代基对PACN的吸收转运有关外,PACN的吡喃D环及其上链接的取代基以及Oxovitisin A本身的非氧鎓离子结构对其也有影响[43]。此外,当pH为3~9时,蓝莓中的甲基PACN也能有效抑制宫颈癌HeLa细胞增殖活性,并且能够激活p38 MAPK/p53信号通路以抑制HeLa细胞增殖[48]。尽管癌症治疗仍面临诸多挑战,安全高效治疗药物的研发需持续探索,但PACN因兼具明确的抗癌功效与安全的来源特性,在抗癌药物开发领域展现出巨大潜力。
3.3 抗炎作用
除抗氧化和抗癌作用外,PACN还具有较好的抗炎作用。前期研究显示,从鹿角中分离得到的酚基PACN能够显著降低H2O2/TNF-α在结肠癌细胞Caco-2中诱导的炎症因子水平,其机理为通过促进核因子抑制蛋白磷酸化进一步抑制核因子κB(nuclear factor kappa-B,NF-κB)活化实现的[49]。此外,Vitisin A能够通过降低C3在库普弗细胞(Kupffer cells)的C3a受体1(complement C3a receptor1,C3AR1)、炎症因子和TNF-α的mRNA水平来缓解酒精性肝病[50]。因此,PACN对炎症缓解也具有一定作用,在炎症药物开发上具有广泛前景。
3.4 其他作用
PACN除已证实的抗氧化与抗癌活性外,还展现出多种其他生物功能:其对H2O2诱导的细胞损伤具有显著保护作用,并具备抑制病菌繁殖的活性[34,51]。此外,在小鼠模型及HepG2细胞实验中发现,Vitisin A可通过抑制肝脏甘油三酯合成并促进β氧化,有效稳定小鼠体内甘油三酯水平,且其降甘油三酯能力显著优于C3G[52]。综上所述,PACN在抗癌、抗炎、抗乳腺癌等方面均有一定成效,在医疗领域具有可观的应用前景。
4 PACN的应用
作为天然植物色素,PACN在安全性、环保性及健康属性上具有不可比拟的优势。其高稳定性、丰富色泽及多样功能活性,使其在医疗保健、食品工业、化妆品及光伏材料等领域展现出显著应用价值:
1)在食品与酒类开发中,由于PACN在红酒中含量丰富,其应用已延伸至果酒与果醋领域。例如,白卫滨[53]证实,通过促进甲基PACN衍生化可有效维持酒体色泽稳定性;此外,基于PACN开发的功能性食品,如蓝莓-桑葚花色苷复合胶囊等微胶囊产品,已实现抗衰老、美容护眼等保健功能[54]。
2)在材料科学领域,PACN在光伏染料行业的应用值得关注。研究人员通过理论模拟与实验表征发现,PACN类染料敏化电池的光电转化效率可达1.79%,其吡喃D环与C环的共轭结构可增强电子离域效应,不仅提升开路电压,还能通过抑制C2位水亲核攻击拓展可见光吸收范围[55-56]。
3)在功能性成分开发中,OLIVEIRA等[57]通过Vitisin A与肉桂酸反应合成了蓝色PACN(类似 Portisin B型),为色素分子设计提供了新思路。目前,PACN相关产品已涵盖医疗、食品、光伏等多个领域,其兼具天然属性与功能优势的特性,证实了在多行业场景中的广阔应用前景。
5 总结与展望
PACN作为一类特殊的多酚类化合物,最早被发现于陈酿果酒中,是一类在果酒发酵过程中形成的新型花色苷衍生物。发酵体系中的温度、pH值及SO2含量等因素均会影响PACN的生成。尽管其在发酵体系中含量较低,但其独特的家族结构和光谱特性使其成为陈酿果酒的主要呈色物质,对红酒的口感与色泽起着关键性作用。
相比单体花色苷,PACN因结构特点具备更高的稳定性、更丰富的颜色表现及更强的功能活性,在保健品、功能性食品及染色剂等领域展现出重要的探索价值。然而,目前针对PACN的动物体内实验较为匮乏,其吸收代谢途径等生理活性机制仍有待深入研究。期待随着研究的推进,PACN能为天然抗氧化剂和天然色素的开发应用提供更多可能性。
[1] 周萍, 郑洁.花色苷改性及应用研究进展[J].食品科学, 2021, 42(3):346-354.
ZHOU P, ZHENG J.Modification of anthocyanins for extended application:A review[J].Food Science, 2021, 42(3):346-354.
[2] 胡苑. 干红葡萄酒陈酿衍生色素颜色稳定性的研究[D].烟台:烟台大学, 2021.
HU Y.Study on color stability of pigment derived from dry red wine aging[D].Yantai:Yantai University, 2021.
[3] 高琛瑜. 赤霞珠干红葡萄酒色泽品质提升工艺优化及模型构建[D].乌鲁木齐:新疆农业大学, 2024.
GAO C Y.Optimization of color quality enhancement process and model construction of Cabernet Sauvignon dry redwine[D].Urumqi:Xinjiang Agricultural University, 2024.
[4] 张铭. 新型黑米酒酿造工艺优化及品质分析[D].武汉:华中农业大学, 2022.
ZHANG M.The brewing process optimization and quality analysis of new black rice wine[D].Wuhan:Huazhong Agricultural University, 2022.
[5] ZHANG X K, LI S Y, ZHAO X, et al.HPLC-MS/MS-based targeted metabolomic method for profiling of malvidin derivatives in dry red wines[J].Food Research International, 2020, 134:109226.
[6] WIMALASIRI P M, HARRISON R, OLEJAR K J, et al.Colour characterisation of two-year-old Pinot noir wines by UV-Vis spectrophotometry and tristimulus colourimetry (CIELab):Effect of whole bunch or grape stems addition[J].International Journal of Food Science &Technology, 2023, 58(3):1176-1185.
[7] NUNES A N, IVASIV V, GOUVEIA L F, et al.Isolation of bluish anthocyanin-derived pigments obtained from blueberry surplus using centrifugal partition chromatography[J].Journal of Chromatography A, 2023, 1705:464150.
[8] ZHU X Y, GIUSTI M M.Pyranoanthocyanin formation rates and yields as affected by cyanidin-3-substitutions and pyruvic or caffeic acids[J].Food Chemistry, 2021, 345:128776.
[9] 张萍玲. 矢车菊素-3-O-葡萄糖苷酰基化修饰及其活性研究[D].广州:华南理工大学, 2020.
ZHANG P L.Enzymatic acylation of cyanidin-3-O-glucoside and its activity research[D].Guangzhou:South China University of Technology, 2020.
[10] WU T, ZHU W Y, CHEN L Y, et al.A review of natural plant extracts in beverages:Extraction process, nutritional function, and safety evaluation[J].Food Research International, 2023, 172:113185.
[11] ENARU B, DRE CANU G, POP T D, et al.Anthocyanins:Factors affecting their stability and degradation[J].Antioxidants, 2021, 10(12):1967.
CANU G, POP T D, et al.Anthocyanins:Factors affecting their stability and degradation[J].Antioxidants, 2021, 10(12):1967.
[12] YUAN Y W, TIAN Y L, GAO S, et al.Effects of environmental factors and fermentation on red raspberry anthocyanins stability[J].LWT, 2023, 173:114252.
[13] GUO C, LI Y, ZHANG H, et al.A review on improving the sensitivity and color stability of naturally sourced pH-sensitive indicator films[J].Comprehensive Reviews in Food Science and Food Safety, 2024, 23(4):e13390.
[14] 滕昭军. 酵母与丙酮酸对果酒发酵过程中色泽变化和呈色机制研究[D].广州:暨南大学, 2021.
TENG Z J.Study on the color change and coloration mechanism by yeast and pyruvic acid during the wine fermentation[D].Guangzhou:Jinan University, 2021.
[15] 曾颖钰, 郭大三, 李旭升, 等.吡喃花色苷结构及其性质研究进展[J].食品科学, 2022, 43(13):199-209.
ZENG Y Y, GUO D S, LI X S, et al.Progress in research on the structure and properties of pyranoanthocyanins[J].Food Science, 2022, 43(13):199-209.
[16] ZIA UL HAQ M, RIAZ M, SAAD B.Anthocyanins and Human Health:Biomolecular and therapeutic aspects[M].Cham:Springer International Publishing, 2016.
[17] 刘馨阳. 酵母破壁技术对强化甜红葡萄酒品质的影响[D].杨凌:西北农林科技大学, 2024.
LIU X Y.Effect of yeast wall breaking technique on the quality of fortified sweet wine[D].Yangling:Northwest A&F University, 2024.
[18] BAKKER J, BRIDLE P, HONDA T, et al.Identification of an anthocyanin occurring in some red wines[J].Phytochemistry, 1997, 44(7):1375-1382.
[19] OLIVEIRA J, DE FREITAS V, MATEUS N.A novel synthetic pathway to vitis in B compounds[J].Tetrahedron Letters, 2009, 50(27):3933-3935.
[20] OLIVEIRA J, PETROV V, PAROLA A J, et al.Chemical behavior of methylpyranomalvidin-3-O-glucoside in aqueous solution studied by NMR and UV-visible spectroscopy[J].The Journal of Physical Chemistry.B, 2011, 115(6):1538-1545.
[21] FRANCIA-ARICHA E M, GUERRA M T, RIVAS-GONZALO J C, et al.New anthocyanin pigments formed after condensation with flavanols[J].Journal of Agricultural and Food Chemistry, 1997, 45(6):2262-2266.
[22] HE J R, CARVALHO A R F, MATEUS N, et al.Spectral features and stability of oligomeric pyranoanthocyanin-flavanol pigments isolated from red wines[J].Journal of Agricultural and Food Chemistry, 2010, 58(16):9249-9258.
[23] CRUZ L, TEIXEIRA N, SILVA A M S, et al.Role of vinylcatechin in the formation of pyranomalvidin-3-glucoside-+-catechin[J].Journal of Agricultural and Food Chemistry, 2008, 56(22):10980-10987.
[24] CAMEIRA-DOS-SANTOS P J, BRILLOUET J M, CHEYNIER V, et al.Detection and partial characterisation of new anthocyanin derived pigments in wine[J].Journal of the Science of Food and Agriculture, 1996, 70(2):204-208.
[25] 江玉婷, 秦昉, 陈洁, 等.天然花色苷色素稳定化研究进展[J].食品与机械, 2019, 35(5):213-218;236.
JIANG Y T, QIN F, CHEN J, et al.Research progress on stabilization of natural anthocyanin pigments[J].Food &Machinery, 2019, 35(5):213-218;236.
[26] 慕妮, 吴海浩, 顾颖娟, 等.咖啡酸对紫玉米花色苷的辅色作用研究[J].食品科学, 2010, 31(5):58-62.
MU N, WU H H, GU Y J, et al.Color enhancing effect caffeic acid on purple corn anthocyanins[J].Food Science, 2010, 31(5):58-62.
[27] MATEUS N, OLIVEIRA J, SANTOS-BUELGA C, et al.NMR structure characterization of a new vinylpyranoanthocyanin-catechin pigment (a portisin)[J].Tetrahedron Letters, 2004, 45(17):3455-3457.
[28] MATEUS N, SILVA A M S, RIVAS-GONZALO J C, et al.A new class of blue anthocyanin-derived pigments isolated from red wines[J].Journal of Agricultural and Food Chemistry, 2003, 51(7):1919-1923.
[29] CARVALHO A R F, OLIVEIRA J, DE FREITAS V, et al.Unusual color change of vinylpyranoanthocyanin—phenolic pigments[J].Journal of Agricultural and Food Chemistry, 2010, 58(7):4292-4297.
[30] HE J R, OLIVEIRA J, SILVA A M S, et al.Oxovitisins:A new class of neutral pyranone-anthocyanin derivatives in red wines[J].Journal of Agricultural and Food Chemistry, 2010, 58(15):8814-8819.
[31] DE FREITAS V, MATEUS N.Formation of pyranoanthocyanins in red wines:A new and diverse class of anthocyanin derivatives[J].Analytical and Bioanalytical Chemistry, 2011, 401(5):1463-1473.
[32] 何静仁, 邝敏杰, 齐敏玉, 等.吡喃花色苷类衍生物家族的研究进展[J].食品科学, 2015, 36(7):228-234.
HE J R, KUANG M J, QI M Y, et al.Recent progress in research on pyranoanthocyanins derivatives[J].Food Science, 2015, 36(7):228-234.
[33] DE FREITAS V, MATEUS N.Chemical transformations of anthocyanins yielding a variety of colours (Review)[J].Environmental Chemistry Letters, 2006, 4(3):175-183.
[34] SUN J X, LI X H, LUO H X, et al.Comparative study on the stability and antioxidant activity of six pyranoanthocyanins based on malvidin-3-glucoside[J].Journal of Agricultural and Food Chemistry, 2020, 68(9):2783-2794.
[35] 邝敏杰. 甲基吡喃花色苷的制备及功能性质研究[D].武汉:武汉轻工大学, 2014.
KUANG M J.Study on preparation and functional properties of methyl pyranoanthocyanin[D].Wuhan:Wuhan Polytechnic University, 2014.
[36] YAN Y Z, NISAR T, FANG Z X, et al.Current developments on chemical compositions, biosynthesis, color properties and health benefits of black goji anthocyanins:An updated review[J].Horticulturae, 2022, 8(11):1033.
[37] 夏玲, 陈小兰, 王自超, 等.酰基化花色苷的结构、稳定性及降血糖作用研究进展[J].食品与发酵工业, 2025, 51(15):374-383.
XIA L, CHEN X L, WANG Z C, et al.Progress in the study of structure, stability and hypoglycemic effect of acylated anthocyanins[J].Food and Fermentation Industries, 2025, 51(15):374-383.
[38] BAKKER J, TIMBERLAKE C F.Isolation, identification, and characterization of new color-stable anthocyanins occurring in some red wines[J].Journal of Agricultural and Food Chemistry, 1997, 45(1):35-43.
[39] VOSS D M, MIYAGUSUKU-CRUZADO G, GIUSTI M M.Thermal stability comparison between 10-catechyl-pyranoanthocyanins and anthocyanins derived from pelargonidin, cyanidin, and malvidin[J].Food Chemistry, 2023, 403:134305.
[40] 何英霞, 李霁昕, 米兰, 等.响应面分析pH值、温度、SO2对干红葡萄酒中吡喃花色苷Vitisins的影响[J].食品与发酵工业, 2016, 42(8):115-120.
HE Y X, LI J X, MI L, et al.Effects of pH, temperature and SO2 on pyranoanthocyanins(Vitisins) in red wine by response surface methodology[J].Food and Fermentation Industries, 2016, 42(8):115-120.
[41] 陈健初. 杨梅汁花色苷稳定性、澄清技术及抗氧化特性研究[D].杭州:浙江大学, 2005.
CHEN J C.Stability of anthocyanin, clarification and antioxidant activity of Yangmei juice[D].Hangzhou:Zhejiang University, 2005.
[42] 罗海霞. 吡喃花色苷的合成及其稳定性与抗氧化活性研究[D].广州:广东工业大学, 2017.
LUO H X.Synthesis, stability and antioxidant activity of pyranosides[D].Guangzhou:Guangdong University of Technology, 2017.
[43] 吴闹. 新型花色苷衍生物Oxovitisin的理化性质及生物活性研究[D].武汉:武汉轻工大学, 2016.
WU N.Physicochemical property and biological activityof new anthocyanin derivative Oxovitisin[D].Wuhan:Wuhan Light Industry University, 2016.
[44] 李锦红. 超声辅助低共熔溶剂提取玫瑰花色苷及其抗氧化性和稳定性研究[D].天津:天津科技大学, 2022.
LI J H.Ultrasound-assisted low eutectic solvent extraction of rose anthocyanin and its antioxidant properties and stability[D].Tianjin:Tianjin University of Science and Technology, 2022.
[45] DUDEK A, SPIEGEL M, STRUGA A-DANAK P, et al.Analytical and theoretical studies of antioxidant properties of chosen anthocyanins;a structure-dependent relationships[J].International Journal of Molecular Sciences, 2022, 23(10):5432.
A-DANAK P, et al.Analytical and theoretical studies of antioxidant properties of chosen anthocyanins;a structure-dependent relationships[J].International Journal of Molecular Sciences, 2022, 23(10):5432.
[46] FRANCAVILLA A, JOYE I J.Anthocyanins in whole grain cereals and their potential effect on health[J].Nutrients, 2020, 12(10):2922.
[47] 由璐, 隋茜茜, 赵艳雪, 等.花色苷分子结构修饰及其生理活性研究进展[J].食品科学, 2019, 40(11):351-359.
YOU L, SUI Q Q, ZHAO Y X, et al.Recent progress in structural modification and physiological activity of anthocyanins[J].Food Science, 2019, 40(11):351-359.
[48] PAN F G, LIU Y J, LIU J B, et al.Stability of blueberry anthocyanin, anthocyanidin and pyranoanthocyanidin pigments and their inhibitory effects and mechanisms in human cervical cancer HeLa cells[J].RSC Advances, 2019, 9(19):10842-10853.
[49] PENG Y, ZHANG H, LIU R H, et al.Antioxidant and anti-inflammatory activities of pyranoanthocyanins and other polyphenols from staghorn sumac (Rhus hirta L.) in Caco-2 cell models[J].Journal of Functional Foods, 2016, 20:139-147.
[50] 朱远琴. 吡喃花色苷Vitisin A对酒精性肝病的干预作用及机制研究[D].广州:暨南大学, 2023.
ZHU Y Q.Regulatory effect and mechanism of pyranoanthocyanins Vitisin A on alcoholic liver disease[D].Guangzhou:Jinan University, 2023.
[51] VEJARANO R, LUJ N-CORRO M.Red wine and health:Approaches to improve the phenolic content during winemaking[J].Frontiers in Nutrition, 2022, 9:890066.
N-CORRO M.Red wine and health:Approaches to improve the phenolic content during winemaking[J].Frontiers in Nutrition, 2022, 9:890066.
[52] 李娅雯. 吡喃花色苷Vitisin A对甘油三酯代谢紊乱的调控作用[D].广州:暨南大学, 2022.
LI Y W.Regulatory effect of pyranoanthocyanin Vitisin A on disorders of triglyceride metabolism[D].Guangzhou:Jinan University, 2022.
[53] 白卫滨, 孙建霞, 蒋鑫炜, 等. 岭南特色富含花色苷的果酒、果醋超声催陈关键技术及产品功能评价研究[Z]. 广东省: 暨南大学, 2020.
BAI W B, AUN J X, JIANG X W, et al. Ultrasonic aging key technology and product function evaluation of Lingnan characteristic anthocyanin-rich fruit wine and fruit vinegar[Z]. Guangdong Province: Jinan University, 2020.
[54] 王倩, 赵彦巧, 张文雅, 等.微胶囊化花色苷及其生物可及性与生物利用度研究进展[J].食品工业科技, 2025,46(23):448-457.
WANG Q, ZHAO Y Q, ZHANG W Y, et al.Research progress in microencapsulated anthocyanins and its bioaccessibility and bioavailability[J].Science and Technology of Food Industry, 2025,46(23):448-457.
[55] 时小龙. 吡喃花青素类染料敏化太阳能电池的制备及光伏性能研究[D].哈尔滨:东北林业大学, 2021.
SHI X L.Physicochemical property and biological activity of new anthocyanin derivative Oxovitisin[D].Harbin:Northeast Forestry University, 2021.
[56] 王二雷, 黄佳莹, 段海章, 等.花色苷稳态化技术研究进展及应用前景[J].食品工业科技, 2024, 45(18):394-403.
WANG E L, HUANG J Y, DUAN H Z, et al.Progress on the stabilization technology of anthocyanins and the application prospects[J].Science and Technology of Food Industry, 2024, 45(18):394-403.
[57] OLIVEIRA H, WU N, ZHANG Q, et al.Bioavailability studies and anticancer properties of malvidin based anthocyanins, pyranoanthocyanins and non-oxonium derivatives[J].Food &Function, 2016, 7(5):2462-2468.