花生四烯酸(arachidonic acid,ARA)是母乳的重要成分,对婴儿认知发育至关重要[1]。由于婴儿体内去饱和酶和延长酶水平较低,无法合成足够的内源性ARA,因此须通过膳食补充来避免对大脑和视觉发育产生不良影响[2]。母乳被视为婴儿最理想的营养来源,能提供生长发育所需的全部营养素。母乳中ARA含量通常为0.36%~0.49%,其水平受哺乳阶段、母亲饮食及遗传因素影响[3]。对于非纯母乳喂养的婴儿,通常需使用ARA强化配方奶粉。然而配方奶粉中的ARA多来源于微生物油,主要含有长链脂肪酸(long-chain fatty acids,LCFA),其甘油三酯(triacylglycerol,TAG)结构与母乳存在差异。婴儿消化系统具有特殊性,虽然其胃脂肪酶活性与成人相当,但胰脂肪酶活性和胆盐水平较低;加之脂肪酶对长链多不饱和脂肪酸(polyunsaturated fatty acids,PUFA)的水解效率有限,进一步降低了微生物油来源ARA的消化率[4]。这些因素凸显了提升婴儿ARA营养吸收效率的策略必要性。
中长链甘油三酯(medium- and long-chain triglycerides,MLCT)是一种在甘油骨架上同时结合中链脂肪酸(medium-chain fatty acids,MCFA)和LCFA的结构化脂质[5]。MCFA可被胃脂肪酶水解,通过门静脉直接吸收至肝脏快速供能。在胃消化过程中产生的甘油二酯(diacylglycerol,DAG)和甘油一酯(monoacylglycerol,MAG)作为天然乳化剂,能增强肠道脂肪溶解性,弥补婴儿胰脂肪酶和胆盐分泌不足的特性[6]。这些特性使MLCT成为重要的能量来源和功能性脂质补充剂,尤其适用于胰脂肪酶或胆盐缺乏患者。作为ARA载体,MLCT可显著提升其在婴儿体内的消化吸收效率[7]。目前MLCT主要通过酶法或化学法合成。相较于化学法,酶法合成具有反应条件温和、脂肪酶特异性高、副产物少及环境友好等优势,是生产结构化脂质的优选方案。在酶法合成中,酸解反应和酯交换反应应用广泛,其中酯交换反应对纯化要求低,在大规模生产MLCT时更具显著优势。然而,脂肪酶活性较低仍是制约反应效率的关键瓶颈,因此提升脂肪酶活性对改善酶法酯交换反应整体效率至关重要。
脂肪酶作为丝氨酸水解酶,是分子质量20~60 kDa的酸性糖蛋白。其三维结构由α-螺旋和β-折叠构成,这种稳定构象对催化活性和底物识别至关重要[8]。脂肪酶活性中心由丝氨酸、天冬氨酸和组氨酸组成的催化三联体构成,其中丝氨酸羟基在水解过程中对酯键的亲核攻击起关键作用。一段短α-螺旋结构的“盖子”通常覆盖活性中心,阻碍底物接触[9]。当遇到油-水界面时,脂肪酶会发生构象变化,“盖子”打开并暴露活性中心,从而激活酶活性[10]。但在非水相溶剂中,这种界面激活效应消失,“盖子”维持闭合状态,显著降低催化效率[11]。因此,如何在反应中保持“盖子”开放状态成为关键问题。生物印迹是一种通过修饰酶微观构象来提升催化特异性和效率的简便可靠技术。酶作为生物大分子具有构象记忆特性:在水溶液中呈现柔性,在非水体系中保持刚性。利用这一特性,可先在水溶液中对脂肪酶进行生物印迹,再通过冻干固定构象后应用于非水体系[12]。印迹后,模板分子能诱导“盖子”持续开放,暴露活性中心内部的疏水基团,从而促进底物接触[13-14]。表面活性剂是一类优良的脂肪酶印迹模板,但需注意的是离子型表面活性剂可能破坏脂肪酶的三级结构导致部分或完全解折叠,而非离子型表面活性剂更有助于维持酶结构完整性[15-16]。因此需对模板进行筛选。
本研究采用生物印迹技术提高脂肪酶催化效率,并以生物印迹脂肪酶(bio-imprinted lipase,BIL)为催化剂,通过酯交换反应制备富含ARA的MLCT。首先,优化脂肪酶生物印迹条件以提升其催化效率,然后优化酯交换反应条件以提高MLCT产率,最后通过重复使用实验测定脂肪酶的活性稳定性。
1 材料与方法
1.1 材料
本研究使用的商业化固定化脂肪酶包括:来自南极假丝酵母的Lipozyme 435、来自米黑根毛霉的Lipozyme RM IM、来自米曲霉的Novozyme 40086以及来自疏棉状嗜热丝孢菌的Lipozyme TL IM,诺维信(中国)北京公司。富含ARA的裂殖壶菌微生物油,厦门汇盛生物技术有限公司;中链甘油三酯(medium-chain triglycerides,MCT)(含60%辛酸和40%癸酸)、吐温-20、曲拉通X-100、十六烷基三甲基溴化铵(cetyltrimethylammonium bromide,CTAB)和十二烷基硫酸钠[sodium bis(2-ethylhexyl) sulfosuccinate,AOT],百灵威化学有限公司;脂肪酸甲酯标准品混合物,上海默克公司;二氯荧光素包被硅胶薄层色谱板(10 cm×20 cm;平均粒径2~25 μm;孔径60 μm;厚度500 μm),尚邦实业有限公司;乙腈、NaOH、正己烷、盐酸、异丙醇等,国药集团化学试剂有限公司。
1.2 仪器与设备
HCJ-2E磁力搅拌水浴锅、XH-C旋涡振荡仪,常州恩培仪器制造有限公司;NEXUS真空冷冻干燥机,美国Labconco公司;Agilent 1260高效液相色谱、7820A气相色谱仪,美国安捷伦科技有限公司;AB104-N分析天平,梅特勒托利多公司;Centrifuge 5810离心机,德国Eppendorf公司;TG 16A-WS离心机,上海卢湘仪离心机设备有限公司。
1.3 实验方法
1.3.1 BIL的制备
参照FISHMAN等[14]的方法并加以改进。首先将500 mg固定化脂肪酶分散于20 mL含表面活性剂的磷酸盐缓冲液(50 mmol/L,pH值通过盐酸和NaOH溶液调节)中,室温下进行30 min生物印迹处理。随后1 000 r/min离心5 min收集印迹脂肪酶,再经真空冷冻干燥48 h。冻干后的生物印迹脂肪酶用色谱级正己烷洗涤3次以去除模板分子,最后真空干燥24 h并于4 ℃保存。
以初始酶活性为基础,系统调整表面活性剂类型(吐温-20、曲拉通X-100、CTAB、AOT)、表面活性剂质量浓度(10、30、50、70、90 mg/mL)和脂肪酶溶液pH(3.0、5.0、7.0、9.0、11.0)等工艺参数,优化BIL的制备工艺。
1.3.2 脂肪酶初始活力的测定
通过MCT与微生物油的酯化反应来评价脂肪酶的催化活性。制备了3 g MCT与微生物油的混合物,底物摩尔比为1∶1。然后加入BIL的质量分数为6%。反应在圆底烧瓶中进行,60 ℃,磁力搅拌,转速为500 r/min。2 h后,收集产品以评估初始活力。一个酶活性单位(U)定义为每小时转化摩尔分数为1% MCT所需的酶量(g)。
1.3.3 MLCT的合成
MCT与微生物油的酯交换反应在无溶剂体系中进行,采用25 mL圆底烧瓶作为反应容器并精确控温。每次反应使用总量为3 g的MCT与微生物油混合物(按二者摩尔比配制)。反应通过添加特定脂肪酶,并在500 r/min磁力搅拌下确保酶与底物充分接触。反应结束后经分离去除脂肪酶,收集所得MLCT产物。
1.3.4 TAG成分分析
采用配备蒸发光散射检测器的反相高效液相色谱系统分析TAG组成。色谱分离使用Lichrospher C18色谱柱(5 μm,4.6 mm×250 mm),蒸发光散射检测器参数设定为检测温度55 ℃、载气流速1.8 mL/min和增益值1。将TAG样品用正己烷稀释至10 mg/mL后,取10 μL进样至高效液相色谱系统。采用乙腈(A相)与异丙醇/正己烷(1∶1,体积比)(B相)二元梯度洗脱,流速0.5 mL/min。A相梯度程序如下:0~20 min保持90%,20 min内降至70%,24 min降至60%,36 min降至40%,37 min回升至90%并维持至50 min分析结束。通过对比反应前后TAG色谱峰保留时间与标准品参照,监测酯交换反应进程。MLCT产率按反应产物中总TAG[MCT+MLCT+长链甘油三酯(long-chain triglycerides,LCT)]的质量百分比计算。
1.3.5 脂肪酸组成分析
采用配备火焰离子化检测器和SP TM-380毛细管色谱柱(60 m×0.32 mm,0.2 μm)的气相色谱系统分析产物的脂肪酸组成[17]。色谱柱初始温度100 ℃保持4 min,随后以15 ℃/min升温至180 ℃并保持4 min,再以4 ℃/min升至215 ℃。进样口和检测器温度均设定为250 ℃。通过对比脂肪酸甲酯与标准品的保留时间进行定性分析,各脂肪酸相对含量以摩尔百分比计算。
1.3.6 脂肪酸sn-2位分析
采用格氏法降解烯丙基溴化镁制备sn-2 MAG[18]。具体步骤为:取约30 mg油样溶于10 mL乙醚,加入0.3 mL烯丙基溴化镁溶液,剧烈振荡1 min后,用8 mL酸性缓冲液(0.27 mol/L盐酸与0.4 mol/L硼酸混合液)终止反应。去除水相后,乙醚萃取液经硼酸溶液洗涤2次,并用Na2SO4干燥。将乙醚使用氮吹浓缩至150 μL,在薄层色谱板上进行分离,展开剂为氯仿/丙酮(90∶10,体积比)。刮取对应sn-2 MAG的条带,用2 mL乙醚分2次萃取,萃取液经Na2SO4干燥后氮吹浓缩。残留物经甲酯化处理后,通过气相色谱分析其脂肪酸组成。
1.3.7 BIL制备的正交试验
以MLCT含量为试验指标,选取L9(33)进行正交试验,考察表面活性质量浓度和缓冲液pH对MLCT产率的影响。正交试验因素水平如表1所示。
表1 正交实验因素和水平设计
Table 1 Factors and levels in the orthogonal design
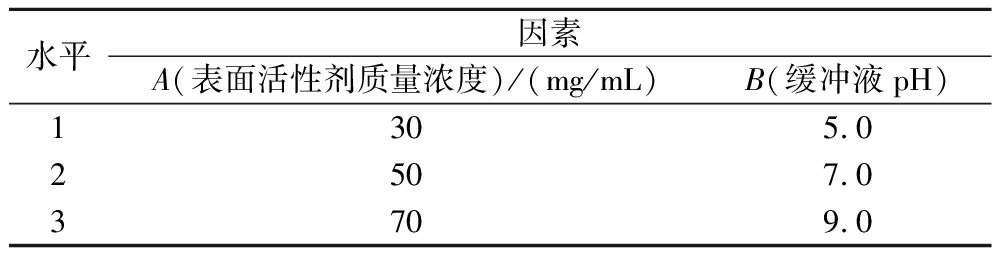
水平因素A(表面活性剂质量浓度)/(mg/mL)B(缓冲液pH)1305.02507.03709.0
1.3.8 脂肪酶的重复利用性分析
重复使用BIL和Lipozyme 435催化MCT和微生物油的酯交换反应。在每次试验结束时离心收集脂肪酶。2种脂肪酶用己烷冲洗3次,真空干燥备用。
1.4 统计分析
所有的样品和实验均重复3次。结果采用Excel 2010和Origin 8.5软件计算,并以“平均值±标准偏差”表示。采用SPSS Statistics 26进行单因素方差分析(P<0.05为差异显著)。
2 结果与分析
2.1 BIL的制备
2.1.1 商用固定化脂肪酶的筛选
如图1所示,反应2 h后,Lipozyme 435生成的MLCT的质量分数为47.58%。该产率高于Lipozyme TL IM(43.53%)、Lipozyme RM IM(42.53%)和Novozyme 40086(37.28%)。与其他3种脂肪酶相比,Lipozyme 435产生的MLCT有显著差异。相比之下,Novozyme 40086在最终产物中显示出最高浓度的MCT和LCT,导致MLCT的产量最低,这表明Novozyme 40086可能不是该特定反应体系的最合适选择。考虑到Lipozyme 435的初始活力最高,为9.97 U/g,因此选择其作为后续制备BIL的模型脂肪酶。
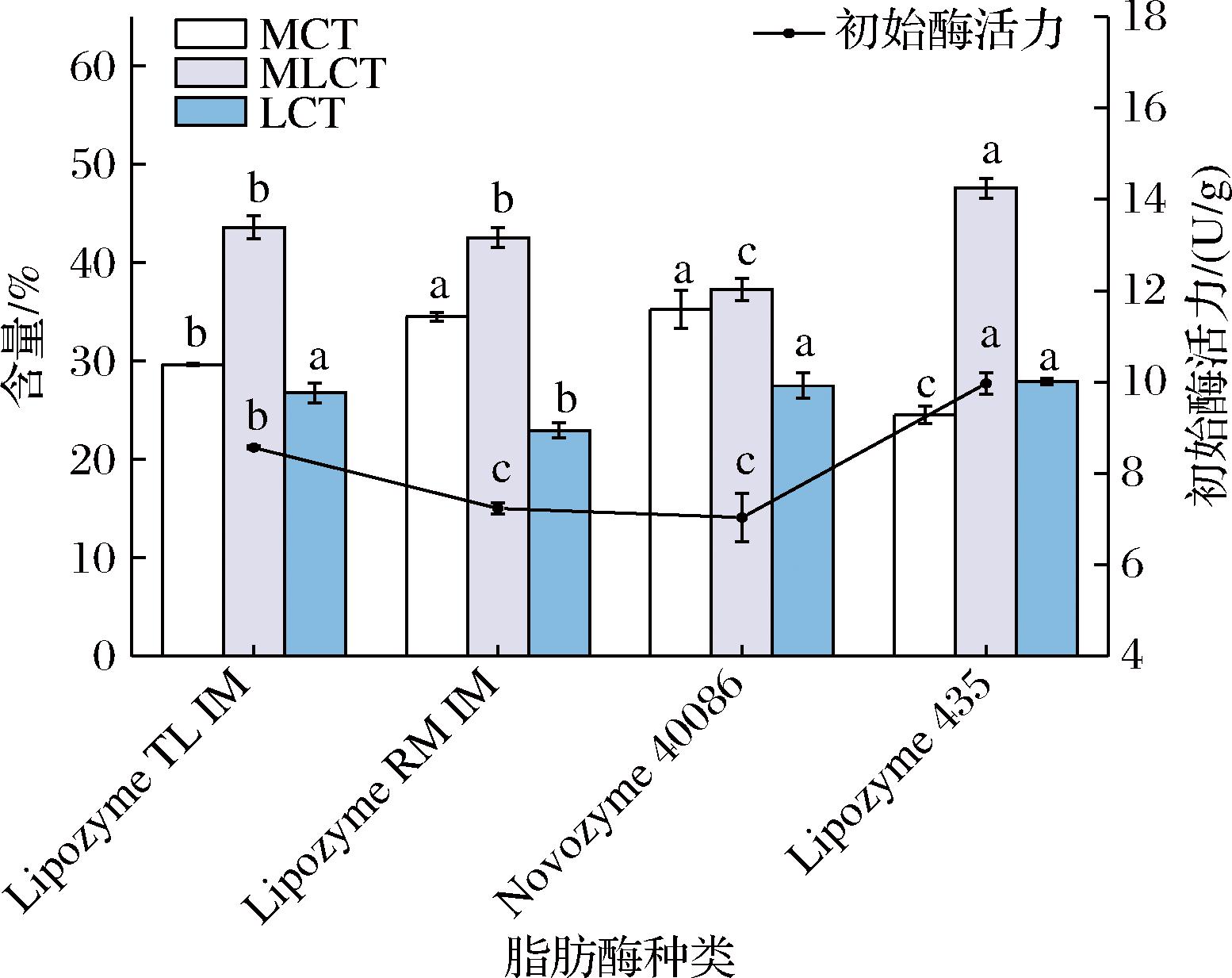
图1 不同脂肪酶对酯交换化反应的影响
Fig.1 Effect of different lipases on interesterification reaction
注:不同小写字母表示相同脂质类型和初始活力在不同BIL制备条件的差异显著(P<0.05)(下同)。
2.1.2 表面活性剂类型对BIL的影响
本研究选取吐温-20、曲拉通X-100、AOT和CTAB这4种表面活性剂,考察其对BIL催化活性的影响。每种表面活性剂的质量浓度保持在50 mg/mL,结果如图2所示。
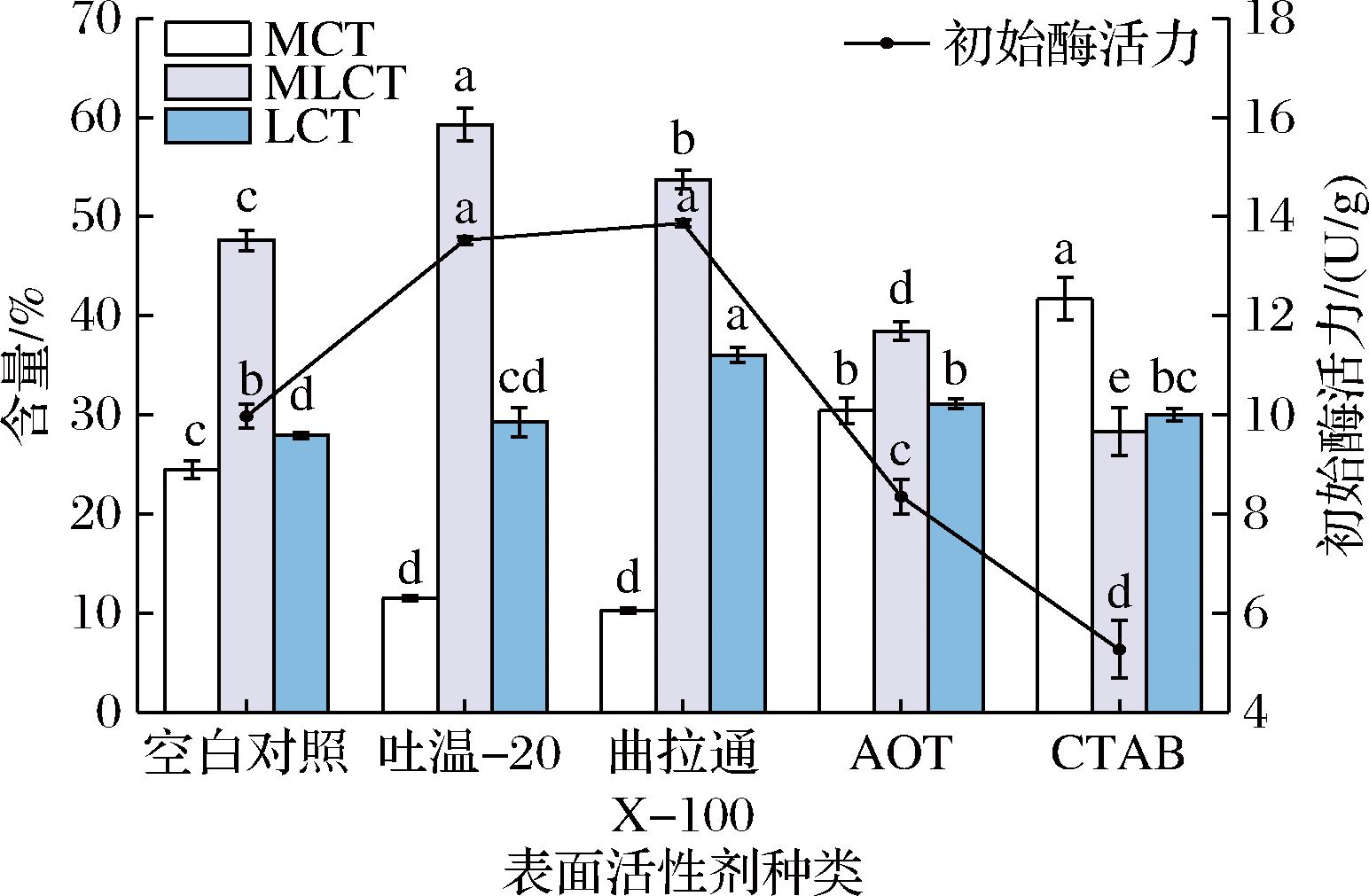
图2 不同表面活性剂对酯交换反应的影响
Fig.2 Effect of different surfactants on interesterification reaction
与阴离子表面活性剂和阳离子表面活性剂相比,非离子表面活性剂(吐温-20和曲拉通X-100)显著提高了脂肪酶的初始活力,MLCT的质量分数分别达到59.25%和53.72%。吐温-20和曲拉通X-100都是具有亲水性聚氧乙烯链和疏水性烷基链的非离子型表面活性剂,它们通过疏水相互作用结合到脂肪酶的疏水区域,诱导脂肪酶形成更适合底物结合的构象,同时避免强烈的静电干扰。此外,非离子型表面活性剂可以形成稳定的油水界面,促进了脂肪酶活性中心“盖子”结构的打开,界面活化增强了脂肪酶与底物之间的亲和力。在类似的研究中,AMENAGHAWON等[19]使用表面活性剂(吐温-80,吐温-20和曲拉通X-100)将脂肪酶活性提高了168.3%。
相比之下,CTAB和AOT表面活性剂对脂肪酶活性有较强的抑制作用。这种抑制可能是由于离子表面活性剂的带电基团和蛋白质表面的带电氨基酸之间的静电排斥,导致构象变化,降低酶的活性[15]。此外,吐温-20还具有生物降解性和环境友好性,以及在特定温度和pH范围内保持脂肪酶稳定性的能力。因此,本研究选择吐温-20作为制备BIL的表面活性剂。
2.1.3 表面活性剂质量浓度对BIL的影响
在10~90 mg/mL考察了不同质量浓度的吐温-20对BIL初始活力的影响。结果如图3所示。在吐温-20质量浓度为10~50 mg/mL的条件下,BIL的初始活力逐渐增加,50 mg/mL时,MLCT产率的质量分数达到最大值(59.25%)。然而,随着吐温-20质量浓度的进一步增加,MLCT的产率在90 mg/mL时下降到51.63%。在较低质量浓度下,非离子表面活性剂主要通过疏水相互作用、增强底物溶解度和改善初始活力来稳定脂肪酶。相反,在较高质量浓度下,过量的非离子表面活性剂会占据脂肪酶的结合位点,阻碍底物的结合,降低催化效率。CARRASCO-L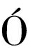 PEZ等[20]指出,低质量浓度的非离子型表面活性剂与脂肪酶的疏水活性位点相互作用。这种相互作用稳定了酶的开放构象,促进了底物的进入和产物的释放,从而提高了酶的活性。然而,在较高质量浓度下,非离子表面活性剂可能进入脂肪酶的活性位点并形成强相互作用,从而抑制脂肪酶催化能力。
PEZ等[20]指出,低质量浓度的非离子型表面活性剂与脂肪酶的疏水活性位点相互作用。这种相互作用稳定了酶的开放构象,促进了底物的进入和产物的释放,从而提高了酶的活性。然而,在较高质量浓度下,非离子表面活性剂可能进入脂肪酶的活性位点并形成强相互作用,从而抑制脂肪酶催化能力。
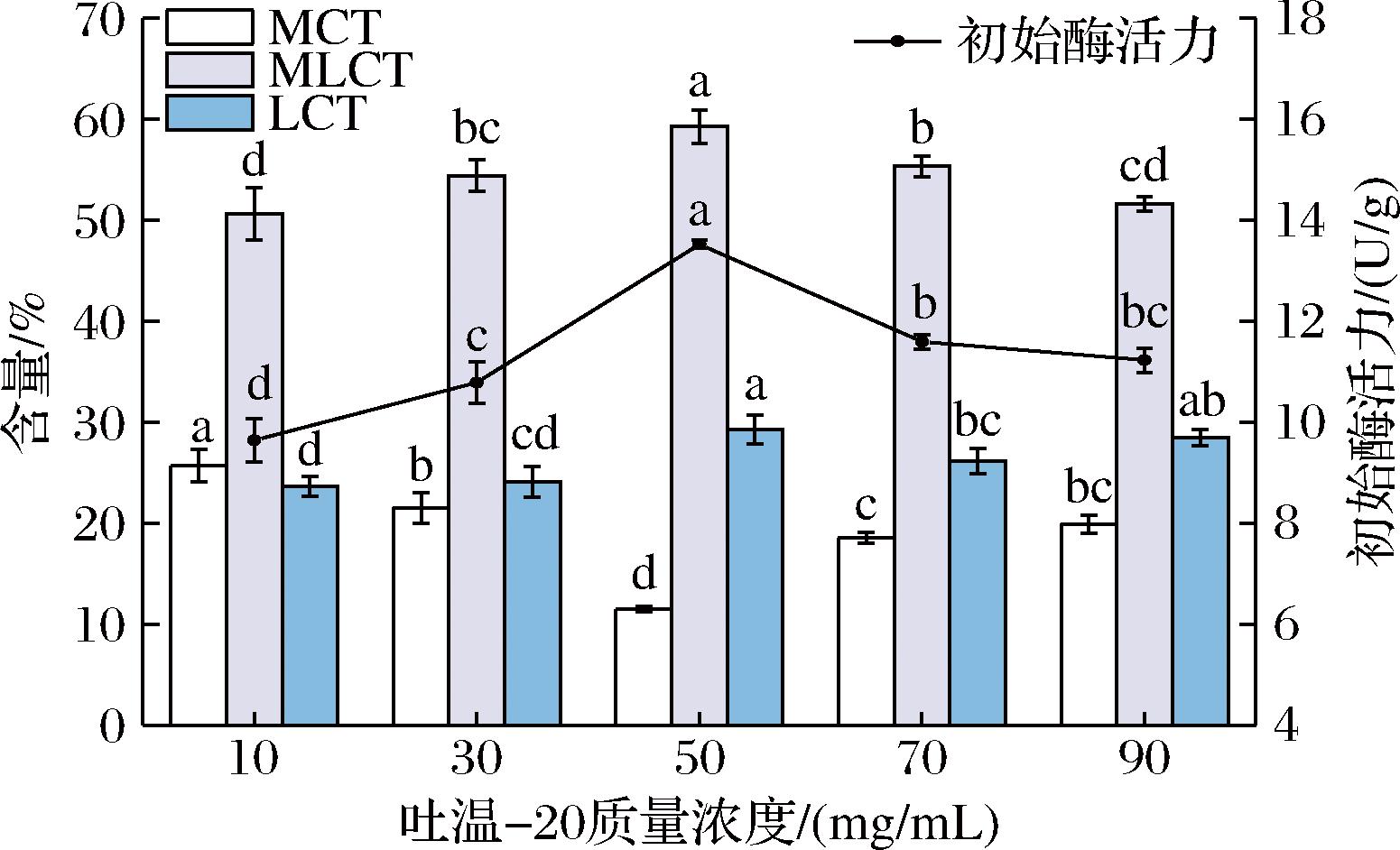
图3 不同吐温-20浓度对酯交换反应的影响
Fig.3 Effect of different concentrations of Tween 20 on interesterification reaction
2.1.4 不同pH值对BIL的影响
不同pH值对BIL初始活力的影响范围为3.0~11.0,结果如图4所示。在pH值为3.0~7.0时,脂肪酶活性逐渐升高,在pH值为7.0时,MLCT产率的质量分数达到59.25%。脂肪酶对pH值非常敏感,过高或过低的pH值都会降低其活性[21]。pH的改变影响了酶活性位点官能团的解离状态。在最佳pH下,这种解离状态增强了酶与其底物之间的相互作用。相反,高于或低于最佳pH会阻碍结合过程,导致酶活性降低。此外,pH还会影响反应体系中底物和其他组分的解离。缓冲体系的离子特性和强度也可能在酶反应中起重要作用。此外,pH对酶的活性和稳定性都起着至关重要的作用。极端的pH值可以改变酶活性位点的构象,甚至改变整个酶的结构,导致变性和失去活性。因此,制备BIL的最佳工艺条件为脂肪酶Lipozyme 435,印迹模板吐温-20,印迹模板质量浓度50 mg/mL,缓冲液pH值为7.0。BIL的初始活力为13.52 U/g,是非生物印迹的1.36倍。
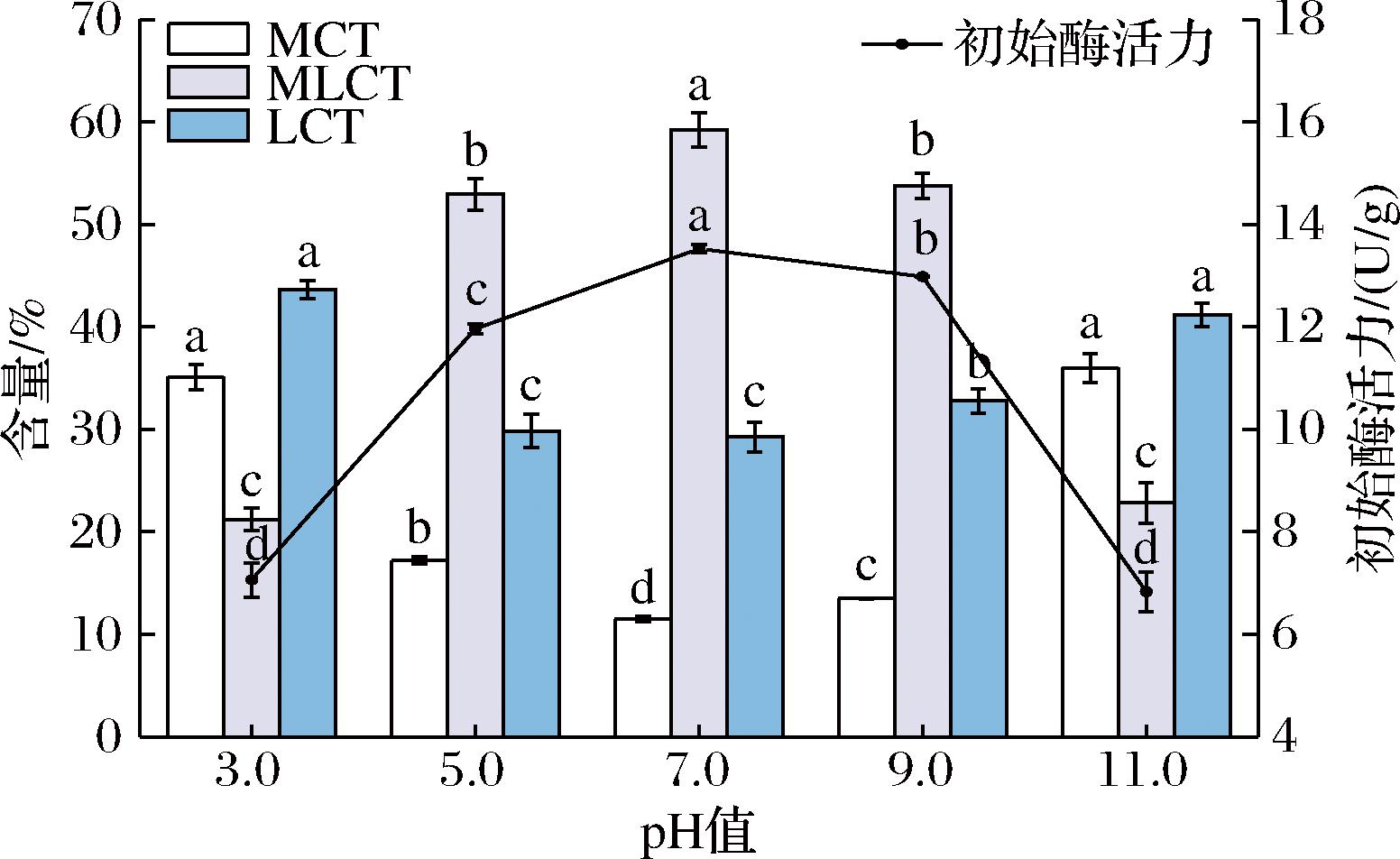
图4 不同pH值对酯交换反应的影响
Fig.4 Effect of different pH levels on interesterification reaction
2.2 正交试验设计结果分析
选择表面活性剂质量浓度、缓冲液pH 2个因素进行正交试验,设计及结果如表2所示,方差分析如表3所示。
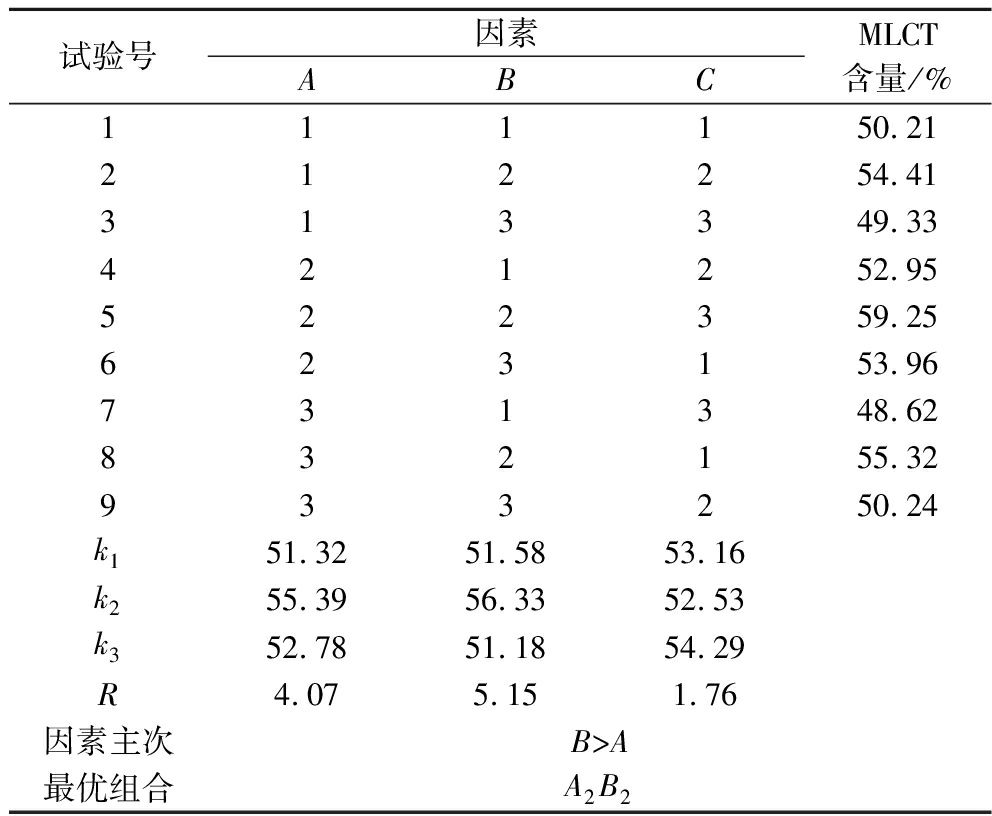
表2 正交试验结果与分析
Table 2 Results and analysis of orthogonal test
试验号因素ABCMLCT含量/%111150.21212254.41313349.33421252.95522359.25623153.96731348.62832155.32933250.24k151.32 51.58 53.16 k255.39 56.33 52.53 k352.78 51.18 54.29 R4.07 5.15 1.76 因素主次B>A最优组合A2B2
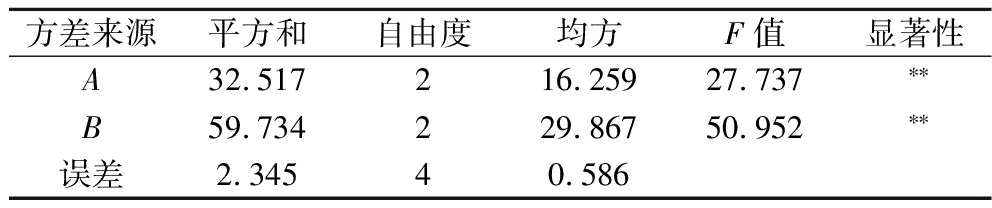
表3 正交试验结果方差分析
Table 3 Variance analysis of orthogonal test results
方差来源平方和自由度均方F值显著性A32.517216.25927.737∗∗B59.734229.86750.952∗∗误差2.34540.586
注:**表示差异极显著(P<0.01)。
由表2可知,影响BIL催化能力的各因素主次关系顺序为缓冲液pH(B)>表面活性剂质量浓度(A)。BIL正交试验结果的优化方案为A2B2,即表面活性剂质量浓度为50 mg/mL,缓冲液pH值为7.0,此条件下BIL催化酯交换反应生成的MLCT的质量分数为59.25%,与试验结果一致。从表3可知,正交试验的9次处理对MLCT含量的影响极显著(P<0.01)。
2.3 反应条件的优化
2.3.1 脂肪酶添加量
当反应接近平衡时,脂肪酶的浓度对反应效率有显著影响[22]。增加脂肪酶的用量可以提高反应速率,但也会导致生产成本的增加。此外,过量使用脂肪酶可能导致中间产物(如MAG和DAG)浓度增加,最终可能降低目标产物的产量[18]。因此,选择合适的BIL添加量需要综合评估反应效率和经济因素。从2%~10% 质量分数的BIL添加量对TAG含量的影响进行了研究。反应在60 ℃的温度下进行,MCT/微生物油的摩尔比为1∶1,持续2 h。结果如图5所示。
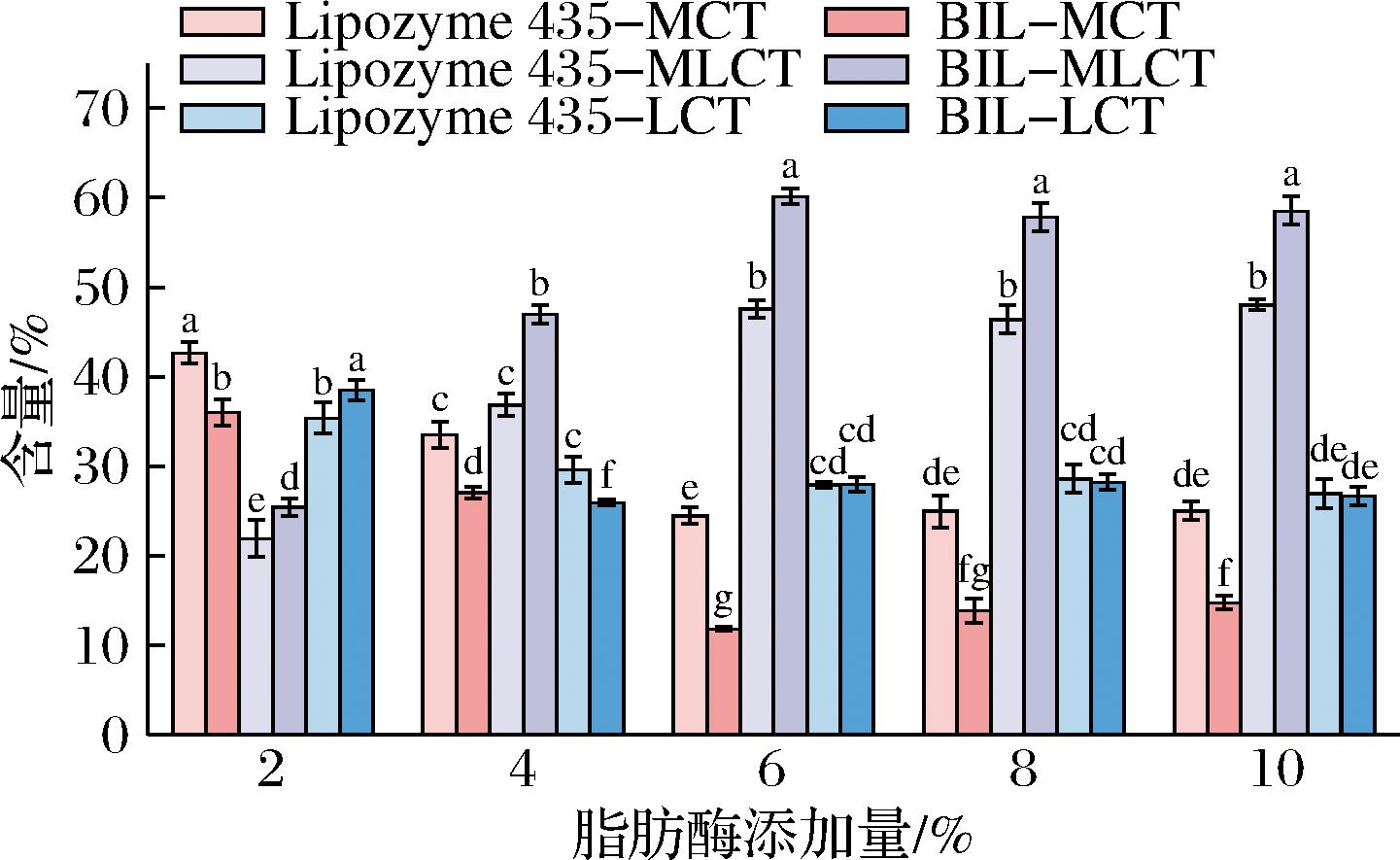
图5 不同脂肪酶添加量对酯交换反应的影响
Fig.5 Effect of different lipase addition amount on interesterification reaction
注:不同小写字母表示相同脂质类型在不同反应条件的差异显著(P<0.05)(下同)。
反应体系中MLCT的产率与BIL的加入量呈正相关。其中,随着BIL添加量从2%增加到6%,MLCT产率的质量分数从25.43%提高到60.17%。然而,进一步增加BIL的添加量并没有导致MLCT产量的显著提高。通常,增加酶的添加量会增加活性催化位点的数量,从而提高反应速率[23]。当反应体系中的酶浓度过高时,会抑制目标产物的产生。这种抑制可能是由于高底物浓度降低了水的有效浓度,从而降低了分子扩散率,减慢了酶促反应速率。因此,选择质量分数为6%的脂肪酶添加量进一步研究。
2.3.2 反应温度
脂肪酶的催化活性和反应速率受反应温度的显著影响,特别是在无溶剂环境下的酶促合成[24]。较高的温度通常会促进分子活化,增强分子迁移率,并增加分子与催化剂之间有效碰撞的频率。因此,在反应过程中提高温度可以减少达到平衡所需的时间。与它们在水溶液中的行为相比,脂肪酶在非水环境中表现出更大的热稳定性。然而,过高的温度会导致酶变性,导致活性丧失[25]。为了确定最大化MLCT合成产率的最佳反应温度,本研究在不同温度(40、50、60、70 ℃和80 ℃)下评估了MLCT的产率,条件是BIL添加量的质量分数6%,底物摩尔比1∶1(MCT/微生物油),反应时间2 h,结果如图6所示。
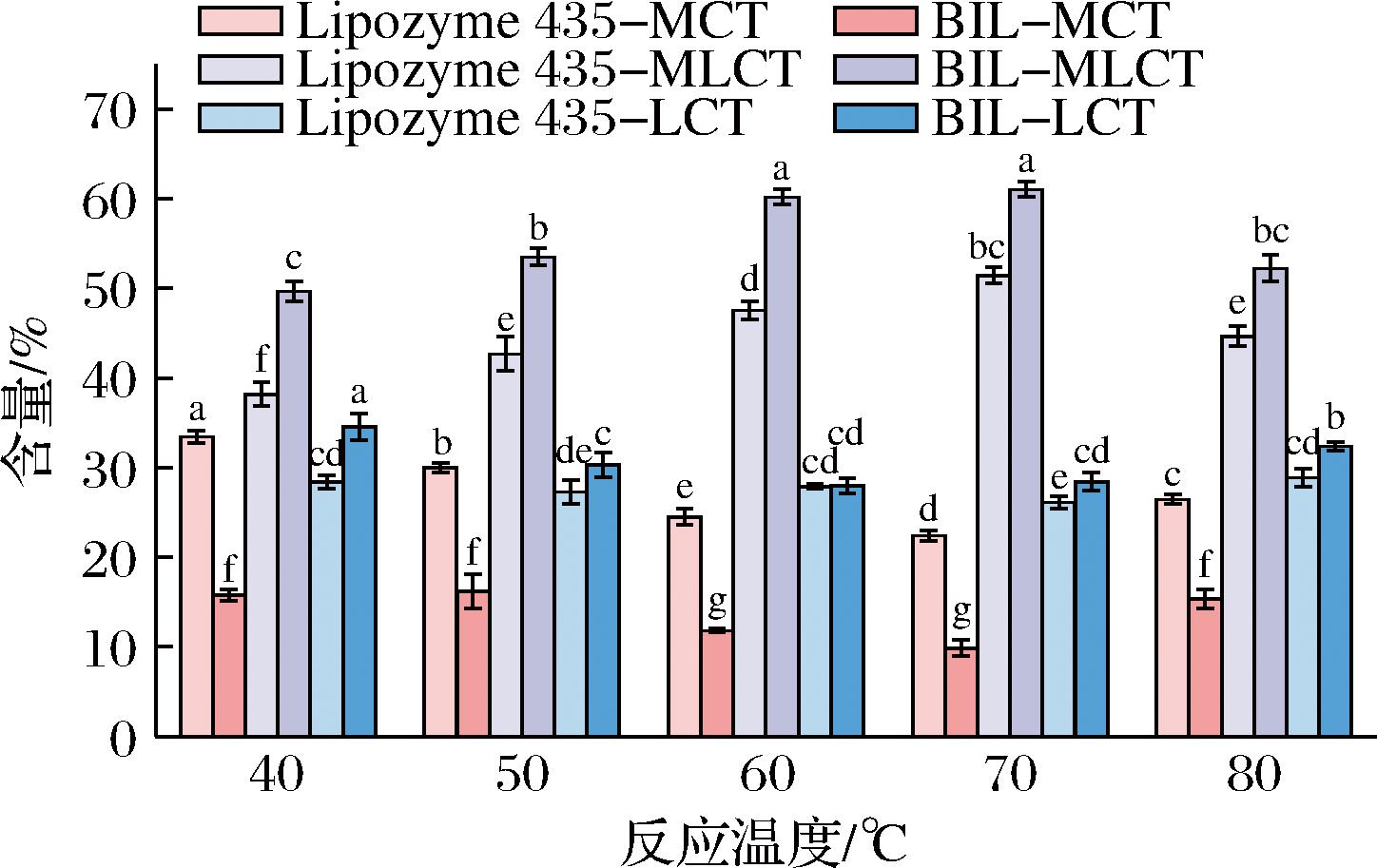
图6 不同反应温度对酯交换反应的影响
Fig.6 Effect of reaction temperature on interesterification reaction
结果表明,反应温度对MLCT产率有显著影响,在达到一定温度后,MLCT产率随温度的升高而升高,然后下降。其中,随着温度从40 ℃升高到70 ℃,反应产物中MLCT的质量分数从49.67%提高到61.02%。然而,当温度从70 ℃进一步升高到80 ℃时,MLCT的产率显著下降,从61.02%下降到52.23%。可能是由于温度升高改变了脂肪酶的内部结构,从而降低了它的催化活性。另外,随着反应温度从50 ℃升高到70 ℃,MCT含量从16.20%下降到9.85%,但随着反应温度从70 ℃升高到80 ℃,MCT含量又上升到15.37%。同样,在40~70 ℃范围内,LCT含量从34.54%下降到28.43%,但在70~80 ℃ 范围内,LCT含量上升到32.40%。因此,为了获得最大的MLCT含量,本研究选择70 ℃的反应温度进一步研究。
2.3.3 底物摩尔比(MCT/微生物油)
底物的摩尔比显著影响可逆反应的平衡点,从而影响产物的产率。为了优化MLCT的合成,在不同的MCT/微生物油的摩尔比(2∶1、1.5∶1、1∶1、1∶1.5和1∶2)下,在BIL添加量的质量分数6%,反应温度70 ℃,反应时间2 h的条件下,对MCT、MLCT、LCT的含量进行了评估,结果如图7所示。
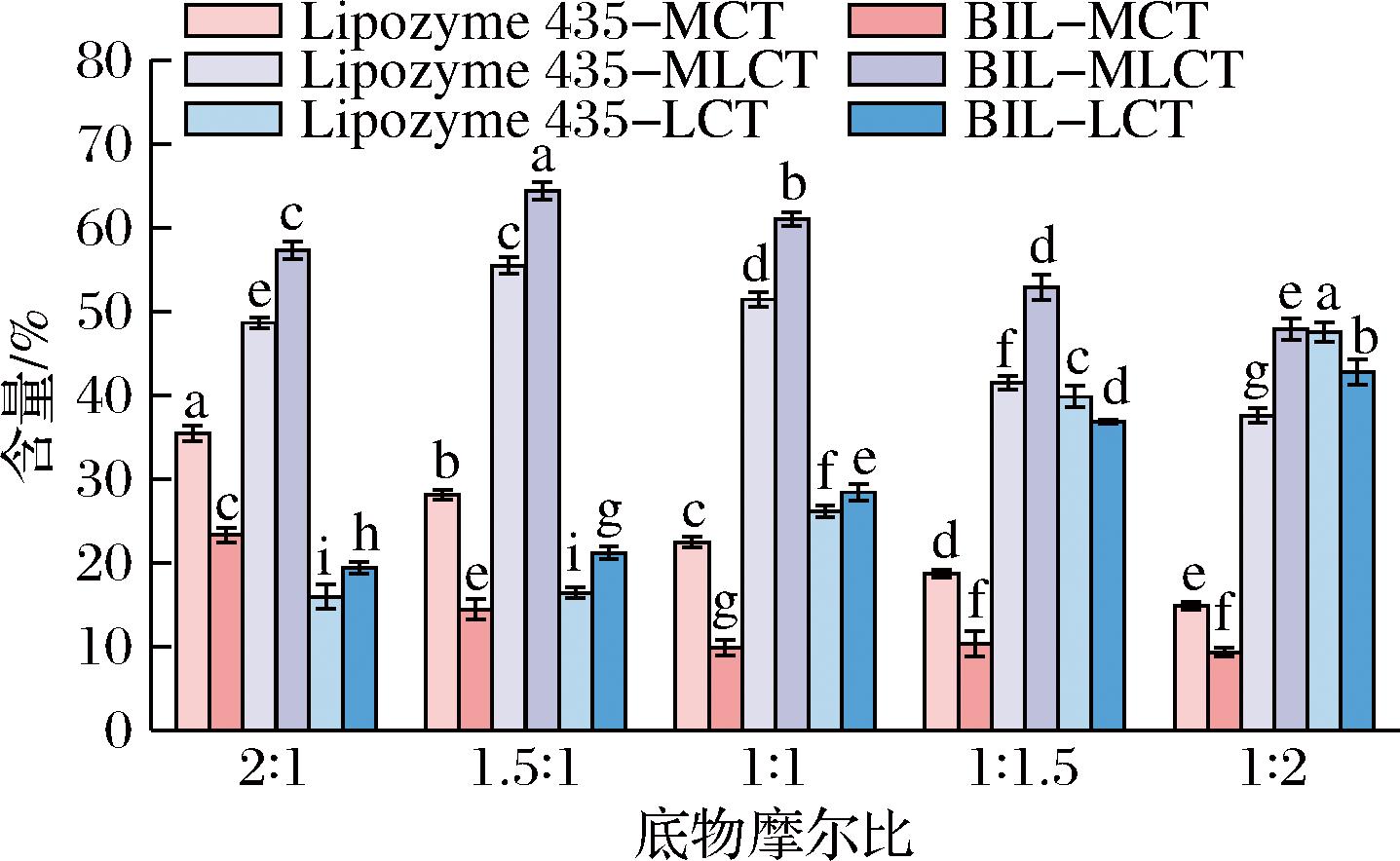
图7 不同底物摩尔比(MCT:微生物油)对酯交换反应的影响
Fig.7 Effect of different substrate molar ratio (MCT:microbial oil) on interesterification reaction
底物比例显著影响MLCT含量的增长率。随着底物摩尔比的增加,MLCT的产率先上升后下降,在底物摩尔比为1.5∶1时达到动态平衡,此时MLCT产率的质量分数达到64.41%。理论上,较高的MCT浓度提高了反应速率,因为底物之间碰撞的可能性增加了。然而,当底物摩尔比从1.5∶1过渡到1∶2时,MLCT的产量下降。过量的微生物油可能积聚在酶分子上,形成无法释放的无活性中间体,进一步降低反应速率。因此,随着反应物中MCT含量的降低,LCT含量增加,导致相应的MCT含量降低,最终产物中LCT含量增加。因此,为了使MLCT含量最大化,本研究选择1.5∶1的底物摩尔比进行后续实验。
2.3.4 反应时间
在BIL添加量的质量分数6%,反应温度70 ℃,底物摩尔比(MCT/微生物油)1.5∶1的特定条件下。考察了适宜的反应时间。以MCT、MLCT、LCT的含量为指标,结果如图8所示。
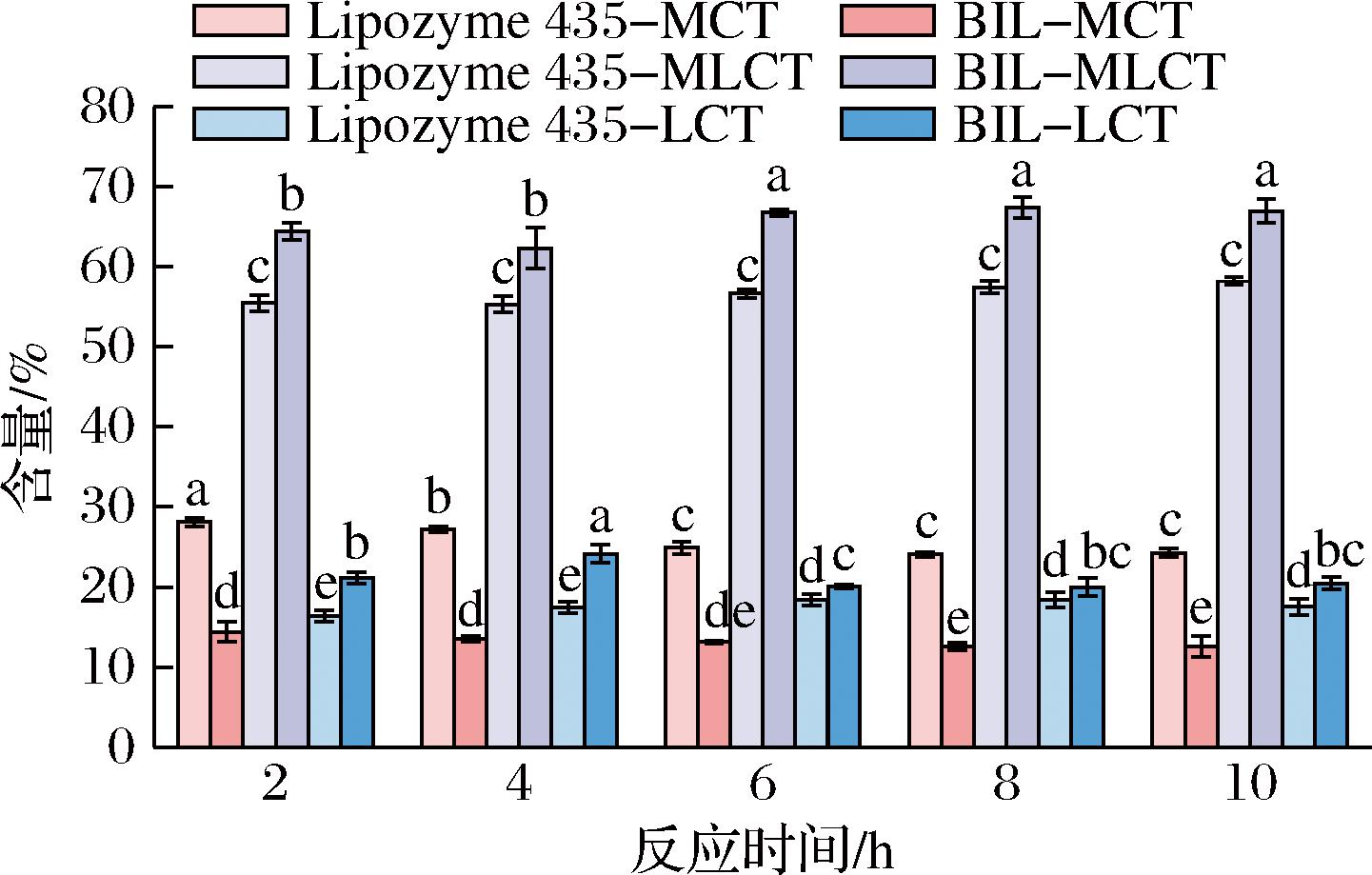
图8 不同反应时间对酯交换反应的影响
Fig.8 Effect of different reaction time on interesterification reaction
在反应开始时,MCT和LCT之间发生了交换作用,导致它们在转化为MLCT时各自的含量下降。在反应结束时,系统达到平衡,导致每个组分含量的变化最小。随着反应的进行,MLCT含量不断增加。反应开始时,反应速度快,2 h时MLCT的质量分数为64.41%,平均每小时增加32.21%,2~6 h时MLCT含量增加到66.80%,平均每小时增加0.48%,而 6~10 h时MLCT产率变化不大,平均每小时增加0.04%。MCT和LCT含量的变化趋势也类似。随着反应时间的延长,MCT和LCT含量在2~6 h逐渐降低,MCT含量显著降低,LCT含量无显著降低。6 h后,MCT和LCT含量变化极小。因此,为了最大限度地提高MLCT的含量,本研究选择反应时间为6 h进一步的研究。最终确定了合成富MLCT油的最佳工艺条件为:BIL添加量的质量分数6%,反应温度70 ℃,MCT/微生物油摩尔比1.5∶1,反应时间6 h。在此最佳工艺条件下,MLCT产品中MCT、MLCT和LCT的质量分数分别为13.12%、66.80%和20.08%。
2.4 脂肪酶的可重复使用性分析
为了进一步证明吐温-20生物印迹Lipozyme 435的稳定性和优越性能,在最佳反应条件下研究了其可重复使用性,并与Lipozyme 435进行了比较,结果如图9所示。
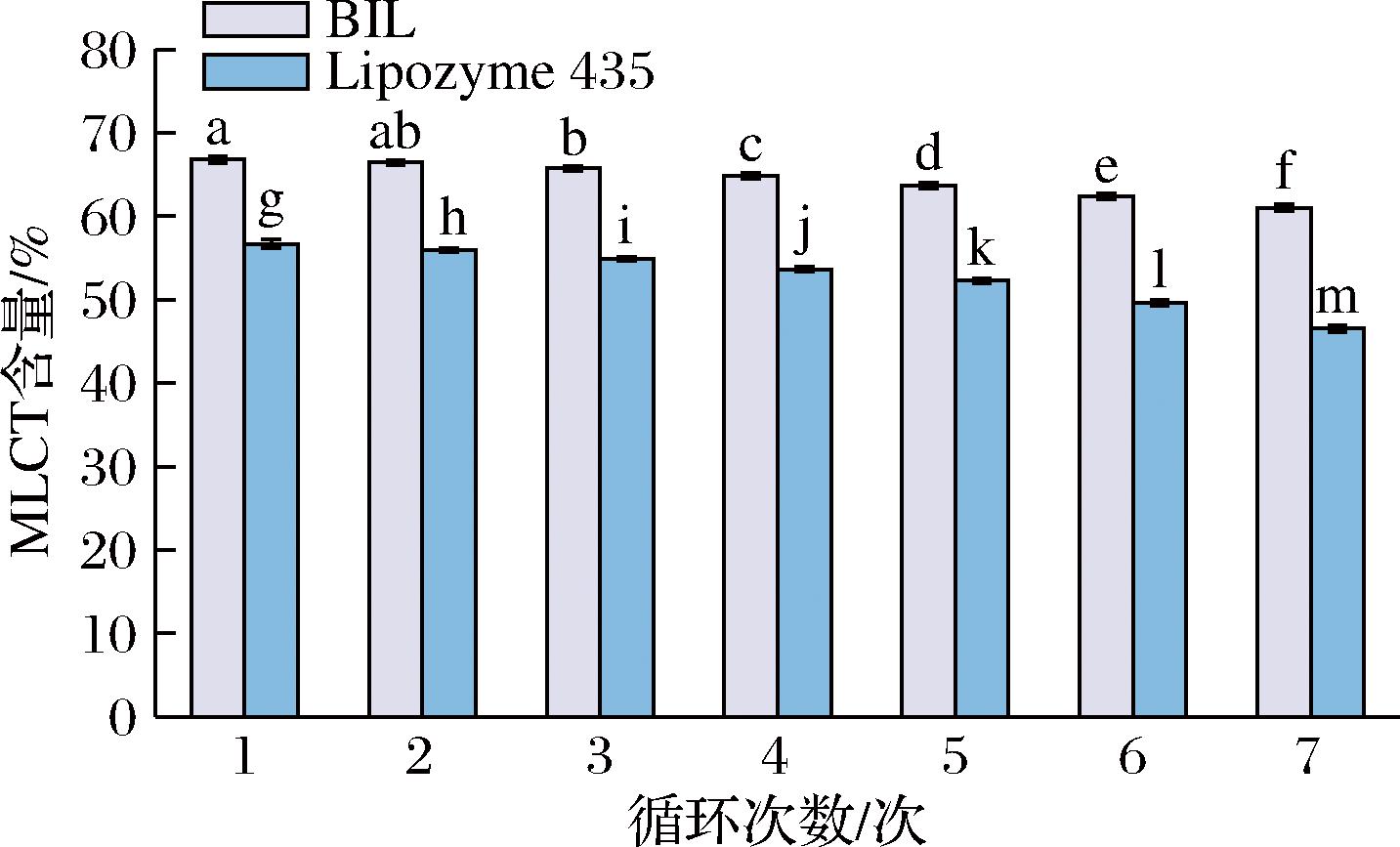
图9 BIL和Lipozyme 435的可重复使用性
Fig.9 Reusability of BIL and Lipozyme 435
注:不同小写字母表示脂肪酶在相同/不同循环次数差异显著(P<0.05)。
经过7个反应循环后,BIL催化的酯化反应中MLCT的质量分数保持在61.05%,仅下降了5.75%,而Lipozyme 435的MLCT产率下降了10.12%。重复使用后转化效率的降低主要是由于酶质量的损失、活性位点的堵塞和酶的结构变化。生物印迹修饰了脂肪酶的空间构象,解锁了活性中心,增强了其开放构象的稳定性,使底物更容易进入催化位点。因此吐温-20生物印迹Lipozyme 435在酶促合成MLCT中表现出优异的适用性、高效率和可重复使用性,证明了其是一种有效的工业应用生物催化剂。
2.5 脂肪酸组成
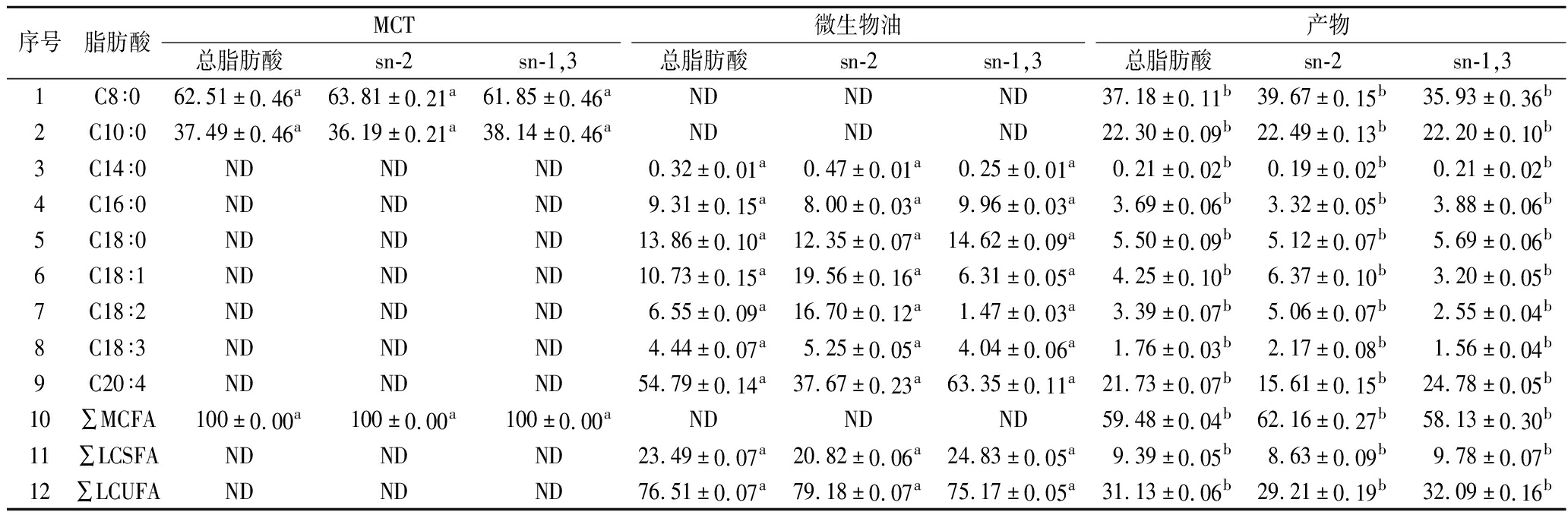
表4为BIL催化的MCT、微生物油及其酯化产物的脂肪酸组成(MCT/微生物油,摩尔比1.5∶1)。MCT主要由摩尔分数为62.51%的C8∶0和37.49%的C10∶0组成。微生物油中脂肪酸完全由LCFA组成,其中长链不饱和脂肪酸(long-chain unsaturated fatty acids,LCUFA)含量的摩尔分数最高,占76.51%,长链饱和脂肪酸(long-chain saturated fatty acids,LCSFA)含量的摩尔分数为23.49%。LCFA在sn-2和sn-1,3位置的分布无显著差异。与微生物油相比,产物中引入了MCFA,其总含量的摩尔分数占59.48%,其中sn-2位置的MCFA含量的摩尔分数为62.16%,高于sn-1,3位置的58.13%。在最终产物的LCFA中,C20∶4的含量的摩尔分数最高,为21.73%,sn-2 C20∶4的含量的摩尔分数为15.61%,低于sn-1,3位的24.78%。其他LCUFA(C18∶1、C18∶2、C18∶3)的含量的摩尔分数为9.4%,其中sn-2位置的含量的摩尔分数为13.6%,约为sn-1,3位置的2倍。
表4 MCT、微生物油及产物的脂肪酸组成(摩尔分数)
Table 4 The fatty acid composition of MCT, microbial oil and product (molar fraction)
序号脂肪酸MCT微生物油产物总脂肪酸sn-2sn-1,3总脂肪酸sn-2sn-1,3总脂肪酸sn-2sn-1,31C8∶062.51±0.46a63.81±0.21a61.85±0.46aNDNDND37.18±0.11b39.67±0.15b35.93±0.36b2C10∶037.49±0.46a36.19±0.21a38.14±0.46aNDNDND22.30±0.09b22.49±0.13b22.20±0.10b3C14∶0NDNDND0.32±0.01a0.47±0.01a0.25±0.01a0.21±0.02b0.19±0.02b0.21±0.02b4C16∶0NDNDND9.31±0.15a8.00±0.03a9.96±0.03a3.69±0.06b3.32±0.05b3.88±0.06b5C18∶0NDNDND13.86±0.10a12.35±0.07a14.62±0.09a5.50±0.09b5.12±0.07b5.69±0.06b6C18∶1NDNDND10.73±0.15a19.56±0.16a6.31±0.05a4.25±0.10b6.37±0.10b3.20±0.05b7C18∶2NDNDND6.55±0.09a16.70±0.12a1.47±0.03a3.39±0.07b5.06±0.07b2.55±0.04b8C18∶3NDNDND4.44±0.07a5.25±0.05a4.04±0.06a1.76±0.03b2.17±0.08b1.56±0.04b9C20∶4NDNDND54.79±0.14a37.67±0.23a63.35±0.11a21.73±0.07b15.61±0.15b24.78±0.05b10∑MCFA100±0.00a100±0.00a100±0.00aNDNDND59.48±0.04b62.16±0.27b58.13±0.30b11∑LCSFANDNDND23.49±0.07a20.82±0.06a24.83±0.05a9.39±0.05b8.63±0.09b9.78±0.07b12∑LCUFANDNDND76.51±0.07a79.18±0.07a75.17±0.05a31.13±0.06b29.21±0.19b32.09±0.16b
注:∑MCFA表示中链脂肪酸总量,∑LCSFA表示长链饱和脂肪酸总量,∑LCUFA表示长链不饱和脂肪酸总量。ND表示未检测到;同一行数值上不同小写字母表示数据之间差异显著(P<0.05);在底物摩尔比1.5∶1(MCT/微生物油,温度70 ℃,反应时间6 h的条件下,以BIL(质量分数为6%)为催化剂制备最终产物;sn-1,3位置的面积百分比计算为(3T-sn-2)/2,其中T表示总脂肪酸含量。
3 结论
本研究以BIL为催化剂,通过MCT与微生物油的酯交换反应,高效合成了ARA型MLCT。经筛选,合成BIL的最佳条件为:Lipozyme 435为催化剂,吐温-20为生物印迹模板,表面活性剂质量浓度为50 mg/L,缓冲液pH值为7.0,初始活力提高1.36倍。通过单因素试验和正交试验确定合成ARA型MLCT的最佳条件为:脂肪酶添加量的质量分数为6%,温度70 ℃,底物摩尔比1.5∶1(MCT/微生物油),反应时间6 h。在此条件下,产物MCT的质量分数为13.12%,MLCT的质量分数为66.80%,LCT的质量分数为20.08%。其中,位于sn-1,3位的MCFA的摩尔分数为58.13%,位于sn-2位的ARA的摩尔分数为15.61%。BIL经7次使用后,MLCT的质量分数仍保持61.05%,与未生物印迹的脂肪酶相比具有更好的重复使用稳定性。此油脂提升了ARA的生物利用率,可应用于功能性食品和营养保健品中。
[1] GARG P, PEJAVER R K, SUKHIJA M, et al.Role of DHA, ARA, &phospholipids in brain development:An Indian perspective[J].Clinical Epidemiology and Global Health, 2017, 5(4):155-162.
[2] BOURLIEU C, MÉNARD O, BOUZERZOUR K, et al.Specificity of infant digestive conditions:Some clues for developing relevant in vitro models[J].Critical Reviews in Food Science and Nutrition, 2014, 54(11):1427-1457.
[3] YUHAS R, PRAMUK K, LIEN E L.Human milk fatty acid composition from nine countries varies most in DHA[J].Lipids, 2006, 41(9):851-858.
[4] ABRAHAMSE E, MINEKUS M, VAN AKEN G A, et al.Development of the digestive system:Experimental challenges and approaches of infant lipid digestion[J].Food Digestion, 2012, 3(1):63-77.
[5] LEE Y Y, TANG T K, CHAN E S, et al.Medium chain triglyceride and medium-and long chain triglyceride:Metabolism, production, health impacts and its applications - a review[J].Critical Reviews in Food Science and Nutrition, 2022, 62(15):4169-4185.
[6] AOYAMA T, NOSAKA N, KASAI M.Research on the nutritional characteristics of medium-chain fatty acids[J].The Journal of Medical Investigation, 2007, 54(3-4):385-388.
[7] YUAN T L, WEI W, ZHANG X H, et al.Medium- and long-chain triacylglycerols composition in preterm and full-term human milk across different lactation stages[J].LWT, 2021, 142:110907.
[8] AKRAM F, FATIMA T, UL HAQ I.Auto-induction, biochemical characterization and application of a novel thermo-alkaline and detergent-stable lipase (S9 peptidase domain) from Thermotoga petrophila as cleaning additive and degrading oil/fat wastes[J].Bioorganic Chemistry, 2024, 151:107658.
[9] ZOU X Q, SU H, ZHANG F C, et al.Bioimprinted lipase-catalyzed synthesis of medium- and long-chain structured lipids rich in docosahexaenoic acid for infant formula[J].Food Chemistry, 2023, 424:136450.
[10] CHENG C, JIANG T Y, WU Y L, et al.Elucidation of lid open and orientation of lipase activated in interfacial activation by amphiphilic environment[J].International Journal of Biological Macromolecules, 2018, 119:1211-1217.
[11] ZHU Y T, FENG Y H, WANG J W, et al.Selective esterification design of lipases for TAG synthesis based on the unique structure of curved DHA[J].ACS Food Science &Technology, 2024, 4(7):1722-1730.
[12] BILAL M, ZHAO Y P, NOREEN S, et al.Modifying bio-catalytic properties of enzymes for efficient biocatalysis:A review from immobilization strategies viewpoint[J].Biocatalysis and Biotransformation, 2019, 37(3):159-182.
[13] DE S BRAND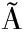 O L M, BARBOSA M S, SOUZA R L, et al.Lipase activation by molecular bioimprinting:The role of interactions between fatty acids and enzyme active site[J].Biotechnology Progress, 2021, 37(1):e3064.
O L M, BARBOSA M S, SOUZA R L, et al.Lipase activation by molecular bioimprinting:The role of interactions between fatty acids and enzyme active site[J].Biotechnology Progress, 2021, 37(1):e3064.
[14] FISHMAN A, COGAN U.Bio-imprinting of lipases with fatty acids[J].Journal of Molecular Catalysis B:Enzymatic, 2003, 22(3-4):193-202.
[15] OTZEN D E.Protein unfolding in detergents:Effect of micelle structure, ionic strength, pH, and temperature[J].Biophysical Journal, 2002, 83(4):2219-2230.
[16] OTZEN D E, OLIVEBERG M.Burst-phase expansion of native protein prior to global unfolding in SDS1[J].Journal of Molecular Biology, 2002, 315(5):1231-1240.
[17] ZOU X Q, HUANG J H, JIN Q Z, et al.Preparation of human milk fat substitutes from palm stearin with arachidonic and docosahexaenoic acid:Combination of enzymatic and physical methods[J].Journal of Agricultural and Food Chemistry, 2012, 60(37):9415-9423.
[18] XU X, BALCHEN S, HØY C E, et al.Production of specific-structured lipids by enzymatic interesterification in a pilot continuous enzyme bed reactor[J].Journal of the American Oil Chemists’ Society, 1998, 75(11):1573-1579.
[19] AMENAGHAWON A N, ESHIEMOGIE S A, EVBARUNEGBE N I, et al.Surfactant-facilitated metabolic induction enhances lipase production from an optimally formulated waste-derived substrate mix using Aspergillus niger:A case of machine learning modeling and metaheuristic optimization[J].Bioresource Technology Reports, 2024, 28:101993.
[20] CARRASCO-L PEZ C, GODOY C, DE LAS RIVAS B, et al.Activation of bacterial thermoalkalophilic lipases is spurred by dramatic structural rearrangements[J].Journal of Biological Chemistry, 2009, 284(7):4365-4372.
PEZ C, GODOY C, DE LAS RIVAS B, et al.Activation of bacterial thermoalkalophilic lipases is spurred by dramatic structural rearrangements[J].Journal of Biological Chemistry, 2009, 284(7):4365-4372.
[21] ROCHA S, RUFINO A T, FREITAS M, et al.Methodologies for assessing pancreatic lipase catalytic activity:A review[J].Critical Reviews in Analytical Chemistry, 2024, 54(8):3038-3065.
[22] YANG T K, XU X B, HE C, et al.Lipase-catalyzed modification of lard to produce human milk fat substitutes[J].Food Chemistry, 2003, 80(4):473-481.
[23] XIE W L, ZHANG C.Propylsulfonic and arenesulfonic functionalized SBA-15 silica as an efficient and reusable catalyst for the acidolysis of soybean oil with medium-chain fatty acids[J].Food Chemistry, 2016, 211:74-82.
[24] ZOU X Q, KHAN I, WANG Y X, et al.Preparation of medium- and long-chain triacylglycerols rich in n-3 polyunsaturated fatty acids by bio-imprinted lipase-catalyzed interesterification[J].Food Chemistry, 2024, 455:139907.
[25] HE Y J, QIU C Y, GUO Z, et al.Production of new human milk fat substitutes by enzymatic acidolysis of microalgae oils from Nannochloropsis oculata and Isochrysis galbana[J].Bioresource Technology, 2017, 238:129-138.