甜味剂作为增加甜度和口感的食品添加剂[1],其发展正从传统蔗糖向健康化、功能化方向转变[2]。甜菊糖是存在于甜叶菊中的一种二萜糖苷类物质[3],是一种具有高甜度(蔗糖的250~300倍)、低热量(蔗糖的1/300)、耐热、稳定、易溶解等优点的非营养型天然甜味剂[4]。甜菊糖逐渐成为替代蔗糖的理想选择,满足了控糖与健康饮食需求。目前广泛应用的甜菊苷(stevioside,ST)和莱鲍迪苷A(Rebaudioside A,Reb A)虽生产技术成熟,但因甜度较低且伴有苦涩后味而应用受限。相比之下,莱鲍迪苷D(Rebaudioside D,Reb D)口感更优,但天然含量极低,传统分离技术难以满足规模化需求。此外,Reb D也是合成更高附加值产物莱鲍迪苷M(Rebaudioside M,Reb M)的关键中间体。随着编码甜菊糖苷生物合成的基因已被鉴定,利用微生物异源表达体系实现Reb D的高效合成,这不仅解决了天然提取瓶颈,还通过生物催化技术推动了甜菊糖苷产业的升级,兼具科学价值与商业化潜力。
随着对甜菊糖苷生物合成路径研究的深入,Reb D的生物合成路径也被解析,主要分为以Reb A和莱鲍迪苷E(Rebaudioside E,Reb E)为底物的2种途径。多项研究表明,酶工程技术可显著提升甜菊糖苷Reb D的合成效率。马媛媛等[5]利用糖基转移酶StUGT构建重组蛋白,以尿苷二磷酸葡萄糖(uridine diphosphate-glucose,UDPG)为糖基供体催化Reb A生成Reb D,在18 ℃反应36 h后转化率达90%以上。LIN等[6]通过计算辅助设计优化葡萄糖基转移酶EUGT11结构,获得单一变异体M2(F379A),催化效率较野生型提升2.18倍。CHEN等[7]开发甜菊糖苷UDP-糖基转移酶UGT76G1、番茄UGTSL2和马铃薯StSUS1的多酶反应体系,实现了甜菊糖苷两步糖基化反应合成Reb D,并通过Asn358Phe突变使Reb D产量提高1.6倍。WANG等[8]在毕赤酵母中异源表达水稻EUGT11,采用两步温度控制策略(28 ℃/35 ℃),将Reb A向Reb D的转化率从62.41%提升至95.31%。此外,OLSSON等[9]证实UGT76G1可催化Reb E转化为Reb D,并通过定点突变使催化活性显著提升。上述研究为Reb D的高效生物合成提供了酶定向改造、多酶协同及工艺优化的系统性策略。
生物酶定向催化法可以以绿色环保的方式获得高浓度的目标产物。大肠杆菌表达重组糖基转移酶能催化Reb A生成Reb D,但其表达水平和催化能力较低,需要后续实验进一步提升。此外,微生物体内UDPG库有限,UDP-葡萄糖醛酸转移酶(uridinediphosphate-glucuronosyltransferase,UGTs)催化需消耗UDPG,可通过构建UDPG再生系统缓解。本研究选取双启动子质粒pETDuet-1,在其多克隆位点插入葡萄糖基转移酶EUGT11和蔗糖合成酶AtSUS3基因,建立重组表达质粒,之后转入大肠杆菌E.coli BL21(DE3),经IPTG诱导,实现生物催化体系UDPG的原位再生,从而实现Reb D的生物合成。在此基础上,探究反应体系温度、底物配比、反应时间等因素对Reb D合成的影响,以期为生物合成Reb D奠定基础。
1 材料与方法
1.1 材料与试剂
Reb A、Reb D、氨苄青霉素,上海源叶生物科技有限公司;载体pETDuet-1,美国Novagen公司;限制性内切酶BamH I、限制性内切酶Hind Ⅲ、T4 DNA连接酶,New England Biolabs公司;0.22 μm有机滤器、0.22 μm水系滤器,北京天林恒泰科技有限公司;1 mL一次性注射器,赛默飞世尔科技有限公司;色谱级乙腈,德国默克集团;十二烷基硫酸钠(sodium dodecyl sulfate,SDS)、SDS-PAGE蛋白上样缓冲液(2×),北京索莱宝科技有限公司;考马斯亮蓝快速染色液,上海碧云天生物技术有限公司;其他试剂均为国产分析纯。
1.2 仪器与设备
NanoDrop 2000核酸定量仪、TSX600超低温冰箱、MicroCL Fresco低温高速离心机,赛默飞世尔科技有限公司;HZ-A水浴恒温振荡器,上海博讯实业有限公司;MLS-3780高压蒸汽灭菌锅,济南欧莱博科学仪器有限公司;PHS-25型pH计,奥豪斯国际贸易(上海)有限公司;SW-CJ-280S超净工作台,英国Malvern公司;Mini-ProteanⅡ型电泳仪、S1000PCR扩增仪、GelDocTM EZ凝胶成像系统,美国伯乐公司;SpectraMax 13连续波长多功能酶标仪,美国Molecular Devices公司;THZ-300C恒温培养摇床,上海一恒科技有限公司;SCIENTZ-950E超声细胞破碎仪,宁波洛尚智能科技有限公司;LC-20高效液相色谱分析仪,日本岛津公司;HH-4恒温水浴锅,常州天瑞仪器有限公司;H2500R-2常温高速离心机,美国SIGMA公司。
1.3 实验方法
1.3.1 共表达EUGT11与AtSUS3重组质粒的构建
根据GenBank数据库中水稻来源的葡萄糖基转移酶EUGT11基因序列(Accession No.AK121682),设计PCR扩增引物,上下游引物分别引入BamH I和Hind Ⅲ位点。引物序列分别为:F:5′-CGCGGATCCATGGACTCCGGCTACTCCTCC-3′和R:5′-CCCAAG-CTTTCAATCCTTGTAAGATCTCAATTGC-3′。随后以水稻cDNA为模板进行PCR扩增,条件为:98 ℃预变性3 min,98 ℃变性10 s、55 ℃退火15 s、72 ℃延伸30 s, 循环30次,72 ℃延伸10 min。将纯化后的PCR产物(EUGT11片段)与表达载体pETDuet-1分别用BamH I和Hind Ⅲ双酶切,回收目的片段后用T4连接酶于16 ℃连接,获得重组质粒pETDuet-EUGT11。通过NCBI数据库查询拟南芥来源的蔗糖合成酶AtSUS3氨基酸序列,送至北京六合华大基因科技有限公司全基因合成得到质粒pETDuet-1-AtSUS3。根据NCBI上AtSUS3(NM_116461.3)的开放阅读框240~2 669 bp序列以及拟插入载体pETDuet1P2下游Fse I-Kpn I位置两端的序列设计引物对,F:5′-TCAATTGGATATCGGCCGGCCAGATGGCAAACCCTA-AGCTCA-3′,R:5′-CTTTACCAGACTCGAGGGTACCTCAGTCATCGGCGGTTGA-3′,以pETDuet-1-AtSUS3为模板进行PCR,反应条件同上。PCR结束后对产物进行电泳并切胶回收。采用Infusion法将纯化后的PCR产物克隆至质粒pETDuet-EUGT11,最终获得重组质粒pETDuet-1-EUGT11-AtSUS3。
1.3.2 重组质粒的转化
从-80 ℃超低温冰箱中取出大肠杆菌感受态细胞冰浴解冻,加入1~2 μL重组质粒,冰浴孵育30 min。随后42 ℃水浴热激90 s,立即冰浴冷却3~5 min。加入800 μL无抗性的LB培养基轻轻混匀,37 ℃、200 r/min振荡培养1 h。5 000 r/min离心5 min收集菌体,重悬后涂布于含氨苄抗菌素的固体LB平板,37 ℃恒温培养箱倒置培养12 h,挑取单菌落培养送往北京六合华大基因科技有限公司进行测序,阳性突变菌株制备甘油管保存于-80 ℃冰箱。
1.3.3 葡萄糖基转移酶和蔗糖合成酶的表达优化
将经过鉴定的含重组质粒的阳性菌株E.coli BL21(DE3)接种于5 mL含100 μg/mL氨苄青霉素的LB液体培养基中,于37 ℃、150 r/min培养16 h。取1 mL培养物,转接至装有50 mL含100 μg/mL氨苄青霉素的LB培养基的250 mL摇瓶中,37 ℃、150 r/min下振荡培养10 h,作为种子液。
将种子液以2.0%的接种量接种至装有含100 μg/mL氨苄青霉素的LB培养基,37 ℃、150 r/min培养2 h后,分别加入0.1、0.4、1 mmol/L的IPTG,在16、20、25 ℃,150 r/min条件下诱导培养16 h。高速离心得到菌体,用磷酸盐缓冲液洗涤2次,随后于-20 ℃冰箱中保存备用。
1.3.4 粗酶液的制备
取发酵液在10 000 r/min、4 ℃下离心20 min,弃上清液收集菌体,用100 mmol/L pH 7.0 Na2PO4缓冲液洗涤菌体2次并重悬菌体,超声波破碎30 min(250 W,工作1 s,停顿1 s)。细胞破碎液在12 000 r/min,低温离心10 min,收集上清液随后于-20 ℃冰箱中保存备用。
1.3.5 SDS-PAGE分析
取20 μL样品与等体积的2×上样缓冲液混匀,沸水浴中加热10 min使蛋白充分变性,待冷却后,12 000 r/min离心10 min去除不溶物。取10 μL蛋白样品上样于质量分数为12%的分离胶,于80 V恒压电泳30 min至样品完全进入分离胶,再于120 V的条件下进行电泳至溴酚蓝指示剂迁移至胶底。切去浓缩胶,使用考马斯亮蓝R-250染色60 min,弃去染色液,经水漂洗后振荡脱色至出现清晰的蛋白条带。
1.3.6 粗酶液蛋白浓度的测定
使用BCA蛋白定量试剂盒测定菌株粗酶液的蛋白浓度。用PBS将牛血清白蛋白(bovine serum albumin,BSA)标准品稀释为500 μg/mL,将BCA Solution与BCA Solution B按50∶1的比例稀释成工作液,按照试剂盒说明建立蛋白质标准曲线(y=0.903 2x+0.107 9,R2=0.999 9)。粗酶液经适当稀释后,取20 μL 与BCA工作液混合,37 ℃孵育30 min,酶标仪562 nm检测吸光值,通过标准曲线计算蛋白浓度。
1.3.7 HPLC分析
使用岛津液相色谱系统,配备INERTSIL ODS-SP C18色谱柱(4.6 mm×250 mm,5 μm),流动相为A(1.38 g/L NaH2PO4缓冲液,pH 2.6)∶B(乙腈)=68∶32(体积比),采用等度洗脱,进样量10 μL,柱温40 ℃,流速1 mL/min,紫外检测波长210 nm。以Reb A和Reb D为标准品,建立外标法标准曲线,Reb A浓度与峰面积的回归方程为:y=2 735.9x+12 253(R2=0.995 2),Reb D浓度与峰面积的回归方程为:y=2 197.7x+13 754(R2=0.999)。利用标准曲线确定样品中Reb A和Reb D的含量。
1.3.8 酶活性测定
糖基转移酶活性测定:总酶促反应体系为200 μL,含有100 mmol/L NaH2PO4-Na2HPO4缓冲液(pH 7.0)、1 mg粗酶蛋白、1 mmol/L底物Reb A、2 mmol/L UDPG和3 mmol/L MgCl2。30 ℃条件下进行孵育,每隔30 min进行取样,样品随后于95 ℃加热10 min,超纯水稀释10倍,离心取上清液,并利用0.22 μmol/L水系滤膜过滤,经HPLC检测对Reb A和Reb D进行定性定量分析。糖基转移酶活性(U)定义为每分钟从Reb A产生1 μmol Reb D所需的酶量。
蔗糖合成酶的活性测定:总酶促反应体系为3 mL,含有100 mmol/L NaH2PO4-Na2HPO4缓冲液(pH 7.0)、1 mg粗酶蛋白、500 mmol/L蔗糖和10 mmol/L尿苷二磷酸(uridine diphosphate,UDP)。30 ℃条件下进行孵育,每小时取出样品在95 ℃下加热10 min,离心取上清液,并采用DNS法测定蔗糖合成酶活性[10]。蔗糖合成酶活性的一个单位定义为在给定测定条件下每分钟释放1 μmol还原糖的酶的量。
1.3.9 糖基化偶联反应条件的优化
采用3 mL反应体系,含100 mmol/L磷酸盐缓冲液(pH 7.0)、1.2 g/L Reb A、蔗糖、粗酶提取物、3 mmol/L MgCl2和体积分数为5%的二甲基亚砜(dimethyl sulfoxide,DMSO)溶液,分别考察:底物配比(Reb A∶蔗糖 = 1∶10~1∶75)、温度(20~45 ℃)、酶质量浓度(0.6~3.0 mg/mL)、时间(0~25 h)对Reb D产率的影响。反应均以95 ℃加热10 min终止,经10 000 r/min离心5 min、0.22 μm滤膜过滤后,HPLC检测Reb D产率,计算如公式(1)所示:
RebD产率![]()
(1)
1.4 统计分析
采用SPSS 30.0软件包进行显著性分析,实验结果以“平均值±标准偏差”表示。所有实验设定3个平行。组间数据比较用单因素方差分析(Duncan法),P<0.05表示有显著性差异。使用Origin 2024软件绘图。
2 结果与分析
2.1 重组质粒的构建及目的蛋白表达验证
将构建成功的重组质粒pETDuet-1-EUGT11-AtSUS3通过化学法转入E.coli BL21(DE3)中,经IPTG诱导表达后,离心收集菌体沉淀,以100 mmol/L pH 7.0 Na2PO4缓冲液漂洗数次后重悬,超声波破碎20 min,进行SDS-PAGE分析。不同培养温度经不同浓度IPTG诱导表达的结果如图1所示。经IPTG诱导的糖基转移酶EUGT11表达分子质量大小为51 kDa,蔗糖合成酶AtSUS3表达分子质量大小为92 kDa,大小均与理论分子质量相符,证明成功构建了表达载体及重组葡萄糖基转移酶和蔗糖合成酶基因工程菌。
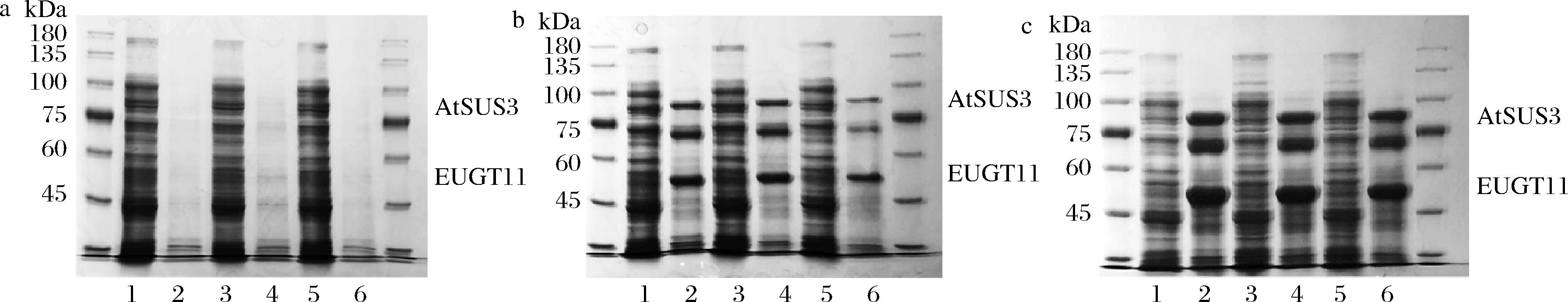
M为蛋白质分子质量标记;条带1为0.1 mmol/L IPTG的菌体上清液;条带2为0.1 mmol/L IPTG的菌体沉淀;条带3为0.4 mmol/L IPTG的菌体上清液;条带4为0.4 mmol/L IPTG的菌体沉淀;条带5为1 mmol/L IPTG的菌体上清液;条带6为1 mmol/L IPTG的菌体沉淀。
a-培养温度16 ℃;b-培养温度20 ℃;c-培养温度25 ℃
图1 重组蛋白的SDS-PAGE分析
Fig.1 SDS-PAGE analysis of recombinant proteins
2.2 IPTG诱导条件对目的蛋白表达的影响
如图1所示,不同终浓度的IPTG诱导剂对目的蛋白表达影响无显著性差异。在较低温度时,目的基因诱导表达量相对较低,随着温度的升高,沉淀中目的蛋白表达量增加,但上清液中的目的蛋白表达仍不明显。这可能是因为在大肠杆菌中原核表达真核蛋白时,翻译几乎与转录同时发生,且缺乏翻译后修饰系统,导致许多蛋白质尤其是真核蛋白质,形成不受欢迎的聚集体(包涵体),限制了活性重组蛋白的生成[11]。本研究发现植物源葡萄糖基转移酶EUGT11和蔗糖合成酶AtSUS3在大肠杆菌中的表达主要以不溶性包涵体形式存在,可溶性蛋白质含量极低。然而,获得的重组蛋白EUGT11-AtSUS3仍具有催化合成Reb D的活性,因此后续实验采用粗酶体系催化合成Reb D。
2.3 不同诱导温度对酶活性的影响
如图2所示,随着诱导温度的增加,葡萄糖基转移酶EUGT11与蔗糖合成酶AtSUS3的酶活性呈现先增加后降低的趋势。当诱导温度为20 ℃时,葡萄糖基转移酶EUGT11与蔗糖合成酶AtSUS3的酶活性最高,分别为13.33 U/mg和39.17 U/mg。当温度持续升高到25 ℃时,两者的酶活性分别降低到7.86 U/mg和26.87 U/mg,当诱导温度为30 ℃时,两者的酶活性分别为6.99 U/mg和25.66 U/mg,这是由于高温诱导使菌体生长过快,导致菌体内形成了包涵体[12]。包涵体与胞质内蛋白质生成速率有关,当温度较高时菌体生长迅速,体系新生成的多肽浓度高,缺少合适的时间充分折叠,从而形成非结晶、无定形的蛋白质的聚集体[13]。基于上述结果,后续实验选用在20 ℃的条件下进行诱导表达,以确保酶活性最大化。
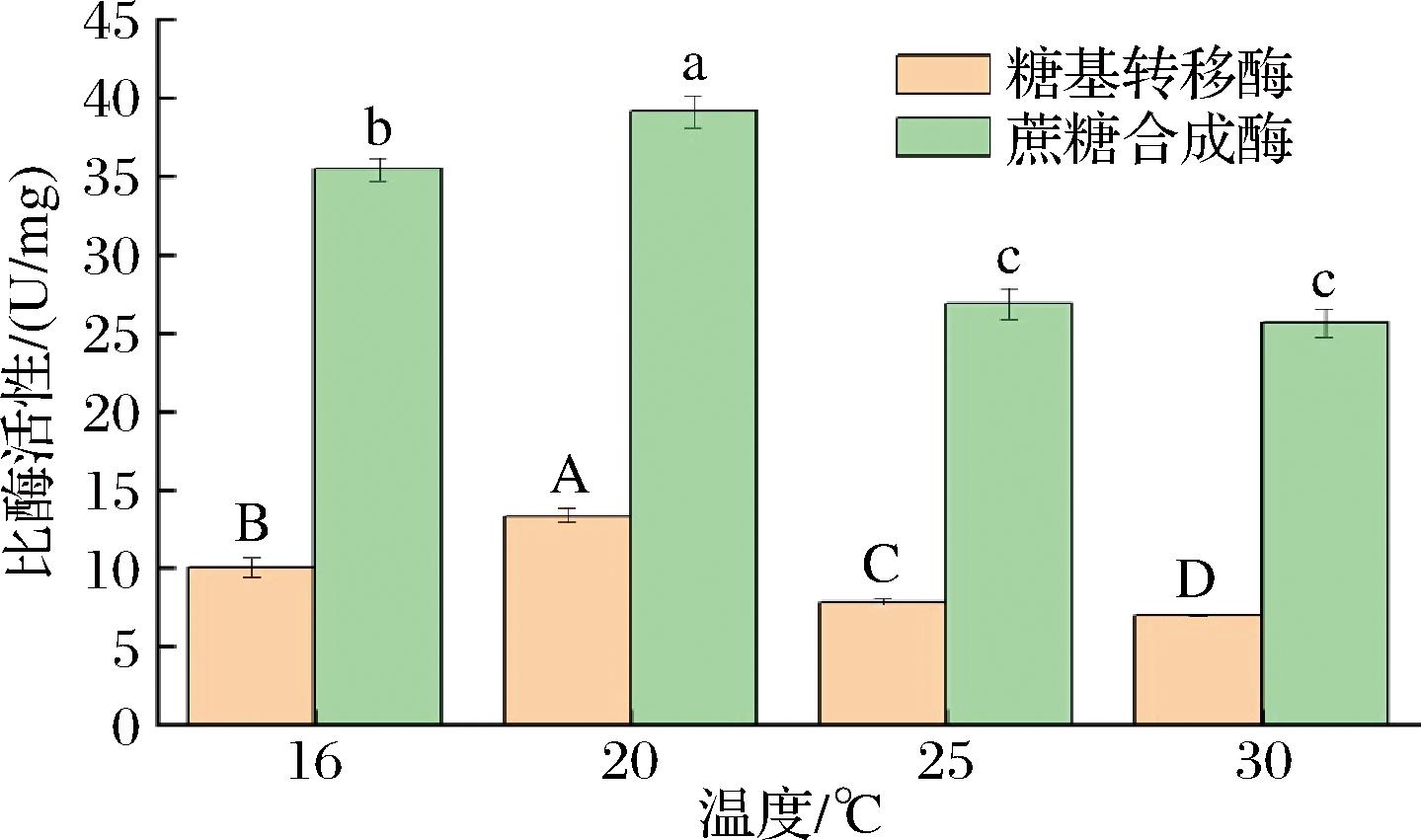
图2 诱导温度对体系葡萄糖基转移酶EUGT11与蔗糖合成酶AtSUS3酶活性的影响
Fig.2 Impact of induction temperature on the enzyme activity of glucosyltransferase EUGT11 and sucrose synthase AtSUS3 within the system
注:不同字母表示差异显著(P<0.05)(下同)。
2.4 双酶催化合成Reb D条件的确定
2.4.1 Reb A与蔗糖配比对糖基偶联反应的影响
当UDPG作为转糖基化的直接糖供体时,反应体系中较高的UDPG浓度虽然有利于产物UDP的积累,但会降低其循环效率,可能是由于高浓度的UDP对葡萄糖基转移酶的抑制作用[14]。由于UDPG价格昂贵,而且在转糖基化反应系统的粗提物中含有UDPG 和UDP。因此,级联反应体系中既无需额外添加UDPG和UDP,只需添加底物Reb A和蔗糖。如图3所示,当底物配比为1∶10时,Reb D的产率仅为50.20%,18 h后,反应液中仍有652.22 mg/L的Reb A残留。随着蔗糖浓度的增加,Reb D的产量不断提高。当底物配比提高到1∶50和1∶75时,Reb D生成量达到最大值868.33 mg/L,对应Reb D的产率为61.97%。结果表明,增加Reb A与蔗糖的比例可以促进Reb D的生成,且最适配比为1∶50。
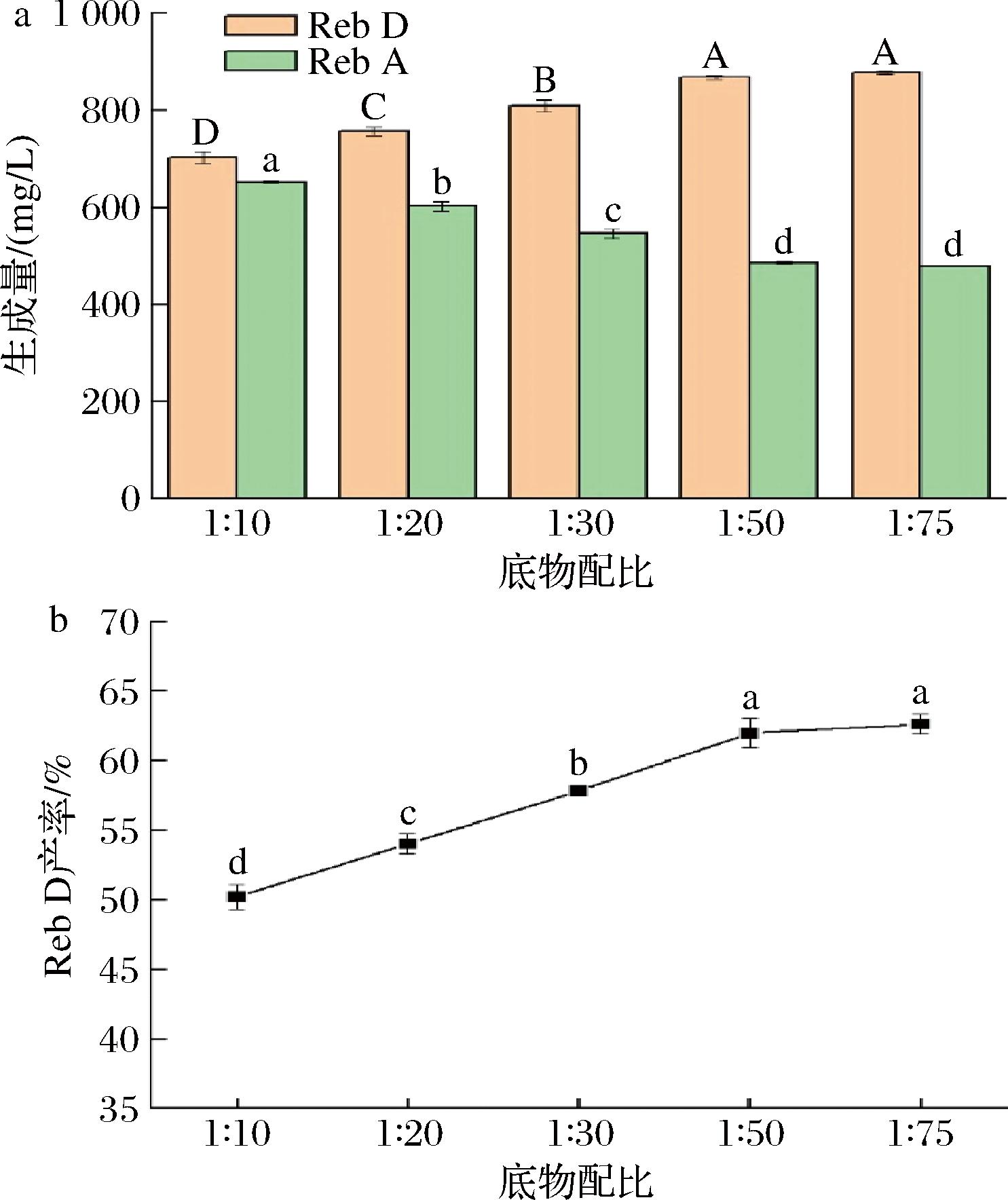
a-生成量;b-Reb D产率
图3 Reb A与蔗糖底物配比对糖基偶联反应的影响
Fig.3 Effect of substrate ratio on glycosyl coupling reaction
注:图3-a中,不同大写字母表示Reb D产量差异显著,不同小写字母表示Reb A产量差异显著(P<0.05);图3-b中,不同小写字母表示Reb D产率差异显著(P<0.05)(下同)。
2.4.2 反应温度对糖基偶联反应的影响
在酶促反应中,反应温度是影响Reb D合成的关键因素。温度不仅影响酶的活性,还影响底物和供体分子的运动能力。当温度较低时,酶催化活力较低,而且分子布朗运动较弱;随着温度的升高,酶活力增强,活化分子数增多,但是酶的相对稳定性可能会降低[13-14]。如图4所示,当温度为20 ℃时,低温使酶的活性受到限制,体系反应速度较慢,反应18 h后仍有823.31 mg/L的Reb A未反应,且Reb D的产率为37.4%。相应地,随着温度的升高,Reb D的产率不断提高。当温度达到30 ℃时,Reb D的产率为64.59%。然而,当温度上升到45 ℃时,Reb D的产率降至44.34%,这可能是由于温度升高影响了酶的活性[15]。实验结果表明,糖基转移酶EUGT11和蔗糖合成酶AtSUS3偶联合成Reb D反应体系的最适温度为30 ℃。
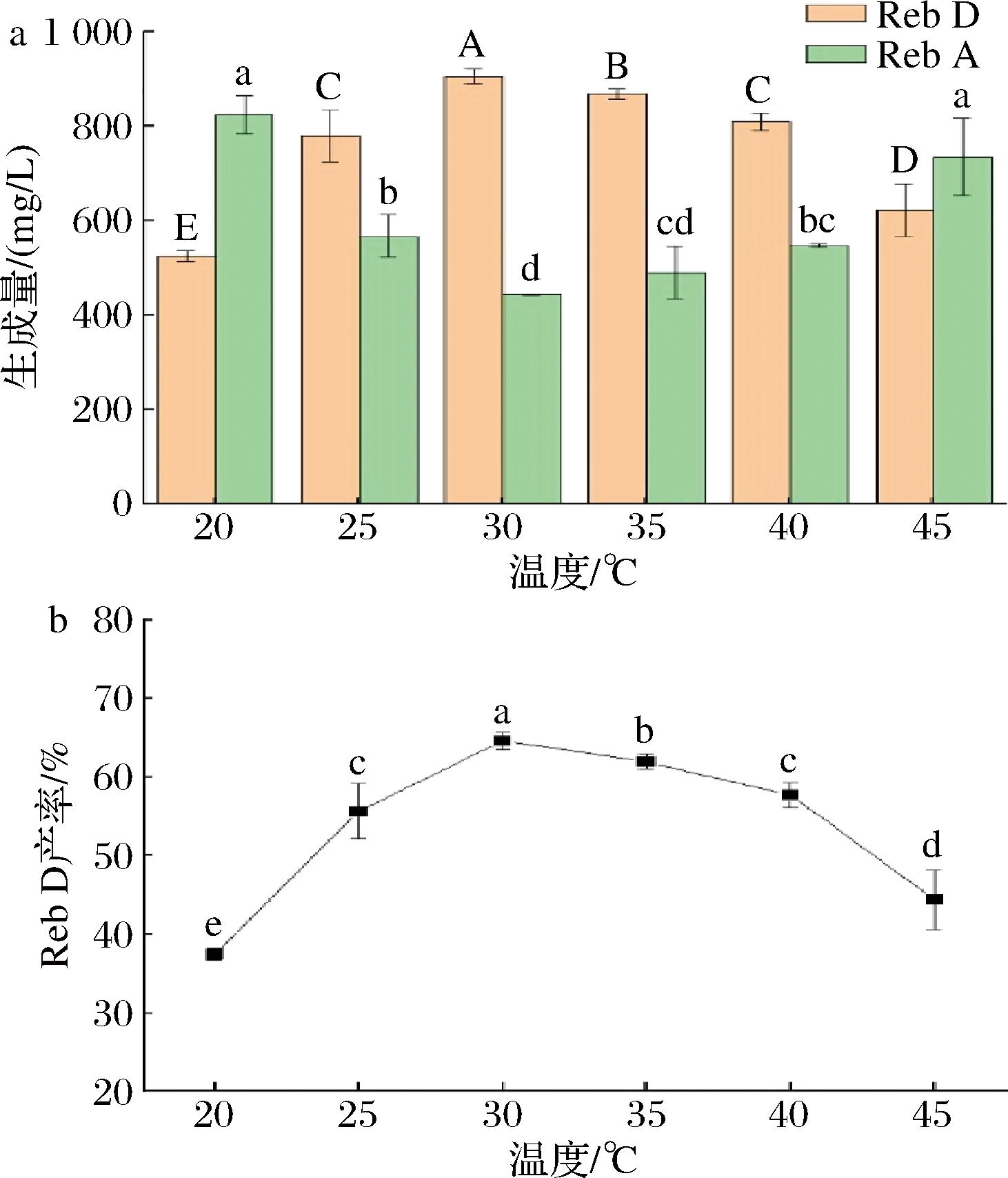
a-生成量;b-Reb D产率
图4 反应温度对糖基偶联反应的影响
Fig.4 Effect of reaction temperature on glycosyl coupling reaction
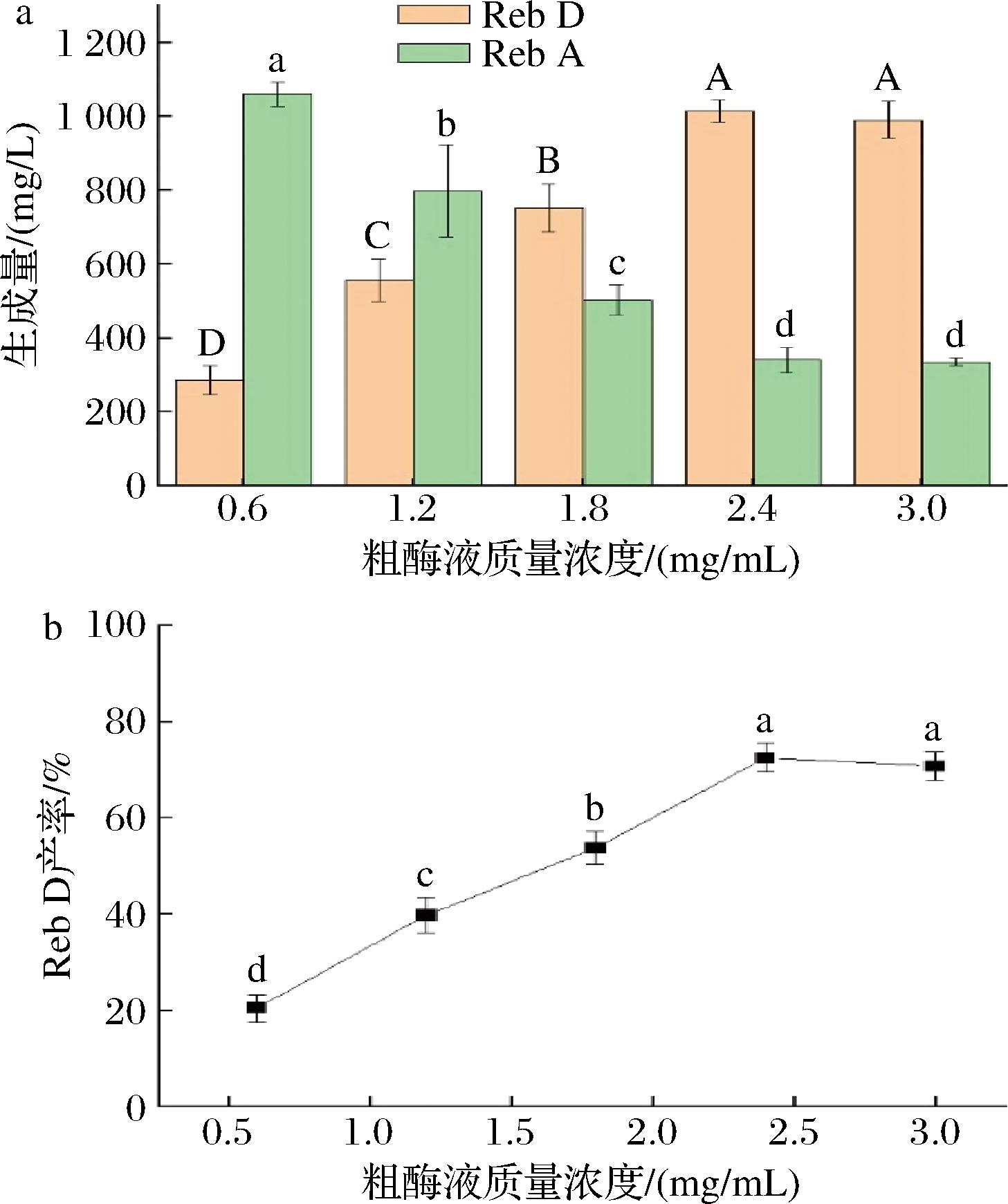
a-生成量;b-Reb D产率
图5 粗酶液浓度对糖基偶联反应的影响
Fig.5 Effect of concentration of crude enzyme solution on glycosyl-conjugation
2.4.3 粗酶液质量浓度对糖基偶联反应的影响
菌体粗酶液中不仅含有2种重组酶糖基转移酶EUGT11和蔗糖合成酶AtSUS3,还含有生物催化所需的辅助因子UDPG和UDP,因此研究粗酶液浓度对Reb D合成的影响具有重要意义[16]。如图5所示,当粗酶液质量浓度为0.6 mg/mL时,反应18 h后Reb D生成量为286.03 mg/L,Reb D的产率仅为20.41%。随着粗酶液质量浓度持续提高至2.4 mg/mL时,Reb D生成量持续增加至1 014.56 mg/L,相应的产率最高达到72.40%。这是因为在一定范围内,菌体粗酶液质量浓度的增加使得反应体系中单位体积中酶蛋白量增多,反应转化率提高。因此,确定糖基转移酶和蔗糖合酶偶联反应中的粗酶液质量浓度为2.4 mg/mL。
2.4.4 反应时间对糖基偶联反应体系合成Reb D的影响
如图6所示,当底物配比为1∶50,粗酶液质量浓度为2.4 mg/mL,反应体系在30 ℃下进行时,随着反应时间的持续进行,Reb D产量不断积累。在反应最初的5 h时内,Reb D产量较低,产率仅为9.02%,此时Reb A大部分未被转化,体系中仍然有1 118.81 mg/L 的Reb A。随着时间的不断延长,Reb D的产量逐渐增加,至20 h时Reb D的产量达到最大值1 205.81 mg/L,Reb D的产率提高到86.06%。然而,当反应时间延长至25 h时,Reb D不再积累,这可能与底物耗尽、反应达到平衡、长时间反应酶活性降低或产物反馈抑制等因素有关[17]。因此,重组糖基转移酶EUGT11和蔗糖合成酶AtSUS3催化合成Reb D的最佳反应时间为20 h。
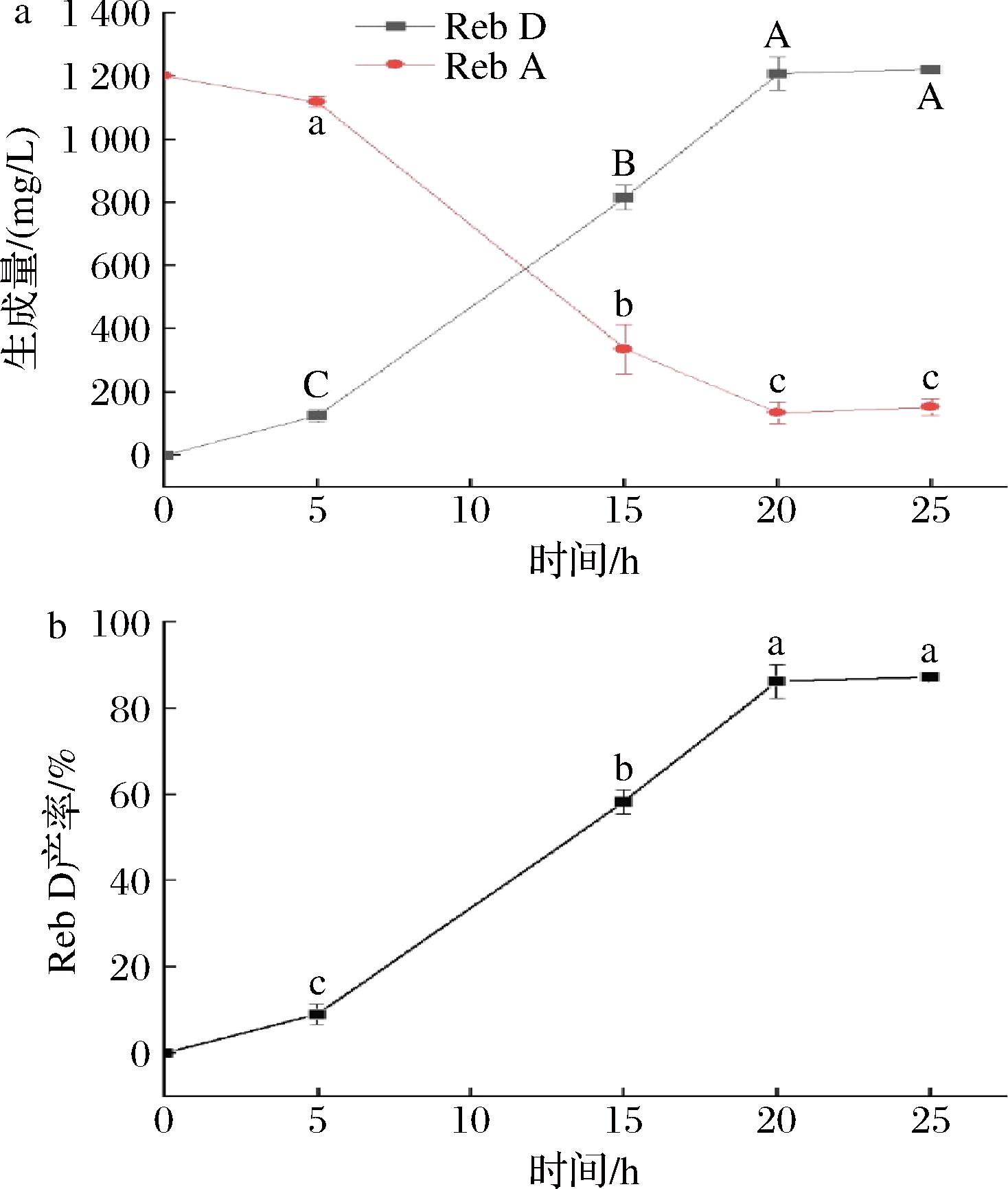
a-生成量;b-Reb D产率
图6 反应时间对糖基化偶联反应的影响
Fig.6 Effect of reaction time on glycosylation coupling reaction
WANG等[8]采用正交设计的一锅法优化Reb A合成Reb D,并开发了一种两步温度控制策略,在28 ℃/35 ℃下实现95.31%的转化率,而在28 ℃单步过程中的转化率为62.41%,为甜味剂生产提供了一种高效的全细胞生物催化剂技术。然而,该实验依赖昂贵的糖基配体UDPG,增加了反应成本。杨玉凤等[12]利用重组大肠杆菌全细胞催化1 mmol/L Reb A转化为0.1 mmol/L Reb D,其产率为10%。CHEN等[15]将龙葵的重组UDP-葡萄糖基转移酶 UGTSL2和来自马铃薯的蔗糖合酶StSUS1偶联,开发了Red D合成和UDPG循环的途径,20 h后从20 g/L Red A中获得17.4 g/L Reb D(产率为74.6%)。本研究借鉴上述方法,通过偶联葡萄糖基转移酶EUGT11和蔗糖合成酶AtSUS3基因,实现了Reb D合成和UDPG循环,评估反应参数,包括底物比例、蔗糖浓度、温度、粗提物浓度和反应时间,20 h后实现Reb D的产率为86.06%,为Reb D合成生产提供了参考基础。
3 结论
本研究构建了含水稻的糖基转移酶EUGT11在和拟南芥来源的蔗糖合成酶AtSUS3基因的重组大肠杆菌BL21(DE3)/ pETDuet-1-EUGT11-AtSUS3。通过摇瓶发酵重组大肠杆菌菌株产酶,外源添加重组酶至反应体系,建立了合成UDPG循环的新途径,形成生物催化级联反应体系,实现Reb A向Reb D的有效生物催化。考察了不同反应条件对催化反应的影响,在100 mmol/L NaH2PO4-Na2HPO4缓冲液(pH 7.0)体系中,含有2.4 mg/mL粗酶提取物,1.2 g/L Reb A和60 g/L蔗糖,30 ℃持续反应20 h,Reb D的产量达到1 205.81 mg/L,产率达到86.06%。本研究为绿色生物合成高附加值甜菊糖苷提供了可行方案。
[1] 励建荣, 蔡成岗.食品工业中甜味剂的应用[J].食品研究与开发, 2003, 24(4):18-21.
LI J R, CAI C G.The application of sweeteners in the food industry[J].Food Research and Development, 2003, 24(4):18-21.
[2] QU G Y, LIU Y F, MA Q Y, et al.Progress and prospects of natural glycoside sweetener biosynthesis:A review[J].Journal of Agricultural and Food Chemistry, 2023, 71(43):15926-15941.
[3] BRANDLE J E, STARRATT A N, GIJZEN M.Stevia rebaudiana:Its agricultural, biological, and chemical properties[J].Canadian Journal of Plant Science, 1998, 78(4):527-536.
[4] 杨旭艳, 路勇, 胡国华.新型天然高倍甜味剂—莱鲍迪苷A[J].中国食品添加剂, 2012, 23(S1):77-81.
YANG X Y, LU Y, HU G H.Research progress on rebaudioside A[J].China Food Additives, 2012, 23(S1):77-81.
[5] 马媛媛, 汪振洋, 来庆英, 等.一种能够催化莱鲍迪苷A生成莱鲍迪苷D的糖基转移酶StUGT:CN112760302B[P].2022-08-26.
[6] LIN M, WANG F, ZHU Y S.Modeled structure-based computational redesign of a glycosyltransferase for the synthesis of rebaudioside D from rebaudioside A[J].Biochemical Engineering Journal, 2020, 159:107626.
[7] CHEN L L, CAI R X, WENG J Y, et al.Production of rebaudioside D from stevioside using a UGTSL2 Asn358Phe mutant in a multi-enzyme system[J].Microbial Biotechnology, 2020, 13(4):974-983.
[8] WANG Z Y, HONG J F, MA S Y, et al.Heterologous expression of EUGT11 from Oryza sativa in Pichia pastoris for highly efficient one-pot production of rebaudioside D from rebaudioside A[J].International Journal of Biological Macromolecules, 2020, 163:1669-1676.
[9] OLSSON K, CARLSEN S, SEMMLER A, et al.Microbial production of next-generation Stevia sweeteners[J].Microbial Cell Factories, 2016, 15(1):207.
[10] 王秀奇, 秦淑媛, 高天慧, 等.基础生物化学实验[M].2版.北京:高等教育出版社, 1999.
WANG X Q, QIN S Y, GAO T H, et al.Basic Biochemistry Experiments[M].Beijing:Higher Education Press, 1999.
[11] SELLECK W, TAN S.Recombinant protein complex expression in E.coli[J].Current Protocols in Protein Science, 2008, 52(1):5-21.
[12] 杨玉凤, 费理文, 李建华, 等.重组大肠杆菌全细胞催化合成莱鲍迪苷D[J].工业微生物, 2017, 47(5):1-7.
YANG Y F, FEI L W, LI J H, et al.Production of rebaudioside D by recombinant Escherichia coli whole cell catalyst[J].Industrial Microbiology, 2017, 47(5):1-7.
[13] 邝爱丽, 陈圆圆, 彭志峰, 等.包涵体的形成原因及其处理方法[J].上海畜牧兽医通讯, 2009(1):62-63.
KUANG A L, CHEN Y Y, PENG Z F, et al.Causes of inclusion body formation and its treatment[J].Shanghai Journal of Animal Husbandry and Veterinary Medicine, 2009(1):62-63.
[14] 陈红, 张绍山, 肖婕妤, 等.一个潜在催化莱鲍迪D苷合成的新型糖基转移酶[J].分子植物育种, 2020, 18(9):2872-2877.
CHEN H, ZHANG S S, XIAO J Y, et al.A novel glycosyltransferase potentially catalyzing the synthesis of rebaudioside D[J].Molecular Plant Breeding, 2020, 18(9):2872-2877.
[15] CHEN L L, SUN P, ZHOU F F, et al.Synthesis of rebaudioside D, using glycosyltransferase UGTSL2 and in situ UDP-glucose regeneration[J].Food Chemistry, 2018, 259:286-291.
[16] WANG J F, LI S Y, XIONG Z Q, et al.Pathway mining-based integration of critical enzyme parts for de novo biosynthesis of steviolglycosides sweetener in Escherichia coli[J].Cell Research, 2016, 26(2):258-261.
[17] LI Y, LI Y Y, WANG Y, et al.Production of rebaudioside a from stevioside catalyzed by the engineered Saccharomyces cerevisiae[J].Applied Biochemistry and Biotechnology, 2016, 178(8):1586-1598.