青春双歧杆菌(Bifidobacterium adolescentis)属于双歧杆菌科(Bifidobacteriaceae)双歧杆菌属(Bifidobacterium)菌种。截至2025年3月,该属包含105个有效发表物种(https://lpsn.dsmz.de/genus/Bifidobacterium[1])。B.adolescentis为革兰氏阳性厌氧菌,广泛存在于人及动物肠道菌群中,已有研究表明其部分菌株可增强肠道屏障功能、调节免疫反应、合成神经递质和维生素,对预防和缓解炎症性肠病、肠易激综合征、糖尿病等具有积极作用[2]。
B.adolescentis的分类始于1963年,REUTER在对婴儿和成人粪便的双歧杆菌菌群进行比较研究中,提出并命名了B.adolescentis[3],其被收录于1980年《核准的细菌名录》中[4]。2014年CHOI等[5]首次从2周龄婴儿粪便样本中分离出粪双歧杆菌(Bifidobacterium faecale),以CU3-7(JCM 19861)为模式菌株,并通过表型特征鉴定、16S rRNA基因序列相似性(98.4%)、hsp60基因序列相似性(94.0%)及传统DNA-DNA杂交(同源性<70%)等多相分类学方法完成物种描述。2025年3月,OKUHASMA等[6]基于全基因组分析将B.faecale分类变迁为B.adolescentis。因此,B.faecale当前分类正确名称为B.adolescentis。
B.adolescentis作为食品用菌种,被收录于我国《可用于食品的菌种名单》中。食品用菌种的鉴定及安全性评价备受行业关注,科学精准的菌种鉴定不仅是菌株安全性评价的基础,也是行业应用的前提。国家卫生健康委员会和国家市场监督管理总局于2025年3月发布GB 31615.2—2025《食品安全国家标准 食品用菌种安全性评价程序》,其中对拟评价微生物菌种,要求提供菌种名称(包括中文名、拉丁名、别名等)基本信息;分类学需提供规范、科学的菌种分类(属、种、亚种等),当菌种分类学地位发生变化时,还应包含其重新分类后的名称及曾用名;鉴定需提供基于表型和基因型的菌种鉴定资料。B.adolescentis在食品等多个领域具有重要的应用价值,对其开展科学分类鉴定确认,是菌株功能深入研究、产业化应用、企业申报和政府监管的重要前提。
近年来,全基因组测序技术迅速发展,为原核生物分类鉴定带来了重大变革。传统DNA-DNA杂交(DNA-DNA hybridization,DDH)依赖大量高质量DNA样本且对实验操作要求极高,结果易受方法差异影响[7],而基于统计模型构建的数字DNA-DNA杂交(digital DNA-DNA hybridization,dDDH)有效规避了传统方法的样本和操作限制,展现出更高的精准度和可重复性[8]。基于全基因组的平均核苷酸一致性(average nucleotide identity,ANI)、平均氨基酸一致性(average amino acid identity,AAI)及dDDH等基因组相关性指标已成为原核生物分类的核心依据[9]。本文以CICC 10187R(JCM 19861)[曾用名粪双歧杆菌(B.faecale)]为研究对象,综合运用16S rRNA基因和全基因组测序及系统发育分析,以及ANI、AAI和dDDH分析的种水平鉴定方法,进行基于全基因组的分类鉴定。旨在为B.adolescentis等细菌菌种的科学鉴定提供理论支持,为菌株的安全性评价及行业应用奠定基础。
1 材料与方法
1.1 材料与试剂
1.1.1 实验菌株
实验菌株CICC 10187R(JCM 19861)由中国工业微生物菌种保藏管理中心(China Center of Industrial Culture Collection,CICC)提供。
1.1.2 试剂
强化梭菌培养基,美国BD公司;细菌基因组DNA提取试剂盒,天根生化科技(北京)有限公司;2×PCR Mix、DNA Marker,北京全式金生物技术有限公司;MGISEQ试剂盒,深圳华大智造科技股份有限公司;Nanopore-GridION试剂盒,英国Oxford Nanopore Technologies公司;所有化学试剂为分析纯。
1.2 仪器与设备
BioDrop μLite超微量核酸蛋白分析仪,英国Biochrom公司;Qubit 3.0荧光计,赛默飞世尔科技公司;MGISEQ-200基因测序仪,深圳华大智造科技股份有限公司;GridION Mk1测序仪,英国Oxford Nanopore Technologies公司。
1.3 实验方法
1.3.1 菌株转接活化
对冻干管菌种CICC 10187R进行转接活化,于强化梭菌培养基中37 ℃厌氧培养48 h,培养后置于4 ℃冰箱备用。
1.3.2 基因序列检测
对菌种CICC 10187R进行了16S rRNA基因和全基因组序列检测,以确保菌种质量符合实验要求。采用天根细菌基因组DNA提取试剂盒(货号:DP302)通过离心柱法提取CICC 10187R基因组DNA,使用BioDrop μLite超微量核酸蛋白分析仪检测纯度,使用Qubit 3.0荧光计测定浓度。以通过质量检测合格的CICC 10187R菌株基因组DNA(核酸浓度≥10 ng/μL,A260/A280=1.8~2.0)为模板,采用细菌通用引物27F/1492R对质量合格的DNA进行16S rRNA基因PCR扩增(退火温度55 ℃,30个循环)。扩增产物经纯化后,采用一代双向测序,获取16S rRNA基因序列数据。采用MGISEQ试剂盒构建文库并制作纳米球(DNA nano ball,DNB),运用MGISEQ-200基因测序仪进行全基因组二代测序,同时使用Nanopore-GridION试剂盒构建文库并运用GridION Mk1测序仪进行全基因组三代测序。完成测序后,对测序数据进行质量控制。使用Fastp(v0.24.0)软件[10]对产生的原始测序数据进行筛选和过滤,去除低质量序列和接头序列。使用Flye(v2.9-b1768)软件[11]对质控后数据进行组装拼接与纠错,最终获得高质量的全基因组完成图。将经拼接获得的16S rRNA基因序列(>1 300 bp)和完整的全基因组序列,分别通过NCBI(https://submit.ncbi.nlm.nih.gov/)提交至GenBank数据库,获取GenBank序列登录号。
1.3.3 16S rRNA基因序列分析
将测得的CICC 10187R的16S rRNA基因序列与模式菌种数据库中有效发表的模式菌株序列进行同源性比对分析,获得CICC 10187R与近缘模式菌株的序列相似性。基于比对结果,使用MEGA 11.0[12]中的最大似然法(maximum-likelihood,ML)构建系统发育树。选取来源于EzBioCloud数据库[13]的双歧杆菌属模式菌株16S rRNA基因序列一同进行系统发育分析,自展值设为100次重复以评估分支可靠性。为提高系统发育树的可视化解析度,使用iTOL 5[14]在线工具对系统发育树进行拓扑结构优化与可视化呈现,以显著提升分支节点分辨率及可读性。
1.3.4 全基因组序列分析
1.3.4.1 全基因组序列来源及质控
全基因组参考序列来源于NCBI数据库,确保全基因组序列质量,使用CheckM(v1.2.3)软件[15]评估基因组完整性及污染率,利用QUAST(v5.0.2)软件[16]计算基因组大小与DNA G+C含量。并整理相关基因组信息,包括菌种名称、基因组大小、组装登录号、DNA G+C含量以及完整性和污染度等。基于全基因组序列系统发育分析Bifidobacterium菌种全基因组序列,均来源于EzBioCloud数据库,并经去重后获取进行研究。
1.3.4.2 基因组特征比较分析及平均核苷酸一致性、平均氨基酸一致性、dDDH分析
对CICC 10187R和B.adolescentis ATCC 15703T进行基因组特征比较分析。通过Prokka 1.14.6[17]进行基因组注释,运用RAST系统注释平台(http://RAST.nmpdr.org)[18]对CICC 10187R (GCA_039830185.1)和B.adolescentis ATCC 15703T (GCA_000010425.1)开展功能基因特征分析。基于基因组学定义的物种标准为同一物种,需满足ANI大于95%~96%、AAI大于95%和dDDH大于70%[19]。进行基因组相关性指数(overall genome relatedness index,OGRI)分析,包括使用fastANI(v1.33)[20]进行全基因组两两比对计算ANI,借助在线AAI计算平台(http://enve-omics.ce.gatech.edu/aai)[21]获取AAI,通过GGDC 3.0(Genome-to-Genome Distance Calculator,http://ggdc.dsmz.de/ggdc.php)[1]计算dDDH值。为了直观呈现分类学相关性,获得的基因组相关性指数参数通过SRplot在线工具(http://www.bioinformatics.com.cn/SRplot)[22]构建三维散点图进行可视化呈现。
1.3.4.3 全基因组序列系统发育分析
基于全基因组序列的系统发育分析具有更高的分辨率,因此本研究进一步进行全基因组的序列系统发育分析。通过Type (Strain) Genome Server (TYGS, https://tygs.dsmz.de/)[1]进行多基因组序列比对及系统发育分析,构建CICC 10187R、B.adolescentis及双歧杆菌属相关菌株基因组序列系统发育树。分支节点处标注的数值代表基于100次重复计算获得的自举支持值(>50%)。运用iTOL 5[14]在线工具对系统发育树进行拓扑结构优化与可视化呈现,以显著提升分支节点分辨率及可读性。
2 结果与分析
2.1 菌株CICC 10187R转接活化
对冻干管菌种CICC 10187R进行了转接活化。在强化梭菌培养基中经过37 ℃厌氧培养48 h后,观察到菌种在强化梭菌培养基上呈现出良好的生长状态。将培养后的菌种置于4 ℃冰箱中保存,以备后续的实验操作和研究使用。
2.2 16S rRNA基因序列复测及系统发育分析
对CICC 10187R的16S rRNA基因序列进行了复测,并将其序列提交至NCBI数据库,获得GenBank登录号PP830001。通过与模式菌种核酸序列数据库进行比对,发现CICC 10187R与菌株B.adolescentis CU3-7 (synonym B.faecale) (KF990498)和模式菌种B.adolescentis ATCC 15703T (AP009256)的16S rRNA基因序列相似性最高,分别为100.00%和98.69%,同其他模式菌种的16S rRNA基因序列相似性均低于98.65%。以Pseudoscardovia suis DPTE4T (HQ842701) 为系统发育树外群,采用MEGA 11.0软件,基于最大似然法(maximum likelihood,ML)构建CICC 10187R与B.adolescentis以及其他双歧杆菌属相关菌种的16S rRNA基因序列系统发育树(图1)。系统发育分析结果表明,CICC 10187R与B.adolescentis的16S rRNA基因序列相似性最高,在系统发育树中聚为同一分支。由于其与模式菌种的序列相似性接近种水平的阈值,同时系统发育分析与模式菌株聚为同一分支,表明CICC 10187R与B.adolescentis亲缘关系最近。

图1 最大似然法构建的CICC 10187R、B.adolescentis和双歧杆菌属相关菌种16S rRNA基因序列系统发育树
Fig.1 Maximum-likelihood phylogenetic tree showing the phylogenetic relationships of the 16S rRNA gene CICC 10187R, B.adolescentis, and phylogenetically related Bifidobacterium reference strains
2.3 全基因组序列质控
使用CheckM(v1.2.3)软件评估基因组完整性及污染率,利用QUAST(v5.0.2)软件计算基因组大小与DNA G+C含量,质控合格。经过质量控制后,获得用于后续分析的基因组序列,其中包括619株B.adolescentis以及1株曾用名为B.faecale的非模式菌株。获得的相关基因组信息,包括菌种名称、基因组大小、组装登录号、DNA G+C 含量以及完整性和污染度等详见电子版增强出版附表1(https://doi.org/10.13995/j.cnki.11-1802/ts.043170,下同)。基于全基因组序列系统发育分析所涉及的Bifidobacterium菌种全基因组序列,经去重后信息见附表2。
表1 CICC 10187R和B.adolescentis ATCC 15703T基因组特征信息
Table 1 Genomic characteristics of CICC 10187R and B.adolescentis ATCC 15703T
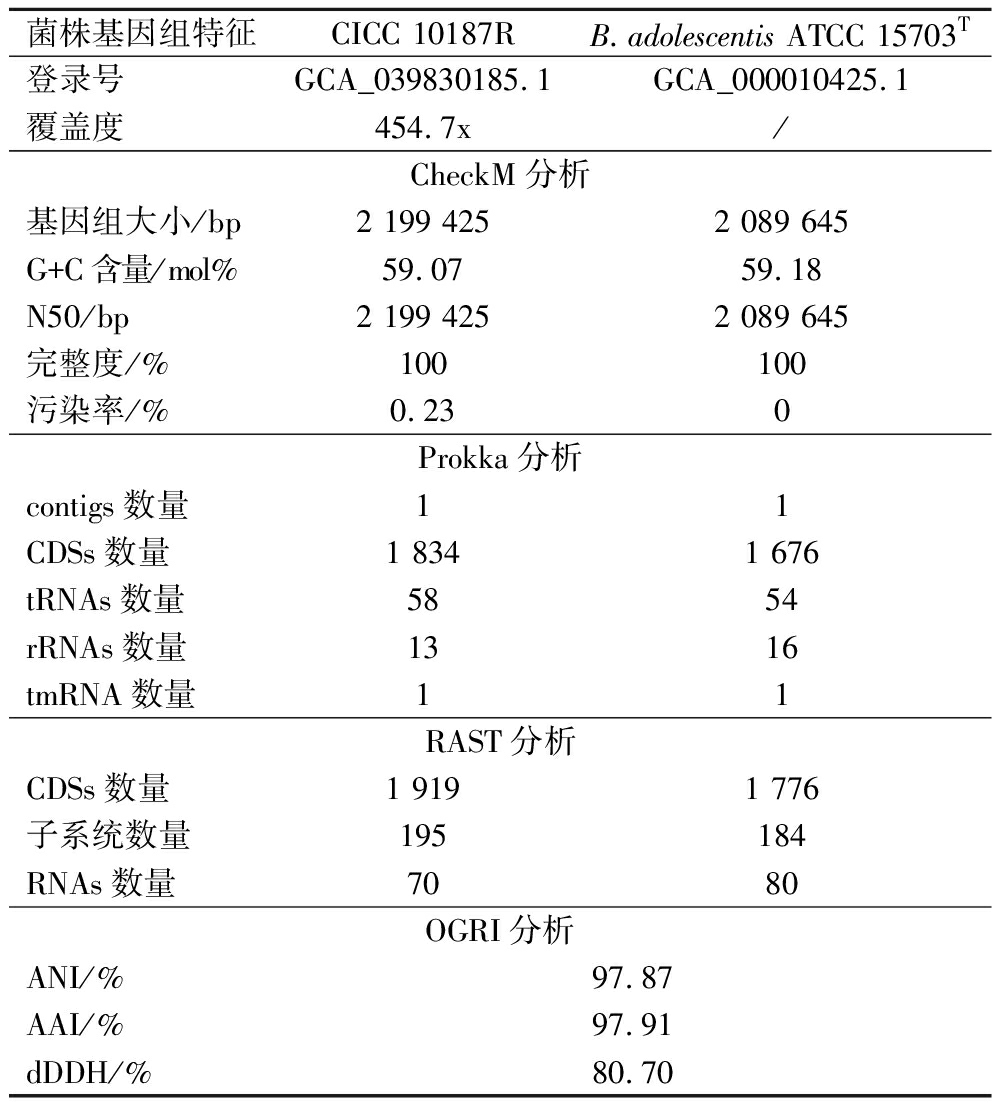
菌株基因组特征CICC 10187RB.adolescentis ATCC 15703T登录号GCA_039830185.1GCA_000010425.1覆盖度454.7x/CheckM分析基因组大小/bp2 199 4252 089 645G+C含量/mol%59.0759.18N50/bp2 199 4252 089 645完整度/%100100污染率/%0.230Prokka分析contigs数量11CDSs数量1 8341 676tRNAs数量5854rRNAs数量1316tmRNA数量11RAST分析CDSs数量1 9191 776子系统数量195184RNAs数量7080OGRI分析ANI/%97.87AAI/%97.91dDDH/%80.70
2.4 基因组特征比较分析及平均核苷酸一致性、平均氨基酸一致性、dDDH分析
对CICC 10187R的全基因组序列进行了复测,并将其提交至NCBI数据库,获得GenBank登录号GCA_039830185.1。通过多基因组学数据分析揭示了CICC 10187R与B.adolescentis的基因组特征及分类学关系。基因组特征信息分析显示,菌株CICC 10187R和B.adolescentis ATCC 15703T的基因组大小分别为2.20 Mb(2 199 425 bp)和2.09 Mb(2 089 645 bp),DNA G+C含量分别为59.07 mol%和59.18 mol%。CheckM评估显示,两菌株基因组完整度均为100%,污染率分别为0.23%和0%,结合Prokka注释结果证实,其基因组数据质量可靠。通过RAST平台分析表明,CICC 10187R包含1 919个编码序列(coding sequences,CDSs)和195个功能子系统,B.adolescentis ATCC 15703T含有1 776个CDSs和184个功能子系统。CICC 10187R和B.adolescentis ATCC 15703T基因组特征信息见表1。
基因组相关性指数(overall genome relatedness index,OGRI)分析显示,CICC 10187R和B.adolescentis ATCC 15703T的ANI、AAI及dDDH分别为97.87%、97.91%和80.70%,均显著高于细菌种水平阈值(ANI>95%~96%、AAI>95%、dDDH>70%)。CICC 10187R与619株B.adolescentis非模式菌株的全基因组序列的ANI、AAI和dDDH值范围分别为97.63%~98.71%、96.99%~98.85%和78.4%~88.6%,均高于物种划分阈值,同时1株4-CP1-AT-SP-D3-35[曾用名B.faecale]非模式菌株与619株B.adolescentis非模式菌株的全基因组序列相似性也均高于物种划分阈值(附表3)。基于SRplot构建的三维散点图(图2)直观呈现了各菌株ANI、AAI和dDDH参数的空间分布特征。综上,多维度分析有力支持CICC 10187R(JCM 19861)[曾用名B.faecale]与B.adolescentis应归类为同一物种的分类学观点。综上,CICC 10187R被鉴定为B.adolescentis。
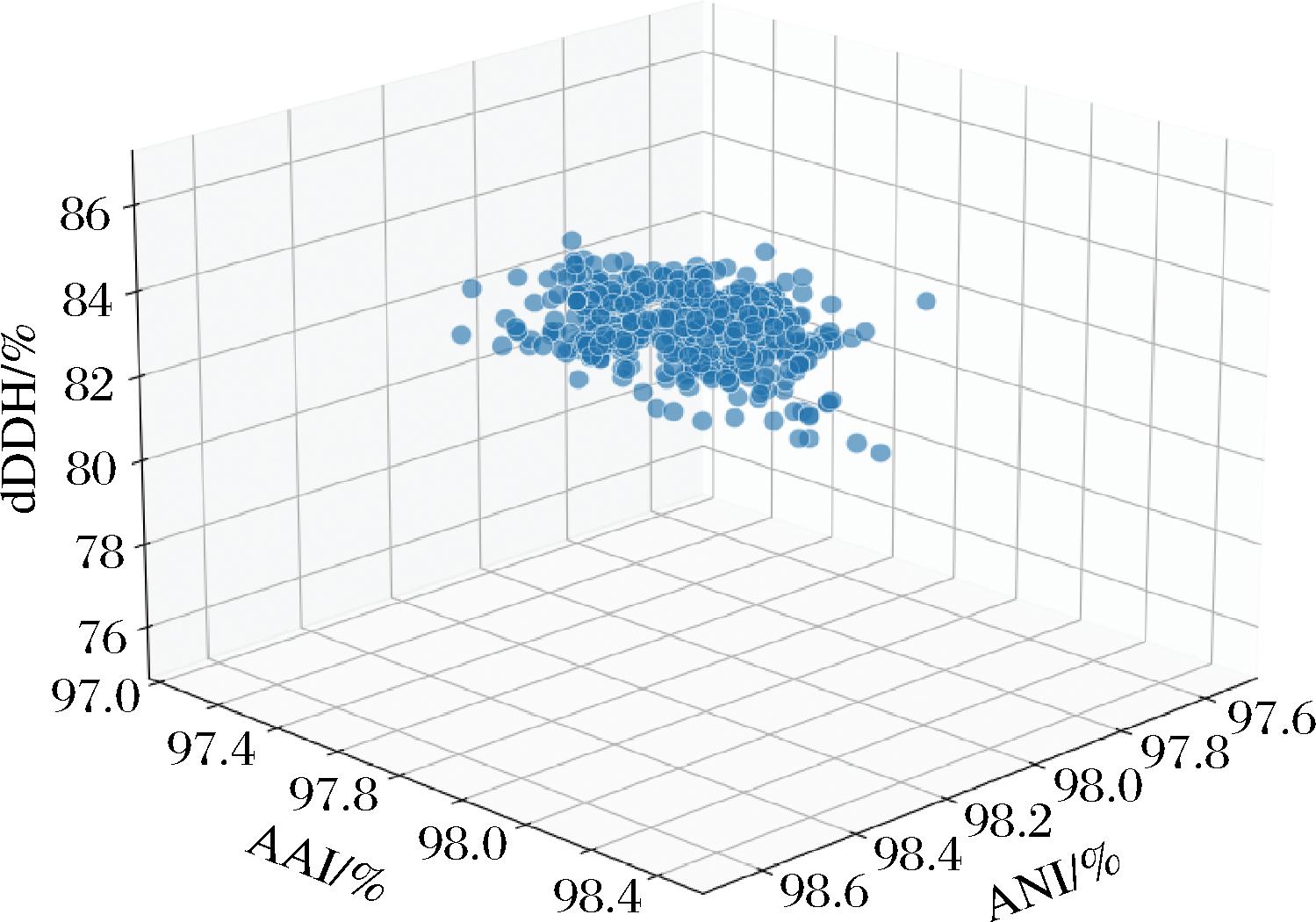
图2 CICC 10187R和B.adolescentis的ANI、AAI和dDDH的三维散点图
Fig.2 The 3D scatter plot of ANI, AAI, and dDDH of CICC 10187R and B.adolescentis
2.5 全基因组序列系统发育分析
采用全基因组序列系统发育分析,通过Type (Strain) Genome Server(TYGS,https://tygs.dsmz.de/)进行多基因组序列比对及系统发育分析,构建了CICC 10187R、B.adolescentis及相关菌株的基因组序列系统发育树(图3)。系统发育树中分支节点处标注的数值为基于100次重复计算获得的自举支持值(>50%),表明各分支的可靠性。进一步运用iTOL 5在线工具对系统发育树进行拓扑结构优化与可视化呈现,显著提升了分支节点的分辨率及可读性。全基因组序列系统发育分析结果表明,CICC 10187R与B.adolescentis种内株间的核心菌株类群在系统发育树中聚于同一分支,表明与B.adolescentis亲缘关系最近,与其他Bifidobacterium菌种能明显区分开。这一结果为CICC 10187R的准确种水平鉴定提供了更有力的依据,同时也显示了全基因组序列系统发育分析在微生物分类鉴定中的优势。

图3 基于全基因组序列构建的CICC 10187R和B.adolescentis及相关菌系统发育树
Fig.3 Whole-genome based phylogenomic tree constructed showing the phylogenomic relationship of CICC 10187R, B.adolescentis and related members
3 结论与讨论
本研究通过全基因组分析系统阐明了B.adolescentis与曾用名B.faecale菌株CICC 10187R(JCM 19861)及NCBI数据库中相关菌株的分类学关系。结果显示,菌株CICC 10187R与B.adolescentis模式菌株ATCC 15703T的ANI值为97.87%、AAI值为97.91%、dDDH值为80.70%,均显著高于细菌种水平划分阈值(ANI>95%~96%、AAI>95%、dDDH>70%)。基于16S rRNA基因序列和全基因组序列的系统发育分析表明,CICC 10187R与B.adolescentis菌株聚于同一分支。此外,通过对NCBI数据库中620株相关菌株的全基因组序列进行分析,进一步验证了CICC 10187R应被鉴定为B.adolescentis,其分类归属符合原核生物国际命名法规(International Code of Nomenclature of Prokaryotes,ICNP)[23]及NCBI数据库分类最新修订。本研究通过多维度基因组学分析,明确了B.adolescentis的分类地位,为双歧杆菌属菌株的精准鉴定和分类提供了科学依据。
微生物鉴定是菌株功能解析与产业化应用的基础,尤其对于食品用菌种而言,准确的分类鉴定直接关系到其安全性评估、功能特性研究及法规监管等。传统分类鉴定方法多依赖于表型分析和单一基因(如16S rRNA基因)序列分析等,在近缘菌种鉴别中存在局限性。本研究基于全基因组的ANI、AAI、dDDH及系统发育分析对CICC 10187R进行鉴定,充分体现了全基因组技术在菌种鉴定中的高分辨率优势。B.adolescentis作为食品工业常用菌种,其菌株功能特性(如产酸能力、肠道定植等)可能因菌株基因组差异而有所不同,但基于基因组的种水平精准鉴定可确保功能研究与安全性评价的靶向性与可靠性。
微生物分类是动态更新的过程,菌种分类可能随新种的发布或分类标准的更新而持续调整。尚需对工业菌种定期开展鉴定,持续不断跟踪菌种分类地位变化,尤其需关注菌种分类修订更新动态,以确保菌种分类地位正确。对于食品用菌种,分类地位的持续跟踪关乎菌株功能研究的准确性。B.adolescentis作为重要的食品用菌种,其准确的分类鉴定是开展菌株功能研究、安全性评价和产业化应用的重要基础。本研究通过全基因组分析方法,为该菌种的精准分类提供了可靠的科学依据,不仅完善了其分类学信息,更为后续的功能机制研究、安全性评价和产业化应用提供了重要的数据支撑,将有效促进B.adolescentis在食品工业中的科学应用,也为食品用菌种及相关领域研究奠定了基础。
[1] MEIER-KOLTHOFF J P, CARBASSE J S, PEINADO-OLARTE R L, et al.TYGS and LPSN:A database tandem for fast and reliable genome-based classification and nomenclature of prokaryotes[J].Nucleic Acids Research, 2022, 50(D1):D801-D807.
[2] LESER T, BAKER A.Bifidobacterium adolescentis - a beneficial microbe[J].Beneficial Microbes, 2023, 14(6):525-551.
[3] NOUIOUI I, CARRO L, GARC A-L
A-L PEZ M, et al.Genome-based taxonomic classification of the Phylum Actinobacteria[J].Frontiers in Microbiology, 2018, 9:2007.
PEZ M, et al.Genome-based taxonomic classification of the Phylum Actinobacteria[J].Frontiers in Microbiology, 2018, 9:2007.
[4] SKERMAN V B D, SNEATH P H A, MCGOWAN V.Approved lists of bacterial names[J].International Journal of Systematic and Evolutionary Microbiology, 1980, 30(1):225-420.
[5] CHOI J H, LEE K M, LEE M K, et al.Bifidobacterium faecale sp.nov., isolated from human faeces[J].International Journal of Systematic and Evolutionary Microbiology, 2014, 64(Pt_9):3134-3139.
[6] OKUHAMA S, TAKAHASHI H, NAKAYAMA Y, et al.Reclassification of Bifidobacterium faecale Choi et al.2014 as a later heterotypic synonym of Bifidobacterium adolescentis Reuter 1963[J].International Journal of Systematic and Evolutionary Microbiology, 2025, 75(3).DOI:10.1099/ijsem.0.006706.
[7] HUSS V A R, FESTL H, SCHLEIFER K H.Studies on the spectrophotometric determination of DNA hybridization from renaturation rates[J].Systematic and Applied Microbiology, 1983, 4(2):184-192.
[8] VERSMESSEN N, MISPELAERE M, VANDEKERCKHOVE M, et al.Average nucleotide identity and digital DNA-DNA hybridization analysis following PromethION nanopore-based whole genome sequencing allows for accurate prokaryotic typing[J].Diagnostics, 2024, 14(16):1800.
[9] RIESCO R, TRUJILLO M E.Update on the proposed minimal standards for the use of genome data for the taxonomy of prokaryotes[J].International Journal of Systematic and Evolutionary Microbiology, 2024, 74(3):006300.
[10] CHEN S F.Ultrafast one-pass FASTQ data preprocessing, quality control, and deduplication using fastp[J].iMeta, 2023, 2(2):e107.
[11] KOLMOGOROV M, YUAN J, LIN Y, et al.Assembly of long, error-prone reads using repeat graphs[J].Nature Biotechnology, 2019, 37(5):540-546.
[12] TAMURA K, STECHER G, KUMAR S.MEGA11:Molecular evolutionary genetics analysis version 11[J].Molecular Biology and Evolution, 2021, 38(7):3022-3027.
[13] CHALITA M, KIM Y O, PARK S, et al.EzBioCloud:A genome-driven database and platform for microbiome identification and discovery[J].International Journal of Systematic and Evolutionary Microbiology, 2024, 74(6):006421.
[14] LETUNIC I, BORK P.Interactive tree of life (iTOL) v5:An online tool for phylogenetic tree display and annotation[J].Nucleic Acids Research, 2021, 49(W1):W293-W296.
[15] CHKLOVSKI A, PARKS D H, WOODCROFT B J, et al.CheckM2:A rapid, scalable and accurate tool for assessing microbial genome quality using machine learning[J].Nature Methods, 2023, 20(8):1203-1212.
[16] GUREVICH A, SAVELIEV V, VYAHHI N, et al.QUAST:Quality assessment tool for genome assemblies[J].Bioinformatics, 2013, 29(8):1072-1075.
[17] SEEMANN T.Prokka:Rapid prokaryotic genome annotation[J].Bioinformatics, 2014, 30(14):2068-2069.
[18] AZIZ R K, BARTELS D, BEST A A, et al.The RAST Server:Rapid annotations using subsystems technology[J].BMC Genomics, 2008, 9:75.
[19] THOMPSON C C, CHIMETTO L, EDWARDS R A, et al.Microbial genomic taxonomy[J].BMC Genomics, 2013, 14(1):913.
[20] JAIN C, RODRIGUEZ-R L M, PHILLIPPY A M, et al.High throughput ANI analysis of 90K prokaryotic genomes reveals clear species boundaries[J].Nature Communications, 2018, 9:5114.
[21] RODRIGUEZ R L M, KONSTANTINIDIS K T.The enveomics collection:A toolbox for specialized analyses of microbial genomes and metagenomes[J].PeerJ Preprints, 2016, 4:e1900v1.
[22] TANG D D, CHEN M J, HUANG X H, et al.SRplot:A free online platform for data visualization and graphing[J].PLoS One, 2023, 18(11):e0294236.
[23] AHARON O,R D A,MARKUS G, et al.International code of nomenclature of prokaryotes.prokaryotic code (2022 revision)[J].International Journal of Systematic and Evolutionary Microbiology,2023,73(5a):DOI:10.1099/IJSEM.0.005585.